Изобретение относится к биотехнологии и генной инженерии, а именно к предсказанию диагностически-значимых антигенных эпитопов белков коронавируса (SARS-CoV), связанного с тяжелым острым респираторным синдромом, а также к получению рекомбинантных белков, содержащих предсказанные теоретическим путем диагностически-значимые антигенные детерминанты белков коронавируса (SARS-CoV), связанного с тяжелым острым респираторным синдромом.
Возбудитель тяжелого острого респираторного синдрома (ТОРС или англ. - SARS) принадлежит к семейству коронавирусов, вызывающих известные заболевания людей и домашних животных. По антигенным свойствам коронавирусы разделяют на 3 группы. К I группе принадлежит респираторный коронавирус человека 229Е, коронавирусы кошек, собак и свиней. Ко II группе принадлежит человеческий коронавирус ОС43, вирус гепатита мышей и коронавирус телят. Кишечные коронавирусы человека и вирусы инфекционного бронхита птиц составляют III группу. По данным анализа нуклеотидной последовательности коронавируса, вызывающего SARS, филогенетически он не принадлежит ни к одной из известных антигенных групп коронавирусов и имеет ряд существенных отличий в геноме от известных ранее вирусов этого семейства. Все известные коронавирусы вызывают, как правило, либо респираторные инфекции различной степени тяжести, либо кишечные инфекции и неврологические синдромы. Инфекция передается аэрозольным, фекально-оральным и контактным путями. Все коронавирусы обладают широким тропизмом и поэтому могут поражать помимо дыхательных путей также печень, почки, сердце и глаза. Типичная коронавирусная инфекция клинически проявляется гриппоподобным заболеванием и/или желудочно-кишечным расстройством. SARS представляет собой наиболее тяжелую форму коронавирусной инфекции, которая в России больше известна под названием “атипичная пневмония”.
Это заболевание впервые было обнаружено в ноябре 2002 г. и получило наиболее широкое распространение в странах Юго-Восточной Азии (Китай, Гонконг, Тайвань, Сингапур, Вьетнам, Малайзия, Таиланд) и Северной Америки (США, Канада). Кроме того, случаи заболевания зарегистрированы в некоторых странах Европы (Франция, Германия, Италия, Ирландия, Румыния, Испания, Швейцария и Великобритания), Южной Америки (Бразилия), Японии и Южной Африки. По данным ВОЗ по состоянию на 19 июня 2003 г. всего в мире заболело более 8400 человек, из которых 806 умерло (Бюллетень Вакцинация, грипп, №3 (27) май/июнь 2003 г.).
Наибольшее значение для диагностики атипичных пневмоний в настоящее время приобретают иммунологические и молекулярно-биологические методы (иммуноферментный анализ, иммунофлюоресценция, полимеразная цепная реакция). Носительство и персистенция, характерные для инфекций, вызываемых данной группой возбудителей, обусловливают необходимость особенно тщательной интерпретации серологических реакций и результатов молекулярно-биологических методов исследования. Дальнейшее совершенствование диагностики атипичных пневмоний связано с поиском новых специфичных антигенных и нуклеотидных маркеров возбудителей, постановкой этиологического диагноза в начальной фазе заболевания, снижением стоимости наиболее чувствительных диагностических тест-систем.
К настоящему времени ученым нескольких исследовательских лабораторий Америки, Голландии и Германии независимо друг от друга удалось полностью расшифровать геном этого вируса. Как оказалось, геном представлен последовательностью 29727 нуклеотидов. Он включает 11 открытых рамок считывания (ORF) и его структурная организация близка к другим представителям семейства коронавирусов. Предложено название для нового вируса: SARS - ассоциированный коронавирус Урбани (Urbani SARS-associated coronavirus) в честь врача Carolo Urbani, погибшего при проведении исследований в самом начале эпидемии SARS.
Сейчас помимо известного штамма Урбани изучены еще три варианта вируса SARS. При сравнении полученных данных показано, что все геномы чрезвычайно близки друг с другом и отличаются только по 24 из 29727 позиций нуклеотидов. Геном вируса представлен полиаденилированой РНК, содержащей в своем составе 41% Г и Ц нуклеотидных остатков (Г/Ц-насыщенность геномов известных коронавирусов составляет 37-42%). Расположение ORF в геноме типично для коронавирусов. На 5’-конце - ген rep, включающий ORF1 и ORF2, которые кодируют полипептиды, подвергающиеся процессингу с образованием ферментов вируса; затем - гены, кодирующие структурные белки, четыре из которых: S (шипа), Е (оболочки), М (мембраны) и N (нуклеокапсида) являются характерными для всех коронавирусов. Продукты rep гена образуются в результате прямой трансляции геномной РНК, тогда как для синтеза других вирусных белков необходима предварительная транскрипция с образованием отдельных молекул мРНК.
Ген гемагглютининэстеразы, присутствующий у коронавирусов второй и некоторых представителей третьей группы, в геноме SARS-CoV не обнаружен.
Сравнительный анализ нуклеотидных последовательностей, кодирующих ферменты и структурные белки вируса SARS и других коронавирусов, указывает на высокую гомологию данных участков геномов. Вместе с тем различия в соответствующих нуклеотидных последовательностях позволяют провести четкую границу между вирусом SARS и другими коронавирусами. Полная расшифровка генома вируса SARS ясно демонстрирует то, что данный вирус несет в себе черты рода коронавирусов и в то же время отличается от всех известных представителей этой группы.
Несмотря на известную нуклеотидную последовательность генома вируса SARS, вопрос о его происхождения до сих пор остается открытым, и потенциальный предшественник данного вируса среди коронавирусов животных еще не известен.
Иммуногистохимические и иммунофлюоресцентные тесты показали наличие реакции на поликлональные антитела к коронавирусам I группы.
В настоящее время разработаны диагностические тесты на основе иммуноферментного анализа, сконструированные с использованием лизатов нативных SARS-CoV.
Например, были синтезированы пептиды величиной 16-25 аминокислотных остатков относительно высокой гидрофильности. Четыре эпитопных участка, S599, M137, N66 и N371-404, в белках S, М и N SARS-CoV соответственно были определены скринингом синтезированных пептидов. Особенно N371 и N385, на СООН конце N белка, ингибировали связывание антител к лизату SARS-коронавируса и связывали антитела в n>94% образцов от SARS исследуемых пациентов. Таким образом, некоторые из пептидов оказались высокоиммуногенными и были предложены для серологического анализа (Wang J и др. Assessment of Immunoreactive Synthetic Peptides from the Structural Proteins of Severe Acute Respiratory Syndrome Coronavirus, Clin Chem. 2003 Nov 13).
В настоящее время не описано рекомбинантных белков, содержащих диагностически-значимые антигенные детерминанты белков коронавируса, связанного с тяжелым острым респираторным синдромом (SARS-CoV).
Задача изобретения состояла в идентификации диагностически - значимых антигенных эпитопов белков данного вируса и конструировании синтетических генов, позволяющих синтезировать рекомбинантные белки, содержащие предсказанные эпитопы.
Разработка рекомбинантных антигенов проводилась на основе данных анализа опубликованной аминокислотной последовательности SARS-CoV коронавируса штамма Urban! (accession number AY 278741).
Анализ выбранных белковых последовательностей проводили при помощи программы DNASTAR Lasergene (Windows версия; DNASTAR Inc., Madison, WI) (http://www. dnastar. com/). Было проведено сравнение выбранных белковых последовательностей SARS-CoV вируса для идентификации консервативных аминокислотных последовательностей. На основе анализа индекса антигенности, гидрофильности, наличия Р- и рэндом структур, вероятности нахождения на поверхности вируса и подвижности были предсказаны и выбраны для синтеза рекомбинантных белков последовательности, содержащие потенциальные эпитопы белков SARS-CoV вируса.
Одним из приемлемых антигенов для определения вирусспецифичных антител является нуклеокапсидный белок, поскольку для него специфичны большинство антител, образующихся в организме во время инфекции. Известно, что уровень экспрессии этого белка в инфицированных клетках очень высок. В структуре нуклеокапсидного белка имеются как консервативные, так и вариабельные эпитопы. Таким образом, для детекции антивирусных антител предпочтителен выбор данного компонента вируса.
Кроме нуклеокапсидного белка антигенными свойствами обладают также белки Е, М, S, включающие определенные фрагменты.
В нуклеокапсидном белке (N) SARS-CoV вируса было идентифицировано 3 антигенных эпитопа, расположенных в пределах 1-49 аминокислоты (последовательность 1), 191-221 аминокислоты (последовательность 2), 339-390 аминокислоты последовательность 3).
В аминокислотной последовательности поверхностного белка Е SARS-CoV вируса было идентифицировано два маленьких эпитопа, расположенные на N- и С-концах белковой молекулы. Ввиду небольшого размера белковой молекулы (76 аминокислот) было решено синтезировать полный белок (последовательность 4).
При анализе аминокислотной последовательности матричного белка М была идентифицирована эпитопная композиция, расположенная на С-конце белковой последовательности, в пределах 182-221 аа (последовательность 5). При анализе аминокислотной последовательности S белка SARS-CoV вируса были идентифицированы потенциальные антигенные эпитопы в пределах 12-53 аминокислоты (последовательность 7), в пределах 90-115 аминокислоты (последовательность 8), в пределах 171-203 аминокислоты (последовательность 9), в пределах 408-470 аминокислоты (последовательность 11), в пределах 540-573 аминокислоты (последовательность 12), в пределах 1051-1076 аминокислоты (последовательность 14), в пределах 1121-1154 аминокислоты (последовательность 15), в пределах 1162-1190 аминокислоты (последовательность 16). Нами было решено не синтезировать в виде отдельного белка последовательность 2, а получить мозаичный белок, содержащий 2 предсказанных эпитопа нуклеокапсидного белка SARS-CoV вируса, расположенных в пределах 1-49аа и 191-221аа (последовательность 6). Аминокислотные последовательности, идентифицированные на основе анализа S белка, были объединены в три мозаичных белка (последовательности 10, 13, 17).




Аминокислотная последовательность была ретранслирована в нуклеотидную последовательность, которая использовалась для дизайна синтетических олигонуклеотидов. Синтетические олигонуклеотиды были использованы для синтеза генов.
Дизайн синтетических олигонуклеотидов и праймеров проводили с заменой вирусных кодонов на кодоны, оптимальные для экспрессии в клетках Escherichia coli.
Конструирование рекомбинантной последовательности 1-SEQ ID NO: 1.
Для получения рекомбинантной последовательности 1 проводят один раунд амплификации ДНК методом ПЦР, используя в качестве матрицы ДНК 2-х синтетических комплементарных олигонуклеотидов размером 78 нуклеотидов каждый и ДНК двух синтетических олигонуклеотидов в качестве праймеров, содержащих сайты узнавания для рестриктаз BamHl и Xho l.

ПЦР проводят в следующих условиях: 25 циклов ПЦР (45 с 94°С, 20 с 50°С, 1 мин 72°С) и инкубация 7 мин при 72°С. В результате получают фрагмент ДНК размером 147 п.о.
Данный фрагмент представляет собой ДНК-последовательность, кодирующую фрагмент белка нуклекапсида SARS-CoV вируса с 1-49 аминокислоту - SEQ ID NO: 1 (см. Приложение 1 в конце текста).
Конструирование рекомбинантной последовательности 3-SEQ ID NO: 2.
Для получения рекомбинантной последовательности 3 проводят один раунд амплификации ДНК методом ПЦР, используя в качестве матрицы ДНК 2-х синтетических комплементарных олигонуклеотидов, размером 104 и 81 нуклеотидов каждый и ДНК двух синтетических олигонуклеотидов в качестве праимеров, содержащих сайты узнавания для рестриктаз BamHl и Xho l.

ПЦР проводят в следующих условиях: 25 циклов ПЦР (45 с 94°С, 20 с 50°С, 1 мин 72°С) и инкубация 7 мин при 72°С. В результате получают фрагмент ДНК размером 156 п.о.
Данный фрагмент представляет собой ДНК-последовательность, кодирующую фрагмент белка нуклеокапсида SARS-CoV вируса с 339-390 аминокислоту-SEQ ID NO: 2 (см. Приложение 1).
Конструирование рекомбинантной последовательности 6 - SEQ ID NO: 3
Для получения рекомбинантной последовательности 6 проводят два раунда амплификации ДНК методом ПЦР, используя в качестве матрицы ДНК 4-х синтетических комплементарных олигонуклеотидов размером 69, 69, 66, 81 нуклеотидов каждый и ДНК 4-х синтетических олигонуклеотидов в качестве праймеров, два из которых содержат сайты узнавания для рестриктаз BamHl и Хhо l.

Каждый раунд ПЦР проводят в следующих условиях: 25 циклов ПЦР (45 с 94°С, 20 с 50°С, 1 мин 72°С) и инкубация 7 мин при 72°С. В результате получают фрагмент ДНК размером 240 п.о.
Данный фрагмент представляет собой ДНК-последовательность мозаичного гена, кодирующую фрагмент белка нуклеокапсида SARS-CoV вируса с 1 по 49 аминокислоту и с 191-221 аминокислоту, при этом две аминокислотные последовательности вирусного белка соединены 3 Gly аминокислотами-SEQ ID NO: 3 (см. Приложение 1).
Конструирование рекомбинантной последовательности 4 - SEQID NO: 4.
Для получения рекомбинантной последовательности 4 проводят два раунда амплификации ДНК методом ПЦР, используя в качестве матрицы ДНК 4-х синтетических комплементарных олигонуклеотидов размером 61, 60, 63, 84 нуклеотидов каждый и ДНК 4-х синтетических олигонуклеотидов в качестве праймеров, два из которых содержат сайты узнавания для рестриктаз BamHl и Xho l.

Каждый раунд ПЦР проводят в следующих условиях: 25 циклов ПНР (45 с 94°С, 20 с 50°С, 1 мин 72°С) и инкубация 7 мин при 72°С. В результате получают фрагмент ДНК размером 228 п.о.
Данный фрагмент представляет собой ДНК-последовательность синтетического гена, кодирующую фрагмент белка Е SARS-CoV вируса с 1 по 76 аминокислоту - SEQ ID NO: 4 (см. Приложение 1).
Конструирование рекомбинантной последовательности 5-SEQ ID NO: 5
Для получения рекомбинантной последовательности 5 проводят один раунд амплификации ДНК методом ПЦР, используя в качестве матрицы ДНК 2-х синтетических комплементарных олигонуклеотидов размером 69 и 63 нуклеотидов каждый и ДНК двух синтетических олигонуклеотидов в качестве праймеров, содержащих сайты узнавания для рестриктаз BamHl и Xho l.

ПЦР проводят в следующих условиях: 25 циклов ПЦР (45 с 94°С, 20 с 50°С, 1 мин 72°С) и инкубация 7 мин при 72°С. В результате получают фрагмент ДНК размером 156 п.о.
Данный фрагмент представляет собой ДНК-последовательность мозаичного гена, кодирующую фрагмент белка S SARS-CoV вируса с 12 по 53 аминокислоту, с 90-115 аминокислоту, с 171 по 203 аминокислоту, при этом между аминокислотными последовательностями вирусного белка расположены 3 Gly аминокислоты - SEQ ID NO: 5 (см. Приложение 1).
Конструирование рекомбинантной последовательности 10 - SEQ ID NO: 6.
Для получения рекомбинантной последовательности 10 два раунда амплификации ДНК методом ПЦР, используя в качестве матрицы ДНК 4-х синтетических комплементарных олигонуклеотидов размером 96, 84, 96, 81 нуклеотидов каждый и ДНК 4-х синтетических олигонуклеотидов в качестве праймеров, два из которых содержат сайты узнавания для рестриктаз ВатНl и Хhо l.

ПЦР проводят в следующих условиях: 25 циклов ПЦР (45 с 94°С, 20 с 50°С, 1 мин 72°С) и инкубация 7 мин при 72°С. В результате получают фрагмент ДНК размером 321 п.о.
Данный фрагмент представляет собой ДНК-последовательность мозаичного гена, кодирующую фрагмент белка S SARS-CoV вируса с 408 по 470 аминокислоту и с 540-573 аминокислоту, при этом две аминокислотные последовательности вирусного белка соединены 3 Gly аминокислотами - SEQ ID NO: 6 (см. Приложение 1).
Конструирование рекомбинантной последовательности 13 - SEQ ID NO: 7.
Для получения рекомбинантной последовательности 13 два раунда амплификации ДНК методом ПЦР, используя в качестве матрицы ДНК 4-х синтетических комплементарных олигонуклеотидов размером 78, 87, 84, 87 нуклеотидов каждый и ДНК 4-х синтетических олигонуклеотидов в качестве праймеров, два из которых содержат сайты узнавания для рестриктаз BamHl и Xho l.

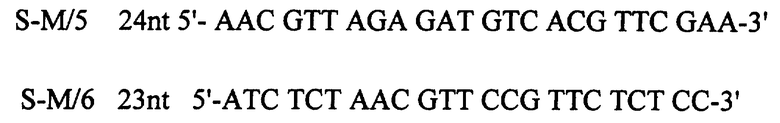
ПЦР проводят в следующих условиях: 25 циклов ПЦР (45 с 94°С, 20 с 50°С, 1 мин 72°С) и инкубация 7 мин при 72°С. В результате получают фрагмент ДНК размером 303 п.о.
Данный фрагмент представляет собой ДНК-последовательность мозаичного гена, кодирующую фрагмент белка S SARS-CoV вируса с 1051 по 1076 аминокислоту, с 1121-1154 аминокислоту, с 1162 по 1190 аминокислоту, при этом между аминокислотными последовательностями вирусного белка расположены 3 Gly аминокислоты-SEQ ID NO: 7 (см. Приложение 1).
Конструирование рекомбинантной последовательности 17-SEQ ID NO: 8.
Для получения рекомбинантной последовательности 17 два раунда амплификации ДНК методом ПЦР, используя в качестве матрицы ДНК 4-х синтетических комплементарных олигонуклеотидов размером 96, 84, 96, 81 нуклеотидов каждый и ДНК 4-х синтетических олигонуклеотидов в качестве праймеров, два из которых содержат сайты узнавания для рестриктаз BamHl и Xho l.


ПЦР проводят в следующих условиях: 25 циклов ПЦР (45 с 94°С, 20 с 50°С, 1 мин 72°С) и инкубация 7 мин при 72°С. В результате получают фрагмент ДНК размером 285 п.о.
Данный фрагмент представляет собой ДНК-последовательность гена, кодирующую фрагмент белка М SARS-CoV вируса с 182 по 221 аминокислоту - SEQ ID NO: 8 (см. Приложение 1).
Фрагменты рекомбинантных белков, кодируемые ДНК-последовательностями, были синтезированы в виде слитых белков (фьюжн-белков) с Glutathione-S-transferase, что позволяло проводить их очистку методом аффинной хроматографии.
Последовательности слитых белков включают последовательность белка
GST-S-transferase (1-244 аминокислота) - SEQ ID NO: 9 (см. Приложение 1) и последовательность соответствующего фрагмента белка SARS-CoV вируса SEQ ID NO 10 - SEQ ID NO 17.




Последовательности фрагментов белков, кодируемых ДНК-последовательностями, приведены как SEQ ID NO: 10 - SEQ ID NO: 17 в Приложении 1.
Слитые белки используются для производства диагностических препаратов. Вышеописанное изобретение может найти широкое применение в области диагностики и медицины.





| название | год | авторы | номер документа |
|---|---|---|---|
| ПОЛИПЕПТИДНЫЙ МОДУЛЬ ДЛЯ СВЯЗЫВАНИЯ КОНСЕРВАТИВНОГО ЭПИТОПА РЕЦЕПТОР-СВЯЗЫВАЮЩЕГО ДОМЕНА БЕЛКА SPIKE КОРОНАВИРУСА SARS-COV-2 | 2022 |
|
RU2809183C1 |
| Набор для выявления коронавируса SARS-CoV-2 | 2021 |
|
RU2765497C1 |
| Вирусоподобные химерные частицы для индукции специфического иммунитета против вируса тяжелого острого респираторного синдрома SARS-CoV-2, содержащие белки коронавируса и ротавируса | 2022 |
|
RU2779810C1 |
| Искусственный ген, кодирующий бицистронную структуру, образованную последовательностями рецептор-связующего домена гликопротеина S коронавируса SARS-CoV-2, P2A-пептида и гликопротеина G VSV, рекомбинантная плазмида pStem-rVSV-Stbl_RBD_SC2, обеспечивающая экспрессию искусственного гена и рекомбинантный штамм вируса везикулярного стоматита rVSV-Stbl_RBD_SC2, используемого для создания вакцины против коронавируса SARS-CoV-2 | 2020 |
|
RU2733831C1 |
| Искусственный ген Stbl_RBD_TrM_SC2, кодирующий бицистронную структуру, образованную последовательностями рецепторсвязывающего домена гликопротеина S коронавируса SARS-CoV-2, трансмембранного региона, P2A-пептида и гликопротеина G VSV, рекомбинантная плазмида pStem-rVSV-Stbl_RBD_TrM_SC2, обеспечивающая экспрессию искусственного гена, и рекомбинантный штамм вируса везикулярного стоматита rVSV-Stbl_RBD_TrM_SC2, используемый для создания вакцины против коронавируса SARS-CoV-2 | 2020 |
|
RU2733832C1 |
| Искусственный ген EctoS_SC2, кодирующий эктодомен гликопротеина S коронавируса SARS-CoV-2 с C-концевым тримеризующим доменом, рекомбинантная плазмида pStem-rVSV-EctoS_SC2, обеспечивающая экспрессию искусственного гена, и рекомбинантный штамм вируса везикулярного стоматита rVSV-EctoS_SC2, используемый для создания вакцины против коронавируса SARS-CoV-2 | 2020 |
|
RU2733834C1 |
| Рекомбинантная ДНК, обеспечивающая получение рекомбинантного белка Cov1, обладающего иммуногенными свойствами в отношении вируса SARS-CoV-2 | 2021 |
|
RU2776484C1 |
| Моноклональное антитело к RBD фрагменту в составе S белка вируса SARS-CoV-2 | 2020 |
|
RU2744274C1 |
| Комбинированное лекарственное средство, обладающее противовирусным эффектом в отношении нового коронавируса SARS-CoV-2 | 2021 |
|
RU2746362C1 |
| Рекомбинантные вирусоподобные частицы для индукции специфического иммунитета против вируса тяжелого острого респираторного синдрома SARS-CoV-2 | 2021 |
|
RU2769224C1 |
Изобретение относится к диагностике атипичных пневмоний с помощью молекулярно-биологических методов, а также к биотехнологии и генной инженерии. Предложены на основе идентифицированных антигенных эпитопов белков SARS-CoV ДНК-последовательности синтетических генов, кодирующих фрагменты рекомбинантного белка, содержащие антигенные детерминанты белков коронавируса SARS-CoV, представленные нуклеотидными последовательностями SEQ ID NO: 1 - SEQ ID NO: 8, а также фрагменты белка SARS-CoV вируса, кодируемые данными ДНК-последовательностями, представленные на фиг.1 аминокислотными последовательностями SEQ ID NO: 10 - SEQ ID NO: 17, при этом фрагменты выделены с использованием предварительно полученного слитого белка путем присоединения к его N-терминальному концу белка GST-S-трансферазы, имеющего последовательность SEQ ID NO: 9. Слитые белки обеспечивают получение диагностических препаратов и могут быть использованы при диагностике SARS-CoV вируса острого респираторного вируса. 2 н.п. ф-лы.
| Wang J.et al | |||
| Clin | |||
| Chem | |||
| Способ и приспособление для нагревания хлебопекарных камер | 1923 |
|
SU2003A1 |
| НУКЛЕОТИДНАЯ ПОСЛЕДОВАТЕЛЬНОСТЬ ВИРУСА КЛАССИЧЕСКОЙ СВИНОЙ ЛИХОРАДКИ (CSFV) (ВАРИАНТЫ), ПОЛИПЕПТИД CSFV, ПЕСТИВИРУСНАЯ ВАКЦИНА ПРОТИВ CSFV, ДИАГНОСТИЧЕСКИЙ НАБОР И СПОСОБ | 1995 |
|
RU2201451C2 |
| RU 2055889 C1, 10.03.1996 | |||
| Устройство для поштучной подачи плодов | 1987 |
|
SU1458281A1 |
| WO 9208487 A, 29.05.1992 | |||
| Гидроимпульсатор-накопитель | 1987 |
|
SU1469126A1 |
Авторы
Даты
2005-06-10—Публикация
2004-04-26—Подача