Изобретение относится к новому способу получения не содержащего побочных продуктов 4,6-диметокси-2-(метилсульфонил)-1,3-пиримидина и к его применению в качестве промежуточного продукта при получении обладающих гербицидными свойствами производных 7-[(4,6-диметоксипиримидин-2-ил)тио]нафталида.
Способы получения 2-алкилсульфонилпиримидиновых производных, которые являются дизамещенными в 4- и 6-положениях, уже известны из ЕР-А 0209779. J.Org.Chem. 26, 792 (1961) и Pestic.Sci. 47, 115 (1996). Некоторые из описанных способов осуществляют сложным путем, посредством множества отдельных реакционных стадий, с выделением соответствующих промежуточных продуктов. Так, например, в первом из двух документов описано окисление до соответствующих 2-алкилсульфонилпиримидиновых производных введением газообразного хлора в двухфазную систему (пример II-1, с.15) или раствор в абсолютном спирте 2-алкилтиопиримидиновых производных [например, 4,6-дихлор-2-(метилсульфонил)пиримидина (соединение XXXVII), с.802]. В Pestic.Sci. описаны как реакция 4,6-дихлор-2-(алкилтио)-1,3 -пиримидина с алкоксидом натрия с получением соответствующих 4,6-диалкоксизамещенных 2-алкилтиопиримидиновых производных, так и их окисление с получением соответствующих 4,6-диалкокси-2-(алкилсульфонил)-1,3-пиримидинов продуктом Oxone или пероксидом водорода в присутствии вольфрамата натрия в качестве катализатора. Чистый конечный продукт готовят перекристаллизацией. Однако отмечаемые при этом выход и степень чистоты продуктов для промышленных процессов получения зачастую оказываются неудовлетворительными. Более того, методы выделения и очистки являются экономически невыгодными и связанными с большими затратами на оборудование.
Целью настоящего изобретения является устранение этих недостатков и разработка более простого способа, который приемлем для промышленного применения. Было установлено, что 4,6-диметокси-2-(метилсульфонил)-1,3-пиримидин может быть получен простым путем с высокими выходом и степенью чистоты, особо выгодным с экономической и экологической точек зрения, из 4,6-дихлор-2-(метилтио)-1,3-пиримидина реакцией этого последнего соединения с метоксидом щелочного металла, окислением полученного 4,6-диметокси-2-(метилтио)-1,3-пиримидина без выделения непосредственно до соответствующего 2-метилсульфонилпиримидинового производного и его отделением на последующей стадии очистки в том же реакционном сосуде по принципу процесса в одном реакторе от любых образующихся побочных продуктов, предоставляя возможность для непосредственного использования, например, при получении гербицидов в соответствии с ЕР-В 0447506.
Соответственно по настоящему изобретению предлагается способ получения 4,6-диметокси-2-(метилсульфонил)-1,3-пиримидина реакцией 4,6-дихлор-2-(метилтио)-1,3-пиримидина в инертном органическом растворителе с метоксидом щелочного металла, переносом полученного 4,6-диметокси-2-(метилтио)-1,3-пиримидина в водную кислую среду и последующим окислением этого соединения в присутствии, если это уместно, катализатора, где за окислением следует стадия очистки, на которой значение рН водной кислой реакционной смеси водным основанием доводят до интервала от 5 до 8 и перемешивают либо в присутствии, либо в отсутствии органического растворителя.
На первой стадии (схема реакции 1) взаимодействие 4,6-дихлор-2-(метилтио)-1,3-пиримидина с метоксидом щелочного металла целесообразно проводить в несмешивающемся с водой инертном органическом растворителе, таком как углеводород, например в ароматическом углеводороде, таком как бензол, толуол или изомерные ксилолы, предпочтительно в толуоле, при реакционных температурах от 0°С до точки кипения используемого растворителя, предпочтительно при температурах от 20 до 60°С.
В качестве метоксида щелочного металла в предпочтительном варианте используют метоксид натрия или метоксид калия, а особенно предпочтительно 30%-ный раствор метоксида натрия в метаноле или твердый метоксид натрия (например, 95%-ный), где для реакции замещения используют от 2 до 3 молярных экв., предпочтительно от 2,05 до 2,50 молярных экв., метоксида, в пересчете на 1 моль 4,6-дихлор-2-(метилтио)-1,3-пиримидина. В предварительно загруженный раствор 4,6-дихлор-2-(метилтио)-1,3-пиримидина в указанном температурном интервале в течение от 2 до 6 ч соответствующим образом по каплям добавляют раствор метоксида или добавляют соответственно твердый метоксид и затем реакционную смесь перемешивают при температуре от 50 до 60°С в течение от 5 до 10 ч или до тех пор, пока уже больше невозможно обнаружить исходный материал.
По прошествии этого времени реакции образовавшуюся смесь подготавливают для окисления на второй стадии. Для оптимизации выхода продукта вначале можно отогнать под пониженным давлением некоторое количество содержащегося в реакционной смеси метанола, причем после отгонки от 50 до 90% от общего количества метанола дистилляцию завершают. Затем в конечную реакционную смесь добавляют воды и не смешивающегося с водой образующего азеотроп инертного органического растворителя, например толуола, и всю смесь нагревают с перемешиванием до температуры от 30 до 80°С, предпочтительно от 30 до 60°С. После охлаждения водную фазу отделяют и для оптимизации выхода продукта еще раз смешивают с инертным органическим растворителем и нагревают с перемешиванием до температуры от 30 до 80°С, предпочтительно от 30 до 60°С. После охлаждения водную фазу отделяют и выбрасывают, а обе органические фазы объединяют и в существенной степени выпаривают под пониженным давлением. К полученному остатку добавляют воды, нагретой до температуры от 40 до 80°С, и весь остаток органического растворителя отгоняют азеотропной перегонкой до тех пор, пока в дистилляте может быть обнаружена только вода.
Окисление полученного 4,6-диметокси-2-(метилтио)-1,3-пиримидина на второй стадии (схема реакции 1) соответствующим образом проводят в протонном растворителе или смеси протонных растворителей и, в зависимости от используемого окислителя, в присутствии, если это уместно, катализатора.
Таким образом, в приготовленную водную реакционную смесь с первой стадии концентрированную кислоту, такую как карбоновая кислота, например 100%-ная уксусная кислота, целесообразным путем добавляют до тех пор, пока не образуется водный раствор соответствующей карбоновой кислоты концентрацией от 1 до 80%, предпочтительно от 2 до 10%. С этой целью, в зависимости от используемого окислителя, добавляют от 0,1 до 0,2 мол.% в пересчете на 4,6-диметокси-2-(метилтио)-1,3-пиримидин катализатора, такого как вольфрамат, например вольфрамат натрия, и эту смесь нагревают до температуры от 70 до 90°С, предпочтительно от 75 до 80°С. Затем по каплям добавляют от 2 до 4 молей, предпочтительно от 2,1 до 3 молей, в пересчете на 4,6-диметокси-2-(метилтио)-1,3-пиримидин окислителя, такого как пероксид, например 20-35%-ный раствор пероксида водорода. Указанную реакционную температуру процесса экзотермического окисления поддерживают в течение от 1 до 6 ч или до тех пор, пока до метилсульфонилпиримидина не окислится весь метилтиопиримидин или метилсульфоксидпиримидин.
После завершения окисления избыток окислителя, содержащегося в реакционной смеси, разрушают по обычному методу, который специалисту в данной области техники известен, например добавлением 40%-ного водного раствора бисульфита натрия в реакционную смесь до тех пор, пока уже больше невозможно обнаружить окислитель (тест с иодидом калия/крахмалом), и обработанную таким путем реакционную смесь подготавливают для последующей стадии очистки, которую осуществляют в том же реакционном сосуде.
Одна особенность последовательности реакций в соответствии с изобретением состоит в стадии очистки, которую осуществляют по принципу процесса в одном реакторе, в том же реакционном сосуде, и которая обусловливает большие преимущества для промышленных процессов, поскольку в результате можно избежать сложного разделения и стадий очистки и уменьшить затраты на оборудование.
С этой целью вначале при температуре от 10 до 90°С рН водной кислой реакционной смеси, полученной при осуществлении предыдущей двухстадийной последовательности реакций, водным основанием доводят до интервала 5-8, а затем либо в соответствии с
вариантом А) эту полученную водную фазу перемешивают в температурном интервале от 10 до 90°С и при указанном значении рН в течение от 0,5 до 5 ч, либо
вариантом Б) смешивают с не смешивающимся с водой инертным органическим растворителем, таким как ароматический углеводород, например бензол, толуол или изомерные ксилолы, и образовавшуюся двухфазную систему перемешивают с добавлением, если это уместно, межфазного катализатора в температурном интервале от 10 до 90°С и при указанном значении рН в течение от 0,5 до 5 ч, либо
вариантом В) смешивают со смешивающимся с водой органическим растворителем, например со спиртом, с приготовлением таким образом водной органической однофазной системы, которую перемешивают в температурном интервале от 10 до 90°С и при указанном значении рН в течение от 0,5 до 5 ч.
Во время осуществления этой стадии побочные продукты, образовавшиеся в количестве <10%, конкретно 2,4-бис(метилсульфонил)-6-метокси-1,3-пиримидин, гидролизуют до водорастворимых побочных продуктов, конкретно до 2-гидрокси-4-(метилсульфонил)-6-метокси-1,3-пиримидина и 6-гидрокси-2-(метилсульфонил)-4-метокси-1,3-пиримидина, за уменьшением и увеличением количеств которых с течением времени соответственно в органической фазе и в водной фазе можно следить непосредственно, например с помощью ГХ, ВЭЖХ или ТСХ (схема реакции 2).
Предпочтительным водным основанием является водный раствор гидроксида, например гидроксида щелочного металла. Предпочтение отдают использованию 30%-ного водного раствора гидроксида натрия. Приемлемым не смешивающимся с водой ароматическим углеводородом в соответствии с вариантом Б) является, в частности, толуол, а приемлемыми смешивающимися с водой органическими растворителями в соответствии с вариантом В) являются, в частности, метанол и этанол.
В случае варианта А) после перемешивания в водной фазе (гидролиз) существует возможность либо в варианте АБ) добавлять не смешивающийся с водой инертный органический растворитель и, если это уместно, межфазный катализатор, как в варианте Б), либо в варианте АВ) добавлять смешивающийся с водой органический растворитель, как сказано в варианте В), с целью упростить выделение продукта с последующим перемешиванием полученной двухфазной [вариант А)+АБ)] или водно-органической однофазной системы [вариант А)+АВ)] в течение от 5 до 15 мин и проводить обработку аналогично тому, как это изложено соответственно в вариантах Б) и В).
В случае двухфазной системы в соответствии с вариантом Б) или А)+АБ) водную фазу отделяют и для завершения экстракции необходимого, целевого соединения еще раз смешивают с тем же не смешивающимся с водой органическим растворителем, как это изложено выше, и всю двухфазную систему перемешивают в течение от 5 до 15 мин. После охлаждения водную фазу отделяют, обе органические фазы объединяют и органический растворитель отгоняют под пониженным давлением. Схема реакции 2 иллюстрирует этот способ обогащения [варианты В) и А)+АВ)].
Приемлемые межфазные катализаторы для вариантов Б) и А)+АБ) представляют собой, например, катализаторы, перечисленные в Angew.Chem., Int.Ed.Engl. 13, 170-179 (1974), в частности четвертичные аммониевые соли, например тетраалкиламмонийгалогениды, в частности трикаприлметиламмонийхлорид (продукт Aliquat 336). Межфазные катализаторы ускоряют гидролиз побочных продуктов, а в качестве солюбилизаторов повышают эффективность растворения этих гидролизованных побочных продуктов в водной фазе. Межфазные катализаторы используют в количествах от 0,1 до 10 мольных % в пересчете на продукт, 4,6-диметокси-2-(метилсульфонил)-1,3-пиримидин.
В соответствии с вариантами В) и А)+АВ) необходимое, целевое соединение находится в форме суспензии, которая обладает низкой водорастворимостью и может быть легко выделена из водной органической фазы фильтрованием, тогда как гидролизованные и водорастворимые побочные продукты, например 2-гидрокси-4-(метилсульфонил)-6-метокси- и 6-гидрокси-2-(метилсульфонил)-4-метокси-1,3-пиримидины, остаются в растворе.
Этот способ обогащения [варианты В) и А)+АВ)] иллюстрирует схема реакции 2.
Для оптимизации выхода продукта в вариантах В) и АВ) долю добавляемых смешивающихся с водой органических растворителей поддерживают как раз на таком уровне, при котором, с одной стороны, гарантируется гомогенность реакционной смеси, а с другой стороны, потери выхода продукта оказываются настолько низкими, насколько это возможно. Обычно доля смешивающихся с водой растворителей находится в интервале от 5 до 50 мас.% в пересчете на количество водной кислой реакционной смеси. Если концентрация смешивающихся с водой органических растворителей оказывается слишком высокой, растворимость целевого соединения в водной среде возрастает, в результате чего уменьшается выход продукта.
В предпочтительных вариантах А), Б) и В) используемое водное основание представляет собой, например, гидроксид, в частности гидроксид щелочного металла, который добавляют по каплям с перемешиванием при реакционных температурах от 10 до 90°С в водную кислую реакционную смесь до тех пор, пока рН реакционной смеси не достигает интервала от 5 до 8, после чего образовавшуюся смесь перемешивают в температурном интервале и интервале рН, которые указаны выше, в течение от 0,5 до 5 ч в соответствии с вариантом A) без добавления органического растворителя, в соответствии с вариантом Б) после добавления органического растворителя, например ароматического углеводорода, в частности бензола, толуола или изомерных ксилолов, или в соответствии с вариантами В) после добавления органического растворителя, например спирта. Среди них предпочтение отдают тем вариантам, в которых используемое водное основание представляет собой 30%-ный водный раствор гидроксида натрия, который добавляют по каплям при реакционных температурах от 75 до 85°С в водную кислую реакционную смесь до тех пор, пока рН не достигает уровня от 6 до 7, после чего либо не добавляют органического растворителя [вариант А)], либо добавляют органический растворитель, в частности толуол [вариант Б)] или метанол или этанол [вариант B)], и эту смесь перемешивают в температурном интервале от 20 до 80°С и в интервале рН, который указан выше, в течение от 1 до 3 ч.
В особенно предпочтительном варианте Б) органический не смешивающийся с водой растворитель, который добавляют в водную реакционную смесь, представляет собой толуол, и при этом в качестве межфазного катализатора используют трикаприлметиламмонийхлорид (продукт Aliquat 336) в количестве от 0,5 до 5 мольных % в пересчете на полученный 4,6-диметокси-2-(метилсульфонил)-1,3-пиримидин.
Промежуточный продукт, 4,6-диметокси-2-(метилтио)-1,3-пиримидин (не выделен, схема реакции 1), является химически стабильным и мог бы быть выделен из реакционной смеси без каких-либо проблем.
Соответственно в качестве альтернативы предлагаемому способу с первоначально двухстадийной последовательностью реакций получения 4,6-диметокси-2-(метилсульфонил)-1,3-пиримидина, исходя из 4,6-дихлор-2-(метилтио)-1,3-пиримидина, существует также возможность применения первоначально одностадийного способа, в котором исходный материал, 4,6-диметокси-2-(метилтио)-1,3-пиримидин, окисляют в водной кислой среде в присутствии, если это уместно, катализатора, где стадию очистки в соответствии с настоящим изобретением осуществляют после окисления. По настоящему изобретению предлагается также этот альтернативный способ.
Схема реакции 2
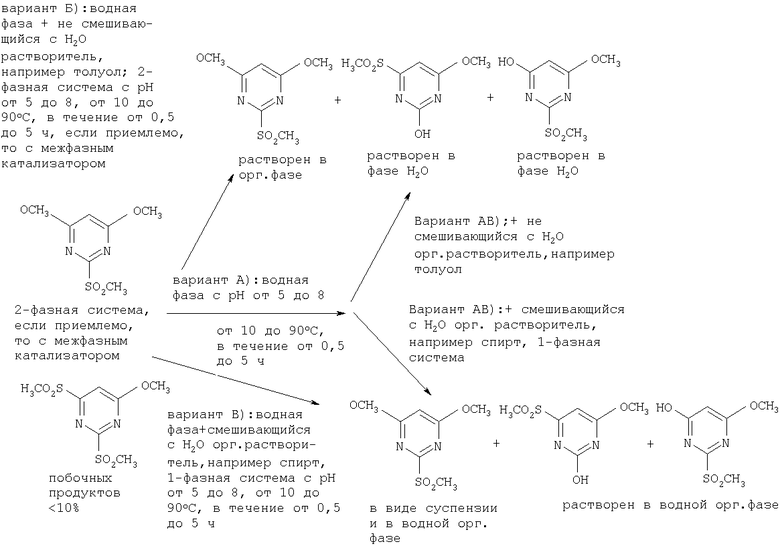
Общий выход выделенного продукта, 4,6-диметокси-2-(метилсульфонил)-1,3-пиримидина, обычно составляет >75%, причем степень чистоты конечного продукта составляет >98%.
Исходный материал, 4,6-дихлор-2-(метилтио)-1,3-пиримидин, известен, например, из J.Org.Chem. 26, 792 (1961). Точно так же известны все используемые реагенты, такие как метоксиды и окислители, и межфазные катализаторы или они могут быть получены по известным способам.
Предлагаемый в соответствии с изобретением способ отличается от известных способов тем, что
1) при его осуществлении целевое соединение, 4,6-диметокси-2-(метилсульфонил)-1,3-пиримидин, получают с высокими степенью чистоты и выходом,
2) его можно осуществлять в многоцелевой установке,
3) его можно осуществлять проведением как непрерывного, так и периодического (не непрерывного) процессов,
4) что касается стадии 2 (окисление) и стадии очистки, то предусмотрено их осуществление "по принципу процесса в одном реакторе",
5) его осуществление не требует проведения сложной перекристаллизации, которая связана с потерей продукта,
6) его осуществление является экономически и экологически целесообразным путем простого и непосредственного доступа к 4,6-диметокси-2-(метилсульфонил)-1,3-пиримидину и
7) его осуществление позволяет проводить in situ последующие реакции, например превращение в 7-[(4,6-диметоксипиримидин-2-ил)тио]фталидные производные.
Таким образом, в сравнении с известными способами предлагаемый способ обладает следующими преимуществами:
1) он особенно приемлем для проведения промышленных процессов,
2) его осуществление позволяет избежать сложных стадий разделения и очистки,
3) его осуществление позволяет легко возвращать в процесс органические растворители (например, толуол и метанол) и/или избегать создающих проблемы отходов (образуются только вода и соли, например хлорид натрия и сульфат натрия, и/или ацетат натрия) и
4) его осуществление позволяет непосредственно in situ проводить дальнейшую обработку образовавшегося 4,6-диметокси-2-(метилсульфонил)-1,3-пиримидина.
4,6-диметокси-2-(метилсульфонил)-1,3-пиримидин, полученный в соответствии с изобретением, является важным промежуточным продуктом в синтезе гербицидов, который используют конкретно в качестве промежуточного продукта при получении обладающего гербицидным действием 7-[(4,6-диметоксипиримидин-2-ил)тио]-3-метилнафталида, как об этом сказано, например, в ЕР-В 0447506 и как проиллюстрировано на схеме реакции 1.
Схема реакции 1
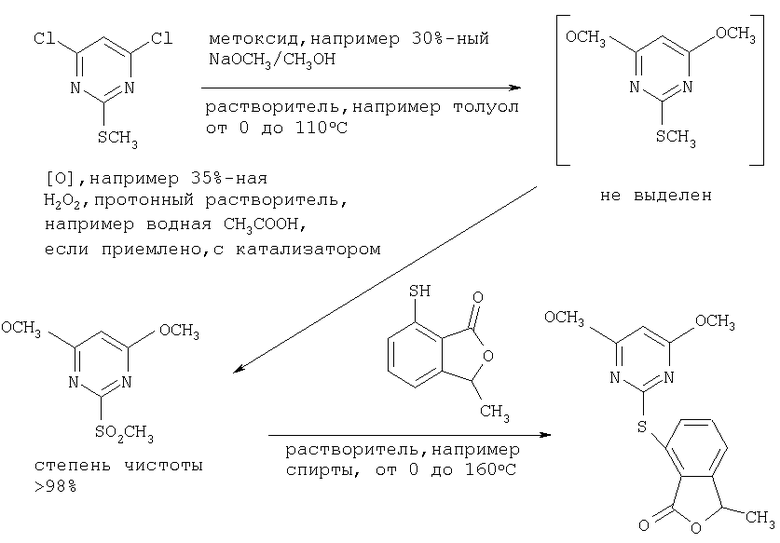
Используемый исходный материал представляет собой 4,6-дихлор-2-(метилтио)-1,3-пиримидин, который в соответствии со схемой реакции 1 и как изложено выше на первой стадии в инертном органическом растворителе вводят во взаимодействие с метоксидом щелочного металла с получением 4,6-диметокси-2-(метилтио)-1,3-пиримидинового промежуточного продукта, который не выделяют, инертный органический растворитель заменяют водным протонным растворителем, а на второй стадии соответствующий 4,6-диметокси-2-(метилсульфонил)-1,3-пиримидин получают в чистом виде окислением и последующим этапом очистки, предусмотренными для проведения по принципу процесса в одном реакторе. Последующую реакцию полученного 4,6-диметокси-2-(метилсульфонил)-1,3-пиримидина с 7-меркапто-3-метилнафталидом согласно схеме реакции 1 соответствующим образом проводят в инертном органическом растворителе, например в спиртах, простых эфирах, кетонах, нитрилах или амидах, в частности в изопропаноле, тетрагидрофуране, бутаноне, ацетонитриле или N,N-диметилформамиде, при температурах от 0 до 160°С. Такие реакции замещения описаны, например, в ЕР-В 0447506.
Способ в соответствии с изобретением более подробно проиллюстрирован приведенным ниже примером,
Пример H1: получение 4,6-диметокси-2-(метилсульфонил)-1,3-пиримидина
При температуре от 20 до 25°С в колбу, снабженную мешалкой, термометром, капельной воронкой, дистилляционной насадкой и датчиком рН, вначале в виде раствора в толуоле (55,7%) загружают 525,6 г 4,6-дихлор-2-(метилтио)-1,3-пиримидина (1,5 моля) и при температуре от 40 до 42°С в течение 4-часового периода по каплям добавляют 583,2 г 30%-ного раствора метоксида натрия (3,24 моля). Эта реакция является экзотермической и протекает с образованием легко перемешиваемой суспензии (хлорид натрия). По прошествии примерно 1 ч реакционную температуру повышают до интервала от 54 до 56°С и смесь перемешивают при этой температуре в течение от 5 до 6 ч, до тех пор, пока не устанавливают, например газовой хроматографией, полноту превращения. Далее под пониженным давлением при 60°С из реакционной смеси отгоняют некоторое количество метанола, т.е. до тех пор, пока не получают примерно 363 г дистиллята. В дальнейшем к остатку реакционной смеси вначале добавляют 360 г толуола, а затем 750 г воды и смесь перемешивают до тех пор, пока не достигают температуры от 40 до 42°С. Смеси дают постоять в течение 15 мин и затем водную фазу (примерно 921 г) отделяют, смешивают с дополнительными 150 г толуола и перемешивают при температуре от 40 до 42°С в течение 5 мин. Далее водной фазе дают постоять в течение 15 мин, после чего ее отделяют и выбрасывают, а обе толуольные фазы объединяют и в существенной степени выпаривают под пониженным давлением при 80°С. К полученному остатку добавляют 330 г воды, предварительно нагретой до 60°С, а оставшийся толуол отгоняют азеотропной перегонкой до тех пор, пока в дистилляте не может быть обнаружена только вода.
Затем в не содержащий толуола водный остаток добавляют 36 г 100%-ной уксусной кислоты (0,6 моля) и 0,5 г вольфрамата натрия (0,0015 моля) и всю смесь нагревают до температуры от 78 до 80°С. При этой температуре по каплям с интенсивным перемешиванием в течение 4-часового периода добавляют 350 г 35%-ного раствора пероксида водорода (3,6 моля). Окисление является экзотермическим процессом, и перемешивание продолжают при температуре от 78 до 80°С в течение от 1 до 2 ч, до тех пор, пока ГХ анализ не показывает полноту превращения, т.е. отсутствие 4,6-диметокси-2-(метилсульфоксид)-1,3-пиримидина. Для деструкции избытка окислителя 110 г раствора бисульфита натрия (40%-ный, 0,412 моля) в реакционную смесь добавляют по каплям в течение 30-минутного периода, до тех пор, пока тест с KI/крахмальной бумажкой не дает отрицательного результата. Затем в водную кислую реакционную смесь добавляют 750 г толуола и при температуре от 78 до 80°С 30%-ный водный раствор гидроксида натрия (примерно 130 г, 0,975 моля) добавляют по каплям до тех пор, пока рН не достигает 6,5, после чего перемешивание продолжают при температуре от 78 до 80°С в течение от 1 до 3 ч, до тех пор, пока побочный продукт не прореагирует и не мигрирует в водную фазу [в соответствии с ГХ анализом в толуольной фазе обнаруживают наличие <0,2% 2,4-бис(метилсульфонил)-6-метокси-1,3-пиримидина]. Реакционной смеси дают постоять в течение 15 мин, а затем водную фазу отделяют и смешивают со 150 г толуола, после чего всю смесь перемешивают при температуре от 75 до 80°С в течение 5 мин. С целью добиться хорошего разделения фаз образовавшейся двухфазной системе дают постоять, водную фазу (800 г) отделяют и выбрасывают, а обе толуольные фазы объединяют и выпаривают при температуре 70°С под пониженным давлением до тех пор, пока не получают примерно 564 г дистиллята. Целевой продукт кристаллизуется даже во время дистилляции. После охлаждения до температуры от 0 до 5°С смесь отфильтровывают, а кристаллический остаток промывают один раз толуолом и охлаждают до температуры от 0 до 5°С. Кристаллический продукт сушат под пониженным давлением при 50°С. В результате получают 251,3 г целевого 2,4-диметокси-2-(метилсульфонил)-1,3-пиримидина (выход: 76,4% от теоретического) степени чистоты >99% (в соответствии с ГХ анализом, колонка OV 1701).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ТИОБАРБИТУРОВОЙ КИСЛОТЫ | 2000 |
|
RU2242467C2 |
| СПОСОБ ПОЛУЧЕНИЯ СЕЛЕКТИВНОГО ИНГИБИТОРА ЦИКЛООКСИГЕНАЗЫ-2 | 2011 |
|
RU2591848C2 |
| ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ | 1991 |
|
RU2062576C1 |
| ПИРИДИНСУЛЬФОНАМИД И ЕГО ПРИГОДНЫЕ В СЕЛЬСКОМ ХОЗЯЙСТВЕ СОЛИ, ГИДРАТЫ ИЛИ КОМПЛЕКСЫ СО СПИРТАМИ C - C, ГЕРБИЦИДНЫЕ КОМПОЗИЦИИ, СПОСОБ БОРЬБЫ С НЕЖЕЛАТЕЛЬНОЙ РАСТИТЕЛЬНОСТЬЮ, СПОСОБ БОРЬБЫ С ЛИСОХВОСТОМ, ПРОМЕЖУТОЧНЫЙ ПРОДУКТ ДЛЯ ЕГО СИНТЕЗА | 1993 |
|
RU2117666C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ ФТАЛИДОВ ИЛИ ГЕТЕРОЦИКЛИЧЕСКИХ ФТАЛИДОВ | 1991 |
|
RU2040522C1 |
| ПРОИЗВОДНЫЕ КАРБОНОВЫХ КИСЛОТ | 1995 |
|
RU2180335C2 |
| СПОСОБ ПОЛУЧЕНИЯ 2-ЗАМЕЩЕННЫХ 4,6-ДИАЛКОКСИПИРИМИДИНОВ,2-N-БУТИЛАМИНО-4,6-ДИМЕТОКСИПИРИМИДИН И СПОСОБ ПОЛУЧЕНИЯ ГАЛОГЕНПРОИЗВОДНЫХ ПИРИМИДИНА | 1992 |
|
RU2117007C1 |
| СПОСОБ ПОЛУЧЕНИЯ СОЕДИНЕНИЙ ТИЕНОПИРИМИДИНА | 2013 |
|
RU2637309C2 |
| ЗАМЕЩЕННЫЕ ДИАМИНОКАРБОКСАМИДНЫЕ И ДИАМИНОКАРБОНИТРИЛЬНЫЕ ПРОИЗВОДНЫЕ ПИРИМИДИНОВ, ИХ КОМПОЗИЦИИ И СПОСОБЫ ЛЕЧЕНИЯ С ИХ ПОМОЩЬЮ | 2012 |
|
RU2625309C2 |
| СПОСОБ ОБРАЗОВАНИЯ КАЛЬЦИЕВОЙ СОЛИ (Е)-7-[4-(4-ФТОРФЕНИЛ)-6-ИЗОПРОПИЛ-2-[МЕТИЛ(МЕТИЛСУЛЬФОНИЛ)АМИНО]ПИРИМИДИН-5-ИЛ](3R,5S)-3,5-ДИГИДРОКСИГЕПТ-6-ЕНОВОЙ КИСЛОТЫ (КАЛЬЦИЕВОЙ СОЛИ РОЗУВАСТАТИНА) | 2004 |
|
RU2361864C2 |
Изобретение относится к улучшенному способу получения 4,6-диметокси-2-(метилсульфонил)-1,3-пиримидина реакцией 4,6-дихлор-2-(метилтио)-1,3-пиримидина в инертном органическом растворителе с метоксидом щелочного металла, переносом полученного 4,6-диметокси-2-(метилтио)-1,3-пиримидина в водную кислую среду и последующим окислением этого соединения в присутствии, если это уместно, катализатора, предпочтительно межфазного катализатора, такого как трикаприлметиламмонийхлорид. Затем проводят очистку, на которой рН водной кислой реакционной смеси водным основанием, таким как гидроксид щелочного металла, например гидроксида натрия, доводят до интервала от 5 до 8 при температуре 10-90°С и перемешивают либо в присутствии, либо в отсутствии органического растворителя, например ароматического углеводорода, такого как бензол, толуол или изомерные ксилолы, или спирта, такого как метанол или этанол. Изобретение относится к применению полученного соединения в качестве промежуточного продукта для синтеза гербиуида, в частности 7-[(4,6-диметоксипиримидин-2-ил)тио]-3-метилфталида реакцией с 7-меркапто-3-метилфталидомсоединения при получении гербицидов, например 7-[(4,6-диметоксипиримидин-2-ил)тио]-3-метилфталида. 3 н. и 21 з.п. ф-лы.
| NEZU YUKIO | |||
| Dimethoxypyrimidines as novel Herbicides | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Synthesis and herbicidal activity of O-pyriminylsalicylates and analogs | |||
| Pesticide Science(English) | |||
| Способ очищения сернокислого глинозема от железа | 1920 |
|
SU47A1 |
| US 5149357 A, 22.09.1992 | |||
| СПОСОБ ОПРЕДЕЛЕНИЯ РАССТОЯНИЙ СВЕТОПРОЕКЦИОННЫМ ДАЛЬНОМЕРОМ | 0 |
|
SU209779A1 |
| Способ получения хромовокислых и двухромовокислых солей | 1931 |
|
SU46213A1 |
| СПОСОБ ПОЛУЧЕНИЯ 2-ЗАМЕЩЕННЫХ 4,6-ДИАЛКОКСИПИРИМИДИНОВ,2-N-БУТИЛАМИНО-4,6-ДИМЕТОКСИПИРИМИДИН И СПОСОБ ПОЛУЧЕНИЯ ГАЛОГЕНПРОИЗВОДНЫХ ПИРИМИДИНА | 1992 |
|
RU2117007C1 |
| KOPPEL HENRY С | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| J | |||
| of Organic Chemistry | |||
| Судно | 1925 |
|
SU1961A1 |
Авторы
Даты
2006-05-10—Публикация
2001-07-19—Подача