Изобретение относится к химической промышленности, а именно, к способу получения металлокомплексов тетра-(5,8-дигидрокси)-антрахинонопорфиразина, которые могут быть использованы в качестве катализаторов, красителей и в других областях науки и техники.
Уровень техники
Известен способ получения металлокомплексов тетра-(5,8-дигидрокси)антрахинонопорфиразина [Борисов А.В., Побединская И.А., Майзлиш В.Е., Шапошников Г.П. Синтез и свойства тетраантрахинонопорфиразинов. Тез. докл. IX Международная конференция по химии порфиринов и их аналогов 8-12 сентября 2003 г. г.Суздаль. Труды конференции Иваново, 2003. С.95-96], включающий взаимодействие 2,3-дикарбокси-5,8-дигидроксиантрахинона с мочевиной и ацетатом меди или кобальта в присутствии хлорида аммония и молибдата аммония.
Способ реализуется в одну стадию:
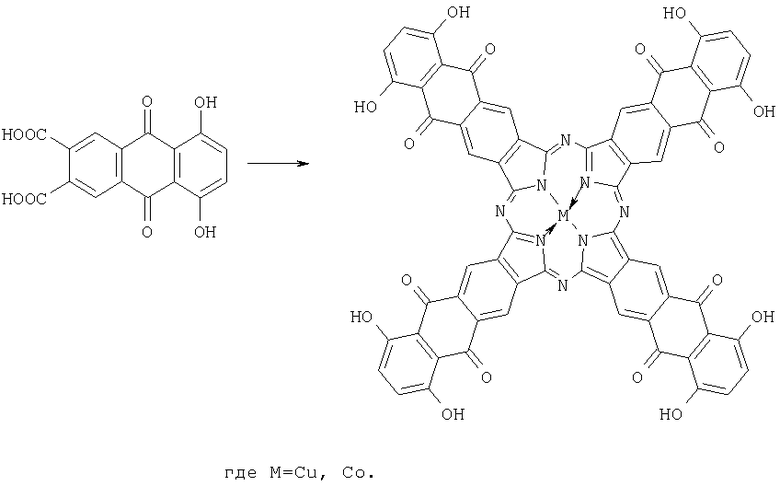
Недостатком этого способа является малый выход целевого продукта - не более 11%.
Сущность изобретения
Изобретательская задача состояла в поиске способа получения металлокомплексов тетра-(5,8-дигидрокси)антрахинонопорфиразина взаимодействием замещенного 2,3-дикарбоксиантрахинона с мочевиной, солью соответствующего металла в присутствии хлорида и молибдата аммония, который позволил бы повысить выход целевого продукта.
Поставленная цель достигается способом получения металлокомплексов тетра-(5,8-дигидрокси)антрахинонопорфиразина взаимодействием замещенного 2,3-дикарбоксиантрахинона с мочевиной, солью соответствующего металла в присутствии хлорида и молибдата аммония, в котором в качестве замещенного 2,3-дикарбоксиантрахинона используют 2,3-дикарбокси-5,8-диметоксиантрахинон, полученный металлокомплекс тетра-(5,8-диметокси)антрахинонопорфиразина подвергают гидролизу путем обработки его гидроксидом натрия.
Предложенный способ позволяет получать целевой продукт с выходом не менее 24%.
Сведения, подтверждающие возможность осуществления изобретения.
Для реализации способа используются следующие вещества:
мочевина - ГОСТ 2081-92
ацетат меди - ГОСТ 5852-70
ацетат кобальта - ГОСТ 5861-79
молибдат аммония - ГОСТ 2677-78
хлорид аммония - ГОСТ 2210-73
Поскольку 2,3-дикарбокси-5,8-диметоксиантрахинон является новым соединением и не выпускается промышленностью, он был получен следующим способом: сначала проводят ацилирование диметилового эфира гидрохинона диангидридом пиромеллитовой кислоты в присутствии безводного хлористого алюминия, затем проводят внутримолекулярную циклизацию путем обработки полученной на первой стадии 5-(2,5-диметокси)бензоилтримеллитовой кислоты концентрированной серной кислотой (моногидратом). В результате внутримолекулярной циклизации получают 2,3-дикарбокси-5,8-диметоксиантрахинон.
Стадия 1. В колбу, снабженную мешалкой, термометром и обратным холодильником, помещают 10.0 г (0.046 моль) диангидрида пиромеллитовой кислоты, 12.66 г (0.091 моль) диметилового эфира гидрохинона и 20 мл гептана. Массу нагревают до 50°С и при интенсивном перемешивании прибавляют 20.0 г (0.154 моль) безводного хлористого алюминия. Выдерживают 3 часа при температуре кипения реакционной массы и отгоняют гептан под вакуумом. Затем реакционную массу нагревают до 120-130°С и выдерживают в течение 6 часов. После охлаждения к реакционной массе добавляют 50 мл воды и 10 мл концентрированной соляной кислоты и перемешивают еще 12 часов. Осадок после фильтрации промывают горячей водой, затем помещают в 10%-ный раствор соды и кипятят в течение 30-40 минут. Горячий раствор фильтруют, осадок обрабатывают таким же образом еще 3 раза. Фильтраты объединяют, подкисляют соляной кислотой до рН 4 и охлаждают до 10-15°С. Выпавший осадок отфильтровывают, промывают водой до нейтральной среды и отсутствия хлорид-ионов и сушат при 80°С.
Получена 5-((2,5-диметокси)бензоил)тримеллитовая кислота.
Стадия 2. В колбу объемом 200 мл, снабженную мешалкой и термометром, помещают 10 мл концентрированной серной кислотой (моногидрата) и нагревают до 130°С. Затем в течение 15 минут при интенсивном перемешивании вносят 5 г полученной 5-((2,5-диметокси)-бензоил)тримеллитовой кислоты, температуру поднимают до 150°С и выдерживают в течение 5 часов. Массу после охлаждения при перемешивании выливают в 200 мл воды, фильтруют, промывают большим количеством ледяной воды, растворяют в содовом растворе и подкисляют соляной кислотой. Осадок отфильтровывают и промывают водой до исчезновения хлорид-ионов. Такую обработку повторяют дважды. Сушат при 100°С.
Найдено, %: С-60.1; Н-3.5;. C18H12O8.
Вычислено, %: С-60.7; Н-3.4.
Выход: 4.0 г (86%). Температура плавления - 354°С.
Полученный целевой продукт - 2,3-дикарбокси-5,8-диметоксиантрахинон - твердое вещество белого цвета, растворимо в водно-щелочных растворах, горячей воде, ацетоне, ДМФА.
Заявленный способ реализуют в две стадии:
Взаимодействием 2,3-дикарбокси-5,8-диметоксиантрахинона с мочевиной, солью соответствующего металла в присутствии хлорида и молибдата аммония, получают металлокомплекс тетра-(5,8-диметокси)антрахинонопорфиразина, который подвергают гидролизу для получения целевого продукта.
Пример 1. Синтез тетра-(5,8-дигидрокси)антрахинонопорфиразина меди.
Стадия 1. В пробирку из кварцевого стекла помещают растертую смесь 0.2 г (0.56 ммоль) 2,3-дикарбокси-5,8-диметоксиантрахинона, 0.24 г (4.0 ммоль) мочевины, 0.036 г (0.18 ммоль) ацетата меди, 0.02 г (0.4 ммоль) хлорида аммония и 0.002 г (0.01 ммоль) молибдата аммония. Массу медленно нагревают до 180°С в течение часа и выдерживают 3 часа. Очистку целевого продукта проводят последовательной промывкой 5%-ной соляной кислотой, ацетоном и переосаждением из серной кислоты.
Выход тетра-(5,8-диметокси)антрахинонопорфиразина меди 0.06 г (32%).
Стадия 2. В пробирку из кварцевого стекла помещают растертую смесь 0.2 г (0.15 ммоль) тетра-(5,8-диметокси)антрахинонопорфиразина меди 10 мл 1%-ного раствора гидроксида натрия и нагревают на водяной бане 40-50 мин. Выделение полученного тетра-(5,8-дигидрокси)антрахинонопорфиразина меди производят подкислением реакционной массы концентрированной соляной кислотой с дальнейшей фильтрацией и промывкой целевого продукта водой до нейтральной среды. Сушат при 75-80°С.
Выход тетра-(5,8-дигидрокси)антрахинонопорфиразина меди 0.15 г (82%).
Темно-синее вещество, обладает растворимостью в водно-щелочных растворах, ДМФА, концентрированной серной кислоте.
Электронный спектр поглощения в водно-щелочном растворе, λmax, нм: 681 (фиг.1).
Найдено, %: С 62.9; Н 1.9; N 9.3. C64N8H24O16Cu.
Вычислено,%: С 62.8; Н 2.0; N 9.2.
Общий выход тетра-(5,8-дигидрокси)антрахинонопорфиразина меди составляет (0.32×0.82)×100=26.2%.
Пример 2. Синтез тетра-(5,8-дигидрокси)антрахинонопорфиразина кобальта.
Стадия 1. Синтез проводят аналогично стадии 1 примера 1, но вместо ацетата меди используют 0.038 г (0.18 ммоль) ацетата кобальта.
Выход тетра-(5,8-диметокси)антрахинонопорфиразина кобальта: 0.06 г (32%).
Стадия 2. Синтез ведут аналогично стадии 2 примера 1, но вместо тетра-(5,8-диметокси)антрахинонопорфиразина меди используют 0.2 г (0.15 ммоль) тетра-(5,8-диметокси)антрахинонопорфиразина кобальта.
Выход тетра-(5,8-дигидрокси)антрахинонопорфиразина кобальта: 0.14 г (77%).
Темно-синее вещество, обладает растворимостью в водно-щелочных растворах, ДМФА, концентрированной серной кислоте.
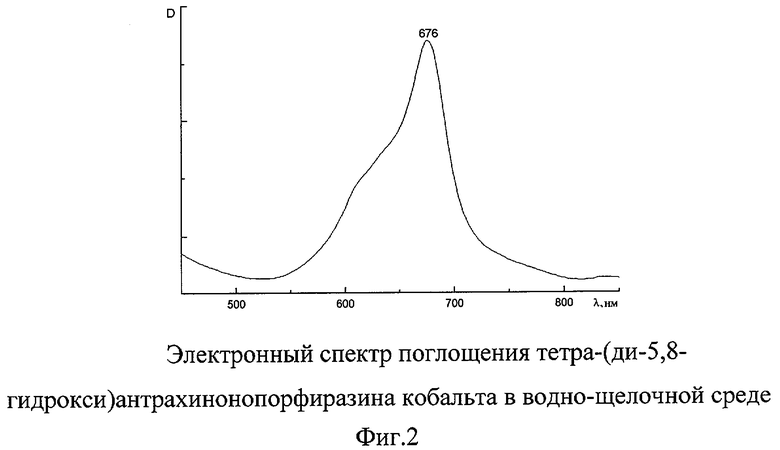
Электронный спектр поглощения в водно-щелочном растворе, λmax, нм: 676 (фиг.2).
Найдено, %: С 63.1; Н 2.0; N 9.3. C64N8H24O16Co.
Вычислено, %: С 63.0; Н 2.0; N 9.2.
Общий выход тетра-(5,8-дигидрокси)антрахинонопорфиразина кобальта составляет (0.32×0.77)×100=24.6%
Заявленные соединения могут быть использованы для окрашивания хлопчатобумажных и вискозных материалов [Лабораторный практикум по применению красителей / Под ред. Мельникова Б.Н. М.: Химия-1972. 342 c.].
Пример 3. Образец хлопчатобумажной ткани массой 1 г смачивают в течение 0.5 мин, отжимают до 100% привеса и помещают в красильную ванну состава (г/л):
В течение 15-30 мин нагревают раствор до кипения и выдерживают 1 час. Затем образец отжимают, тщательно промывают теплой, затем холодной водой, сушат (фиг.3).
Заявленные соединения могут быть использованы в качестве катализаторов окисления сернистых соединений.
Пример 4. Использование тетра-(5,8-дигидрокси)антрахинонопорфиразина кобальта в качестве катализатора в реакции жидкофазного окисления цистеина. Каталитическую активность определяли по методике [Шикова Т.Г. Исследование влияния химической модификации фталоцианина - лиганда на каталитические свойства его металлокомплексов. Дис... канд. хим. наук. Иваново, 1999. 156 с.]
Опыты проводили в жидкой фазе в реакционном сосуде, укрепленном на быстроходной качалке (350 кач/мин), термостатированном с точностью ±0.2°С. Скорость реакции измеряли волюмометрически, точность измерения ±0.05 мл. Процессы проводили при 298 К. В реакционный сосуд, соединенный с газометром, загружали 10 мл раствора субстрата и точную навеску катализатора, помещенную в лодочку. Опыты проводили в кинетической области, когда для скорости реакции наблюдается линейная зависимость от числа качаний.
Активность тетра-(5,8-дигидрокси)антрахинонопорфиразина кобальта (А) в реакции жидкофазного окисления цистеина составляла
А=126 г-моль O2×(г-моль кат-ра)-1×мин-1.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ МЕТАЛЛОКОМПЛЕКСОВ ТЕТРА-(5,8-ДИГИДРОКСИ-6-СУЛЬФО)АНТРАХИНОНОПОРФИРАЗИНА | 2005 |
|
RU2280036C1 |
| 2,3-ДИКАРБОКСИ-5,8-ДИМЕТОКСИАНТРАХИНОН | 2005 |
|
RU2277084C1 |
| 2,3-ДИКАРБОКСИ-5,8-ДИМЕТОКСИ-6-СУЛЬФОАНТРАХИНОН | 2005 |
|
RU2280027C1 |
| 2,3-ДИКАРБОКСИ-6-БРОМ-7-МЕТОКСИАНТРАХИНОН | 2005 |
|
RU2282617C1 |
| 2,3-ДИКАРБОКСИ-6,7-ДИМЕТИЛАНТРАХИНОН | 2004 |
|
RU2264380C1 |
| 2,3-ДИКАРБОКСИ-6-(ПАРА-СУЛЬФОФЕНИЛЕН) АНТРАХИНОН | 2003 |
|
RU2258065C2 |
| 2,3-ДИКАРБОКСИ-5,6,8-ТРИМЕТИЛАНТРАХИНОН | 2004 |
|
RU2264381C1 |
| МЕТАЛЛОКОМПЛЕКСЫ ТЕТРА-(ДИ-6,7-МЕТИЛ)АНТРАХИНОНОПОРФИРАЗИНА | 2004 |
|
RU2268891C1 |
| МЕТАЛЛОКОМПЛЕКСЫ ТЕТРА-(ТРИ-5,6,8-МЕТИЛ)АНТРАХИНОНОПОРФИРАЗИНА | 2004 |
|
RU2264406C1 |
| ТЕТРА-(5-ОКТАДЕЦИЛСУЛЬФАМОИЛ)АНТРАХИНОНОПОРФИРАЗИНЫ МЕДИ И КОБАЛЬТА | 2008 |
|
RU2382788C1 |

Изобретение относится к улучшенному способу получения металлокомплексов тетра-(5,8-дигидрокси)антрахиноно-порфиразина, которые могут быть использованы в качестве катализаторов, красителей и в других областях науки и техники. Способ включает взаимодействие 2,3-дикарбокси-5,8-диметоксиантрахинона с мочевиной, солью соответствующего металла в присутствии хлорида и молибдата аммония, и последующим гидролизом полученного металлокомплекса - тетра-(5,8-диметокси)антрахинонопорфиразина. Способ позволяет повысить выход целевого продукта до 24%. 3 ил.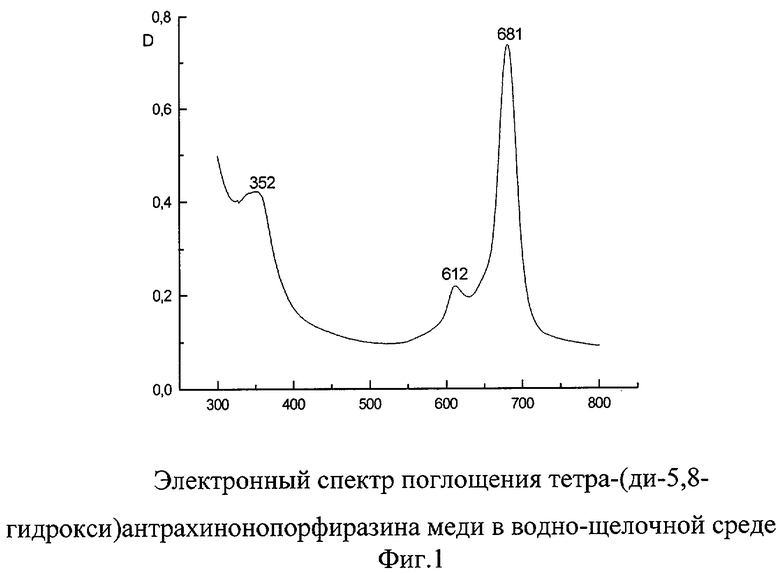
Способ получения металлокомплексов тетра-(5,8-дигидрокси)-антрахинонопорфиразина, включающий взаимодействие замещенного 2,3-дикарбоксиантрахинона с мочевиной, солью соответствующего металла в присутствии хлорида и молибдата аммония, отличающийся тем, что в качестве замещенного 2,3-дикарбоксиантрахинона используют 2,3-дикарбокси-5,8-диметоксиантрахинон, полученный металлокомплекс тетра-(5,8-диметокси)антрахинонопорфиразина подвергают гидролизу путем обработки его гидроксидом натрия.
| БОРИСОВ А.В., ПОБЕДИНСКАЯ И.А., МАЙЗЛИШ В.Е., ШАПОШНИКОВ Г.П., Тезисы докладов IX Международная конференция по химии порфиринов и их аналогов 8-12 сентября 2003 г | |||
| Суздаль | |||
| Труды конференции | |||
| Иваново, 2003, с.95-96 | |||
| ТОНКОПЛЕНОЧНОЕ ЗАПОМИНАЮЩЕЕ УСТРОЙСТВО | 1967 |
|
SU223857A1 |
Авторы
Даты
2006-05-27—Публикация
2005-01-11—Подача