Область техники, к которой относится изобретение
Настоящее изобретение касается новых конъюгатов полипептида фактора VII (FVII) или фактора VIIa (FVIIa), их получения и применения в медицине, в частности, при лечении ряда заболеваний, связанных со свертыванием крови.
Уровень техники
Свертывание крови - это процесс, состоящий из сложных взаимодействий между различными компонентами (или факторами) крови, который приводит в конечном счете к образованию фибринового сгустка. Как правило, компоненты крови, участвующие в том, что было названо коагуляционным "каскадом", являются проферментами или зимогенами, то есть ферментативно неактивными белками, которые превращаются в активные формы под действием активатора. Одним из таких коагуляционных факторов является FVII.
FVII - зависимый от витамина К белок плазмы, который синтезируется в печени и секретируется в кровь в виде одноцепочечного гликопротеина с молекулярным весом 53 кД (Broze & Majerus. J.Biol. Chem., 1980; 255: 1242-12247). Зимоген FVII обращается в активную форму (FVIIa) при ферментативном расщеплении в единственном сайте, R152-I153, что приводит к образованию двух цепей, связанных одним дисульфидным мостиком. FVIIa в комплексе с тканевым фактором (комплекс FVIIa) способен превращать факторы IX и Х в активные формы, что вызывает реакции, приводящие к быстрому образованию тромбина и фибрина (Osterud & Rapaport, Proc Natl Acad Sci USA 1977; 74: 5260-5264).
FVII подвергается посттрансляционным модификациям, включая витамин К-зависимое карбоксилирование, приводящее к образованию десяти остатков γ-карбоксиглутаминовой кислоты в N-концевом участке молекулы. Так, остатки под номерами 6, 7, 14, 16, 19, 20, 25, 26, 29 и 35, приведенные в SEQ ID NO: 1, являются остатками γ-карбоксиглутаминовой кислоты в домене Gla, важном для активности FVII. Другие посттрансляционные модификации включают присоединение углеводной части в двух природных сайтах N-гликозилирования в положении 145 и 322, соответственно, и в двух природных сайтах O-гликозилирования в положении 52 и 60, соответственно.
Ген, кодирующий FVII человека (hFVII), был картирован в области q34-qter9 хромосомы 13 (de Grouchy et al., Hum. Genet. 1984; 66: 230-233). Он содержит девять экзонов и имеет протяженность в 12,8 Kb (O'Hara et al., Proc Natl Acad Sci USA 1987; 84: 5158-5162). Организация гена и структура белка FVII близки таковым у других витамин К-зависимых прокоагулянтных белков, при этом экзоны 1а и 1b кодируют сигнальную последовательность, экзон 2 кодирует пропептид и домен Gla, экзон 3 - короткий гидрофобный участок, экзоны 4 и 5 - домены, подобные фактору роста эпидермиса, а экзоны 6-8 кодируют каталитический домен сериновой протеазы (Yoshitake et al., Biochemistry 1985; 24: 3736-3750).
Существуют экспериментальные работы по трехмерной структуре hFVIIa (Pike et al., PNAS, USA, 1999; 96: 8925-30 и Kemball-Cook et al., J.Struct. Biol., 1999; 127: 213-223), по комплексу hFVIIa с растворимым тканевым фактором с применением методов рентгеноструктурного анализа (Banner et al., Nature, 1996; 380: 41 и Zhang et al., J.Mol. Biol., 1999, 285: 2089), а также по мелким фрагментам hFVII (Muranyi et al., Biochemistry, 1998; 37: 10605 и Као et al., Biochemistry, 1999; 38: 7097).
Известно лишь сравнительно небольшое число искусственно сконструированных вариантов FVII (Dickinson & Ruf, J. Biol. Chem., 1997; 272:19875-19879, Kemball-Cook et al., J. Biol. Chem., 1998; 273: 8516-8521, Bharadwaj et al., J.Biol. Chem., 1996; 271:30685-30691, Ruf et al., Biochemistry, 1999; 38: 1957-1966).
Имеются работы по экспрессии FVII в клетках ВНК или других клетках млекопитающих (WO 92/15686, WO 91/11514 и WO 88/10295) и по экспрессии FVII вместе с эндопротеазой kex2 в эукариотических клетках (WO 00/28065).
Коммерческие препараты рекомбинантного FVIIa человека имеются в продаже под названием NovoSeven®. NovoSeven® показан при лечении кровотечений у больных гемофилией А или В. NovoSeven® является единственным коммерчески доступным препаратом rFVIIa для эффективного и надежного лечения кровотечений.
В патенте WO 91/1154 приводится неактивная форма FVII с модифицированным аргинином 152 и/или изолейцином 153. Эти аминокислоты располагаются в сайте активации. В WO 96/12800 описана инактивация FVIIa ингибитором сериновых протеиназ, а инактивация путем карбамоилирования FVIIa по α-аминокислотной группе I153 была описана Petersen et al., Eur. J.Biochem., 1999; 261: 124-129. Инактивированная форма способна конкурировать с FVII или FVIIa дикого типа за связывание с тканевым фактором и ингибировать свертывающую активность. Было предложено применять инактивированную форму FVIIa при лечении пациентов в состоянии гиперкоагуляции, например, пациентов с сепсисом, с риском инфаркта миокарда или тромботического инсульта.
Как сообщалось в "Summary Basis for Approval for NovoSeven®", PDA №96-0597, период полужизни циркулирующего rFVIIa составляет 2,3 часа. Для достижения и поддержания нужного терапевтического или профилактического эффекта требуются относительно высокие дозы и частое введение препарата. Вследствие этого трудно добиться адекватной регуляции дозы, а необходимость в частом внутривенном введении налагает ограничения на образ жизни пациента.
Другая проблема применяемого в настоящее время лечения с помощью rFVIIa состоит в относительной неустойчивости молекулы к протеолитической деградации. Протеолитическая деградация является основной помехой при получении препарата в растворе по сравнению с лиофилизированным продуктом. Преимущество получения стабильного растворимого препарата заключается в более простом обращении для больного и в случае критических состояний - в более быстром действии, которое может стать критическим для спасения жизни. Попытки предотвращения протеолитической деградации при помощи направленного мутагенеза в основных сайтах протеолиза были описаны в WO 88/10295.
Молекулы с более длительным периодом полужизни при циркуляции могли бы снизить число необходимых введений. Учитывая, что существующие продукты FVIIa требуют частых инъекций и то, что есть возможность получения более оптимальных терапевтических уровней FVIIa с сопутствующим усилением терапевтического действия, очевидно, существует потребность в усовершенствовании молекул, подобных FVII или FVIIa.
Один из путей для увеличения периода полужизни циркулирующего белка состоит в том, чтобы уменьшить почечный клиренс белка. Этого можно достичь путем конъюгации белка с химической группой, способной обеспечить снижение почечного клиренса белка.
Кроме того, присоединение химической группы к белку или замещение подверженных протеолизу аминокислот может эффективно блокировать контакт с протеолитическим ферментом, ведущий к протеолитической деградации белка. Одной из химических групп, применявшихся при получении терапевтических белковых препаратов, является полиэтиленгликоль (ПЭГ).
В WO 98/32466 предполагается, что FVII, как и многие другие белки, может быть ПЭГилирован, но в нем не содержится никакой дополнительной информации об этом.
Сущность изобретения
Настоящая заявка раскрывает усовершенствованные молекулы FVII и FVIIa, в частности, рекомбинантные молекулы hFVII и hFVIIa, обеспечивающие одно или несколько вышеуказанных преимуществ. Так, конъюгат настоящего изобретения обладает одним или более усовершенствованными свойствами по сравнению с существующими коммерческими rFVIIa, включая увеличение функционального периода полужизни in vivo и/или повышение периода полужизни в плазме и/или повышение биодоступности и/или снижение чувствительности к протеолитической деградации. Соответственно, медицинское применение конъюгата изобретения дает ряд преимуществ перед коммерчески доступным соединением rFVIIa, например более длительные промежутки между инъекциями.
Таким образом, первый аспект изобретения касается конъюгата, включающего, по меньшей мере, одну неполипептидную молекулу, ковалентно присоединенную к полипептиду, у которого аминокислотная последовательность отличается от приведенной в SEQ ID NO:1 последовательности FVII или FVIIa дикого типа тем, что в нее был введен или из нее удален, по меньшей мере, один аминокислотный остаток, содержащий группу для связывания указанной неполипептидной молекулы.
Другой аспект изобретения касается полипептида, у которого аминокислотная последовательность отличается от приведенной в SEQ ID NO: 1 последовательности FVII или FVIIa дикого типа тем, что в нее был введен или из нее удален, по меньшей мере, один аминокислотный остаток, содержащий группу для связывания указанной неполипептидной молекулы. Такие новые полипептиды FVII можно считать полезными для лечения, диагностики или других целей как таковые, но они представляют особый интерес в качестве промежуточных соединений для получения конъюгата по изобретению.
Следующие аспекты изобретения касаются нуклеотидной последовательности, кодирующей полипептид изобретения или полипептидную часть конъюгата изобретения; а также экспрессионного вектора, несущего нуклеотидную последовательность изобретения, и клеток хозяина, содержащих нуклеотидную последовательность изобретения или экспрессионный вектор изобретения.
Другие аспекты изобретения касаются фармацевтических композиций, содержащих конъюгат изобретения, а также способов получения и применения таких конъюгатов.
Подробное раскрытие изобретения
Определения
В контексте настоящей заявки и изобретения применяются следующие определения.
Термин "конъюгат" (или эквивалентный ему "конъюгированный полипептид") служит для определения гетерогенной (в смысле составной или химерной) молекулы, которая образуется при ковалентном присоединении к одному или нескольким полипептидам одной или нескольких неполипептидных частей типа молекул полимеров, липофильных соединений, углеводов или органических реагентов. Предпочтительно конъюгат растворим при соответствующих концентрациях и условиях, а именно растворим в таких физиологических жидкостях, как кровь. Примеры конъюгированных полипептидов изобретения включают гликозилированные и/или ПЭГилированные полипептиды.
Термин "ковалентное соединение" означает, что полипептид и неполипептидная молекула ковалентно соединены друг с другом либо непосредственно, либо через промежуточную группу или группы - мостик, спейсер или соединительную группу или группы.
Термин "неконъюгированный полипептид" может применяться к полипептидной части конъюгата.
В настоящем изобретении термин "неполипептидная молекула" означает молекулу, способную конъюгировать с соответствующей группой связывания на полипептиде изобретения. Предпочтительные примеры таких молекул включают молекулы полимеров, углеводы, липофильные соединения или органические реагенты. При использовании в контексте конъюгата изобретения следует иметь в виду, что неполипептидная молекула соединяется с полипептидом конъюгата через соответствующую группу (группу связывания) самого полипептида. Как указано выше, неполипептидная молекула может ковалентно присоединяться к группе связывания либо непосредственно, либо через промежуточную группу или группы - мостик, спейсер или соединительную группу или группы.
"Полимерная молекула" - это молекула, которая образуется при ковалентном соединении двух или более мономеров, причем ни один из мономеров не является аминокислотным остатком, за исключением случаев, когда полимер является альбумином человека или другим распространенным белком плазмы. Термин "полимер" может быть заменен термином "молекула полимера". Этот термин также охватывает углеводные молекулы, присоединенные путем гликозилирования in vitro, то есть химического гликозилирования, проводимого in vitro, которое в норме включает ковалентное присоединение молекулы углевода к группе связывания на полипептиде, необязательно с помощью перекрестно-сшивающего агента.
Углеводные молекулы, присоединенные при гликозилировании in vivo типа N- или O-гликозилирования (как будет описано ниже) обозначаются в настоящем изобретении как "углеводная часть". За исключением тех случаев, когда число неполипептидных молекул типа полимеров или углеводных молекул в конъюгате указано прямо, каждое упоминание неполипептидной части" в составе конъюгата или в каком-нибудь другом смысле в настоящем изобретении означает одну или несколько неполипептидных молекул типа полимеров или углеводов.
Термин "группа связывания" служит для обозначения функциональной группы полипептида, в частности его аминокислотного остатка или углеводной группы, способной к присоединению неполипептидной молекулы, такой как молекула полимера, липофильная молекула, сахарид или органический реагент. Полезные группы связывания и соответствующие им неполипептидные молекулы приведены ниже в таблице.
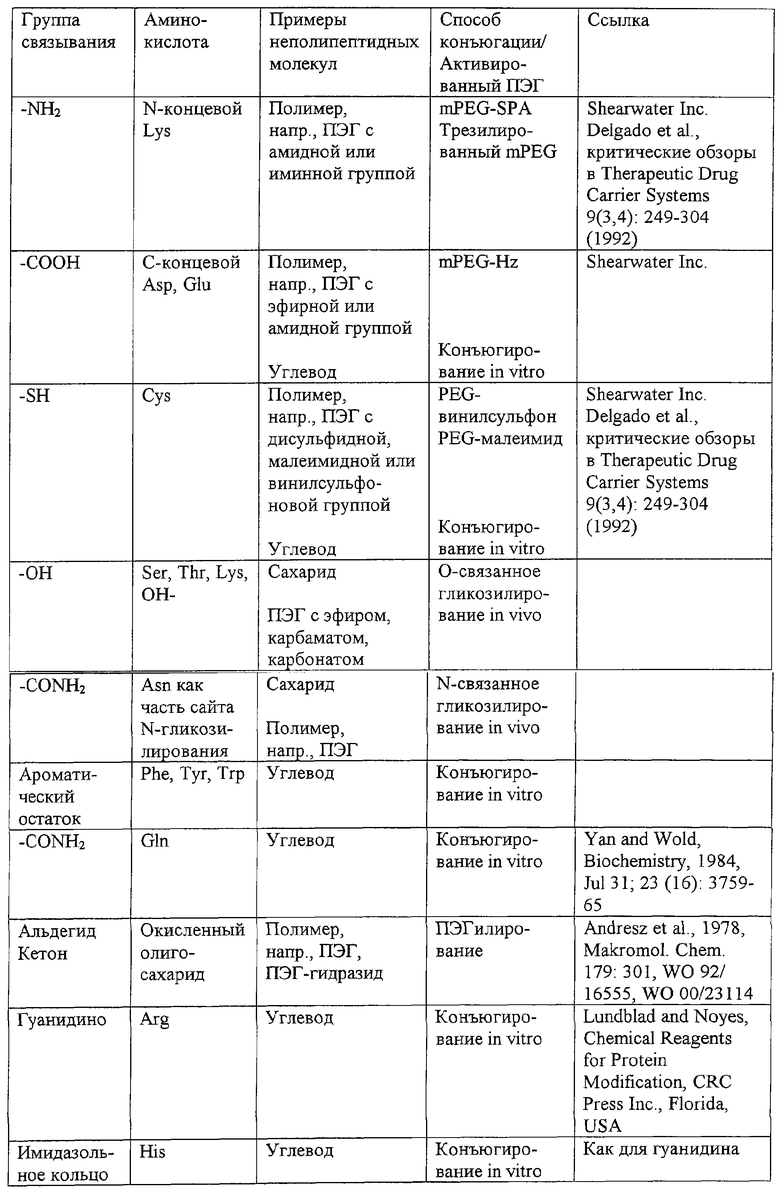
Для N-гликозилирования in vivo термин "группа связывания" применяется нестандартным образом для указания аминокислотных остатков, составляющих сайт N-гликозилирования (с последовательностями N-X-S/T/C, где Х - любой аминокислотный остаток, кроме пролина, N - аспарагин и S/T/C - серии, треонин или цистеин, предпочтительно серин или треонин, и наиболее предпочтительно треонин). Хотя именно остаток аспарагина в сайте N-гликозилирования является местом присоединения сахарида в процессе гликозилирования, такое присоединение невозможно, если в сайте N-гликозилирования нет остальных аминокислотных остатков.
Соответственно, в случае, когда неполипептидная молекула представлена сахаридом и конъюгация достигается путем N-гликозилирования, термин "аминокислотный остаток, содержащий группу для связывания неполипептидной молекулы", употребляемый в связи с изменениями аминокислотной последовательности конкретного полипептида, следует понимать в том смысле, что один или несколько аминокислотных остатков, входящих в состав сайта N-гликозилирования, следует изменить таким образом, чтобы в аминокислотную последовательность был введен функциональный сайт N-гликозилирования или же удален из нее.
В настоящей заявке названия аминокислот и атомов (к примеру, СА, СВ, CD, CG, SG, NZ, N, О, С и т.д.) применяются в соответствии с Банком Данных по Белкам (PDB) (www.pdb.org) на основании номенклатуры IUPAC (IUPAC Nomenclature and Symbolism for Amino Acids and Peptides (residue names, atom names etc.), Eur. J.Biochem., 138, 9-37 (1984) с поправками в Eur. J.Biochem., 152, 1 (1985)).
Термин "аминокислотный остаток" служит для обозначения аминокислотных остатков из числа остатков аланина (Ala или А), цистеина (Cys или С), аспарагиновой кислоты (Asp или D), глутаминовой кислоты (Glu или Е), фенилаланина (Phe или F), глицина (Gly или G), гистидина (His или Н), изолейцина (Ile или I), лизина (Lys или К), лейцина (Leu или L), метионина (Met или М), аспарагина (Asn или N), пролина (Pro или Р), глутамина (Gln или Q), аргинина (Arg или R), серина (Ser или S), треонина (Thr или Т), валина (Val или V), триптофана (Тгр или W) и тирозина (Туг или Y).
Терминология, применяемая для определения положения аминокислот, иллюстрируется следующим образом: G124 означает, что положение 124 в аминокислотной последовательности, приведенной в SEQ ID NO:1, занято остатком глицина. G124R означает, что остаток глицина в положении 124 был замещен остатком аргинина. Альтернативные замещения указываются значком "/", например K32D/E обозначает аминокислотную последовательность, в которой лизин в положении 32 замещен аспарагиновой или глутаминовой кислотой. Множественные замены обозначаются значком "+", например K143N+N145S/T означает аминокислотную последовательность, содержащую замену остатка лизина в положении 143 остатком аспарагина и замещение остатка аспарагина в положении 145 остатком серина или треонина. Введение дополнительного аминокислотного остатка, скажем, введение остатка аланина после G124, обозначается как G124GA. Удаление аминокислотного остатка обозначается звездочкой. К примеру, удаление глицина в положении 124 обозначается как G124*. Если не указано иначе, нумерация аминокислотных остатков в настоящем изобретении соответствует аминокислотной последовательности FVII/FVIIa дикого типа, приведенной в SEQ ID NO: 1.
Термин "отличается от" в применении к конкретным мутациям служит для отображения дополнительных отличий, присутствующих отдельно от указанных аминокислотных отличий. Так, наряду с удалением и/или введением аминокислотных остатков, содержащих группу связывания для неполипептидной части, полипептид FVII или FVIIa может содержать другие замены, не связанные с введением и/или удалением этих аминокислотных остатков. Таким образом, наряду с аминокислотными изменениями, раскрытыми в настоящем изобретении с целью удаления и/или введения сайтов для присоединения неполипептидной части, следует иметь в виду, что аминокислотная последовательность полипептида по изобретению может, если потребуется, содержать другие изменения, которые не обязательно связаны с введением или удалением сайтов присоединения, то есть другие замены, вставки или делеции. Например, к ним относятся укорочение N- и/или С-концевых участков на один или несколько аминокислотных остатков или введение одного или нескольких дополнительных остатков в N- и/или С-конец, например добавление остатка метионина в N-конец, а также "консервативные аминокислотные замены", то есть замены, проводимые в пределах группы аминокислот со схожими характеристиками, например небольших аминокислот, кислых аминокислот, полярных аминокислот, основных аминокислот, гидрофобных аминокислот и ароматических аминокислот.
В частности, предпочтительные замены в настоящем изобретении можно выбрать из числа консервативных замен по группам, перечисленным в нижеследующей таблице.
Термины "мутация" и "замена" в настоящем изобретении могут заменять друг друга.
Термин "нуклеотидная последовательность" служит для обозначения непрерывного отрезка из двух или более молекул нуклеотидов. Нуклеотидная последовательность может происходить из генома, кДНК, РНК, иметь полусинтетическое или синтетическое происхождение или представлять любую их комбинацию.
Термин "полимеразная цепная реакция" или "ПЦР" в общем означает метод амплификации требуемой нуклеотидной последовательности in vitro, как описано, к примеру, в US 4683195. В общем случае метод ПЦР заключается в многократном повторении цикла реакций удлинения праймера с помощью олигонуклеотидных праймеров, способных предпочтительно гибридизироваться с матричной нуклеиновой кислотой.
"Клетка", "клетка-хозяин", "клеточная линия" или "культура клеток" в настоящем изобретении применяются взаимозаменяемо и следует иметь в виду, что все эти термины включают поколения, образующиеся в результате роста или культивирования клетки. "Трансформация" и "трансфекция" могут заменять друг друга и означают процесс введения ДНК в клетку.
"Функционально связанный" обозначает ковалентное соединение двух или более нуклеотидных последовательностей путем ферментативного лигирования или другим способом в такой конфигурации друг относительно друга, чтобы могло осуществляться нормальное функционирование этих последовательностей. Например, нуклеотидная последовательность, кодирующая последовательность предшественника или лидера секреции функционально связана с нуклеотидной последовательностью, кодирующей полипептид, если при этом экспрессируется белок-предшественник, участвующий в секреции этого полипептида; промотор или энхансер функционально связан с кодирующей последовательностью, если он влияет на транскрипцию этой последовательности; сайт связывания с рибосомой функционально связан с кодирующей последовательностью, если он находится в таком положении, что способствует трансляции. Обычно "функционально связанный" означает, что соединенные нуклеотидные последовательности прилегают друг к другу и, в случае лидера секреции, прилегают друг к другу и находятся в одной рамке считывания. Соединение совершается путем лигирования в соответствующих сайтах рестрикции. Если таких сайтов нет, то применяются синтетические олигонуклеотидные адаптеры или линкеры в соответствии со стадартными методами рекомбинантной ДНК.
Термин "ввести" относится к введению аминокислотного остатка, содержащего группу связывания для неполипептидной части, особенно путем замены существующего аминокислотного остатка или же введения дополнительного аминокислотного остатка.
Термин "удалить" относится к удалению аминокислотного остатка, содержащего группу связывания для неполипептидной части, особенно путем замены аминокислотного остатка, который следует удалить, другим аминокислотным остатком, или же путем делеции (без замены) аминокислотного остатка, подлежащего удалению.
Термин "FVII" или "полипептид FVII" относится к молекуле FVII, находящейся в одноцепочечной форме.
Термин "FVIIa" или "полипептид FVIIa" относится к молекуле FVIIa, находящейся в активированной двухцепочечной форме, после расщепления пептидной связи между R152 и I153 в одноцепочечной форме. Когда при описании аминокислотной последовательности FVIIa используется аминокислотная последовательность SEQ ID NO: 1, то следует иметь в виду, что одна цепь содержит аминокислотные остатки 1-152, а другая- 153-406.
Термины "rFVII" и "rFVIIa" обозначают молекулы FVII и FVIIa, полученные методами рекомбинантной ДНК соответственно.
Термины "hFVII" и "hFVIIa" обозначают FVII и FVIIa дикого типа человека соответственно.
Термин "каталитический сайт" применяется для обозначения каталитической триады, состоящей из S344, D242 и H193 полипептида FVII.
Термины "активный FVIIa", "активный полипептид FVIIa", "активный конъюгат FVIIa" или "активный конъюгат" применяются для обозначения полипептида или конъюгата FVIIa, обладающего, по меньшей мере, 10% каталитической активности hFVIIa дикого типа. Каталитическую активность можно соответственно определить методом, описанным в разделе "Методы измерения каталитической активности ", или методом, озаглавленным "Метод измерения низких уровней каталитической активности" (см. раздел Материалы и Методы). Предпочтительно активный конъюгат обладает, по меньшей мере, 15%, например не менее 20% или 25%, более предпочтительно не менее 30% или 40%, наиболее предпочтительно не менее 50% или 60% каталитической активности hFVIIa дикого типа при определении методами, описанными выше.
Предпочтительно активный конъюгат способен связываться с тканевым фактором, а также активировать фактор Х и/или IX плазмы. Так, в предпочтительном варианте воплощения активный полипептид FVIIa или его конъюгат обладает коагуляционной активностью не менее 25% по сравнению с FVIIa дикого типа, например не менее 50% или не менее 75% от коагуляционной активности FVIIa дикого типа. Так, коагуляционная активность активного полипептида FVIIa или его конъюгата предпочтительно составляет от 25% до 200% от активности FVIIa дикого типа. Особенно предпочтительно, чтобы полипептид или конъюгат FVIIa обладал коагуляционной активностью в пределах от 30% до 150% по сравнению с FVIIa дикого типа, например в интервале 30-100% по сравнению с FVIIa дикого типа. Коагуляционную активность можно определять любым методом, известным в этой области, как будет описано далее в разделе Материалы и Методы. Однако особенно предпочтительно, чтобы определение коагуляционной активности проводилось в соответствии с методом, описанным в разделе "Методы измерения коагуляционной активности" (см. раздел Материалы и Методы).
Термин "иммуногенность" в применении к конкретному веществу служит для обозначения способности вещества индуцировать ответ иммунной системы. Иммунный ответ может быть опосредован клетками или антителами (см. подробное определение иммуногенности, к примеру, в Roitt: Essential Immunology (8th Edition, Blackwell)). В норме пониженная реакция антител указывает на снижение иммуногенности. Снижение иммуногенности можно определить любым подходящим методом, известным в этой области, например in vivo или in vitro.
Термины "неактивный FVIIa", "неактивный полипептид FVIIa", "неактивный конъюгат FVIIa" или "неактивный конъюгат" применяются для обозначения полипептида или конъюгата FVIIa, имеющего менее 10% каталитической активности по сравнению с hFVIIa дикого типа. Каталитическую активность можно соответственно определить методом, описанным в разделе "Методы измерения каталитической активности", или методом, озаглавленным "Метод измерения низких уровней каталитической активности" (см. раздел Материалы и Методы). Предпочтительно неактивный конъюгат имеет менее 8%, например менее 6% или 5%, более предпочтительно менее 4% или 3%, наиболее предпочтительно менее 2% или 1% каталитической активности hFVIIa дикого типа при определении методами, описанными выше.
Обычно неактивный конъюгат имеет очень низкую коагуляционную активность in vitro или in vivo по сравнению с hFVIIa дикого типа. Неактивный FVII или полипептид либо конъюгат FVIIa могут конкурировать с FVII или FVIIa дикого типа за связывание с тканевым фактором, ингибируя тем самым коагуляционную активность. Предпочтительно, неактивный FVII или полипептид либо конъюгат FVIIa имеет менее 1% коагуляционной активности hFVII или hFVIIa дикого типа. Более предпочтительно, неактивный FVII или полипептид либо конъюгат FVIIa имеет менее 0,05% коагуляционной активности hFVII или hFVIIa дикого типа. Наиболее предпочтительно, неактивный FVII или полипептид либо конъюгат FVIIa имеет менее 0,01% коагуляционной активности hFVII или hFVIIa дикого типа. Подобно тому, что описано выше, коагуляционную активность можно определять любым методом, известным в этой области, как будет описано далее в разделе Материалы и Методы, но предпочтительно определяют в соответствии с методом, описанным в разделе "Метод определения коагуляционной активности ".
Термин "функциональный период полужизни in vivo" применяется в его обычном значении как время, по прошествии которого в организме/органе-мишени остается 50% биологической активности полипептида или конъюгата, или как время, по прошествии которого активность полипептида или конъюгата составляет 50% от первоначального значения. В качестве альтернативы определению функционального периода полужизни in vivo может определяться "время полужизни в сыворотке", то есть время, по прошествии которого в плазме или кровотоке циркулирует 50% молекул полипептида или конъюгата до их выведения. Определение времени полужизни в сыворотке часто бывает проще, чем определение функционального времени полужизни in vivo, и время полужизни в плазме обычно является хорошим показателем величины функционального времени полужизни in vivo. Альтернативные времени полужизни в сыворотке термины - это "время полужизни в плазме", "полупериод существования в крови", "сывороточный клиренс", "плазменный клиренс" и "период полувыведения". Полипептиды и конъюгаты выводятся при участии ретикулоэндотелиальной системы (RES), почек, селезенки или печени, опосредованной тканевым фактором, SEC-рецептором или другими рецепторами элиминации или путем специфического или неспецифического протеолиза. Обычно выведение зависит от размера (относительно предела исключения для клубочковой фильтрации), заряда, присоединенных углеводных цепей и наличия клеточных рецепторов для данного белка. Функция, о которой идет речь, обычно заключается в прокоагулянтной, протеолитической активности или связывании с рецептором. Функциональное время полужизни in vivo и время полужизни в плазме можно определить любым пригодным методом, известным в этой области, как будет подробно описано ниже в разделе Материалы и Методы.
Термин "повышение" в применении к времени полужизни in vivo или времени полужизни в плазме служит для указания того, что время полужизни данного конъюгата или полипептида статистически достоверно повышается по сравнению с контрольной молекулой типа неконъюгированного rFVIIa (например, NovoSeven®), при определении в сравнимых условиях. К примеру, соответствующее время полужизни может повышаться, по меньшей мере, на 25%, например, по меньшей мере, на 50%, 100%, 150%, 200%, 250%, 300%, 500% или 1000%.
Термин "почечный клиренс" или "выведение через почки" применяется в его обычном значении, обозначая любой способ выведения через почки, например, посредством клубочковой фильтрации, выделения из трубочек или деградации в клетках трубочек. Выведение через почки зависит от физических характеристик конъюгата, включая размер (диаметр), гидродинамический объем, симметрию, форму/упругость и заряд. Обычно молекулярный вес примерно в 67 кД считается предельным для выведения через почки. Почечный клиренс можно установить любым подходящим методом, например, одним из принятых методов in vivo. Обычно почечный клиренс определяют путем введении больному меченного (с помощью радиоактивной или флуоресцентной метки) полипептидного конъюгата и измерения активности метки в собранной у больного моче. Снижение почечного клиренса определяется по сравнению с соответствующим контрольным полипептидом, например соответствующим неконъюгированным полипептидом, неконъюгированным полипептидом соответствующего дикого типа или другим конъюгированным полипептидом (конъюгированным полипептидом, не соответствующим изобретению) в сравнимых условиях. Предпочтительно, скорость выведения конъюгата через почки снижается, по меньшей мере, на 50%, предпочтительно, по меньшей мере, на 75% и наиболее предпочтительно, по меньшей мере, на 90% по сравнению с соответствующим контрольным полипептидом.
Способность конъюгата по изобретению проявлять пониженную чувствительность к протеолитической деградации имеет исключительное значение. Композиции, содержащие продукты деградации, обычно обладают меньшей удельной активностью по сравнению с композициями, не содержащими или содержащими очень незначительную долю деградированного конъюгата. Кроме того, наличие нефизиологических продуктов деградации во вводимой композиции может активировать иммунную систему пациента.
Термин "пониженная чувствительность к протеолитической деградации" главным образом служит для обозначения того, что конъюгат обладает пониженной чувствительностью к протеолитической деградации по сравнению с неконъюгированным FVIIa дикого типа при определении в сравнимых условиях. Предпочтительно протеолитическая деградация снижается, по меньшей мере, на 10%, например, по меньшей мере, на 25% (то есть на 10-25%), более предпочтительно, по меньшей мере, на 35%, например, по меньшей мере, на 50% (то есть на 10-50% например на 25-50%), еще более предпочтительно, по меньшей мере, на 60%, например, по меньшей мере, на 75% или даже 90%. Наиболее предпочтительно снижение протеолитической деградации на 100%. Таким образом, конъюгат по изобретению предпочтительно подвергается протеолитической деградации в меньшей степени, чем FVIIa дикого типа, то есть по сравнению с неконъюгированным FVIIa дикого типа протеолитическая деградация конъюгата изобретения предпочтительно снижена на 10-100%, например на 25-100%, более предпочтительно на 50-100% и наиболее предпочтительно на 75-100%.
Авторы настоящего изобретения разработали подходящий предварительный тест in vitro, который может применяться для оценки того, обладают ли такие конъюгаты пониженной чувствительностью к протеолитическому расщеплению (пониженным автопротеолизом). Так, в предпочтительном воплощении изобретения конъюгат изобретения имеет пониженную чувствительность к протеолитической деградации (как определено выше) по сравнению с FVIIa дикого типа при определении методом, описанным в разделе "Измерение пониженной чувствительности к протеолитической деградации", при определении методом, описанным в разделе "Метод измерения каталитической активности", или при определении методом, описанным в разделе "Метод измерения низких уровней каталитической активности" (см. раздел Материалы и Методы).
Термин "родительский FVII" или "родительский полипептид" служит для обозначения молекулы, подвергаемой модификации в соответствии с настоящим изобретением. Типичным родительским FVII является hFVII или hFVIIa (включая rFVIIa, то есть Novo Seven®) с аминокислотной последовательностью, приведенной в SEQ ID NO: 1.
"Вариант" означает полипептид, отличающийся от родительского полипептида по одному или нескольким аминокислотным остаткам, обычно по 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислотным остаткам.
Конъюгаты изобретения
Конъюгаты по изобретению являются результатом по большей части новой стратегии разработки усовершенствованных молекул FVII или FVIIa. Более конкретно, при удалении и/или включении аминокислотного остатка, содержащего группу для связывания неполипептидной части, стало возможным более специфически адаптировать полипептид таким образом, чтобы сделать молекулу более чувствительной к конъюгированию с выбранной неполипептидной молекулой, оптимизировать профиль конъюгации (обеспечить оптимальное распределение и число неполипептидных частей на поверхности молекулы FVII или FVIIa и гарантировать, чтобы в молекуле были только те группы связывания, что предназначены для конъюгации) и таким образом получить новую молекулу конъюгата, обладающую или не обладающую активностью FVII и к тому же одним или более усовершенствованными свойствами по сравнению с молекулами FVII и FVIIa, доступными в настоящее время. Например, когда общее число аминокислотных остатков, содержащих группу для связывания выбранного неполипептида, повышается или сокращается до оптимального уровня, то выведение конъюгата через почки обычно значительно снижается вследствие изменения формы, размера и/или заряда молекулы при конъюгации.
В предпочтительных вариантах воплощения настоящего изобретения изменению подвергается более одного аминокислотного остатка полипептида FVII или FVIIa, например изменения включают как удаление, так и добавление аминокислотных остатков, содержащих группу для связывания выбранной неполипептидной молекулы. Наряду с удалением и/или введением аминокислотных остатков, полипептид может содержать другие замены или гликозилирования, не связанные с удалением и/или включением аминокислотных остатков, содержащих группу для связывания неполипептидной части. Кроме того, полипептид может быть соединен, к примеру, с ингибитором сериновых протеиназ, чтобы заингибировать каталитический сайт полипептида.
Аминокислотный остаток, содержащий группу для связывания неполипептидной части, который подлежит удалению или введению, выбирается на основании природы выбранной неполипептидной части и, в большинстве случаев, на основании метода, с помощью которого достигается конъюгация между полипептидом и неполипептидной молекулой. Например, когда неполипептидная часть представлена молекулой полимера типа молекул, происходящих из полиэтиленгликоля или полиалкиленоксида, аминокислотные остатки, содержащие группу связывания, можно выбрать из числа лизина, цистеина, аспарагиновой кислоты, глутаминовой кислоты, гистидина и тирозина, предпочтительно цистеина и лизина, в особенности лизина.
Всякий раз, когда в полипептид FVII или FVIIa надо ввести или удалить группу для связывания неполипептидной части в соответствии с настоящим изобретением, подлежащее модификации положение в полипептиде предпочтительно находится на поверхности полипептида и более предпочтительно занято аминокислотным остатком, у которого более 25% боковой цепи доступно растворителю, предпочтительно более 50% боковой цепи доступно растворителю. Такие положения были определены на основании анализа трехмерной структуры молекулы FVII или FVIIa, как описано далее в разделе Материалы и Методы. Кроме того, эти положения предпочтительно выбирают из той части молекулы FVII, которая находится в стороне от области сайта связывания тканевого фактора и/или активного сайта. Такие области определены далее в разделе Материалы и Методы. Следует подчеркнуть, однако, что в определенных ситуациях, например, когда требуется инактивированный конъюгат, предпочтительно проводят модификации вблизи или прямо в этих участках. Например, предусматривается, что одну или более групп для связывания неполипептидных молекул, скажем, сайтов N-гликозилирования in vivo, можно с пользой ввести в область активного сайта или на гребень связывающего углубления активного сайта молекулы FVII. Область активного сайта и гребень связывающего углубления активного сайта определены далее в разделе Материалы и Методы, они состоят из следующих остатков: I153, Q167, V168, L169, L170, L171, Q176, L177, С178, G179, G180, Т181, V188, V189, S190, А191, А192, Н193, С194, F195, D196, К197, I198, W201, V228, I229, I230, Р231, S232, Т233, Y234, V235, Р236, G237, Т238, Т239, N240, Н241, D242, I243, А244, L245, L246, V281, S282, G283, W284, G285, Q286, Т293, Т324, Е325, Y326, М327, F328, D338, S339, С340, К341, G342, D343, S344, G345, G346, Р347, Н348, L358, Т359, G360, I361, V362, S363, W364, G365, С368, V376, Y377, Т378, R379, V380, Q382, Y383, W386, L387, L400 и F405 (область активного сайта); и N173, А175, К199, N200, N203, D289, R290, G291, А292, Р321 и Т370 (гребень связывающего углубления активного сайта).
Для определения оптимального распределения групп связывания на основании трехмерной структуры полипептида рассчитывают расстояния между аминокислотными остатками, расположенными на поверхности молекулы FVII или FVIIa. В частности, определяется расстояние между группами СВ аминокислотных остатков, содержащих такие группы связывания, или расстояние между функциональными группами (NZ для лизина, CG для аспарагиновой кислоты, CD для глутаминовой кислоты, SG для цистеина) одного и СВ другого аминокислотного остатка, содержащих группу связывания. В случае глицина применяется СА вместо СВ. В полипептидной части конъюгата FVII или FVIIa по изобретению любое из указанных расстояний составляет предпочтительно более 8 Å, в особенности более 10 Å для избежания или снижения гетерогенной конъюгации.
В случае удаления группы связывания определяется соответствующий аминокислотный остаток, содержащий такую группу и занимающий указанное выше положение, предпочтительно замещают другим аминокислотным остатком, не содержащим группы для связывания данной неполипептидной части. Обычно аминокислотным остатком, подлежащим удалению, является такой остаток, конъюгация с которым не выгодна, например аминокислотный остаток, находящийся в/или рядом с функциональным сайтом полипептида (поскольку конъюгация в таком сайте может привести к инактивации или снижению активности полученного конъюгата FVII или FVIIa вследствие нарушения узнавания рецептора). В данном контексте термин "функциональный сайт" служит для определения одного или более аминокислотных остатков, необходимых или каким-либо другим образом участвующих в функционировании FVII или FVIIa. Такие аминокислотные остатки являются частью функционального сайта. Функциональный сайт может быть определен методами, известными в этой области, и предпочтительно устанавливается путем анализа структуры комплекса FVIIa-тканевой фактор (см. Banner et al., Nature 1996; 380: 41-46).
В случае введения группы связывания аминокислотный остаток, содержащий такую группу, предпочтительно вводится в соответствующее положение путем замены аминокислотного остатка, занимающего это положение.
Точное число наличных и способных к конъюгации групп связывания в полипептиде FVII или FVIIa зависит от намеченного эффекта, достигаемого конъюгацией. Искомый эффект, к примеру, зависит от природы и степени конъюгации (природы неполипептидной молекулы, числа неполипептидных молекул, которые нужно или можно конъюгировать с полипептидом, места, в котором они должны быть конъюгированы или где следует избегать конъюгации, и т.д.).
Функциональный период полужизни in vivo зависит, среди прочего, от молекулярного веса конъюгата, а количество групп связывания, необходимых для обеспечения увеличенного периода полужизни, таким образом, зависит от молекулярного веса данной неполипептидной молекулы. В одном из вариантов конъюгат изобретения имеет молекулярный вес не менее 67 кД, в особенности не менее 70 кД, при определении, к примеру, методом SDS-PAGE по Laemmli, Nature Vol.227 (1970), р.680-85. Молекулярный вес FVII составляет около 53 кД, поэтому требуется еще 10-20 кД для достижения желаемого эффекта. Это можно обеспечить, к примеру, при конъюгации 2-4 молекул ПЭГ по 10 кД или другим описанным далее способом.
Чтобы избежать чрезмерного нарушения структуры и функции родительской молекулы, аминокислотная последовательность полипептидной части конъюгата должна быть более чем на 90% идентична последовательности, приведенной в SEQ ID NO:1, предпочтительно более чем на 95% или 96%. В частности, аминокислотная последовательность полипептидной части конъюгата должна быть более чем на 97% идентична SEQ ID NO: 1, например более чем на 98%, 99%, 99,25%, 99,25% или 99,5%.
Гомология/тождественность аминокислотной последовательности без труда определяется при сопоставлении последовательностей, например, с помощью программы ClustalW, версия 1.8, июнь 1999, применяя параметры по умолчанию (Thompson et al., 1994, ClustalW: Improving the sensitivity of progressive multiple sequence alignment through sequence weighting, position-specific gap penalties and weight matrix choice, Nucleic Acids Research, 22: 4673-4680) или из базы данных семейства PFAM, версия 4.0 (http://pfam.wustl.edu/) (Nucleic Acids Res. 1999, Jan.1; 27(1):260-2) с помощью программы GENEDOC, версия 2.5 (Nicholas K.B., Nicholas H.B. Jr., and Deerfield D.W.II. 1997, GeneDoc: Analysis and Visualization of Genetic Variation, EMBNEW.NEWS 4: 14; Nicholas K.B. and Nicholas H.B. Jr. 1997 GeneDoc: Analysis and Visualization of Genetic Variation).
Иными словами, общее число аминокислотных остатков, подлежащих изменению согласно настоящему изобретению (относительно аминокислотной последовательности, приведенной в SEQ ID NO: 1), не должно превышать 15. Предпочтительно полипептидная часть конъюгата FVII или FVIIa по изобретению или полипептид по изобретению имеет аминокислотную последовательность, которая отличается по 1-15 аминокислотным остаткам от последовательности, приведенной в SEQ ID NO: 1, обычно по 1-10 или 2-10 аминокислотным остаткам, например по 1-8 или 2-8 остаткам либо по 3-7 или 4-6 остаткам от последовательности, приведенной в SEQ ID NO: 1. Так, в норме полипептидная часть конъюгата FVII или FVIIa по изобретению или полипептид по изобретению имеет аминокислотную последовательность, которая отличается от приведенной в SEQ ID NO: 1 не более чем по 15 аминокислотным остаткам (например, по 15 остаткам), не более чем по 14 аминокислотным остаткам (например, по 14 остаткам), не более чем по 13 аминокислотным остаткам (например, по 13 остаткам), не более чем по 12 аминокислотным остаткам (например, по 12 остаткам), не более чем по 11 аминокислотным остаткам (например, по 11 остаткам), не более чем по 10 аминокислотным остаткам (например, по 10 остаткам), не более чем по 9 аминокислотным остаткам (например, по 9 остаткам), не более чем по 8 аминокислотным остаткам (например, по 8 остаткам), не более чем по 7 аминокислотным остаткам (например, по 7 остаткам), не более чем по 6 аминокислотным остаткам (например, по 6 остаткам), не более чем по 5 аминокислотным остаткам (например, по 5 остаткам), не более чем по 4 аминокислотным остаткам (например, по 4 остаткам), не более чем по 3 аминокислотным остаткам (например, по 3 остаткам) или не более чем по 2 аминокислотным остаткам (например, по 2 остаткам).
Аналогичным образом, конъюгат изобретения обычно содержит 1-15 неполипептидных частей, например 1-10 или 2-10 неполипептидных частей, например 1-8 или 2-8 неполипептидных частей либо 1-6, 1-4, 3-7 или 4-6 неполипептидных частей.
Предпочтительно конъюгат изобретения обладает как минимум одним из следующих улучшенных свойств: увеличенным функциональным периодом полужизни in vivo, повышенным периодом полужизни в плазме, пониженным почечным клиренсом и пониженной чувствительностью к протеолитической деградации по сравнению с rFVIIa, например (NovoSeven®).
Из WO 88/10295 известно, что протеолитическая деградация FVII/PVIIa в основном происходит в различных протеолитических сайтах молекулы, а именно в положениях К32, К38, I42, I44, К143, R290, R315, R341, R392, R396 и R402 (или скорее между K32-D33, K38-L39, I42-S43, Y44-S45, K143-R144, R290-G291, R315-K316, К341-G342, R392-S393, R396-P397 и R402-A403). Поэтому одна из предпочтительных стратегий для увеличения функционального периода полужизни in vivo, функционального периода полужизни в плазме или для понижения чувствительности к протеолитической деградации заключается в модифицировании родительского полипептида в и/или вблизи от одного или нескольких из этих сайтов протеолитической деградации, например введением неполипептидных молекул в и/или вблизи от таких сайтов. Так, в предпочтительном воплощении изобретения группа связывания вводится как минимум в одно из указанных выше идентифицированных положений или в положения -4, -3, -2, -1, 1, 2, 3, 4, предпочтительно в положения -2, -1, 1, 2, например в положения -1, 1 относительно того положения, которое непосредственно участвует в протеолитической деградации.
В частности, искусственный сайт гликозилирования in vivo, в особенности искусственный сайт N-гликозилирования in vivo (см. ниже), предпочтительно вводится в положение, выбранное из группы, состоящей из 28-48, 139-147, 286-294, 311-319, 338-345 и 388-406. Особенно предпочтительно, чтобы сайт гликозилирования in vivo, например сайт N-гликозилирования in vivo (см. ниже), вводился в положение, выбранное из группы, состоящей из 30-34, 36-46, 141-144, 288-292, 313-317, 341-343, 390-398 и 400-404. Более предпочтительно, чтобы сайт гликозилирования in vivo, например сайт N-гликозилирования in vivo (см. ниже), вводился в положения, выбранные из группы, состоящей из положений 31-33 (например, 31, 32 или 33), 37-39 (например, 37, 38, 39), 41-46 (например, 41, 42, 43, 44, 45 или 46), 142-144 (например, 142, 143 или 144), 289-291 (например, 289, 290 или 291), 314-316 (например, 314, 315 или 316), 341-342 (например, 341, 342 или 343), 391-393 (например, 391, 392 или 393), 395-397 (например, 395, 396 или 397) и 401-403 (например, 401, 402 или 403). Введение предпочтительно осуществляется путем замещения.
Конъюгаты изобретения, у которых группой для связывания молекулы неполипептидной части служит лизин
В одном интересном варианте осуществления изобретения группой для связывания неполипептидной части служит лизин, то есть конъюгат изобретения содержит как минимум одну неполипептидную часть, ковалентно связанную с полипептидом, аминокислотная последовательность которого отличается от приведенной в SEQ ID NO: 1 последовательности FVII или FVIIa дикого типа тем, что в нее был введен или из нее удален, по меньшей мере, один остаток лизина.
FVII/FVIIa содержит 17 остатков лизина. Три остатка лизина (К18, К62 и К85) располагаются в домене связывания тканевого фактора и два остатка лизина (К197 и К341) располагаются в области активного сайта.
Вследствие относительно высокого содержания остатков лизина в родительском полипептиде предусматривается, что, по меньшей мере, один остаток лизина должен быть предпочтительно удален, лучше всего путем замены остатка лизина другим остатком для того, чтобы избежать чрезмерной конъюгации с неполипептидной частью.
Так, в одном из воплощений аминокислотная последовательность полипептидной части конъюгата FVII или FVIIa отличается от приведенной в SEQ ID NO:1 тем, что, по меньшей мере, один остаток лизина был удален, например, 1-15 остатков лизина, в частности 1-10, 1-6 или 2-4 остатка лизина, предпочтительно путем замещения. Например, остаток (остатки) лизина, подлежащие удалению, выбирают из группы, состоящей из К18, К32, К38, К62, К85, К109, К137, К143, К148, К157, К161, К197, К199, К316, К337, К341, К389 и их сочетаний. В особенности предпочтительно удалить один или более остатков лизина, входящих в состав участка связывания тканевого фактора и/или области активного сайта, например К18, К62, К85, К197, К341 или их сочетания. Остаток лизина может быть замещен любым другим аминокислотным остатком, но предпочтительно заменяется на R, Q, N или Н, более предпочтительно R.
В другом воплощении аминокислотная последовательность полипептидной части конъюгата FVII или FVIIa отличается от приведенной в SEQ ID NO: 1 тем, что в нее был введен, по меньшей мере, один остаток лизина, например, 1-15 остатков лизина, в частности 1-10, 1-6 или 2-4 остатка лизина, предпочтительно путем замещения. Следует иметь в виду, что особенно предпочтительно, чтобы введение как минимум одного остатка лизина в намеченный сайт в родительской молекуле сопровождалось удалением, по меньшей мере, одного из вышеупомянутых остатков лизина. Итак, в предпочтительном воплощении изобретения аминокислотная последовательность полипептидной части конъюгата FVII или FVIIa отличается от приведенной в SEQ ID NO: 1 тем, что, по меньшей мере, один остаток лизина был удален и как минимум один остаток лизина был введен.
Примеры положений, в которые можно вводить остатки лизина, включают, но не ограничиваются положениями в или вблизи от сайтов протеолитической деградации, указанных выше. Так, в предпочтительном воплощении замены остатка лизина другим остатком выбирают из группы, состоящей из I42K, Y44K, L288K, D289K, R290K, G291K, А292К, Т293К, Q313K, S314K, R315K, V317K, L390K, М391К, R392K, S393K, Е394К, Р395К, R396K, Р397К, G398K, V399K, L400K, L401K, R402K, А403К, Р404К, F405K и их сочетаний, в особенности из группы, состоящей из R290K, R315K, R392K, R396K, R402K и их сочетаний.
Неполипептидая часть конъюгата согласно этому аспекту изобретения может быть любой молекулой, для присоединения которой с помощью данного способа конъюгации служит лизин, однако предпочтительно, чтобы неполипептидная часть была молекулой полимера. Полимерной молекулой может быть любая из молекул, описанных в разделе "Конъюгация с молекулой полимера", но предпочтительно выбирается из числа линейных или разветвленных полиэтиленгликолей или иных полиалкиленоксидов. Примерами предпочтительных полимерных молекул являются SS-PEG, NPC-PEG, альдегид-PEG, mPEG-SPA, mPEG-SCM, mPEG-BTC фирмы Shearwater Polymers, Inc., SC-PEG фирмы Enzon, Inc., трезилированный PEG как описано в US 5880255 или оксикарбонил-окси-К-дикарбоксиимид-PEG (US 5122614).
Обычно для конъюгации с лизиновым остатком неполипептидная часть должна иметь молекулярный вес от 5 до 20 кД, например от 5 до 10 кД, например около 5 или около 10 кД.
Следует иметь в виду, что любые изменения аминокислот, в особенности замены, указанные в этом разделе, могут сочетаться с любыми аминокислотными изменениями, предпочтительно заменами, указанными в других разделах, в которых раскрываются конкретные модификации аминокислот, включая введение и/или удаление сайтов гликозилирования.
Конъюгаты изобретения, у которых группой для связывания молекулы неполипептидной части служит цистеин
В еще одном интересном варианте осуществления изобретения группой для связывания неполипептидной части служит цистеин, то есть конъюгат изобретения содержит как минимум одну неполипептидную часть, ковалентно связанную с полипептидом, аминокислотная последовательность которого отличается от приведенной в SEQ ID NO: 1 последовательности FVII или FVIIa дикого типа тем, что в нее был введен или из нее удален, по меньшей мере, один остаток цистеина.
FVII/FVIIa содержит 24 остатка цистеина и между следующими остатками цистеина образуются дисульфидные мостики: С17 и С22, С50 и С61, С55 и С70, С72 и С81, С91 и С102, С98 и С112, С114 и С127, С135 и С262, С159 и С164, С178 и С194, С310 и С329, и между С340 и С368.
В следующем интересном воплощении аминокислотная последовательность полипептида FVII или FVIIa отличается от приведенной в SEQ ID NO: 1 тем, что из нее было удалено не менее одного остатка цистеина, например 1-15 остатков цистеина, в особенности 1-10, 1-6 или 2-4 остатка, предпочтительно путем замещения.
Примеры положений, в которые может быть введен остаток цистеина, включают положения в или вблизи сайтов протеолитической деградации, описанных выше, но не ограничиваются ими.
Так, в интересном варианте осуществления изобретения остаток (остатки) цистеина, который должен быть введен, выбирают из группы, состоящей из I30С, К32С, D33C, А34С, Т37С, К38С, W41C, Y44C, S45C, D46C, L141C, Е142С, К143С, R144C, L288C, D289C, R290C, G291C. А292С, S314C, R315C, К316С, V317C, L390C, М391С, R392C, S393C, Е394С, Р395С, R396C, Р397С, G398C, V399C, L401C, R402C, А403С, Р404С и их сочетаний, в особенности из группы, состоящей из К32С, Y44C, К143С, R290C, R315C, К341С, R392C, R396C, R402C и их сочетаний.
В следующем интересном воплощении изобретения остатки цистеина вводят в те положения, которые в hFVII дикого типа заняты остатками треонина или серина, у которых не менее 25% боковой цепи выходит на поверхность. Например, в полипептиде FVII или FVIIa остаток цистеина вводится предпочтительно путем замещения, по меньшей мере, в одно положение, выбранное из группы, состоящей из S12, S23, S43, S45, S52, S53, S60, S67, Т83, S103, Т106, Т108, S111, S119, S126, Т128, Т130, S147, Т185, S214, S222, S232, Т233, Т238, Т239, Т255, Т267, Т293, Т307, S320, Т324, S333, S336, Т370 и S393. Еще более предпочтительно, чтобы остаток цистеина был введен, по меньшей мере, в одно положение, которое в hFVII занято остатком S, выбранное из группы, состоящей из S12, S23, S43, S45, S52, S53, S60, S67, S103, S111, S119, S126, S147, S214, S222, S232, S320, S333, S336 и S393.
В следующем воплощении изобретения остатки цистеина вводят в те положения, которые в hFVII дикого типа заняты остатками треонина или серина, у которых не менее 50% боковой цепи выходит на поверхность. Например, в полипептиде FVII или FVIIa остаток цистеина вводят предпочтительно путем замещения, по меньшей мере, в одно положение, выбранное из группы, состоящей из S23, S43, S52, S53, S60, S67, Т106, Т108, S111, S119, S147, S214, Т238, Т267 и Т293, еще более предпочтительно из группы, состоящей из S23, S43, S52, S53, S60, S67, S111, S119, S147 и S214.
В еще одном воплощении остаток цистеина вводится, по меньшей мере, в одно из вышеуказанных положений, но не входящих в область активного сайта. Предпочтительно это положение занято остатком Т или S. Например, в полипептиде FVII остаток цистеина вводят, по меньшей мере, в одно положение, выбранное из группы, состоящей из S12, S23, S43, S45, S52, S53, S60, S67, Т83, S103, Т106, Т108, S111, S119, S126, Т128, Т130, S147, Т185, S214, S222, Т255, Т267, Т307, S320, S333, S336, Т370 и S393 (у которых не менее 25% боковой цепи выходит на поверхность), предпочтительно из группы, состоящей из S12, S23, S43, S45, S52, S53, S60, S67, S103, S111, S119, S126, S147, S214, S222, S320, S333, S336 и S393 (занятых остатком S), более предпочтительно из группы, состоящей из S23, S43, S52, S53, S60, S67, Т106, Т108, S111, S119, S147, S214 и Т267 (у которых не менее 50% боковой цепи которой выходит на поверхность), в особенности из группы, состоящей из S23, S43, S52, S53, S60, S67, S111, S119, S147 и S214 (занятых остатком S).
В следующем воплощении остаток цистеина вводится, по меньшей мере, в одно положение, выбранное из любой из описанных выше групп, которое не располагается в области сайта связывания тканевого фактора. Предпочтительно это положение занято остатком Т или S. Например, в полипептиде FVII остаток цистеина вводят, по меньшей мере, в одно положение, выбранное из группы, состоящей из S12, S23, S45, S52, S53, S67, Т83, S103, Т106, Т108, S111, S119, S126, Т128, Т130, S147, Т185, S214, S222, S232, Т233, Т238, Т239, Т255, Т267, Т293, S320, Т324, S333, S336, Т370 и S393 (у которых не менее 25% боковой цепи выходит на поверхность), в особенности из группы, состоящей из S12, S23, S45, S52, S53, S67, S103, S111, S119, S126, S147, S214, S222, S232, S320, S333, S336 и S393 (занятых остатком S), более предпочтительно из группы, состоящей из S23, S52, S53, S67, Т106, Т108, S111, S119, S147, S214, Т238, Т267 и Т293 (у которых не менее 50% боковой цепи выходит на поверхность), в особенности из группы, состоящей из S23, S52, S53, S67, S111, S119, S147 и S214 (занятых остатком S).
В следующем воплощении остаток цистеина вводится, по меньшей мере, в одно положение, выбранное из любой из описанных выше групп, которое не находится в области сайта связывания тканевого фактора или активного сайта. Предпочтительно это положение занято остатком Т или S. Например, в полипептиде FVII остаток цистеина вводят, по меньшей мере, в одно положение, выбранное из группы, состоящей из S12, S23, S45, S52, S53, S67, Т83, S103, Т106, Т108, S111, S119, S126, Т128, Т130, S147, Т185, S214, S222, Т255, Т267, S320, S333, S336, Т370 и S393 (у которых не менее 25% боковой цепи выходит на поверхность), в особенности из группы, состоящей из S12, S23, S45, S52, S53, S67, S103, S111, S119, S126, S147, S214, S222, S320, S333, S336 и S393 (занятых остатком S), более предпочтительно из группы, состоящей из S23, S52, S53, S67, Т106, T108, S111, S119, S147, S214 и Т267 (у которых не менее 50% боковой цепи выходит на поверхность), в особенности из группы, состоящей из S23, S52, S53, S67, S111, S119, S147 и S214 (занятых остатком S).
Неполипептидая часть конъюгата согласно этому аспекту изобретения может быть любой молекулой, для присоединения которой с помощью данного способа конъюгации служит цистеин, однако предпочтительно, чтобы неполипептидная часть была молекулой полимера. Полимерной молекулой может быть любая из молекул, описанных в разделе "Конъюгация с молекулой полимера", но предпочтительно выбирается из числа линейных или разветвленных полиэтиленгликолей или иных полиалкиленоксидов.
В особенно интересном воплощении молекулой полимера является PEG, например VS-PEG. Конъюгация между полипептидом и полимером осуществляется любым удобным способом, например, описанным в разделе "Конъюгация с молекулой полимера", используя одностадийный метод или постадийно, как указано в этом разделе. Когда полипептид FVII или FVIIa содержит только один способный к конъюгации остаток цистеина, то его предпочтительно конъюгируют с неполипептидной частью, имеющей молекулярный вес от 5 кД до 20 кД, например от 10 до 20 кД, например с молекулярным весом около 5кД, 10кД, 12 кД, 15 кД или 20 кД, причем конъюгируют непосредственно или через низкомолекулярный полимер (как описано в WO 99/55377). Когда же конъюгат содержит два или более способных к конъюгации остатка цистеина, обычно каждая из неполипептидных частей имеет молекулярный вес от 5 кД до 10 кД, например около 5 кД или 10 кД.
Следует иметь в виду, что любые изменения аминокислот, в особенности замены, указанные в этом разделе, могут сочетаться с любыми аминокислотными изменениями, предпочтительно заменами, указанными в других разделах, в которых раскрываются конкретные модификации аминокислот, включая введение и/или удаление сайтов гликозилирования.
Конъюгаты изобретения, у которых группой для связывания молекулы неполипептидной части служит аспарагиновая кислота или глутаминовая кислота
В следующем интересном воплощении изобретения группой для связывания неполипептидной части служит аспарагиновая кислота или глутаминовая кислота, то есть конъюгат изобретения содержит как минимум одну неполипептидную часть, ковалентно связанную с полипептидом, аминокислотная последовательность которого отличается от приведенной в SEQ ID NO: 1 последовательности FVII или FVIIa дикого типа тем, что в нее был введен или из нее удален, по меньшей мере, один остаток аспарагиновой кислоты или один остаток глутаминовой кислоты.
В другом интересном воплощении аминокислотная последовательность полипептида FVII и FVIIa отличается от приведенной в SEQ ID NO: 1 тем, что в нее было введено не менее одного остатка аспарагиновой кислоты и/или глутаминовой кислоты, например 1-15 остатков аспарагиновой кислоты и/или глутаминовой кислоты, в особенности 1-10, 1-6 или 2-4 остатка аспарагиновой кислоты и/или глутаминовой кислоты, предпочтительно путем замещения.
Примеры положений, в которые можно ввести остатки аспарагиновой кислоты или глутаминовой кислоты, включают положения в/или вблизи сайтов протеолитической деградации, описанных выше, но не ограничиваются ими.
Так, в одном интересном воплощении изобретения остатки аспарагиновой кислоты и/или глутаминовой кислоты, которые могут быть введены, предпочтительно путем замещения, выбирают из группы, состоящей из I30D/E, K32D/E, A34D/E, T37D/E, K38D/E, W41D/E, Y44D/E, S45D/E, D46C, L141D/E, E142D/E, K143D/E, R144D/E, L288D/E, R290D/E, G291D/E, A292D/E, Q313D/E, S314D/E, R315D/E, K316D/E, V317D/E, L390D/E, M391D/E, R392D/E, S393D/E, P395D/E, R396D/E, P397D/E, G398D/E, V399D/E, L401D/E, R402D/E, A403D/E, P404D/E и их сочетаний, в особенности из группы, состоящей из K32D/E, Y44D/E, K143D/E, R290D/E, R315D/E, K341D/E, R392D/E, R396D/E, R402D/E и их сочетаний.
Наряду с вышеперечисленными заменами полипептид конъюгата по вышеописанному воплощению может содержать удаление, предпочтительно путем замены, не менее одного остатка аспарагиновой кислоты и/или остатка глутаминовой кислоты.
Вследствие относительно высокого содержания остатков лизина в родительском полипептиде предусматривается, что, по меньшей мере, один остаток аспарагиновой кислоты или глутаминовой кислоты должен быть предпочтительно удален, лучше всего путем замещения, чтобы избежать чрезмерной конъюгации с неполипептидной частью.
Так, в одном из воплощений аминокислотная последовательность полипептидной части конъюгата FVII или FVIIa отличается от приведенной в SEQ ID NO: 1 тем, что, по меньшей мере, один остаток аспарагиновой кислоты или глутаминовой кислоты был удален, например, 1-15 остатков аспарагиновой или глутаминовой кислоты, в особенности 1-10, 1-6 или 2-4 остатка аспарагиновой или глутаминовой кислоты, предпочтительно путем замещения. Например, остатки аспарагиновой или глутаминовой кислоты, подлежащие удалению, предпочтительно путем замещения, выбирают из группы, состоящей из D33, D46, D48, Е77, Е82, D86, D87, Е94, Е99, D104, Е116, D123, Е132, Е142, Е163, D196, Е210, D212, Е215, D217, D219, Е220, D256, Е265, Е270, D289, Е296, D309, D319, Е325, D334, D338, D343, Е385, Е394 и их сочетаний.
Следует иметь в виду, что особенно предпочтительно, чтобы введение как минимум одного остатка аспарагиновой или глутаминовой кислоты в намеченный сайт в родительской молекуле сопровождалось удалением, по меньшей мере, одного из указанных выше остатков аспарагиновой или глутаминовой кислоты. Так, в предпочтительном воплощении изобретения аминокислотная последовательность полипептидной части конъюгата FVII или FVIIa отличается от приведенной в SEQ ID NO: 1 тем, что, по меньшей мере, один остаток аспарагиновой или глутаминовой кислоты был удален, предпочтительно путем замещения, и как минимум один остаток аспарагиновой или глутаминовой кислоты был введен, предпочтительно путем замещения.
Неполипептидая часть конъюгата, согласно этому аспекту изобретения, может быть любой молекулой, для присоединения которой с помощью данного способа конъюгации служит аспарагиновая или глутаминовая кислота, однако в настоящее время предпочтительно, чтобы неполипептидная часть была молекулой полимера или органического реагента, в особенности молекулой полимера, а конъюгат был получен, к примеру, как описано Sakane and Pardridge, Pharmaceutical Research, Vol.14, №8, 1997, pp.1085-1091.
Следует иметь в виду, что любые изменения аминокислот, в особенности замены, указанные в этом разделе, могут сочетаться с любыми аминокислотными изменениями, в частности заменами, указанными в других разделах, в которых раскрываются конкретные изменения аминокислот, включая введение и/или удаление сайтов гликозилирования.
Конъюгаты изобретения, неполипептидная часть которых представлена сахаридом
В следующем интересном воплощении изобретения была введена и/или удалена группа связывания для сахарида, например сайт гликозилирования, в особенности сайт гликозилирования in vivo.
Предпочтительно конъюгат изобретения содержит, по меньшей мере, один сахарид, ковалентно связанный с полипептидом, аминокислотная последовательность которого отличается от приведенной в SEQ ID NO: 1 последовательности FVII или FVIIa дикого типа тем, что в нее был введен, по меньшей мере, один искусственный сайт гликозилирования и/или из нее был удален, по меньшей мере, один природный сайт гликозилирования. В частности, был введен искусственный сайт гликозилирования, либо искусственный сайт гликозилирования был введен вместе с удалением природного сайта гликозилирования. Введенный сайт гликозилирования может быть сайтом O-гликозилирования или сайтом N-гликозилирования. Предпочтительно сайт гликозилирования является сайтом O-гликозилирования in vivo или сайтом N-гликозилирования in vivo, в особенности сайтом N-гликозилирования in vivo.
В контексте настоящего изобретения термин "природный сайт гликозилирования" охватывает сайты гликозилирования в положениях N145, N322, S52 и S60. Аналогичным образом, термин "природный сайт in vivo O-гликозилирования" включает положения S52 и S60, тогда как термин "природный сайт in vivo N-гликозилирования" включает положения N145 и N322.
В типичном случае аминокислотная последовательность полипептида FVII и FVIIa отличается от приведенной в SEQ ID NO: 1 тем, что в нее был введен, по меньшей мере, один искусственный сайт гликозилирования (например, по меньшей мере, один искусственный сайт N-гликозилирования in vivo), например 1-15 искусственных сайтов гликозилирования (например, 1-15 искусственных сайтов N-гликозилирования in vivo), в особенности 1-10, 1-6 или 2-4 искусственных сайта гликозилирования (например, 1-10, 1-6 или 2-4 искусственных сайта N-гликозилирования in vivo), предпочтительно путем замещения.
Следует иметь в виду, что для получения конъюгата, полипептидная часть которого содержит один или более сайтов гликозилирования, этот полипептид необходимо экспрессировать в клетках хозяина, способного к присоединению сахаридов (олигосахаридов) в сайтах гликозилирования, либо подвергнуть его гликозилированию in vitro. Примеры гликозилирующих клеток хозяина приведены ниже в разделе "Конъюгирование с молекулой сахарида".
В интересном вполощении этого аспекта сайт гликозилирования in vivo вводится в положение родительской молекулы FVII или FVIIa, занимаемое аминокислотным остатком, экспонированным на поверхности молекулы, у которого предпочтительно более 25% боковой цепи доступно для растворителя, в особенности более 50% боковой цепи доступно для растворителя (эти положения определены далее в разделе Методы). Сайт N-гликозилирования затем вводится таким образом, что его N-остаток располагается в этом положении. Аналогично, сайт O-гликозилирования вводится таким образом, что остатки S и Т, входящие в этот сайт, располагаются в этом положении. Примеры таких положений включают K32S/T, I42S/T, Y44S/T, K143S/T, R290S/T, R315S/T, K341S/T, R392S/T, R396S/T, R402S/T и их сочетания.
В отношении N-гликозилирования сайт гликозилирования in vivo вводится в то положение, в котором требуется только одна мутация для создания сайта (то есть туда, где уже есть все остальные аминокислотные остатки, необходимые для создания функционального сайта гликозилирования).
Иными словами, конъюгат по изобретению предпочтительно является конъюгатом, у которого аминокислотная последовательность полипептида отличается от SEQ ID NO: 1 тем, что, по меньшей мере, одна природная последовательность N-X'-Х замещена последовательностью N-X'-S или N-X'-T, где X' - любая аминокислота, кроме Р, а X - любая аминокислота, кроме S и Т.
Аналогичным образом конъюгат по изобретению предпочтительно является конъюгатом, у которого аминокислотная последовательность полипептида отличается от SEQ ID NO: 1 тем, что, по меньшей мере, одна природная последовательность Х-Х'-S или Х-Х'-Т, представленная в SEQ ID NO: 1, заменена последовательностью N-X'-S или N-X'-T, где X' - любая аминокислота, кроме Р, а Х - любая аминокислота, кроме N.
Конкретные примеры таких замен, ведущих к созданию сайтов N-гликозилирования in vivo, включают замены, выбранные из группы, состоящей из F4S/T, P10N, Q21N, W41N, S43N, A51N, G58N, L65N, G59S/T, E82S/T, N95S/T, G97S/T, Y101N, D104N, T106N, K109N, G117N, G124N, S126N, T128N, A175S/T, G179N, I186S/T, V188N, R202S/T, I205S/T, D212N, E220N, I230N, P231N, P236N, G237N, V253N, E265N, T267N, E270N, R277N, L280N, G291N, P303S/T, L305N, Q312N, G318N, G331N, D334N, K337N, G342N, H348N, R353N, Y357N, I361N, V376N, R379N, M391N и их сочетаний. Предпочтительно замены выбираются из группы, состоящей из F4S/T, P10N, Q21N, W411N, A51N, G58N, G59S/T, N95S/T, G97S/T, Y101N, D104N, T106N, K109N, G117N, G124N, S126N, T128N, A175S/T, I186S/T, V188N, R202S/T, I205S/T, D212N, E220N, V253N, E265N, T267N, E270N, L280N, G291N, P303S/T, G318N, G331N, D334N, K337N, R353N, Y357N, M391N и их сочетаний.
Альтернативно, сайт гликозилирования in vivo вводится в положение, занимаемое остатком лизина или аргинина, предпочтительно остатком лизина, в особенности таким образом, чтобы N-остаток сайта N-гликозилирования или остатки S или Т сайта O-гликозилирования замещали остаток лизина.
Иными словами, конъюгат по изобретению предпочтительно является конъюгатом, у которого аминокислотная последовательность полипептида отличается от SEQ ID NO:1 тем, что, по меньшей мере, одна природная последовательность К-Х'-X или R-X'-X, предпочтительно K-X'-X, представленная в SEQ ID NO:1, заменена последовательностью N-X'-S или N-X'-T, где X' - любая аминокислота, кроме Р, а Х - любая аминокислота, кроме S или Т.
Конкретные примеры таких замен, создающих сайты гликозилирования in vivo, включают замены, выбранные из группы, состоящей из K32N+A34S/T, K38N+F40S/T, K62N+Q64S/T, K85N+D87S/T, K137N+P139S/T, K143N+N145S/T, K148N+Q149S/T, K161N+E163S/T, K197N+K199S/T, K199N+W201S/T, K316N+G318S/T, K337N, K341N+D343S/T, K389N+M391S/T и их сочетаний.
В следующем интересном воплощении аспекта гликозилирования, описанного выше, сайт гликозилирования, в особенности сайт N-гликозилирования, может быть введен в положение, находящееся в или вблизи от сайтов протеолитического расщепления, описанных выше (см. раздел "Конъюгат изобретения").
Так, конкретные примеры таких замещений, создающих сайты N-гликозилирования in vivo, включают замены, выбранные из группы, состоящей из K32N+A34S/T, F31N+D33S/T, I30N+K32S/T, A34N+R36S/T, K38N+F40S/T, T37N+L39S/T, R36N+K38S/T, L39N+W41S/T, F40N+I42S/T, W41N, I42N+Y44S/T, S43N, Y44N+D46S/T, S45N+G47S/T, D46N+D48S/T, G47N+Q49S/T, K143N+N145S/T, E142N+R144S/T, L141N+K143S/T, I140N+E142S/T, R144N+A146S/T, A146N+K148S/T, S147N+P149S/T, R290N+A292S/T, D289N+G291S/T, L288N+R290S/T, L287N+D289S/T, G291N, A292N+A294S/T, T293N+L295S/T, R315N+V317S/T, S314N+K316S/T, Q313N+R315S/T, Q312N, K316N+G318S/T, V317N+D319S/T, G318N, K341N+D343S/T, S339N+K341S/T, G342N, D343N+G345S/T, R392N+E394S/T, M391N, L390N+R392S/T, K389N+M391S/T, S393N+P395S/T, E394N+R396S/T, P395N+P397S/T, R396N+G398S/T, P397N+V399S/T, G398N+L400S/T, V399N+L401S/T, L400N+R402S/T, L401N+A403S/T, R402N+P404S/T, A403N+F405S/T, P404N+P406S/T и их сочетаний, например K143N+N145S/T+R315N+V317S/T. Предпочтительно замены выбираются из группы, состоящей из K32N+A34S/T, K38N+F40S/T, Y44N+D46S/T, K143N+N145S/T, R290N+A292S/T, R315N+V317S/T, K341N+D343S/T, R392N+E394S/T, R396N+G398S/T, R402N+P404S/T и их сочетаний, например K143N+N145S/T+R315N+V317S/T. Более предпочтительно замены выбираются из группы, состоящей из K32N+A34T, K38N+F40T, Y44N+D46T, K143N+N145T, R290N+A292T, R315N+V317T, K341N+D343T, R392N+E394T, R396N+G398T, R402N+P404T и их сочетаний, в особенности K143N+N145ST+R315N+V317Т.
В дальнейшем интересном воплощении изобретения сайт гликозилирования in vivo предпочтительно вводится в положение, которое не входит в состав сайта связывания тканевого фактора и не входит в область активного сайта и гребня связывающего углубления активного сайта, которые определены выше. Предусматривается, что такие варианты гликозилирования будут в основном принадлежать к классу активных конъюгатов, как определено выше.
Так, конкретные примеры замещений, создающих такие сайты N-гликозилирования in vivo, включают замены, выбранные из группы, состоящей из K32N+A34S/T, I30N+K32S/T, A34N+R36S/T, K38N+F40S/T, T37N+L39S/T, W41N, Y44N+D46S/T, S45N+G47S/T, D46N+D48S/T, G47N+Q49S/T, K143N+N145S/T, E142N+R144S/T, L141N+K143S/T, I140N+E142S/T, R144N+A146S/T, A146N+K148S/T, S147N+P149S/T, L288N+R290S/T, L287N+D289S/T, R315N+V317S/T, S314N+K316S/T, K316N+G318S/T, V317N+D319S/T, G318N, R392N+E394S/T, M391N, L390N+R392S/T, K389N+M391S/T, S393N+P395S/T, E394N+R396S/T, P395N+P397S/T, R396N+G398S/T, P397N+V399S/T, G398N+L400S/T, V399N+L401S/T, L401N+A403S/T, R402N+P404S/T, A403N+F405S/T, P404N+P406S/T и их сочетаний, например K143N+N145S/T+ R315N+V317S/T. Предпочтительно замены выбираются из группы, состоящей из K32N+A34S/T, K38N+F40S/T, Y44N+D46S/T, K143N+N145S/T, R315N+V317S/T, R392N+E394S/T, R396N+G398S/T, R402N+P404S/T и их сочетаний, например K143N+N145S/T+R315N+V317S/T. Более предпочтительно замены выбираются из группы, состоящей из K32N+A34T, K38N+F40T, Y44N+D46T, K143N+N145T, R315N+V317T, R392N+E394T, R396N+G398T, R402N+P404T и их сочетаний, в особенности K143N+N145T+R315N+V317Т.
В еще более интересном воплощении изобретения сайт гликозилирования in vivo предпочтительно вводится в положение, которое не входит в область тканевого фактора, но входит в область активного сайта и гребня связывающего углубления активного сайта, которые определены выше. Предусматривается, что такие варианты гликозилирования в основном будут принадлежать к классу неактивных конъюгатов, как определено выше.
Так, конкретные примеры замещений, создающих такие сайты N-гликозилирования in vivo, включают замены, выбранные из группы, состоящей из I153N+ G155S/T, Q167N+L169S/T, V168N+L170S/T, L169N+L171S/T, L170N+V172S/T, L171N+N173S/T, A175S/T, A175N+L177S/T, L177N+G179S/T, G179N, G180N+L182S/TM T181N+I183S/T, V188N, V189N+A191S/T, S190N+A192S/T, A191N+H193S/T, H193N+F195S/T, F195N+K197S/T, D196N+I198S/T, K197N+K199S/T, I198N+N200S/T, K199N+W201S/T, W201N+N203S/T, R202S/T, I205S/T, V228N+I230S/T, I229N+P231S/T, I230N, P231N, S232N+Y234S/T, T233N+V235S/T, Y234N+P236S/T, V235N+G237S/T, P236N, G237N, T238N+N240S/T, T239N+H241S/T, H241N+I243S/T, D242S/T, I243N+L245S/T, A244N+L246S/T, L245N+R247S/T, L246N+L246S/T, V281N+G283S/T, S282N+W284S/T, G283N+G285S/T, W284N+Q286S/T, G285N+L287S/T, Q286N+L288S/T, D289N+G291S/T, R290N+A292S/T, G291N, A292N+A294S/T, T293N+L295S/T, P321N+I323S/T, T324N+Y326S/T, E325N+M327S/T, Y326N+F327S/T, F328N+A330S/T, S339N+K341S/T, K341N+D343S/T, G342N+S344S/T, D343N+G345S/T, S344N+G346S/T, G345N+P347S/T, P347N+A349S/T, H348N, L358N+G360S/T, T359N+I361S/T, G360N+V362S/T, I361N, V362N+W364S/T, S363N+G365S/T, W364N+Q366S/T, G365N+G367S/T, T370N+G372S/T, V376N, Y377N+R379S/T, T378N+V380S/T, R379N, V380N+Q382S/T, Q382N+I384S/T, Y383N+E385S/T, W386N+Q388S/T, L387N+K389S/T, L400N+R402S/T и их сочетания. Предпочтительно, замены выбираются из группы, состоящей из D289N+G291S/T, R290N+A292S/T, G291N, A292N+A294S/T, T293N+L295S/T, S339N+K341S/T, K341N+D343S/T, G342N+S344S/T, D343N+G345S/T и их сочетаний. Более предпочтительно, замены выбираются из группы, состоящей из D289N+G291T, R290N+A292T, G291N, A292N+A294T, T293N+L295T, S339N+K341T, K341N+D343T, G342N+S344T, D343N+G345T и их сочетаний.
Наряду с сахаридом, конъюгат по тому аспекту изобретения, что изложен в настоящем разделе, может содержать дополнительные неполипептидные части, в особенности молекулу полимера, как описано в настоящей заявке, конъюгированную по одной или нескольким группам связывания, присутствующим в полипептидной части конъюгата.
Следует иметь в виду, что любые изменения аминокислот, в особенности замены, указанные в этом разделе, могут сочетаться с любыми аминокислотными изменениями, в частности заменами, указанными в других разделах, в которых раскрываются конкретные изменения аминокислот.
Так, любые гликозилированные варианты, раскрытые в настоящем разделе, в которые был введен и/или удален, по меньшей мере, один сайт гликозилирования, например вариант, содержащий замены R315N+V317T и/или K143N+N145T, можно дополнительно конъюгировать с молекулой такого полимера, как PEG, или с любой другой неполипептидной молекулой. С этой целью для конъюгации можно использовать те группы связывания, которые уже имеются в полипептиде FVII или FVIIa, либо ввести и/или удалить группы связывания, особенно таким образом, чтобы они в количестве 1-6, в особенности 3-4 или 1, 2, 3, 4, 5 или 6 групп связывания были доступны для конъюгации.
Предпочтительно в конъюгате изобретения, в котором полипептид FVII или FVIIa содержит два сайта гликозилирования, число и молекулярный вес неполипептидных частей выбирают таким образом, чтобы их суммарный молекулярный вес находился в пределах 5-25 кД, например в пределах 10-25 кД, в особенности около 5 кД, 12 кД, 15 кД или 20 кД.
Неактивные конъюгаты
Конъюгаты изобретения можно сделать неактивными путем удаления, по меньшей мере, одного аминокислотного остатка в положении, выбранном из группы, состоящей из R152, I153, S344, D242 и H193 в SEQ ID NO: 1. Удаление может проводиться путем замещения или делеции одного или нескольких из вышеперечисленных аминокислотных остатков. Предпочтительно удаление осуществляют путем замещения, в частности путем консервативной замены. Соответственно, в настоящем изобретении неактивный полипептид FVII или FVIIa может содержать одну или несколько из следующих замен: R152X, I153X, S344X, D242X или Н193Х, где Х означает любой аминокислотный остаток, предпочтительно такой, который приводит к консервативной замене. Например, неактивный полипептид FVII или FVIIa содержит мутации R152X, где Х - это любой аминокислотный остаток, кроме лизина (так как лизин входит в состав сайта расщепления протеазами). Другие примеры специфических замен включают I153A/V/L; S344T/A/G/Y; D242E/A и/или H193R/A.
С другой стороны, активный полипептид FVII или FVIIa можно сделать неактивным путем карбамоилирования α-аминокислотной группы I153 или комплексирования с ингибитором сериновых протеаз. Подходящий белковый ингибитор сериновых протеаз выбирают из группы, состоящей из фосфорорганических соединений, сульфанилфторида, пептидных галометилкетонов, предпочтительно дансил-Phe-Pro-Arg-хлорометилкетона, дансил-Glu-Glu-Arg-хлорометилкетона, дансил-Phe-Phe-Arg-хлорометилкетона или Phe-Phe-Arg-хлорометилкетона, а также азапептида.
Конъюгат также можно сделать неактивным путем введения, по меньшей мере, одного сайта гликозилирования в положение, выбранное так, чтобы последующее гликозилирование вело к инактивации конъюгата.
Как объяснялось выше в последней части раздела "Конъюгат изобретения, в котором неполипептидная часть представлена сахаридом", такие сайты гликозилирования предпочтительно вводятся в положение, которое не входит в область тканевого фактора, но входит в область активного сайта и гребня связывающего углубления активного сайта, которые определены выше. Конкретные примеры предпочтительных замен приведены выше в разделе "Конъюгат изобретения, в котором неполипептидная часть представлена сахаридом".
Неполипептидная часть конъюгатов изобретения
Как указывалось выше, неполипептидная часть конъюгата изобретения предпочтительно выбирается из группы, состоящей из молекул полимеров, липофильных соединений, сахаридов (путем in vivo гликозилирования) и органических реагентов. Все эти агенты могут придавать желаемые свойства полипептидной части конъюгата, в частности увеличивать функциональный период полужизни in vivo и/или функциональный период полужизни в плазме. Полипептидную часть конъюгата обычно конъюгируют с неполипептидными молекулами только одного типа, но можно конъюгировать и с неполипептидными молекулами двух и более типов, например, с полимерной молекулой и сахаридом, с липофильной группировкой и сахаридом, с органическим реагентом и сахаридом, с липофильной группировкой и молекулой полимера и т.д. Конъюгирование с двумя или несколькими неполипептидными молекулами может осуществляться одновременно или поочередно.
Способы получения конъюгатов изобретения
В следующих разделах "Конъюгация с липофильным соединением", "Конъюгация с полимерной молекулой", "Конъюгация с сахаридом", "Конъюгация с органическим реагентом" описывается конъюгация с конкретными типами неполипептидных молекул. В общем, полипептидный конъюгат по изобретению может быть получен путем культивирования в соответствующих клетках хозяина в условиях, способствующих экспрессии полипептида, и выделения полипептида, причем а) полипептид содержит, по меньшей мере, один сайт N- или O-гликозилирования, а клетки хозяина являются эукариотическими клетками, обладающими способностью к гликозилированию in vivo, и/или b) полипептид конъюгируют с неполипептидной молекулой in vitro.
Следует иметь в виду, что конъюгирование нужно планировать таким образом, чтобы получить оптимальную молекулу в отношении числа присоединенных неполипептидных молекул, размера и формы таких молекул (например, будут они линейными или разветвленными), а также наличия сайтов связывания в полипептиде. Молекулярный вес используемой неполипептидной молекулы выбирают с учетом того эффекта, которого требуется достичь. Так, если главная цель конъюгации заключается в получении конъюгата с высоким молекулярным весом (например, чтобы уменьшить выведение почками), то обычно следует конъюгировать как можно меньше высокомолекулярных неполипептидных молекул, чтобы достичь требуемого молекулярного веса. Когда же нужно получить высокую степень экранирования, то это достигается посредством достаточно большого числа низкомолекулярных неполипептидных молекул (например, с молекулярным весом от 300 Д до 5 кД, например от 300 Д до 2 кД) для эффективного экранирования всех или большинства сайтов расщепления протеаз или других уязвимых сайтов полипептида.
Конъюгация с липофильным соединением
Полипептид и липофильное соединение можно конъюгировать друг с другом, непосредственно или с помощью линкера. Липофильное соединение может быть природным соединением - насыщенной или ненасыщенной жирной кислотой, дикетоном жирной кислоты, терпеном, простагландином, витамином, каротеноидом или стероидом, либо синтетическим соединением - карбоновой кислотой, спиртом, амином или сульфоновой кислотой с одной или несколькими алкил-, арил-, алкенильными группами, или же другим ненасыщенным соединением. Конъюгация между полипептидом и липофильным соединением, необязательно через линкер, может осуществляться методами, известными в этой области, например, как описано Bodanszky в Peptide Synthesis, John Wiley, New York, 1976 и в WO 96/12505.
Конъюгация с молекулой полимера, включая конъюгацию молекулы полимера по N-концу полипептида
Для конъюгации с полипептидом можно использовать любые подходящие молекулы полимеров, например природные и синтетические гомополимеры или гетерополимеры с молекулярным весом обычно в пределах приблизительно от 300 до 100000 Д, например 500-20000 Д, более предпочтительно в пределах 500-15000 Д, еще более предпочтительно в пределах 2-12 кД, например в интервале 3-10 кД. Когда применяется термин "приблизительно" в связи с определенным молекулярным весом, то слова "приблизительно", "примерно", "около" означают приблизительный средний молекулярный вес и отражают тот факт, что обычно существует определенный разброс молекулярных весов в данном препарате полимера.
Примеры гомополимеров включают полиолы (то есть поли-ОН), полиамины (поли-NH2), поликарбоновые кислоты (поли-СООН). Гетерополимер - это полимер, содержащий различные функциональные группы связывания, например, гидроксильные группы и аминогруппы.
Примеры подходящих полимерных молекул включают молекулы полимеров из числа полиалкиленоксидов (РАО), включая полиалкиленгликоли (PAG) типа полиэтиленгликоля (PEG) и полипропиленгликоля (PPG), разветвленных PEG, поливинилового спирта (PVA), поликарбоксилата, поливинилпиролидона, коангидрида полиэтилена и малеиновой кислоты, коангидрида полистирена и малеиновой кислоты, декстрана, включая карбоксиметилдекстран, или любые другие биополимеры, подходящие для уменьшения иммуногенности и/или увеличения функционального периода полужизни in vivo и/или функционального периода полужизни в плазме. Другим примером молекулы полимера может служить альбумин человека или другой распространенный белок плазмы. В общем, полимеры, получаемые из полиалкиленгликолей, биосовместимы, нетоксичны, неантигенны, неиммуногенны, обладают разнообразием в отношении водорастворимости и легко секретируются живыми организмами.
Предпочтительной полимерной молекулой является PEG, так как он обладает небольшим количеством групп, способных к перекрестным сшивкам, по сравнению с полисахаридами, например декстраном. Особый интерес представляет монофункциональный PEG, например метоксиполиэтиленгликоль (mPEG), так как химизм его реакций относительно прост (только одна реактивная группа доступна для конъюгации с группами связывания на полипептиде). Вследствие этого устраняется риск перекрестных сшивок, образуются более гомогенные полипептидные конъюгаты и реакцию молекул полимера с полипептидом легче контролировать.
Для ковалентного присоединения полимерной молекулы к полипептиду конечные гидроксильные группы молекулы полимера должны находиться в активированной форме, то есть иметь реакционноспособные функциональные группы, примеры которых включают первичные аминогруппы, гидразид (HZ), тиол, сукцинат (SUC), сукцинимидилсукцинат (SS), сукцинимидилсукцинамид (SSA), сукцинимидилпропионат (SPA), сукцинимидилкарбоксиметилат (SCM), бензотриазолкарбонат (ВТС), N-гидроксисукцинимид (NHS), альдегид, нитрофенилкарбонат (NPC) и тресилат (TRES). Соответствующие активированные молекулы полимеров имеются в продаже, например фирмы Shearwater Polymers, Inc., Huntsville, AL, USA, или фирмы PolyMASC Pharmaceuticals plc, UK.
Альтернативно, полимерные молекулы могут быть активированы методами, известными в этой области, к примеру, раскрытыми в WO 90/13540. Конкретные примеры активированных линейных или разветвленных полимеров, пригодных для применения в настоящем изобретении, описаны в каталогах Shearwater Polymers, Inc., за 1997 и 2000 г. г. (Functionalized Biocompatible Polymers for Research and Pharmaceuticals, Polyethylene Glycol and Derivates, включены в настоящее изобретение в виде ссылки).
Конкретные примеры активированных PEG-полимеров включают следующие линейные полиэтиленгликоли: NHS-PEG (например, SPA-PEG, SSPA-PEG, SBA-PEG, SS-PEG, SSA-PEG, SC-PEG, SG-PEG и SCM-PEG), а также NOR-PEG, BTC-PEG, EPOX-PEG, NCO-PEG, NPC-PEG, CDI-PEG, ALD-PEG, TRES-PEG, VS-PEG, IODO-PEG и MAL-PEG, и разветвленные полиэтиленгликоли типа PEG2-NHS и тех, что описаны в US 5932462 и US 5643575, которые включены в виде ссылки. Кроме того, в следующих публикациях, включенных в виде ссылки, раскрыты полезные полимерные молекулы и/или химизм ПЭГилирования: US 5824778, US 5476653, WO 97/32607, ЕР 229108, ЕР 402378, US 4902502, US 5281698, US 5122613, US 5219564, WO 92/16555, WO 94/04193, WO 94/14758, WO 94/17039, WO 94/18247, WO 94/28024, WO 95/00162, WO 95/11924, WO 95/13090, WO 95/33490, WO 96/00080, WO 97/18832, WO 98/41562, WO 98/48837, WO 99/32134, WO 99/32139, WO 99/32140, WO 96/40791, WO 98/32466, WO 95/06058, ЕР 439508, WO 97/03106, WO 96/21469, WO 95/13312, ЕР 921131, US 5736625, WO 98/05363, ЕР 809996, US 5629384, WO 96/41813, WO 96/07670, US 5473034, US 5516673, ЕР 605963, US 5382657, ЕР 510356, ЕР 400472, ЕР 183503 и ЕР 154316.
Конъюгация полипептида с активированными молекулами полимеров проводится любым стандартным методом, например, как описано в следующих ссылках (в которых также описаны полезные методы активации полимерных молекул): R.F. Taylor (1991) "Protein immobilisation. Fundamental and applications", Marcel Dekker, N.Y.; S.S.Wong (1992) "Chemistry of Protein Conjugation and Crosslinking", CRC Press, Florida, USA; G.T. Hermanson et al. (1993) "Immobilized Affinity Ligand Techniques", Academic Press, N.Y.). Специалисты знают, что применяемый метод активации и/или химизм конъюгации зависят от групп(ы) связывания полипептида (примеры которых приведены выше), а также от функциональных групп полимера (представлены они амином, гидроксилом, карбоксилом, альдегидом, сульфгидрилом, сукцинимидилом, малеимидом, винилсульфоном или галоацетатом). ПЭГилирование может быть направлено на конъюгирование со всеми доступными группами связывания на полипептиде (то есть тех групп связывания, которые экспонированы на поверхности полипептида) или может быть направлено на одну или несколько конкретных групп связывания, например, N-концевую аминогруппу, как описано в US 5985265. Кроме того, конъюгация может осуществляться в одну стадию или постадийно (например, как описано в WO 99/55377).
Следует иметь в виду, что ПЭГилирование нужно планировать таким образом, чтобы получить оптимальную молекулу в отношении числа присоединенных молекул PEG, размера и формы таких молекул (например, будут они линейными или разветвленными), а также наличия сайтов связывания в полипептиде. Молекулярный вес используемого полимера выбирают с учетом того эффекта, которого требуется достичь. Так, если главная цель конъюгации заключается в получении конъюгата с высоким молекулярным весом (например, чтобы уменьшить выведение почками), то обычно следует конъюгировать как можно меньше высокомолекулярных молекул полимера, чтобы достичь требуемого молекулярного веса. Когда же нужно получить высокую степень экранирования, то это достигается посредством достаточно большого числа низкомолекулярных молекул полимера (например, с молекулярным весом от 300 Д до 5 кД) для эффективного экранирования всех или большинства сайтов расщепления протеаз или других уязвимых сайтов полипептида. К примеру, можно использовать 2-8, например 3-6 таких полимеров.
При конъюгации по единственной группе связывания на белке (например, по N-концевой аминогруппе) лучше всего использовать молекулу полимера, линейного или разветвленного, с высоким молекулярным весом, предпочтительно в 10-25 кД, например 15-25 кД, например около 20 кД.
Обычно конъюгация с полимером проводится в условиях, направленных на то, чтобы как можно большее число предназначенных для полимера групп связывания прореагировало с молекулами полимера. Это достигается посредством соответствующего молярного избытка полимера относительно полипептида. Как правило, молярное соотношение активированных молекул полимера к полипептиду достигает 1000:1, например достигает 200:1 или 100:1. В некоторых случаях это соотношение, однако, может быть несколько ниже, например 50:1, 10:1 или 5:1 для достижения оптимальной реакции.
В изобретении также предусматривается присоединение полимерных молекул к полипептиду через линкер. Соответствующие линкеры хорошо известны специалистам. Предпочтительным примером служит цианурихлорид (Abuchowski et al. (1977) J.Biol. Chem., 252, 3578-3581; US 4179337; Shafer et al. (1986) J.Polym. Sci. Polym. Chem. Ed., 24, 375-378).
После конъюгации остаточные активированные молекулы полимера блокируют методами, известными в этой области, например добавлением первичного амина в реакционную смесь, после чего инактивированные молекулы полимера удаляют одним из соответствующих методов.
Следует иметь в виду, что в зависимости от условий, например аминокислотной последовательности полипептида, природы используемого активированного соединения PEG и конкретных условий ПЭГилирования, включая молярное соотношение PEG к полипептиду, можно получить варьирующие степени ПЭГилирования, причем более высокая степень ПЭГилирования получается при более высоком соотношении PEG к полипептиду. Однако ПЭГилированные полипептиды, образующиеся при любом процессе ПЭГилирования, обычно имеют статистическое распределение полипептидных конъюгатов с небольшими различиями в степени ПЭГилирования.
В одном интересном воплощении изобретения полипептидный конъюгат по изобретению содержит молекулу полимера, ковалентно присоединенную к A1 на N-конце полипептида FVII или FVIIa дикого типа, приведенного в SEQ ID NO: 1, причем эта молекула полимера является единственной молекулой полимера, присоединенной к полипептиду. Предпочтительно такие полипептидные конъюгаты содержат единственную молекулу PEG, присоединенную к N-концу полипептида, и не содержат других молекул PEG. В частности, предпочтительны линейные или разветвленные молекулы PEG с молекулярным весом не менее 5 кД, особенно 10-25 кД или 15-25 кД, например около 20 кД. Полипептидный конъюгат по этому воплощению может дополнительно содержать один или несколько сахаридов, присоединенных по сайтам N- или O-гликозилирования в полипептиде, или сахариды, присоединенные путем гликозилирования in vitro.
В следующем интересном воплощении изобретения полипептидный конъюгат по изобретению содержит молекулы полимера, ковалентно присоединенные к А1 и I153 на N-концах полипептида FVIIa дикого типа, приведенного в SEQ ID NO: 1, причем эти молекулы полимера являются единственными молекулами полимера, присоединенными к полипептиду. Предпочтительно такие полипептидные конъюгаты содержат молекулы PEG, присоединенные к обоим N-концам FVIIa, и не содержат других молекул PEG. В частности, предпочтительны линейные или разветвленные молекулы PEG с молекулярным весом не менее 5 кД, особенно 10-25 кД или 15-25 кД, например около 20 кД. Полипептидный конъюгат по этому воплощению может дополнительно содержать один или несколько сахаридов, присоединенных по сайтам N- или O-гликозилирования в полипептиде, или сахариды, присоединенные путем гликозилирования in vivo.
Одним из предпочтительных способов избирательной конъюгации таких молекул полимеров, как молекулы PEG, с N-концом полипептида является способ, раскрытый в US 5985265. Этот способ заключается в восстановительном алкилировании (реакции N-концевых аминогрупп полипептида с содержащим альдегид полипептидом, например с альдегид-PEG, в присутствии восстанавливающего агента типа NaCNBH3). В этом способе используют отличия в реакционной способности различных типов первичных аминогрупп (лизина по сравнению с N-концевой аминогруппой) полипептида, доступных для реакции, что дает возможность практически избирательно проводить реакцию полипептида по N-концу с молекулой полимера, содержащей карбонильную группу, например с альдегид-PEG. Реакцию проводят при таком рН, которое позволяет воспользоваться отличиями в рКа между ε-аминогруппами остатков лизина и α-аминогруппой N-концевого остатка полипептида. Для проявления отличий в реакционной способности реакцию обычно проводят в слабокислой среде. Конкретные примеры соответствующего интервала рН включают рН 4,5-7, например рН 4,5-6 или рН 5-6, в особенности примерно рН 5.
В другом особом воплощении полипептидный конъюгат по изобретению содержит молекулу PEG, соединенную с каждым из остатков лизина в полипептиде, доступных для ПЭГилирования, в частности линейную или разветвленную молекулу PEG с молекулярным весом 1-15 кД, как правило 2-12 кД или 3-10 кД, например около 5 или 6 кД.
В следующем воплощении полипептидный конъюгат по изобретению содержит молекулу PEG, соединенную с каждым из остатков лизина в полипептиде, доступных для ПЭГилирования, и дополнительно с N-концевым аминокислотным остатком полипептида.
Может применяться и ковалентное присоединение углеводных молекул (типа декстрана) in vitro по аминокислотным остаткам полипептида, например, как описано в WO 87/05330 и в Aplin et al., CRC Crit. Rev. Biochem., pp.259-306, 1981. Присоединение углеводных молекул или PEG in vitro по остаткам Gln белка или пептида может проводиться с помощью трансглутаминаз (ТГаз). Трансглутаминазы катализируют перенос донорских аминогрупп на остатки Gln белка или пептида в так называемой реакции перекрестного сшивания. Донорские аминогруппы могут находиться на белке или пептиде как ε-аминогруппы остатков Lys или могут входить в состав больших или небольших органических молекул. Примером небольшой органической молекулы, служащей донором аминогрупп в катализируемом ТГазой перекрестном сшивании, служит путресцин (1,4-диаминобутан). Примером большой органической молекулы, служащей донором аминогрупп в катализируемом ТГазой перекрестном сшивании, служит аминосодержащий PEG (Sato et al., 1996, Biochemistry 35, 13072-13080).
ТГазы в общем являются высокоспециализированными ферментами, и не каждый остаток Gln, выходящий на поверхность белка, доступен для катализируемого ТГазами перекрестного сшиванию с аминосодержащими веществами. Наоборот, только немногие остатки Gln естественно функционируют в качестве субстрата для ТГаз, однако точные параметры, определяющие, какие остатки Gln являются хорошими субстратами для ТГаз, остаются неизвестными. Так, чтобы сделать белок подверженным катализируемым ТГазами реакциям перекрестного сшивания, зачастую необходимо вставить в удобные положения куски аминокислотных последовательностей, хорошо известных в качестве субстратов ТГаз. Известно несколько аминокислотных последовательностей, являющихся отличными природными субстратами ТГаз или содержащими такие субстраты, например субстанция Р, елафин, фибриноген, фибронектин, ингибитор α2-плазмина, α-казеины и β-казеины.
Конъюгирование с молекулой сахарида
Для того чтобы осуществить гликозилирование in vivo молекулы FVII, содержащей один или несколько сайтов гликозилирования, нуклеотидную последовательность, кодирующую полипептид, необходимо ввести в гликозилирующий эукариотический экспрессионный организм. Клетки экспрессионного организма можно выбрать из клеток грибов (нитчатых грибов или дрожжей), насекомых или животных либо трансгенных растений. В одном из воплощений клетка-хозяина является клеткой млекопитающих типа клеток СНО, ВНК или НЕК, например, НЕК 293, или клеткой насекомых типа клеток SF9, или клеткой дрожжей, например, S. cerevisiae или Pichia pastoris, или любой из клеток-хозяина, указанных далее.
Конъюгирование с органическим реагентом
Ковалентная модификация полипептида может осуществляться путем реакции одной или нескольких групп связывания полипептида с органическим реагентом. Соответствующие реагенты и методы хорошо известны в этой области. Так, цистеиниловые остатки чаще всего подвергают реакции с α-галоацетатами (и соответствующими аминами) типа хлоруксусной кислоты или хлорацетамида, получая карбоксиметильные или карбоксиамидометильные производные. Остатки цистеинила также модифицируют в реакции с бромотрифторацетоном, α-бром-β-(4-имидазоил)пропионовой кислотой, хлорацетилфосфатом, N-алкилмалеимидами, 3-нитро-2-пиридилдисульфидом, метил-2-пиридилдисульфидом, n-хлормеркурибензоатом, 2-хлоромеркури-4-нитрофенолом или хлоро-7-нитробензо-2-оксо-1,3-диазолом. Остатки гистидила модифицируют в реакции с диэтилпирокарбонатом при рН 5,5-7,0, так как этот реагент относительно специфичен к боковой цепи гистидила. Применяется также пара-бромфенацилбромид. Реакцию предпочтительно проводят в 0,1 М какодилате натрия при рН 6,0. Остатки лизинила и концевые аминогруппы подвергают реакции с ангидридом янтарной или другой карбоновой кислоты. Модификация с помощью таких агентов вызывает обращение заряда остатков лизинила. Другие полезные реагенты для модификации α-аминосодержащих остатков включают имидоэфиры, такие как метилпиколинимидат, пиридоксальфосфат, пиридоксаль, хлороборгидрид, тринитробензолсульфоновая кислота, O-метилизомочевина, 2,4-пентандион, а также катализируемая трансаминазой реакция с глиоксилатом. Остатки аргинила модифицируют с помощью реакции с одним или несколькими стандартными реагентами, в числе которых фенилглиоксаль, 2,3-бутандион, 1,2-циклогександион и нингидрин. При модификации остатков аргинина необходимо проводить реакцию в щелочных условиях из-за высокого значения рКа функциональной группы гуанидина.
Кроме того, эти реагенты могут реагировать с группами лизина, а также с гуанидиновой группой аргинина. Боковые карбоксильные группы (аспартила или глутамила) избирательно модифицируют в реакции с карбодиимидами (R-N=C=N-R'), где R и R' - различные алкильные группы, такие как 1-циклогексил-3-(2-морфолинил-4-этил)карбодиимид или 1-этил-3-(4-азониа-4,4-диметилпентил)карбодиимид. Кроме того, остатки аспартила и глутамила превращают в остатки аспарагинила и глутаминила при реакции с ионами аммония.
Блокирование функционального сайта
Сообщалось, что чрезмерная конъюгация с полимерами может приводить к потере активности полипептида, с которым конъюгирована неполипептидная часть. Эту проблему можно устранить, например, путем удаления групп связывания, находящихся в функциональном сайте, или обратимого блокирования функционального сайта до конъюгации так, чтобы функциональный сайт был блокирован во время конъюгации. Последняя стратегия составляет следующие воплощения изобретения (первая стратегия была раскрыта выше, например удаление остатков лизина, которые могут находиться вблизи от функционального сайта). В частности, согласно второй стратегии конъюгация между полипептидом и неполипептидной частью проводится в условиях, когда функциональный сайт полипептида блокирован вспомогательной молекулой, например тканевым фактором, способным связываться с функциональным сайтом полипептида, или ингибитором сериновых протеаз.
Предпочтительно вспомогательной молекулой служит молекула, которая специфически распознает функциональный сайт полипептида, к примеру рецептор, особенно молекула тканевого фактора - целая молекула либо соответствующим образом укороченная форма тканевого фактора, или же две молекулы, одна из которых является тканевым фактором, а другая - пептидом или пептидным ингибитором, который связывается в области вокруг каталитической триады и таким образом защищает ее (эта область предпочтительно определяется как аминокислотные остатки в пределах 10Å от любого из атомов в каталитической триаде).
С другой стороны, вспомогательной молекулой может служить антитело, особенно моноклональное антитело, распознающее полипептид FVII. В частности, вспомогательной молекулой может служить нейтрализующее моноклональное антитело.
Полипептид подвергают реакции со вспомогательной молекулой до проведения конъюгации. Это обеспечивает экранирование или защиту функционального сайта полипептида, вследствие чего он становится недоступным для модификации неполипептидной молекулой, например полимером. После отмывки от вспомогательных молекул можно выделить конъюгат полипептида и неполипептидной части при сохранении, по крайней мере, частичном, функционального сайта.
Последующая конъюгация между полипептидом с блокированным функциональным сайтом и полимером, липофильным соединением, сахаридом, органическим реагентом или любым другим соединением проводится обычным образом, например, как описано выше в разделах "Конъюгация с..."
Независимо от природы вспомогательной молекулы, используемой для экранирования функционального сайта полипептида от конъюгации, желательно, чтобы вспомогательная молекула не содержала или содержала лишь небольшое число групп связывания для выбранной неполипептидной части в той части (частях) молекулы, где конъюгация по таким группам будет препятствовать отсоединению конъюгированного полипептида от вспомогательной молекулы. При этом можно достичь избирательной конъюгации с группами связывания, присутствующими в незащищенных частях полипептида, и можно повторно использовать вспомогательные молекулы для новых циклов конъюгации. Например, если неполипептидная молекула является молекулой полимера типа PEG, для которого группой связывания служит ε-аминогруппа лизина или N-концевой аминокислотный остаток, желательно, чтобы вспомогательная молекула практически не содержала способных к конъюгации ε-аминогрупп, предпочтительно от любых ε-аминогрупп. Соответственно, в предпочтительном воплощении вспомогательная молекула является белком или пептидом, способным связываться с функциональным сайтом полипептида, и не содержит никаких способных к конъюгации групп связывания для выбранной неполипептидной части.
В следующем воплощении вспомогательную молекулу сначала ковалентно присоединяют к твердой фазе типа носителей для колоночной хроматографии, например гранулам Sephadex или агарозы, или к поверхности, например, лабораторной посуды. После этого полипептид наносят на колонку со вспомогательной молекулой и проводят конъюгирование методами, известными в этой области, например, как описано выше в разделах "Конъюгация с...." Такая процедура позволяет отделить полипептидный конъюгат от вспомогательной молекулы при помощи элюции. Полипептидный конъюгат элюируют стандартными методами в таких физико-химических условиях, которые не вызывают значительной деградации полипептидного конъюгата. Жидкую фазу, содержащую полипептидный конъюгат, отделяют от твердой фазы, с которой вспомогательная молекула остается ковалентно связанной. Разделение может осуществляться и другими способами. Так, вспомогательную молекулу можно соединить со второй молекулой (например, биотином), которая распознается специфическим лигандом (например, стрептавидином). Специфический лиганд можно соединить с твердой фазой, что позволит отделить полипептидный конъюгат от комплекса вспомогательная молекула-вторая молекула при пропускании через вторую колонку со вспомогательной молекулой на твердой фазе, на которой при последующей элюции будет задерживаться комплекс вспомогательная молекула-вторичная молекула, но не полипептидный конъюгат. Полипептидный конъюгат можно освободить от вспомогательной молекулы любым подходящим образом. Разблокирование достигается при создании условий, в которых вспомогательная молекула диссоциирует из функционального сайта FVII, с которым она связана. Например, комплекс между антителом, с которым конъюгирован полипептид, и антиидиотипическим антителом может быть диссоциирован при изменении рН в кислую или щелочную сторону. Еще более предпочтительно применение конформационно-специфических антител, которые распознают Са2-специфическую конформацию FVII и затем могут быть элюированы с помощью ЭДТА в мягких условиях.
Присоединение ингибитора сериновых протеаз
Присоединение ингибитора сериновых протеаз может проводиться в соответствии с методом, описанным в WO 96/12800.
Конъюгация полипептида с меткой
В альтернативном воплощении полипептид экспрессируется в виде слитого белка с меткой, то есть аминокислотной последовательностью или отрезком пептида, обычно состоящим из 1-30, например 1-20 аминокислотных остатков. Помимо того что метка дает возможность быстрой и легкой очистки, она является удобным инструментом для обеспечения конъюгации между меченым полипептидом и неполипептидной молекулой. В частности, метка может применяться для проведения конъюгации в микропланшетах или на носителях типа магнитных шариков, на которых полипептид с меткой можно иммобилизировать через метку. Конъюгация несущего метку полипептида в микропланшетах имеет то преимущество, что несущий метку полипептид можно иммобилизовать в микропланшетах прямо из культуральной жидкости (в принципе, без какой-либо очистки) и подвергнуть конъюгации. При этом уменьшается общее число стадий процесса (от экспрессии до конъюгации). Кроме того, метка может функционировать в качестве молекулы спейсера, обеспечивая лучший доступ к иммобилизованному полипептиду при конъюгации. Несущий метку полипептид можно конъюгировать с любой из описанных неполипептидных молекул, например, с молекулой полимера типа PEG.
Конкретная природа применяемой метки не является критической, если только она способна экспрессироваться вместе с полипептидом и быть иммобилизированной на соответствующей поверхности или носителе. Целый ряд таких меток имеется в продаже, например, от фирмы Unizyme Laboratories, Дания. Например, метка может представлять собой любую из следующих последовательностей:
His-His-His-His-His-His
Met-Lys-His-His-His-His-His-His
Met-Lys-His-His-Ala-His-His-Gln-His-His
Met-Lys-His-Gln-His-Gln-His-Gln-His-Gln-His-Gln-His-GIn
Met-Lys-His-Gln-His-Gln-His-Gln-His-Gln-His-Gln-His-Gln-GIn
или любую из следующих:
EQKLI SEEDL (С-концевая метка, описанная в Mol. Cell. Biol. 5: 3610-16, 1985)
DYKDDDDK (С- или N-концевая метка)
YPYDVPDYA
Антитела к вышеуказанным меткам имеются в продаже, например, от фирм ADI, Aves Lab и Research Diagnostics.
Впоследствии метку можно отщепить от полипептида с помощью коммерчески доступных ферментов.
Способы получения полипептида изобретения или полипептидной части конъюгата изобретения
Полипептид настоящего изобретения или полипептидную часть конъюгата изобретения, необязательно в гликозилированной форме, можно получить любым подходящим способом, известным в этой области. Такие способы включают конструирование нуклеотидной последовательности, кодирующей полипептид, и экспрессию этой последовательности в соответствующих трансформированных или трансфецированных клетках хозяина. Предпочтительно клетка-хозяин обладает способностью к γ-карбоксилированию, как клетки млекопитающих. Однако полипептиды изобретения могут быть получены, хотя и с меньшей эффективностью, путем химического синтеза или комбинации химического синтеза и технологии рекомбинантной ДНК.
Нуклеотидная последовательность, кодирующая полипептид или полипептидную часть конъюгата изобретения, может быть сконструирована путем выделения или синтеза нуклеотидной последовательности, кодирующей родительский FVII, например hFVII с аминокислотной последовательностью, приведенной в SEQ ID NO: 1, с последующим изменением нуклеотидной последовательности так, чтобы обеспечить введение (то есть вставку или замену) или удаление (то есть делецию или замену) соответствующих аминокислотных остатков.
Нуклеотидную последовательность удобно модифицировать с помощью направленного мутагенеза в соответствии со стандартными методами. С другой стороны, нуклеотидную последовательность можно получить химическим синтезом, например, с помощью синтезатора олигонуклеотидов, при этом олигонуклеотиды конструируют на основе аминокислотной последовательности искомого полипептида и предпочтительно выбирают кодоны, которые преимущественно употребляются в тех клетках, которые будут вырабатывать рекомбинантный полипептид. Например, можно синтезировать несколько небольших олигонуклеотидов, кодирующих отдельные отрезки искомого полипептида, и собрать их вместе с помощью ПЦР, лигирования или цепной реакции лигирования (LCR) (Barany, PNAS 88: 189-193, 1991). Индивидуальные олигонуклеотиды, как правило, содержат свисающие 5'- или 3'-концы для комплементарной сборки.
Имеются альтернативные способы модификации нуклеотидных последовательностей для получения вариантов полипептидов для высокопроизводительного скринирования, например способы, включающие гомологический кроссинговер, как описано в US 5093257, и способы, включающие перетасовку генов, то есть рекомбинацию между двумя или более гомологичными нуклеотидными последовательностями, приводящую к образованию новых нуклеотидных последовательностей, содержащих ряд нуклеотидных изменений по сравнению с исходными нуклеотидными последовательностями. Перетасовка генов (также известная как перетасовка ДНК) включает один или несколько циклов произвольной фрагментации и сборки новых нуклеотидных последовательностей с последующим скринированием для отбора нуклеотидных последовательностей, кодирующих полипептиды с желательными свойствами. Для того чтобы произошла основанная на гомологии перетасовка нуклеиновых кислот, соответствующие части нуклеотидных последовательностей предпочтительно должны быть идентичными не менее чем на 50%, например не менее чем на 60%, более предпочтительно не менее чем на 70%, например не менее чем на 80%. Рекомбинация может проводиться in vitro или in vivo.
Примеры соответствующих методов перетасовки генов in vitro раскрыты в Stemmer et al. (1994) Proc. Natl. Acad. Sci. USA; vol.91, pp.10747-10751; Stemmer (1994) Nature, vol.370, pp.389-391; Smith (1994) Nature, vol.370, pp.324-325; Zhao et al., Nat. Biotechnol. 1998, Mar; 16(3): 258-61; Zhao H. and Arnold FB, Nucleic Acids Research, 1997, Vol.25, №6, pp.1307-1308; Shao et al., Nucleic Acids Research. 1998, Jan 15, 26(2): pp.681-83; и WO 95/17413.
Пример соответствующего метода перетасовки in vivo раскрыт в WO 97/07205. Другие методы мутагенеза последовательностей нуклеиновых кислот путем рекомбинации in vitro или in vivo раскрыты в WO 97/20078 и US 5837458. Примеры специфических методов перетасовки включают "семейную перетасовку", "синтетическую перетасовку" и "перетасовку in silico".
При семейной перетасовке семейство гомологичных генов из различных видов подвергают одному или нескольким циклам перетасовки с последующим скринированием или селекцией. Методы семейной перетасовки раскрыты, к примеру, в Crameri et al. (1998) Nature, vol.391, pp.288-291; Christians et al. (1999) Nature Biotechnology, vol.17, pp.259-264; Chang et al. (1999) Nature Biotechnology, vol.17, pp.793-797; и Ness et al. (1999) Nature Biotechnology, vol.17, pp.893-896.
Синтетическая перетасовка включает получение библиотек перекрывающихся синтетических олигонуклеотидов на основе сопоставления последовательностей соответствующих гомологичных генов. Синтетические олигонуклеотиды подвергают рекомбинации и полученные рекомбинантные последовательности нуклеиновых кислот скиринируют и, при желании, используют для дальнейших циклов перетасовки. Методы синтетической перетасовки раскрыты в WO 00/42561.
Перетасовка in silico относится к методу перетасовки ДНК, осуществляемой или моделируемой с помощью компьютерных систем, при этом частично или полностью устраняется необходимость в физической манипуляции с нуклеиновыми кислотами. Методы перетасовки in silico раскрыты в WO 00/42560.
После сборки (путем синтеза, направленного мутагенеза или другим способом) нуклеотидную последовательность, кодирующую полипептид, встраивают в рекомбинантный вектор и функционально связывают с контрольными последовательностями, необходимыми для экспрессии FVII в нужных транформированных клетках хозяина.
Конечно, следует иметь в виду, что не все векторы и контролирующие экспрессию последовательности функционируют одинаково хорошо при экспрессии нуклеотидной последовательности, кодирующей описанный здесь полипептид. Также не все клетки-хозяева функционируют одинаково хорошо с одной и той же экспрессионной системой. Однако специалист в этой области имеет возможность сделать выбор из этих векторов, контролирующих экспрессию последовательностей и клеток-хозяев без излишнего экспериментирования. Например, при выборе вектора следует учитывать клетки-хозяев, так как вектор должен реплицироваться в них или быть способным встраиваться в хромосому. Следует также учитывать число копий вектора, способность контролировать это число копий и экспрессию любых других белков, кодируемых вектором, таких как маркеры-антибиотики. При выборе контролирующей экспрессию последовательности также следует учитывать целый ряд факторов. К ним относятся, например, относительная сила последовательности, ее контролируемость и совместимость с нуклеотидной последовательностью, кодирующей полипептид, особенно в отношении возможных вторичных структур. Хозяев следует выбирать с учетом их совместимости с выбранным вектором, токсичности продукта, кодируемого нуклеотидной последовательностью, особенностей секреции, способности к правильной сборке полипептида, требований к ферментации и культивированию и легкости очистки продуктов, кодируемых нуклеотидной последовательностью.
Рекомбинантный вектор может быть автономно реплицирующимся вектором, то есть вектором, существующим в виде внехромосомной единицы, репликация которого не зависит от хромосомной репликации, представляя собой, к примеру, плазмиду. С другой стороны, вектором может быть такой вектор, который при введении в клетку-хозяина встраивается в ее геном и реплицируется вместе с хромосомой, в которую он встроился.
Вектором предпочтительно служит экспрессионный вектор, в котором нуклеотидная последовательность, кодирующая полипептид изобретения, функционально связана с дополнительными сегментами, необходимыми для транскрипции этой нуклеотидной последовательности. Как правило, вектор происходит из плазмиды или вирусной ДНК. Целый ряд экспрессионных векторов, подходящих для экспрессии в указанных клетках, коммерчески доступны или описаны в литературе. К числу полезных экспрессионных векторов для эукариотических клеток относятся векторы, содержащие контролирующие экспрессию последовательности из SV40, вируса коровьей папилломы, аденовирусов и цитомегаловируса. Конкретно, такими векторами являются, к примеру, pCDNA3.1 (+)/Hyg (Invitrogen, Carlsbad, CA, USA) и pCI-Neo (Stratagene, La Jola, CA, USA). К числу полезных экспрессионных векторов для дрожжевых клеток относятся плазмида 2 μ ее производные, вектор РОТ1 (US 4931373), вектор pJSО37, описанный Okkels, Ann. New York Acad. Sci. 782, 202-207, 1996, и pPICZ А, В или С (Invitrogen). К числу полезных векторов для клеток насекомых относятся pVL941, pBG311 (Cate et al., "Isolation of the Bovine and Human Genes for Mullerian Inhibiting Substance and Expression of the Human Gene in Animal Cells", Cell, 45, pp.685-98 (1986)), pBlueBac 4.5 и pMelbac (оба фирмы Invitrogen). К числу полезных экспрессионных векторов для бактериальных клеток относятся известные бактериальные плазмиды, такие как плазмиды из Е.coli, включая pBR322, рЕТ3а и рЕТ12а (оба фирмы Novagen Inc., WI, USA), плазмиды для более широкого круга хозяев типа RP4, многочисленные производные фага лямбда, напр., NM989, и других ДНК-содержащих фагов, как М13 и нитчатые фаги с одноцепочечной ДНК.
Другие векторы для применения в этом изобретении включают те, которые позволяют амплификацию нуклеотидных последовательностей, кодирующих полипептид. Такие амплификационные векторы хорошо известны в этой области. К ним относятся векторы, способные амплифицироваться путем DHFR-амплификации (см., к примеру, Kaufman, U.S. Pat. №4470461, Kaufman and Sharp, "Construction of a Modular Dihydrofolate Reductase cDNA Gene: Analysis of Signals Utilized for Efficient Expression", Mol. Cell. Biol., 2, pp.1304-19 (1982) и глутаминсинтетазной амплификации ("GS"-амплификации) (см., к примеру, US 5122464 и ЕР 338841).
Рекомбинантный вектор может также содержать последовательность ДНК, дающую вектору способность реплицироваться в нужных клетках. Примером этого (когда клетки хозяина являются клетками млекопитающих) является начало (origin) репликации SV40. Когда клетки являются клетками дрожжей, то подходящими последовательностями, дающими вектору способность к репликации, являются гены репликации REP 1-3 и начало репликации дрожжевой плазмиды 2μ.
Вектор может также содержать селектируемый маркер, скажем, ген, продукт которого восполняет дефект в клетках хозяина, например, ген, кодирующий дигидрофолатредуктазу (DHFR), или ген TPI Schizosaccharomyces pombe (описаны P.R. Russel, Gene 40, 1985, pp. 125-130), или ген, придающий устойчивость к лекарственному препарату - ампициллину, канамицину, тетрациклину, хлорамфениколу, неомицину, гигромицину или метотрексату). К селекционным маркерам для Schizosaccharomyces cerevisiae относятся ura3 и leu2. К селекционным маркерам для нитчатых грибов относятся amdS, pyrG, arcB, niaD и sC.
Термин "контрольная последовательность" в настоящем изобретении относится ко всем компонентам, необходимым или полезным для экспрессии полипептида изобретения. Каждая контрольная последовательность может быть природной или чужеродной для последовательности нуклеиновой кислоты, кодирующей полипептид. К таким контрольным последовательностям относятся лидерные последовательности, последовательности полиаденилирования, последовательности пропептидов, промоторы, энхансеры или вышерасположенные (upstream) активирующие последовательности, последовательности сигнальных пептидов и терминаторы транскрипции, но не ограничиваются ими. Как минимум, контрольная последовательность включает промотор.
В настоящем изобретении может применяться широкий набор контрольных последовательностей экспрессии. К таким полезным последовательностям относятся последовательности, контролирующие экспрессию, связанные со структурными генами вышеупомянутых экспрессионных векторов, а также любые последовательности, которые известны как контролирующие экспрессию генов прокариотических и эукариотических генов или их вирусов, и различные их сочетания.
К числу подходящих контрольных последовательностей, управляющих транскрипцией в клетках млекопитающих, относятся ранние и поздние промоторы SV40 и аденовирусов, например основной поздний промотор аденовирусов 2, промотор МТ-1 (гена металлотионеина), промотор самых ранних генов цитомегаловируса человека (CMV), промотор фактора элонгации человека 1α (EF-1α), минимальный промотор белка теплового шока 70 у Drosophila, промотор вируса саркомы Rous (RSV), промотор убиквитина С человека (UbC), терминатор гормона роста человека, сигналы полиаденилирования области Elb SV40 или аденовирусов, и консенсусные последовательности Козака (Kozak M., J. Mol. Biol. 1987, Aug. 20; 196(4); 947-50).
Для усиления экспрессии в клетках млекопитающих можно встроить синтетический интрон в 5'-нетраслируемый участок нуклеотидной последовательности, кодирующей полипептид. Примером синтетического интрона может служить искусственный интрон из плазмиды pCI-Neo (фирмы Promega Corporation, WI, USA).
К числу подходящих контрольных последовательностей, управляющих транскрипцией в клетках насекомых, относятся промотор полигедрина, промотор Р10, промотор основного белка вируса полигедроза Autographa californica, промотор самого раннего гена 1 бакуловируса, промотор отдаленно-раннего гена 39К бакуловируса и последовательность полиаденилирования SV40.
К числу подходящих контрольных последовательностей для дрожжевых клеток относятся промоторы α-системы спаривания дрожжей, промотор дрожжевой триозофосфатизомеразы (TPI), промоторы гликолитических генов или генов алкогольдегидрогеназы дрожжей, промотор ADH2-4c и индуцибельный промотор GAL. К числу подходящих контрольных последовательностей для клеток нитчатых грибов относятся промотор и терминатор ADH3, промоторы из генов, кодирующих ТАКА-амилазу, триозофосфатизомеразу или щелочную протеазу Aspergillus oryzae, α-амилазу A.niger, глюкоамилазу A.niger или A.nidulans, ацетамидазу A.nidulans, аспартатную протеиназу или липазу Rhizomucor miehei, терминатор ТРI1 и терминатор ADH3. К числу подходящих контрольных последовательностей для бактериальных клеток относятся промоторы системы lac, системы trp, системы ТАС или TRC и основные промоторные участки фага λ.
Присутствие или отсутствие сигнального пептида зависит от того, какие клетки хозяина используются для получения экспрессируемого полипептида (является он внутриклеточным или внеклеточным полипептидом) и желательна ли его секреция. Для нитчатых грибов сигнальный пептид можно легко получить из гена, кодирующего амилазу или глюкоамилазу Aspergillus sp., из гена, кодирующего липазу или протеазу Rhizomucor miehei или липазу Humicola lanuginosa. Сигнальный пептид предпочтительно получают из гена, кодирующего ТАКА-амилазу A.oryzae, нейтральную α-амилазу A.niger, кислотоустойчивую амилазу A.niger или глюкоамилазу А.niger. Для клеток насекомых сигнальный пептид можно легко получить из таких генов насекомых (см. WO 90/05783), как предшественник адипокинетического гормона бабочки Manduca sexta, (см. US 5023328), мелиттин пчел (Invitrogen), UDP-глюкозилтрансфераза экдистероидов (egt) (Murphy et al., Protein Expression and Purification 4, 349-357 (1993) или панкреатическая липаза человека (hpl) (Methods in Enzymology 284, pp. 262-272, 1997). Предпочтительным сигнальным пептидом для клеток млекопитающих является таковой FVII или сигнальный пептид легкой цепи Ig k грызунов (Coloma М. (1992) J.Imm. Methods 152: 89-104). Для дрожжевых клеток подходящим сигнальным пептидом оказался сигнальный пепид α-фактора S.cerevisiae (см. US 4870008), модифицированный сигнальный пептид карбоксипептидазы (см. L.A.Valls et al., Cell 48, 1987, pp. 887-897), сигнальный пептид BAR1 дрожжей (см. WO 87/02670), сигнальный пептид аспартатной протеазы 3 (YAP3) дрожжей (см. М. Egel-Mitani et al., Yeast 6, 1990, pp. 127-137) и искусственная лидерная последовательность ТА57 (WO 98/32867). Для клеток Е.coli подходящим сигнальным пептидом оказался сигнальный пептид ompA (EP 581821).
Нуклеотидная последовательность изобретения, кодирующая полипептид FVII, полученная путем направленного мутагенеза, синтеза, ПЦР или других методов, может необязательно включать нуклеотидную последовательность, кодирующую сигнальный пептид. Сигнальный пептид присутствует в случае, когда полипептид должен секретироваться из клеток, в которых он экспрессируется. Такой сигнальный пептид, если он есть, должен быть узнаваемым клетками, выбранными для экспрессии полипептида. Сигнальный пептид может быть гомологичным (родственным FVII) или гетерологичным (то есть происходить из другого источника, чем FVII) полипептиду FVII, или может быть гомологичным или гетерологичным клеткам хозяина, то есть либо представлять собой сигнальный пептид, который в норме экспрессируется в клетках хозяина, либо в норме не экспрессируется в клетках хозяина. Соответственно, сигнальный пептид может быть прокариотическим, например, из таких бактерий, как Е.coli, или эукариотическим, к примеру, из клеток млекопитающих, насекомых или дрожжей.
Для получения полипептида или полипептидной части конъюгата изобретения можно использовать клетки или клеточные линии любых подходящих хозяев, включая бактерии, грибы (включая дрожжи), растения, насекомых, млекопитающих или других подходящих животных, а также трансгенных животных или растений. Примеры бактериальных клеток включают такие грамположительные бактерии, как штаммы Bacillus, к примеру В.brevis или В.subtilis, Pseudomonas или Streptomyces, или такие грамотрицательные бактерии, как штаммы Е. coli. Введение вектора в бактериальную клетку может осуществляться, например, путем трансформации протопластов (см., к примеру, Chang and Cohen, 1979, Molecular General Genetics 168: 111-115), с помощью компетентных клеток (см., к примеру, Young and Spizizin, 1961, Journal of Bacteriology 81: 823-829 или Dubnau and Davidoff-Abelson, 1971, Journal of Molecular Biology 56: 209-221), электропорации (см., к примеру, Shigekawa and Dower, 1988, Biotechniques 6: 742-751) или конъюгации (см., к примеру, Koehler and Thorne, 1987, Journal of Bacteriology 169: 5771-5278). К числу подходящих клеток нитчатых грибов относятся штаммы Aspergillus, например A.oryzae, A.niger или A.nidulans, Fusarium или Trichoderma. Клетки грибов можно трансформировать способом, включающим образование протопластов, трансформацию протопластов и регенерацию клеточной стенки известными методами. Подходящие способы трансформации клеток Aspergillus описаны в ЕР 238023 и US 5679543. Подходящие способы трансформации штаммов Fusarium описаны Malardier et al., 1989, Gene 78: 147-156, и WO 96/00787. К числу подходящих дрожжевых клеток относятся штаммы Saccharomyces, например S.cerevisiae, Schizosaccharomyces, Klyveromyces, Pichia, как P.pastoris или Р.methanolica, Hansenula, как Н.polymorpha или yarrowia. Дрожжи можно трансформировать способами, описанными Becker and Guarente, In Abelson J.N. and Simon M.I., editors, Guide to Yeast Genetics and Molecular Biology, Methods in Enzymology, Volume 194, pp. 182-187, Academic Press, Inc., New York; Ito et al., 1983, Journal of Bacteriology 153: 163; Hinnen et al., 1978, Proceedings of the National Academy of Sciences USA 75: 1920, a также как раскрыто фирмой Clontech Laboratories, Inc., Palo Alto, CA, USA (в методичке для продукта Yeastmaker™ Yeast Transformation System Kit). К числу подходящих клеток насекомых относятся клеточные линии бабочек Spodoptera frugiperda (Sf9 или Sf21) или клетки Trichoplusia ni (High Five) (US 5077214). Трансформация клеток насекомых и выработка в них гетерологичных полипептидов может проводиться как описано Invitrogen. К числу подходящих клеток млекопитающих относятся клеточные линии яичников китайского хомячка (СНО), например СНО-К1 (АТСС CCL-61); клеточные линии зеленой мартышки (COS), например COS 1 (АТСС CRL-1650), COS 7 (АТСС CRL-1651); клетки мышей (например, NS/О); клеточные линии почек новорожденных хомячков (ВНК), например АТСС CRL-1632 или АТСС CCL-10, и клетки человека, например НЕК 293 (АТСС CRL-1573), а также клетки растений в клеточных культурах. В этой области известны и другие подходящие клеточные линии из таких общедоступных хранилищ, как American Type Culture Collection, Rockville, Maryland. Кроме того, можно так модифицировать клетки млекопитающих, к примеру клетки СНО, чтобы они экспрессировали сиалилтрансферазу, например 1,6-сиалилтрансферазу, как описано в US 5047335, чтобы улучшить гликозилирование полипептида FVII или FVIIa.
Для улучшения секреции особый интерес может представлять получение полипептида изобретения вместе с эндопротеазой, в частности РАСЕ (Paired basic amino acid converting enzyme), как описано в US 5986079, например эндопротеазой Кех2, как описано в WO 00/28065.
Способы введения экзогенной ДНК в клетки млекопитающих включают трансфекцию с помощью фосфата кальция, электропорацию, трансфекцию с помощью DEAE-декстрана, трансфекцию с помощью липосом, вирусные векторы и способ трансфекции с помощью Lipofectamine 2000, описанный Life Technologies Ltd, Paisley, UK. Эти способы хорошо известны в данной области и описаны, к примеру, в Ausbel et al. (eds.), 1996, Current Protocols in Molecular Biology, John Wiley & Sons, New York, USA. Культивирование клеток млекопитающих проводят согласно общепринятым методам, например, как описано в Animal Cell Biotechnology, Methods and Protocols, Edited by Nigel Jenkins, 1999, Human Press Inc., Totowa, New Jersey, USA, и Harrison MA and Rae IF, General Technologies of Cell Culture, Cambridge University Press, 1997.
В способах получения по настоящему изобретению клетки культивируют в питательной среде, пригодной для получения полипептида способами, известными в этой области. Например, клетки можно культивировать в колбах со встряхиванием либо в лабораторных или промышленных ферментерах на большие или малые объемы (включая непрерывные, периодические, подпитываемые культуры или в твердых средах), в соответствующей среде и в условиях, способствующих экспрессии и/или выделению полипептида. Культивирование проводят в подходящей питательной среде, содержащей источники углерода и азота и неорганические соли, применяя методики, известные в этой области. Соответствующие среды доступны от коммерческих поставщиков или могут быть приготовлены согласно опубликованным составам (например, в каталогах American Type Culture Collection). Если полипептид секретируется в питательную среду, его можно выделить прямо из этой среды. Если полипептид не секретируется, его можно выделить из клеточных лизатов.
Полученный полипептид может быть выделен способами, известными в этой области. Так, полипептид может быть выделен из питательной среды общепринятыми методами, которые включают центрифугирование, фильтрование, экстракцию, распылительную сушку, упаривание или осаждение, но не ограничиваясь ими.
Полипептид может быть очищен при помощи ряда способов, известных в этой области, включая хроматографию (например, ионообменную хроматографию, аффинную, гидрофобную, хроматофокусирование и гель-фильтрацию), электрофоретические методы (например, препаративное изофокусирование), дифференциальную растворимость (например, высаживание сульфатом аммония), SDS-PAGE или экстракцию (см., к примеру, Protein Purification, J.-C.Janson and Lars Ryden, editors, VCH Publishers, New York, 1989), но не ограничиваясь ими.
Одноцепочечный FVII может быть очищен и активирован в двухцепочечный FVII с помощью ряда методов, описанных в литературе (Broze and Majerus, 1980, J.Biol. Chem. 255: 1242-47 и Hedner and Kisiel, 1983, J.Clin. Invest. 71: 1836-41). Другой метод, при помощи которого одноцепочечный FVII может быть очищен, - это включение ионов Zn в процессе очистки, как описано в US 5700914.
В предпочтительном воплощении полипептид очищают в виде одноцепочечного FVII, который затем ПЭГилируют. ПЭГилированный одноцепочечный полипептид FVII активируют с помощью иммобилизованного фермента (например, факторов IIa, IXa, Xa и XIIa) или путем автоактивации с помощью положительно заряженного ионообменного матрикса, либо другим подобным образом.
Выгодно сначала очистить FVII в одноцепочечной форме, затем ПЭГилировать (при желании) и в последнюю очередь активировать одним из методов, описанных выше, или путем автоактивации, как описано Pedersen et al., 1989, Biochemistry 28: 9331-36. Преимущество проведения ПЭГилирования перед активацией заключается в том, что предотвращается ПЭГилирование нового N-конца, образующегося при расщеплении по R152-I153. ПЭГилирование нового N-конца может сделать молекулу неактивной, так как для активации необходимо образование водородной связи между D242 и N-концевым I153.
Фармацевтическая композиция изобретения и ее применение
Следующий аспект настоящего изобретения касается композиции, в частности фармацевтической композиции, содержащей полипептид или конъюгат (включая неактивный конъюгат, как описано выше) изобретения и фармацевтически приемлемый носитель или наполнитель.
Конъюгат, полипептид или фармацевтическая композиция по изобретению может применяться в качестве медикамента.
Предпочтительно полипептид или (активный) конъюгат может применяться для производства препаратов для лечения или профилактики FVIIa/TF-связанных заболеваний или нарушений у млекопитающих. Например, полипептид или (активный) конъюгат может применяться для производства препаратов для лечения или профилактики заболеваний, при которых нужно увеличить свертываемость крови, например, для лечения больных с заболеваниями, приводящими к недостаточной свертываемости крови в ответ на повреждение кровеносных сосудов. В частности, полипептид или (активный) конъюгат может применяться для производства медикамента для лечения гемофилии, гемофилии с ингибиторами FVIII или FIX, тромбоцитопении, различных тромбоцитопатий типа тромбастении Гланцманна, нарушений выделения хранящихся в тромбоцитах веществ, болезни Виллебранда, заболеваний печени, или же в целом здоровых людей при сильных кровотечениях, например, вследствие травмы или тяжелой операции, тех, у кого образовались ингибиторы FVIIa, кровотечений при гемофилии и других нарушениях, обычно связанных с обширными повреждениями тканей.
Аналогично, неактивный конъюгат изобретения может применяться для производства лекарств для лечения или профилактики FVIIa/TF-связанных заболеваний или нарушений у млекопитающих. Например, неактивный конъюгат изобретения может применяться для производства лекарств для лечения или профилактики заболеваний, при которых желательно уменьшение свертываемости крови, например профилактики и лечения пациентов со статусом гиперкоагуляции - при сепсисе, тромбозе глубоких вен, при риске инфаркта миокарда или тромболитического инсульта, эмболии легких, при острых коронарных синдромах (инфаркт миокарда, неустойчивая стенокардия), при операциях на сердце и коронарных сосудах, для профилактики сердечных заболеваний и рестеноза у больных после ангиопластики, при заболеваниях переферических сосудов.
Неактивный конъюгат изобретения может также быть использован для производства медикаментов для лечения респираторных заболеваний, роста опухоли и метастазов.
В другом аспекте изобретения полипептиды, (активные) конъюгаты или фармацевтические композиции, содержащие (активные) конъюгаты изобретения, могут применяться для лечения млекопитающих, имеющих FVIIa/TF-связанные заболевания или нарушения (таких как одно или более заболеваний или нарушений, обозначенных выше), лечению, которое включает введение млекопитающему, нуждающемуся в нем, эффективного количества такого полипептида, конъюгата или композиции.
Аналогично, неактивный конъюгат или фармацевтическая композиция, содержащая этот неактивый конъюгат изобретения, могут быть использованы в способе лечения млекопитающего, имеющего FVIIa/TF-связанные заболевания или нарушения (такие, как одно или более заболевание или нарушение, обозначенные выше), способе, который включает введение млекопитающему, нуждающемуся в нем, эффективного количества таких неактивированных коньюгата или композиции.
Полипептиды или конъюгаты изобретения вводятся больным в терапевтически эффективной дозе, обычно такой, которая соответствует дозе, применяемой при лечении с помощью rFVII типа NovoSeven®, или в более высоких дозах.
"Терапевтически эффективная доза" означает дозу, достаточную для достижения желаемого действия в отношении заболевания, при котором она вводится. Точная доза зависит от обстоятельств, и специалист в этой области сможет ее определить, пользуясь известными методами. Обычно доза должна предотвращать либо облегчать тяжесть или распространение заболевания или симптома, подвергающегося лечению. Специалисты в этой области знают, что эффективное количество полипептида, конъюгата или композиции изобретения зависит, среди прочего, от заболевания, дозы, режима введения, от того, вводится ли полипептид, конъюгат или композиция сама по себе или вместе с другими терапевтическим средствами, от периода полужизни композиции в плазме и общего состояния больного. Предпочтительно полипептид, конъюгат или композиция изобретения вводится в эффективной дозе, в частности в дозе, достаточной для нормализации нарушения коагуляции.
Полипептид или конъюгат изобретения предпочтительно вводится в композиции, включающей фармацевтически приемлемый носитель или наполнитель. "Фармацевтически приемлемый" означает носитель или наполнитель, не вызывающий никаких нежелательных эффектов у пациентов, которым он вводится. Такие фармацевтически приемлемые носители и наполнители хорошо известны в этой области (см., к примеру, Remington's Pharmaceutical Sciences, 18th edition, A.R. Gennaro, Ed., Mack Publishing Company [1990]; Pharmaceutical Formulation Development of Peptides and Proteins, S. Frokjaer and L. Hovvgaard, Eds., Taylor & Francis [2000]; и Handbook of Pharmaceutical Excipients, 3rd edition, A. Kibbe, Ed., Pharmaceutical Press [2000]).
Из полипептида или конъюгата изобретения можно составить фармацевтические композиции при помощи хорошо известных методов. Походящие составы описаны E.W. Martin в Remington's Pharmaceutical Sciences (Mark Publ. Co., 16th Ed., 1980).
Полипептид или конъюгат изобретения может применяться "как есть" и/или в виде соли. Приемлемые соли включают соли щелочных или щелочно-земельных металлов - натриевые, калиевые, кальциевые и магниевые, а также соли цинка, но не ограничиваются ими. Эти соли или комплексы могут находиться в кристаллическом и/или аморфном состоянии.
Фармацевтическая композиция изобретения может вводиться сама по себе или в сочетании с другими терапевтическими средствами. Эти средства могут входить в состав одной и той же фармацевтической композиции или могут вводиться отдельно от полипептида или конъюгата изобретения, как одновременно, так и в соответствии с режимом другого лечения. Кроме того, полипептид, конъюгат или фармацевтическая композиция изобретения может применяться как адьювант к другим лекарствам.
"Больной" в применении к настоящему изобретению означает как человека, так и других млекопитающих. Поэтому эти способы применимы как к лечению человека, так и в ветеринарии. Фармацевтическая композиция полипептида или конъюгата изобретения может быть составлена в различных формах - жидкости, геля, в лиофилизованном виде или в виде прессованного твердого вещества. Предпочтительная форма зависит от того, какой симптом собираются лечить, и она ясна специалистам в этой области.
В частности, фармацевтическая композиция полипептида или конъюгата изобретения может быть составлена в лиофилизованном или устойчивом растворимом виде. Полипептид или конъюгат можно лиофилизировать с помощью ряда методов, известных в этой области. Полипептид или конъюгат можно перевести в устойчивую растворимую форму путем удаления или экранирования сайтов протеолитического расщепления. Преимущество получения препаратов в устойчивой растворимой форме заключается в более легком пользовании ими для больного и, в экстренных случаях, более быстром действии, что может стать решающим для спасения жизни. Предпочтительная форма зависит от того, какой симптом собираются лечить, и она ясна специалистам в этой области.
Введение композиций настоящего изобретения может осуществляться различным образом, включая пероральное, подкожное, внутривенное, внутримозговое, интраназальное, чрезкожное, интраперитонеальное, внутримышечное, внутрилегочное, вагинальное, ректальное, внутриглазное введение, или любым другим приемлемым способом. Композиции можно вводить непрерывно путем инфузии, хотя приемлемы и болюсные инъекции, пользуясь методами, хорошо известными в этой области, такими как вливание или имплантантация. В некоторых случаях композиции можно наносить непосредственно в виде раствора или аэрозоля.
Парентеральное введение
Предпочтительным примером фармацевтической композиции служит раствор для парентерального введения. Несмотря на то что во многих случаях растворы фармацевтических композиций находятся в жидкой форме, удобной для немедленного применения, такие парентеральные составы могут находиться и в замороженном или лиофилизованном виде. Замороженную композицию необходимо оттаять перед употреблением. Лиофилизация часто применяется для увеличения стабильности содержащегося в композиции активного соединения при хранении в широком диапазоне условий, поскольку, как известно специалистам в этой области, лиофилизованные препараты обычно более стабильны, чем аналогичные жидкие препараты. Такие лиофилизованные препараты реконституируют перед употреблением, добавляя один или несколько подходящих фармацевтически приемлемых растворителей, таких как стерильная вода для инъекций или стерильный физраствор.
Препараты для парентерального введения готовят для хранения в виде лиофилизованных композиций или водных растворов, смешивая их с одним или несколькими фармацевтически приемлемыми носителями, наполнителями или стабилизаторами, обычно применяющимися в этой области (все они именуются "наполнителями"), например буферными веществами, стабилизирующими веществами, консервантами, веществами, поддерживающими изотоничность, неионными детергентами, антиоксидантами и/или разнообразными другими добавками.
Буферные вещества способствуют поддержанию рН в диапазоне, близком к физиологическим условиям. Как правило, они присутствуют в концентрациях от 2 мМ до 50 мМ. К числу пригодных для применения в настоящем изобретении буферных веществ относятся и органические, и неорганические кислоты и их соли, например цитратные буферы (смесь однонатриевого цитрата и двунатриевого цитрата, смесь лимонной кислоты и тринатриевого цитрата, смесь лимонной кислоты и однонатриевого цитрата и т.д.), сукцинатные буферы (смесь янтарной кислоты и однонатриевого сукцината, смесь янтарной кислоты и гидроокиси натрия, смесь янтарной кислоты и двунатриевого сукцината и т.д.), тартратные буферы (смесь виннокаменной кислоты и тартрата натрия, смесь виннокаменной кислоты и тартрата калия, смесь виннокаменной кислоты и гидроокиси натрия и т.д.), фумаратные буферы (смесь фумаровой кислоты и однонатриевого фумарата, смесь фумаровой кислоты и двунатриевого фумарата, смесь однонатриевого фумарата и двунатриевого фумарата и т.д.), глюконатные буферы (смесь глюконовой кислоты и глюконата натрия, смесь глюконовой кислоты и гидроокиси натрия, смесь глюконовой кислоты и глюконата калия и т.д.), оксалатные буферы (смесь щавелевой кислоты и оксалата натрия, смесь щавелевой кислоты и гидроокиси натрия, смесь щавелевой кислоты и оксалата калия и т.д.), лактатные буферы (смесь молочной кислоты и лактата натрия, смесь молочной кислоты и гидроокиси натрия, смесь молочной кислоты и лактата калия и т.д.) и ацетатные буферы (смесь уксусной кислоты и ацетата натрия, смесь уксусной кислоты и гидроокси натрия и т.д.). Дополнительно к этому могут применяться фосфатные буферы, гистидиновые буферы и такие триметиламиновые соли, как трис.
Стабилизаторы относятся к обширной категории наполнителей с разнообразными функциями, от увеличения объема до солюбилизации лекарственного средства, либо предотвращения денатурации или прилипания к стенкам посуды. К типичным стабилизаторам относятся многоатомные сахароспирты (перечисленные выше); такие аминокислоты, как аргинин, лизин, глицин, глутамин, аспарагин, гистидин, аланин, орнитин, L-лейцин, 2-фенилаланин, глутаминовая кислота, треонин и т.д.; такие органические сахара или сахароспирты, как лактоза, трегалоза, стахиоза, маннитол, сорбитол, ксилитол, рибитол, миоинозитол, галактитол, глицерин и им подобные, включая циклитолы типа инозитола; полиэтиленгликоль; аминокислотные полимеры; такие серусодержащие восстановители, как мочевина, глутатион, липоевая кислота, тиогликолат натрия, тиоглицерин, α-монотиоглицерин и тиосульфат натрия; низкомолекулярные полипептиды (<10 аминокислотных остатков); такие белки, как сывороточный альбумин человека, бычий сывороточный альбумин, желатин или иммуноглобулины; гидрофильные полимеры типа поливинилпирролидона; такие моносахариды, как ксилоза, манноза, фруктоза и глюкоза; такие дисахариды, как лактоза, мальтоза и сахароза; такие трисахариды, как раффиноза, и такие полисахаридыы, как декстран. Как правило, стабилизаторы присутствуют в пределах от 0,1 до 10000 весовых частей относительно веса активного белка.
Консерванты добавляют для сдерживания роста микробов, и обычно их добавляют в количестве 0,2%-1% (вес./об.). К числу подходящих консервантов для применения в настоящем изобретении относятся фенол, бензиловый спирт, метакрезол, метилпарабен, пропилпарабен, октадецилдиметилбензиламмония хлорид, галогениды бензалкония (бензалкония хлорид, бромид или иодид), гексаметония хлорид, такие алкилпарабены, как метил- или пропилпарабен, катехол, резорцинол, циклогексанол и 3-пентанол.
Вещества, поддерживающие изотоничность, добавляются для обеспечения изотоничности жидких композиций. К ним относятся многоатомные сахароспирты, предпочтительно трехатомные и выше, такие как глицерин, эритритол, арабитол, ксилитол, сорбитол и маннитол. Многоатомные спирты могут присутствовать в количестве от 0,1% до 25% по весу, обычно от 1% до 5%, с учетом относительных количеств других ингредиентов.
Неионные поверхностно-активные вещества, или детергенты (также известные как "смачивающие вещества"), могут присутствовать для обеспечения солюбилизации лекарственного средства, а также для защиты лекарственного полипептида от агрегации, вызванной взбалтыванием, что также позволяет подвергать композицию поверхностному напряжению сдвига без денатурации полипептида. К числу подходящих неионных детергентов относятся полисорбаты (20, 80 и т.д.), полиоксамеры (184, 188 и т.д.), полиоли Pluronic®, моноэфиры полиоксиэтиленсорбитана (Tween®-20, Tween®-80 и т.д.).
К дополнительным разнообразным добавкам относятся вещества, увеличивающие объем, или наполнители (например, крахмал), хелатирующие вещества (например, ЭДТА), антиоксиданты (например, аскорбиновая кислота, метионин, витамин Е) и вспомогательные растворители.
Активный ингредиент также может быть заключен в микрокапсулы, полученные, к примеру, методами коацервации или межфазной полимеризации, например микрокапсулы из гидроксиметилцеллюлозы, желатина или полиметилметакрилата, в коллоидные системы доставки лекарств (например, липосомы, микросферы из альбумина, микроэмульсии, наночастицы и нанокапсулы) или в макроэмульсии. Такие методы изложены в Remington's Pharmaceutical Sciences, supra.
Композиции для парентерального введения in vivo должны быть стерильными. Это легко осуществляется, к примеру, фильтрованием через стерильные фильтровальные мембраны.
Препараты пролонгированного действия
Примеры препаратов пролонгированного действия включают полупроницаемые матрицы из твердых гидрофобных полимеров, содержащие полипептид или конъюгат, причем эти матрицы находятся в соответствующем виде типа пленки или микрокапсул. Примеры матриц пролонгированного действия включают полиэфиры, гидрогели (например, поли(2-гидроксиэтилметакрилат) или поливиниловый спирт), полилактиды, сополимеры L-глутаминовой кислоты и этил-L-глутамата, недеградируемый этилен-винилацетат, деградируемые сополимеры молочной кислоты и гликолевой кислоты, такие как технология ProLease® или Lupron Depot® (микросферы для инъекций, состоящие из сополимера молочной кислоты и гликолевой кислоты и лейпролида ацетата), и поли-D-(-)-3-гидроксимасляная кислота. В то время как полимеры, такие как этилен-винилацетат и молочная кислота-гликолевая кислота позволяют высвобождение молекул в течение длительного времени, до 100 дней и более, некоторые гидрогели высвобождают белки в течение более короткого времени. Когда инкапсулированные полипептиды находятся в организме долгое время, они могут денатурировать или агрегировать под влиянием влажности при 37°С, что ведет к потере биологической активности и вероятным изменениям иммуногенности. Можно придумать рациональные способы стабилизации в зависимости от действующих механизмов. Например, если окажется, что механизм аггрегации состоит в образовании межмолекулярных S-S-связей через тио-дисульфидный обмен, стабилизация может быть достигнута модификацией сульфгидрильных остатков, лиофилизацией из кислых растворов, контролированием степени влажности с помощью соответствующих добавок и разработкой специфических составов полимерного матрикса.
Далее изобретение раскрывается на следующих не ограничивающих примерах.
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
SEQ ID NO: 1 представляет белок hFVII (включая γ-карбоксилированные остатки).
SEQ ID NO: 2 представляет последовательность кДНК, кодирующей белок hFVII.
SEQ ID NO: 3 представляет белок hFVII (без γ-карбоксилированных остатков).
SEQ ID NO: 4 представляет экспрессионную кассету для экспрессии FVII в клетках млекопитающих.
SEQ ID NO: 5 представляет праймер CBProFpr174.
SEQ ID NO: 6 представляет праймер CBProFpr175.
SEQ ID NO: 7 представляет праймер CBProFpr216.
SEQ ID NO: 8 представляет праймер CBProFpr229.
SEQ ID NO: 9 представляет праймер CBProFpr221.
SEQ ID NO: 10 представляет праймер CBProFpr228.
SEQ ID NO: 11 представляет праймер CBProFpr226.
МАТЕРИАЛЫ И МЕТОДЫ
Методы определения аминокислот, подлежащих модификации
Площадь доступной поверхности (ПДП)
Для рассчета площади доступной поверхности (ПДП) индивидуальных атомов в структуре применяется компьютерная программа Access (В. Lee and F.M. Richards, J. Mol. Biol. 55: 379-400 (1971), версия 2 (© 1983 Yale University). В этом методе обычно применяется зонд размером в 1,4 Å, а площадь доступной поверхности (ПДП) определяется как площадь, образуемая центром зонда. Перед выполнением этих рассчетов из набора координат следует удалить все молекулы воды и все атомы водорода, а также другие атомы, не связанные непосредственно с белком.
Относительные значения ПДП боковых цепей
Относительные значения ПДП атомов боковой цепи расчитываются путем деления суммы ПДП атомов в боковой цепи на величину, представляющую ПДП атомов боковой цепи остатков этого типа в развернутом трипептиде Ala-x-Ala (см. Hubbard, Campbell & Thornton (1991) J.Mol. Biol. 220, 507-530). В этом примере атом СА рассматривается как часть боковой цепи остатков глицина, но не остальных остатков. В качестве стандарта значений 100% ПДП для боковой цепи применяется следующая таблица:
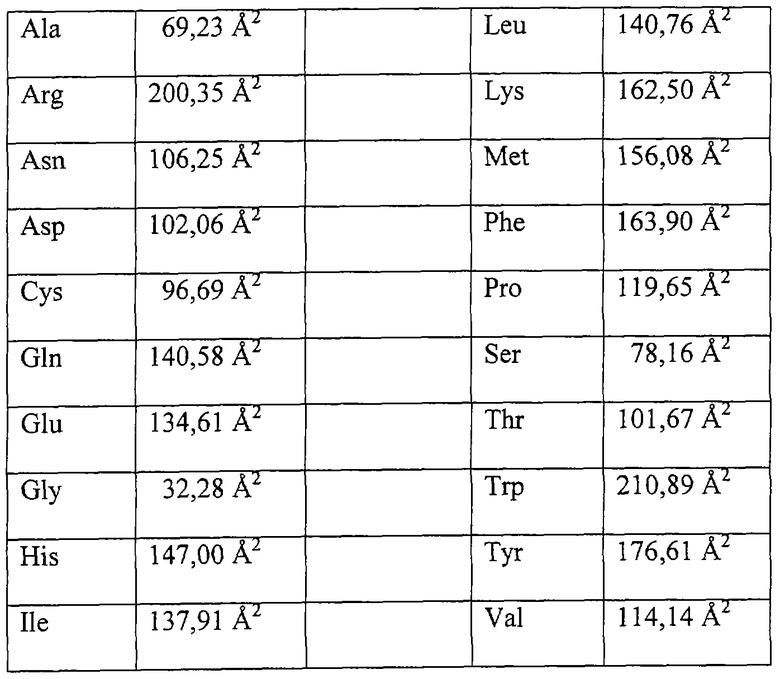
Остатки, не обнаруженные в структуре, определяются как доступные на 100%, так как считается, что они находятся в гибких участках. Все остатки γ-карбоксиглутаминовой кислоты в положениях 6, 7, 14, 16, 19, 20, 25, 26, 29 и 35 определяются как доступные на 100%.
Определение расстояний между атомами
Расстояния меду атомами наиболее просто определяются с помощью компьютерных программ молекулярной графики, например InsightII® v.98.0 фирмы MCI Inc.
Область каталитического сайта
Область каталитического сайта определяется как остатки, у которых, по меньшей мере, один атом находится в пределах 10 Å от любого атома в каталитической триаде (остатков H193, D242, S344).
Определение сайта связывания тканевого фактора
Сайт рецепторного связывания определяется как сайт, включающий все остатки, у которых площадь доступной поверхности изменяется при связывании с рецептором. Это определяется по данным не менее двух рассчетов ПДП, одного на изолированном лиганде в комплексе лиганд/рецептор и другого на полном комплексе лиганд/рецептор.
Методы тестирования свойств FVII и FVTIa
Измерение функционального периода полужизни in vivo
Измерение биологического периода полужизни in vivo можно проводить различными способами, как описано в литературе. Один из примеров метода измерения периода полужизни in vivo rFVIIa или его вариантов описан в документе FDA за номером 96-0597. Вкратце, измеряют коагуляционную активность FVII в плазме, полученной до и в течение 24 часов после введения конъюгата, полипептида или композиции. Измеряют медианное значение кажущегося объема распределения в стационарном состоянии и определяют медианное значение клиренса.
Определение пониженной чувствительности к протеолитической деградации
Готовят композицию, содержащую конъюгат (100-750 мкг/мл, предпочтительно 600 мкг/мл), 1,5 мг Са2+/мл (в виде хлористого кальция), маннитол (30 мг/мл), полисорбат 80 (0,1 мг/мл), хлористый натрий (3 мг/мл) и глицил-глициновый буфер (1,3 мг/мл, рН 5,5).
Готовят такую же композицию, содержащую rFVII дикого типа.
Затем измеряют исходную коагуляционную активность или, альтернативно, исходную амидолитическую активность, как описано в разделе "Методы измерения коагуляционной активности" или в разделе "Методы измерения низких уровней каталитической активности" или в разделе "Метод измерения каталитической активности", Композиции затем инкубируют при 37°С до тех пор, пока композиция, содержащая rFVII дикого типа, не потеряет, по меньшей мере, 25%, предпочтительно, по меньшей мере, 50% своей исходной коагуляционной активности или амидолитической активности.
Затем измеряют коагуляционную или амидолитическую активность композиции, содержащей конъюгат изобретения.
Снижение чувствительности к протеолитической деградации конъюгата изобретения по сравнению с rFVII дикого типа выражают в процентах.
Альтернативные методы измерения пониженной чувствительности к протеолитической деградации
Протеолитическую деградацию можно измерить методом, описанным в US 5580560, пример 5, где протеолиз представлен автопротеолизом.
Кроме того, снижение протеолиза можно тестировать в модели in vivo, используя радиоактивные образцы и сравнивая конъюгаты с протеолизом дикого типа путем отбора образцов крови и проверки их методами SDS-PAGE и авторадиографии.
Независимо от метода определения протеолитической деградации, "снижение протеолитической деградации" служит для обозначения измеримого снижения расщепления по сравнению с неконъюгированным FVIIa дикого типа при измерении сканированием окрашенных Кумасси гелей SDS-PAGE, HPLC, либо по измерению оставшейся каталитической активности по сравнению с диким типом при помощи хромогенных методов, описанных ниже.
Определение молекулярного веса rFVII и его конъюгатов
Молекулярный вес конъюгированного или неконъюгарованного rFVII или его конъюгатов определяют методами SDS-PAGE, гель-фильтрации, Western-гибридизации, лазерной десорбционной масс-спектрометрии с матричным управлением или равновесного центрифугирования, например, методом SDS-PAGE согласно Laemmli U.K., Nature, Vol 227 (1970), pp. 680-85.
Метод определения низких уровней каталитической активности
Амидолитическую активность в разбавленных образцах FVII/FVIIa и в культуральной жидкости можно определить с помощью набора COASET® FVII (Chromogenix, изделие №821900). Амидолитическую активность определяют в соответствии с инструкциями производителя. Вкратце, находящийся в избытке FX превращается в FXa под действием FVIIa при 37°С. Затем образовавшийся FXa гидролизует хромогенный субстрат S2765 (N-α-Cbo-D-Arg-Gly-Arg-pNA), что ведет к высвобождению хромогенной молекулы пара-нитроанилина (pNA), поглощающего свет при длине волны 450 нм. Реакцию останавливают добавлением уксусной кислоты. Количество FVII/FVIIa в образце определяют путем сравнения со стандартной кривой, полученной с применением FVIIa (в концентрации от 125 пг/мл до 1 нг/мл в буфере для измерения).
Метод измерения каталитической активности
Способность конъюгатов расщеплять небольшие пептидные субстраты можно измерить с помощью хромогенного субстрата S-2288 (D-Ile-Pro-Arg-р-нитроанилида). Рекомбинантный FVIIa разбавляют в 0,1 М трис, 0,1 М NaCI, 5 mM CaCl2, рН 8,3, содержащем 0,1% BSA. Реакцию запускают добавлением субстрата S-2288 до 1 мМ и измеряют поглощение при 405 нм после инкубации в течение 30 мин при 37°С.
Метод измерения коагуляционной активности
Активность FVIIa измеряют стандартным методом одностадийной коагуляции, в основном как описано в WO 92/15686. Вкратце, тестируемый образец разбавляют в 50 мМ трис (рН 7,5), 0,1% BSA, отбирают 100 мкл и инкубируют вместе со 100 мкл плазмы без FVII и 200 мкл тромбопластина С, содержащего 10 мМ Са++. Измеряют время коагуляции и сравнивают со стандартной кривой, полученной при серийном разведении смешанного образца нормальной цитратной плазмы человека.
Метод измерения антикоагуляционной активности
Антикоагуляционную активность неактивного конъюгата FVII или FVIIa можно измерить методом одностадийной коагуляции, описанным выше (Метод измерения коагуляционной активности), в котором неактивный конъюгат конкурирует с FVII дикого типа за ограниченное количество релипидированного тканевого фактора. Определение проводят в основном как описано в WO 92/15686, пример III, включенном в виде ссылки. Регистрируют способность неактивного конъюгата пролонгировать время коагуляции FVII дикого типа, что и принимают как меру антикоагуляционной активности.
ПРИМЕРЫ
Пример 1
В этом примере использовали структуру hFVIIa в комплексе с растворимым тканевым фактором согласно Banner et al., J.Mol. Biol., 1996; 285: 2089. Следует отметить, что нумерация остатков в этой ссылке не отвечает последовательности. Мы использовали последовательную нумерацию согласно SEQ ID NO: 1. Все остатки γ-карбоксиглутаминовой кислоты в положениях 6, 7, 14, 16, 19, 20, 25, 26, 29 и 35 обозначены как GLU (трехбуквенное сокращение) или Е (однобуквенное сокращение). Остатки 143-152 не представлены в структуре.
Экспозиция на поверхности
Проведение расчетов относительных значений ПДП свободных фрагментов FVII в сочетании с определением доступностей необычных и/или отсутствующих остатков, описанных в методах, показало, что у следующих остатков более 25% боковой цепи экспонировано на поверхности: A1, N2, A3, F4, L5, Е6, Е7, L8, R9, Р10, S12, L13, Е14, Е16, К18, Е19, Е20, Q21, S23, F24, Е25, Е26, R28, Е29, F31, К32, D33, А34, Е35, R36, К38, L39, W41, I42, S43, S45, G47, D48, Q49, А51, S52, S53, Q56, G58, S60, К62, D63, Q64, L65, Q66, S67, I69, F71, L73, Р74, А75, Е77, G78, R79, Е82, Т83, Н84, К85, D86, D87, Q88, L89, I90, V92, N93, Е94, G97, Е99, S103, D104, Н105, Т106, G107, Т108, К109, S111, R113, Е116, G117, S119, L120, L121, А122, D123, G124, V125, S126, Т128, Р129, Т130, V131, Е132, I140, L141, Е142, К143, R144, N145, А146, S147, К149, Р149, Q150, G151, R152, G155, К157, V158, Р160, К161, Е163, L171, N173, G174, А175, N184, Т185, I186, Н193, К197, К199, N200, R202, N203, I205, S214, Е215, Н216, D217, G218, D219, S222, R224, S232, Т233, V235, Р236, G237, Т238, Т239, N240, Н249, Q250, Р251, V253, Т255, D256, Е265, R266, Т267, Е270, R271, F275, V276, R277, Е278, L280, L287, L288, D289, R290, G291, А292, Т293, L295, Е296, N301, М306, Т307, Q308, D309, L311, Q312, Q313, R315, К316, V317, G318, D319, S320, Р321, N322, Т324, Е325, Y326, Y332, S333, D334, S336, К337, К341, G342, Н351, R353, G354, Q366, G367, Т370, V371, G372, R379, Е385, Q388, К389, R392, S393, Е394, Р395, R396, Р397, G398, V399, L400, L401, R402, Р404 и Р406.
У следующих остатков более 50% боковой цепи экспонировано на поверхности: А1, A3, F4, L5, Е6, Е7, L8, R9, Р10, Е14, Е16, К18, Е19, Е20, Q21, S23, Е25, Е26, Е29, К32, А34, Е35, R36, К38, L39, I42, S43, G47, D48, А51, S52, S53, Q56, G58, S60, К62, L65, Q66, S67, I69, F71, L73, Р74, А75, Е77, G78, R79, Е82, Н84, К85, D86, D87, Q88, L89, I90, V92, N93, Е94, G97, Т106, G107, Т108, К109, S111, E116, S119, L121, A122, D123, G124, V131, E132, L141, E142, K143, R144, N145, A146, S147, K148, P149, Q150, G151, R152, G155, K157, P160, N173, G174, A175, K197, K199, N200, R202, S214, E215, H216, G218, R224, V235, P236, G237, T238, H249, Q250, V253, D256, T267, F275, R277, F278, L288, D289, R290, G291, A292, T293, L295, N301, M306, Q308, D309, L311, Q312, Q313, R315, К316, G318, D319, N322, Е325, D334, К341, G354, G367, V371, Е385, К389, R392, Е394, R396, Р397, G398, R402, Р404 и Р406.
Сайт связывания тканевого фактора
При проведении расчетов относительных значений ПДП следующие остатки FVII человека проявляли изменения значений ПДП в комплексе. Эти остатки по определению составляют сайт рецепторного связывания: L13, К18, F31, Е35, R36, L39, F40, I42, S43, S60, К62, D63, Q64, L65, I69, С70, F71, С72, L73, Р74, F76, Е77, G78, R79, Е82, К85, Q88, I90, V92, N93, Е94, R271, А274, F275, V276, R277, F278, R304, L305, М306, Т307, Q308, D309, Q312, Q313, Е325 и R379.
Область активного сайта
Участок активного сайта определяется как любой остаток, у которого, по меньшей мере, один атом находится в пределах 10 Å от любого атома в каталитической триаде (остатков Н193, D242, S344): I153, Q167, V168, L169, L170, L171, Q176, L177, С178, G179, G180, Т181, V188, V189, S190, А191, А192, Н193, С194, F195, D196, К197, I198, W201, V228, I229, I230, Р231, S232, Т233, Y234, V235, Р236, G237, Т238, Т239, N240, Н241, D242, I243, А244, L245, L246, V281, S282, G283, W284, G285, G286, Т293, Т324, Е325, Y326, М327, F328, D338, S339, С340, К341, G342, D343, S344, G345, G346, Р347, Н348, L358, Т359, G360, I361, V362, S363, W364, G365, G368, V376, Y377, Т378, R379, V380, Q382, Y383, W386, L387, L400 и F405.
Гребень связывающего углубления активного сайта
Область гребня связывающего углубления активного сайта была определена путем визуального изучения структуры FVIIa 1FAK.pdb следующим образом: N173, А175, К199, N200, N203, D289, R290, G291, А292, Р321 и Т370.
Пример 2
Конструирование экспрессионной кассеты для экспрессии коагуляционного фактора VII человека в клетках млекопитающих
Чтобы обеспечить высокий уровень экспрессии в клетках млекопитающих, была синтезирована последовательность ДНК, приведенная в SEQ ID NO: 2, которая заключает укороченную форму кДНК, кодирующей коагуляционный фактор VII человека вместе с его собственным коротким сигнальным пептидом (Hagen et al., 1986, PNAS 83: 2412). Во-первых, было модифицировано окружение стартового кодона ATG согласно консенсусной последовательности Козака (Kozak M., J.Mol. Biol. 1987 Aug 20; 196(4): 947-50) таким образом, чтобы обеспечить идеальное соответствие консенсусной последовательности выше стартового кодона ATG. Во-вторых, была модифицирована открытая рамка считывания кДНК природного коагуляционного фактора человека так, чтобы сдвинуть употребление кодонов в сторону тех кодонов, которые чаще используются в генах человека с высоким уровнем экспрессии. Далее, в конец открытой рамки считывания были вставлены два стоп-кодона трансляции, чтобы обеспечить остановку трансляции. Полностью синтетический и оптимизированный для экспрессии ген FVII человека был собран из 70-мерных олигонуклеотидов, а затем амплифицирован с помощью конечных праймеров, вводя при этом сайты BamHI и HindIII в 5'- и 3'-концы соответственно при помощи стандартных методов ПЦР, что дало следующую последовательность (SEQ ID NO: 4):

Вектор для клонирования образовавшегося продукта ПЦР, заключающего экспрессионную кассету для природного коагуляционного фактора VII человека, был получен клонированием интрона из pCI-Neo (Promega). Синтезированный интрон из pCI-Neo амплифицировали при стандартных условиях ПЦР, как описано выше, с помощью праймеров:
CBProFpr174: 5'-AGCTGGCTAGCCACTGGGCAGGTAAGTATCA-3'
CBProFpr175: 5'-TGGCGGGATCCTTAAGAGCTGTAATTGAACT-3'
получая ПЦР-фрагмент в 332 bp. Этот фрагмент разрезали с помощью Nhel и BamHI и клонировали в pCDNA3.1/HygR (фирмы InVitrogen), получая плазмиду PF#34.
Экспрессионную кассету для природного коагуляционного фактора VII человека клонировали между сайтами BamHI и HindIII в PF#34, получая плазмиду PF#226.
Пример 3
Конструирование экспрессионных кассет, кодирующих различные формы коагуляционного фактора VII человека, содержащие дополнительный сайт гликозилирования in vivo
Для получения конструкций с вариантами открытой рамки считывания коагуляционного фактора человека с заменами кодонов применяли метод ПЦР с наращиванием свисающей последовательности (sequence overhang extension, или SOE-ПЦР). В методе SOE-ПЦР сначала по отдельности амплифицировали N-концевую часть и С-концевую часть открытой рамки считывания FVII в индивидуальных реакциях первичного ПЦР.
Например, для изменения кодонов для R315 и V317 на кодоны для N315 и Т317 использовали следующие пары праймеров для первичных реакций ПЦР:
CBProFpr216: 5'-CTTAAGGATCCCGCCACCATGGTCAGCCAG-3',
CBProFpr229. 5 '-GGAGTCCCCGGTTTTGTTGGACTGCTGC-3';
и
CBProFpr221: 5'-ACTTAAGCTTTTATCAAGGGA-3',
CBProFpr228: 5'-GCAGCAGTCCAACAAAACCGGGGACTCC-3',
После этого продукты первичного ПЦР объединяли и добавляли терминальные праймеры (CBPrFpr216 и CBPrFpr221), получая вторичный продукт полной длины, кодирующий требуемый вариант FVII R315N+V317T. Вторичный продукт ПЦР затем обрабатывали BamHI и HindIII и клонировали в вектор PF#34 между сайтами BamHI и HindIII, получая PF#249.
Кроме того, в случаях, когда вводимые мутации находились достаточно близко к уникальному сайту расщепления эндонуклеазы в экспрессионной плазмиде, варианты генов конструировали, применяя метод, включающий одну стадию ПЦР с последующим клонированием. Например, замену K143N+N145T вводили с помощью ПЦР-праймеров:
CBProFpr226: 5'-CATTCTAGAAAACCGGACCGCTAGCAAACC-3',
CBProFpr221: 5'-ACTTAAGCTTTTATCAAGGGA-3',
в одной единственной реакции ПЦР.
После этого продукт ПЦР клонировали по рестрикционным сайтам эндонуклеаз XbaI и HindIII.
При помощи такого подхода были получены следующие гликозилированные конъюгаты и протестированы на амидолитическую активность, как описано в разделе "Метод измерения низких уровней каталитической активности". Кроме того, некоторые конъюгаты подвергали одностадийной оценке коагуляционной активности, как описано в разделе "Метод измерения коагуляционной активности". Полученные результаты представлены в нижеследующей таблице.
Пример 4
Улучшение эффективности сайта гликозилирования введением другого проксимального (N-концевого) сайта гликозилирования
Для того чтобы предотвратить автолиз FVII дикого типа человека, вводили сайт гликозилирования в положение 315, произведя замены R315N и V317T, как описано выше, получая PF#249.
После трансфекции клеток СНО К1 с помощью Lipofectamine 2000 наблюдались низкие уровни кратковременной экспрессии. Определение амидолитической активности с помощью набора COASET® FVII в супернатанте после 24 часов экспрессии показало, что этот вариант активен. После селекции в присутствии 400 мкг/мл гигромицина В получили пул стабильных клонов. Они экспрессировали вариант R315N+V317T на уровне примерно 0,2 мкг/мл, что позволило провести Western-гибридизацию для определения степени использования введенного сайта гликозилирования. При анализе 24-часового супернатанта из пула стабильных клонов методом Western-гибридизации обнаружилось, что введенный в положение 315 сайт гликозилирования используется лишь частично - приблизительно половина полностью процессированного секретируемого белка была гликозилирована. Однако, когда природный сайт гликозилирования в положении 145 перемещали в положение 143 путем замены K143N+N145T, то введенный в положение 315 сайт гликозилирования становился полностью гликозилированным, судя по данным Western-гибридизации.
Пример 5
Экспрессия FVII в клетках НЕК
Клеточную линию НЕК 293 (АТСС # CRL-1573) инокулировали на уровне 20% в колбы Т-25, заполненные средой DMEM с высоким содержанием глюкозы, 10% инактивированной нагреванием телячей сыворотки (Gibco/BRL, кат. №10091) и 5 мкг/мл филохинона, и выращивали до полной конфлюэнтности. Образовавшие монослой клетки трансфецировали, используя 1, 2, 5, 10 и 20 мкг плазмиды р226, описанной выше, с помощью трансфецирующего агента Lipofectamine 2000 (Life Technologies) согласно инструкциям производителя. Через 24 часа после трансфекции отбирали образец среды. Концентрация FVII в опытах по 24-часовой экспрессии в среднем составляла около 0,15 мкг/мл.
После этого к клеткам добавляли селекционную среду, содержащую 100 мкг/мл гигромицина В. После 3 недель селекции, с обновлением среды через каждые 3 или 4 дня, устойчивые к гигромицину В клетки достигали конфлюэнтности в колбах, трансфецированных 1 и 2 мкг плазмидной ДНК. Клетки из каждой из пяти чашек собирали и объединяли. Полученный пул стабильных трансфектантов, экспрессирующих коагуляционный фактор FVII человека, замораживали в жидком азоте по стандартной методике.
Пример 6
Получение клеток НЕК293, стабильно экспрессирующих FVII
Оттаивали пробирку, содержащую пул трансфектантов НЕК293 с плазмидой PF#226, инокулировали клетки в колбу на 75 см2, содержащую 15 мл среды DMEM с высоким содержанием глюкозы, 10% телячей сыворотки, филлохиноном (5 мкг/мл), 100 Ед/л пенициллина и 100 мкг/л стрептомицина, которую использовали во всех последующих экспериментах, и выращивали в течение 24 часов. Клетки собирали, разбавляли и высевали в микропланшеты на 96 лунок при плотности 1/2 клетки/лунку. Через 12 дней в лунках были колонии примерно в 20-100 клеток, и лунки, содержащие только одну колонию, помечали. Через дальнейшие два дня добавляли еще 100 мкл среды в каждую лунку. Через два дня после этого меняли среду во всех лунках, содержащих только одну колонию. Первые колонии переносили в колбы на 25 см2, выращивали 3 дня и, в зависимости от уровня конфлюэнтности, переносили колонии в колбы на 25 см2 и выращивали еще 11 дней. При достижении конфлюэнтности среду в колбах Т-25 меняли и давали клонам секретировать FVII в ростовую среду в течение 24 часов, после чего отбирали супернатанты и анализировали на наличие фактора VII по амидолитической активности с помощью набора COASET FVII. Был обнаружен один клон, С 18, который экспрессировал 29 мкг/мл FVII.
Пример 7
Экспрессия гликозилированных вариантов FVII, не обладающих амидолитической активностью и способных ингибировать функцию FVIIa
Экспрессионные плазмиды для экспрессии мутантов по гребню активного сайта R290N+A292N и G291N были в основном сконструированы, как описано в примере 3.
Используя метод оценки амидолитической активности COASET® FVII (см. выше), определяли способность двух гликозилированных вариантов FVII, R290N+A292T и G291N, ингибировать активность rFVIIa. Плазмиду PF#250, кодирующую R290N+A292T, и плазмиду PF#294, кодирующую G292N, трансфецировали в выращенные в присутствии сыворотки клетки НЕК293, близкие к конфлюэнтности, с помощью Lipofectamine 2000. Трансфецированные клетки инкубировали при 37°С в 5% CO2 в течение трех часов после трансфекции, после чего меняли среду на бессывороточную (DMEM, ITS-A, ExCyte, филлохинон, пенициллин/стрептомицин). Через 40 часов после трансфекции собирали культуральную жидкость и осветляли для анализа центрифугированием.
Составляли стандартную кривую по rFVIIa: 0,0125 нг, 0,025 нг, 0,05 нг, 0,075 нг и 0,1 нг. В аликвоты по 50 мкл неразбавленной, разбавленной в 2 раза, 5 раз, 10 и 50 раз культуральной жидкости от каждого из гликозилированных вариантов R290N+A292T и G291N или культуральной жидкости от холостой трансфекции добавляли по 0,025 нг rFVIIa. При измерении методом COASET FVII 0,025 нг FVIIa соответствовало величине поглощения OD405=0,35 (первая проба) и OD405=0,26 (вторая проба).
Как видно из вышеприведенных данных, гликозилированные конъюгаты G291N и R290N+A292T ингибируют функцию rFVIIa.
Пример 8
Очистка и последующая активация FVII
Очистка фактора VII дикого типа и его конъюгатов проводилась при 4°С. Супернатант от клеток, экспрессирующих конъюгат (или FVII дикого типа), стерилизовали фильтрованием (0,22 мкм) и разбавляли в 2 раза холодной водой milliQ. Добавляли ЭДТА до 5 мМ, доводили рН до 8,6 и сопротивление было меньше 10 mS/см. Образец наносили на колонку, заполненную Q-сефарозой Fast Flow (Pharmacia) и уравновешенную при 4°С в 10 мМ трис, рН 8,6. После нанесения образца колонку промывали 10 мМ трис (рН 8,6), 150 мМ NaCl до тех пор, пока поглощение при 280 нм не достигало исходных значений. Затем колонку уравновешивали в 10 мМ трис (рН 8,6), 100 мМ NaCl. Связавшийся конъюгат (или FVII дикого типа) элюировали 10 мМ трис (рН 8,6), 100 мМ NaCl, 5 мМ CaCl2. Обогащенные конъюгатом (или FVII дикого типа) фракции объединяли и концентрировали с помощью диализа или концентрационного набора Vivaspin (Vivascience).
Автоактивацию конъюгата (или FVII дикого типа) осуществляли путем концентрирования и инкубации элюированного белка в 10 мМ трис (рН 7,8-8,6), 100 мМ NaCl, 5 мМ CaCl2.
Альтернативно, конъюгат (или FVII дикого типа) активировали при 37°С с помощью фактора Ха, пришитого к CNBr-активированной сефарозе в 10 мМ трис (рН 7,4-8,0), 100 мМ NaCl, 5 мМ CaCl2.
Конъюгат (или FVII дикого типа) заменой буфера переводили в раствор, содержащий 10 мМ CaCl2, 50 мМ NaCl, 3% маннитол, 0,05% твин80, забуференный при рН 5,6 и стерилизованный фильтрованием перед хранением при -80°С.
Пример 9
N-концевое ПЭГилирование FVII
Фактор VII конъюгировали с метоксиполиэтиленгликолем (mPEG), имеющим молекулярный вес около 5 кД, с помощью M-PEG-CHO (M-ALD-5000 фирмы Shearwater) в буфере, содержащем 10 мМ цитрата натрия, 20 мМ CaCl2, 100 мМ NaCl, рН 5,5. M-PEG-CHO был в 50-100-кратном молярном избытке, а концентрация белка составляла 0,2-0,5 мг/мл. Реакцию проводили порциями по 300-1500 мкл при комнатной температуре в течение 1 часа с перемешиванием, затем добавляли NaBH3CN в 500-1000-кратном избытке и продолжали инкубацию в течение ночи с перемешиванием при комнатной температуре.
ПЭГилированный FVII заменой буфера переводили в буфер А (10 мМ трис, рН 7,6) и наносили при 4°С на колонку, заполненную moho-Q (Pharmacia), уравновешенную буфером А. Связавшийся белок элюировали в градиенте 0-100% В (10 мМ трис, рН 7,6, 500 мМ NaCl), используя 40 колоночных объемов.
Пример 10
Фармакокинетические исследования на крысах
FVII дикого типа и конъюгаты изобретения переводили в глицил-глициновый буфер (1,3 мг/мл, рН 5,5), содержащий 1,5 мг/мл CaCl2, 30 мг/мл маннитола, 0,1 мг/мл полисорбата 80 и 3 мг/мл NaCl. Для определения функционального периода полужизни in vivo каждый препарат вводили крысам Sprague-Dawley внутривенно в виде одной болюсной инъекции. Инъекции проводили медленно в течение примерно 10 с, чтобы уменьшить возможный риск сердечной недостаточности вследствие высокой концентрации Са2+ Отбирали образцы крови у каждого из девяти анестезированных животных через соответствующие интервалы, например, 1 минуту, 15 минут, 30 минут, 45 минут и 1 час после инъекции. Образцы крови собирали в пробирки на 1 мл, содержащие 50 мкл цитрат-фосфат-декстрозного раствора с аденином (Sigma, #C4431), для предотвращения свертывания крови. Тотчас после отбора образцы помещали при 0°С до центрифугирования и последующего сбора супернатантов плазмы в цитрате для анализа. Образцы анализировали методом одностадийного измерения коагуляционной активности, как описано в разделе "Методы измерения коагуляционной активности", после чего рассчитывали период полужизни.
| название | год | авторы | номер документа |
|---|---|---|---|
| ВАРИАНТЫ ДОМЕНА GLA ФАКТОРА VII ИЛИ VIIa | 2004 |
|
RU2373282C2 |
| КОНЪЮГАТЫ G-CSF | 2001 |
|
RU2290411C2 |
| ВАРИАНТЫ ПОЛИПЕПТИДА ГАММА-ИНТЕРФЕРОНА | 2002 |
|
RU2296130C2 |
| КОНЪЮГАТЫ γ-ИНТЕРФЕРОНА | 2000 |
|
RU2268749C2 |
| ПРОИЗВОДНЫЕ ФАКТОРОВ СВЕРТЫВАНИЯ КРОВИ VII И VIIa, КОНЪЮГАТЫ И КОМПЛЕКСЫ, СОДЕРЖАЩИЕ ИХ, И ИХ ПРИМЕНЕНИЕ | 2012 |
|
RU2620072C2 |
| ХИМЕРНЫЕ МОЛЕКУЛЫ ФАКТОРА VII | 2010 |
|
RU2563231C2 |
| ПОЛИПЕПТИДЫ НА ОСНОВЕ МОДИФИЦИРОВАННОГО ФАКТОРА VII И ИХ ПРИМЕНЕНИЕ | 2008 |
|
RU2571931C2 |
| КОНЪЮГАТ ПОЛИПЕПТИДА ФАКТОРА VII, СПОСОБ ЕГО ПОЛУЧЕНИЯ, ЕГО ПРИМЕНЕНИЕ И СОДЕРЖАЩАЯ ЕГО ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2003 |
|
RU2362807C2 |
| МОДИФИЦИРОВАННЫЙ КОАГУЛИРУЮЩИЙ ФАКТОР VIIa С ПРОДЛЕННЫМ ВРЕМЕНЕМ ПОЛУЖИЗНИ | 2007 |
|
RU2466141C2 |
| КОНЪЮГАТ АНТИТЕЛА И ЛЕКАРСТВЕННОГО СРЕДСТВА, КОМПОЗИЦИИ НА ЕГО ОСНОВЕ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2015 |
|
RU2728235C2 |
Настоящее изобретение касается новых конъюгатов полипептида фактора VII (FVII) или фактора VIIa (FVIIa), их получения и применения в медицине, в частности, при лечении ряда заболеваний, связанных со свертыванием крови. Предложен конъюгат, содержащий, по меньшей мере, одну молекулу сахарида, ковалентно присоединенную к введенному сайту N-гликозилирования in vivo, в котором полипептидная часть конъюгата имеет аминокислотную последовательность, которая отличается от приведенной в SEQ ID NO:1 последовательности FVII или FVIIa дикого типа по 1-15 аминокислотным остаткам. Конъюгаты настоящего изобретения обладают как минимум одним из улучшенных свойств по сравнению с коммерчески доступным rFVIIa, включая увеличение функционального периода полужизни in vivo, и/или повышение периода полужизни в плазме, и/или уменьшение чувствительности к протеолитической деградации. 15 з.п. ф-лы, 5 табл.
Приоритет по пунктам:
| СПОСОБ ПОЛУЧЕНИЯ БЕЛКА, ОБЛАДАЮЩЕГО ОПОСРЕДОВАННОЙ ФАКТОРОМ VII АКТИВНОСТЬЮ В СВЕРТЫВАНИИ КРОВИ | 1986 |
|
RU2122583C1 |
| WO 9835026 A1, 13.08.1998 | |||
| US 4904584 A, 27.02.1990 | |||
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ПИРОНА-2 | 0 |
|
SU370205A1 |
| US 5580560 A, 03.12.1996. | |||
Авторы
Даты
2006-06-20—Публикация
2001-02-12—Подача