Изобретение относится к химии азотсодержащих гетероциклов и фосфороорганических соединений, а именно к соли бис(оксиметил)-фосфиновой кислоты с гидразидом изоникотиновой кислоты формулы I (в дальнейшем обозначаемой «тубофен»), которая может быть использована в качестве противотуберкулезного средства в ветеринарной и медицинской практике для профилактики и лечения туберкулеза. Заявляемое соединение, его свойства и способ получения в литературе не описаны.
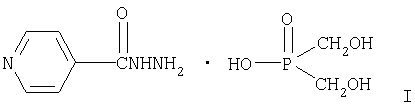
Существует большое количество противотуберкулезных препаратов, и их современная классификация основана на эффективности их влияния на возбудителя. В классификацию входят наиболее эффективные препараты: химиопрепарат изониазид (ГИНК) и антибиотик рифампицин; препараты средней эффективности: антибиотики стрепомицин, канамицин, флоримицин (виомицин), циклосерин, химиопрепараты этамбутол, этионамид, протионамид, пиразинамид (тизамид) и препараты умеренной эффективности: ПАСК (n-аминосалициловая кислота), тибон (тиоцетазон).
Несмотря на наличие большого количества противотуберкулезных средств изониазид, представляющий собой гидразид изоникотиновой кислоты, является лучшим из существующих препаратов и входит в состав практически всех схем профилактики и лечения туберкулеза животных и людей (Визель А.А. Лечение туберкулеза органов дыхания. Казань, ГПВЭО «Саламат», 1998, 119 с.), (Машковский М.Д. Лекарственные средства. Т.2. Харьков, 1998, с.331-333), (Смолянинов Ю.И., Кощеев Н.Н. Специфическая профилактика туберкулеза у молодняка крупного рогатого скота.// Сб. науч. тр./ ВНИИБТЖ. - Омск, 2001: Инфекционная патология животных. С. 168-170).
Известны структурные аналоги заявляемого соединения. Оротат гидразида изоникотиновой кислоты проявляет антимикобактериальную и иммунотропную активность (Пат. RU 2044728, опубл. 27.09.1995). Меламиновая соль бис(оксиметил)фосфиновой кислоты является регулятором роста и развития растений (Пат. RU 2158735, опубл. 10.11.2000). Однако изониазид является ближайшим структурным аналогом предлагаемого изобретения, обладающего тем же видом активности.
Известно, что изониазид, используемый для профилактики и лечения туберкулеза, не свободен от побочного действия и как фармакологическое средство обладает определенной биологической активностью, способной вызывать изменение показателей обмена веществ и структурно-функционального состояния органов и систем, а при передозировке сопровождаться отравлением и летальным исходом (Саджая Л.А. Биохимическое обоснование путей снижения гепатотоксичности изониазида на основе сочетания с полисахаридами: Автореф. дис.канд. фарм. наук/ Пятигорская гос.фарм. академия. Пятигорск, 1999, 21 с.). Важно отметить, что токсичность изониазида связана в основном с его метаболитами (Скакун Н.П., Шманько В.В. Сущность гепатотоксического действия изониазида.// Врачебное дело, 1984, №1, с.49-52), поэтому синтез аналога изониазида, возможно, с другим типом метаболизма, приводящим к снижению токсичности, вызывает особый интерес.
Цель изобретения - новое, более эффективное соединение, обладающее противотуберкулезным действием, не оказывающее гепатотоксического действия, способствующее быстрому оздоровлению, расширяющее арсенал известных противотуберкулезных средств, и способ его получения.
Технический результат предлагаемого изобретения заключается в снижении токсичности противотуберкулезного средства при сохранении высокой терапевтической эффективности и отсутствии местной и общей реактогенности средства при лечебной дозе.
Поставленная техническая цель достигается предлагаемым изобретением, а именно солью бис(оксиметил)фосфиновой кислоты с гидразидом изоникотиновой кислоты формулы I (тубофен) и способом ее получения. Сущность предлагаемого способа получения тубофена заключается во взаимодействии бис(оксиметил)фосфиновой кислоты и гидразида изоникотиновой кислоты в метаноле при перемешивании с последующим нагреванием до 60°С, выдерживанием при комнатной температуре в течение 12-15 ч и отделением выпавшего осадка обычными приемами. Для лучшего понимания изобретения приводим примеры получения заявляемой соли и результаты исследования ее противотуберкулезных свойств.
Пример конкретного выполнения.
К взвеси 7,61 г (0,055 моль) гидразида изоникотиновой кислоты в 40 мл метанола при комнатной температуре прикапывают раствор 7,75 г (0,061 моль) бис(оксиметил)фосфиновой кислоты в 40 мл метанола. Реакционную массу перемешивают, достигая полной прозрачности раствора, затем нагревают до 60°С и оставляют на 12-15 ч. Отфильтровывают выпавший за это время продукт и высушивают. Получают 8,8 г (60,2%) продукта - соли бис(оксиметил)фосфиновой кислоты с гидразидом изоникотиновой кислоты в виде белого кристаллического вещества. Т.пл. 109-110°С. ЯМР 31P (36,48 МГц, Д2O): δP 37.20 м.д. Найдено, %: С 36.40; Н 5.28; N 15.64; Р 10.88. C8H14N3PO5. Вычислено, %: С 36.50; Н 5.32; N 15.97; Р 11.79.
Сравнительное исследование эффективности тубофена - соли бис(оксиметил)фосфиновой кислоты с гидразидом изоникотиновой кислоты и изониазида при туберкулезе проводилось в течение двух лет на 180 животных (24 белых мышах, 76 белых беспородных крысах и 80 морских свинках).
Бактериостатическая активность тубофена и изониазида была изучена в опытах in vitro на 2 видах микобактерий туберкулеза, в концентрации препаратов от 10 до 0,018 мкг/мл, используя метод последовательных серийных разведений (Першин Г.Н. Методы экспериментальной химиотерапии. М., «Медицина», 1971, с.171-192).
За титр активности изучаемого вещества принимали то его наибольшее разведение, или ту наименьшую концентрацию, которые полностью подавляли рост микобактерий туберкулеза. Основными параметрами для оценки действия тубофена и изониазида служила способность микобактерий к росту и размножению. Оценка ростовых свойств микобактерий определялась по скорости и количеству выросших колоний. Оценка числа колоний определялась в крестах по схеме, предложенной Г.Н.Першиным: обильный рост (+++); глубинный рост штаммов менее обилен, осадок меньших размеров, комочки культуры меньше, чем в контроле (++); глубинный рост в виде слабозаметного осадка, зерна мелкие в небольшом количестве (+); полный бактерицидный эффект, засеянная культура не дает роста (-). Результаты исследования бактериостатической активности противотуберкулезных препаратов отражены в таблице 1.
Из данных таблицы 1 видно, что бактериостатическая активность тубофена высока и не уступает таковой изониазида. Тубофен в концентрации 0,075 мкг/мл оказывал полное бактериостатическое подавляющее действие на штамм 14 M.bovis и штамм H37Rv M. tuberculosis как на чистой питательной среде, так и с добавлением в нее 10% раствора лошадиной сыворотки. Концентрации тубофена 0,037 и 0,018 мкг/мл с теми же штаммами, на среде Сотона и среде Сотона, содержащей 10% раствор лошадиной сыворотки, оказывали лишь частичное подавление размножения микобактерий туберкулеза в виде слабо заметного осадка с мелкими зернами.
В свою очередь изониазид оказывал полное бактериостатическое действие на штамм 14 M.bovis и штамм H37Rv М.tuberculosis только при концентрации препарата 0,15 мкг/мл. Причем штамм H37Rv М.tuberculosis оказался более устойчив к изониазиду, чем штамм 14 М.bovis, и в концентрации 0,018 мкг/мл рост микобактерий туберкулеза практически не отличался от их роста в контрольных пробирках как на среде Сотона, так и с добавлением в нее 10% раствора лошадиной сыворотки. Концентрации изониазида 0,075; 0,037 и 0,018 мкг/мл на среде Сотона и среде Сотона, содержащей 10% раствор лошадиной сыворотки, оказывали лишь частичное подавление размножения микобактерий туберкулеза штамма 14.
В контрольных посевах рост тест-культур был обильный, характерный для каждого вида микобактерий.
Таким образом, по современной классификации (Г.Н.Першин, 1971) новое противотуберкулезное средство - тубофен следует отнести к высокоактивным противотуберкулезным препаратам по бактериостатическому действию.
С целью изучения бактерицидного действия тубофена также использовали метод последовательных серийных разведений. Взвесь микобактерий туберкулеза штамма 14, стандартизированную по стандарту БЦЖ, вносили в пробирки с питательной средой Сотона, содержащие различные концентрации тубофена. Пробирки помещали в термостат, при температуре 37°С и через 1,3,6,24 часа и 2,5 и 8 суток содержимое бактериальных пробирок переносили в центрифужные пробирки и центрифугировали при 3000 оборотов в минуту в течение 1/4 часа. Жидкость сливали, а осадок культуры отмывали от препарата физиологическим раствором с последующим центрифугированием. Осадок после удаления физиологического раствора пересевали в 2 пробирки со средой Левенштейна-Йенсена. Посев выдерживали в термостате при температуре 37°С в течение 2,5 месяцев. Отсутствие в этот срок отдельных или сливающихся колоний микобактерий туберкулеза свидетельствовало о бактерицидном действии соответствующих концентраций тубофена. Результаты исследования бактерицидной активности тубофена отражены в таблице 2.
Из данных таблицы 2 видно, что тубофен в минимальной концентрации - 0,75 мкг/мл оказывает полное бактерицидное действие на штамм 14 микобактерий туберкулеза бычьего вида, только при максимальном времени контакта - 8 суток. При воздействии на штамм микобактерий минимальной концентрации препарата в течение 5 суток на питательной среде Левенштейна-Йенсена обнаруживались лишь единичные колонии (частичный бактерицидный эффект).
Частичное бактерицидное действие тубофена впервые начало проявляться через 6 часов контакта препарата со штаммом микобактерий туберкулеза в концентрациях 50, 25 и 12,5 мкг/мл. Полная гибель всех микобактерий туберкулеза бычьего вида наступила через 5 суток при концентрации препарата 6,2 мкг/мл. При максимальном сроке экспозиции тубофена с микобактериями туберкулеза (8 суток) отмечалось выраженное бактерицидное действие препарата во всех экспериментальных концентрациях. Во всех контрольных пробирках отмечался сплошной рост микобактерий туберкулеза бычьего вида.
Определение параметров острой токсичности тубофена на белых мышах и крысах обоего пола проводили, используя методику А.А.Ступникова (Ступников А.А. Токсичность гербицидов и арборицидов и профилактика отравлений у животных. Л., «Колос», 1975, с.212-219). Результаты исследования острой токсичности тубофена на белых мышах приведены в таблице 3. Параметры острой токсичности водного раствора тубофена при внутрижелудочном введении белым мышам составили: максимально переносимая доза (МПД) - 400 мг/кг; среднесмертельная доза (ЛД50) - 668±63 мг/кг; доверительный интервал генеральной (ДИГ) средней ЛД50 - 668 (538-798) мг/кг; ЛД100 - 1000 мг/кг. В соответствии с «Гигиенической классификацией пестицидов по основным параметрам вредности» (Л.И.Медведь, Ю.С.Каган, Е.И.Спыну, 1986) тубофен является веществом, обладающим средней токсичностью. По степени опасности III класс, опасные химические вещества (ГОСТ 12.1.007.76). В свою очередь С.П.Булавин (Булавин С.П. Фармакологическая характеристика тубазида.// Бюлл. ВИЭВ. М., 1982. Вып.48, с.61-62) установил, что изониазид является высокотоксичным соединением для мышей - ЛД50 равна 178,0±6,79 мг/кг массы.
Результаты исследования острой токсичности тубофена на белых крысах отражены в таблице 4. Параметры токсичности водного раствора тубофена для белых крыс составили: максимально переносимая доза - 4500 мг/кг; среднесмертельная доза (ЛД50) - 5675±245 мг/кг; доверительный интервал генеральной средней ЛД50 - 5675 (5195-6155) мг/кг; ЛД100 - 7000 мг/кг. В соответствии с «Гигиенической классификацией пестицидов по основным параметрам вредности» (Л.И.Медведь, Ю.С.Каган, Е.И.Спыну, 1986) предлагаемое противотуберкулезное средство является малотоксичным соединением. По степени опасности IV класс, незначительно опасные химические вещества (ГОСТ 12.1.007.76).
Для изучения кумулятивных свойств тубофена использовали субхронический тест по R.Lim и др. (Lim R., Rink К., Glass H., et al. A metod for the evalution of cumulation and tolerance by the determination of acute and subchronic median effective doses.// Arch. intern. Pfrmocodyn. 1961. V.130. P.335-336). Полученные результаты представлены в таблице 5. Коэффициент кумуляции предлагаемого противотуберкулезного средства составил 4,72. По принятой в настоящее время классификации (Л.И.Медведь, Ю.С.Каган, Е.И.Спыну, 1986) тубофен соответствует веществам, обладающим умеренной кумуляцией.
Аллергизирующие свойства препарата изучали в соответствии с «Методическими рекомендациями по постановке исследований по гигиеническому нормированию промышленных аллергенов в воздухе рабочей зоны», утвержденными Министерством здравоохранения РФ в 1997 году (Требования к постановке экспериментальных исследований по обоснованию ПДК промышленных химических аллергенов в воздухе рабочей зоны и атмосферы. Методические указания 1.1.578-96. Минздрав России. - М., 1997. - 16 с.). Выявление сенсибилизации проводили с помощью реакции специфического лизиса лейкоцитов крови (РСЛЛ). Показатель РСЛЛ у животных первой опытной группы, сенсибилизированных тубофеном в дозе 50 мкг на животное, составил 1,19%, а у второй опытной группы, сенсибилизированной в дозе 200 мкг на животное, - 2,23%. Поэтому РСЛЛ расценивали как отрицательную, так как показатель лизиса лейкоцитов у обеих групп подопытных животных был менее 9%.
Анализ проведенных исследований показал, что предлагаемое противотуберкулезное средство при внутрикожной сенсибилизации морских свинок не обладает аллергенными свойствами.
Эмбриотоксическое и тератогенное действие средства оценивали в соответствии с «Методическими указаниями по изучению эмбриотоксического действия фармакологических веществ и влияния их на репродуктивную функцию» (Методические указания по изучению эмбриотоксического действия фармакологических свойств и влияние их на репродуктивную функцию. Одобрена фармакологическим комитетом МЗ СССР 14.03.86. - 18 с.) на 20 беспородных самках белых крыс половозрелого возраста. Животные были разделены на 2 группы по 10 крыс в каждой. Первая опытная группа получала тубофен внутрижелудочно в дозе, составляющей 1/20 от ЛД50 - 283,75 мг/кг массы, в течение 20 дней. Вторая, контрольная группа в аналогичных дозах получала растворитель (дистиллированную воду). На 20 сутки беременности посредством декапитации умерщвляли по 5 крыс из каждой группы для исследования эмбрионального материала. Критериями оценки эмбриотоксического действия препарата служили показатели количества желтых тел в яичниках, число мест имплантации, живых и мертвых плодов, определяли краниокаудальный размер плодов и диаметр планцет. По формулам определяли следующие показатели:
общая эмбриональная смертность - В - А/В×100;
предимплантационная гибель зигот - В - (А+Б)/В×100;
постимплантационная гибель эмбрионов - Б/А+Б×100;
где А - число живых эмбрионов; Б - число мертвых эмбрионов; В - количество желтых тел беременности.
Для выявления тератогенного эффекта опытных и контрольных животных убивали в конце беременности. Плоды взвешивали, измеряли их длину. Исследования проводили под бинокулярной лупой, разместив плоды в чашки Петри с физиологическим раствором. Далее плоды разделяли на две группы, одну фиксировали в жидкости Буэна в течение недели и использовали для послойной оценки макроструктуры внутренних органов по методу Вильсона (Willson, 1965) в модификации отдела эмбриологии ИЭМ АМН СССР. Вторую использовали для изучения развития скелета методом Даусона (Dawson, 1926), модифицированным в отделе эмбриологии ИЭМ АМН СССР (Мланин Л.П. Ветеринарные препараты. М.: Агропромиздат, 1988, с.250-258). Показатели эмбриотоксической активности тубофена представлены в таблице 6.
Анализ проведенных исследований показал, что тубофен не влияет на репродуктивные качества крыс. Показатели пред- и постимплантационной гибели у опытных и контрольных животных практически не отличались. При этом количество желтых тел и мест имплантации в группах примерно было равным и не отличалось более чем на 5,8%. Вскрытие самок белых крыс на 20 сутки беременности показало практически равное количество живых и мертвых плодов в обеих группах.
Изучение тератогенного действия тубофена при внешнем осмотре извлеченных из матки плодов животных опытной и контрольной групп, видимых морфологических изменений не наблюдалось. В ходе исследования состояния внутренних органов плодов методом Вильсона, аномалий развития, а также нарушение их топографии не установлено.
По мере приготовления препаратов плодов по методу Даусона проводили их визуальное изучение под бинокулярной лупой. В результате чего было установлено, что топография костных и хрящевых закладок в скелете плодов опытной группы не нарушается. Нарушений в оссификации костей черепа, плечевого, тазового пояса конечностей и отклонений в строении скелета также не установлено.
Изучение нарушений эмбрионального развития, проявляющихся в постнатальном периоде, проводили на 5 крысах, от которых было получено потомство. Анализ полученных результатов показал, что тубофен не влияет на массу тела и продолжительность беременности самок опытной группы (таблица 7).
Также существенно не менялись показатели постнатальной смертности и прироста массы тела крысят за первые 4 недели их жизни (таблица 8).
Таким образом, основные показатели, указывающие на эмбриотоксическое и тератогенное действие тубофена у подопытных и контрольных животных, были в близких пределах и свидетельствовали об отсутствии эмбриотоксического и тератогенного действия тубофена.
Изучение туберкулостатической активности тубофена проводили на экспериментальной модели туберкулеза морских свинок, которых разделили на 8 групп, из них 6 групп опытные и 2 контрольные. Животных 6-ти опытных и одной контрольной групп заражали 20 дневной оттитрованной культурой возбудителя туберкулеза бычьего вида (штамм 14). Бактериальную массу из расчета 0,15 мг на животное вводили подкожу правой паховой области в 0,5 мл физиологического раствора.
Химиопрофилактику туберкулеза морских свинок начали производить на следующий день после заражения. Животным шести контрольных групп перорально с помощью атравматического зонда с оливой, надетого на шприц, ежедневно вводили растворы предлагаемого противотуберкулезного средства - тубофена и изониазида. Причем морские свинки первой опытной группы получали тубофен в дозе 20 мг/кг массы, второй - 10 мг/кг массы, третьей - 5 мг/кг массы, четвертой - 2,5 мг/кг массы, пятой - 1 мг/кг массы и животные шестой группы получали изониазид в профилактической дозе - 10 мг/кг массы. Животные 7 и 8 контрольных групп получали ежедневно перорально растворитель (дистиллированную воду).
Опыт продолжался 60 дней. За животными вели клинические наблюдения, проводили гематологические исследования, а также аллергические исследования на туберкулез.
Результаты исследования профилактических свойств тубофена и изониазида при экспериментальном туберкулезе морских свинок отражены в таблице 9.
Из полученных данных видно, что за время проведения опыта все животные 1, 2, 3, 4 и 6 опытных групп выжили, в то время как 3 морские свинки из 5-й опытной, получавшие тубофен в дозе 1 мг/кг массы, и все животные 7-й контрольной группы (зараженные, не леченные) погибли.
В результате аллергических исследований морских свинок установлено, что животные 1, 2, 3 и 6 опытных групп не реагировали на введение туберкулина ни через 30 дней, ни через 60 дней после заражения их микобактериями туберкулеза бычьего вида.
У морских свинок 4 и 5 групп, получавших тубофен в дозах 2,5 и 1 мг/кг массы, а также у животных 7-й контрольной группы через 30 и 60 дней после заражения наблюдалось резко выраженная аллергическая реакция в местах введения ППД туберкулина для млекопитающих (стандартный раствор), которая проявлялась в виде гиперемии кожи в местах введения аллергена и образования уплотненной припухлости диаметром более 5 мм.
Отрицательный результат аллергических исследований также отмечался у 8-й контрольной группы.
При контрольном убое двух морских свинок из 1, 2, 3 и 6 контрольных групп через 30 дней после заражения во внутренних органах и тканях патологических изменений, характерных для туберкулеза, не обнаружено. При лабораторном исследовании патологического материала от животных данных групп выделить исходную культуру микобактерий туберкулеза не удалось.
У морских свинок 4-й опытной группы отмечались единичные туберкулезные очажки в печени и легких, а также увеличение регионарных лимфатических узлов до размеров крупной горошины в местах заражения животных микобактериями туберкулеза. У животных 5-й опытной и 7-й контрольной групп через 30 дней после заражения отмечали резкое увеличение объема печени и селезенки, содержащие в себе множественные туберкулезные очажки. В легких также отмечались единичные бугорковые высыпания. Регионарные лимфатические узлы были увеличены и достигали размеров фасоли. При лабораторном исследовании патологического материала от животных 4 и 5 опытных групп, а также от 7-й контрольной группы получен положительный результат, от всех животных была выделена исходная культура микобактерий туберкулеза.
Всех животных контрольных и опытных групп, прошедших курс химиопрофилактики (60 дней), подвергали убою и проводили патологоанатомические, бактериоскопические, бактериологические и гистологические исследования.
На основании патологоанатомических и бактериологических исследований установили средний общий индекс поражения органов и высеваемости микобактерий туберкулеза. У первых трех опытных групп, получавших тубофен в дозах 5, 10 и 20 мг/кг массы, а также у 8-й интактной группы этот индекс равнялся 0/0. При исследовании патологического материала от 4-й группы, получившей тубофен в дозе 2,5 мг/кг массы, средний общий индекс поражения органов и высеваемости микобактерий составил 6,45/6,65, у 5-й контрольной группы, получавшей тубофен в дозе 1 мг/кг массы, этот показатель оказался выше 17,06/12,46 и практически достигал таковой у 7-й контрольной группы (зараженные, не леченные) 20,2/12,8.
При исследовании патологического материала от 6-й контрольной группы, получившей изониазид в дозе 10 мг/кг массы, у 2 из 8 морских свинок отмечалось значительное увеличение регионарных правых паховых лимфатических узлов. Однако при посеве последних на питательную среду Левенштейна-Йенсена роста микобактерий туберкулеза не отмечалось, и средний общий индекс поражения органов и высеваемость микобактерий у морских свинок данной группы составил 0,37/0.
Таким образом, проведенные исследования свидетельствуют, что предлагаемое противотуберкулезное средство проявило достаточно высокий профилактический эффект и обладает выраженными туберкулостатическими свойствами в дозах 5 и 10 мг/кг массы животного. Вместе с тем, изониазид в дозе 10 мг/кг массы оказался менее активным и в 2 из 8 случаев экспериментального туберкулеза у морских свинок не достаточно полно проявил профилактический эффект.
Для проведения сравнительной оценки характера влияния изониазида и тубофена на структуру печени было использовано 20 голов морских свинок, разделенных на 3 группы, зараженные подкожно М. bovis (штамма 14) в дозе 0,15 мг бактериальной массы на 1 кг массы животного. Морские свинки первой группы не подвергались действию лечебных препаратов. Инфицированные животные второй группы на второй день после заражения подвергались ежедневному пероральному введению изониазида в профилактической дозе - 10 мг/кг массы в течение 2-х месяцев, а морским свинкам третьей группы вводили ежедневно перорально тубофен в дозе 10 мг/кг массы на протяжении того же срока. Убой подопытных животных проводили по истечении 60-ти суток после начала применения испытуемых средств. Для гистологических исследований кусочки печени фиксировали по методике Лилли, этанол-формалине (9:1), нейтральном 10%-ном формалине. Гистологические срезы толщиной 7 мкм окрашивали гематоксилин-эзином по Маллори, азур II-эозином, кислые мукополисахариды выявляли толуидиновым синим (Меркулов Г.А. Курс патологогистологической техники. Л.: «Медицина», 1969, 423 с.).
Результаты морфологических исследований показали, что у животных первой группы патоморфологические изменения в печени проявлялись по смешанному типу в виде сочетанного расположения в органе гранулематозных миллиарных узелков и очагов с преобладанием некротических изменений, что характеризовало волнообразное течение инфекционного процесса в организме. Инфекционные иммунопатологические реакции особенно ярко проявлялись в микроциркуляторном русле партальной системы органа. Они выделялись как мукоидным, фибриноидным набуханиями стенки кровеносных сосудов, так и полной дезорганизацией всей толщи их стенки. В периваскулярных зонах неравномерно располагались мононуклеарные клетки, по переферии которых отмечали фибробласты с признаками резкого ослабления синтетической активности. Продолжительное, активное течение инфекционного процесса в органе сочеталась с гепатоциллюлярной патологией в виде тяжелых деструктивных процессов, завершающихся гиалиново-капельной дистрофией, жировой декомпрозицией, некробиозом и некрозом (фиг.1).
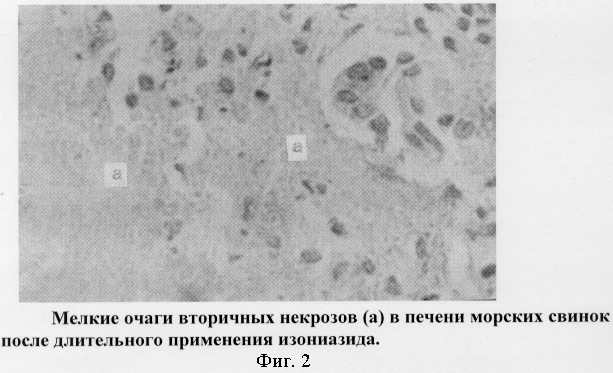
У зараженных микобактериями туберкулеза и подвергнутых продолжительному воздействию изониазида морских свинок отмечали резкое снижение выраженности деструктивных явлений, свойственных инфекционному процессу в ее активной фазе течения. Действие препарата подавляло выраженность аллергических реакций повышенной чувствительности немедленного и в меньшей степени гиперчувствительность замедленного типов. В этой связи в структуре печени отмечали резкое уменьшение количества и площади очагов некроза, а окружающие их зоны специфической грануляции выделялись резким разрежением клеток. Лимфопролиферативные, фибробластические реакции в структуре мезенхимальной ткани органа имели умеренную выраженность, что характеризовало продолжительное течение формирования процессов отграничения очагов некроза от окружающей ткани органа. Вместе с тем, действие изониазида оказало выраженный гепатотоксический эффект, проявлявшийся формированием новых очагов деструктивных процессов в виде обратимых и необратимых дистрофических изменений, переходящих в очаги некроза (фиг.2), что существенно снижало его профилактическую эффективность.
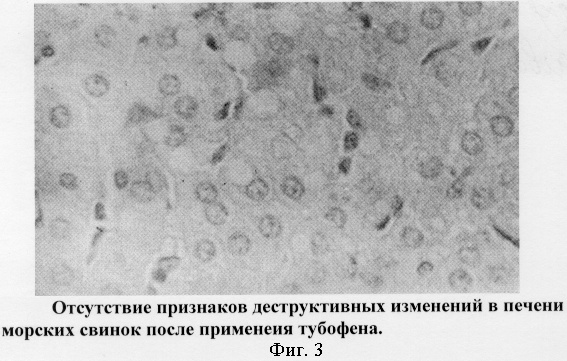
Наибольшую профилактическую эффективность оказало заявляемое средство - тубофен. По истечении 60-ти суток его применения у зараженных морских свинок в печени отмечали полное подавление проявлений гиперчувствительности немедленного и замедленного типов. Туберкулостатическое действие тубофена препятствовало образованию в печени очагов некроза и формированию специфических гранулем, что свидетельствовало о минимизации процессов деструкции на самых ранних этапах дезорганизации компонентов соединительной ткани и элементов паренхимы органа. Необратимое разрушение микобактерий стимулировало фибробластические процессы, преимущественно по ходу сосудов партальной системы органа, где ранее располагались очаги поражения. В них отмечали интенсивное разрастание аргирофильных и коллагеновых волокон, а в стенках прилегающих к ним кровеносных сосудов - отсутствие реакций инфекционной аллергии. В печени этих животных отмечали отсутствие разрастания соединительной ткани в синусоидах, зоны отека вокруг них, сплошной линии базальной мембраны капилляров, что в сочетании с малочисленностью звездчатых ретикулоэндотелиоцитов отражало высокий уровень транскапиллярного обмена в органе. Отсутствие признаков выраженной токсичности тубофена и продуктов его биотрансформации по сравнению с изониазидом способствовало низкому уровню проявления гепатоцилюлярной патологии (фиг.3). По окончанию курса химиопрофилактики тубофеном отсутствовали не только вторичные очаги некроза, возникающие после применения изониазида, но также дистрофические процессы необратимого характера.
Выявленные структурные изменения свидетельствуют о низком уровне повреждающего действия на паренхиму печени тубофена (по сравнению с изониазидом), а его высокие показатели туберкулостатического действия позволяют эффективно профилактировать данную инфекцию.
Показатели бактериостатической активности тубофена и изониазида в опыте in vitro.
Показатели бактерицидной активности тубофена в опыте in vitro
+ - от 1 до 10 колоний;
++ - от 11 до 30 колоний;
+++ - от 31 до 100 колоний;
++++ - сплошной рост.
Результаты исследования острой токсичности тубофена на белых мышах.
Результаты исследования острой токсичности тубофена на белых крысах
Результаты исследования по определению кумулятивных свойств тубофена
Показатели эмбриотоксической активности тубофена
Изменение массы тела и продолжительность беременности крыс при внутрижелудочном введении тубофена в течение всей беременности
Показатели развития потомства белых крыс
Результаты испытания химиопрофилактической активности тубофена и изониазида при экспериментальном туберкулезе морских свинок.
2 - индекс высеваемости микобактерий
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОТИВОТУБЕРКУЛЕЗНОЕ СРЕДСТВО В ВИДЕ РАСТВОРА ДЛЯ ИНЪЕКЦИИ | 2007 |
|
RU2358742C2 |
| СПОСОБ ОГРАНИЧЕНИЯ ОСЛОЖНЕНИЙ И ПОБОЧНЫХ ЯВЛЕНИЙ ПРИ ЛЕЧЕНИИ ТУБЕРКУЛЕЗА | 2001 |
|
RU2217137C2 |
| ПРЕПАРАТ ДЛЯ ЛЕЧЕНИЯ ТУБЕРКУЛЕЗА | 1994 |
|
RU2080114C1 |
| ИЗОНИКОТИНОИЛГИДРАЗОНЫ, ПРОЯВЛЯЮЩИЕ ПРОТИВОТУБЕРКУЛЕЗНУЮ АКТИВНОСТЬ | 1993 |
|
RU2054002C1 |
| СПОСОБ ЛЕЧЕНИЯ ЭКСПЕРИМЕНТАЛЬНОГО ТУБЕРКУЛЕЗА | 2000 |
|
RU2165761C1 |
| ОРОТАТ ГИДРАЗИДА ИЗОНИКОТИНОВОЙ КИСЛОТЫ, ОБЛАДАЮЩИЙ АНТИМИКОБАКТЕРИАЛЬНОЙ И ИММУНОТРОПНОЙ АКТИВНОСТЬЮ | 1990 |
|
RU2044728C1 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ТУБЕРКУЛЕЗА | 2013 |
|
RU2523792C9 |
| ТАБЛЕТКА ПРОТИВОТУБЕРКУЛЕЗНОГО ДЕЙСТВИЯ | 2007 |
|
RU2363475C2 |
| СПОСОБ ЛЕЧЕНИЯ ЭКСПЕРИМЕНТАЛЬНОГО ТУБЕРКУЛЕЗА | 2001 |
|
RU2207127C1 |
| ПРОТИВОТУБЕРКУЛЕЗНЫЙ ПРЕПАРАТ | 2002 |
|
RU2211035C1 |
Описывается соль бис(оксиметил)фосфиновой кислоты с гидразидом изоникотиновой кислоты формулы I:
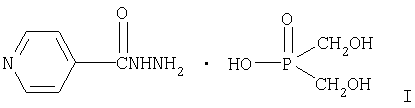
Описывается также способ получения соединения формулы I. Технический результат заключается в снижении токсичности противотуберкулезного средства при сохранении высокой терапевтической эффективности и отсутствии местной и общей реактогенности средства при лечебной дозе. 2 н. и 1 з.п. ф-лы, 3 ил., 9 табл.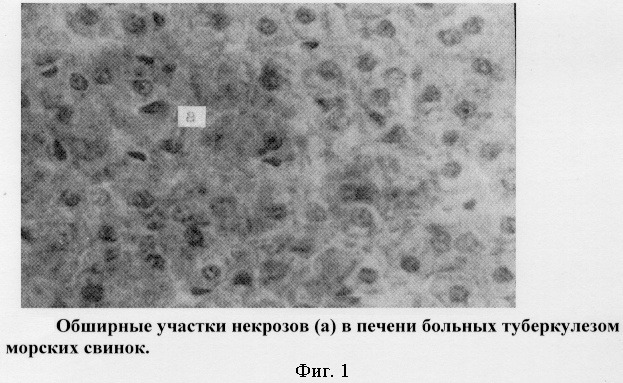
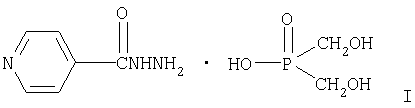
| ОРОТАТ ГИДРАЗИДА ИЗОНИКОТИНОВОЙ КИСЛОТЫ, ОБЛАДАЮЩИЙ АНТИМИКОБАКТЕРИАЛЬНОЙ И ИММУНОТРОПНОЙ АКТИВНОСТЬЮ | 1990 |
|
RU2044728C1 |
| ПРЕПАРАТ ДЛЯ ЛЕЧЕНИЯ ТУБЕРКУЛЕЗА | 1994 |
|
RU2080114C1 |
| Переходная токопроводящая конструкция для сетевого переходника | 2024 |
|
RU2838914C1 |
| Система для сейсмической разведки | 1982 |
|
SU1056098A1 |
| Устройство для центрирования элементов сборной кольцевой крепи | 1978 |
|
SU774684A1 |
| МЕЛАМИНОВАЯ СОЛЬ БИС(ОКСИМЕТИЛ)ФОСФИНОВОЙ КИСЛОТЫ(МЕЛАФЕН) В КАЧЕСТВЕ РЕГУЛЯТОРА РОСТА И РАЗВИТИЯ РАСТЕНИЙ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1999 |
|
RU2158735C1 |
Авторы
Даты
2006-08-20—Публикация
2005-03-25—Подача