Изобретение относится к медицине, в частности, к лекарственным противотуберкулезным средствам и может быть использовано при получении препаратов на основе изониазида и при химиотерапии туберкулеза.
К основным проблемам лечения туберкулеза относятся ограниченность арсенала противотуберкулезных средств, быстрое развитие устойчивых форм микобактерий туберкулеза (МБТ) на фоне лечения и, как следствие, рост числа больных, инфицированных первично устойчивыми МБТ к основным противотуберкулезным препаратам (11111). Поэтому постоянно идет поиск новых ПТП (патенты РФ 2153339, 27.07.2000; 2099056, 20.12.1997; 2080114, 27.05.1997), а также путей повышения эффективности известных противотуберкулезных препаратов: (патенты РФ 2169565, 27.06.2001; 2168994, 20.06.2001; 2136276, 10.09.1999; 2045278, 10.10.95; 2008902, 15.03.1994).
В стандартной комбинированной химиотерапии туберкулеза в качестве основного и наиболее эффективного противотуберкулезного препарата используется изониазид - гидразид изоникотиновой кислоты (М.Д.Машковский. Лекарственные средства. - М. : Медицина, 1988. - Т.2. - С.315-316). Поэтому за наиболее близкий аналог и выбрана эта фармацевтическая композиция, обладающая противотуберкулезным действием, включающая изониазид и фармацевтически приемлемый носитель (прототип). Эффективная и безопасная доза изониазида находится в интервале 5-15 мг/кг. Фармацевтически приемлемый носитель может быть в виде растворителя (изониазид для инъекций) или наполнителя (таблетки изониазида).
Отличаясь высокой терапевтической активностью, изониазид обладает и побочными эффектами в виде нарушений гемопоэза, функции печени, нейротоксических проявлений. Но его основным недостатком является быстрое развитие лекарственной устойчивости микобактерий туберкулеза, что снижает его эффективность. Резистентность МБТ к изониазиду у 70% больных развивается через три месяца после начала лечения, а 30% пациентов переходят в разряд хронических больных.
Задача заявляемого изобретения - расширение ассортимента противотуберкулезных препаратов.
Технический результат - повышение противотуберкулезной активности препарата, бактериостатическое воздействие на изониазидоустойчивый штамм МБТ, снижение токсического действия изониазида.
Для достижения этого технического результата фармацевтическая композиция, обладающая противотуберкулезным действием, включающая изониазид - гидразид изоникотиновой кислоты и фармацевтически приемлемый носитель, дополнительно содержит эффективное и безопасное количество 2,4-диоксо-5-фторпиримидина (фторурацила). При этом соотношение изониазида и фторурацила составляет 2: 1-150:1 по весу. Композиция может быть выполнена, в частности, в виде раствора и введена как внутримышечно, так и внутривенно.
Экспериментально in vivo и in vitro обнаружено, что дополнение композиции, включающей изониазид и фармацевтически приемлемый носитель, фторурацилом повышает ее противотуберкулезную активность, при этом композиция оказывает бактериостатическое воздействие и на изониазидоустойчивый штамм МБТ. Это позволяет использовать минимальные дозы изониазида, что, естественно, снижает его токсическое действие. В эксперименте на лабораторных животных было установлено эффективное и безопасное количество фторурацила в композиции для лечения туберкулеза, при этом соотношение изониазида и фторурацила составило 2:1-150:1 по весу. Фармацевтически приемлемыми носителями в композиции могут являться, в частности, вода, 0,9-5% растворы натрия хлорида и др. Выполнение композиции в виде раствора удобно для внутримышечного или внутривенного введения препарата.
Традиционно фторурацил относят к антиметаболической группе цитостатических средств и применяют при лечении рака в суточных дозах 10-15 мг/кг короткими курсами до 10 дней (М.Д.Машковский. Лекарственные средства. - М.: Медицина, 1988, т. 2, с.455). Туберкулостатические свойства фторурацила впервые нами были обнаружены в опытах in vitro (патент РФ 2153339, 2000), а его противотуберкулезная активность - при лечении экспериментального туберкулеза (патент РФ 2165761, 2001).
Можно предположить, что композиция, включающая два препарата, обладающих противотуберкулезной активностью, также будет оказывать противотуберкулезное действие. Однако известно, что комбинация нескольких туберкулостатических средств не всегда целесообразна из-за взаимного увеличения токсичности, а также из-за возможной несовместимости препаратов и особенностей их воздействия на биологический объект. Эксперименты, проведенные нами in vitro методом вертикальной диффузии, показали, что изониазид и фторурацил совместимы при смешивании, при этом туберкулостатическая активность композиции резко возрастает. Острая токсичность ЛД50 заявляемой композиции, определенная нами по методу Кербера (Г.Н. Першин. Методы экспериментальной химиотерапии. - М.: Медицина, 1971, с.526-529) на 80 белых мышах, составила 267,75 мг/кг. ЛД50 изониазида равно 188,4 мг/кг (патент РФ 2153878, 2000), т.е. заявляемая композиция обладает лучшей переносимостью.
Противотуберкулезная активность заявляемой композиции, изученная нами in vivo, оказалась выше, чем в прототипе. В этом эксперименте было определено эффективное и безопасное количество фторурацила при длительном лечении экспериментального туберкулеза у лабораторных животных, зараженных лабораторным Н37Rv (пример 1) или клиническим изониазидоустойчивым штаммами МБТ (пример 2). При этом было установлено, что введение животным композиции, содержащей 5-15 мг/кг изониазида и 0,1÷2,5 мг/кг фторурацила (что соответствует соотношению изониазида и фторурацила от 2:1 до 150:1 по весу), является эффективным и безопасным. Содержание в композиции фторурацила менее 0,1 мг/кг не приводит к существенным отличиям от прототипа, т.е. не является эффективным, а более 2,5 мг/кг - сопровождается токсическими поражениями организма. Высокая противотуберкулезная активность заявляемой композиции подтверждена также при клиническом испытании (пример 3).
Заявляемую композицию можно приготовить следующим образом.
Вариант 1. Путем смешивания сухих веществ "изониазид" и "фторурацил" в указанных соотношениях с последующим растворением в 5% растворе натрия хлорида и стерилизацией. Доза зависит от конкретного человека, массы тела и характера туберкулезного процесса. Обычно подходящей является композиция, содержащая от 5 до 10 мг/кг изониазида и от 1 до 1,5 мг/кг фторурацила, т.е. разовая доза для человека весом 50 кг может содержать 250÷500 мг изониазида и 50÷75 мг фторурацила.
Вариант 2. Путем добавления в готовый раствор изониазида необходимого количества готового раствора фторурацила. Например, к 10 мл 5% официнального раствора изониазида добавляют 1,5 мл 5% официнального раствора фторурацила. В результате получают разовую дозу препарата объемом 11,5 мл для внутривенного введения человеку массой 50 кг, в которой содержится 500 мг (10 мг/кг) изониазида и 75 мг (1,5 мг/кг) фторурацила. Композицию для лечения экспериментальных животных массой 200 г, содержащую 10 мг/кг изониазида и 1,5 мг/кг фторурациала, приготовляли путем смешения 4 мл 5% раствора изониазида и 0,6 мл 5% раствора фторурацила с 45,4 мл физиологического раствора. В 0,5 мл (разовая доза для внутримышечного введения) полученного раствора содержится 2 мг изониазида и 0,3 мг фторурацила. Аналогичным образом можно приготовить все заявляемые композиции.
Изучение противотуберкулезной активности композиции
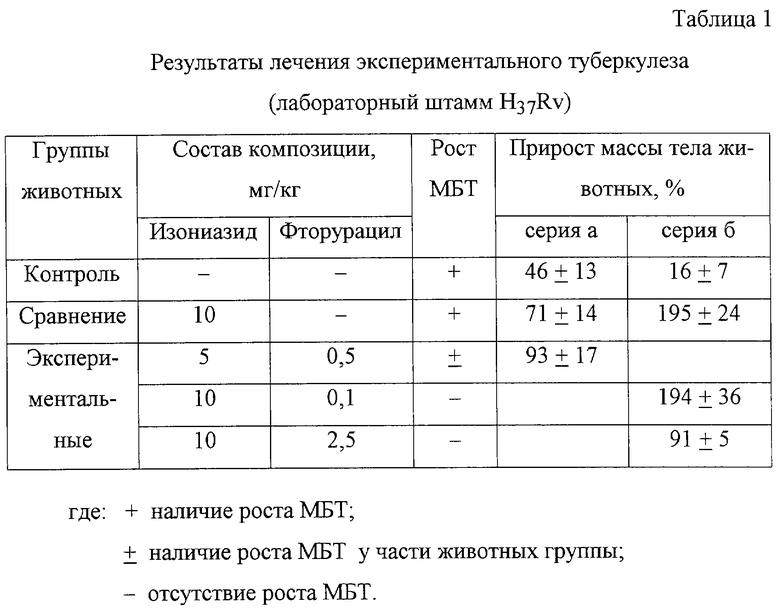
Пример 1. Проведены две серии экспериментов (а и б) продолжительностью по 2 месяца на морских свинках, самцах и самках, массой от 200 до 400 г с формированием однородных групп по массе и полу. Каждая группа состояла из 7 животных, всего 77 животных. Моделирование заболевания проводили путем подкожной инъекции культуры МБТ (лабораторный штамм Н37Rv) в дозе 0,025 мг/кг в объеме 0,5 мл в правую паховую область. Лечение начинали через 2 недели после заражения.
По группам животные были разделены следующим образом: две контрольные группы - без лечения; две группы сравнения - животные, которым ежедневно внутримышечно вводили композицию, содержащую официнальный раствор изониазида в дозе 10 мг/кг; семь экспериментальных групп - животные, получавшие ежедневно внутримышечно композицию, содержащую изониазид и фторурацил в соотношении 2: 1-150:1 по весу (минимальное количество препаратов в композициях составило: изониазид - 5 мг/кг и фторурацил - 0,1 мг/кг; максимальное количество: изониазид - 15 мг/кг и фторурацил - 2,5 мг/кг). Композиции приготовлены по вышеописанному варианту 2.
Методы исследования: прижизненная оценка течения туберкулеза у животных (изменение массы тела в конце эксперимента); биохимические и клинические исследования крови; патоморфологические исследования паренхиматозных органов и лимфоузлов; микробиологическое исследование гомогенатов паренхиматозных органов на наличие МБТ методом посева.
Результаты исследования. В контрольных группах к окончанию эксперимента пало более 50% животных, у всех животных был выявлен генерализованный туберкулез с характерными лабораторными и патоморфологическими изменениями, МБТ (+).
Все животные, получавшие лечение, выжили. Изменения лабораторных показателей у них не имели существенных различий и не выходили за пределы возрастной нормы, за исключением животных групп сравнения и группы, получавшей композицию с 2,5 мг/кг фторурацила, у которых была выявлена умеренная анемия.
Заявляемая композиция оказалась эффективнее прототипа, так как в результате лечения по сравнению с прототипом:
- снижено количество положительных посевов МБТ (табл. 1), уменьшены специфические патологические изменения паренхиматозных органов в группах, получавших композицию с наименьшим количеством фторурацила (0,1 и 0,5 мг/кг);
- отсутствует рост МБТ в гомогенатах паренхиматозных органов при использовании композиций с большими концентрациями фторурацила (до 2,5 мг/кг); при патоморфологическом исследовании обнаружены лишь остаточные изменения перенесенного генерализованного туберкулеза.
Прирост массы тела животных как экспериментальных групп, так и групп сравнения значительно превышал этот показатель у животных контрольных групп, что подтверждает противотуберкулезную активность применяемой композиции (табл. 1).
Пример 2. Эксперимент проведен на морских свинках, самцах и самках, массой от 300 до 400 г с формированием однородных групп по массе и полу. Каждая группа состояла из 7 животных, всего 49 животных. Продолжительность эксперимента - три месяца. Моделирование заболевания у животных всех групп проводили путем подкожной инъекции культуры МБТ (клинический изониазидоустойчивый штамм, выделенный из мокроты больного) в дозе 0,025 мг/кг в объеме 0,5 мл в правую паховую область. Штамм идентифицирован и установлена его лекарственная устойчивость к изониазиду в концентрации 100 мкг/мл. Лечение начинали через 2 недели после заражения. По группам животные были разделены следующим образом. Контрольная группа - без лечения; группа сравнения - животные, которым ежедневно внутримышечно вводили композицию, включающую изониазид в дозе 10 мг/кг; пять экспериментальных групп - животные, получавшие ежедневно внутримышечно композицию, включающую изониазид и фторурацил в соотношении 4:1-100:1 по весу (количество изониазида в композициях составило 10 мг/кг, фторурацила - от 0,1 до 2,5 мг/кг). Композиции приготовлены по вышеописанному варианту 2.
Методы исследования аналогичны первому примеру. Все животные во всех группах выжили. Клиническая картина заболевания во всех случаях была стертой. Изменения лабораторных показателей у исследуемых животных не имели существенных различий и не выходили за пределы возрастной нормы. Результаты посевов гомогенатов внутренних органов на выявление МБТ у всех животных всех групп оказались отрицательными. Животные контрольной группы, не получавшие лечения, по приросту массы значительно отставали от животных остальных групп (табл. 2). При патоморфологическом исследовании у всех этих животных были обнаружены множественные туберкулезные поражения внутренних органов с многочисленными очагами казеозного некроза. Таким образом, несмотря на стертую клиническую картину, обусловленную слабым клиническим штаммом МБТ, у всех животных контрольной группы был выявлен генерализованный туберкулез.
Композиция, включающая изониазид и фторурацил, оказалась эффективнее прототипа, так как в результате лечения по сравнению с прототипом:
- возрос прирост массы животных (табл. 2);
- в группах, получавших композиции с наименьшим количеством фторурацила (0,1 и 0,5 мг/кг), специфические патологические изменения менее выражены, в лимфоузлах отсутствуют очаги казеозного некроза;
- в группах, получавших композиции с наибольшим количеством фторурацила, отсутствуют патологические изменения паренхиматозных органов, т.е. после проведенного лечения ни в легких, ни в печени, ни в селезенке, ни в лимфоузлах не было найдено патоморфологических изменений, что свидетельствует о выздоровлении животных.
Результаты проведенных исследований (примеры 1 и 2) показали высокую противотуберкулезную активность заявляемой композиции вне зависимости от характера возбудителя. Преимущества использования данной композиции для лечения туберкулеза (в отличие от прототипа) заключаются как в ускорении элиминации МБТ из организма животных (в сроки до 2 месяцев от начала лечения) на фоне нормализации показателей гомеостаза, так и в уменьшении или отсутствии специфических патологических изменений паренхиматозных органов. Экспериментально показано, что использование фармацевтической композиции, содержащей изониазид и фторурацил, при лечении туберкулеза приводит к излечению животных в сроки эксперимента.
Пример 3. Проведено клиническое испытание противотуберкулезного действия фармацевтической композиции, включающей фармацевтически приемлемый носитель, изониазид в дозе 10 мг/кг и фторурацил в дозе 1-1,5 мг/кг, на 4-х больных прогрессирующим инфильтративным туберкулезом легких в фазе распада. Объем поражения в двух случаях ограничивался одной долей легкого. У двух других больных имелись очаги обсеменения с противоположной стороны. Во всех случаях была доказана устойчивость МБТ к двум и более основным ПТП. Продолжительность комбинированной химиотерапии у больных до поступления в клинику составляла от 12 до 14 месяцев. В клинике больным была продолжена химиотерапия с дополнительным назначением вышеуказанной композиции, которую вводили в виде раствора ежедневно внутривенно курсом до 3-х месяцев. Оценку состояния больных проводили на основании изменений клинической картины заболевания и показателей гомеостаза, динамики рентгенологической картины и сроков прекращения бактериовыделения.
В результате проведения комплексной противотуберкулезной терапии, дополненной композицией, включающей изониазид с добавлением фторурацила, у всех больных наблюдали положительную динамику процесса, которая выражалась в быстром, до 2-3 недель, купировании симптомов интоксикации и нормализации показателей крови. Через месяц после начала лечения у всех больных отмечался регресс рентгенологических изменений в виде рассасывания инфильтратов, уменьшения размеров или закрытия полостей распада, полного или частичного рассасывания очагов обсеменения. Абациллирование во всех случаях было достигнуто в сроки до 2 месяцев.
Двое больных через 2 месяца после начала лечения были прооперированы - выполнены лобэктомии. В обоих случаях в операционном материале были обнаружены процессы фиброзирования легочной ткани в пределах резецированных участков. Послеоперационная противорецидивная терапия проводилась с использованием только композиции, включающей изониазид и фторурацил, и продолжалась в течение одного месяца, после чего больные были выписаны под наблюдение фтизиатра. При контрольном обследовании через 12 месяцев признаков реактивации туберкулеза у этих больных выявлено не было.
В двух других случаях лечение ограничивали проведением описанной выше химиотерапии. Через три месяца после начала лечения у больных при рентгенологическом обследовании в легких на месте имевшихся полостей распада обнаружены рубцовые изменения с полным рассасыванием инфильтрации. При контрольном обследовании этих больных через 6 и 12 месяцев новых патологических изменений в легких у них не обнаружено.
Таким образом, заявляемая композиция расширяет ассортимент противотуберкулезных препаратов, так как обладает высокой противотуберкулезной активностью, оказывает воздействие и на изониазидоустойчивый штамм МБТ, позволяет снизить токсическое действие изониазида.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ ТУБЕРКУЛЕЗА | 2002 |
|
RU2212240C1 |
| СПОСОБ ЛЕЧЕНИЯ ЭКСПЕРИМЕНТАЛЬНОГО ТУБЕРКУЛЕЗА | 2000 |
|
RU2165761C1 |
| СПОСОБ ЛЕЧЕНИЯ ЭКСПЕРИМЕНТАЛЬНОГО ТУБЕРКУЛЕЗА | 2001 |
|
RU2207127C1 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ТУБЕРКУЛЕЗА | 2013 |
|
RU2523792C9 |
| СПОСОБ ЛЕЧЕНИЯ ТУБЕРКУЛЕЗА | 2004 |
|
RU2269346C1 |
| ТУБЕРКУЛОСТАТИЧЕСКОЕ СРЕДСТВО | 2001 |
|
RU2185170C1 |
| ТУБЕРКУЛОСТАТИЧЕСКОЕ СРЕДСТВО | 2002 |
|
RU2207126C1 |
| СПОСОБ СНИЖЕНИЯ НЕПЕРЕНОСИМОСТИ ПРОТИВОТУБЕРКУЛЕЗНЫХ ПРЕПАРАТОВ | 2009 |
|
RU2412701C2 |
| СПОСОБ ЛЕЧЕНИЯ ИНФИЛЬТРАТИВНОГО ТУБЕРКУЛЕЗА ЛЕГКИХ, ВЫЗВАННОГО МНОЖЕСТВЕННО-ЛЕКАРСТВЕННОУСТОЙЧИВЫМИ И ВЫСОКОТОКСИЧНЫМИ ШТАММАМИ МИКОБАКТЕРИЙ ТУБЕРКУЛЕЗА | 2009 |
|
RU2423129C1 |
| СПОСОБ ОЦЕНКИ ТЯЖЕСТИ ТУБЕРКУЛЕЗНОЙ ИНФЕКЦИИ | 2005 |
|
RU2305286C2 |

Изобретение относится к медицине, а именно к лекарственным средствам для лечения туберкулеза. Противотуберкулезный препарат представляет собой фармацевтическую композицию, содержащую изониазид - гидразид изоникотиновой кислоты в количестве 5-15 мг/кг, 2,4-диоксо-5-фторпиримидин (фторурацил) в количестве 0,1-2,5 мг/кг и фармацевтически приемлемый носитель. Соотношение изониазида и фторурацила может составлять 2:1-150:1 по весу. Композиция может быть выполнена в виде раствора и введена внутримышечно или внутривенно. Препарат обладает высокой противотуберкулезной активностью в сочетании с пониженным токсическим действием. 3 з.п.ф-лы, 2 табл.
| МАШКОВСКИЙ М.Д | |||
| Лекарственные средства | |||
| - М.: Медицина, 1988, т.2, с.315-316 | |||
| КОНЪЮГАТ ИЗОНИАЗИД-ДЕКСТРАН И ЕГО ПРИМЕНЕНИЕ В КАЧЕСТВЕ ПРОТИВОТУБЕРКУЛЕЗНОГО ПРЕПАРАТА | 1999 |
|
RU2163120C1 |
| ФАРМАЦЕВТИЧЕСКИЙ СОСТАВ, ОБЛАДАЮЩИЙ ПРОТИВОТУБЕРКУЛЕЗНОЙ АКТИВНОСТЬЮ | 1999 |
|
RU2146130C1 |
| Натриевую или каливую соль 1-(тетрагидрофурил-2)-5-фторурацила обладающие противоопухолевой активностью | 1977 |
|
SU590949A1 |
| Способ измерения амплитудной и фазовой анизотропииОпТичЕСКОгО Об'ЕКТА | 1978 |
|
SU753269A1 |
| US 4450274 A1, 22.05.1984 | |||
| WO 6310039 А2, 30.10.2001. | |||
Авторы
Даты
2003-08-27—Публикация
2002-03-18—Подача