Изобретение относится к химико-фармацевтической промышленности и касается получения лиофилизированного препарата АФП, относящегося к группе иммуномодуляторов и используемого в качестве средства для лечения онкологических, аутоиммунных и аллергических заболеваний.
АФП представляет собой фетальный гликопротеин с молекулярной массой около 70 кДа. АФП в большом количестве продуцируется клетками печени и брюшной стенки плода. Сырьем для получения АФП служит абортивная, пуповинная и плацентарная кровь, получаемая при медицинских абортах от клинически здоровых женщин, прошедших стандартное обследование. Получаемый абортивный материал обязательно тестируется на отсутствие антител к вирусу иммунодефицита человека (ВИЧ) и на отсутствие вируса гепатита В и антител к вирусу гепатита С.
Применяют АФП преимущественно парентерально. Водные растворы АФП нестабильны в процессе хранения, поэтому задача получения высокостабильных лекарственных форм является актуальной. Наиболее эффективным способом стабилизации препаратов для целей длительного хранения является их лиофилизация с соответствующими добавками [1].
Онкофетальные белки получают из эмбриональной или опухолевой ткани человека или животных. Высокоочищенный АФП получают из абортивной крови методами аффинной хроматографии.
Известен способ получения АФП из опухолевой ткани человека, включающий выделение и хроматографическую очистку целевого продукта последовательно на нескольких сорбентах [2]. Его недостатком является высокая трудоемкость процесса и низкий выход целевого продукта.
Разработан способ получения АФП из эмбриональной ткани человека [3], включающий ее измельчение, отмывку, гомогенизацию, обработку трипсином в течение 1 ч при температуре не более 37°С. Полученную суспензию клеток культивируют в питательной среде в течение 7-8 суток при 37°С, а целевой продукт отделяют центрифугированием при 3000 об/мин. Получают прозрачную жидкость оранжево-желтого цвета, содержащую 10% АФП.
Недостатками данного способа являются низкий выход и высокое содержание примесных белков.
Существует способ получения АФП из эмбриональной ткани человека [2], включающий обработку исходного материала бутиловым спиртом, центрифугирование, диализ водно-белковой фазы относительно 0,9%-ного раствора натрия хлорида, центрифугирование, инкубирование полученного супернатанта с эстрогеном в конечной концентрации 0,005% при температуре 0-10°С в течение 8 ч и выделение целевого продукта из супернатанта хроматографией на сефарозе CL-4B с иммобилизованным эстрогеном. Выход целевого продукта составляет 60-70%, а чистота препарата 90-95%.
Недостатками способа являются недостаточная чистота целевого продукта, наличие примеси альбумина и гемоглобина, а также высокая трудоемкость способа и необходимость работы с легковоспламеняющимся резко пахнущим органическим реактивом - бутиловым спиртом.
Одним из наиболее близких к изобретению является способ получения АФП из эмбриональной ткани человека 8-12 недель, полученной при медицинских абортах, включающий стадии [4]: измельчение и гомогенизация эмбриональной ткани; центрифугирование гомогената при 5000 об/мин; осветление супернатанта центрифугированием 12000 об/мин; очистка целевого продукта хроматографией на DEAE-целлюлозе; очистка целевого продукта хроматографией на сефадексе G-100 с иммобилизованным на нем красителем цибакрон голубой F36-A; очистка целевого продукта рехроматографией на сефадексе G-100 с иммобилизованным на нем красителем цибакрон голубой F26-A; очистка целевого продукта хроматографией на DEAE-целлюлозе.
Недостатками описанного способа являются длительность процедуры, низкий выход (25-30%) и недостаточная чистота (85-90%) целевого продукта, высокая трудоемкость и необходимость в сложном аппаратурном оснащении (высокоскоростные центрифуги).
Ближайшим аналогом является способ получения АФП [5]: абортивную кровь человека центрифугируют, полученный супернатант подвергают двустадийной хроматографической очистке (аффинная хроматография на Br-CN-сефарозе с иммобилизованными антителами к АФП и аффинная хроматография на Br-CN-сефарозе с иммобилизованным сбалансированным комплексом антител к белкам крови человека. Полученный раствор АФП обессоливают путем диализа против воды, стерилизуют и лиофилизируют.
Недостатками прототипа являются низкий выход (60-70%) и высокая контаминация примесными белками (чистота 90-95%) целевого продукта.
Техническим результатом изобретения является увеличение выхода АФП, сокращение времени технологического цикла и достижение максимальной чистоты.
Способ осуществляют следующим образом.
Абортивную, плацентарную или пуповинную кровь размораживают при температуре 2-6°С и проводят анализ на отсутствие вирусов. В проверенную на отсутствие вируса гепатита В, антител к ВИЧ, гепатиту С абортивную, пуповинную или плацентарную кровь или экстракт эмбриональных тканей добавляют при интенсивном перемешивании раствор хлороформа до достижения 0,1% концентрации с целью растворения липидов и инактивации оболочечных вирусов и бактерий. Затем с целью осаждения высокомолекулярных («тяжелых») белков (в основном белков системы свертывания крови и Ig классов А, М, G) и для блокирования реакций протеолиза в кровь с хлороформом при интенсивном перемешивании добавляют апротинин из расчета 0,1-1,0 г/л. Обработанную таким образом кровь оставляют на 24 часа в холодильнике при температуре 2-6°С. Через 24 часа на дне емкости с кровью отмечается образование значительного количества осадка, который удаляют центрифугированием (при 6000-16000 об/мин).
В супернатант добавляют натрия хлорид (0,1-1,0 моль/л) и тритон X-100 (0,01-0,5%) для блокирования неспецифической сорбции и дополнительной инактивации вирусов. Затем сыворотку или экстракт подвергают стерилизующей фильтрации: сначала через три слоя хлопчатобумажной проавтоклавированной и заправленной в фильтродержатель ткани, а затем через каскад фильтров с размером пор от 3,0 до 0,22 мкм.
Супернатант подвергают стерилизующей фильтрации: в разведенную стерильную сыворотку добавляют натрия хлорид (0,1-1,0 моль/л) и тритон X-100 (0,01-0,5%) для блокирования неспецифической сорбции и инактивации вирусов. Подготовленную таким образом стерильную сыворотку доводят раствором натрия гидроксида до рН 8,0-9,0 с целью создания условий усиления аффинного связывания АФП с антителами. Сорбент с иммобилизованными антителами к АФП перед нанесением сыворотки подвергают обработке 1,5 М раствором магния хлорида: сорбент/MgCl2=1:3, экспозиция в течение 30 минут (2 раза). Затем сорбент отмывают 0,15 М раствором натрия хлорида (10 объемов). После этого с целью блокирования активных центров неспецифической сорбции, иммуносорбент с антителами против АФП подвергают обработке сывороткой крупного рогатого скота (КРС).
Сыворотку КРС нагревают до 37°С в термостате и соединяют с сорбентом. Блокировка длится в течение 30 минут при температуре 18-20°С (в соотношении сорбент/сыворотка=1/3). После этого сорбент отмывают 0,15 М раствором натрия хлорида (10 объемов).
Неспецифически сорбировавшиеся компоненты крови вымывают с сорбента последовательно 4-5 объемами 0,15 М фосфатно-солевого буфера с рН 7,0-7,5, содержащего 0,5 М натрия хлорида, и таким же объемом раствора натрия хлорида (0,15 моль/л).
Сыворотку крови (рН 8,0-9,0) соединяют с сорбентом и осуществляют иммуносорбцию АФП в «свободном объеме» до полного истощения сыворотки. Сорбцию продолжают в течение 60 минут при температуре 18-20°С и при интенсивном перемешивании на верхнеприводной мешалке с последующим отстаиванием.
После отстаивания сыворотку декантируют и отмывают 1,0 М раствором магния хлорида на фильтре Шотта с экспозицией в течение 30 минут при перемешивании. Повторную неспецифическую элюцию проводят 2,0 М раствором магния хлорида в аналогичных условиях. Затем сорбент промывают 0,15 М раствором натрия хлорида (10 объемов).
Элюцию аффинносвязанного АФП проводят дважды в «свободном объеме» (по 1,5 часа) при интенсивном перемешивании и температуре 18-20°С 4,0 М раствором магния хлорида, доведенного 0,1 М Gly-HCl буфером до рН 2,0-3,0 при постоянном контроле рН. Отношение элюента к объему сорбента составляет 1:1. Затем сорбент отмывают 0,15 М раствором натрия хлорида до рН 6,0-7,0.
Элюат нейтрализуют 0,5 М раствором натрия гидроксида до рН 6,0-8,0 и подвергают диализу против 0,15 М натрия хлорида в диализных мешках или на специальном оборудовании (ультрафильтрационные или диализные установки).
Концентрирование элюата до необходимого объема проводят по содержанию АФП 0,6-1,2 мг/мл на концентрирующей ячейке типа «Amicon» с порами мембраны 30 мкм.
Затем с целью осаждения неспецифически сорбировавшегося IgG человека к концентрату АФП при интенсивном перемешивании добавляют 95%-ный охлажденный в морозильной камере этанол до насыщения его до 19-40% по объему (формула 1), предварительно доведя рН концентрата до 5,7-5,8 Gly-HCl буферным раствором (0,1 М). Экспозиция смеси при температуре минус 3-5°С длится двое суток.
Формула для расчета насыщения раствора АФП этанолом:
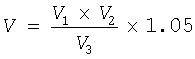 , где
, где
V - объем 95% этанола;
V1 - необходимое об.% содержание этанола в растворе белка;
V2 - объем раствора белка, который необходимо насытить этанолом;
V3 - об.% содержание раствора белка в смеси после добавления этанола;
1,05 - коэффициент разведения этанола до 95%.
Через 2 суток образовавшийся осадок в растворе АФП (IgG человека) отделяют центрифугированием в режиме 10000 - 26000 об/мин при температуре минус 3 - 5°С.
Супернатант подвергают диализу против 0,15 М натрия хлорида.
После выполнения описанного технологического процесса определяют электрофоретическую чистоту белка АФП (денситометрически) и проводят количественное определение IgG человека (метод иммунотурбидиметрии).
Чистота препарата АФП должна быть не менее 97%.
При содержании примесных белков не более 3% АФП стабилизируют полисахаридами (декстраны), производят стерилизующую фильтрацию, розлив и лиофильную сушку препарата АФП.
При наличии примесных белков (IgG человека; по данным двумерного электрофореза в градиенте и масс-спектрофотометрии) более 3% проводят дополнительную очистку концентрата АФП на иммуноаффинном сорбенте с антителами против IgG человека. Концентрат АФП после диализа наносят на сорбент с иммобилизованными антителами против IgG человека в «колоночном» варианте, где происходит аффинная сорбция человеческих иммуноглобулинов (негативная иммуносорбция), контаминирующих препарат после первой аффинной очистки и спиртового фракционирования. Препарат, полученный после негативной иммуносорбции, разбавляют 0,9% раствором натрия хлорида и реополиглюкином до концентрации АФП 0,6-0,9 мг/мл и декстрана 4-10 мг/мл. После стерилизующей фильтрации субстанцию АФП лиофилизируют.
Существенными отличиями предлагаемого способа от прототипа являются предварительная очистка исходной крови путем фракционирования белков сыворотки апротинином, насыщение крови раствором хлороформа и Тритона Х-100 для растворения липидов и инактивации вирусов, подавление неспецифической сорбции за счет обработки иммуноаффинного сорбента сывороткой КРС, нанесение сыворотки на иммуноаффинный сорбент при рН 8,0-9,0, снятие неспецифически сорбированных белков 1М и 2М раствором магния хлорида, элюирование АФП 4М раствором магния хлорида при рН 2,0-3,0, доочистка препарата АФП методом фракционирования этанолом (19-40% насыщение) и «негативной» хроматографией на втором иммуносорбенте, представляющем собой сефарозу, с иммобилизованными антителами против IgG человека.
Следует также отметить, что предлагаемый способ получения препарата АФП сокращает сроки технологического цикла с 14 до 4 суток и не требует наличия дорогостоящего хроматографического оборудования.
Пример конкретного исполнения.
Подготовка сыворотки крови
Разморозка 10 л крови. В кровь добавляют хлороформ в количестве 100 мл на 10 л и апротинин в количестве 5 г. Отстаивание крови в холодильнике при температуре 2-6°С в течение 24 часов. Центрифугирование при 6000 об/мин в течение 40 минут, декантация. Объем сыворотки после центрифугирования составил 7680 мл. Добавляют к сыворотке тритон Х-100 до 0,01% насыщения и 156 г натрия хлорида. Фильтрация через 3 слоя хлопчатобумажной ткани и мембранные фильтры 3,0-0,22 мкм. Добавляют к сыворотке раствор Тритона Х-100 до 0,01% насыщения.
II. Подготовка сорбента
Сорбент (сефароза CL-4B) с ковалентно пришитыми антителами (4-6 мг/мл) против АФП человека объемом 180 мл отмывают 5 объемами раствора 0,15 М натрия хлорида.
Перед нанесением сыворотки сорбент прошел обработку 1,5 М раствором магния хлорида: cop6eнт/MgCl2=1:3, экспозиция в течение 30 минут (2 раза). Затем сорбент отмывают 0,15 М раствором натрия хлорида (10 объемов).
Сыворотку КРС нагревают до 37°С в термостате и соединяют с сорбентом. Блокировка длится в течение 30 минут при температуре 18-20°С (в соотношении 1:3). После этого сорбент отмывают 0,15 М раствором натрия хлорида (10 объемов).
III. Сорбция АФП.
Сорбция происходит при рН 9,0 в течение 60 минут при комнатной температуре и интенсивном перемешивании верхнеприводной мешалкой до полного истощения содержания АФП с последующим отстаиванием в течение 2 часов.
IV. Неспецифическая элюция. После отстаивания сыворотку декантируют и сорбент отмывают 1,0 М раствором магния хлорида на фильтре Шотта с экспозицией в течение 30 минут при перемешивании. Повторную неспецифическую элюцию проводят 2,0 М раствором магния хлорида в аналогичных условиях. Затем сорбент промывают 0,15 М раствором натрия хлорида (10 объемов).
V. Элюция АФП.
Элюцию АФП проводят дважды (по 1,5 часа) при интенсивном перемешивании и комнатной температуре 4М магния хлоридом, доведенным 0,1 М Gly-HCl буфером до рН 2,2 при постоянном контроле рН. Отношение элюента к объему сорбента составляет 1:1. Затем сорбент отмывают 0,15 М раствором натрия хлорида до рН 7,0. Элюент нейтрализуют раствором натрия гидроксида до рН 6,8.
VI. Концентрирование элюата и спиртовое осаждение.
Концентрирование элюата проводят на концентрирующей ячейке «Amicon» до объема 113 мл с заменой раствора на 0,15 М натрия хлорид. Затем к концентрату добавляют охлажденный 95%-ный этанол до насыщения его до 32%, предварительно доведя рН концентрата до 5,7-5,8 0,1 М Gly-HCl буферным раствором. Экспозиция смеси при температуре минус 3-5°С длится двое суток.
После центрифугирования на скоростной центрифуге при 13400 об/мин в течение 15 минут и температуре минус 3-5°С осадок количественно отделяют от надосадочной жидкости. Надосадочная жидкость с содержанием АФП диализуют против раствора натрия хлорида. Концентрат подвергают анализу (см. таблицу; чертеж, серия 44-45). В результате технологических операций получают препарат АФП с чистотой 99,82-98,41%. После «негативной» хроматографии с сефарозой CL 4 В с антителами к IgG человека чистота препарата АФП составляет около 100%.
Полученный препарат тестируют на отсутствие антител к ВИЧ, вируса гепатита В и антител к вирусу гепатита С. Препарат стерилен, не содержит пирогенных и токсических примесей.
Использование предлагаемого способа позволяет по сравнению с прототипом: повысить чистоту целевого продукта за счет предварительного фракционирования белков исходной сыворотки крови апротинином, этанолом и двойной аффинной хроматографией на сорбентах высокой специфичности; увеличить выход АФП с аффинного сорбента с иммобилизованными антителами к АФП благодаря применению 4,0 М раствора магния хлорида и Gly-HCI буферного раствора; сократить время полного технологического цикла за счет отсутствия стадии гель-фильтрации.
Источники информации
1. Никитин В.В., Звягин И.В. Замораживание и высушивание биологических препаратов. М.: Колос, 1971, 344 с.
2. А.с. 1497806 СССР МКИ4 А61К 37/02, 48 "Способ получения альфа-фетопротеина".
3. А.с. №403407, кл3 А61К 35/48 "Способ получения биостимулятора"; заявл. 26.11.68; опубл. 26.10.73.
4. Huse Klaus et all "A novel purification procedure for human fetoproteun by application of immobilized Cibacron Blu F36-A as affinity ligand Clinica Chimica Acta", 133, 1983, 335-340.
5. Патент РФ №2100031 «Способ получения альфа-фетопротеина». / В.В.Стариков, С.Ю.Родионов, Мягкоходов В.А., Пак Н.А. (Россия).-№95120418/113; заявл. 01.12.95; опубл. 27.12.97; Бюл. №36.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПРЕПАРАТА АЛЬФА-ФЕТОПРОТЕИН СУХОЙ | 2005 |
|
RU2283131C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТАБЛЕТОК ПРЕПАРАТА АЛЬФА-ФЕТОПРОТЕИНА | 2005 |
|
RU2319479C2 |
| СОСТАВ ПРЕПАРАТА И СПОСОБ ЕГО ПОЛУЧЕНИЯ ДЛЯ ЛЕЧЕНИЯ ХРОНИЧЕСКИХ ВИРУСНЫХ ГЕПАТИТОВ В ИЛИ С И СПИДА | 2010 |
|
RU2440133C2 |
| СПОСОБ ВЫДЕЛЕНИЯ И ОЧИСТКИ АЛЬФА-ФЕТОПРОТЕИНА | 2005 |
|
RU2302424C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРЕПАРАТА АЛЬФА-ФЕТОПРОТЕИНА | 1998 |
|
RU2123009C1 |
| СПОСОБ ВЫДЕЛЕНИЯ И ОЧИСТКИ ТРОФОБЛАСТИЧЕСКОГО БЕТА-1-ГЛИКОПРОТЕИНА | 2007 |
|
RU2325171C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОБОГАЩЕННОГО УГЛЕВОДАМИ АЛЬФАФЕТОПРОТЕИНА | 2002 |
|
RU2232770C2 |
| СПОСОБ ПРОМЫШЛЕННОГО ПОЛУЧЕНИЯ ПРЕПАРАТА АЛЬФА-ФЕТОПРОТЕИНА | 2010 |
|
RU2448727C2 |
| ХРОМАТОГРАФИЧЕСКИЙ СПОСОБ ВЫДЕЛЕНИЯ АЛЬФА-ФЕТОПРОТЕИНА | 1996 |
|
RU2094078C1 |
| СПОСОБ ВЫДЕЛЕНИЯ И ОЧИСТКИ ТРОФОБЛАСТИЧЕСКОГО БЕТА-1-ГЛИКОПРОТЕИНА | 2008 |
|
RU2367449C1 |
Изобретение относится к химико-фармацевтической промышленности и касается способа получения альфа-фетопротеина (АФП). Сущность метода заключается в следующем: препарат получают путем выделения из сыворотки крови и очистки с помощью двойной аффинной хроматографии, причем между хроматографическими очистками проводят фракционирование белков апротинином 0,1-1 г/л и этиловым спиртом 19-40% насыщения по объему при рН 5,7-5,8 и температуре минус 3 - минус 5°С, а инактивацию бактерий и вирусов осуществляют перед первой очисткой на иммуносорбенте в присутствии растворов хлороформа и Тритона Х-100. Нанесение на аффинный сорбент сыворотки крови проводят с предварительной блокадой активных центров неспецифической сорбции сывороткой крупного рогатого скота, а нанесение на иммуноаффинный сорбент с антителами против альфа-фетопротеина производят при рН 8,0-9,0 и при температуре 18-20°С. Примесные белки сыворотки крови удаляют неспецифической элюцией 1 и 2 М раствором магния хлорида, а аффинно-связанный АФП элюируют с помощью 4 М раствора магния хлорида и буферного раствора Gly-HCl с рН 2,0-3,0, при этом в качестве второго аффинного сорбента используют сефарозу с антителами против IgG человека. 1 табл., 1 ил.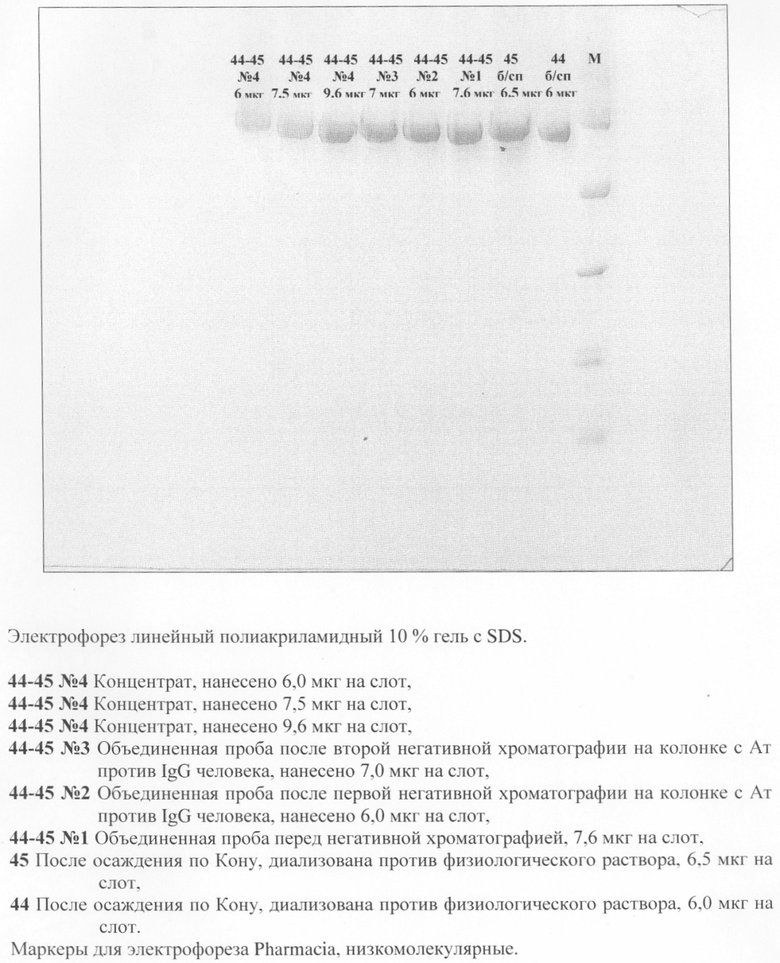
Способ получения альфа-фетопротеина (АФП), включающий выделение из сыворотки крови и очистку с помощью двойной аффинной хроматографии, отличающийся тем, что проводят предварительную очистку исходной крови путем насыщения крови раствором хлороформа для отделения липидов, фракционирование белков сыворотки апротинином и насыщение крови раствором Тритона Х-100 для инактивации вирусов и растворения липидов, подавление неспецифической сорбции на сорбенте с антителами против АФП за счет обработки иммуноаффинного сорбента сывороткой крупного рогатого скота (КРС), нанесение сыворотки на иммуноаффинный сорбент при рН 8,0-9,0, снятие неспецифически сорбированных белков 1М и 2М раствором магния хлорида, элюирование АФП осуществляют 4М раствором магния хлорида в 0,1М Gly-HCl буфере при рН 2,0-3,0 и доочистку АФП методом фракционирования этанолом 19-40% насыщения и «негативной» хроматографией на втором иммуносорбенте, представляющем собой сефарозу, с иммобилизованными антителами против IgG человека.
| СПОСОБ ПОЛУЧЕНИЯ АЛЬФА-ФОТОПРОТЕИНА | 1995 |
|
RU2100031C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРЕПАРАТА АЛЬФА-ФЕТОПРОТЕИНА | 1996 |
|
RU2121350C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРЕПАРАТА АЛЬФА-ФЕТОПРОТЕИНА | 1998 |
|
RU2123009C1 |
| реф | |||
| Tatarinov Y.S | |||
| et al., "Human alpha-fetoprotein and its purification by chromatography on immobilized estrogens.", Tumour Biol | |||
| Циркуль-угломер | 1920 |
|
SU1991A1 |
| реф | |||
| Tecce MF et al., "High-yield and high-degree purification of human alpha-fetoprotein produced by adaptation of | |||
Авторы
Даты
2007-10-20—Публикация
2006-01-10—Подача