Изобретение относится к области химической технологии, а именно к способу получения хлороформа, который широко используется в качестве растворителя и сырья в производстве фторхлоруглеводородов и других химических продуктов.
Поскольку хлороформ представляет известную ценность, существует целый ряд способов его получения путем газофазного или жидкофазного хлорирования углеводородов (Ф.Ф.Муганлинский, Ю.А.Трегер, М.М.Люшин. Химия и технология галогенорганических соединений. - М.: Химия, 1991, с.68-71).
Хлорирование углеводородов имеет ряд существенных недостатков:
- возможность образования взрывоопасных смесей (Н.Н.Лебедев. Химия и технология основного органического и нефтехимического синтеза. - М.: Химия, 1975, с.120-121);
- образуется большое количество экологически опасного четыреххлористого углерода, производство и применение которого запрещено по Монреальскому протоколу.
Известен способ получения хлороформа из смеси, содержащей хлораль, путем ее обработки известковым молоком при температуре 50-80°С с отпаркой образующегося хлороформа (SU 125425, кл. С07С 19/04, 1960):
2CCl3СНО+2Са(ОН)2→2CHCl3+Са(НСОО)2.
Недостатком способа является образование формиата кальция, который требует сложной очистки и переработки в муравьиную кислоту или ее производные. Продукты не конкурентоспособны из-за более высокой цены, чем те же продукты, получаемые целевым синтезом.
Хлороформ можно получить из ацетона, этанола или метилацетата обработкой хлорной известью (Ф.Ф.Муганлинский, Ю.А.Трегер, М.М.Люшин. Химия и технология галогенорганических соединений. - М.: Химия, 1991, с.68) по следующей реакции:
2СН3СОСН3+6СаОСl2→2CHCl3+Са(СН3СОО)2+2Са(ОН)2+3CaCl2.
Метод долгое время использовался в промышленном масштабе, но из-за низких технико-экономических показателей в настоящее время потерял значимость по сравнению с более экономичными и эффективными современными методами получения хлороформа.
Известен способ получения хлороформа взаимодействием гексахлорацетона с раствором щелочи при значениях рН не более 10 и температуре не более 50°С (патент Японии №19927, 1968):
CCl3COCCl3+NaOH→CHCl3+CCl3COONa.
В данном способе наряду с целевым продуктом - хлороформом - получается трихлорацетат натрия, на образование которого расходуется щелочь. Ранее это соединение применяли как гербицид. В настоящее время используются гербициды нового поколения, более экологичные и эффективные.
Наиболее близким по технической сущности к предлагаемому способу является способ получения хлороформа (патент РФ №2206558, 2003), по которому гексахлорацетон гидролизуют водой в присутствии катализатора - этаноламинов - при температуре 95-150°С с одновременной отгонкой образующегося хлороформа.
CCl3COCCl3+Н2О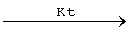 2CHCl3+CO2.
2CHCl3+CO2.
Основным недостатком этого способа является то, что в процессе синтеза катализатор постепенно дезактивируется за счет протекания побочных реакций образования трихлорацетата амина, формиата амина, гидрохлорида амина. Регенерация катализатора из отработанного водного раствора довольно длительный и энергоемкий процесс. Сначала раствор отработанного катализатора кипятят при температуре выше 100°С в течение 3-5 часов для разложения трихлорацетата амина. Далее раствор охлаждают до 20-30°С и в него подают 40-45%-ную щелочь до рН 8-9 для разложения гидрохлорида амина и формиата амина. Выпавшие кристаллы хлористого натрия отфильтровывают.
Задачей предлагаемого способа является упрощение технологии получения хлороформа путем гидролиза гексахлорацетона водой.
Это достигается тем, что получение хлороформа каталитическим взаимодействием гексахлорацетона с водой при повышенной температуре осуществляют с использованием в качестве катализатора неорганического соединения кремния природного или синтетического происхождения или смеси таких соединений кремния с последующим выделением хлороформа из реакционной смеси известными способами.
По предлагаемому способу в качестве неорганического соединения кремния природного или синтетического происхождения или смеси таких соединений кремния преимущественно используют соединение, выбранное из группы включающей тальк, волластонит, ксонотлит, диатомит, силикагель, аэросил, белую сажу, силикаты и/или гидросиликаты металлов, преимущественно натрия, калия, магния, кальция, алюминия, меди, титана, свинца, марганца, железа, никеля, или их смеси в различных массовых соотношениях.
По предлагаемому способу катализатор используют предпочтительно в количестве 1-25% от массы реакционной смеси. В общем случае количество катализатора должно быть необходимым и достаточным для ускорения процесса гидролиза гексахлорацетона и может быть менее 1% или более 25% от массы смеси. Однако увеличение количества катализатора более 25% от массы смеси технически нецелесообразно, поскольку обусловливает снижение производительности технологического оборудования и количества получаемого продукта на единицу массы катализатора.
Предлагаемый процесс может быть реализован периодическим и непрерывным способом при атмосферном или избыточным давлении в пределах 0,05-6,0 ати.
Проведение процесса при атмосферном давлении позволяет использовать обычное технологическое оборудование, а проведение процесса при небольшом избыточном давлении позволяет снизить потери хлороформа и повысить его качество при выделении его из газовой смеси.
Процесс по предлагаемому способу осуществляют в любом обычном реакторе, который снабжен устройствами для перемешивания и для подачи гексахлорацетона и воды. Например, в реактор загружают необходимое количество воды и катализатора. Затем при перемешивании дозируют гексахлорацетон и воду в мольном соотношении 1:1,01-1,2 при температуре 90-160°С. Образующийся при гидролизе гексахлорацетона хлороформ выделяют из реакционной массы отгонкой или разделением водного и органического слоев. Существенным преимуществом предлагаемого способа является то, что не требуется дополнительного расхода реагентов, энергоресурсов, трудозатрат на регенерацию отработанного катализатора. Последний может быть использован без дополнительной обработки как добавка в строительные материалы (бетонные растворы, штукатурные массы и т.п.). К преимуществам относятся также доступность катализатора и легкость его выделения из реакционной массы, более высокая эффективность катализатора, его пожаро- и взрывобезопасность, а также экологическая безопасность по сравнению с этаноламинами.
Кроме того, ресурс работы предлагаемого катализатора существенно превышает ресурс работы этаноламинов.
Ниже приведены некоторые примеры, демонстрирующие сущность предлагаемого способа получения хлороформа, которые не ограничивают объем притязаний, определенный формулой и описанием данного способа.
Пример 1.
В реактор, снабженный перемешивающим устройством, термометром, системой подачи гексахлорацетона, обратным холодильником, оборудованным ловушкой Дина-Старка и соединенным с системой поглощения абгазов, заливают 40 г воды, добавляют 4,4 г гидросиликата натрия, нагревают до температуры 95-105°С и дозируют в него гексахлорацетон со скоростью 30 г/ч, одновременно дозируют воду, которая берется в мольном отношении 1,01-1,2 к молю гексахлорацетона. Температуру реакционной массы поддерживают в тех же пределах. Выделяющиеся при этом пары хлороформа, воды и углекислый газ охлаждают в холодильнике, который снабжен ловушкой-разделителем. Из ловушки вода возвращается в реактор, а хлороформ собирается в сборник.
За 16 часов работы получено 426 г хлороформа, выход его составил 98,4%.
Пример 2.
В реактор, снабженный перемешивающим устройством, термометром, системой подачи гексахлорацетона, обратным холодильником, соединенным с системой поглощения абгазов, заливают 40 г воды, добавляют 5 г белой сажи марки БС-100, нагревают до температуры 95-105°С и дозируют в него гексахлорацетон со скоростью 25 г/ч. Далее так же, как описано в примере 1.
За 24 часа работы получено 537 г хлороформа, выход его составил 99,0%.
Пример 3.
В реактор, снабженный перемешивающим устройством, термометром, системой подачи гексахлорацетона, обратным холодильником, соединенным с системой поглощения абгазов, заливают 40 г воды, добавляют 7 г силиката кальция. Водную суспензию катализатора нагревают до температуры 95-105°С и дозируют в него гексахлорацетон со скоростью 20 г/ч. Далее осуществляют синтез так же, как описано в примере 1.
За 45 часов работы получено 800 г хлороформа, выход его составил 98,6%.
Пример 4.
В реактор, снабженный перемешивающим устройством, термометром, системой подачи гексахлорацетона, обратным холодильником, соединенным с системой поглощения абгазов, заливают 40 г воды, добавляют 10 г волластонита. Водную суспензию катализатора нагревают до температуры 95-105°С и дозируют в него гексахлорацетон со скоростью 20 г/ч. Далее так же, как описано в примере 1.
За 15 часов работы получено 268 г хлороформа, выход его составил 99,1%.
Пример 5.
В реактор, снабженный перемешивающим устройством, термометром, системой подачи гексахлорацетона, обратным холодильником, соединенным с системой поглощения абгазов, заливают 50 г воды, добавляют 2 г гидросиликата алюминия и 3 г аэросила. Водную суспензию катализатора нагревают до температуры 95-105°С и дозируют в него гексахлорацетон со скоростью 35 г/ч. Далее синтез проводят так же, как описано в примере 1.
За 72 часа работы получено 2250 г хлороформа, выход его составил 99,0%.
Пример 6.
В реактор, снабженный перемешивающим устройством, термометром, системой подачи гексахлорацетона, обратным холодильником, соединенным с системой поглощения абгазов, заливают 40 г воды, добавляют 8 г силиката кальция. Водную суспензию катализатора нагревают до температуры 95-105°С и дозируют в него гексахлорацетон со скоростью 35 г/ч. Далее осуществляют процесс так же, как описано в примере 1.
За 240 часов (10 суток) работы получено 7477 г хлороформа, при этом его выход составил 98,7% от теоретического.
Из приведенных примеров следует, что предлагаемый способ получения хлороформа позволяет существенно упростить технологию его получения методом каталитического гидролиза гексахлорацетона и исключить необходимость регенерации используемого катализатора.
Кроме того, использование в предлагаемом процессе указанных катализаторов значительно расширяет сырьевую базу технологии и определяет снижение себестоимости целевого продукта и снижение экологической нагрузки на окружающую среду за счет применения более доступных, экономичных, негорючих и нетоксичных неорганических соединений кремния вместо этаноламинов, относящихся ко второму и третьему классам опасности.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ ХЛОРОФОРМА И АЛКИЛЕНКАРБОНАТОВ | 2006 |
|
RU2309935C1 |
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРОФОРМА | 2001 |
|
RU2206558C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕКСАХЛОРАЦЕТОНА | 2007 |
|
RU2351582C1 |
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРАЦЕТОНОВ | 2001 |
|
RU2225858C2 |
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРАЦЕТОНОВ | 2001 |
|
RU2224738C2 |
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРИРОВАННЫХ ПОЛИМЕРОВ И СОПОЛИМЕРОВ ВИНИЛХЛОРИДА | 2007 |
|
RU2337924C1 |
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРИРОВАННЫХ ПОЛИМЕРОВ И СОПОЛИМЕРОВ ОЛЕФИНОВЫХ УГЛЕВОДОРОДОВ | 2007 |
|
RU2346955C1 |
| СПОСОБ ПОЛУЧЕНИЯ КАРБОНАТНОГО СОЕДИНЕНИЯ | 2008 |
|
RU2494088C2 |
| СПОСОБ ПОЛУЧЕНИЯ КАРБОНАТНОГО СОЕДИНЕНИЯ | 2008 |
|
RU2489418C2 |
| Ресурсосберегающий способ получения фенилацетилена | 2023 |
|
RU2807280C1 |
Изобретение относится к способу получения хлороформа путем гидролиза гексахлорацетона водой при повышенной температуре в присутствии катализатора, в качестве которого используют неорганическое соединение кремния природного или синтетического происхождения или смеси таких соединений кремния с выделением хлороформа из реакционной массы известными способами. В качестве указанных соединений кремния преимущественно используют тальк, волластонит, ксонотлит, диатомит, силикагель, аэросил, белую сажу, силикаты и/или гидросиликаты металлов, таких как натрий, калий, магний, кальций, алюминий, медь, титан, свинец, марганец, железо, никель. Катализатор используют преимущественно в количестве 1-25% от массы реакционной смеси. Технический результат - существенное упрощение технологии получения хлороформа за счет исключения стадии регенерации катализатора, а также расширение сырьевой базы каталитического процесса. 2 з.п. ф-лы.
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРОФОРМА | 2001 |
|
RU2206558C1 |
| Способ ранней диагностики заболеваний мягких тканей кисти у работников от физического перенапряжения и микротравматизации с применением метода ультразвуковой диагностики | 2018 |
|
RU2695918C1 |
| Способ одновременного получения хлороформа и формиата кальция | 1959 |
|
SU125245A1 |
| Способ получения хлороформа | 1976 |
|
SU729182A1 |
Авторы
Даты
2007-11-10—Публикация
2006-05-10—Подача