Бромид 1-гексадецил-R(-)-3-окси-1-азониабицикло[2.2.2]октана (далее вещество I) относится к кватернатам оптически активных бициклических аминоспиртов и может быть использован в медицине в качестве химио- и радиопротектора в сочетании с химио- и лучевой терапией для улучшения качества жизни больных и уменьшения интервалов между курсами специфического лечения рака, при хирургическом лечении химиорезистентных форм рака (рак легкого, пищевода, желудка и т.д.) в качестве стимулятора противоопухолевого иммунитета у больных в послеоперационном периоде; для профилактики онкологических заболеваний у лиц с высоким фактором риска (генетическая предрасположенность к раку, профессиональные факторы и т.д.) на фоне мониторинга противоопухолевых составляющих иммунитета; при лечении иммунодефицитов и хронических инфекций различной природы; в качестве антикоагулянта у больных с повышенной свертываемостью крови для профилактики тромбообразования; в лабораторной практике: в качестве активатора натуральных киллеров и индуктора цитокинов (интерлейкинов, фактора некроза опухолей, интерферонов и т.д.).
В качестве аналогов вещества I могут рассматриваться иммуномодуляторы цитокиновой природы с противоопухолевой активностью. К таким соединениям относятся препараты интерлейкина-2 (Ронколейкин, Россия, и Пролейкин, Голландия) и интерферона (Реоферон, Россия, Интрон-А, США). Эти препараты при воздействии в терапевтических дозах могут вызывать побочные реакции в виде лихорадки, снижения уровня артериального давления, почечной и дыхательной недостаточности (Биологические методы лечения онкологических заболеваний: Пер. с англ. / Под ред. В.Т.ДеВита, С.Хеллмана, С.А.Розенберга. - М.: Медицина, 2002. - Д.Дж.Шварцентрубер. Биологические методы лечения интерлейкином-2: клиническое применение, с.247-262; К.А.Фун. Биологические методы лечения интерфероном-α и -β: клиническое применение с.382-390; X.Р.Кесада. Биологические методы лечения интерфероном-γ, с.452-460). Побочные эффекты этих рекомбинантных пептидов требуют проведения длительных (до 18 ч ) инфузий или подкожных введений, при которых происходит потеря до 30% активности действующего начала (Справочник для иммунотерапии для практического врача. / Под ред. А.С.Симбирцева. - С. - Пб.: Диалог, 2002. - В.К.Козлов. Ронколейкин: биологическая активность, иммунокорригирующая эффективность и клиническое применение). Кроме того, эти препараты при длительном применении вызывают образование антител, что снижает их эффективность (G. Sarna et al. A comparative study of intravenous versus intralymphatic interleukin-2, with assessment of effects of interleukin-2 on both peripheral blood and thoracic-duct lymph. JT. Immunother, 1994. - №15 - P.140-146). Рекомбинантные цитокины требуют особых условий хранения и транспортирования и не могут храниться в водных растворах. Известны также иммуномодуляторы небелковой природы (ликопид, полиоксидоний, иммунофан, неовир), которые используются для коррекции иммунного статуса у онкологических больных, однако их противоопухолевое действие не установлено (Добрица В.И, Ботерашвили Н.М., Добрица Е.В. Современные иммуномодуляторы для клинического применения. Руководство для врачей. - С. - Пб.: Политехника, 2001-251 с.; Справочник для иммунотерапии для практического врача. / Под ред. А.С.Симбирцева. - С. - Пб.: Диалог, 2002. - А.А.Старченко. Общая характеристика иммунотропных препаратов, с.100-151).
Вещество I в отличие от рекомбинантных цитокиновых противоопухолевых препаратов характеризуется низкой токсичностью и в дозах, в тысячи раз превышающих терапевтические, не оказывает токсического действия на системы жизнеобеспечения у лабораторных животных. Вещество I не вызывает гипертермических реакций у животных, не оказывает аллергезирующего действия и не обладает кумулятивным эффектом. Препарат высоко стабилен в водных растворах, не требует особых условий транспортирования и хранения, сохраняет свою биологическую активность в растворах не менее 3 лет. Вещество I наряду с иммуномодулирующим действием обладает противоопухолевой и бактериостатической активностью. Вещество I хотя и является синтетическим соединением с низкой молекулярной массой, наиболее близким по спектру биологической активности для него является рекомбинантный пептид ИЛ-2, который может рассматриваться в качестве его прототипа.
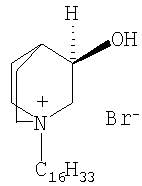
Препарат представляет собой индивидуальное органическое вещество - бромид 1-гексадецил-R(-)-3-окси-1-азониабицикпо[2.2.2]октана, см. формулу
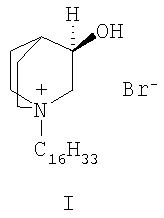
Способ получения. Бромид 1-гексадецил-R(-)-3-окси-1-азониабицикло[2.2.2]октана (I) получают по реакции обмена аниона между хлоридом 1-гексадецил R(-)-3-окси-1-азониабицикло[2.2.2]октана (II) и бромистоводородной кислотой (III)
Схема 1
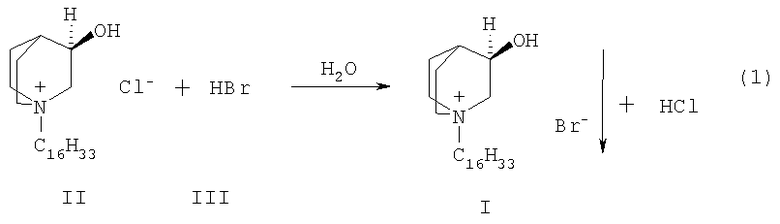
или ее неорганической солью (IV) в воде при комнатной температуре по схемам 1 и 2.
Схема 2
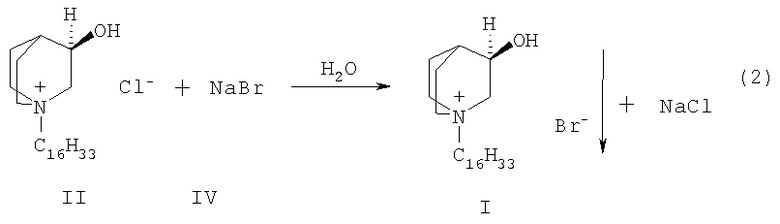
По окончании реакции продукт I отфильтровывают и очищают перекристаллизацией.
Необходимый для получения продукта I по схемам 1 и 2 хлорид 1-гексадецил-R(-)-3-окси-1-азониабицикло[2.2.2]октана (II) получают кватернизацией R(-)-1-азабицикло[2.2.2]октан-3-ола (V) хлористым цетилом (IV) по схеме 3
Схема 3
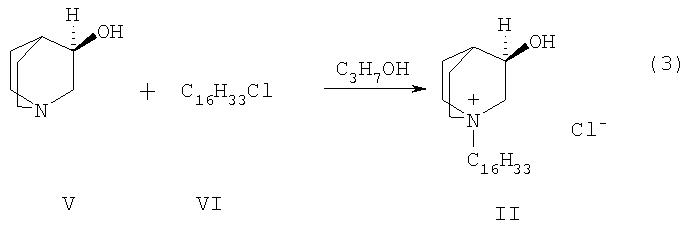
при нагревании в органическом растворителе (например, в изопропаноле или этаноле). По окончании реакции продукт II отфильтровывают и очищают перекристаллизацией.
Бромид 1-гексадецил-R(-)-3-окси-1-азониабицикло[2.2.2]октана (I) имеет R-абсолютную конфигурацию хирального центра, и поэтому исходным веществом для его получения является R(-)-1-азабицикло[2.2.2]октан-3-ол (V).
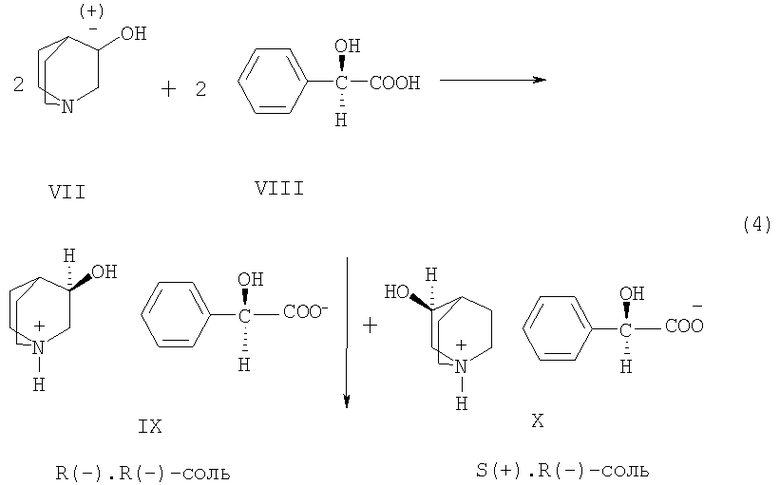
Исходное вещество - R(-)-1-азабицикло[2.2.2]октан-3-ол (V) выделяют при расщеплении RS(±)-1-азабицикло[2.2.2]октан-3-ола (VII) через диастереомерные соли с хиральной кислотой (например, с R(-)- или S(+)-энантиомерами миндальной кислоты) в органическом растворителе (например, в ацетоне или метилэтилкетоне). При использовании для расщепления RS(±)-1-азабицикло[2.2.2]октан-3-ола (VII) в качестве хирального расщепляющего реагента кислого характера R(-)-миндальной кислоты (VIII) по схеме 4 происходит преимущественная кристаллизация R(-)·R(-) - диастереомерной соли (IX), которую отфильтровывают и очищают от второй S(+)·R(-)-диастереомерной соли (X) кристаллизацией.
Схема 4
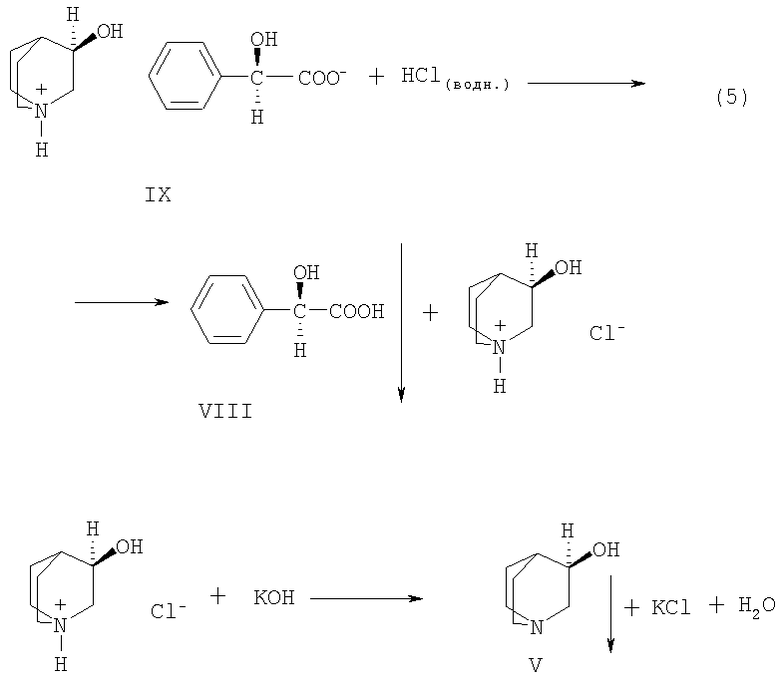
Разложение диастереомерных солей производится в следующем порядке (схема 5). В начале из водного раствора диастереомерной соли действием разбавленной соляной кислоты регенерируют хиральный реагент (VIII), извлекая его эфиром. Затем из водного кислого раствора действием твердого едкого кали выделяют R(-)-энантиомер 1-азабицикло[2.2.2]октан-3-ола (V), который отфильтровывают и очищают перекристаллизацией.
Схема 5
Используемые для получения бромида 1-гексадецил-R(-)-3-окси-1-азониабицикло[2.2.2]октана (I) RS(±)-3-азабицикло[2.2.2]октан-3-ол, хлористый гексадецил, R(-)- и S(+)-миндальные кислоты, бромистоводородная кислота и ее неорганические соли являются доступными реагентами органического синтеза.
Следует отметить, что так как хлористый гексадецил более доступен, чем бромистый гексадецил, предлагаемый способ получения бромида 1-гексадецил- R(-)-3-окси-1-азониабицикло[2.2.2]октана (I) более экономически выгоден, R(-)-3-окси-1-азониабицикло[2.2.2]октана (I) более экономически выгоден, чем способ получения вещества I прямым алкилированием R(-)-1-азабицикло[2.2.2]октан-3-ола бромистым гексадецилом.
Бромид 1-гексадецил-R(-)-3-окси-1-азониабицикло[2.2.2]октана (I) представляет собой мелкокристаллическое химически и оптически стабильное вещество с температурой плавления Tпл=228-230°С и удельным вращением 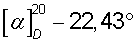 (с 1.5, 50% С2Н5ОН),
(с 1.5, 50% С2Н5ОН), 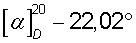 (с 1.5, С5Н5-СН3ОН, 1:1). Вещество растворимо в воде, метаноле, этаноле, хлороформе, пиридине, диметилсульфоксиде.
(с 1.5, С5Н5-СН3ОН, 1:1). Вещество растворимо в воде, метаноле, этаноле, хлороформе, пиридине, диметилсульфоксиде.
Пример 1. Бромид 1-гексадецил-R(-)-3-окси-1-азониабицикло[2.2.2]октана.
К раствору 7,8 г (0,02 моля) хлорида 1-гексадецил-R(-)-3-окси-1-азониабицикло[2.2.2]октана в 50 мл воды добавляют раствор 2,6 г (0,025 моля) бромида натрия в 25 мл воды. Происходит быстрое выпадение белого осадка, который отфильтровывают, промывают водой, сушат и перекристаллизовывают из воды, а затем из изопропанола. Получают 7,8 г (90,2%) бромида 1-гексадецил-R(-)-3-окси-1-азониабицикло[2.2.2]октана в виде мелкокристаллического вещества с Тпл 229,1°С, 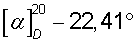 (с 1.5, 50% С2Н5ОН),
(с 1.5, 50% С2Н5ОН), 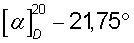 (с 1.5, 96% C2H5OH),
(с 1.5, 96% C2H5OH), 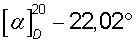 (с 1.5, С2Н5N-СН3ОН, 1:1).
(с 1.5, С2Н5N-СН3ОН, 1:1).
Найдено, %: С 64,05; H 11,18; N 3.06; Br 18.72. C23H46BrNO.
Вычислено, %: С 63,87; Н 30,72; N 3.24; Br 18,47.
Пример 2. Бромид 1-гексадецид-R(-)-3-окси-1-азониабицикло[2.2.2] октана.
К раствору 7,8 г (0,02 моля) хлорида 1-гексадецил-R(-)-3-окси-1-азониабицикло[2.2.2]октана в 50 мл воды добавляют раствор 18,9 мл 10%-ной бромистоводородной кислоты (0,025 моля). Происходит быстрое выпадение белого осадка, который отфильтровывают, промывают водой, сушат и перекристаллизовывают из воды, а затем из изопропанола. Получают 7,7 г (88,6%) бромида 1-гексадецил-R(-)-3-окси-1-азониабицикло[2.2.2]октана в виде мелкокристаллического вещества с Тпл 229,3°С, 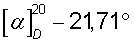 (с 1.5, 96% С2Н5ОН),
(с 1.5, 96% С2Н5ОН), 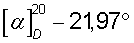 (с 1.5, С2Н5N-СН3ОН, 1:1).
(с 1.5, С2Н5N-СН3ОН, 1:1).
Найдено, %: С 64,01; H 11,04; N 3.10; Br 18.68. C23H46BrNO.
Вычислено, %: С 63,87; Н 10,72; N 3.24; Br 18.47.
Пример 3. Хлорид 1-гексадецил-R(-)-3-окси-1-азониабицикло[2.2.2] октана.
Раствор 12,7 г (0,1 моля) R(-)-1-азабицикло[2.2.2]октан-3-ола и 33,2 мл (28,7 г, 0,11 моля) хлористого цетила в 50 мл изопропанола нагревают в колбе с обратным холодильником в течение 24 ч. Осадок отфильтровывают, промывают ацетоном и сушат. Перекристаллизовывают из изопропанола. Получают 34,3 г (88,4%) хлорида 1-гексацедил-R(-)-3-окси-1-азабицикло[2.2.2]октана в виде белого порошка с Тпл 94,5°С и 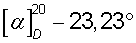 (с 2, H2O),
(с 2, H2O), 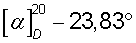 (с 2, С5Н5N-СН3ОН, 1:1).
(с 2, С5Н5N-СН3ОН, 1:1).
Найдено, %: С 70,98, Н 12,16; N 3,45; Cl 9,22; 9,30.
С23Н46 Cl NO.
Вычислено, %: С 71,19; Н 11,95; N 3,61; Cl 9,14.
Пример 4. R(-)- и S(+)-энантиомеры 1-азабицикло[2.2.2]октан-3-ола (расщепление RS(±)-1-азабицикло[2.2.2]октан-3-ола R(-)- и S(+)-миндальными кислотами).
К раствору 30,4 г (0,2 моля) R(-)- миндальной кислоты в 800 мл ацетона при перемешивании добавляют небольшими порциями 25,4 г (0,2 моля) RS(±)-1-азабицикло[2.2.2]октан-3-ола. Перемешивание продолжают до полного растворения 1-азабицикло[2.2.2]октан-3-ола. Через 12 ч образовавшийся осадок отфильтровывают, промывают ацетоном (2×30 мл) и сушат. Получают 27,8 г кристаллов с Тпл 111,8-112,3°С и 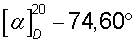 (с 3, Н2О), которые растирают в порошок и перекристаллизовывают из 1200 мл ацетона. Через 12 ч отфильтровывают 21,4 г (-)·(-) - соли с
(с 3, Н2О), которые растирают в порошок и перекристаллизовывают из 1200 мл ацетона. Через 12 ч отфильтровывают 21,4 г (-)·(-) - соли с 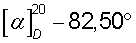 (с 3, H2O). Вторую кристаллизацию проводят из 1000 мл ацетона. Через 12 ч выделяют 19,0 г (68,0%) R(-)-манделата R(-)-1-азабицикло[2.2.2]октан-3-ола, Тпл =120,8°С,
(с 3, H2O). Вторую кристаллизацию проводят из 1000 мл ацетона. Через 12 ч выделяют 19,0 г (68,0%) R(-)-манделата R(-)-1-азабицикло[2.2.2]октан-3-ола, Тпл =120,8°С, 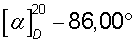 (с 3, Н2О). Последующая кристаллизация не приводит к изменению Тпл и [α]D соли.
(с 3, Н2О). Последующая кристаллизация не приводит к изменению Тпл и [α]D соли.
Найдено, %: С 65,11; Н 7,52; N 4,89. С7Н13NO·С7Н8O3.
Вычислено, %: С 64,54; Н 7,58; N 5,05.
К 50, 4 мл 6%-ной соляной кислоты (0,085 моля) при перемешивании и охлаждении ледяной водой небольшими порциями добавляют 19,0 г (0,068 моля) R(-)-манделата R(-)-1-азабицикло[2.2.2]октан-3-ола. После полного растворения соли R(-)-миндальную кислоту экстрагируют эфиром (5×30 мл).
Эфирные экстракты промывают насыщенным раствором хлорида натрия (2×10 мл). Эфир отгоняют. Остаток перекристаллизовывают из смеси гептан - ацетон (5:1). Получают 9,8 г R(-)-миндальной кислоты (регенерированный хиральный реагент), Тпл=133,2°С, 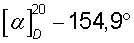 (с 3, Н2О).
(с 3, Н2О).
К водному слою, оставшемуся после отделения R(-)-миндальной кислоты, при перемешивании и охлаждении ледяной водой небольшими порциями добавляют 24,7 г (0,44 моля) твердого едкого кали. Всплывший осадок отфильтровывают, сушат и перекристаллизовывают из толуола. Получают 7,9 г (91,3%) R(-)-1-азабицикло[2.2.2]октан-3-ола, Тпл=222,3°С, 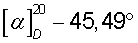 (с 2, 1 н. СН3СО2Н).
(с 2, 1 н. СН3СО2Н).
Первый ацетоновый маточный раствор, полученный после отделения 27,8 г (-)·(-)- соли, упаривают на водяной бане, и из остатка действием 6%-ной соляной кислоты выделяют 14,4 г R(-)-миндальной кислоты (регенерированный хиральный реагент), Тпл=133,4°С (из смеси гептан - ацетон (5:1)), 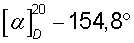 (с 3, H2O), a затем действием едкого кали 11,6 г 1-азабицикло[2.2.2]октан-3-ола, обогащенного S(+)-энантиомером, Тпл=222,5°С (из толуола),
(с 3, H2O), a затем действием едкого кали 11,6 г 1-азабицикло[2.2.2]октан-3-ола, обогащенного S(+)-энантиомером, Тпл=222,5°С (из толуола), 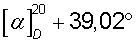 (с 2, 1 н. СН3СО2Н, о.ч. 85,7%).
(с 2, 1 н. СН3СО2Н, о.ч. 85,7%).
К раствору 13,9 г (0,091 моля) S(+)-миндальной кислоты в 800 мл ацетона при перемешивании добавляют небольшими порциями 11,6 г (0,091 моля 1-азабицикло[2.2.2]октан-3-ола, обогащенного S(+)-энантиомером с 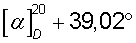 (с 2,1 н. СН3СО2Н). Через 12 ч образовавшийся осадок отфильтровывают, промывают ацетоном (2×20 мл) и сушат. Получают 21,9 г (+)·(+)- соли с
(с 2,1 н. СН3СО2Н). Через 12 ч образовавшийся осадок отфильтровывают, промывают ацетоном (2×20 мл) и сушат. Получают 21,9 г (+)·(+)- соли с 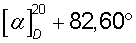 (с 3, Н2О). Последующая кристаллизация приводит к 19,4 г (82,0%) S(+)-манделата S(+)-1-азабицикло[2.2.2]октан-3-ола, Тпл=121,0°С,
(с 3, Н2О). Последующая кристаллизация приводит к 19,4 г (82,0%) S(+)-манделата S(+)-1-азабицикло[2.2.2]октан-3-ола, Тпл=121,0°С, 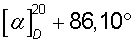 (с 3, Н2О).
(с 3, Н2О).
К 51,5 мл 6%-ной соляной кислоты (0,087 моля) при перемешивании и охлаждении ледяной водой небольшими порциями добавляют 19,4 г (0,069 моля) S(+)-манделата S(+)-1-азабицикло[2.2.2]октан-3-ола, S(+)-миндальную кислоту экстрагируют эфиром (5×30 мл). Экстракт промывают насыщенным раствором хлорида натрия (2×10 мл). Эфир отгоняют. Остаток перекристаллизовывают из смеси гептан - ацетон (5:1). Получают 10,0 г S(+)-миндальной кислоты (регенерированный хиральный реагент), Тпл=131,1°С, 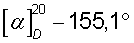 (c 3, H2O).
(c 3, H2O).
К водному слою, оставшемуся после отделения S(+)-миндальной кислоты, при перемешивании и охлаждении ледяной водой небольшими порциями добавляют 25,2 г (0,45 моля) твердого едкого кали. Всплывшее вещество отфильтровывают, сушат и перекристаллизовывают из толуола. Получают 8,1 г (91,7%) S(+)-1-азабицикло[2.2.2]октан-3-ола, Тпл=222,4°С, 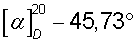 (с 2,1 н. СН3СО2Н).
(с 2,1 н. СН3СО2Н).
Таким образом, при расщеплении 25,4 г RS(±)-1-азабицикло[2.2.2]октан-3-ола получают 7,9 г (62,2%) R(-)-1-азабицикло[2.2.2]октан-3-ола и 8,1 г (63,8%) S(+)-1-азабицикло[2.2.2]октан-3-ола.
Цель патентуемой разработки: способ получения нового синтетического низкомолекулярного препарата, обладающего выраженным стимулирующим действием на систему противоопухолевого иммунитета, не уступающего, а по возможности превосходящего по эффективности современные отечественные и зарубежные препараты - иммуномодуляторы, которые являются природными высокомолекулярными биологически-активными веществами, полученными с помощью методов генной инженерии.
Была проведена оценка токсической и биологической активности вещества I.
Опенка испытаний вещества I на острую токсичность.
Результаты проведенных испытаний показали отсутствие половых различий в чувствительности животных к токсическому действию вещества I. Категории доз острой токсичности препарата для мышей и крыс представлены в таблице 1.
В соответствии с табуляцией классов токсичности (Саноцкий И. В. Методы определения токсичности и опасности химических веществ (токсикометрия), М., 1970, стр.16) вещество I относится к классу «малотоксичных» веществ.
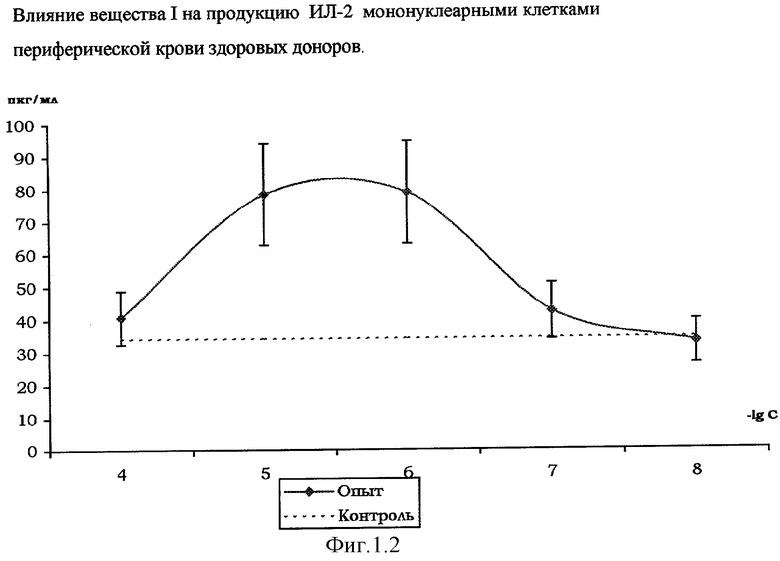
Влияние вещества I на продукцию цитокинов мононуклеарными клетками периферической крови здоровых доноров
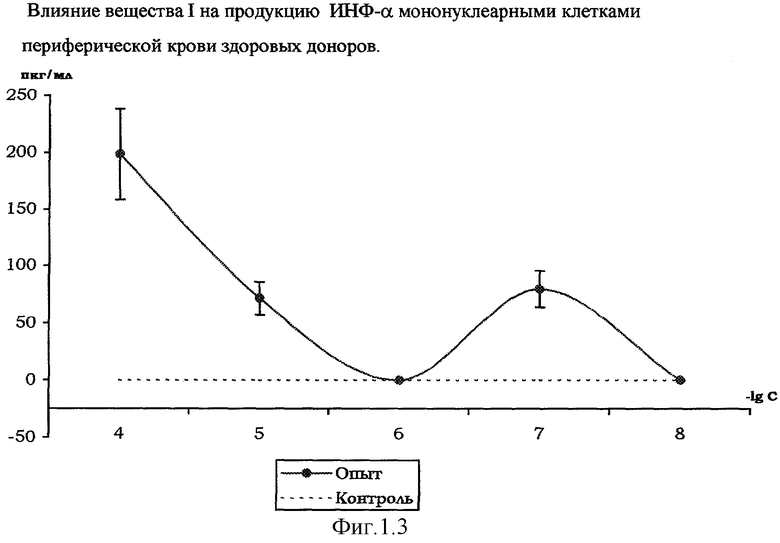
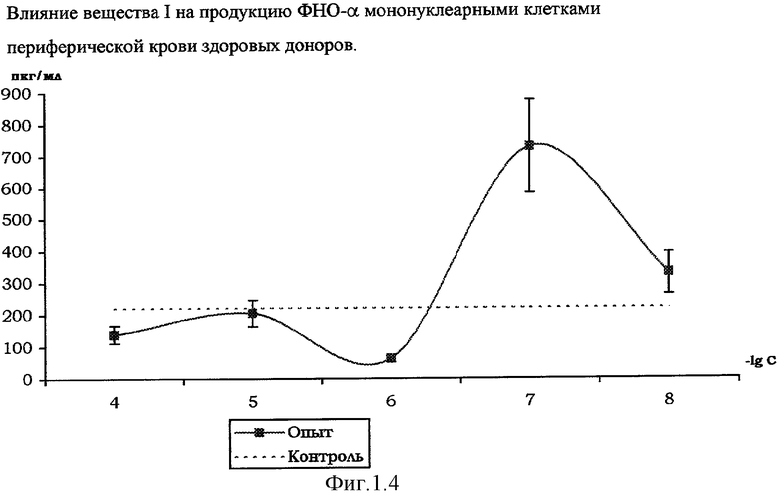
На фиг. 1.1., 1.2, 1.3 и 1.4 показано стимулирующее действие вещества I на продукцию цитокинов интерлейкина-1β (ИЛ-1β), интерферона-α (ИФН-α), интерлейкина-2 (ИЛ-2), фактора некроза опухоли (ФНО-α) мононуклеарными клетками здоровых доноров, выделенных из периферической крови согласно методике [Справочник. Лабораторные методы исследования в клинике. / Под ред. В.В.Меньшикова: Д.В.Белокриницкий «Методы клинической иммунологии». - М.: Медицина, 1987. - с.307].
Количественное определение цитокинов в супернатанте мононуклеарных клеток, инкубированных с растворами вещества I (диапазон концентраций 10-4-10-8 М), по методике [Шпакова А.С., Павлова К.С., Булычева Т.И. Клиническая лабораторная диагностика, №2, 2000. - с.20-23], проводили с использованием твердофазного иммуноферментного метода с применением пероксидазы хрена в качестве индикаторного фермента [«Иммунология» под ред. У.Пола в 3-х т. - М.: Мир, 1989, т.3, гл.28, с.260, Ed.W.Paul «Fundamental Immunology» - Raven Press, N.Y., 1984].
Соотношение клеток-мишеней и клеток-эффекторов 1:10; контроль - с добавлением физиологического раствора хлорида натрия (0,9% NaCl). Результаты, представленные на фиг.1.1, 1.2, 1.3, 1.4, свидетельствуют о стимулирующем влиянии вещества I на продукцию мононуклеарными клетками цитокинов ИЛ-1β, ИЛ-2, ИФН-α и ФНО-α, обладающих иммуномодулирующими и противоопухолевыми свойствами. Этот эффект выражен наиболее ярко при действующей концентрации вещества I в супернатанте в диапазоне 10-4-10-7 М.
Влияние вещества I на естественную киллерную активность мононуклеарных клеток периферической крови здоровых доноров.
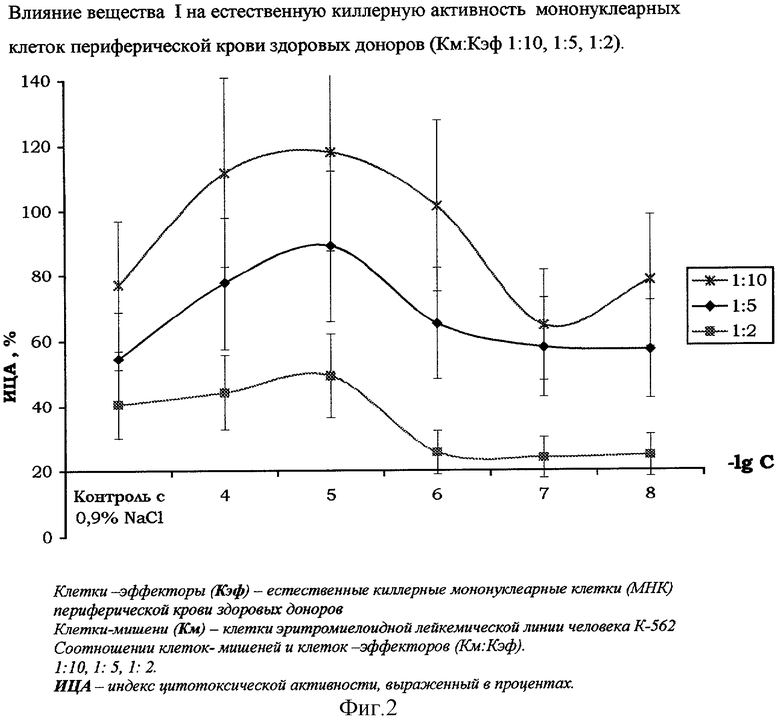
На фиг.2 показано стимулирующее влияние вещества I на естественную киллерную активность мононуклеарных клеток периферической крови здоровых доноров, выделенных согласно методике [«Справочник. Лабораторные методы исследования в клинике.» под ред. В.В.Меньшикова, Д.В.Белокриницкий «Методы клинической иммунологии» - М.: Медицина, 1987, с.307].
Количественное определение цитотоксической активности естественных киллерных клеток, инкубированных с растворами вещества I (диапазон концентраций 10-4-10-8 М) (контроль - с 0,9% NaCl), проводили с использованием МТТ-колориметрического теста по методике [Шпакова А.С., Павлова К.С., Булычева Т.И. Клиническая лабораторная диагностика, №2, 2000, с.20-23].
Наиболее оптимальные соотношения «опухолевая клетка / естественная киллерная клетка» - 1:10 и 1:5, при которых цитотоксическая активность МНК совместно инкубированных с тестируемым препаратом достигает наибольшего значения.
Максимальный, стабильно воспроизводимый эффект повышения противоопухолевой активности естественных киллеров отмечается при воздействии на МНК вещества I в диапазоне концентраций 10-4-10-6 М.
Вещество I не оказывает прямого цитотоксического воздействия на изолированные мононуклеарные клетки крови и опухолевые клетки.
Изучение противоопухолевой активности вещества I
Исследование противоопухолевого эффекта проводили на мышах линии СВА и гибридах F1 весом 20-25 г. Животные содержались согласно «Правилам доклинических испытаний фармакологических препаратов» (PD 64-126-91).
Клетки опухоли Эрлиха вводили внутрибрюшинно (ip), а меланомы В 16 - подкожно (sc) в дозе 2 млн./мышь. Опытные и контрольные группы состояли из 6-10 животных. Контрольной группе вводили физиологический раствор. Действие тестируемых образцов сравнивали с эффектом препарата Пролейкин, Голландия (ИЛ-2). Наблюдение осуществлялось в течение 1 мес. после трансплантации опухоли. Оценку состояния животных производили визуально. Динамику роста опухолевой массы оценивали по весу животных.
Изучение противоопухолевой активности вещества I в отношении опухоли Эрлиха проводили на мышах линии СВА в дозе 0,05 мг/кг, а Пролейкин в дозе 10 000 МЕ/мышь. Тестируемые вещества вводили за 3-е сут. до и на 1, 3, 5, 7, 10, 12, 14, 15, 17, 18 и 20 сут. после трансплантации опухоли. В контрольной группе на 15-е сут. осталась жива одна особь из 6. В группе мышей, получавших вещество I в указанной дозе, погибло 3 из 7 мышей. Среди животных, получавших Пролейкин, к 20 сут. погибло 2 из 6 особей.
Динамика роста опухоли у животных, леченных препаратом Пролейкин и веществом I, была достоверно меньше по сравнению с контрольной группой.
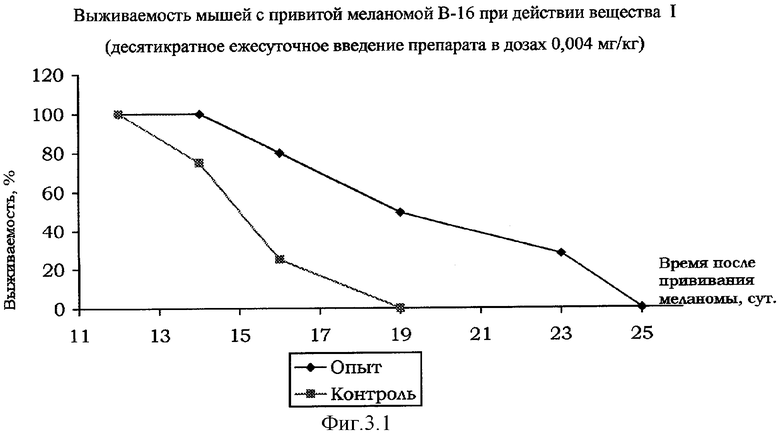
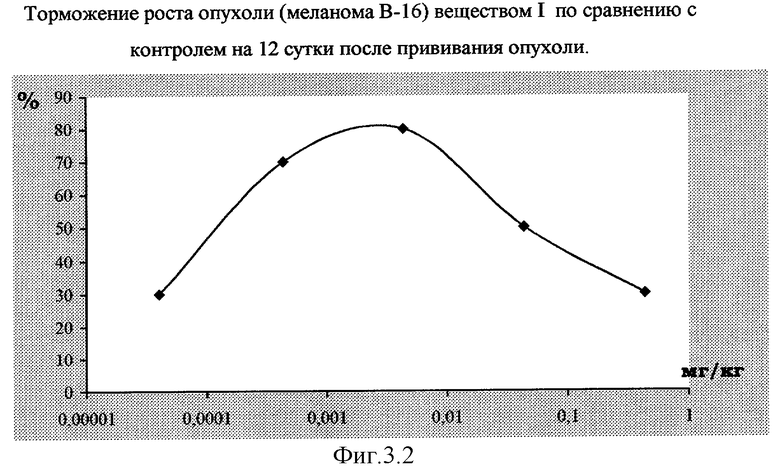
Вещество I оказывало тормозящее влияние на динамику роста опухоли меланомы В-16 у мышей гибридов F1 и увеличивал продолжительность их жизни. В частности, в дозе 0,005 мг/кг отмечено торможение опухолевого роста на 80%. Гибель животных в контрольной группе наступала на 19 сут., в то время как мыши, получавшие вещество I в указанной дозе, оставались живы до 25 сут. (см. фиг.3.1 и 3.2).
Таким образом, вещество I в дозах 0,05-0,005 мг/кг оказывает сходное цитостатическое действие по сравнению с препаратом Пролейкин при испытании на мышах с привитыми опухолями и вызывает стимуляцию противоопухолевого иммунитета.
Противоопухолевую активность также изучали на мышах-самцах линии СВА, которым подкожно перевивали аденокарциному яичников СаО-1. Опухоль была получена на потомстве мышей-самок линии СВА, которым во время беременности вводили эстрогены. Опухоль по гистологическому строению, клиническому течению и даже антигенному строению близка к раку яичника человека (БЭБиМ. - 2000 г., N 129, стр.456-459). Опухолевые клетки перевивали в количестве 1 млн. клеток / мышь.
Лечение осуществляли по схеме.
Мышам (30 штук) через 24 часа после перевивки опухолевых клеток начинали вводить разведенное в физиологическом растворе вещество I подкожно в 0.2 мл в нечетные дни (1-й, 3-й, 5-й и т.д.). Всего 7 введений. В контрольной группе животным вводили в этом же режиме физиологический раствор (растворитель препарата) (20 штук). Препарат вводили в трех дозах: 0,005 мг/кг, 0,05 мг/кг, 0,5 мг/кг.
Оценку действия препарата на рост опухоли проводили по регистрации различий в скорости роста опухоли. Расчет объема опухоли осуществляли по формуле
V=ав2(усл.ед).
Объем опухоли измеряли на 10, 12 и 15 дни после перевивки. Результаты исследований представлены в таблице 3.
2 - измерения объема опухали проводили на 10 и 15 дни после трансплантации.
Вещество I замедляет рост аденокарциномы яичников СаО-1. Торможение роста опухоли на 10-й день измерения составило 42%, 45%, 52%, на 12-й день 43%, 49%, 45%, а на 15-й день 32%, 42%, 40% для режимов 0,005 мг/кг, 0,05 мг/кг, 0,5 мг/кг соответственно. Данный эффект является пограничным эффектом для цитостатиков. Токсического действия препарата не обнаружено.
Приведенные выше примеры свидетельствуют о выраженной противоопухолевой активности вещества I.
Изучение влияния вещества I на фагоцитарную активность нейтрофильных лейкопитов крови здоровых доноров.
Данное исследование проводилось в 2 этапа: изучение влияния препарата на бактерицидную активность нейтрофилов и воздействие вещества I на способность нейтрофилов к захвату частиц латекса.
Для выделения нейтрофилов из венозной крови здорового донора получали лейкоконцентрат по методике [Медицинские лабораторные технологии и диагностика. Справочник. Медицинские лабораторные технологии / Под редакцией профессора А.И.Карпищенко. - Санкт -Петербург: Интермедика, 2002. - 408 с.]. Его разводили физиологическим раствором (рН=7,2) до концентрации 5×104 лейкоцитарных клеток в 1 мкл. Полученную суспензию по 180 мкл разливали в лунки 24-луночной плашки Falcon, получая, таким образом, 4 параллельных ряда по 6 лунок. Затем в лунки добавляли вещество I в различной концентрации действующего вещества (10-3-10-7 М) по 20 мкл, в последние в ряду лунки вносили 0,9% раствора хлорида натрия в качестве контроля.
Для изучения бактерицидной активности клеток вносили во все лунки по 10 мкл взвеси суточной агаровой дрожжевой культуры Saccharomyces cerevisiae (2×1011 кл/мл). Описанные манипуляции проводились с соблюдением условий стерильности.
Планшет с клетками термостатировали в течение 6 часов при 37°С. Далее удаляли пипеткой супернатант из лунок, из осадка готовили тонкие мазки, которые фиксировали в смеси Никифорова (5-10 мин) и окрашивали по Романовскому - Гимзе [В.С.Ронин, Г.М.Старобинец, Н.Л.Утевский / Руководство к практическим занятиям по методам клинических лабораторных исследований. - М.: Медицина, 1977, 335 с.].
Учет результатов проводили следующим образом: при микроскопировании окрашенных мазков учитывают 100 нейтрофилов, в которых подсчитывают количество клеток с признаками фагоцитоза.
Поглотительную способность фагоцитов оценивают с помощью фагоцитарного показателя. Фагоцитарный показатель (ФП) - процент фагоцитов из числа сосчитанных нейтрофилов. Результаты исследований приведены в таблице 4.
Из данных таблицы 4 следует, что совместная инкубация лейкоцитов с веществом I достоверно повышает способность нейтрофилов к поглощению микроорганизмов по сравнению с контролем.
Кроме того, было проведено исследование влияния изучаемого препарата на способность нейтрофилов к захвату опсонизированных частиц латекса. Для этого в лунки с фагоцитами, активированными изучаемым препаратом, вносили по 10 мкл взвеси опсонизированных частиц латекса в физиологическом растворе (концентрация частиц составляла 5000 в 1 мл). Фагоциты инкубировали с латексом в течение 8 ч. Результаты проведенного теста представлены в таблице 5.
Из данных статистической обработки результатов таблиц 4 и 5 следует, что совместная инкубация лейкоцитов с веществом I в действующих концентрациях 10-4-10-5 М достоверно повышает фагоцитарную активность нейтрофилов, увеличивая ФП по сравнению с контролем.
Бактериостатическая активность вещества I
В проведенной серии экспериментов была исследована чувствительность к веществу I штаммов микроорганизмов, выделенных из патологического материала от больных (экссудат, транссудат, кровь, моча, содержимое толстого кишечника, раневое отделяемое, слизь из зева) в послеоперационный период, и с предметов, окружающих больного в этот период - из воздуха, с предметов ухода за больными, с перевязочного материала, смывы с рук (санитарная группа микроорганизмов).
Видовой состав используемых штаммов бактериальных культур определялся исходя из того, что до недавнего времени основной причиной возникновения инфекций у больных являлись грамотрицательные бактерии, в частности псевдомонады, кишечная палочка, а в настоящее время все возрастающую отрицательную роль играют грамположительные бактерии (мецитиллинрезистентные штаммы золотистого стафилококка, энтерококки и др.). Эти бактериальные штаммы характеризуются антибиотикорезистентностью к широкому спектру химиопрепаратов.
Бактериостатическое воздействие вещества I на рост штаммов микроорганизмов определяли согласно луночно-диффузной методике [В.S.Reisner, Gl. Woods, R.В.Thomson - Specium Processing in Manual of Clinical Microbiology - Washington, 1999, 64-104; Сидоренко С.В., Колупаев В.Е. - Антибиотикограмма: Диско-диффузионный метод. Интерпретация результатов. - 1999]
+ штамм, умеренно чувствительный к действию тестируемого препарата
- штамм, устойчивый к действию тестируемого препарата
Вещество I характеризуется высокой бактериостатической активностью и широким спектром действия по отношению к большинству исследованных штаммов микроорганизмов.
Антитромбоцитагрегирующее действие вещества I
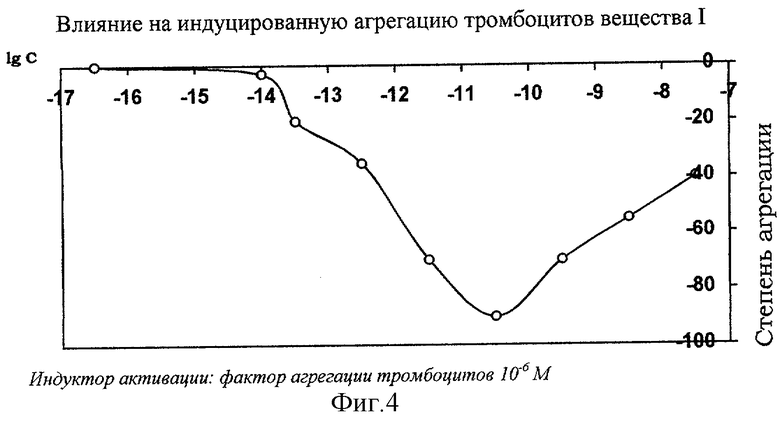
Вещество I оказывает активное антитромбоцитагрегирующее действие. Оно снижает агрегацию, вызываемую адреналином, АДФ и практически на 100% тормозит агрегацию, индуцируемую фактором агрегации тромбоцитов (ФАТ) и тромбином (см. фиг.4). Индекс антитромбоцитагрегирующей активности вещества I по тромбину и ФАТ равен 1×10-11 М, что относит препарат к разряду активных антагонистов ФАТ.
Таким образом, к преимуществам вещества I можно отнести высокую иммуномодулирующую и противоопухолевую активность, бактерицидное и антиагрегантное действие, низкую токсичность, высокую стабильность в водных растворах, простую технологию получения.
| название | год | авторы | номер документа |
|---|---|---|---|
| БРОМИД 1-ГЕКСАДЕЦИЛ-R-(-)-3-ОКСИ-1-АЗОНИАБИЦИКЛО[2.2.2]ОКТАНА - ИММУНОМОДУЛЯТОР С ПРОТИВООПУХОЛЕВЫМИ, БАКТЕРИОСТАТИЧЕСКИМИ И АНТИАГРЕГАНТНЫМИ СВОЙСТВАМИ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2005 |
|
RU2296761C2 |
| ХИНУКЛИДИНОВЫЕ ПРОИЗВОДНЫЕ (ГЕТЕРО)АРИЛЦИКЛОГЕПТАНКАРБОНОВОЙ КИСЛОТЫ В КАЧЕСТВЕ АНТАГОНИСТОВ МУСКАРИНОВЫХ РЕЦЕПТОРОВ | 2007 |
|
RU2456286C2 |
| КАРБАМАТЫ ХИНУКЛИДИНА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2001 |
|
RU2296762C2 |
| ГЕМИНАПАДИЗИЛАТ 5-(2-{[6-(2,2-ДИФТОР-2-ФЕНИЛЭТОКСИ)ГЕКСИЛ]АМИНО}-1-ГИДРОКСИЭТИЛ)-8-ГИДРОКСИХИНОЛИН-2(1H)-ОНА КАК АГОНИСТ β2 АДРЕНЕРГИЧЕСКОГО РЕЦЕПТОРА | 2008 |
|
RU2495029C2 |
| СПОСОБ ПОЛУЧЕНИЯ 3(R)-(2-ГИДРОКСИ-2,2-ДИТИЕН-2-ИЛАЦЕТОКСИ)-1-(3-ФЕНОКСИПРОПИЛ)-1-АЗОНИАБИЦИКЛО[2.2.2]ОКТАНБРОМИДА | 2007 |
|
RU2439070C2 |
| АЗА-КОЛЬЦЕВОЕ СОЕДИНЕНИЕ С ВНУТРЕННИМ МОСТИКОМ | 2008 |
|
RU2441868C2 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ВИРУЛИЦИДНЫМ, БАКТЕРИЦИДНЫМ И ДЕЗИНФИЦИРУЮЩИМ ДЕЙСТВИЕМ | 2009 |
|
RU2403042C1 |
| Хинуклидиновые эфиры 1-азагетероциклилуксусной кислоты в качестве антимускариновых средств, способ их получения и их лекарственные композиции | 2012 |
|
RU2628082C2 |
| ПРОИЗВОДНЫЕ ХИНУКЛИДИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2001 |
|
RU2282629C2 |
| (2S,3R)-N-(2-((3-ПИРИДИНИЛ)МЕТИЛ)-1-АЗАБИЦИКЛО[2.2.2]ОКТ-3-ИЛ)БЕНЗОФУРАН-2-КАРБОКСАМИД, НОВЫЕ СОЛЕВЫЕ ФОРМЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2008 |
|
RU2476220C2 |
В настоящем изобретении описывается способ получения бромида 1-гексадецил-R(-)-3-окси-1-азониабицикло[2.2.2]октана, представленного следующей формулой:
заключающийся в том, что хлорид 1-гексадецил-R(-)-3-окси-1-азониабицикло[2.2.2]октана вводят в реакцию ионного обмена с бромистоводородной кислотой или ее неорганической солью (например, бромидом натрия или бромидом калия) в воде. Бромид 1-гексадецил-R(-)-3-окси-1-азониабицикло[2.2.2]октана является иммунотропным средством, которое оказывает многостороннее влияние на иммунный статус человека, проявляя при этом противоопухолевое, бактериостатическое и антиагрегантное действия. Целью настоящего изобретения является способ получения нового синтетического низкомолекулярного препарата, обладающего выраженным стимулирующим действием на систему противоопухолевого иммунитета, не уступающего, а по возможности превосходящего по эффективности современные отечественные и зарубежные препараты - иммуномодуляторы, которые являются природными высокомолекулярными биологически активными веществами и которые получают с помощью методов генной инженерии. 8 ил., 6 табл.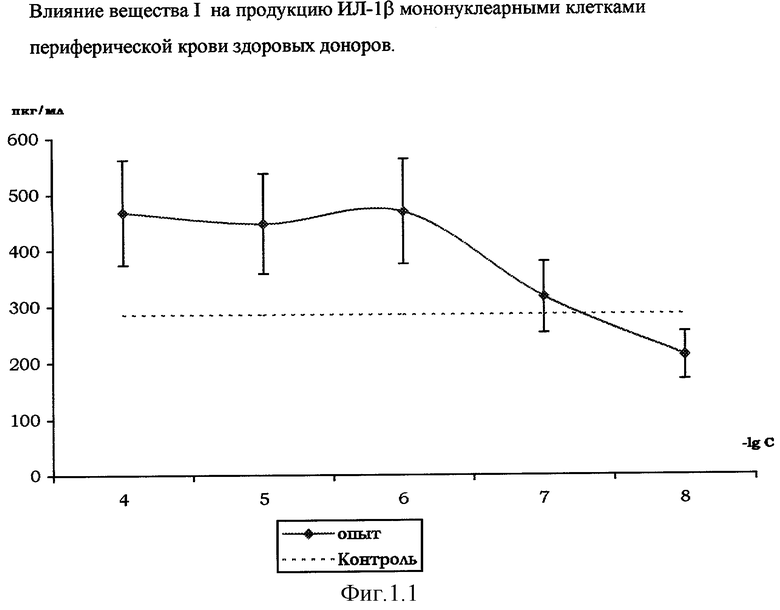
Способ получения бромида 1-гексадецил-R(-)-3-окси-1-азониабицикло[2.2.2]октана,
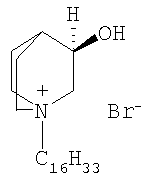
заключающийся в том, что хлорид 1-гексадецил-R(-)-3-окси-1-азониабицикло[2.2.2]октана вводят в реакцию ионного обмена с бромистоводородной кислотой или ее неорганической солью (например, бромидом натрия или бромидом калия) в воде, образующийся продукт фильтруют и очищают перекристаллизацией.
| Burkin A.A., Zoryan V.G., "Immunochemical simulation of ligand-receptor relationships III | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| СПОСОБ СПЕКТРАЛЬНОЙ СЕНСИБИЛИЗАЦИИ ОСОБОМЕЛКОЗЕРНИСТЫХ БРОМИОДСЕРЕБРЯНЫХ ФОТОГРАФИЧЕСКИХ ЭМУЛЬСИЙ ДЛЯ АМПЛИТУДНО-ФАЗОВЫХ ГОЛОГРАММ | 1987 |
|
RU2035761C1 |
| ИММУНОМОДУЛЯТОР | 1993 |
|
RU2108100C1 |
| Разъемное профилировочное кольцо к литейной форме для отливки калиброванных прокатных валков | 1988 |
|
SU1532196A1 |
| БРОМИД L-(-)-ЭНАНТИОМЕРА(ЭНДО,СИН)-(-)-3-(3-ОКСИ-1-ОКСО-2-ФЕНИЛПРОПОКСИ)-8-МЕТИЛ- 8-(1-МЕТИЛЭТИЛ)-8-АЗОНИ-АБИЦИКЛО[3.2.1]ОКТАНА С ЧИСТОТОЙ 90-100% И ИНГАЛЯЦИОННЫЙ ПРЕПАРАТ ДЛЯ ИНГИБИРОВАНИЯ БРОНХОСПАЗМА, ВЫЗВАННОГО АЦЕТИЛХОЛИНОМ | 1996 |
|
RU2171258C2 |
Авторы
Даты
2008-04-10—Публикация
2005-08-19—Подача