Настоящее изобретение относится к новым пиридилцианогуанидиновым пролекарствам и к их включению в фармацевтические композиции, а также к их применению для получения лекарственных препаратов.
Первоначально было установлено, что пиридилцианогуанидины, такие как пинацидил (N-1,2,2-триметилпропил-N'-циано-N"-(4-пиридил)гуанидин), способны открывать калиевые каналы, поэтому впоследствии они разрабатывались как гипотензивные агенты. Замещение боковых цепей пинацидила более длинными арилсодержащими боковыми цепями вызывает потерю гипотензивной активности, однако, с другой стороны, было установлено, что такие соединения проявляют противоопухолевую активность при пероральном введении на модели крыс, имеющих опухоли асцита Йошиды (Yoshida).
Были описаны различные классы пиридилцианогуанидинов с антипролиферативной активностью, например, в ЕР 660823, WO 98/54141, WO 98/54143, WO 98/54144, WO 98/54145, WO 00/61559 и WO 00/61561. Связи структура-активность (SAR) таких соединений описаны С. Schou et al., Bioorganic and Medicinal Chemistry Letters 7(24), 1997, pp. 3095-3100, при этом антипролиферативное действие ряда пиридилцианогуанидинов исследовали in vitro на различных клеточных линиях рака легких и молочной железы человека, а также на нормальных фибробластах человека. Данные соединения также исследовали in vivo на голых мышах с ксенотрансплантатом раковой опухоли легких человека. На основании анализа SAR, благодаря высокой антипролиферативной активности in vitro и потенциальной противоопухолевой активности на модели голых мышей, было выбрано конкретное соединение (N-(6-(4-хлорфеноксигексил)-N'-циано-N"-(4-пиридил)гуанидин).
P-J.V. Hjarnaa et al., Cancer Res. 59, 1999, pp.5751-5757, описывают результаты дальнейшего исследования соединения N-(6-(4-хлорфенокси)гексил)-N'-циано-N"-(4-пиридил)гуанидин в тестах in vitro и in vivo. Указанное соединение проявляет эффективность in vitro, сравнимую с эффективностью используемых для сравнения цитостатических агентов даунорубицин и паклитаксель, оказывая при этом существенно более низкое действие на нормальные эндотелиальные клетки человека. В тестах in vivo с использованием голых мышей с трансплантированными клетками опухоли человека данное соединение проявляет существенную противоопухолевую активность также против опухолевых клеток, резистентных к известным противораковым лекарственным препаратам, таким как паклитаксель.
Краткое описание изобретения
В то время как пиридилцианогуанидины, как указано выше, представляют собой многообещающие противоопухолевые агенты с чрезвычайно интересным профилем активности, они являются высоколипофильными и, следовательно, труднорастворимыми соединениями, и, как таковые, в целом могут быть использованы только для перорального введения. Однако многие раковые пациенты в результате своего заболевания находятся в сильно ослабленном состоянии, что вызывает проблемы с пероральным введением лекарственных препаратов.
Поэтому задачей настоящего изобретения является разработка пиридилцианогуанидинов в виде пролекарств с улучшенной растворимостью, которые могут быть включены в фармацевтические композиции, подходящие для парентерального введения, т.е. композиции, в которых пролекарство растворено в достаточном количестве таким образом, что при введении композиции оно может быть превращено в терапевтически эффективное количество активного соединения. Соединения в соответствии с настоящим изобретением обладают хорошей растворимостью в воде, даже при рН, приближающемся к физиологическому рН, что делает их идеальными для парентерального введения.
Более того, было установлено, что пиридилцианогуанидиновые пролекарства в соответствии с данным изобретением имеют улучшенную всасываемость в желудочно-кишечном тракте при пероральном введении. Следовательно, другой задачей данного изобретения является разработка пероральных составов пиридилцианогуанидинов в качестве пролекарств с улучшенной биодоступностью.
Соответственно, настоящее изобретение относится к соединению общей формулы I
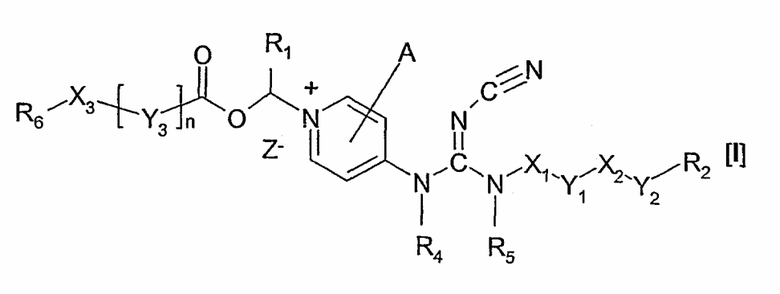
где Х1 представляет собой прямолинейный, разветвленный и/или циклический углеводородный дирадикал, необязательно замещенный одним или более заместителями, такими как гидрокси, галоген, нитро, амино или циано;
Х2 представляет собой связь; прямолинейный, разветвленный и/или циклический углеводородный дирадикал, необязательно замещенный одним или более заместителями, такими как гидрокси, галоген, амино, нитро, циано, аминосульфонил, алкилсульфониламино, алкилкарбонил, формил, аминокарбонил или алкилкарбониламино; дирадикал гетероарилена или неароматического гетероциклического углеводорода, каждый из которых необязательно замещен одним или более прямолинейными, разветвленными и/или циклическими неароматическими углеводородными радикалами, гидроксилом, галогеном, нитро, амино, циано, аминосульфонилом, алкилсульфониламино, алкилкарбонилом, формилом, аминокарбонилом или алкилкарбониламино;
Х3 представляет собой прямолинейный, разветвленный и/или циклический углеводородный дирадикал, необязательно замещенный одним или более заместителями, выбранными из группы, состоящей из гидрокси, галогена, нитро, амино, циано, аминосульфонила, алкилсульфониламино, алкилкарбонила, формила, аминокарбонила или алкилкарбониламино; при условии, что когда R6 представляет собой -NH2, Х3 включает пять или более атомов углерода; а также при условии, что когда n равно 0, а R6 представляет собой гетероциклическое кольцо или кольцевую систему с 3-10 кольцевыми атомами, в которой, по меньшей мере, 1 атом кольца представляет собой алифатический амин, Х3 также может представлять собой связь;
Y1 представляет собой связь, О, S, S(O), S(O)2, C(O), NH-C(O) или C(O)-NH;
Y2 представляет собой связь, дирадикал простого эфира (R'-O-R"), дирадикал амина (R'-N-R"), O, S, S(O), S(O)2, C(O), NH-C(O), C(O)-NH, SO2-N(R') или N(R')-SO2, где R' и R" независимо представляют собой прямолинейные или разветвленные углеводородные дирадикалы, содержащие до 4 атомов углерода;
Y3 представляет собой О;
R1 представляет собой водород или прямолинейный, разветвленный и/или циклический алкил, необязательно замещенный фенилом; или ароматический углеводородный радикал;
R2 представляет собой водород либо арил или гетероарил, необязательно замещенные одним или более заместителями, выбранными из группы, состоящей из галогена, трифторметила, гидрокси, С1-4алкокси, нитро, циано, С1-4гидроксиалкила или С1-4алкила, необязательно замещенных галогеном, гидрокси, циано или нитро; тетрагидропиранилокси, ди(С1-4алкокси)фосфиноилокси или С1-4алкоксикарбониламино;
каждый из R4 и R5 независимо представляет собой водород; прямолинейный, разветвленный и/или циклический углеводородный радикал, необязательно замещенный галогеном, гидроксилом, амино, нитро или циано;
R6 представляет собой аминогруппу, или гетероциклическое кольцо, или конденсированную кольцевую систему с 3-10 кольцевыми атомами, в которой, по меньшей мере, 1 атом кольца представляет собой алифатический амин;
А представляет собой водород, необязательно замещенный прямолинейный, разветвленный и/или циклический углеводородный радикал, гидрокси, галоген, нитро, циано, гетероарил, гетероаралкил или тиол;
n равно 0 или 1; и
Z- представляет собой фармацевтически приемлемый анион, такой как хлорид, бромид, иодид, сульфат, метансульфонат, п-толуолсульфонат, нитрат или фосфат.
Кроме того, данное изобретение относится к соединению формулы II, представляющему собой свободноосновную форму соединений формулы I, в которых R4 представляет собой водород
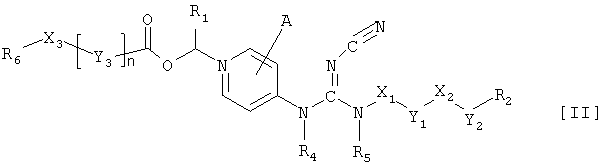
где A, R1, R2, R5, R6, X1, Х2, Х3, Y1, Y2, Y3 и n имеют вышеуказанные значения.
Подразумевается, что соединения в соответствии с настоящим изобретением включают любые таутомерные формы, их оптические изомеры или диастереоизомеры, либо в чистом виде, либо в виде их смесей. Также подразумевается, что данное изобретение включает фармацевтически приемлемые соли соединений формулы I или II.
При введении соединения формулы I или формулы II пациенту сложноэфирная или карбонатная группа R6-Х3-(Y3)n-С(О)O-CHR1- гидролизуется под воздействием ферментов, освобождая активное соединение формулы III
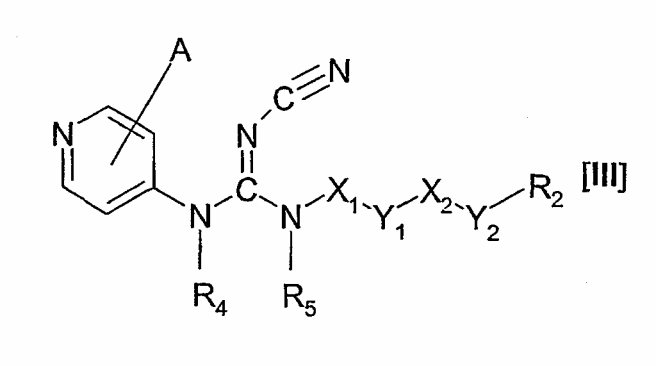
где А, R2, R4, R5, X1, X2, Y1 и Y2 имеют вышеуказанные значения, вместе с альдегидом R1СНО.
Подробное описание изобретения
Определения
В данном контексте термин "пролекарство" означает производное активного соединения, которое не проявляет или необязательно проявляет физиологическую активность активного соединения, но которое может быть подвергнуто ферментному расщеплению, такому как гидролиз in vivo, высвобождая активное соединение при введении пролекарства. В данном конкретном случае пролекарство включает активное соединение, которое само по себе является в высшей степени липофильным и имеет боковую цепь с преобладающими гидрофильными свойствами, придающими пролекарству повышенную растворимость, тем самым делая его более подходящим для парентерального введения в виде раствора или для перорального введения, обеспечивая улучшенную биодоступность. Более конкретно, гидрофильная боковая цепь, выбранная для соединений в соответствии с настоящим изобретением, включает сложноэфирную или карбонатную группу R6-Х3-(Y3)n-С(О)O-CHR1- (где R6, R1, X3, Y3 и n имеют вышеуказанные значения).
Термин "алкил" подразумевает одновалентный радикал, полученный из прямолинейного, разветвленного или циклического алкана в результате удаления атома водорода из любого атома углерода, предпочтительно включающего 1-8 атомов углерода. Данный термин включает подклассы первичного, вторичного и третичного алкила, такого как метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, изобутил, трет-бутил, изопентил, изогексил, циклогексил, циклопентил и циклопропил.
Термин "арил" означает радикалы карбоциклических ароматических колец, необязательно, конденсированных би-, три- или тетрациклических колец, в которых, по меньшей мере, одно кольцо является ароматическим, например, фенил, нафтил, инданил, инденил, 1,4-дигидронафтил, флуоренил или тетралинил.
Термин "гетероарил" означает радикалы гетероциклических ароматических колец, в частности, 5- или 6-членных колец с 1-3 гетероатомами, выбранными из О, S и N, либо необязательно конденсированные бициклические кольца, из которых, по меньшей мере, одно является ароматическим, с 1-4 гетероатомами, например, пирролил, фуранил, тиофенил, имидазолил, оксазолил, тиазолил, пиразолил, пиридил, пиримидил, пуринил, хинолинил, хроменил или карбазолил.
Термин "аралкил" означает ароматическое кольцо с алкильной боковой цепью, имеющей вышеуказанные значения, например бензил.
Термин "галоген" означает фтор, хлор, бром или йод.
Термин "аминосульфонил" означает радикал формулы -S(О)2NRa 2, где каждый из Ra независимо представляет собой водород или алкил, имеющий вышеуказанные значения.
Термин "алкилсульфониламино" означает радикал формулы -NRa 2-S(О)2-Rb, где каждый из Ra независимо представляет собой водород или алкил, имеющий вышеуказанные значения, a Rb независимо представляет собой алкил, имеющий вышеуказанные значения.
Термин "алкилкарбонил" означает радикал формулы -С(О)Rb, где Rb имеет вышеуказанные значения.
Термин "амино" означает радикал формулы -N(Ra)2, где каждый из Ra независимо представляет собой водород или алкил, имеющий указанные выше значения.
Термин "алкилкарбониламино" означает радикал формулы -NRaС(О)Rb, где Ra и Rb имеют вышеуказанные значения.
Термин "алкокси" означает радикал формулы ORb, где Rb имеет вышеуказанные значения.
Термин "алкоксикарбонил" означает радикал формулы -С(О)-ORb, где Rb имеет вышеуказанные значения.
Термин "аминоациламино" означает радикал формулы -NH-С(О)-Rс-NH2, где Rc представляет собой дирадикал, известный из любой натуральной аминокислоты, H2N-Rc-COOH или его энантиомер.
Термин "аминокарбонил" означает радикал формулы -С(О)-NRa 2, где каждый из Ra независимо представляет собой водород или алкил, имеющий вышеуказанные значения.
Термин "алкоксикарбониламино" означает радикал формулы -NRa-С(О)-ORb, где Ra и Rb имеют вышеуказанные значения.
Термин "углеводород(ный)" означает соединение, включающее только атомы водорода и углерода; оно может включать одну и более двойных или тройных связей углерод-углерод, а также циклические остатки в сочетании с разветвленными или линейными остатками. Указанный углеводород предпочтительно включает 1-18, например, 1-12 атомов углерода. Термин также может включать понятие "неароматический, гетероциклический", относящееся к насыщенным или частично насыщенным циклическим соединениям с 1-3 гетероатомами, выбранными из О, S или N, либо необязательно конденсированным бициклическим кольцам с 1-4 гетероатомами, таким как пирролидинил, 3-пирролинил, тетрагидрофуранил, тетрагидротиофенил, пиперидинил, пиперазинил.
Термин "гетероциклическое кольцо или конденсированная кольцевая система с 3-10 кольцевыми атомами, в которой, по меньшей мере, один кольцевой атом представляет собой алифатический амин" означает, что соединение включает радикалы, такие как пирролидинил, пиперидил, гексагидро-1Н-азапинил, имидазолидинил, пиперазинил, декагидроизохинолинил, октагидроизоиндолил, 1,2,3,4-тетрагидроизохинолинил, 2,3-дигидро-1Н-изоиндолил и морфолинил.
Термин "фармацевтически приемлемая соль" означает соли, полученные взаимодействием соединения формулы I или II, включающего основную группу, с подходящей неорганической или органической кислотой, например, хлористоводородной, бромистоводородной, йодистоводородной, серной, азотной, уксусной, фосфорной, молочной, малеиновой, фталевой, лимонной, пропионовой, бензойной, глутаровой, глюконовой, метансульфоновой, салициловой, янтарной, винной, толуолсульфоновой, сульфаниловой или фумаровой кислотой.
Предпочтительные варианты соединения формулы I или II
В предпочтительном варианте данного изобретения как Х2, так и Y1 представляют собой связи, при этом Х1 представляет собой прямолинейный, разветвленный или циклический, насыщенный или ненасыщенный углеводородный дирадикал с 4-20 атомами углерода; Y2 представляет собой О, S, C(O) или связь;
R2 представляет собой арил или гетероарил, необязательно замещенные одним или более заместителями, выбранными из группы, состоящей из галогена, трифторметила, гидрокси, С1-4алкокси, нитро, циано, С1-4гидроксиалкила или С1-4алкила, необязательно замещенных галогеном, гидрокси, циано или нитро; тетрагидропиранилокси, ди(С1-4алкокси)фосфиноилокси или С1-4алкоксикарбониламино;
Х3 представляет собой прямолинейный углеводородный дирадикал, включающий от 1 до 10 атомов углерода;
R6 представляет собой -NH2 или пиперидил, прикрепленный в положении 2, 3 или 4 к Х3, особенно в положении 3 или 4;
R1 представляет собой водород, прямолинейный или разветвленный С1-4алкил, аралкил или арил;
каждый из А, R4 и R5 представляет собой водород;
n равно 0 или 1; и
Z- представляет собой фармацевтически приемлемый анион, такой как хлорид, бромид, иодид, сульфат, метансульфонат, п-толуолсульфонат или нитрат.
В предпочтительном варианте соединений формулы I или II R2 представляет собой арил, в частности фенил, необязательно замещенный одним или более заместителями, выбранными из группы, состоящей из галогена, трифторметила, гидрокси, С1-4алкокси, нитро, циано, С1-4гидроксиалкила или С1-4алкила, необязательно замещенных галогеном, гидрокси, циано или нитро. Особенно предпочтительным заместителем является галоген, такой как хлор.
В предпочтительном варианте соединений формулы I или II Y1 представляет собой связь, а Y2 представляет собой О.
В дальнейшем предпочтительном варианте соединений формулы I или II Х1 представляет собой С4-12 углеводородный дирадикал, а Х2 представляет собой связь.
Примеры конкретных соединений формулы I включают:
гидрохлорид 1-[2-(4-пиперидил)этоксикарбонилоксиметил]-4-[N'-циано-N"-(6-(4-хлорфенокси)-1-гексил)-N-гуанидино]пиридинийхлорида;
гидрохлорид 1-[3-пиперидилметоксикарбонилоксиметил]-4-[N'-циано-N"-(6-(4-хлорфенокси)-1-гексил)-N-гуанидино]пиридинийхлорида;
гидрохлорид 1-[4-пиперидилметоксикарбонилоксиметил]-4-[N'-циано-N"-(6-(4-хлорфенокси)-1-гексил)-N-гуанидино]пиридинийхлорида;
гидрохлорид 1-[8-амино-1-октилоксикарбонилоксиметил]-4-[N'-циано-N"-(6-(4-хлорфенокси)-1-гексил)-N-гуанидино]пиридинийхлорида;
гидрохлорид 1-[4-пиперидилкарбонилоксиметил]-4-[N'-циано-N"-(6-(4-хлорфенокси)-1-гексил)-N-гуанидино]пиридинийхлорида.
Как указано выше, преимуществом пролекарственных форм цианогуанидинов в соответствии с настоящим изобретением является их повышенная растворимость по сравнению с растворимостью самих цианогуанидинов. Такая растворимость обусловлена, по меньшей мере, двумя факторами, т.е. положительным зарядом азота пиридина и гидрофильным характером пролекарственного остатка, т.е.
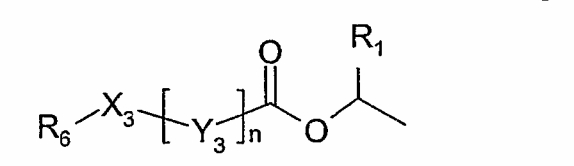
В целом, величина рКВ пиридинов составляет около 9. Это означает, что при повышении рН с кислотных значений, например, с 3 до физиологического рН, соединения в соответствии с настоящим изобретением превращаются из соединений формулы I в соответствующее свободное основание, т.е. в соединения формулы II. Таким образом, при физиологическом рН положительный заряд азота пиридина большей частью исчезает, что приводит к снижению растворимости соединений. Авторы полагают, что особое преимущество соединений в соответствии с настоящим изобретением заключается в том, что остаток пролекарства в R6 несет единицу заряда или, по меньшей мере, часть единицы заряда при физиологическом рН. Как указано выше, R6 включает остаток алифатического амина, при этом хорошо известно, что алифатические амины имеют величины рКВ в интервале 3-5 [Frenna, J. Chem. Soc. Perkin Trans. II, 1865, 1985], что позволяет предположить, что остаток амина в основном протонируется при физиологическом рН. Протонирование обеспечивает заряд, повышающий растворимость.
Более того, было установлено, что применение следующих соединений особенно целесообразно для получения соединений формулы I и II:
хлорметил 2-(1-(трет-бутоксикарбонил)-4-пиперидил)этилкарбонат;
хлорметил 1-(трет-бутоксикарбонил)-3-пиперидилметилкарбонат;
хлорметил 1-(трет-бутоксикарбонил)-4-пиперидилметилкарбонат;
йодметил 2-(1-(трет-бутоксикарбонил)-4-пиперидил)этилкарбонат;
йодметил 1-(трет-бутоксикарбонил)-3-пиперидилметилкарбонат;
йодметил 1-(трет-бутоксикарбонил)-4-пиперидилметилкарбонат;
хлорметил 8-(трет-бутоксикарбониламино)-1-октилкарбонат;
йодметил 8-(трет-бутоксикарбониламино)-1-октилкарбонат;
хлорметил N-трет-бутоксикарбонил-4-пиперидилкарбоксилат;
йодметил N-трет-бутоксикарбонил-4-пиперидилкарбоксилат;
йодид 1-[2-[1-(трет-бутоксикарбонил)-4-пиперидил]этоксикарбонилоксиметил]-4-[N'-циано-N"-(6-(4-хлорфенокси)-1-гексил)-N-гуанидино]пиридиния;
йодид 1-[1-(трет-бутоксикарбонил)-3-пиперидилметоксикарбонилоксиметил]-4-[N'-циано-N"-(6-(4-хлорфенокси)-1-гексил)-N-гуанидино]пиридиния;
йодид 1-[1-(трет-бутоксикарбонил)-4-пиперидилметоксикарбонилоксиметил]-4-[N'-циано-N"-(6-(4-хлорфенокси)-1-гексил)-N-гуанидино]пиридиния;
йодид 1-[8-(N-трет-бутоксикарбониламино)-1-октилоксикарбонилоксиметил]-4-[N'-циано-N"-(6-(4-хлорфенокси)-1-гексил)-N-гуанидино]пиридиния; и
йодид 1-[1-(трет-бутоксикарбонил)-4-пиперидилкарбонилоксиметил]-4-[N'-циано-N"-(6-(4-хлорфенокси)-1-гексил)-N-гуанидино]пиридиния.
Общие способы получения
Соединения формулы I могут быть получены взаимодействием соединения формулы III
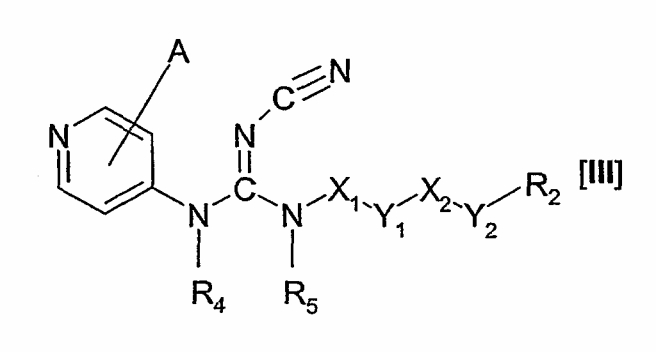
где А, R2, R4, R5, R6, X1, X2, Y1 и Y2 имеют значения, указанные в формуле I, с соединением формулы IV
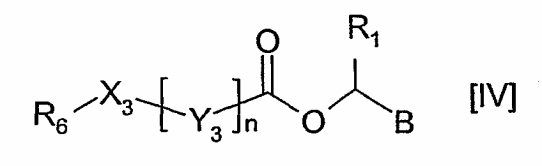
где R1, R6, X3, Y3 и n имеют вышеуказанные значения, а В представляет собой удаляемую группу, такую как Cl, Br или I. Кроме того, R6 и X3 могут необязательно содержать защитные группы.
Взаимодействие соединения формулы III с соединением формулы IV может быть осуществлено в свободной от растворителя среде либо в инертном растворителе, таком как ацетонитрил, при температуре от комнатной температуры до 150°С с получением соединения формулы I, необязательно после удаления защитных групп.
Соединения формулы IV известны из литературы или могут быть получены способами, хорошо известными специалистам в данной области техники.
Если n равно 1, соединения формулы IV могут быть получены взаимодействием соединения формулы V
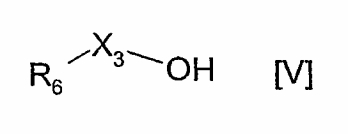
где R6 и Х3 имеют значения, указанные в формуле IV, с соединением формулы VI
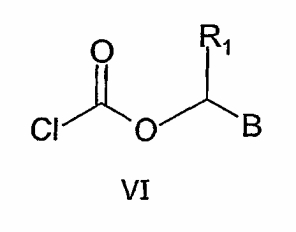
где R1 и В имеют вышеуказанные значения.
Взаимодействие соединения формулы V с соединением формулы VI может быть осуществлено при температуре от комнатной температуры до -70°С в инертном органическом растворителе, таком как дихлорметан, в присутствии подходящего основания, такого как пиридин.
Если n равно нулю, то соединения формулы IV, в которых В представляет собой хлор, могут быть получены взаимодействием соединения формулы VII
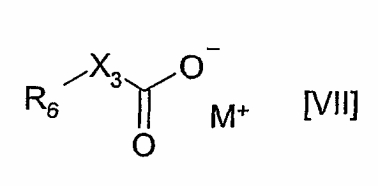
где R6 и Х3 имеют значения, указанные в формуле IV, а М+ представляет собой подходящий катион металла, например, катион щелочного металла, или ион третичного аммония, с соединением формулы VIII
Х-СН(R1)-Cl VIII
где R1 имеет вышеуказанные значения, а Х представляет собой йод, бром или хлорсульфонилокси.
Взаимодействие соединений формул VII и VIII может быть осуществлено в подходящем растворителе, таком как диметилформамид, при подходящей температуре, например, при комнатной температуре, в том случае, когда Х представляет собой йод или бром. Если Х представляет собой хлорсульфонилокси, то взаимодействие может быть осуществлено в условиях фазового переноса, как описано в Synthetic Communications 14, 857-864 (1984).
Соединения формулы IV, в которых В представляет собой хлор, могут быть превращены в соответствующие соединения, в которых В представляет собой йод, путем взаимодействия с иодидом натрия в ацетоне или ацетонитриле.
Соединения формул V, VI, VII, VIII либо известны из литературы, либо могут быть получены способами, хорошо известными специалистам в данной области техники.
Соединения формулы III известны из литературы и могут быть получены любым способом, описанным, например, в ЕР 660823, WO 98/54141, WO 98/54143, WO 98/54144, WO 98/54145, WO 00/61559 и WO 00/61561.
Соединение формулы I, при условии что R4 представляет собой водород, может быть превращено в соответствующее свободное основание формулы II обработкой раствора соединения формулы I в соответствующем инертном растворителе, например дихлорметане, подходящим основанием, например, водным бикарбонатом натрия. Свободное основание формулы II может быть вновь превращено в соль формулы I обработкой раствора соединения формулы II в соответствующем инертном растворителе, например дихлорметане, подходящей кислотой формулы ZH, где Z имеет вышеуказанные значения.
Фармацевтические композиции
Согласно другому аспекту данное изобретение относится к фармацевтическим составам, включающим соединения формулы I или II, предназначенным для лечения пролиферативных заболеваний. Составы в соответствии с настоящим изобретением, предназначенные для лечения как животных, так и людей, включают активные ингредиенты в сочетании с фармацевтически приемлемым носителем (носителями) и, необязательно, другим терапевтическим ингредиентом (ингредиентами). Носитель (носители) должны быть "приемлемыми" в смысле совместимости с другими ингредиентами составов и не причинять вреда их реципиенту.
Как правило, активный ингредиент включает 0,1-100 мас.% состава. Лекарственная доза обычно содержит от 0,07 мг до 1 г соединения формулы I или II.
Под термином "лекарственная доза" подразумевается стандартная, т.е. разовая доза, которая может быть введена пациенту и которая может быть легко использована и упакована, оставаясь физически и химически стойкой стандартной дозой, включающей либо активный ингредиент как таковой, либо его смесь с твердыми или жидкими фармацевтическими разбавителями или носителями.
Составы включают, например, дозы в форме, подходящей для перорального (включая пролонгированное или рассчитанное высвобождение), ректального, парентерального (включая подкожное, интраперитонеальное, внутримышечное, интраартикулярное и внутривенное), трансдермального, офтальмологического, местного, назального или трансбуккального введения.
Составы обычно могут быть представлены в форме разовой дозы и получены любым из способов, хорошо известных в области фармации, например, описанным Remington, The Science and Practice of Pharmacy, 20th ed., 2000. Все способы включают стадию смешивания активного ингредиента с носителем, содержащим один или несколько вспомогательных ингредиентов. В целом, составы получают, равномерно и тщательно смешивая активный ингредиент с жидким носителем или тонкоизмельченным твердым носителем либо с тем и другим, а затем, при необходимости, придавая продукту форму желаемого состава.
Составы в соответствии с настоящим изобретением, подходящие для перорального введения, могут иметь вид дискретных единиц, таких как капсулы, саше, таблетки, или лепешки, каждая из которых содержит заранее установленное количество активного ингредиента; вид порошка или гранул; вид раствора или суспензии в водной или безводной жидкости, такой как этанол или глицерин; либо вид эмульсии типа "масло-в-воде" или "вода-в-масле". Подобные масла могут представлять собой пищевые масла, такие как, например, хлопковое масло, кунжутное масло, кокосовое масло или арахисовое масло. Подходящие диспергирующие или суспендирующие агенты для водных суспензий включают синтетические или натуральные смолы, такие как трагакант, альгинат, акацию, декстран, карбоксиметилцеллюлозу натрия, желатин, метилцеллюлозу, гидроксипропилметилцеллюлозу, гидроксипропилцеллюлозу, карбомеры и поливинилпирролидон. Активные ингредиенты также могут быть введены в виде болюса, электуария или пасты.
Таблетка может быть получена прессованием или формованием активного ингредиента, необязательно с одним или более вспомогательными ингредиентами. Прессованные таблетки могут быть получены прессованием на соответствующей машине активного ингредиента (активных ингредиентов) в свободнотекущей форме, такой как порошок или гранулы, необязательно смешанного со связующим, таким как, например, лактоза, глюкоза, крахмал, желатин, смола акации, смола трагаканта, альгинат натрия, карбоксиметилцеллюлоза, метилцеллюлоза, гидроксипропилметилцеллюлоза, полиэтиленгликоль, воски и т.п.; смазывающего агента, такого как, например, олеат натрия, стеарат натрия, стеарат магния, бензоат натрия, ацетат натрия, хлорид натрия и т.п.; расщепляющего агента, такого как, например, крахмал, метилцеллюлоза, агар, бентонит, натрия кроскармеллоза, натриевый гликолят крахмала, кросповидон и т.п., или диспергирующего агента, такого как полисорбат 80. Формованные таблетки могут быть получены формованием на соответствующей машине смеси порошкообразного активного ингредиента и подходящего носителя, увлажненного инертным жидким разбавителем.
Составы для ректального введения могут иметь вид суппозиториев, в которых соединение в соответствии с настоящим изобретением смешано с низкоплавкими, растворимыми или нерастворимыми в воде твердыми веществами, такими как масло какао, гидрогенизированные растительные масла, полиэтиленгликоль или сложные эфиры жирных кислот полиэтиленгликолей, в то время как эликсиры могут быть получены с применением миристилпальмитата.
Составы, подходящие для парентерального введения, обычно включают стерильный маслянистый или водный препарат активного ингредиента, предпочтительно изотоничный с кровью реципиента, например, изотонический физиологический раствор, изотонический раствор глюкозы или буферный раствор. Состав может быть подвергнут соответствующей стерилизации, например, фильтрацией через задерживающий бактерии фильтр, добавлением к составу стерилизующего агента, облучением или нагреванием состава. Липосомальные составы, описанные, например, в Encyclopedia of Pharmaceutical Technology, vol.9, 1994, также подходят для парентерального введения.
Альтернативно соединение формулы I может иметь вид стерильного, твердого препарата, например лиофилизированного порошка, легко растворимого в стерильном растворителе непосредственно перед использованием.
Трансдермальные составы могут иметь вид пластыря или накладки.
Составы, подходящие для офтальмологического введения, могут иметь вид стерильного водного препарата активных ингредиентов, которые могут иметь микрокристаллическую форму, например, форму водной микрокристаллической суспензии. Для того чтобы сделать активный ингредиент пригодным для офтальмологического введения, могут быть также использованы липосомальные составы или биорасщепляемые полимерные системы, описанные, например, в Encyclopedia of Pharmaceutical Technology, vol.2, 1989.
Составы, подходящие для местного или офтальмологического введения, включают жидкие или полужидкие препараты, такие как линименты, лосьоны, гели, аппликации, эмульсии типа "масло-в-воде" или "вода-в-масле", такие как кремы, мази или пасты; либо растворы или суспензии, такие как капли.
Составы, пригодные для назального или трансбукального введения, включают порошок, автоматически подаваемые и распыляемые составы, такие как аэрозоли и пульверизаторы.
Помимо вышеуказанных ингредиентов составы соединения формулы I или II могут включать один или несколько дополнительных ингредиентов, таких как разбавители, буферы, вкусовые вещества, краситель, поверхностно-активные вещества, загустители, консерванты, например, метилгидроксибензоат (включая антиоксиданты), эмульгаторы и т.п.
При системном лечении с применением настоящего изобретения суточные вводимые дозы соединения I или II составляют 0,001-500 мг на килограмм массы тела, предпочтительно - 0,002-100 мг/кг массы тела млекопитающего, например, 0,003-20 мг/кг или от 0,003 до 5 мг/кг, что, как правило, соответствует суточной дозе для взрослого человека, составляющей от 0,01 до 37000 мг. Однако в настоящем изобретении также предусмотрены соединения и композиции, предназначенные для введения с более длительными интервалами, например, каждую неделю, каждые три недели или каждый месяц. При местном лечении дерматологических заболеваний применяют мази, кремы или лосьоны, содержащие 0,1-750 мг/г, предпочтительно - 0,1-500 мг/г, например, 0,1-200 мг/г соединения формулы I или II. При местном лечении в офтальмологии применяют мази, капли или гели, содержащие 0,1-750 мг/г, предпочтительно - 0,1-500 мг/г, например, 0,1-200 мг/г соединения формулы I или II. Композиции для перорального введения получают, предпочтительно, в виде таблеток, капсул или капель, содержащих 0,07-1000 мг, предпочтительно - 0,1-500 мг, соединения формулы I или II на лекарственную единицу.
Согласно предпочтительному варианту данное изобретение относится к фармацевтическим композициям, включающим соединение формулы I или II в сочетании с одним или более другими фармакологически активными соединениями, применяемыми для лечения пролиферативных заболеваний. Примеры соединений, применяемых для лечения пролиферативных заболеваний, которые могут быть использованы вместе с соединениями в соответствии с настоящим изобретением, включают производные S-триазина, такие как альтретамин; ферменты, такие как аспарагиназа; антибиотики, такие как блеомицин, дактиномицин, даунорубицин, доксорубицин, идарубицин, митомицин, эпирубицин и пликамицин; алкилирующие агенты, такие как бусульфан, карбоплатин, кармустин, хлорамбуцил, цисплатин, циклофосфамид, дакарбазин, ифосфамид, ломустин, меклоретамин, мелфалан, прокарбазин и тиотепа; антиметаболиты, такие как кладрибин, цитарабин, флоксуридин, флударабин, фторурацил, гидроксимочевина, меркаптопурин, метотрексат, гемцитабин, пентостатин и тиогуанин; антимитотические агенты, такие как этопозид, паклитаксель, тенипозид, винбластин, винорелбин и винкристин; гормональные вещества, например, ингибиторы ароматазы, такие как аминоглютетимид, кортикостероиды, такие как дексаметазон и преднизон, а также лютеинизирущего гормона, высвобождающий гормон (ЛГ-ВГ); антиэстрогены, такие как тамоксифен, форместан и летрозол; антиандрогены, такие как флутамид; модификаторы биологического ответа, например лимфокины, такие как альдеслейкин и другие интерлейкины; интерферон, такой как интерферон-α; факторы роста, такие как эритропоэтин, филграстим и саграмостим; дифференцирующие агенты, такие как производные витамина D, например, сеокальцит и полностью транс-ретиновая кислота; иммунорегуляторы, такие как левамизол; а также моноклональные антитела, фактор некроза опухоли α и ингибиторы ангиогенеза. И, наконец, лечение опухолевых заболеваний сильно зависит от ионизирующего облучения, хотя и не определяемого как соединение, которое может быть использовано в сочетании с соединениями в соответствии с настоящим изобретением. Из-за тяжелого побочного действия, нередко испытываемого пациентами, получающими противоопухолевое лечение, зачастую желательно также применять лекарственные препараты, которые сами по себе не являются противоопухолевыми, но облегчают побочное действие противоопухолевой терапии. Такие соединения включают амифостин, лейковорин и месну.
В частности, противоопухолевые соединения, такие как паклитаксель, фторурацил, этопозид, циклофосфамид, цисплатин, карбоплатин, винкристин, гемцитабин, винорелбин, хлорамбуцил, доксорубицин и мелфалан оказывают благоприятное действие в сочетанных композициях в соответствии с настоящим изобретением.
Предусматривается, что комбинированная композиция в соответствии с настоящим изобретением может быть получена в виде смесей соединений или в виде отдельных соединений, предназначенных для одновременного или последовательного введения. Опытный врач или ветеринар способен установить интервалы времени при последовательном режиме введения.
Согласно следующему аспекту данное изобретение относится к способу лечения или облегчения пролиферативных заболеваний или состояний, включающему введение нуждающемуся в этом пациенту фармацевтической композиции, содержащей соединение формулы I или II, гидролизуемое после введения с помощью ферментов с получением соединения формулы III в количестве, достаточном для осуществления лечения или облегчения указанного пролиферативного заболевания или состояния, необязательно вместе с другим противоопухолевым соединением и/или ионизирующим облучением.
В частности, пролиферативные заболевания или состояния, подвергаемые лечению данным способом, включают различные виды рака и неопластических заболеваний или состояний, включая лейкемию, острую миелоидную лейкемию, хроническую миелоидную лейкемию, хроническую лимфатическую лейкемию, миелодисплазию, множественную миелому, болезнь Ходжкина или неходжкинскую лимфому, мелкоклеточную или немелкоклеточную карциному легких, рак желудка, кишечника или толстой кишки, рак предстательной железы, яичников или молочной железы, рак мозга, головы или шеи, рак мочевых путей, рак почек или мочевого пузыря, злокачественную меланому, рак печени, рак матки или поджелудочной железы.
Также предполагается, что цианогуанидины оказывают благоприятное действие при лечении воспалительных заболеваний. Таким образом, один из аспектов данного изобретения касается способа лечения воспалительных заболеваний, включающего введение пациенту эффективного количества соединения в соответствии с настоящим изобретением либо как такового, либо в сочетании с другими терапевтически активными соединениями.
Данное изобретение также относится к применению соединений формулы I или II, как указано выше, необязательно вместе с другими противоопухолевыми соединениями, для получения лекарственных препаратов. В частности, указанный лекарственный препарат предназначен для лечения пролиферативных заболеваний, например, упомянутых выше видов рака.
Как указано выше, соединения в соответствии с данным изобретением предпочтительно вводят парентерально, например, в жидком, предпочтительно водном, растворе, предназначенном для внутривенных инъекций или вливаний. Подходящая доза соединения в соответствии с данным изобретением зависит, inter alia, от возраста и состояния пациента, тяжести подвергаемого лечению заболевания и других факторов, хорошо известных практикующему врачу. В соответствии с различными схемами применения данное соединение может быть введено перорально или парентерально, например, ежесуточно или с недельными интервалами. В целом, разовая доза составляет, от 0,1 до 400 мг/кг массы тела. Соединение может быть введено парентерально в виде болюса (т.е. всю дозу вводят сразу) либо разделено для приема два или три раза в сутки, либо, предпочтительно, может быть введено в виде внутривенного вливания.
Данное изобретение более подробно описано в следующих примерах, никоим образом не ограничивающих объем заявленного изобретения.
ПРИМЕРЫ
Для спектров 1Н ядерно-магнитного резонанса (ЯМР) (300 МГц) и 13C (ЯМР) (75,6 МГц) величины химического сдвига указаны относительно внутренних стандартов тетраметилсилана (δ=0,00) или хлороформа (δ=7,25), или дейтериохлороформа (δ=76,81 для 13C ЯМР). При отсутствии указания интервала приведено значение установленного (синглет (с), дублет (д), триплет (т), квартет (к)) или неустановленного (уширенного (ушир.)) мультиплета приблизительно в средней его точке. Применяют безводные органические растворители.
Приготовление 1
Хлорметил 2-(1-(трет-бутоксикарбонил)-4-пиперидил)этилкарбонат
Пиридин (3,22 мл) добавляют к охлажденному льдом раствору 2-(1-(трет-бутоксикарбонил)-4-пиперидил)этанола (7,6 г) в дихлорметане (33 мл) с последующим добавлением хлорформиата хлорметила (3,23 мл) со скоростью, обеспечивающей температуру ниже 10°С. После перемешивания при комнатной температуре в течение ночи реакционную смесь дважды промывают 0,5 M HCl, затем водой и водным бикарбонатом натрия. Органическую фазу сушат над сульфатом магния, фильтруют и упаривают в вакууме, получая указанное в заголовке соединение в виде бесцветного масла.
1Н-ЯМР (CDCl3) δ = 5,73 (с, 2H), 4,28 (т, 2H), 4,09 (д, 2H), 2,69 (т, 2H), 1,75-1,50 (м, 5H), 1,45 (с, 9H), 1,15 (м, 2H).
Приготовление 2
Хлорметил 1-(трет-бутоксикарбонил)-3-пиперидилметилкарбонат
Соединение получают способом, описанным в разделе "Приготовление 1", но применяя 1-(трет-бутоксикарбонил)-3-пиперидилметанол вместо 2-(1-(трет-бутоксикарбонил)-4-пиперидил)этанола. Светло-желтое масло.
1Н-ЯМР (CDCl3) δ = 5,73 (с, 2H), 4,11 (м, 2H), 4,0-3,75 (м, 2H), 3,00-2,60 (м, 2H), 2,00-1,60 (м, 3Н), 1,45 (с, 9H), 1,29 (м, 2H).
Приготовление 3
Хлорметил 1-(трет-бутоксикарбонил)-4-пиперидилметилкарбонат
Соединение получают способом, описанным в разделе "Приготовление 1", но применяя 1-(трет-бутоксикарбонил)-4-пиперидилметанол вместо 2-(1-(трет-бутоксикарбонил)-4-пиперидил)этанола. Светло-желтое масло.
1Н-ЯМР (CDCl3) δ = 5,73 (с, 2H), 4,13 (д, 2H), 4,09 (д, 2H), 2,71 (д, 2H), 1,88 (м, 1H), 1,71 (д, 2H), 1,45 (с, 9H), 1,21 (м, 2H).
Приготовление 4
Йодметил 2-(1-трет-бутоксикарбонил)-4-пиперидил)этилкарбонат
К раствору йодида натрия (9 г) в ацетоне (20 мл) добавляют хлорметил 2-(1-(трет-бутоксикарбонил)-4-пиперидил)этилкарбонат (4,9 г). После перемешивания при 40°С в течение 2,5 часов реакционную смесь охлаждают до комнатной температуры, фильтруют и выпаривают в вакууме. Остаток поглощают дихлорметаном, промывают водным бикарбонатом натрия и тиосульфатом натрия, сушат над сульфатом магния, фильтруют и упаривают в вакууме. После очищения на силикагеле с применением гексана/этилацетата (2:1) в качестве элюента, получают указанное в заголовке соединение в виде светло-желтого масла.
1Н-ЯМР (CDCl3) δ = 5,95 (с, 2H), 4,28 (т, 2H), 4,09 (д, 2H), 2,69 (т, 2H), 1,75-1,50 (м, 5H), 1,45 (с, 9H), 1,13 (м, 2H).
Приготовление 5
Йодметил 1-(трет-бутоксикарбонил)-3-пиперидилметилкарбонат
Получают способом, описанным в разделе "Приготовление 4", но применяя хлорметил 1-(трет-бутоксикарбонил)-3-пиперидилметилкарбонат вместо хлорметил 2-(1-(трет-бутоксикарбонил)-4-пиперидил)этилкарбоната. Светло-желтое масло.
1Н-ЯМР (CDCl3) δ = 5,95 (с, 2H), 4,11 (м, 2H), 4,0-3,75 (м, 2H), 3,00-2,60 (м, 2H), 2,00-1,60 (м, 3Н), 1,45 (с, 9H), 1,29 (м, 2H).
Приготовление 6
Йодметил 1-(трет-бутоксикарбонил)-4-пиперидил-метил карбонат
Получают способом, описанным в разделе "Приготовление 4", но применяя хлорметил 1-(трет-бутоксикарбонил)-4-пиперидилметилкарбонат вместо хлорметил 2-(1-(трет-бутоксикарбонил)-4-пиперидил)этилкарбоната. Светло-желтое масло.
1Н-ЯМР (CDCl3) δ = 5,95 (с, 2H), 4,13 (м, 2H), 4,08 (д, 2H), 2,70 (т, 2H), 1,87 (м, 1H), 1,70 (д, 2H), 1,46 (с, 9H), 1,20 (м, 2H).
Приготовление 7
Хлорметил 8-(трет-бутоксикарбониламино)-1-октилкарбонат
Раствор пиридина (1,57 мл) и 8-(трет-бутоксикарбониламино)-1-октанола (4 г) в дихлорметане (40 мл) охлаждают на сухом льду. Полученный в процессе охлаждения осадок и хлорформиат хлорметила (1,6 мл) добавляют к перемешиваемой суспензии со скоростью, обеспечивающей температуру ниже -50°С. После перемешивания в течение 2 часов при температуре ниже -50°С охлаждающую баню удаляют и температуру реакционной смеси поднимают до комнатной температуры. Смесь дважды промывают 0,5 M HCl, затем водой, водным бикарбонатом натрия и насыщенным хлоридом натрия. Органическую фазу сушат над сульфатом магния, фильтруют и упаривают в вакууме, получая указанное в заголовке соединение в виде бесцветного масла.
1Н-ЯМР (CDCl3) δ = 5,73 (с, 2H), 4,52 (ушир., 1H), 4,22 (т, 2H), 3,10 (кв, 2H), 1,69 (м, 2H), 1,44 (с, 9H), 1,55-1,20 (м, 10H).
Приготовление 8
Йодметил 8-(трет-бутоксикарбониламино)-1-октилкарбонат
Данное соединение получают способом, описанным в разделе "Приготовление 4", но применяя хлорметил 8-(трет-бутоксикарбониламино)-1-октилкарбонат вместо хлорметил 2-(1-(трет-бутоксикарбонил)-4-пиперидил)этилкарбоната. Светло-желтое масло.
1Н-ЯМР (CDCl3) δ = 5,95 (с, 2H), 4,51 (ушир., 1H), 4,21 (т, 2H), 3,10 (кв, 2H), 1,68 (м, 2H), 1,44 (с, 9H), 1,55-1,20 (м, 10Н).
Приготовление 9
Хлорметил N-трет-бутоксикарбонил-4-пиперидилкарбоксилат
К раствору N-трет-бутоксикарбонил-4-пиперидилкарбоновой кислоты (6,4 г) в дихлорметане (30 мл) добавляют воду (30 мл), бикарбонат натрия (8,91 г) и гидросульфат тетрабутиламмония (0,95 г). Смесь перемешивают при комнатной температуре, медленно добавляя хлорсульфат хлорметила (3,19 мл). После перемешивания в течение 30 минут органическую фазу отделяют и упаривают в вакууме. Сырой продукт распределяют между простым диэтиловым эфиром и водой. Органическую фазу отделяют, сушат и упаривают, получая указанное в заголовке соединение в виде масла.
13С-ЯМР (CDCl3) δ = 172,6, 154,6, 79,7, 68,7, 42,8, 40,8, 28,4, 27,5.
Приготовление 10
Йодметил N-трет-бутоксикарбонил-4-пиперидилкарбоксилат
Данное соединение получают способом, описанным в разделе "Приготовление 4", но применяя хлорметил N-трет-бутоксикарбонил-4-пиперидилкарбоксилат вместо хлорметил 2-(1-(трет-бутоксикарбонил)-4-пиперидил)этилкарбоната. Светло-желтое масло.
13С-ЯМР (CDCl3) δ = 172,6, 154,6, 79,7, 42,8, 41,0, 30,5, 28,4, 27,4.
Приготовление 11
Йодид 1-[2-[1-(трет-бутоксикарбонил)-4-пиперидил]этоксикарбонилоксиметил]-4-[N'-циано-N''-(6-(4-хлорфенокси)-1-гексил)-N-гуанидино]пиридиния
Йодметил [2-[1-(трет-бутоксикарбонил)-4-пиперидил]этилкарбонат (5 г) добавляют к горячему раствору N-(6-(4-хлорфенокси)-1-гексил)-N'-циано-N''-(4-пиридил)гуанидина (2,8 г) в сухом ацетонитриле (110 г) с последующей дефлегмацией в течение 20 минут. После охлаждения до комнатной температуры и концентрации в вакууме указанное в заголовке соединение подвергают кристаллизации и выделяют фильтрованием. После перекристаллизации из ацетонитрила получают указанное в заголовке соединение в виде бледно-желтых кристаллов.
1Н-ЯМР (CDCl3) δ = 11,24 (ушир., 1H), 8,58 (д, 2H), 8,24 (ушир., 2H), 7,81 (ушир., 1H), 7,20 (д, 2H), 6,82 (д, 2H), 6,19 (с, 2H), 4,26 (т, 2H), 4,08 (д, 2H), 3,94 (т, 2H), 3,77 (кв, 2H), 2,67 (т, 2H), 1,78 (м, 4H), 1,64 (м, 4H), 1,52 (м, 5H), 1,44 (с, 9H), 1,14 (м, 2H).
Приготовление 12
Йодид 1-[1-(трет-бутоксикарбонил)-3-пиперидилметоксикарбонилоксиметил]-4-[N'-циано-N''-(6-(4-хлорфенокси)-1-гексил)гуанидино]пиридиния
Йодметил 1-(трет-бутоксикарбонил)-3-пиперидилметилкарбонат (5,4 г) добавляют к горячему раствору N-(6-(4-хлорфенокси)-1-гексил)-N'-циано-N"-(4-пиридил)гуанидина (2,8 г) в сухом ацетонитриле (110 мл) с последующей дефлегмацией в течение 20 минут. После охлаждения до комнатной температуры и концентрации в вакууме добавляют этилацетат, указанное в заголовке соединение подвергают кристаллизации и выделяют фильтрацией. После перекристаллизации из этилацетата получают указанное в заголовке соединение в виде бледно-желтых кристаллов.
1Н-ЯМР (CDCl3) δ = 11,28 (ушир., 1H), 8,57 (д, 2H), 8,27 (ушир., 2H), 7,85 (ушир., 1H), 7,20 (д, 2H), 6,82 (д, 2H), 6,19 (с, 2H), 4,10 (д, 2H), 3,94 (т, 2H), 3,87 (м, 2H), 3,79 (м, 2H), 2,93 (м, 1H), 2,71 (м, 1H), 2,00-1,48 (м, 11H), 1,44 (с, 9H), 1,26 (м, 2H).
Приготовление 13
Йодид 1-[1-(трет-бутоксикарбонил)-4-пиперидилметоксикарбонилоксиметил]-4-[N'-циано-N''-(6-(4-хлорфенокси)-1-гексил)-N-гуанидино]пиридиния
Йодметил 1-(трет-бутоксикарбонил)-4-пиперидилметилкарбонат (9 г) добавляют к горячему раствору N-(6-(4-хлорфенокси)-1-гексил)-N'-циано-N''-(4-пиридил)гуанидина (4 г) в сухом ацетонитриле (160 мл) с последующей дефлегмацией в течение 20 минут. После охлаждения до комнатной температуры и концентрации в вакууме добавляют этилацетат, указанное в заголовке соединение подвергают кристаллизации и выделяют фильтрованием в виде бледно-желтого порошка.
1Н-ЯМР (CDCl3) δ = 11,25 (ушир., 1H), 8,57 (д, 2H), 8,25 (ушир., 2H), 7,96 (ушир., 1H), 7,19 (д, 2H), 6,83 (д, 2H), 6,19 (с, 2H), 4,12 (ушир., 2H), 4,06 (д, 2H), 3,93 (т, 2H), 3,77 (т, 2H), 2,69 (т, 2H), 1,93-1,48 (м, 11H), 1,45 (с, 9H), 1,18 (м, 2H).
Приготовление 14
Йодид 1-[8-(трет-бутоксикарбониламино)-1-октилоксикарбонилоксиметил]-4-[N'-циано-N''-(6-(4-хлорфенокси)-1-гексил)-N-гуанидино]пиридиния
Йодметил 8-(трет-бутоксикарбониламино)-1-октилкарбонат (5,47 г) добавляют к горячему раствору N-(6-(4-хлорфенокси)-1-гексил)-N'-циано-N"-(4-пиридил)гуанидина (3,16г) в сухом ацетонитриле (140 мл) с последующей дефлегмацией в течение 20 минут. После охлаждения до комнатной температуры указанное в заголовке соединение подвергают кристаллизации и после дополнительного охлаждения на льду кристаллический продукт выделяют фильтрованием.
13С-ЯМР (CDCl3) δ = 157,7, 156,0, 154,9, 153,8, 143,8, 129,2, 125,2, 115,8, 114,4, 80,4, 79,1, 70,5, 68,0, 43,0, 40,5, 30,0, 29,2, 29,0, 28,9, 28,4, 28,2, 26,6, 26,3, 25,4, 25,4.
Приготовление 15
Йодид 1-[1-(трет-бутоксикарбонил)-4-пиперидилкарбонилоксиметил]-4-[N'-циано-N"-(6-(4-хлорфенокси)-1-гексил)-N-гуанидино]пиридиния
Йодметил N-трет-бутоксикарбонил-4-пиперидилкарбоксилат (6,52 г) добавляют к горячему раствору N-(6-(4-хлорфенокси)-1-гексил)-N'-циано-N"-(4-пиридил)гуанидина (4,38 г) в сухом ацетонитриле (170 мл) с последующей дефлегмацией в течение 20 минут. После охлаждения до комнатной температуры и концентрации в вакууме указанное в заголовке соединение подвергают кристаллизации и после дополнительного охлаждения на льду кристаллический продукт выделяют фильтрованием.
13С-ЯМР (CDCl3) δ = 173,5, 157,7, 154,6, 154,5, 153,9, 143,9, 129,3, 125,2, 115,9, 114,5, 80,0, 77,7, 68,0, 43,0, 40,6, 29,2, 28,9, 28,4, 27,6, 26,3, 25,5.
Пример 1
Гидрохлорид 1-[2-(4-пиперидил)этоксикарбонилоксиметил]-4-[N'-циано-N"-(6-(4-хлорфенокси)-1-гексил)-N-гуанидино]пиридинийхлорида
Раствор йодида 1-[2-[1-(трет-бутоксикарбонил)-4-пиперидил]этоксикарбонилоксиметил]-4-[N'-циано-N"-(6-(4-хлорфенокси)-1-гексил)-N-гуанидино]пиридиния (1,9 г) в дихлорметане (60 мл) взбалтывают с избыточным количеством водного бикарбоната натрия и тиосульфата натрия. Органическую фазу сушат над сульфатом магния и фильтруют. После концентрирования в вакууме до объема приблизительно 15 мл прозрачный фильтрат охлаждают на льду с перемешиванием и обрабатывают избыточным количеством хлористого водорода в простом эфире. Ледяную баню удаляют и после перемешивания в течение 4 часов растворитель удаляют в вакууме. При добавлении этанола остаток кристаллизуется, и после перекристаллизации из метанола/простого эфира получают указанное в заголовке соединение в виде чистых бесцветных кристаллов.
1Н-ЯМР (ДМСО) δ = 12,10 (ушир., 1H), 9,18 (ушир., 2H), 8,94 (ушир., 1Н), 8,75 (д, 2H), 7,58 (ушир., 2H), 7,31 (д, 2H), 6,95 (д, 2H), 6,22 (с, 2H), 4,20 (т, 2H), 3,96 (т, 2H), 3,41 (м, 2H), 3,19 (м, 2H), 2,78 (кв, 2H), 1,86-1,25 (м, 15H).
Пример 2
Гидрохлорид 1-[3-пиперидилметоксикарбонилоксиметил]-4-[N'-циано-N"-(6-(4-хлорфенокси)-1-гексил)-N-гуанидино]пиридинийхлорида
Раствор йодида 1-[1-(трет-бутоксикарбонил)-3-пиперидилметоксикарбонилоксиметил]-4-[N'-циано-N"-(6-(4-хлорфенокси)-1-гексил)-N-гуанидино]пиридиния (1,7 г) в дихлорметане (60 мл) взбалтывают с избыточным количеством водного бикарбоната натрия и тиосульфата натрия. Органическую фазу сушат над сульфатом магния и фильтруют. После концентрирования в вакууме до объема приблизительно 15 мл прозрачный фильтрат охлаждают на льду с перемешиванием и обрабатывают избыточным количеством хлористого водорода в простом эфире. Ледяную баню удаляют и после перемешивания в течение 4 часов растворитель удаляют в вакууме. При добавлении этанола остаток кристаллизуется, и после перекристаллизации из метанола/простого эфира получают указанное в заголовке соединение в виде бесцветных кристаллов.
1Н-ЯМР (ДМСО) δ = 12,10 (ушир., 1H), 9,27 (ушир., 3H), 8,76 (д, 2H), 7,61 (ушир., 2H), 7,31 (д, 2H), 6,95 (д, 2H), 6,24 (с, 2H), 4,09 (м, 2H), 3,96 (т, 2H), 3,41 (ушир., 2H), 3,18 (д, 2H), 2,65 (м, 2H), 2,18 (ушир., 1H), 1,85-1,13 (м, 12Н).
Пример 3
Гидрохлорид 1-[4-пиперидилметоксикарбонилоксиметил]-4-[N'-циано-N"-(6-(4-хлорфенокси)-1-гексил)-N-гуанидино]пиридинийхлорида
Раствор йодида 1-[1-(трет-бутоксикарбонил)-4-пиперидилметоксикарбонилоксиметил]-4-[N'-циано-N"-(6-(4-хлорфенокси)-1-гексил)-N-гуанидино]пиридиния (1 г) в дихлорметане (30 мл) взбалтывают с избыточным количеством водного бикарбоната натрия и тиосульфата натрия. Органическую фазу сушат над сульфатом магния и фильтруют. После концентрирования в вакууме до объема приблизительно 15 мл прозрачный фильтрат охлаждают на льду с перемешиванием и обрабатывают избыточным количеством хлористого водорода в простом эфире. Ледяную баню удаляют и после перемешивания в течение 4 часов растворитель удаляют в вакууме с получением указанного в заголовке соединения в виде бесцветной пены.
1Н-ЯМР (ДМСО) δ = 12,05 (ушир., 1H), 9,19 (ушир., 2H), 8,93 (ушир., 1H), 8,78 (д, 2H), 7,65 (ушир., 2H), 7,31 (д, 2H), 6,95 (д, 2H), 6,24 (с, 2H), 4,50 (д, 2H), 3,96 (т, 2H), 3,42 (кв, 2H), 3,22 (д, 2H), 2,82 (м, 2H), 1,8-1,25 (м, 13H).
Пример 4
Гидрохлорид 1-[8-амино-1-октилоксикарбонилоксиметил]-4-[N'-циано-N"-(6-(4-хлорфенокси)-1-гексил)-N-гуанидино]пиридинийхлорида
Получают способом, описанным в примере 1, но применяя йодид 1-[8-(N-трет-бутоксикарбониламино)-1-октилоксикарбонилоксиметил]-4-[N'-циано-N"-(6-(4-хлорфенокси)-1-гексил)-N-гуанидино]пиридиния вместо йодида 1-[2-[1-(трет-бутоксикарбонил)-4-пиперидил]этоксикарбонилоксиметил]-4-[N'-циано-N"-(6-(4-хлорфенокси)-1-гексил)-N-гуанидино]пиридиния. Светло-желтые кристаллы.
13С-ЯМР (ДМСО) δ = 157,4, 154,9, 153,0, 144,9, 129,1, 123,9, 116,1, 115,0, 112,7, 80,1, 68,9, 67,6, 42,1, 28,3, 28,2, 27,7, 26,7, 25,7, 25,6, 25,0, 24,8.
Пример 5
Гидрохлорид 1-[4-пиперидилкарбонилоксиметил]-4-[N'-циано-N"-(6-(4-хлорфенокси)-1-гексил)-N-гуанидино]пиридинийхлорида
Получают способом, описанным в примере 2, но применяя йодид 1-[1-(трет-бутоксикарбонил)-4-пиперидилкарбонилоксиметил]-4-[N'-циано-N"-(6-(4-хлорфенокси)-1-гексил)-N-гуанидино]пиридиния вместо йодида 1-[2-[1-(трет-бутоксикарбонил)-4-пиперидил]этоксикарбонилоксиметил]-4-[N'-циано-N"-(6-(4-хлорфенокси)-1-гексил)-N-гуанидино]пиридиния. Кристаллический порошок.
13С-ЯМР (ДМСО) δ = 172,2, 157,4, 154,8, 144,8, 129,1, 123,9, 116,1, 115,0, 78,1, 67,6, 41,7, 37,2, 28,3, 25,7, 25,0, 23,9.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОЛЕКАРСТВА ЦИАНОГУАНИДИНА | 2001 |
|
RU2312858C2 |
| ПРОИЗВОДНЫЕ ПИРИДИЛЦИАНОГУАНИДИНОВ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2002 |
|
RU2292344C2 |
| СПОСОБ ЛЕЧЕНИЯ АЛЛЕРГИИ С ИСПОЛЬЗОВАНИЕМ ЗАМЕЩЕННЫХ ПИРАЗОЛОВ | 2001 |
|
RU2259202C2 |
| ЗАМЕЩЕННЫЕ 3-ПИРИДИЛМЕТИЛАМИНЫ И ФОКУСИРОВАННАЯ БИБЛИОТЕКА | 2003 |
|
RU2228930C1 |
| КОНДЕНСИРОВАННОЕ ГЕТЕРОЦИКЛИЧЕСКОЕ СОЕДИНЕНИЕ | 2005 |
|
RU2389731C2 |
| ПРОИЗВОДНЫЕ 2-ЗАМЕЩЕННЫХ ФЕНИЛ-5, 7-ДИГИДРОКАРБИЛ-3, 7-ДИГИДРОПИРРОЛО [2, 3-d] ПИРИМИДИН-4-ОНОВ, ИХ ПОЛУЧЕНИЕ И ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2004 |
|
RU2323220C2 |
| ПРЕДОТВРАЩАЮЩИЙ ПРЕЖДЕВРЕМЕННУЮ ОВУЛЯЦИЮ АГЕНТ | 2006 |
|
RU2419435C2 |
| НОВЫЕ СОЕДИНЕНИЯ, ИХ ИЗОМЕР ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ В КАЧЕСТВЕ АНТАГОНИСТА ВАНИЛОИДНОГО РЕЦЕПТОРА И СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2007 |
|
RU2448108C2 |
| КОНДЕНСИРОВАННЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ | 2006 |
|
RU2408586C2 |
| ПРОИЗВОДНЫЕ АМИДИНОНАФТИЛА И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1995 |
|
RU2154633C2 |
Изобретение относится к цианогуанидиновым производным общей формулы I
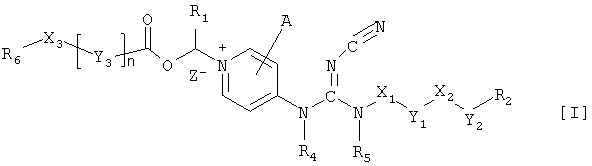
где A, X1, X2, Х3, Y1, Y2, Y3, R1, R2, R5, R6 и n имеют значения, указанные в формуле изобретения. Также изобретение относится к фармацевтической композиции, обладающей антипролиферативной активностью на основе соединений формулы I, и к применению данных соединений для получения лекарственного препарата для лечения и облегчения пролиферативных заболеваний или состояний. Технический результат: получение новых соединений, которые могут быть полезны в лечении пролиферативных заболеваний, таких как различные виды рака, у людей и животных. 7 н. и 18 з.п. ф-лы.
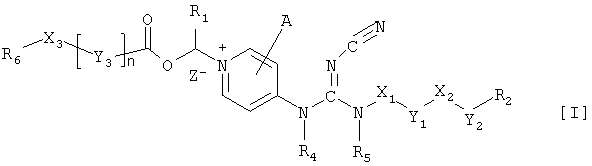
где X1 представляет собой прямолинейный, разветвленный и/или циклический углеводородный дирадикал, необязательно замещенный одним или более заместителями, такими как гидрокси, галоген, нитро, амино или циано;
Х2 представляет собой связь; прямолинейный, разветвленный и/или циклический углеводородный дирадикал, необязательно замещенный одним или более заместителями, такими как гидрокси, галоген, нитро, амино, циано, аминосульфонил, алкилсульфониламино, алкилкарбонил, формил, аминокарбонил или алкилкарбониламино; дирадикал гетероарилена или неароматического гетероциклического углеводорода, каждый из которых необязательно замещен одним или более прямолинейными, разветвленными и/или циклическими неароматическими углеводородными радикалами, гидроксилом, галогеном, нитро, амино, циано, аминосульфонилом, алкилсульфониламино, алкилкарбонилом, формилом, аминокарбонилом или алкилкарбониламино;
Х3 представляет собой прямолинейный, разветвленный и/или циклический углеводородный дирадикал, необязательно замещенный одним или более заместителями, выбранными из группы, состоящей из гидрокси, галогена, нитро, амино, циано, аминосульфонила, алкилсульфониламино, алкилкар-бонила, формила, аминокарбонила или алкилкарбониламино; при условии, что когда n равно 0, Х3 также может представлять собой связь;
Y1 представляет собой связь, О, S, S(O), S(O)2, C(O), NH-C(O) или С(O)-NH;
Y2 представляет собой связь, дирадикал простого эфира (R'-O-R"), дирадикал амина (R'-N-R"), О, S, S(O), S(O)2, С(O), NH-C(O), C(O)-NH, SO2-N(R') или N(R')-SO2, где R' и R" независимо представляют собой прямолинейные или разветвленные углеводородные дирадикалы, содержащие до 4 атомов углерода;
Y3 представляет собой О;
R1 представляет собой водород или прямолинейный, разветвленный и/или циклический алкил, необязательно замещенный фенилом; или ароматический углеводородный радикал;
R2 представляет собой водород либо арил или гетероарил, необязательно замещенные одним или более заместителями, выбранными из группы, состоящей из галогена, трифторметила, гидрокси, С1-4алкокси, нитро, циано, С1-4гидроксиалкила или С1-4алкила, необязательно замещенного галогеном, гидрокси, циано или нитро; тетрагидропиранилокси, ди(С1-4алкокси)фосфиноилокси или С1-4алкоксикарбониламино;
R4 представляет собой водород;
R5 представляет собой водород или прямолинейный, разветвленный и/или циклический углеводородный радикал, необязательно замещенный галогеном, гидроксилом, амино, нитро или циано;
R6 представляет собой пипередил, присоединенный по 3 или 4 положению к Х3;
А представляет собой водород, необязательно замещенный прямолинейный, разветвленный и/или циклический углеводородный радикал, гидрокси, галоген, нитро, циано, гетероарил, гетероаралкил или тиол;
n равно 0 или 1; и
Z- представляет собой фармацевтически приемлемый анион, такой как хлорид, бромид, иодид, сульфат, метансульфонат, п-толуолсульфонат,
нитрат или фосфат.
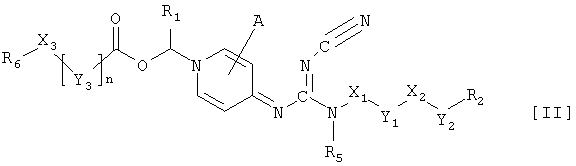
где A, X1, X2, Х3, Y1, Y2, Y3, R1, R2, R5 и n имеют значения, указанные в п.1.
X1 представляет собой прямолинейный, разветвленный или циклический, насыщенный или ненасыщенный углеводородный дирадикал с 4-20 атомами углерода;
Y2 представляет собой О, S, С(O) или связь;
R2 представляет собой арил или гетероарил, необязательно замещенный одним или более заместителями, выбранными из группы, состоящей из галогена, трифторметила, гидрокси, С1-4алкокси, нитро, циано, С1-4гидроксиалкила или С1-4алкила, необязательно замещенных галогеном, гидрокси, циано или нитро; тетрагидропиранилокси, ди(С1-4алкокси)фосфиноилокси или С1-4алкоксикарбониламино;
Х3 представляет собой прямолинейный углеводородный дирадикал, состоящий из 1 до 10 атомов углерода;
R6 представляет собой пиперидил, прикрепленный в положении 3 или 4 к
Х3;
R1 представляет собой водород, прямолинейный или разветвленный С1-4алкил, аралкил или арил;
каждый из А, R4 и R5 представляет собой водород;
n равно 0 или 1; и
Z- представляет собой хлорид, бромид, иодид, сульфат, метансульфонат,
п-толуолсульфонат или нитрат.
гидрохлорид 1-[2-(4-пиперидил)этоксикарбонилоксиметил]-4-[N'-циано-N"-(6-(4-хлорфенокси)-1-гексил)-N-гуанидино]пиридинийхлорида;
гидрохлорид 1-[3-пиперидилметоксикарбонилоксиметил]-4-[N'-циано-N"-(6-(4-хлорфенокси)-1-гексил)-N-гуанидино]пиридинийхлорида;
гидрохлорид 1-[4-пиперидилметоксикарбонилоксиметил]-4-[N'-циано-N"-(6-(4-хлорфенокси)-1-гексил)-N-гуанидино]пиридинийхлорида;
гидрохлорид 1-[4-пиперидилкарбонилоксиметил]-4-[N'-циано-N"-(6-(4-хлорфенокси)-1-гексил)-N-гуанидино]пиридинийхлорида.
хлорметил 2-(1-(трет-бутоксикарбонил)-4-пиперидил)этилкарбонат;
хлорметил 1-(трет-бутоксикарбонил)-3-пиперидилметилкарбонат;
хлорметил 1-(трет-бутоксикарбонил)-4-пиперидилметилкарбонат;
йодметил 2-(1-(трет-бутоксикарбонил)-4-пиперидил)этилкарбонат;
йодметил 1-(трет-бутоксикарбонил)-3-пиперидилметилкарбонат;
йодметил 1-(трет-бутоксикарбонил)-4-пиперидилметилкарбонат;
хлорметил 8-(трет-бутоксикарбониламино)-1-октилкарбонат;
йодметил 8-(трет-бутоксикарбониламино)-1-октилкарбонат;
хлорметил N-трет-бутоксикарбонил-4-пиперидилкарбоксилат;
йодметил N-трет-бутоксикарбонил-4-пиперидилкарбоксилат;
йодид 1-[2-[1-(трет-бутоксикарбонил)-4-пиперидил]этоксикарбонилоксиметил]-4-[N'-циано-N"-(6-(4-хлорфенокси)-1-гексил)-N-гуанидино]пиридиния;
йодид 1-[1-(трет-бутоксикарбонил)-3-пиперидилметоксикарбонилоксиметил]-4-[N'-циано-N"-(6-(4-хлорфенокси)-1-гексил)-N-гуанидино]пиридиния;
йодид 1-[1-(трет-бутоксикарбонил)-4-пиперидилметоксикарбонилоксиметил]-4-[N'-циано-N"-(6-(4-хлорфенокси)-1-гексил)-N-гуанидино]пиридиния;
йодид 1-[8-(N-трет-бутоксикарбониламино)1-октилоксикарбонилоксиметил]-4-[N'-циано-N"-(6-(4-хлорфенокси)-1-гексил)-N-гуанидино]пиридиния; и
йодид 1-[1-(трет-бутоксикарбонил)-4-пиперидилкарбонилоксиметил]-4-[N'-циано-N"-(6-(4-хлорфенокси)-1-гексил)-N-гуанидино]пиридиния.
| Дорожная спиртовая кухня | 1918 |
|
SU98A1 |
| WO 00/61559 A1, 19.10.2000 | |||
| N-ЦИАНО-N'-ПИРИДИЛГУАНИДИНЫ, ИЛИ ИХ N-ОКСИДЫ, ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ НЕТОКСИЧНЫЕ СОЛИ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ИНГИБИРОВАНИЯ ПРОЛИФЕРАЦИИ ОПУХОЛЕВЫХ КЛЕТОК | 1993 |
|
RU2141951C1 |
Авторы
Даты
2008-06-20—Публикация
2003-05-15—Подача