Изобретение относится к способу получения (пиримидин-2-ил)метилкетонов общей формулы
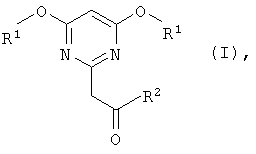
в которой R1 в каждом случае обозначает C1-С10алкильную группу, С3-С8циклоалкильную группу, аллильную группу или арилС1-С4алкильную группу, а R2 обозначает С1-С10алкильную группу или арильную группу. Понятие "C1-С10алкильные группы" в данном случае и ниже использовано как обозначающее все линейные или разветвленные первичные, вторичные или третичные алкильные группы, содержащие от 1 до 10 углеродных атомов, такие как, например, метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил, трет-бутил, пентил, изопентил, трет-пентил, неопентил, гексил, гептил, октил, нонил или децил.
Понятие "С3-С8циклоалкил" следует воспринимать как обозначающее, в частности, циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и циклооктил.
Понятием "арилС1-С4алкильные" группы обозначают группы, состоящие из арильной группы и алкильной группы, содержащей от 1 до 4 углеродных атомов, причем понятие "арильные группы" используют как обозначающее, в частности, фенильные или нафтильные группы. Арильные группы также могут быть замещенными одной или несколькими С1-С4алкильными группами, C1-С4алкоксигруппами или атомами галогена. Примерами арилС1-С4алкильных групп являются, в частности, бензил, 1-фенилэтил, 2-фенилэтил и 3-фенилпропил.
Соединения формулы I, в частности 1-(4,6-диметоксипиримидин-2-ил)пропан-2-он (R1 и R2 обозначают Me), являются потенциальными промежуточными продуктами в синтезе агрохимических действующих компонентов.
Синтезы этих соединений до настоящего времени в литературе, посвященной данной области техники, не описаны.
Объектом настоящего изобретения является разработка способа получения, который прост и приемлем для осуществления в промышленном масштабе.
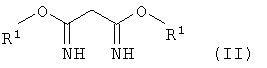
В соответствии с изобретением этой цели добиваются благодаря способу по п.1 формулы изобретения. Было установлено, что реакцией малондиимидатов, которые могут быть легко получены из малодинитрила и соответствующих спиртов (DE-A 2426913, ЕР-А 0024200), общей формулы
 ,
,
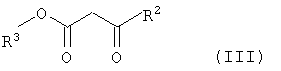
в которой R1 имеет указанные выше значения, с β-кетоэфирами общей формулы
 ,
,
в которой R2 имеет указанные выше значения, a R3 обозначает C1-С10алкильную группу, непосредственно и с хорошим выходом получают целевые соединения (I).
Эту реакцию целесообразно проводить таким путем, при котором из реакционной смеси удаляют образующуюся во время реакции воду. Это может быть достигнуто, например, добавлением осушителя или азеотропной дистилляцией с подходящим азеотропообразователем.
Малондиимидаты (II) могут быть либо использованы без разбавителя (в виде свободного основания), либо, кроме того, могут быть получены in situ из соответствующих соли и основания. В предпочтительном варианте их используют без разбавителя. Для этого они могут быть, например, экстрагированы растворителем низкой полярности, таким как дихлорметан и диэтиловый эфир, из нейтрализованного раствора одной из их солей и выделены выпариванием растворителя (ЕР-А 0024200).
Предпочтительные используемые соли малондиимидатов (II) представляют собой дигидрохлориды.
В предпочтительном варианте способ в соответствии с изобретением применяют для получения (4,6-диметоксипиримидин-2-ил)метилкетонов с использованием диметилмалондиимидата (R1 обозначает Me) в виде малондиимидата (II).
В предпочтительном варианте используемые β-кетоэфиры (III) представляют собой ацетоуксусные эфиры (R2 обозначает Me), 3-оксопентановые эфиры (R2 обозначает Et) или бензоилуксусные эфиры (R2 обозначает Ph).
Предпочтительными β-кетоэфирами являются метиловый и этиловый эфиры (R3 обозначает Me, Et).
Способ в соответствии с изобретением целесообразно осуществлять в инертном растворителе, таком как, например, толуол или ксилол. Целесообразная реакционная температура составляет от 50 до 150°С.
Приведенные ниже примеры иллюстрируют, каким образом осуществляют способ в соответствии с изобретением, но их не следует рассматривать как налагающие какие-либо ограничения.
Пример 1
1-(4,6-диметоксипиримидин-2-ил)пропан-2-он
(I, R1 и R2 обозначают Me)
В колбе, снабженной обратным холодильником и отделителем воды, в нагретый до 135°С (кипячение с обратным холодильником) раствор метилацетоацетата (5,92 г, 50 ммолей) в ксилоле (80 мл) в течение 135 мин вводили раствор диметилмалондиимидата (6,51 г, 0,61 моля) в ксилоле (20 мл) таким образом, чтобы реакционная смесь продолжала кипеть. После кипячения с обратным холодильником в течение еще 90 мин вначале реакционную смесь фильтровали при 70°С, далее фильтрат охлаждали до комнатной температуры, а затем выпаривали. Оранжево-коричневый маслянистый сырой продукт (8,35 г) очищали хроматографией в колонке гексаном/этилацетатом (в объемном соотношении 5:1) на силикагеле 60.
Выход: 5,56 г (56%-ный в пересчете на диимидат) продукта в виде желтоватого масла, которое по истечении некоторого промежутка времени затвердевает.
1Н-ЯМР (CDCl3, δ): 5,92 (s, 1Н); 3,91 (s, 6Н); 3,86 (s, 2H); 2,27 (s, 3Н).
Спектр содержал дополнительные сигналы, соответствовавшие енольной форме.
Пример 2
1-(4,6-диметоксипиримидин-2-ил)бутан-2-он
(I, R1 обозначает Me, R2 обозначает Et)
Процесс проводили аналогично примеру 1, за исключением того, что метилацетоацетат заменяли эквивалентным количеством метил-3-оксопентаноата, период добавления составлял 150 мин с постреакционным временем 120 мин и реакционную смесь фильтровали при 90°С.
Выход: 6,7 г (64%-ный) вещества в виде желтого масла
1Н-ЯМР (CDCl3, δ): 5,91 (s, 1H); 3,91 (s, 6H); 2,59 (q, 2H); 1,09 (t, 3H).
Спектр содержал дополнительные сигналы, соответствовавшие енольной форме.
Пример 3
1-(4,6-диметоксипиримидин-2-ил)пропан-2-он
(I, R1 и R2 обозначают Me)
Процесс проводили аналогично примеру 1, за исключением того, что метилацетоацетат заменяли эквивалентным количеством этилацетоацетата, период добавления составлял 130 мин с постреакционным временем 280 мин и реакционную смесь фильтровали при 90°С.
Выход: 5,18 г (54%-ный в пересчете на диимидат) продукта в виде желтоватого масла, которое по прошествии некоторого промежутка времени затвердевало.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 1-(ПИРИМИДИН-2-ИЛ)ПРОПАН-2-ОНОВ | 2002 |
|
RU2325380C2 |
| ПРОИЗВОДНЫЕ НИКОТИНОВОЙ КИСЛОТЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ | 1994 |
|
RU2133746C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННОГО АНИЛИНОВОГО СОЕДИНЕНИЯ (ВАРИАНТЫ) И ПРОМЕЖУТОЧНЫЕ ПРОДУКТЫ | 2001 |
|
RU2292338C2 |
| ПРОИЗВОДНЫЕ ПИКОЛИНОВОЙ КИСЛОТЫ ИЛИ ИХ КИСЛОТНО-АДДИТИВНЫЕ СОЛИ, СПОСОБ ИХ ПОЛУЧЕНИЯ, НЕРБИЦИДНАЯ КОМПОЗИЦИЯ И СПОСОБ БОРЬБЫ С СОРНЯКАМИ | 1991 |
|
RU2091380C1 |
| ПРОИЗВОДНЫЕ ПИРИМИДИНА, СПОСОБ БОРЬБЫ С СОРНЯКАМИ И ГЕРБИЦИДНЫЙ СОСТАВ | 1990 |
|
RU2041214C1 |
| ПРОИЗВОДНЫЕ АМИДА N-СУЛЬФОНИЛКАРБОНОВОЙ КИСЛОТЫ, ВКЛЮЧАЮЩИЕ N-СОДЕРЖАЩЕЕ 6-ЧЛЕННОЕ АРОМАТИЧЕСКОЕ КОЛЬЦО, ФУНГИЦИДНАЯ И ГЕРБИЦИДНАЯ КОМПОЗИЦИИ И СПОСОБЫ БОРЬБЫ С СОРНЯКАМИ И ФИТОПАТОГЕННЫМИ ГРИБКАМИ | 1993 |
|
RU2117662C1 |
| КОНДЕНСИРОВАННОЕ ГЕТЕРОЦИКЛИЧЕСКОЕ ПРОИЗВОДНОЕ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ГЕРБИЦИДНОЕ СРЕДСТВО | 1993 |
|
RU2105005C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ТИОБАРБИТУРОВОЙ КИСЛОТЫ | 2000 |
|
RU2242467C2 |
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ПИРИДИНСУЛЬФОНАМИДА, ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ, ПРОИЗВОДНЫЕ ПИРИДИНСУЛЬФОНАМИДА | 1992 |
|
RU2054427C1 |
| СПОСОБ ПОЛУЧЕНИЯ АМИНОФЕНИЛСУЛЬФОНИЛМОЧЕВИН (ВАРИАНТЫ), ПРОМЕЖУТОЧНЫЕ ПРОДУКТЫ | 1996 |
|
RU2177003C2 |
Изобретение относится к новым (пиримидин-2-ил) метилкетонам формулы (I) и новому способу их получения. Соединения настоящего изобретения являются промежуточными продуктами для синтеза агрономически активных действующих начал. Способ получения (пиримидин-2-ил)метилкетонов общей формулы
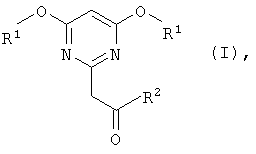
в которой R1 и R2 в каждом случае независимо обозначает C1-С10алкильную группу, заключается в том, что проводят реакцию малондиимидата общей формулы
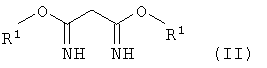 ,
,
в которой R1 имеет указанные выше значения, с β-кетоэфиром общей формулы
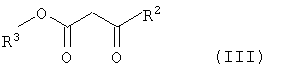 ,
,
в которой R2 имеет указанные выше значения, а R3 обозначает C1-С10алкильную группу. Обычно из реакционной смеси удаляют образующуюся во время реакции воду. Используемый исходный малондиимидат (II) можно получить in situ из соответствующих соли и основания. Предпочтительно используемая соль малондиимидата (II) представляет собой дигидрохлорид, а используемый малондиимидат (II) представляет собой диметилмалондиимидат. Предпочтительно используемый β-кетоэфир (III) представляет собой ацетоуксусный эфир, 3-оксопентановый эфир. 2 н. и 8 з.п. ф-лы.
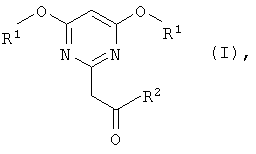
в которой R1 и R2 в каждом случае независимо обозначает C1-С10алкильную группу, отличающийся тем, что проводят реакцию малондиимидата общей формулы
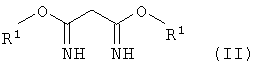 ,
,
в которой R1 имеет указанные выше значения, с β-кетоэфиром общей формулы
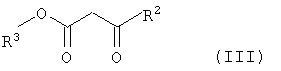 ,
,
в которой R2 имеет указанные выше значения, а R3 обозначает C1-C10алкильную группу.

в которой R1 и R2 в каждом случае независимо обозначает C1-С10алкильную группу, при условии, что R1 и/или R2 не означают метил.
| US 5276152 A, 04.01.1994 | |||
| DE 3842218 А1, 21.08.2000 | |||
| СПОСОБ ПОЛУЧЕНИЯ 2-ЗАМЕЩЕННЫХ 4,6-ДИАЛКОКСИПИРИМИДИНОВ,2-N-БУТИЛАМИНО-4,6-ДИМЕТОКСИПИРИМИДИН И СПОСОБ ПОЛУЧЕНИЯ ГАЛОГЕНПРОИЗВОДНЫХ ПИРИМИДИНА | 1992 |
|
RU2117007C1 |
| EILINGSFELD H | |||
| et al | |||
| "Synthese von pyrimidinen aus malondiimidsaeureestern", Chem | |||
| Ber., 1968, v.l01, p.2426-2434. | |||
Авторы
Даты
2008-06-20—Публикация
2002-10-09—Подача