Изобретение относится к биотехнологии, в частности к медицине, к композициям для определения содержания метаболитов оксида азота (NO) в биологических жидкостях.
Изобретение наиболее эффективно может быть использовано в диагностике заболеваний, критерием которых является содержание оксида азота в биологических жидкостях, например крови.
В связи с патогенетическим значением NO необходима разработка способов определения содержания метаболитов оксида азота (нитрат- и нитрит-ионов) в биологических материалах для диагностических целей (Маеда X., Акаике Т. Оксид азота и кислородные радикалы при инфекции, воспалении и раке. // Биохимия. - 1998. - т.63, вып.7. - С.1007-1019).
Оксид азота (NO) - активное неорганическое соединение со свойствами радикала (N=О), имеет неспаренный электрон, придающий ему высокую реакционную способность. Радикал NO может реагировать в биологических системах с кислородом, супероксидным анион-радикалом и ионами металлов переходной валентности. Поэтому функциональный ответ на действие NO многообразен и в значительной степени зависит не только от фенотипа клеток-мишеней, но и от количества NO в клетках. Время жизни NO не превышает 6-10 сек, после чего он при участии кислорода и воды превращается в метаболиты - нитраты и нитриты (Недоспасов А.А. Биогенный NO в конкурентных отношениях. // Биохимия. - 1998 - Т.63, Вып.7. - Сдли. 881-904).
Известен способ определения нитрат- и нитрит-ионов в биологических жидкостях с помощью системы высокоэффективной хроматографии высокого давления, в которой проходит реакция на нитрит-анион с использованием реагента Грисса - раствор сульфаниламида и N-(1-нафтил)-этилендиамина в 2,5% ортофосфорной кислоте, и кадмиевых колонок в системе (Laura С.Green, D.A.Wagner, J.Glogowski, P.Skipper et al. Analysis of Nitrate, Nitrite, and [15N] Nitrate in Biological Fluids // Analytical Biochemistry. - 1982. - Vol.126. - P.131-138).
Недостатком способа является его трудоемкость, необходимость приобретения дорогостоящего оборудования, специализированных реагентов и лабораторных помещений, многоэтапность процесса определения и невозможность одновременного определения нитрат- и нитрит-ионов.
Известна композиция для определения нитрат-ионов в растворах (Патент РФ №2141115), содержащая компоненты (мас.%):
Композиция может быть использована для фотометрического определения нитрат-ионов при контроле очистки природных вод, в продуктах питания, фруктовых соках, овощах, экстрактах почв. Этот состав наиболее близок по сущности и достигаемому результату и избран нами в качестве прототипа.
Известно также, что для протекания цветной реакции нитрат-ионов с компонентами известного состава необходимо обеспечение кислотности раствора в интервале рН 6-8, для чего используется дополнительное подщелачивание анализируемой биологической жидкости.
Недостатком известной композиции является необходимость предварительного подщелачивания анализируемого раствора биологического материала. Это дополнительные и длительные этапы аналитической процедуры, повышающие ее трудоемкость и снижающие точность анализа.
Задачей данного изобретения является создание композиции для определения содержания метаболитов оксида азота в биологических жидкостях.
Поставленная задача решается тем, что композиция включает аммония сукцинат, аммония бромид, винную кислоту, цинковую пыль, сульфаниловую кислоту и динатриевую соль хромотропной кислоты и дополнительно содержит аммония ацетат в качестве подщелачивающего агента при следующем соотношении компонентов (мас. частях):
Состав приготовляют смешиванием и тщательной гомогенизацией указанных компонентов порошка в керамической посуде. При хранении в сухом месте состав устойчив в течение 1 года.
Существенным отличием заявляемой композиции от известной является дополнительное введение ацетата аммония в количестве 5,0-15,0 мас. частей в качестве подщелачивающего агента, что позволяет исключить из аналитической процедуры этап подщелачивания путем добавления раствора NaOH и повысить экспрессность и точность определения нитрат-ионов в биологических материалах. Ацетат аммония в смеси с винной кислотой выбран для обеспечения оптимальной кислотности, его наличие в композиции способствует одновременному протеканию процессов восстановления, диазотирования и азосочетания.
Состав для определения метаболитов оксида азота в биологических материалах содержит бромид аммония в качестве катализатора диазотирования, что ускоряет развитие окраски анализируемого раствора и позволяет уменьшить содержание сульфаниловой кислоты до 0,5-1,5 мас.%.
Использование в качестве азосоставляющей динатриевой соли хромотроповой кислоты повышает стабильность композиции во времени. Динатриевая соль хромотроповой кислоты не обладает канцерогенными свойствами.
Цинковая пыль входит в композицию как катализатор процесса восстановления нитрат-ионов до нитрит-ионов, этот процесс ускоряется с увеличением содержания цинковой пыли в композиции.
Особенностью предлагаемого состава является композиция реагентов, позволяющих одновременно проводить реакцию восстановления нитрат-ионов (NO3) в нитрит-ионы (NO2), которые непосредственно участвуют в реакции диазотирования аминов и последующего их взаимодействия с азосоставляющей. Эта реакция специфична, поскольку диазотирование протекает только в присутствии нитрит-ионов по следующей схеме:
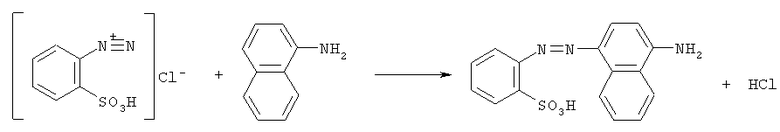
При этом образуется окрашенное в красный цвет соединение в концентрации, пропорциональной содержанию нитрат-ионов в анализируемом растворе.
Композиция может быть использована для определения нитрат-ионов в сыворотке крови, моче, спинномозговой жидкости, экссудате, транссудате и других биологических материалах с использованием фотометра.
Перед использованием указанной композиции реагентов для количественного определения метаболитов оксида азота в биологических жидкостях пробы биологических жидкостей освобождают от белка путем добавления 35% раствора сульфосалициловой кислоты с последующим добавлением заявляемой композиции.
Способ осуществляется следующим образом: в полипропиленовую пробирку вносят 1 мл сыворотки крови и добавляют 100 мкл 35% раствора сульфосалициловой кислоты. Смесь тщательно перемешивают на смесителе Vortex до гомогенного состояния и инкубируют 20 мин при комнатной температуре, затем центрифугируют при 5000 об/мин в течение 20 мин для осаждения белка. Прозрачную надосадочную часть (супернатант) крови переливают в чистую пробирку, тщательно перемешивают с заявляемым составом для определения нитрат-ионов в биологических жидкостях из расчета 20 мг на 1 мл супернатанта и инкубируют в течение 10 минут при комнатной температуре.
После центрифугирования пробы (3000 об/мин 10 мин) супернатант переносят в кювету для фотометрического определения содержания метаболитов оксида азота при длине волны 520 нм.
Пример 1
Композицию готовят путем смешивания при тщательном перетирании винной кислоты, сульфаниловой кислоты, аммония ацетата, аммония бромида, динатриевой соли хромотроповой кислоты и цинковой пыли до образования гомогенного порошка.
Указанная композиция оптимальна для фотометрического определения нитрат-ионов в сыворотке крови по следующей методике:
Содержание нитрат-ионов определяют по заранее построенному градуировочному графику с известными концентрациями рабочего раствора от 500 мкМ/л NaNO3 с последующим разведением в тех же условиях, что и обработка проб, в координатах оптическая плотность - концентрация нитрат-ионов, мкМ/л. Диапазон определяемых концентраций 15,6-500 мкМ/л, Sr=0,08.
Конкретные примеры заявляемых композиций приведены в табл.1.
Количественный состав композиции
Проведенные исследования показали, что уменьшение содержания цинковой пыли в составе менее 2 мас. частей приводит к замедлению процесса восстановления (Пример 1).
При использовании композиции с содержанием цинковой пыли более 6 мас. частей происходит восстановление образующегося красителя, вследствие чего раствор обесцвечивается (Пример 3).
Уменьшение содержания аммония бромида менее 5 мас. частей увеличивает время развития окраски и снижает экспрессность определения. Увеличение содержания аммония бромида более 20 мас. частей нецелесообразно, так как повышает расход реактивов.
При уменьшении содержания ацетата аммония менее 5 мас. частей сужается рабочий диапазон кислотности исследуемого раствора. Увеличение содержания ацетата аммония более 15 мас. частей для поддержания необходимой кислотности нецелесообразно и приводит к излишнему расходу реагентов (Примеры 1-3). Оптимальный состав смеси представлен в примере 2, именно такой состав устойчив и позволяет работать в необходимом диапазоне кислотности без дополнительного подщелачивания рабочего раствора.
Использование предложенного состава позволяет быстро и с высокой точностью определить содержание нитрат-ионов в биологических материалах и применить полученные данные для диагностики различных форм патологии. Состав экономичен при использовании и позволяет проводить одновременно исследование более 100 аналитов.
Пример использования композиции для диагностики
Для определения диагностического значения количественного анализа суммарных концентраций метаболитов оксида азота было проведено клинико-лабораторное обследование 238 детей в возрасте от 2 до 17 лет (средний возраст 8,7±1,8 года) с различными формами хронической бронхолегочной патологии и длительностью заболевания от 1 года до 12 лет (в среднем 6,3±1,5 года). Из них было 73 больных ребенка с хронической пневмонией (30,7%), 81 - с врожденными пороками развития легких и бронхов (34,0%), 49 - с бронхиальной астмой (20,6%), 15 - с альвеолитами (6,3%), 10 - с муковисцидозом (4,2%) и 10 детей с хроническим бронхитом (4,2%). Референтную группу составили 18 условно здоровых детей. В таблице 2 приведены средние значения суммарной концентрации метаболитов NO для групп больных детей с различной активностью хронического воспалительного процесса в легких.
Содержание метаболитов оксида азота в сыворотке крови при хронических воспалительных бронхолегочных заболеваниях
Как следует из представленных данных, наиболее значительное увеличение эндогенной продукции оксида азота было отмечено прежде всего у больных муковисцидозом. У этих больных концентрации метаболитов оксида азота в крови - 58,45±5,26 мкМ/л в 2,5 раза (Р<0,01) превышали их уровни у детей референтной группы (23,57±2,35 мкМ/л).
Выраженное повышение содержания метаболитов оксида азота было установлено также у больных с врожденными пороками развития легких и бронхов с распространенным и гнойным эндобронхитом (47,68±3,43 мкМ/л). При этом было выявлено, что на уровень эндогенной продукции оксида азота особенно влияет распространенность воспалительного бронхолегочного процесса: при двусторонней локализации процесса у детей с хронической пневмонией содержание метаболитов оксида азота (46,72±3,85 мкМ/л) более чем в 1,9 раза (Р<0,05) превышало их уровни у детей референтной группы и было в 1,4 раза большим (Р<0,05) по сравнению с их концентрациями у больных с односторонней локализацией бактериального воспаления (33,36±3,78 мкМ/л).
Таким образом, при хроническом течении воспалительных заболеваний легких у детей оксид азота синтезируется в больших количествах как активный медиатор и эффектор антипатогенной защиты.
Следовательно, предлагаемая композиция в качестве индикаторного порошка для определения метаболитов оксида азота в биологических материалах позволяет быстро и эффективно провести диагностику хронических воспалительных заболеваний у значительного числа больных одновременно, что имеет медико-социальное значение.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОСТАВ ДЛЯ ОПРЕДЕЛЕНИЯ НИТРАТ-ИОНОВ В РАСТВОРАХ | 1997 |
|
RU2141115C1 |
| СПОСОБ ДИАГНОСТИКИ АКТИВНОСТИ ВОСПАЛЕНИЯ ПРИ ХРОНИЧЕСКОЙ ПНЕВМОНИИ У ДЕТЕЙ | 2005 |
|
RU2305845C1 |
| СПОСОБ РАННЕЙ ДИАГНОСТИКИ РАЗЛИЧНЫХ ФОРМ ЭССЕНЦИАЛЬНОЙ АРТЕРИАЛЬНОЙ ГИПЕРТЕНЗИИ У ДЕТЕЙ И ПОДРОСТКОВ | 2016 |
|
RU2648453C1 |
| РЕАГЕНТ ДЛЯ КОЛОРИМЕТРИЧЕСКОГО И ФОТОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ НИТРИТОВ В ВОДНЫХ РАСТВОРАХ | 1992 |
|
RU2038579C1 |
| Способ выявления онкологических заболеваний и устройство для его осуществления | 2020 |
|
RU2755073C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ НИТРАТВОССТАНАВЛИВАЮЩЕЙ СПОСОБНОСТИ БИОЛОГИЧЕСКОЙ ЖИДКОСТИ | 1994 |
|
RU2114435C1 |
| СПОСОБ ЛЕЧЕНИЯ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ ЖЕЛУДКА И ДВЕНАДЦАТИПЕРСТНОЙ КИШКИ У ДЕТЕЙ | 2012 |
|
RU2483761C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ЭНДОТЕЛИОПРОТЕКТОРНОЙ АКТИВНОСТЬЮ | 2017 |
|
RU2643605C1 |
| СПОСОБ ДИАГНОСТИКИ ЛЕГОЧНОЙ ДЕСТРУКЦИИ ПРИ ОСТРОЙ ПНЕВМОНИИ У ДЕТЕЙ РАННЕГО ВОЗРАСТА | 2003 |
|
RU2235333C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ХРОНИЧЕСКОГО ВИРУСНОГО ГЕПАТИТА И ЦИРРОЗА ПЕЧЕНИ | 2008 |
|
RU2383021C1 |
Изобретение относится к биотехнологии, в частности к медицине, и может быть использовано для определения содержания метаболитов оксида азота в сыворотке крови. Изобретение представляет собой способ определения метаболитов оксида азота в сыворотке крови с помощью композиции, содержащей цинковую пыль, аммония бромид, винную кислоту, аммония сукцинат, аммония ацетат, сульфаниловую кислоту и динатриевую соль хромотроповой кислоты. Изобретение позволяет быстро и эффективно провести диагностику хронических воспалительных заболеваний у значительного числа больных одновременно, что имеет медико-социальное значение, а также за счет введения в композицию ацетата аммония в количестве 5,0-15,0 мас. частей в качестве подщелачивающего агента позволяет исключить из аналитической процедуры этап подщелачивания путем добавления раствора NaOH и повысить экспрессность и точность определения нитрат-ионов в биологических материалах, а ацетат аммония в смеси с винной кислотой обеспечивает оптимальную кислотность, что способствует одновременному протеканию процессов восстановления, диазотирования и азосочетания. 2 табл.
Способ определения содержания метаболитов оксида азота в сыворотке крови у больных хроническими воспалительными бронхолегочными заболеваниями, характеризующийся тем, что в пробирку вносят 1 мл сыворотки крови и добавляют 100 мкл 35%-ного раствора сульфосалициловой кислоты, смесь тщательно перемешивают на смесителе Vortex до гомогенного состояния и инкубируют 20 мин при комнатной температуре, затем центрифугируют при 5000 об/мин в течение 20 мин для осаждения белка, затем супернатант крови переливают в чистую пробирку, тщательно перемешивают с композицией, содержащей цинковую пыль, аммония бромид, винную кислоту, аммония сукцинат, аммония ацетат, сульфаниловую кислоту и динатриевую соль хромотроповой кислоты при следующем соотношении компонентов, мас.ч.:
из расчета 20 мг на 1 мл супернатанта при рН 6-8 и инкубируют в течение 10 мин при комнатной температуре, затем центрифугируют пробы при 3000 об/мин 10 мин, супернатант переносят в кювету для фотометрического определения содержания метаболитов оксида азота при длине волны 520 нм.
| СОСТАВ ДЛЯ ОПРЕДЕЛЕНИЯ НИТРАТ-ИОНОВ В РАСТВОРАХ | 1997 |
|
RU2141115C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ НИТРАТВОССТАНАВЛИВАЮЩЕЙ СПОСОБНОСТИ БИОЛОГИЧЕСКОЙ ЖИДКОСТИ | 1994 |
|
RU2114435C1 |
| Tsikas D | |||
| et | |||
| al | |||
| Прибор для нагревания перетягиваемых бандажей подвижного состава | 1917 |
|
SU15A1 |
| - J | |||
| Chromatogr В Biomed Appi, 1994 Nov 18; 661(2):185-9 | |||
| Tsikas D | |||
| et | |||
| al | |||
| Gas chromatographic-tandem mass | |||
Авторы
Даты
2008-07-27—Публикация
2007-03-01—Подача