Изобретение относится к медицине, биотехнологии и фармацевтике и может быть использовано для профилактики и лечения неврологических заболеваний.
Все неврологические заболевания условно подразделяются по двум основным признакам: функциональные нарушения, когда структурные элементы органа еще не пострадали, и органические поражения, когда страдает сама структура. Если функциональные расстройства могут быть полностью восстановлены, то органические - только за счет новых элементов, старые уже повреждены. Наиболее известные органические заболевания нервной системы: болезнь Альцгеймера, Паркинсона, рассеянный склероз, боковой амиотрофический склероз, последствия инсультов, нейротравм и пр.
Многие заболевания нервной системы, включая рассеянный склероз, характеризуются повреждениями нервной ткани в результате какого-либо инфекционного или аутоиммунного процесса (рассеянный склероз, боковой амиотрофический склероз), перенесенных нейроинфекций (клещевой энцефалит), нарушений мозгового кровообращения (инсульт), после травмы и пр., а также повреждениями проводящих путей (аксональных связей) между нейронами (аксонопатия).
Известно применение для лечения неврологических заболеваний лекарственного препарата КОРТЕКСИН. Согласно фармацевтической статье №99/136/14 от 09.07.1998 г. КОРТЕКСИН представляет собой комплексный препарат, состоящий из полипептидного комплекса (50%) и глицина (50%).
КОРТЕКСИН применяют для больных при черепно-мозговой травме, нарушениях мозгового кровообращения, вирусных и бактериальных нейроинфекциях, астенических состояниях, энцефалопатиях различного генеза, острых и хронических энцефалитах и энцефаломиелитах, эпилепсии, нарушениях памяти, мышления, сниженной способности к обучению, надсегментарных вегетативных расстройствах различных формах детского церебрального паралича, задержке психомоторного и речевого развития у детей.
КОРТЕКСИН обладает тканеспецифическим действием на кору головного мозга, оказывает церебропротекторное (защищает мозг), ноотропное (улучшает обменные процессы нейрона), противосудорожное действие, снижает токсические эффекты нейротропных веществ, улучшает процессы обучения и памяти, стимулирует репаративные процессы в головном мозге (восстановление структуры ткани). Механизм действия Кортексина связан с его метаболической (обмен веществ) активностью: препарат регулирует соотношение тормозных и возбуждающих аминокислот, уровень серотонита и дофамина (одни из множества важных белков, регулирующих в основном внутримозговые функции), оказывает гамкергическое действие, обладает антиоксидантной активностью и способностью восстанавливать биоэлектрическую активность головного мозга. При описании действия КОРТЕКСИНА приводится достаточно широкий спектр состояний, когда препарат оказывался эффективным.
Однако эффекты КОРТЕКСИНА ограничены головным мозгом и не имеется данных о действии препарата на периферии, в частности на проводящие пути нервной системы, а именно на регенерацию аксонов. Кроме того, отсутствуют сведения об иммуномодулирующем действии КОРТЕКСИНА при аутоиммунных заболеваниях. Многие заболевания центральной нервной системы, в том числе рассеянный склероз имеют аутоиммунный механизм, а повреждение нейронов - следствие аутоиммунной атаки. Отсутствие точных биохимических характеристик препарата (действие препарата неопределенно вследствие того, что сам экстракт не может иметь формулы из-за его сложной структуры, а также в связи с вариабельностью биологических характеристик исходного сырья) не дает возможности его стандартизации. Препарат получается из потенциально небезопасного сырья (мозг крупного рогатого скота), сведения о проведении контроля на прионовую безопасность (отсутствие возбудителя губчатого энцефалита - «коровьего бешенства») отсутствуют (очевидно, этот контроль просто не производится).
Известно лекарственное вещество того же назначения по отношению к заявленному изобретению - эритропоэтин (далее - ЭПО) - гормон организма млекопитающих, в том числе человека, продуцируемый интерстициальными клетками почек и регулирующий эритропоэз у млекопитающих. Циркулирующий в крови гликопротеидный гормон ЭПО обеспечивает контроль дифференцировки клеток эритроидного ряда, т.е. представляет собой высокоспецифичный природный индуктор эритропоэза.
В 1986-1987 гг. были проведены клинические испытания рекомбинантного ЭПО (РЭПО), продуцируемого клетками млекопитающих (Eschbach J.W., Egrie J.C., Dowing M.R., et al., N.Eng.J.Med., 316. 73-78, 1987; Jelkmann W., Curr. Pharmaceut. Biotechnol., 1, 11-31, 2000), и он с успехом был введен в клиническую практику для коррекции анемии, связанной с хронической почечной недостаточностью в 1989 г., и утвердился в качестве золотого стандарта высокоспецифического лечения данного заболевания. В настоящее время РЭПО широко применяется для лечения больных в областях, связанных со стимуляцией гемо- и эритропоэза.
РЭПО обладает высокой специфичностью и действует в очень низких концентрациях при практически полном отсутствии побочных эффектов. Рекомбинантный ЭПО почти полностью идентичен природному гормону и представляет собой семейство близкородственных белков с одинаковой полипептидной цепью, включающей 165 аминокислот, ковалентно связанных с четырьмя разветвленными олигосахаридными цепями, составляющими около 40% общей массы молекулы 30400 Д. Олигосахаридные цепи терминально сиалированы, причем степень модификации, достигающая 14 остатков сиаловых кислот на молекулу ЭПО, служит доминирующим фактором, ответственным за проявление гематопоэтической активности in vivo (Strickland T.W., U.S. Patent, 5856298, 5 Jan., 1999).
В настоящее время установлено (Grasso G., Sfacteria A., Cerami A., Brines M., Neuroscientist, 10, 93-98, 2004), что РЭПО способен предотвращать спазм сосудов, развитие воспалительного процесса и индукцию апоптоза не только у кроветворных клеток, но и у многих других типов клеток - нейронов, кардиомиоцитов и пр. Показано (Jelkmann W., Current Pharmaceut. Biotechnol., 6, 65-79, 2005), что молекулы РЭПО могут преодолевать гематоэнцефалический барьер и уменьшать площадь некротического поражения коры головного мозга при инсультах, стимулировать частичную регенерацию аксонов. На моделях рассеянного склероза продемонстрирована (Sattier M.B., Merkler D., Maier К., Stadelman С., Enhreich H., Bahr M., Diem R., Cell. Death. Differ., 11, Suppl. 2, S181-92, 2004.) способность РЭПО уменьшать демиелинизацию и повреждение аксонов. Нейротропное действие РЭПО показано также для нейронов спинного мозга (церебральная ишемия, компрессия спинного мозга, ишиаз) и периферических нервных клеток. В связи с выявленными новыми свойствами РЭПО рассматривается в качестве перспективного препарата для лечения широкого спектра неврологических заболеваний, характеризующихся аксонопатией.
Как известно, рекомбинантный человеческий эритропоэтин имеет несколько изоформ. Клетки, производящие рекомбинантный эритропоэтин, синтезируют приблизительно 15 различных изоформ, отличающихся содержанием сиаловых кислот от 0 до 14 молекул на молекулу эритропоэтина. Смесь изоформ разделяется на фракции по содержанию сиаловых кислот.Фракция, содержащая изоформы (6 шт.) со средним количеством сиаловых кислот не менее 10 молекул на молекулу эритропоэтина, составляет фракцию высокосиалированного эритропоэтина (ВЭПО), который и используется в настоящее время для лечения анемии. До настоящего времени интересы производителей направлены на производство и сохранение клеточных линий, секретирующих (выделяющих) ЭПО, обладающий большим эффектом в отношении стимуляции гемо-эритропоэза. Это, в частности, достигается за счет увеличения содержания в ЭПО сиаловых кислот, заряда молекулы и продолжительности ее жизни в организме. Низкосиалированные формы ЭПО (НЭПО), являющиеся в существующих технологиях отходами производства, удаляются в процессе очистки препарата для повышения его эффективности при лечении анемий.
Однако эксперименты на животных показывают, что дозы РЭПО, используемые для лечения заболеваний головного мозга, должны быть существенно выше, чем при лечении анемии (Digicaylioglu M., Lipton S.A., Nayure, 412. 641-647, 2001). Фармакологические дозы ЭПО стимулируют продукцию гиперреактивных тромбоцитов, что может приводить к тромбозам (Brines M.L., Chezzi P., Keenan S., Agnello D., de Lanerolle N.C., Cerami C., Itri L.M., Cerami A., Proc. Natl. Acad. Sci. USA., 97, 10526-10531, 2000). Многократное введение РЭПО может также вызвать увеличение массы красных кровяных клеток. На моделях с использованием животных показано, что ЭПО - зависимое увеличение гематокрита может вызывать и амплифицировать повреждения мозга (Xenocostas A, Cheung W.K., Farrell F.X., et al., Proc. Am. Soc. Clin. Oncol., 22, 230, 2003).
С целью исключения гематопоэтического действия препарата, в результате обработки нейроминидазой были изучены защитные свойства формы эритропоэтина, полностью лишенной сиаловых кислот (асиалированный ЭПО), (Erbayraktar S., Grasso G., Sfacteria A., et al., Proc. Natl. Acad. Sci. USA, 100. 6741-6746. 2003). Оказалось, что при очень коротком времени жизни в плазме и, как следствие, отсутствии эритроидной активности асиалированный ЭПО в фармакологических дозах проникает через гематоэнцефалический барьер, связывается с рецепторами ЭПО в коре и гиппокампе и обладает защитными свойствами, аналогичными сиалированному эритропоэтину (Brines М, Cerami A., Cerami С., U.S. Patent, 0034799 А1, 16 Feb., 2006). Недостатком подобного препарата для практического применения является очевидная технологическая сложность его получения и низкая стабильность в водных растворах.
В водных растворах эритропоэтин является очень нестабильным веществом. Концентрация гормона в препаратах составляет десятки микрограммов на мл и он легко инактивируется за счет факторов окружающей среды, в том числе за счет адгезии к поверхности сосудов из стекла и пластика.
Известен препарат ЭПО «Эритростим» (ФС 42-3656-98), содержащий альбумин сыворотки крови человека в качестве стабилизатора. Недостатками препарата являются возможность контаминации инфекционными вирусами, аллергенность для лиц с повышенной чувствительностью к препаратам белков крови, высокая стоимость апирогенных препаратов человеческого альбумина.
Из известных препаратов близким по составу к предлагаемому является водный раствор высокосиалированного ЭПО, содержащий в качестве стабилизатора низкомолекулярный декстран с молекулярной массой 30000-60000 в концентрации 6-10 мас.%. Раствор содержит также хлористый натрий, цитрат натрия и лимонную кислоту для создания изотонии и рН 6,5-7,5. Количество ЭПО составляет 5-40 мкг на мл раствора. Раствор может быть получен добавлением цитрата натрия и лимонной кислоты к плазмозаменяющему раствору «Реополиглюкин».
Наиболее близким лекарственным препаратом аналогичного назначения, выбранным в качестве прототипа, является известная («Стабилизированный водный раствор эритропоэтина» RU 2128517 С1, 04.10. 1999) фармацевтическая композиция (далее - ФК), содержащая высокосиалированный ЭПО в качестве активного вещества и раствор низкомолекулярного декстрана (реополиглюкин) в качестве стабилизатора.
Задачей настоящего изобретения является расширение арсенала эффективных лекарственных средств для неврологических заболеваний.
Основной технический результат, получаемый при осуществлении изобретения, заключается в реализации данного назначения: создании нового, более эффективного препарата для лечения неврологических заболеваний.
Данный технический результат достигается за счет того, что в известной фармацевтической композиции в качестве ее активного начала используются низкосиалированные формы эритропоэтина с содержанием 6-8 остатков сиаловых кислот на молекулу белка.
В графических материалах на диаграммах представлено:
Фиг.1 - выживаемость клеток TF1 в отсутствие G-CSF при добавлении 15 нг/мл НЭПО и ЭПО.
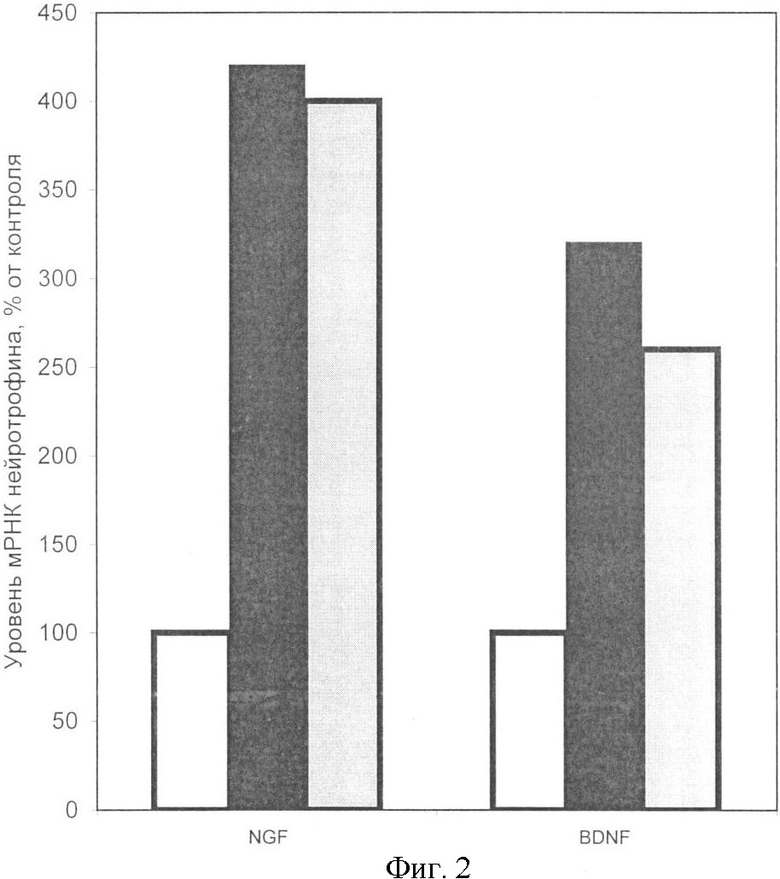
Фиг.2 - влияние препаратов НЭПО и ЭПО в концентрации 3 нМ на экспрессию нейротрофических факторов в культивируемых клетках астроцитов коры больших полушарий мозга крысы после инкубации в течение 4 час (белый - контроль, черный - НЭПО, серый - ЭПО).
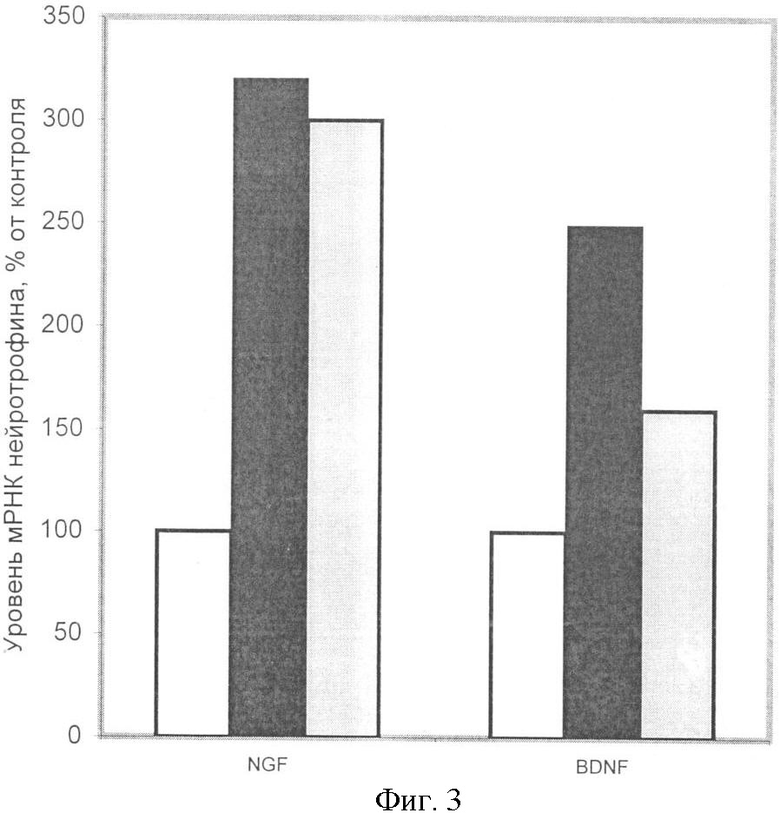
Фиг.3 - влияние препаратов НЭПО и ЭПО на экспрессию нейротрофический факторов в коре мозга крысы через 1 час после внутрибрюшинного введения препарата (100 мкг/кг веса).
Смысл изобретения заключается в использовании изоформ эритропоэтина, обладающих низкой гематопоэтической активностью, но полностью сохраняющих способность взаимодействовать с нервными клетками.
В предлагаемой фармацевтической композиции количество активного вещества составляет 50-500 мкг/мл или 0,005-0,05% от общей массы. Интервал содержания активного вещества обусловлен необходимым содержанием ЭПО в инъекционной форме препарата, т.е. его возможной минимальной и максимальной одноразовой дозой. Стабилизатором ЭПО в ФК может служить раствор низкомолекулярного декстрана (10%) - реополиглюкин, который использован для получения растворов низкосиалированной формы ЭПО в концентрации 50-500 мкг на мл раствора, либо другие синтетические стабилизирующие добавки, выбранные из группы, включающей полиэтиленгликоль, белки, сахара, аминокислоты и т.д. Реополиглюкин является разрешенным медицинским препаратом который благодаря высокому содержанию полисахаридов (10%) проявляет высокие стабилизирующие свойства с полным сохранением активности ЭПО. В результате, содержание активного препарата в растворах сохраняется в течение года при хранении в темном месте при 2-5°С.
Биологическая активность растворов была определена в тестах in vitro с использованием клеток TF-1 (фиг.1).
Концентрацию низкосиалированного ЭПО в водных растворах после их получения и по истечении одного года хранения определяли спектрофотометрически, исходя из значения оптической плотности субстанции при 280 нм с коррекцией на светорассеяние при 400 нм, например:
C=1,34(A280-A400),
где с - рассчитываемая концентрация ЭПО,
А280 - значение поглощения при 280 нм,
А400 - значение поглощения при 400 нм,
1,34 - коэффициент экстинкции низкосиалированного ЭПО (значение оптической плотности при 280 нм раствора с концентрацией 1 мг/мл).
Анализ показал, что содержание препарата в водном растворе после хранения при 5°С составляет 97% от номинальной.
Заявляемый препарат обладает низкой гематопоэтической активностью (порядка 10% от стандартного препарата ЭПО «Эритростим»). Исследование токсичности препарата показало, что дозы, характеризующие токсичность, не определяются: ЛД50 для мышей составляет более чем 7 мг/кг, для крыс - более чем 9 мг/кг.
Уменьшение содержания сиаловых кислот приводит к потере стабильности гормона in vivo, но не влияет на его активность in vitro. Уменьшение стабильности при лечении неврологических заболеваний является преимуществом вследствие того, что эффект препарата не аккумулируется и препарат, подействовав, разрушается обычным физиологическим путем.
В таблице 1 приведены сравнительные характеристики РЭПО и его низкосиалированной формы, которая используется в заявленной фармацевтической композиции (ФК).
Данные по активности высокосиалированного и низкосиалированного препарата, приведенные в таблице, получены нами в соответствии с рекомендациями ФС 42-3658-98 от 11.02.1999. Принципиально они соответствуют данным, приведенным в патенте US 5856298.
Сравнительное исследование нейрофизиологической активности препаратов РЭПО и низкосиалированного ЭПО проводили в экспериментах in vitro и in vivo, изучая их влияние на регуляцию экспрессии нейротофических факторов NGF и BDNF. Нейротрофины - семейство регуляторных белков нервной ткани, которые синтезируются нейронами и клетками нейроглии, и способствуют дифференцировке и поддержанию жизнеспособности и функционирования периферических и центральных нейронов. При этом используется аутокринный и паракринный механизмы регуляции. Нейротрофины регулируют нейрональную дифференцировку, индуцируют ветвление дендритов (арборизацию) и рост аксонов (спрутинг) в направлении клеток-мишеней. В зрелой нервной системе нейротрофины регулируют как краткосрочную синаптическую передачу, так и долговременное потенцирование, участвуя таким образом в обеспечении пластичности нервной системы, необходимой для ее нормального функционирования. Регуляция экспрессии нейротрофинов и их рецепторов в мозге в настоящее время рассматривается как один из самых перспективных путей воздействия на ряд патологических состояний ЦНС, связанных с дегенерацией и гибелью нейронов. В то же время известные к настоящему времени соединения, способные регулировать экспрессию нейротрофинов в мозге, например антидепрессанты, обладают негативными побочными эффектами, ограничивающими их использование.
Для культивируемых нейроглиальных клеток коры больших полушарий крысы показано, что в концентрации 3 нМ происходит статистически достоверная стимуляция экспрессии как BDNF, так и NGF в 2-5 раз по сравнению с контролем через 1 и 4 часа после введения препаратов. Наиболее высокая стимуляция экспрессии нейротрофического фактора BDNF через 4 часа после введения отмечена для низкосиалированной формы ЭПО, которая составила 340% от контроля (Фиг.2).
Аналогичный результат был получен при исследовании влияния препаратов на экспрессию NGF и BDNF в коре головного мозга in vivo. Через час после введения РЭПО и его низкосиалированной формы происходит статистически достоверная стимуляция экспрессии обоих нейротрофинов в 2-3 раза (Фиг.3).
Пример 1 (изготовление лекарственной формы)
К реополиглюкину добавляют цитрат натрия и лимонную кислоту с доведением рН раствора до 6,5-7,5 и затем добавляют субстанцию низкосиалированной формы эритропоэтина. Полученный раствор подвергают стерилизующему фильтрованию с использованием фильтровальных элементов Millex (Millipore) 0,22 мкм. Полученные растворы помещают в ампулы из нейтрального стекла или стеклянные флаконы из дрота вместимостью 3-5 мл. Ампулы и флаконы закрывают резиновыми пробками и обкатывают алюминиевыми колпачками.
Пример 2
Для исследования цитопротекторной активности низкосиалированного ЭПО в сравнении с РЭПО использовали человеческую эритролейкозную клеточную линию TF-1, которая применяется для тестирования различных цитокинов (IL-3, IL-5, GM-CSF, ЕРО), NGF, TGF-B. Эти универсальные клетки могут быть использованы как в пролиферативном, так и в антиапоптотическом вариантах теста для определения биологической активности экзогенных клеточных регуляторов.
Клетки TF-1, как и другие клетки эритроидного ряда, содержат 2 типа эритропоэтиновых рецепторов (EpoR) - высокоаффинный (EpoR2) и низкоаффинный (EpoR1). Рецептор EpoR2 характерен только для эритроидных клеток. EpoR1 обнаружен в клетках различного происхождения: кардиомиоцитах, периферических нейронах, клетках головного мозга (нейроны, глиальные клетки, астроциты) и т.д. (Leist M., Chezzi P., Grasso G., Bianchini R.,et al., Science, 305, 239-242). Наличием низкоаффинных рецепторов (EpoR1) объясняется, по-видимому, антиапоптотическое действие Еро на неэритроидные клетки как in vitro, так и in vivo.
Препараты ЭПО исследовали в пролиферативном тесте (MTS-test - CellTiter 96 Aqueous Solution Cell Proliferation Assay, Promega). Цитопротекторная активность препаратов изучалась при удалении из среды культивирования GM-CSF.
Клетки TF-1 рассевали в 96-луночные платы по 10000 клеток на лунку в среде следующего состава: RPMI 1640, 10 mM HEPES, 20 тМ глюкоза, 2% FCS и инкубировали при 37°С, 5% CO2 3 суток с различными концентрациями препаратов. Количество живых клеток в лунках определяли после окрашивания MTS и анализа результатов считывания на Мультискане при 650 нм. Показано, что наблюдается линейная зависимость выживаемости клеток TF-1 в диапазоне концентраций обоих препаратов ЭПО от 0,05 до 5 МЕ/мл. При этом цитопротекторная активность низкосиалированного ЭПО на 30-50% выше, чем у его высокосиалированной формы (Фиг.1).
Пример 3
Первичную культуру клеток нейроглии получали согласно стандартной методике. Крыс линии Sprague-Dowly возраста 1-3 дня забивали с помощью углекислотной асфиксии (15 минут) и помещали на 1 минуту в 80% водный раствор этанола. Далее все операции проводили в асептических условиях при температуре 4-7°С. Выделенный мозг помещали в раствор Хэнкса и далее выделяли кору больших полушарий, освобождая ткань от оболочек. Выделенную ткань один раз промывали раствором Хэнкса и переносили в среду MEM/F12 (1:1), содержащую 20% эмбриональной сыворотки коровы и 2 мМ L-глютамина. Ткань диссоциировали на отдельные клетки механически. Полученную клеточную суспензию один раз промывали средой того же состава с помощью центрифугирования при 200 g. Клетки засевали плотностью 200 тыс.клеток/см2 на обработанные поли-L-лизином культуральные флаконы площадью 75 см2. Культивирование клеток проводили в CO2-инкубаторе при 37°С в атмосфере, содержащей 5% CO2 и 95% воздуха, в среде MEM/F12, содержащей 15% эмбриональной сыворотки коровы, 6 г/л D-глюкозы, 2 мМ L-глютамин, 25 мг/л инсулина, 100 мг/л трансферрина, 20 нМ прогестерона, 100 нМ путресцина и 30 нМ селенита натрия, 100 мкг/мл гентамицина. Культуральную среду меняли каждые 3-4 дня. Пересев клеток проводили после достижения монослоя в соотношении 1:3 (время достижения монослоя 1.5-2 недели).
Для выделения тотальной РНК использовали полученные после третьего пересева клетки: плотностью 100 тыс/см2 высевали на обработанные поли-L-лизином 6-луночные культуральные планшеты в указанной культуральной среде. После достижения клетками монослоя культуральную среду заменяли на бессывороточную (указанная среда без эмбриональной сыворотки коровы). После 48 ч инкубации в среду вводили стерильные растворы (40 мкл) тестируемых соединений до конечной концентрации 3 нМ (3 параллели на точку). В качестве контроля вводили равный объем 0.9% раствора NaCl в воде. Через указанные промежутки времени отбирали культуральную среду, клетки промывали холодным фосфатно-солевым буфером и выделяли тотальную РНК фенолхлороформным методом с использованием набора YeliowSolve (Клоноген, Россия) с использованием методики производителя. Чистоту и концентрацию РНК в полученных образцах проводили спектрофотометрически и в дальнейших экспериментах использовали образцы с соотношением А260/А280≥1.6.
Для проведения обратной транскрипции отбирали 1 мкг тотальной РНК и проводили реакцию 1 час при 37°С в среде, содержащей 8 ед/мл Moloney Murine Leukemia Virus (М-MLV-)-обратную транскриптазу, 10 мМ дитиотрейтол, 800 мкМ dNTPs, случайные гексапраймеры (20 мкг/мл) и first-strand buffer (50 мМ Трис-HCl, 75 мМ KCl, 3 мМ MgCl2) в объеме 25 мкл. После последующей инкубации 10 минут при 70°С образцы полученной кДНК хранили при -20°С.
Оценку уровня экспрессии BDNF мРНК проводили с использованием количественной ПЦР в реальном времени (real-time quantitative PCR, система М×3000Р, Stratagene). Применяли высокоспецифичный dsДНК-связывающий краситель SYBR green I. Реакцию проводили в смеси объемом 25 мкл, содержащей 2 мкл кДНК образца или стандарта, или 2 мкл воды (негативная проба), 250 мкМ смеси дНТФ (дезоксинуклеозидтрифосфаты), 2.5 мМ MgCl2,15 мМ Трис-HCl (рН 8.8), 50 мМ KCI, 0,5% глицерола, 0.1% Tween 20, интеркалирующий краситель SYBR Green I, 1 ед Taq ДНК-полимеразу с ингибирующими активность фермента антителами ("Синтол", Россия) и по 10 пмоль смысловых и антисмысловых праймеров ("Синтол", Россия; Таблица) при следующих условиях: старт - 5 минут при 95°С, затем 40 циклов, включающих плавление - 30 секунд при 95°С, отжиг - 30 сек при 68°С, элонгация - 30 секунд при 72°С с детекцией флуоресценции в конце каждого шага элонгации.
Для подтверждения специфичности продуктов амплификации после окончания амплификации образцы охлаждали до 60°С и через 20 минут получали кривые плавления нагреванием до 95°С со скоростью 0.03°С/сек с непрерывной детекцией флуоресценции. Для получения калибровочных кривых смесь кДНК образцов последовательно разбавляли водой, свободной от ДНКаз, получали стандартные растворы с известной относительной концентрацией соответствующего продукта. С использованием программного обеспечения производителя определяли номер цикла, соответствующий максимальному ускорению процесса амплификации, получали калибровочную кривую числа данных циклов от относительной концентрации продукта и определяли относительную концентрацию в неизвестном образце с последующей нормализацией по бета-актину.
В результате экспериментов проведено тестирование способности препаратов РЭПО и низкосиалированного ЭПО регулировать экспрессию наиболее изученных нейротрофинов BDNF (brain-derived neurotrophic factor) и NGF (nerve growth factor) в культивируемых астроцитах коры больших полушарий крысы. Для этого с использованием метода количественной ОТ-ПЦР в реальном времени (полимеразная цепная реакция продуктов обратной транскрипции) протестирована способность препаратов влиять на экспрессию на уровне мРНК генов BDNF и NGF в культивируемых астроцитах коры больших полушарий мозга крысы.
В результате проведенных исследований было показано, что при введении культуральную среду обоих препаратов в концентрации 3 нМ обнаружено сильное изменение экспрессии как BDNF, так и NGF, составляющее 2-5 раз по сравнению с контролем. Такое увеличение экспрессии является длительным и наблюдается через 4 ч после введения (Фиг.2). Наиболее значительным и длительным эффектом на увеличение экспрессии BDNF обладает препарат низкосиалированного ЭПО. По сравнению с контролем экспрессия BDNF составила 340% (Фиг.2).
Пример 4
Для сравнительного исследования влияния препаратов РЭПО и низкосиалированной формы ЭПО на экспрессию NGF и BDNF в коре головного мозга in vivo использовали самцов крыс линии Вистар, массой 200 г.Изучаемые препараты однократно вводили внутрибрюшинно в дозе 100 мкг/кг массы животного. Контрольным животным вводили растворитель. В каждой группе было по четыре животных. Через 1 ч после введения препарата крыс забивали с помощью углекислотной асфиксии и сразу после этого выделяли фронтальную кору мозга. Ткань замораживали в жидком CO2 и хранили при - 80°С. Выделение тотальной РНК, обратную транскрипцию и ПЦР, а также оценку уровня экспрессии нейротрофинов проводили аналогично описанному выше.
В результате проведенного исследования обнаружено, что через час после введения как РЭПО, так и низкосиалированного ЭПО, происходит статистически достоверная стимуляция экспрессии обоих нейротрофинов в 2-3 раза (фиг.3).
Таким образом, в результате проведенных исследований было показано, что при введении РЭПО и его низкосиалированного ЭПО, как in vitro так и in vivo, обнаружено сильное изменение экспрессии BDNF и NGF, составляющее 2-5 раз по сравнению с контролем. Такое увеличение экспрессии является длительным и наблюдается через как через 1 ч, так и через 4 ч после введения. Наиболее значительным и длительным эффектом на увеличение экспрессии BDNF обладает препарат низкосиалированного ЭПО.
Поддержание жизнеспособности нейронов является NGF- и BDNF-зависимым процессом, осуществляемым нейроглиальными клетками. Можно предположить, что увеличение экспрессии NGF и BDNF под действием рекомбинантного эритропоэтина и его низкосиалированной формы является одним из основных молекулярных механизмов терапевтического действия гормона на центральную нервную систему. Поскольку BDNF обладает высокой нейропротекторной и нейротрофической активностью, то на основе низкосиалированного ЭПО возможно создание фармпрепарата, проявляющего активность при нейродегенеративных заболеваниях.
Активное вещество новой фармацевтической композиции (никосиалированный ЭПО) может быть создано на основе модификации существующей технологии получения рекомбинантного ЭПО (Зеленин М.Г., Крамерова И.А., Колобков С.Л., Филякина Н.С., Филатов И.А, RU 2089611 С1, 09.10.1995) путем:
- отбора из банка клеточных линий эффективных продуцентов ЭПО с повышенным содержанием низкосиалированных форм;
- очистки и фракционирования пула ЭПО с целью более полного извлечения низкосиалированных изоформ.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИММУНОМОДУЛИРУЮЩЕЕ СРЕДСТВО НЕИНЪЕКЦИОННОГО ПРИМЕНЕНИЯ | 2001 |
|
RU2197986C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИМЕРНЫХ НАНОЧАСТИЦ НИЗКОСИАЛИРОВАННОГО ЭРИТРОПОЭТИНА С ВЫСОКОЙ СТЕПЕНЬЮ СОРБЦИИ ДЛЯ ЛЕЧЕНИЯ НЕВРОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2014 |
|
RU2616258C2 |
| СПОСОБ ОЦЕНКИ ЭКСПРЕССИИ ГЕНОВ НЕЙРОТРОФИНОВ | 2009 |
|
RU2383619C1 |
| СПОСОБ СКРИНИНГА ФАРМАКОЛОГИЧЕСКИХ СОЕДИНЕНИЙ НА НЕЙРОПРОТЕКТОРНУЮ АКТИВНОСТЬ | 2009 |
|
RU2383615C1 |
| Способ получения глиальных производных индуцированных плюрипотентных стволовых клеток с повышенной экспрессией NGF для терапии нейродегенеративных заболеваний | 2023 |
|
RU2829363C1 |
| Способ получения глиальных производных индуцированных плюрипотентных стволовых клеток с повышенной экспрессией BDNF для терапии ишемического инсульта | 2023 |
|
RU2829361C1 |
| СТАБИЛИЗИРОВАННЫЙ ВОДНЫЙ РАСТВОР ЭРИТРОПОЭТИНА | 1998 |
|
RU2128517C1 |
| ШТАММ КЛЕТОК ЯИЧНИКОВ КИТАЙСКОГО ХОМЯЧКА СНО-ЕРО 4А9 - ПРОДУЦЕНТ ВЫСОКОСИАЛИРОВАННОГО ЭРИТРОПОЭТИНА | 2016 |
|
RU2652884C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЭМБРИОНАЛЬНЫХ СТВОЛОВЫХ КЛЕТОК МЛЕКОПИТАЮЩИХ, МОДИФИЦИРОВАННЫХ ГЕНОМ ФАКТОРА РОСТА НЕРВОВ ЧЕЛОВЕКА | 2011 |
|
RU2458984C1 |
| Искусственный пептид для лечения черепно-мозговой травмы | 2023 |
|
RU2816919C1 |
Фармацевтическая композиция в качестве лекарственного средства включает низкосиалированные формы эритропоэтина с содержанием 6-8 остатков сиаловых кислот на молекулу белка. Изобретение обеспечивает расширение арсенала эффективных лекарственных средств для лечения неврологических заболеваний. 3 ил., 2 табл.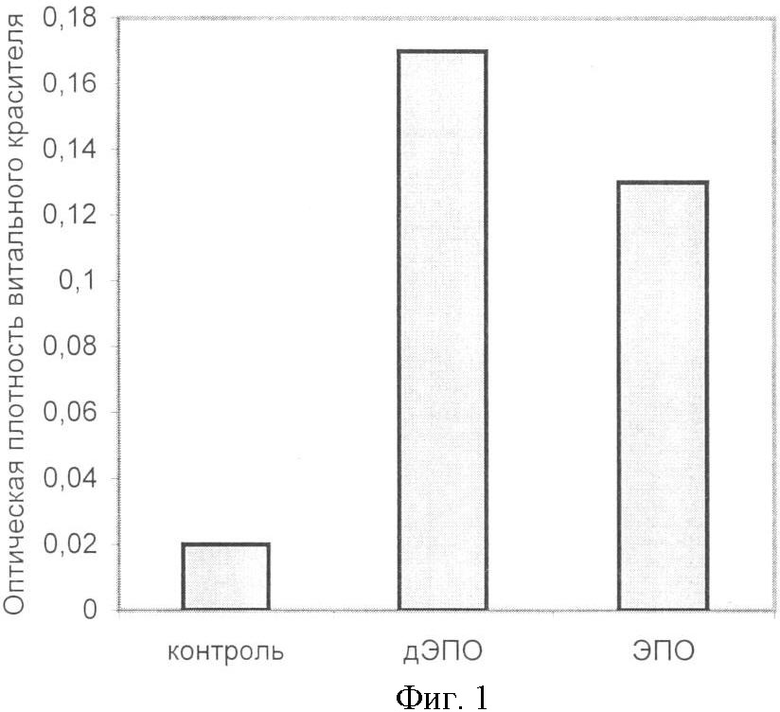
Фармацевтическая композиция для профилактики и лечения неврологических заболеваний на основе низкосиалированных форм эритропоэтина с содержанием 6-8 остатков сиаловых кислот на молекулу белка.
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| МАШКОВСКИЙ М.Д | |||
| Лекарственные средства | |||
| - М.: ООО «Новая Волна», 2001, т.2, с.124 | |||
| СПОСОБЫ ОПРЕДЕЛЕНИЯ IN VITRO БИОАКТИВНОСТИ ЭРИТРОПОЭТИНА | 1996 |
|
RU2176793C2 |
| АНАЛОГ ЭРИТРОПОЭТИНА | 1994 |
|
RU2159814C2 |
| СТАБИЛИЗИРОВАННЫЙ ВОДНЫЙ РАСТВОР ЭРИТРОПОЭТИНА | 1998 |
|
RU2128517C1 |
| ШТАММ СНО КУЛЬТИВИРУЕМЫХ КЛЕТОК КИТАЙСКОГО ХОМЯЧКА - ПРОДУЦЕНТ ЭРИТРОПОЭТИНА ЧЕЛОВЕКА | 1995 |
|
RU2089611C1 |
Авторы
Даты
2008-10-10—Публикация
2007-06-26—Подача