Изобретение относится к области разработки медицинских препаратов, в частности к разработке противоопухолевых препаратов.
Известен метод получения N,N-диметиламинометильных производных хлорофилла, заключающийся во взаимодействии производных хлорофилла (а) (метилфеофорбида (а), метилпирофеофорбида (а), триметилового эфира хлорина (e6) и их цинковых комплексов с диметилметиленаммоний иодидом («солью Эшенмозера») [Pandey R.K., Shiau F.U., Smith N.N., Dougherty D.J., Smith K.M. // Tetragedron (1992) v.48, №36, p.7591-7600]. Недостатком этого способа является то, что действием диметилметиленаммоний иодида удается ввести на периферию хлоринового макроцикла только одну N,N-диметиламинометильную группу. Кроме того, недостатком этого способа является то, что при проведении реакции с безметальными хлоринами выходы продуктов реакции относительно невысоки. Высокие выходы продуктов реакции удается получить только с использованием цинковых комплексов, что требует введения дополнительных стадий (синтез комплекса и деметаллирование продукта реакции), уменьшающих выход целевых продуктов. Недостатком этого способа является также необходимость использования безводных растворителей, что также осложняет выполнение реакции.
Известен также метод получения N,N-диметиламинометильных производных природных и синтетических порфиринов, заключающийся в реакции металлокомплексов порфириновых соединений с «комплексом Вильсмейера» (реакция Вильсмейера) с последующим восстановлением образующегося иминосоли борогидридом натрия [Пономарев Г.В., Розынов Б.В. // Химия гетероциклических соединений (1973) №9, с.1172]. Этот метод позволяет ввести N,N-диметиламинометильную группу в мезо-положение порфиринового макроцикла и, в случае природных порфиринов с винильной группой, получать хлорины с 2-(N,N-диметиламинометил)-винильной группой. Недостатком этого способа, как и предыдущего, является то, на периферию хлоринового макроцикла удается ввести, как правило, только одну N,N-диметиламинометильную группу. Кроме того, к недостаткам этого метода можно отнести сложность выполнения реакции и низкие выходы при деметаллировании комплексов в случае, если необходимо получить безметальные порфирины.
Задачей изобретения является разработка эффективного и простого в исполнении метода синтеза производных хлорина е6 с двумя N,N-диметиламинометильными группами.
Предлагаемый способ позволяет получать производные хлорина е6 с двумя N,N-диметиламинометильными группами с высоким выходом и без применения сложных процедур.
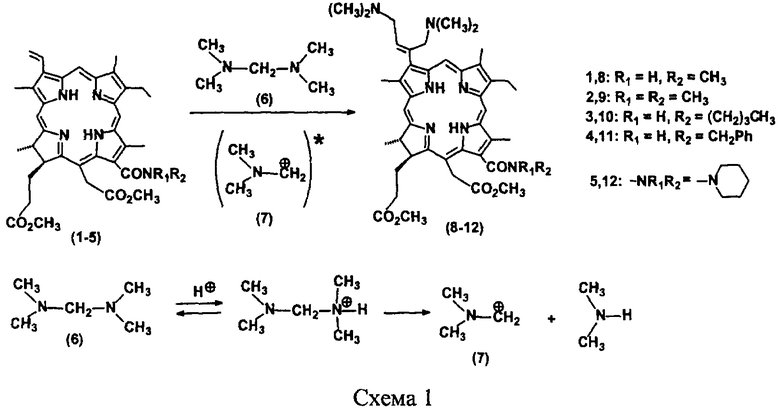
Технический результат достигается тем, что производное хлорина е6 подвергают действию бис-N,N-диметиламинометана в смеси тетрагидрофурана с уксусной кислотой при температуре кипения реакционной смеси с последующим выделением целевого продукта колоночной хроматографией для получения производных хлорофилла с двумя N,N-диметиламинометильными группами.
Предложенный способ осуществляют следующим образом. Исходный амид хлорина е6 кипятят с бис-N,N-диметиламинометаном в смеси тетрагидрофурана с уксусной кислотой в течение 20-30 минут.
Пример 1. К раствору 194 мг хлорина е613-N-метиламида 15,17-диметилового эфира (1) в 4 мл тетрагидрофурана добавляют 4 мл ледяной уксусной кислоты и 0.4 мл бис-N,N-диметиламинометана (6). Смесь кипятят с обратным холодильником в течение 25 минут. Реакционную смесь разбавляют 50 мл хлороформа и отмывают остатки кислоты и бисамина (6) дистиллированной водой до нейтральной реакции промывных вод. Полученный раствор сушат безводным сульфатом натрия, после чего растворитель отгоняют. Продукт реакции выделяют колоночной хроматографией на силикагеле марки 100/400 (Silicagel L) (элюент - CCl4-ацетон - 50:1-1:1). Выход продукта (8) 204 мг.
Пример 2. К раствору 30 мг хлорина е6 13-N,N-диметиламида 15,17-диметилового эфира (2) в 2 мл тетрагидрофурана добавляют 2 мл ледяной уксусной кислоты и 0.1 мл бис-N,N-диметиламинометана (6). Смесь кипятят с обратным холодильником в течение 20 минут. Реакционную смесь разбавляют 50 мл хлороформа и отмывают остатки кислоты и бисамина (6) дистиллированной водой до нейтральной реакции промывных вод. Полученный раствор сушат безводным сульфатом натрия, после чего растворитель отгоняют. Продукт реакции выделяют колоночной хроматографией на силикагеле марки 100/400 (Silicagel L) (элюент - CCl4-ацетон - 50:1-1:1). Выход продукта (10) 28 мг.
Пример 3. К раствору 24 мг хлорина е6 13-N-бутиламида 15,17-диметилового эфира (3) в 2 мл тетрагидрофурана добавляют 2 мл ледяной уксусной кислоты и 0.1 мл бис-N,N-диметиламинометана (6). Смесь кипятят с обратным холодильником в течение 20 минут. Реакционную смесь разбавляют 50 мл хлороформа и отмывали остатки кислоты и бисамина (6) дистиллированной водой до нейтральной реакции промывных вод. Полученный раствор сушат безводным сульфатом натрия, после чего растворитель отгоняют. Продукт реакции выделяют колоночной хроматографией на силикагеле марки 100/400 (Silicagel L) (элюент - CCl4-ацетон - 50:1-1:1). Выход продукта (10) 20 мг.
Таким образом, предлагаемый способ позволяет с высоким выходом получить производные хлорина е6 с двумя N,N-диметиламинометильными группами без применения сложных процедур и нестабильных или труднодоступных реагентов.
| название | год | авторы | номер документа |
|---|---|---|---|
| ВОДОРАСТВОРИМОЕ ПРОИЗВОДНОЕ ХЛОРОФИЛЛА α, МОДИФИЦИРОВАННОЕ ФРАГМЕНТОМ МИРИСТИНОВОЙ КИСЛОТЫ | 2017 |
|
RU2680523C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПЛЕКСОВ ПРОИЗВОДНЫХ ХЛОРОФИЛЛА (А) С ПЕРЕХОДНЫМИ МЕТАЛЛАМИ | 2006 |
|
RU2310658C1 |
| Новые производные хлорина е, содержащие фрагменты галактозы | 2019 |
|
RU2706698C1 |
| ПРОИЗВОДНЫЕ ХЛОРОФИЛЛА α, МОДИФИЦИРОВАННЫЕ ФРАГМЕНТАМИ МИРИСТИНОВОЙ КИСЛОТЫ | 2018 |
|
RU2673888C1 |
| СПОСОБ СИНТЕЗА ДИ- И ТРИАМИНОХЛОРИНОВ | 2006 |
|
RU2304583C1 |
| СПОСОБ ПОЛУЧЕНИЯ 18-КАРБОКСИ-20-(КАРБОКСИМЕТИЛ)-8-ЭТЕНИЛ-13-ЭТИЛ-2,3-ДИГИДРО-3,7-12,17-ТЕТРАМЕТИЛ-21Н, 23НПОРФИН-2-ПРОПИОНОВОЙ КИСЛОТЫ ИЛИ ЕЕ СОЛЕЙ | 1993 |
|
RU2054476C1 |
| Способ получения монокарбоксилпроизводных деметаллированных нефтяных порфиринов | 2021 |
|
RU2783726C1 |
| N-ХИНОЛИЛ- ИЛИ ИЗОХИНОЛИЛЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ПУРИНА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ИСПОЛЬЗОВАНИЯ | 2006 |
|
RU2417230C2 |
| СПОСОБ ПОЛУЧЕНИЯ МЕТИЛФЕОФОРБИДА (А) | 2012 |
|
RU2490273C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ N-АРИЛПИПЕРАЗИНАЛКАНАМИДА | 1988 |
|
RU2014328C1 |
Изобретение относится к области разработки медицинских препаратов, в частности противоопухолевых препаратов. Описывается способ получения новых производных хлорофилла с двумя N,N-диметиламинометильными группами. Способ состоит в том, что производное хлорина е6 подвергают действию бис-N,N-диметиламинометана в смеси тетрагидрофурана с уксусной кислотой при температуре кипения реакционной смеси с последующим выделением целевого продукта колоночной хроматографией. Предложенный способ обеспечивает получение новых производных хлорофилла с двумя N,N-диметиламинометильными группами с высоким выходом по простой технологии.
Способ получения производных хлорофилла с двумя N,N-диметиламинометильными группами, заключающийся в том, что производное хлорина е6 подвергают действию бис-N,N-диметиламинометана в смеси тетрагидрофурана с уксусной кислотой при температуре кипения реакционной смеси с последующим выделением целевого продукта колоночной хроматографией.
| RAVINDRA K | |||
| PANDEY et al | |||
| Syntheses of water-soluble cationic porphyrins and chlorines | |||
| Tetragedron | |||
| Пуговица для прикрепления ее к материи без пришивки | 1921 |
|
SU1992A1 |
| СОЛИ 2,7,12,18-ТЕТРАМЕТИЛ-3,8-ДИЭТИЛ-13,17-ДИ-(3-ДИМЕТИЛАМИНОПРОПИЛ)-ПОРФИРИНА, ОБЛАДАЮЩИЕ ПРОТИВОЛУЧЕВОЙ АКТИВНОСТЬЮ, И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1985 |
|
SU1287521A1 |
| СПОСОБ ПОЛУЧЕНИЯ 18-КАРБОКСИ-20-(КАРБОКСИМЕТИЛ)-8-ЭТЕНИЛ-13-ЭТИЛ-2,3-ДИГИДРО-3,7-12,17-ТЕТРАМЕТИЛ-21Н, 23НПОРФИН-2-ПРОПИОНОВОЙ КИСЛОТЫ ИЛИ ЕЕ СОЛЕЙ | 1993 |
|
RU2054476C1 |
| 5,15-БИС(4'-АКРИЛАМИДОФЕНИЛ)-3,7,13,17-ТЕТРАМЕТИЛ-2,8,12,18-ТЕТРАБУТИЛПОРФИН В КАЧЕСТВЕ КРАСЯЩЕГО ВЕЩЕСТВА ОПТИЧЕСКИХ ФИЛЬТРОВ | 2005 |
|
RU2281303C1 |
| RU 99108790 A, 10.02.2001. | |||
Авторы
Даты
2008-10-27—Публикация
2007-04-09—Подача