Изобретение относится к новым химическим соединениям порфиринового ряда, конкретно к солям 2,7,12,18-тетраметил-3,8-диэтил-13,17-ди-(3-диметиламинопропил)порфирина общей формулы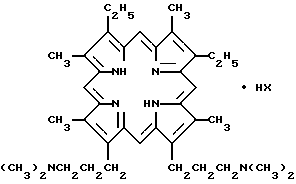
a) HX 2CH3SO3H;
б) HX 4HCl,
обладающим противолучевой активностью, и способу их получения.
Целью изобретения является поиск в ряду водорастворимых соединений, проявляющих выраженную противолучевую активность при введении их по истечению нескольких часов после момента облучения, и разработка нового способа их получения.
П р и м е р 1. Диметансульфонат 2,7,12,18-тетраметил-3,8-диэтил-13,17-ди-(3-диметиламинопропил)порфирина (1а).
Растворяют 1,66 г (3 ммоль) мезопорфирина-IX в 25 мл хлористого тионила, через 1 ч упаривают досуха, остаток растворяют в 100 мл хлороформа, охлаждают до 0oC и обрабатывают 20 мл 30%-ного водного раствора диметиламина. Органический слой отделяют, сушат Na2SO4 и нагревают до кипения 0,5 ч с 2 г ацетата цинка. Раствор фильтруют через слой (2 см) окиси алюминия, упаривают до небольшого объема, порфирин осаждают, добавляя избыток метанола, и получают 1,86 г (90%) цинкового комплекса диметиламида мезопорфирина-IX. Кипятят 1,86 г (2,76 ммоль) цинкового комплекса диметиламида мезопорфирина-IX c 262 мг (6,9 моль) LiAIH4 в 150 мл тетрагидрофурана. Через 3 ч добавляют 5 мл воды, осадок отфильтровывают, фильтрат упаривают досуха, растворяют в 200 мл хлороформа и обрабатывают 50 мл конц. соляной кислоты. Добавляя водный раствор аммиака, реакцию среды доводят до рН 7 8, органический слой отделяют и хроматографически выделяют 1,29 г (80%) 2,7,12,18-тетраметил-3,8-диэтил-13,17-ди-(3-диметиламинопропил)порфирина. Суспендируют 1,29 г (2,18 ммоль) 2,7,12,18-тетраметил-3,8-диэтил-13,17-ди-(3-диметиламинопропил)-порфирина в 100 мл этанола, добавляют 0,42 г (4,36 ммоль) метансульфокислоты, растворитель упаривают досуха, а остаток перекристаллизовывают из изопропанола и получают 1,57 г (92% 68% на исходный мезопорфирин-IX) диметансульфоната 2,7,12,18-тетраметил-3,8-диэтил-13,17-ди-(3-диметиламинопропил)порфирина (Ia).
ИК-спектр: ν(CH3SO
Электронный спектр в хлороформе, λ макс/нм (e•10-3): 400(156); 500 (12,7); 534 (9,73); 567 (6,55); 620 (5,02), добавлено два эквивалента триэтиламина.
Электронный спектр в воде l, макс/нм (e•10-3):375 (53,9); 398 плечо (44,0); 504 (6,37); 538 (4,97); 565 (3,95); 617 (1,66).
Найдено, C 61,0; H 7,7; N 10,7.
C40H60N6O6S2.
Вычислено, C 61,2; H 7,7; N 10,7.
П р и м е р 2. Тетрахлоргидрат 2,7,12,18-тетраметил-3,8-диэтил-13,17-ди-(3-диметиламинопропил)порфирина (Iб).
К суспензии 2,7,12,18-тетраметил-3,8-диэтил-13,17-ди-(3-диметиламинопропил)порфирина, полученного аналогично синтезу порфирина 1a, из 24 г мезопорфирина-IX, в 0,5 л этанола прибавляют по каплям при интенсивном перемешивании спиртовой раствор хлористого водорода до кислой реакции по метиловому оранжевому. Растворитель упаривают досуха, остаток перекристаллизовывают из изопропилового спирта и получают 20,11 г (62,6% в расчете на исходный мезопорфирин-IX) тетрахлоргидрата 2,7,12,18-тетраметил-3,8-диэтил-13,17-ди-(3-диметиламинопропил)порфирина (Iб).
ИК-спектр: ν(NH(CH3)
Электронный спектр в воде, λ макс/нм (e•10-3):391(53,9); 504(4,99); 539(4,85); 563(4,85); 609(2,02).
Найдено, N 11,4; Cl 19,2.
C38H56N6Cl4.
Вычислено, N 11,4; Cl 19,2.
Данные о токсичности диметансульфоната 2,7,12,18-тетраметил-3,8-диэтил-13,17-ди-(3-диметиламинопропил)порфирина Ia и тетрахлоргидрата 2,7,12,18-тетраметил-3,8-диэтил-13,17-ди-(3-диметиламинопропил)порфирина Iб, полученные в опытах in vitro на асинхронной культуре клеток СОЦ, представлены в табл. 1.
Сравнение противолучевой активности соединений Ia и Iб проводилось с 2,7,12,17-тетраметил-3,8,13,18-тетраэтил-5-диметиламинометилпорфирином (II).
Опыты in vitro проводили на асинхронной культуре клеток СОЦ. Порфирины Ia и Iб в нетоксичных для интактных клеток дозах вносили в инкубационную среду через 0,25, 15,3 и 7 ч после облучения культуры. Клетки облучали на рентгеновской установке РУМ-7 в дозе 4 Гр при мощности дозы 0,4 Гр/мин и фильтре 0,47 мм Al. О пострадиационном эффекте соединений судили по разности сохранения способности клеток к образованию нормальных колоний в облученном контроле и в опыте с внесенными в среду порфиринами. Результаты экспериментов приведены в табл. 2.
Парафин Ia изучали в опытах на мышах-самцах линии C57Bl (6 со средним весом 20 г). Токсичность соединения Ia определяли методом Литчфилда и Уилкоксона. По тесту трехсуточной выживаемости дозы соответствующие СД16, CД50 и СД84 оказались равны 24, 35 (27 + 44) и 45 мг/кг. Терапевтический эффект порфирина Ia изучали при введении его в дозе 1/2 СД16 через 0,25, 3, 6, 24 ч после облучения. Подопытным животным препарат вводили внутрибрюшинно, животным контрольной группы вводили внутрибрюшинно физиологический раствор. Мышей опытных и контрольных групп (по 10 животных в каждой) облучали однократно в дозе 8 Гр (ЛД95-99/30) на гамма-установке "ИГУР-1"; мощность дозы 0,72 Гр/мин. Лечебный эффект препарата оценивали по выживаемости мышей на 30-е сутки после облучения. Результаты экспериментов приведены в табл. 3.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения конъюгатов на основе производного сефарозы | 1988 |
|
SU1684289A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОРФИРИНОВ | 1973 |
|
SU374301A1 |
| ПРОИЗВОДНЫЕ ФТОРИРОВАННОГО ПОРФИРИНА, ПРОЯВЛЯЮЩИЕ ПРОТИВООПУХОЛЕВУЮ АКТИВНОСТЬ | 2019 |
|
RU2707754C1 |
| ВОДОРАСТВОРИМЫЕ СОЛИ 2,4-ДИ -( α -МЕТОКСИЭТИЛ)ДЕЙТЕРОПОРФИРИНА-IX, ОБЛАДАЮЩИЕ СПОСОБНОСТЬЮ ЛОКАЛИЗОВАТЬСЯ В РАКОВЫХ ТКАНЯХ | 1984 |
|
SU1160710A1 |
| Способ получения порфиринов | 1979 |
|
SU792884A1 |
| МЕТАЛЛОКОМПЛЕКСЫ КАРБОРАНИЛПОРФИРИНОВ, ОБЛАДАЮЩИЕ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 2002 |
|
RU2236411C2 |
| ПРОИЗВОДНЫЕ ФТОРСОДЕРЖАЩИХ ХЛОРИНОВ, ПРОЯВЛЯЮЩИЕ ПРОТИВООПУХОЛЕВУЮ АКТИВНОСТЬ | 2019 |
|
RU2725876C1 |
| 11β -АЦИЛОКСИ- 17α -ГИДРОПЕРОКСИ- 16α -МЕТИЛПРЕГНАНЫ, ОБЛАДАЮЩИЕ МЕСТНОЙ ПРОТИВОВОСПАЛИТЕЛЬНОЙ АКТИВНОСТЬЮ | 1991 |
|
RU2030421C1 |
| 1,5,9,11- ТЕТРААЗАТРИЦИКЛО [7,3,3,1] ГЕКСАДЕКАНЫ | 1981 |
|
SU1014252A1 |
| КАРБОРАНОВЫЕ ПРОИЗВОДНЫЕ 4,4-ДИФТОР-4-БОРА-3а,4а-ДИАЗА-s-ИНДАЦЕНА, ПРОЯВЛЯЮЩИЕ ПРОТИВООПУХОЛЕВУЮ АКТИВНОСТЬ | 2022 |
|
RU2789401C1 |
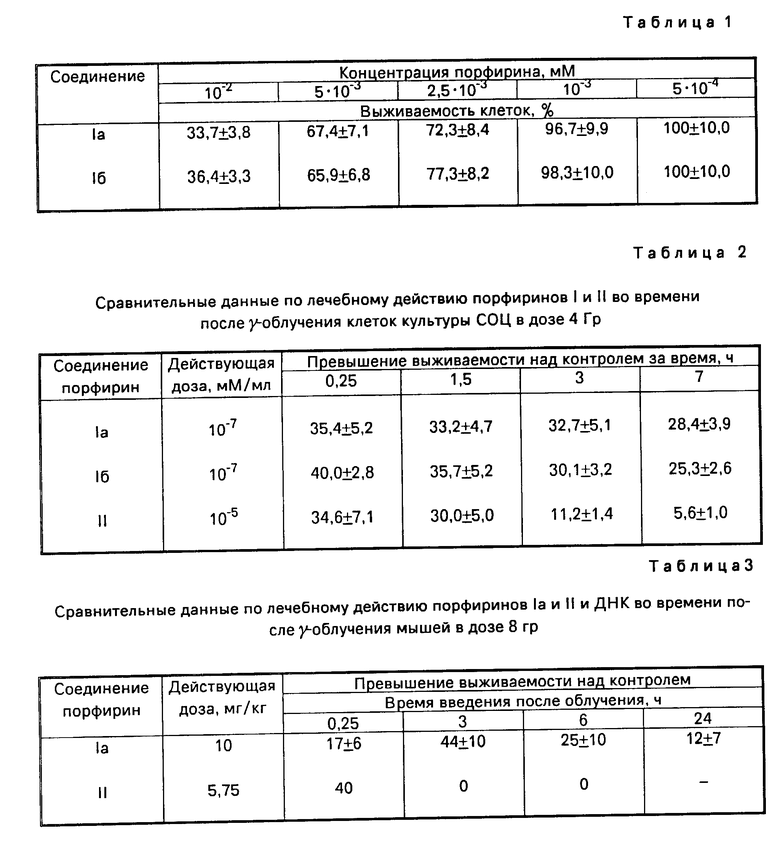
1. Соли 2,7,12,18 - тетраметил-3,8-диэтил-13,17-ди-(3-диметиламинопропил)-порфирина общей формулы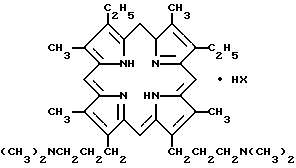
где а) НХ - 2CH3SO3H,
б) НХ - 4HCl,
обладающие противолучевой активностью.
2. Способ получения солей 2,7,12,18-тетраметил-3,8-диэтил-13,17-ди-(3-диметиламинопропил)-порфирина общей формулы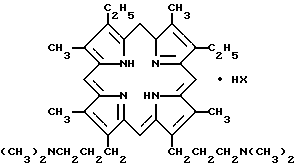
где а) НХ - 2CH3SO3H,
б) НХ - 4HCl,
отличающийся тем, что мезопорфирин-IX обрабатывают хлористым тионилом, на полученный хлорангидрид действуют диметиламином, образовавшийся при этом диметиламид мезопорфирина-IX подвергают взаимодействию с ацетатом цинка с последующим восстановлением алюмогидридом лития образовавшегося цинкового комплекса и деметаллированием последнего действием соляной кислоты.
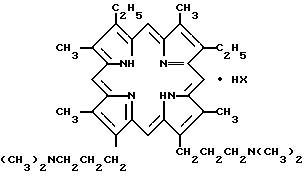
где а) НХ 2CH3SO3H,
б) НХ 4HCl,
обладающие противолучевой активностью.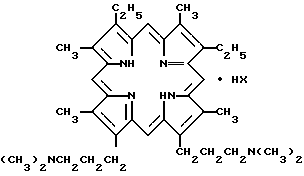
где а) НХ 2CH3SO3H,
б) НХ 4HCl,
отличающийся тем, что мезопорфирин-IX обрабатывают хлористым тионилом, на полученный хлорангидрид действуют диметиламином, образовавшийся при этом диметиламид мезопорфирина-IX подвергают взаимодействию с ацетатом цинка с последующим восстановлением алюмогидридом лития образовавшегося цинкового комплекса и деметаллированием последнего действием соляной кислоты.
| Строганова Л.Т., Тужилкова Т.Н | |||
| Радиозащитные свойства экзогенных профиринов, как проявление их общей биологической активности | |||
| Материалы III Всесоюзной конференции по химии и биохимии порфиринов | |||
| Самарканд | |||
| Гребенчатая передача | 1916 |
|
SU1983A1 |
Авторы
Даты
1996-10-27—Публикация
1985-01-10—Подача