Изобретение относится к фармакологии, а именно к лекарственным препаратам и пищевым добавкам противодиабетического действия, и может быть использовано в качестве нового средства для коррекции нарушений углеводного обмена с целью профилактики и лечения сахарного диабета II типа.
Сахарный диабет является следствием относительного или абсолютного дефицита инсулина. В соответствии с классификацией ВОЗ различают две формы заболевания: инсулинзависимый (сахарный диабет I типа) и инсулиннезависимый (сахарный диабет II типа). Сахарный диабет I типа характеризуется абсолютной недостаточностью образования инсулина b-клетками островков Лангерганса поджелудочной железы и требует заместительной гормонотерапии препаратами инсулина. Больные сахарным диабетом II типа нуждаются в назначении пероральных противодиабетических препаратов, к которым относятся производные сульфонилмочевины и бигуаниды. Сахароснижающий эффект производных сульфонилмочевины обусловлен повышением под их действием секреции инсулина b-клетками островков поджелудочной железы, усилением действия инсулина, циркулирующего в кровотоке, усилением утилизации глюкозы скелетными мышцами и печенью, торможением образования глюкозы из жира в печени и липолиза жировой ткани. Лечение производными сульфонилмочевины показано при сахарном диабете II типа средней тяжести у взрослых. Эти препараты противопоказаны при инсулинзависимом диабете, заболеваниях крови, сопровождающихся снижением в крови количества лейкоцитов и тромбоцитов, и в ряде других случаев. Наименее выраженным побочным действием из всех препаратов этой группы обладают манинил, предиан, глюренорм. Второй группой пероральных противодиабетических средств являются бигуаниды. Эти препараты эффективны при наличии в организме эндогенного или экзогенного происхождения, поскольку не влияют на его синтез и высвобождение из b-клеток островков поджелудочной железы. Бигуаниды потенцируют действие инсулина путем усиления утилизации глюкозы скелетными мышцами, торможения образования глюкозы из жиров, уменьшения всасывания глюкозы в тонком кишечнике, усиления липолиза и снижения интенсивности синтеза жира. Противопоказаниями к использованию бигуанидов служат сахарный диабет I типа, истощение, поражение печени, почек, коматозные состояния, заболевания, сопровождающиеся гипоксией (Маковецкий А.Г., Велихов В.К. Сахарный диабет. М., 1987. 102 С.).
Задачей изобретения является расширение арсенала средств гиполипидемического и противоишемического действия, получение препарата низкой себестоимости из доступного растительного сырья, обладающего повышенной эффективностью.
Техническим результатом настоящего изобретения является создание средства из возобновляемого дешевого растительного сырья для лечения инсулиннезависимого диабета (диабета II типа), обладающего не только сахароснижающим действием, но и обладающим гиполипидемической активностью, поскольку развитие диабета, как правило, сопровождается выраженным сдвигом в состоянии липидного обмена.
Технический результат достигается тем, что в качестве средства, обладающего противодиабетической и гиполипидемической активностью, при терапии и профилактике сахарного диабета II типа применяют экдистероидсодержащую субстанцию, выделенную из надземной части растений серпухи венценосной Serratula coronata L. (Asteraceae), представляющей собой смесь 20-гидоксиэкдизона в количестве не менее 75% и 25S-инокостерона в количестве не менее 10%.
Известна смесь экдистероидов, выделенных по способу, описанному в патенте РФ №2153346, содержащая 20-гидроксиэкдизона не менее 75% и 25S-инокостерона не менее 10% со структурными формулами, указанными ниже, являющихся действующими веществами, проявляющими физиологическую активность.
Предлагаемое средство, названное нами «Серпистен», представляет собой белый кристаллический порошок, не имещий запаха, малорастворимый в воде, хорошо растворимый в метаноле и 70%-ном этаноле.
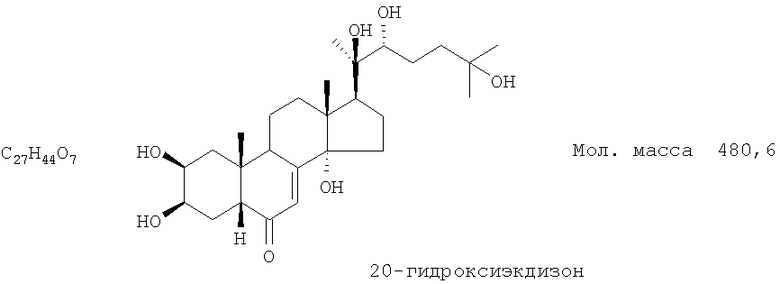
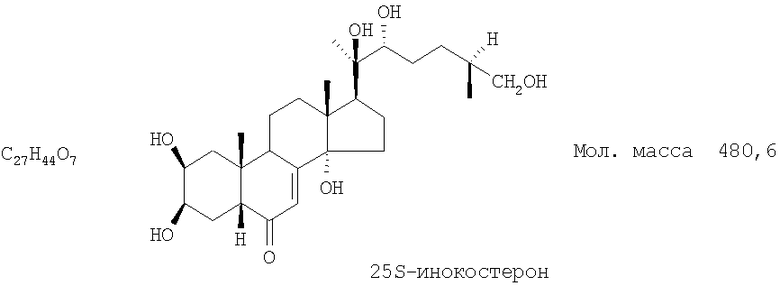
Смесь фитоэкдистероидов получают известным способом (по патенту 2153346) следующим образом.
Заготовку сырья, предпочтительно листьев, осуществляют в фазу вегетации, массовой бутонизации или начала цветения. Экспериментально установлено, что в эти фазы развития содержание действующих экдистероидов максимально. Исследование распределения экдистероидов в растениях серпухи венценосной проводили у средневозрастных генеративных особей. По содержанию экдистероидов серпуха венценосная намного превосходит рапонтик сафлоровидный. Использование надземной части растения в отличие от корневищ рапонтика значительно облегчает заготовку и переработку экдистероидсодержащего растительного сырья.
Измельченное растительное сырье (надземная часть растения рода Serratula семейства Asteraceae) неоднократно экстрагируют водой при температуре не выше 100°С не более 1 ч при постоянном перемешивании и соотношении сырье экстрагент - 1:10 соответственно. Густой водный экстракт упаривают при пониженном давлении, обрабатывают смесью этилацетат-метанол, взятой при соотношении 4:1, или хлороформ-метанол при соотношении 6:1. Процедуру повторяют до полного извлечения экдистероидов из густого экстракта. Органические извлечения упаривают досуха, затем экдистероиды очищают путем хроматографии на оксиде алюминия в системе хлороформ-метанол или этилацетат-метанол возрастающей полярности и перекристаллизацией в системе этилацетат-метанол или этилацетат-этанол при соотношении 9:1.
Пример осуществления способа
6 кг измельченных листьев растения рода Serratula семейства Asteraceae заливают 60 л воды и экстрагируют в течение 1 часа при температуре 50°С при постоянном перемешивании, затем экстракт сливают, а растительное сырье подвергают повторной экстракции. Объединенный экстракт упаривают в вакуумном роторно-пленочном испарителе при пониженном давлении до 2 л. 2 л густого экстракта обрабатывают трижды 8 л смеси этилацетат-метанол при соотношении 4:1 при постоянном перемешивании и фильтруют. Фильтрат упаривают досуха, остатки объединяют и переносят на колонку с оксидом алюминия и элюируют смесью хлороформ-метанол возрастающей полярности. Элюат собирают в колбы по 1 л и определяют в них содержание экдистероидов методом тонкослойной хроматографии (ТСХ). Целевые фракции, содержащие экдистероиды, упаривают досуха и перекристаллизовывают в смеси этилацетат-метанол (9:1).
Таким образом, способ позволяет получать субстанцию Серпистен, представляющую собой смесь фитоэкдистероидов, содержащую не менее 75% 20-гидроксиэкдизона и не менее 10% инокостерона (белый кристаллический порошок, не имеет запаха, малорастворим в воде (1,9 г/л), хорошо растворим в 70%-ном этаноле (61 г/л) и метаноле (75 (г/л)). Выход 42 г или 0,7% к массе сырья, что составляет 70% к теоретически рассчитанному выходу.
Известен способ выделения 20-гидроксиэкдизона и 25S-инокостерона (патент РФ 2155599, позволяющий получить индивидуальные соединения из смеси фитоэкдистероидов и смешивать их в эффективном количестве.
Изобретение подтверждается фотографиями.
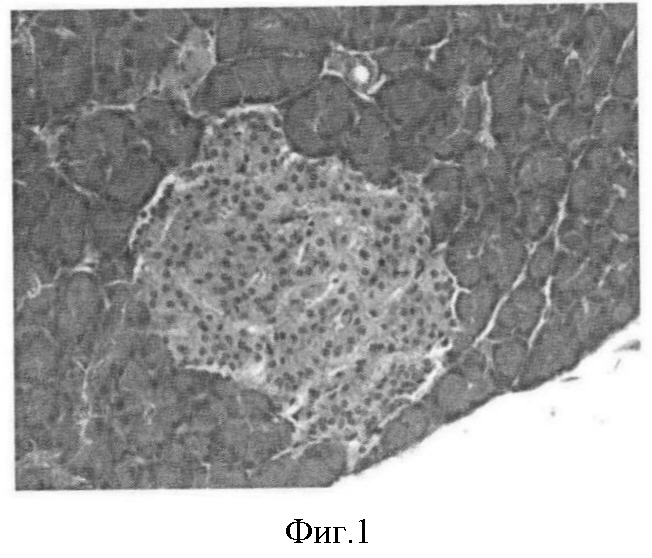
Фиг.1. Нормальное строение островка Лангерганса поджелудочной железы интактной крысы. 20-й день. Окраска гематоксилин-эозин. Ув. 40×7.
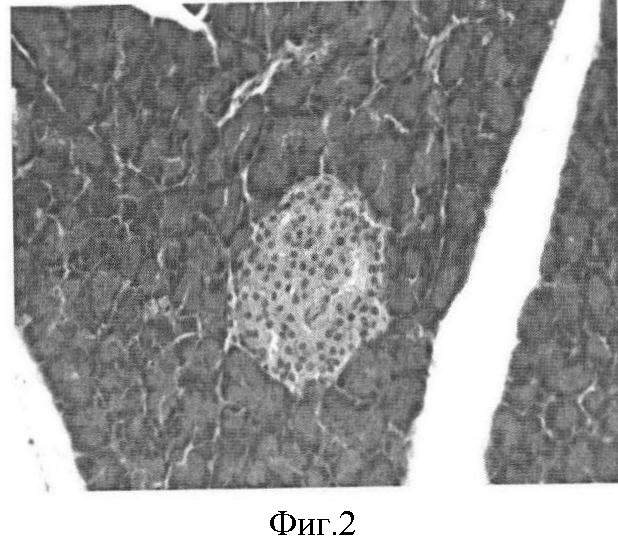
Фиг.2. Нормальное строение островка Лангерганса поджелудочной железы интактной крысы. 20-й день. Окраска гематоксилин-эозин. Ув. 40×7.
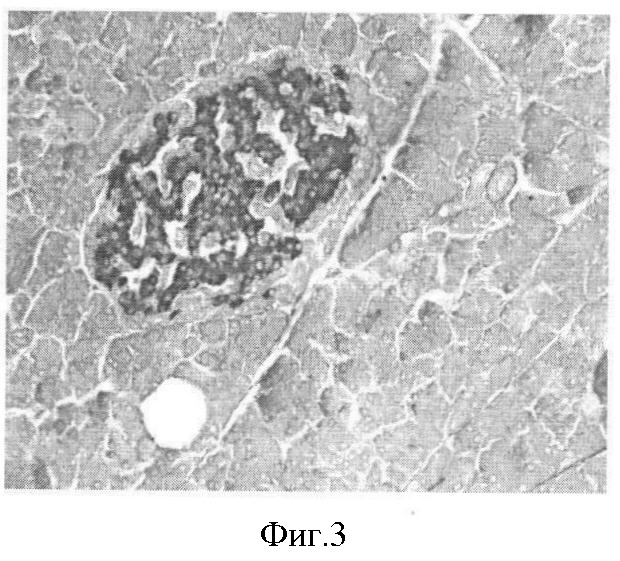
Фиг.3. Нормальное строение островка Лангерганса поджелудочной железы интактной крысы. 20-й день. Окраска альдегидфуксин. Ув. 20×7.
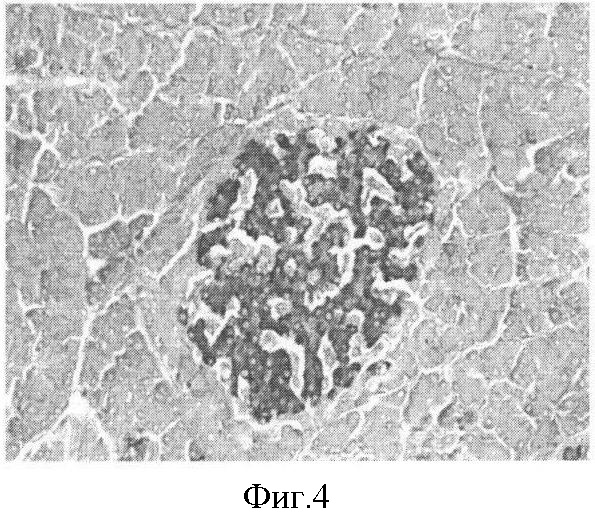
Фиг.4. Нормальное строение островка Лангерганса поджелудочной железы интактной крысы. 20-й день. Окраска альдегидфуксин. Ув. 20×7.
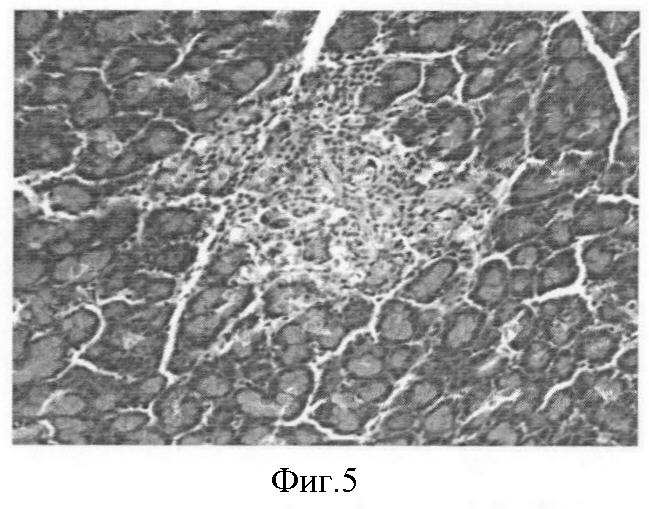
Фиг.5. Аллоксановый диабет у крысы. 20-е сутки. Нарушение строения островков Лангерганса. Окраска гематоксилин-эозин. Ув. 40×7.
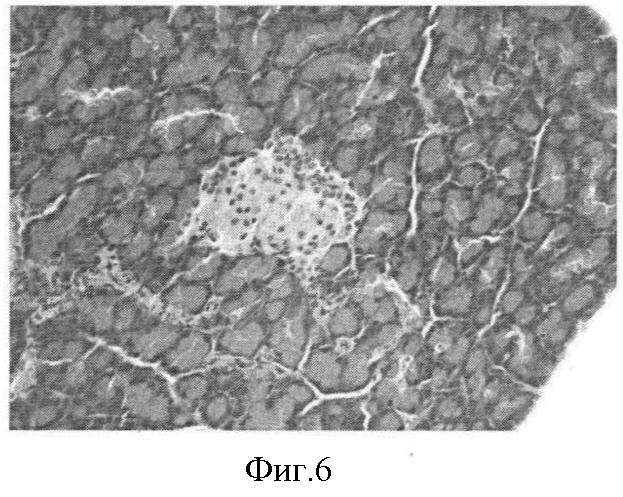
Фиг.6. Аллоксановый диабет у крысы. 20-е сутки. Нарушение строения островков Лангерганса. Лизис клеток и уменьшение количества ядер. Окраска гематоксилин-эозин. Ув. 40×7.
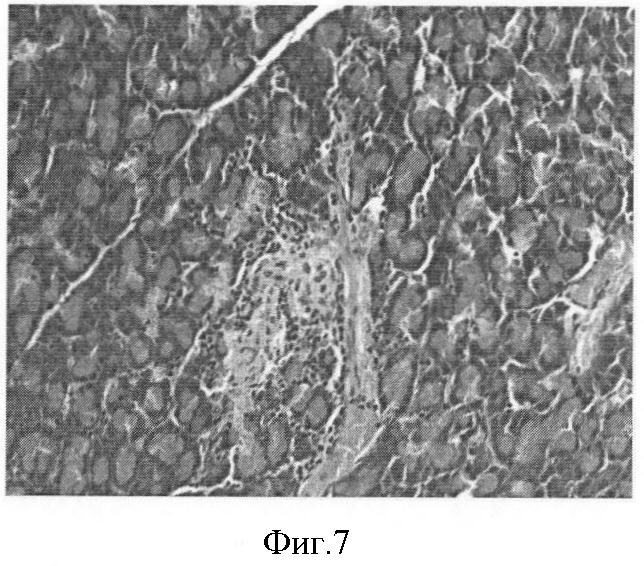
Фиг.7. Аллоксановый диабет у крысы. 10-е сутки. Разрушение островка Лангерганса. Лизис клеток и уменьшение количества ядер. Окраска гематоксилин-эозин. Ув. 40×7.
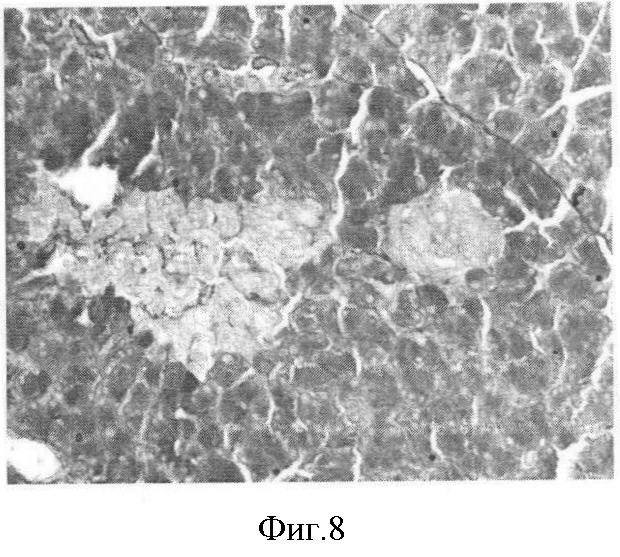
Фиг.8. Аллоксановый диабет у крысы. 20-е сутки. Разрушение островка Лангерганса. Лизис клеток, замещение стромальными элементами. Окраска альдегид фуксин. Ув. 20×7.
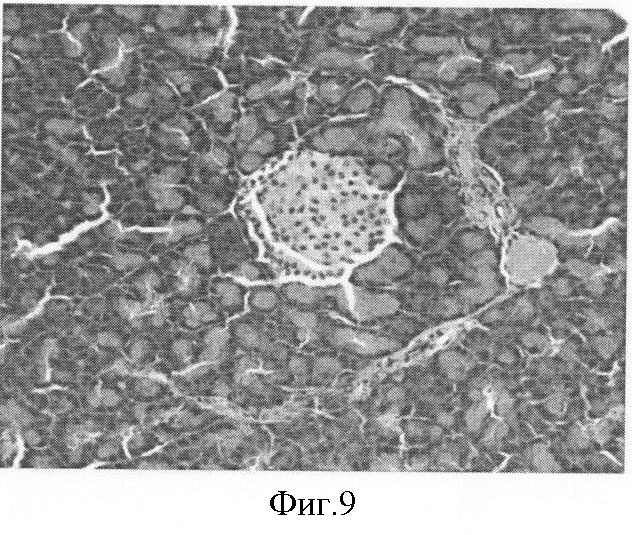
Фиг.9. Восстановление островка Лангерганса поджелудочной железы подопытной крысы через 20 дней лечения метформином. Увеличение количества ядер и клеток. Окраска гематоксилин-эозин. Ув. 40×7.
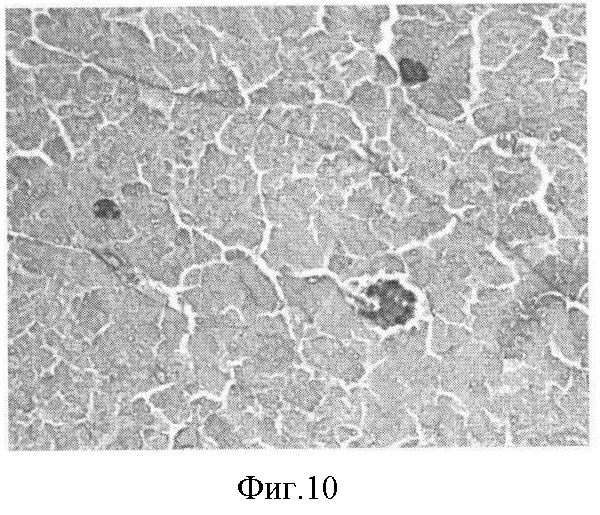
Фиг.10. Восстановление островка Лангерганса поджелудочной железы подопытной крысы через 20 дней лечения метформином. Увеличение количества ядер и клеток. Окраска альдегидфуксин. Ув. 20×7.
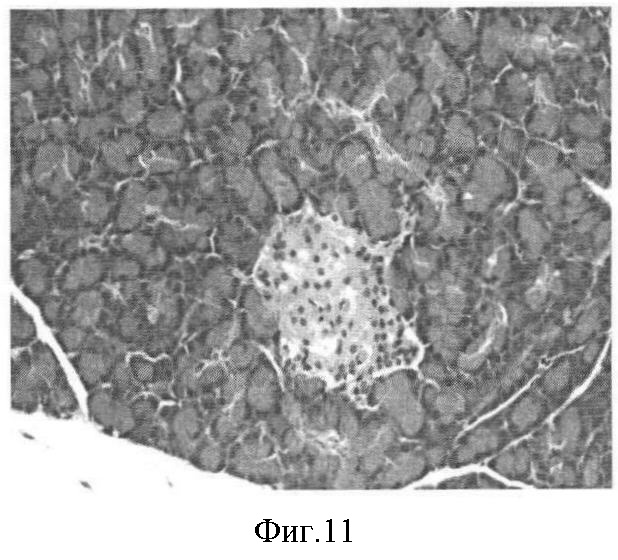
Фиг.11. Восстановление островка Лангерганса поджелудочной железы подопытной крысы через 20 дней лечения Серпистеном. Увеличение количества ядер и клеток. Окраска гематоксилин-эозин. Ув. 40×7.
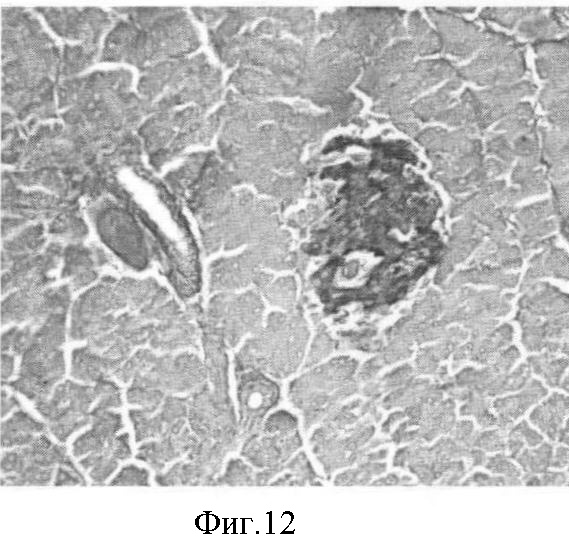
Фиг.12. Восстановление островка Лангерганса поджелудочной железы подопытной крысы через 20 дней лечения Серпистеном. Заметное увеличение размеров самого островка, количества ядер и синтезирующих инсулинклеток. Окраска альдегидфуксин. Ув. 20×7.
Проверка противодиабетической и гиполипидемической активности субстанции Серпистен осуществлялась в ЗАО «Адаптоген» (г.Санкт-Петербург). Эксперименты выполнялись на нелинейных белых крысах при внутрижелудочном пути введения на модели аллоксанового диабета. Животных содержали в стандартных условиях вивария при естественном освещении. Воду и пищу (стандартизованный брикетированный корм) животным предоставляли без ограничений. Работа выполнялась в соответствии с «Методическими рекомендациями по экспериментальному изучению новых пероральных гипогликемических фармацевтических средств» [1986].
Аллоксановый диабет вызывали однократным подкожным введением водного раствора аллоксангидрата (фирма ICN Biomedicals, США) в дозе 150 мг/кг голодавшим в течение суток крысам массой 180-200 г. Исследовались следующие группы животных: интактные; нелеченые крысы с диабетом; животные с диабетом, получавшие ежедневно в течение 23 дней препарат метморфин (200 мг/кг), взятый нами за прототип, производства фирмы «Польфа-Кутно А/О», Польша., рег. №008422 от 22.08.1997 г; животные с диабетом, получавшие ежедневно в течение 23 дней препарат Серпистен (5 мг/кг). Препараты вводились внутрижелудочно 1 раз в день в крахмальном геле.
Введение препаратов начинали на третий день после введения аллоксана, когда уровень глюкозы крови повысился по сравнению с контролем приблизительно в 3 раза [Гацура В.В., Саратиков А.С., 1977; Николайчук Л.В., 1988]. Каждая группа содержала по 20 животных обоего пола. В ходе эксперимента фиксировали общее состояние животных, потребление воды, массу тела.
В сыворотке крови определяли уровень глюкозы, общих липидов, триглицеридов, холестерина по общепринятым методам [Медицинские..., 2002].
В эритроцитах определяли концентрацию гемоглобина и гликозилированного гемоглобина. Содержание гемоглобина оценивали гемоглобинцианидным методом, предложенным Кушаковским М.С. [1968] с помощью стандартного набора реагентов (НПФ «Абрис+»). Гликозилированный гемоглобин определяли спектрофотометрически [Медицинские..., 2002].
Кроме этого, проводили исследование гистологического строения поджелудочной железы экспериментальных животных при окрашивании срезов гематоксилин-эозином и альдегидфуксином.
Применение нового средства приводит к увеличению выживаемости животных в условиях аллоксанового диабета и уменьшает такое проявление данной патологии, как полидипсия. При экспериментальном сахарном диабете II типа Серпистен снижает уровень гипергликемии и концентрацию гликозилированнного гемоглобина в крови экспериментальных животных, оказывая тем самым профилактическое действие в отношении развития основных осложнений сахарного диабета. На фоне лечения Серпистеном уровень общих липидов, холестерина и β-липопротеинов нормализовались практически до уровня интактных животных, что свидетельствует о гиполипидемическом действии исследованного вещества.
Пример 1. Влияние препарата Серпистен на физикальные показатели крыс с экспериментальным диабетом.
Показано позитивное влияние исследуемого препарата и препарата сравнения (метформин - группа бигуанидов) на выживаемость животных. Достоверное изменение веса животных было зарегистрировано только через 20 дней эксперимента и только в группе нелеченых животных. В то же время потребление воды - показатель, который считается одним из «больших» симптомов сахарного диабета, достоверно изменялся во всех группах животных. Наиболее выраженная полидипсия наблюдалась в группе нелеченых животных на 20 день эксперимента. Применение препарата Серпистен приводило к значимому снижению потребления воды (табл.1).
Результаты физикального исследования у крыс с экспериментальным диабетом
Пример 2. Влияние препарата Серпистен на уровень глюкозы и степень гликозилирования гемоглобина у крыс с экспериментальным диабетом.
Как видно из представленных в табл.2 данных, у экспериментальных нелеченых животных наблюдается хорошо выраженная гипергликемия. При лечении исследуемым препаратом Серпистен наблюдалось достоверное снижение уровня глюкозы, практически до уровня интактных животных. При применении препарата сравнения позитивные, изменения на уровень глюкозы были аналогичны, но несколько менее выражены.
Как и многие белки, гемоглобин в процессе функционирования в организме человека при контакте с глюкозой способен неферментативно гликозилироваться, т.е. присоединять глюкозу. Эффект гликозилирования зависит только от величины и длительности гипергликемии. У экспериментальных животных уровень гликозилированного гемоглобина закономерно увеличивается к 10 дню эксперимента и еще более выражено увеличивается к 20 дню эксперимента. Под влиянием препарата Серпистен к 10 дню лечения уровень гликозилированного гемоглобина достоверно понижается. К 20 дню под влиянием исследуемого препарата и метформина концентрация HbA1c также была ниже уровня нелеченых животных в 2 раза, однако уровень интактных животных не достигался.
Параллельно снижался уровень неизмененного гемоглобина, достоверно снижаясь в группе нелеченых животных, при применении препаратов уровень гемоглобина несколько повышался, но уровень интактных животных не достигался (табл.2).
Уровень глюкозы и степень гликозилирования гемоглобина у крыс с экспериментальным диабетом
Пример 3. Влияние препарата Серпистен на показатели липидного обмена у крыс с экспериментальным диабетом.
При развитии диабета наблюдаются выраженные сдвиги в состоянии липидного обмена. Отмечается увеличение общих липидов и холестерина в сыворотке крови животных без лечения к 10 дню, которое незначительно увеличивалось к 20 дню. На фоне лечения Серпистеном и препаратом сравнения оба показателя нормализовались и к 20 дню снижались практически до уровня интактных животных. Схожие изменения наблюдались в уровне β-липопротеинов, что также характеризовало положительную динамику процесса при лечении Серпистеном.
Несколько другие тенденции установлены в отношении триглицеридов, уровень которых достоверно не изменялся ни в одной группе животных к 10 дню эксперимента. К 20 дню эксперимента у нелеченых крыс уровень триглицеридов также не изменился, а при применении метформина и Серпистена достоверно снижался, что свидетельствует о липолитическом действии препаратов.
Показатели липидного обмена у крыс с экспериментальным диабетом
Пример 4. Данные гистологического исследования поджелудочной железы.
Строение островков Лангерганса поджелудочной железы интактных крыс представлено на фиг.1-4.
Результаты гистологических исследований поджелудочной железы крыс с экспериментальным диабетом свидетельствуют о нарушениях строения островков Лангерганса (фиг.5-8).
Результаты гистологических исследований поджелудочной железы при лечении крыс с экспериментальным диабетом Серпистеном и препаратом сравнения метформином наглядно демонстрируют восстановление островков Лангерганса и свидетельствуют о выраженном противодиабетическом действии препарата Серпистен (фиг.9-12).
Таким образом, субстанция Серпистен, представляющая собой смесь экдистероидов 20-гидроксиэкдизона и 25S-инокостерона из надземной части растений серпухи венценосной, обладает выраженным противодиабетическим действием:
- серпистен оказывет позитивное влияние на состояние животных, увеличивая выживаемость животных в условиях аллоксанового диабета и уменьшая такое проявление данной патологии, как полидипсия;
- при экспериментальном сахарном диабете Серпистен снижает уровень глюкозы и концентрацию гликозилированнного гемоглобина в крови экспериментальных животных, оказывая тем самым профилактическое действие в отношении развития основных осложнений сахарного диабета;
- при развитии диабета наблюдаются выраженные сдвиги в состоянии липидного обмена, на фоне лечения Серпистеном уровень общих липидов, холестерина и β-липопротеинов нормализуется практически до уровня интактных животных, что свидетельствует о гиполипидемическом действии исследованного вещества и может быть дополнительным критерием эффективности терапии.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ ПРОТИВОДИАБЕТИЧЕСКОЙ, ГИПОЛИПИДЕМИЧЕСКОЙ, ГИПОГЛИКЕМИЧЕСКОЙ И ГИПОХОЛЕСТЕРИНЕМИЧЕСКОЙ АКТИВНОСТЬЮ, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И СПОСОБЫ ЛЕЧЕНИЯ УКАЗАННЫХ ЗАБОЛЕВАНИЙ | 2007 |
|
RU2361581C2 |
| ГИПОЛИПИДЕМИЧЕСКОЕ И ПРОТИВОИШЕМИЧЕСКОЕ СРЕДСТВО "СЕРПИСТЕН" | 2007 |
|
RU2337701C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ОСНОВЕ ЭКСТРАКТА ЗЕЛЕНОЙ ЯГОДЫ КОФЕ, СПОСОБ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2008 |
|
RU2378003C1 |
| КЛАТРАТНЫЙ КОМПЛЕКС АРАБИНОГАЛАКТАНА ИЛИ ГУММИАРАБИКА С 20-ГИДРОКСИЭКДИЗОНОМ, СПОСОБ ЕГО ПОЛУЧЕНИЯ (ВАРИАНТЫ), ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2013 |
|
RU2572334C2 |
| АНТИДИАБЕТИЧЕСКОЕ СРЕДСТВО | 2000 |
|
RU2165767C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ САХАРНОГО ДИАБЕТА | 2006 |
|
RU2329813C2 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИДИАБЕТИЧЕСКОЙ АКТИВНОСТЬЮ | 2006 |
|
RU2313361C1 |
| АНТИАГРЕГАЦИОННОЕ И СТРЕСС-ЛИМИТИРУЮЩЕЕ СРЕДСТВО | 2008 |
|
RU2375071C1 |
| СРЕДСТВО И СПОСОБ КОМПЛЕКСНОЙ ТЕРАПИИ БОЛЬНЫХ САХАРНЫМ ДИАБЕТОМ | 2012 |
|
RU2548731C2 |
| НОВОЕ КОМПЛЕКСНОЕ СОЕДИНЕНИЕ ОКСОВАНАДИЯ (IV) С ГИДРАЗИДОМ ИЗОНИКОТИНОВОЙ КИСЛОТЫ, ОБЛАДАЮЩЕЕ АНТИДИАБЕТИЧЕСКИМ ДЕЙСТВИЕМ И ПРОЯВЛЯЮЩЕЕ АНТИМИКОБАКТЕРИАЛЬНУЮ АКТИВНОСТЬ | 1999 |
|
RU2190618C2 |
Изобретение относится к фармации, а именно к лекарственным препаратам противодиабетического действия, и может быть использовано в качестве нового средства для коррекции нарушений углеводного обмена с целью профилактики и лечения сахарного диабета II типа. Средство представляет собой экдистероидсодержашую субстанцию, выделенную из надземной части растений серпухи венценосной Serratula coronata L. (Asteraceae), представляющую собой смесь 20-гидоксиэкдизона в количестве не менее 75% и 25S-инокостерона в количестве не менее 10%. Предлагаемое средство для лечения инсулиннезависимого диабета (диабета II типа) обладает не только сахароснижающим действием, но и гиполипидемической активностью. 3 табл., 12 ил.
Противодиабетическое средство с гиполипидемической активностью для лечения и профилактики сахарного диабета II типа, содержащее экдистероидсодержащую субстанцию, выделенную из надземной части растений серпухи венценосной Serratula coronata L. (Asteraceae), представляющую собой смесь 20-гидоксиэкдизона в количестве не менее 75% и 25S-инокостерона в количестве не менее 10%.
| Турищев С.Н | |||
| Фитотерапия | |||
| - М., 2003, с.160-165 | |||
| Соколов С.Я | |||
| Фитотерапия и фитофармакология | |||
| - М., 2000, с.516-520 Телятьев В.В | |||
| Целебные клады | |||
| - Иркутск, 1991, с.250 | |||
| ТОНИЗИРУЮЩЕЕ И АКТОПРОТЕКТОРНОЕ СРЕДСТВО "СЕРПИСТЕН" | 2005 |
|
RU2276991C1 |
| ОНКОЛОГИЧЕСКИЙ РАСТИТЕЛЬНЫЙ СБОР ДЛЯ ЛЕЧЕНИЯ РАКА | 2003 |
|
RU2246963C1 |
Авторы
Даты
2008-11-10—Публикация
2007-02-06—Подача