Область техники, к которой относится изобретение
Настоящее изобретение касается анализа ароматических углеводородов, в частности полициклических ароматических углеводородов (ПАУ), таких как бензо[a]пирен (БаП), в пищевых маслах, пищевых жирах и родственных продуктах, таких как дистилляты данных материалов. В особенности оно касается способа и аппаратуры для такого анализа с применением расположенных линейно гельпроникающей хроматографии (ГПХ)/высокоэффективной жидкостной хроматографии (ВЭЖХ). Описываются определение суб-ppb уровней ПАУ и определение многих ПАУ одновременно.
Ссылки
Cejpek, K. et al., Int.J.Environmental Anal. Chem. 61(1):65-80 (1995).
Germuska, R. and Michalski, R., Central European Journal of Public Health 8 (Suppl.):92-93 (2000).
Kraak, J.C., Int.J.Environ.Anal.Chem. 25(1-3):209-220 (1986).
Moret, S. and Conte, L.S., J. High Resolut. Chromatogr. 21(4):253-257 (Apr 1998).
Moret, S. and Conte, L.S., J.Sep.Sci. 25(1-2):96-100 (Jan 2002).
Moret, S. et al., J.Chtomatogr. A 750(1-2):361-368 (25 Oct 1996).
Myojyo, K. et al., EP632267 A1 (Jan 1995).
Perrin, J.L. et al., Fett Wiss. Technol. 95(2):40-51 (Feb 1993).
Sengupta, P. and Sil, S., J. Oil Technol. Assoc. India 15(3):54-55 (Jul-Sep 1083).
Vaessen, H.A.M.G. et al., Fresenius' Z. Anal. Chem. 332(4):325-332 (Nov 1988).
van Stijn, F. et al., J. Chomatogr. A 750(1-2):263-273 (1996).
Williams, R.A. et al., J. Chromatogr. 477:315-315 (1989).
Предшествующий уровень техники
Присутствие полициклических ароматических углеводородов (ПАУ) в пищевых маслах и жирах, например подсолнечном масле, кокосовом масле, пальмовом масле и т.д., приводит к высоким аналитическим затратам при переработке данных материалов. Источник такого загрязнения включает в себя сушку прямым нагреванием с воздухом, который содержит газообразные продукты сгорания. Использование сушки копры непосредственным обогревом представляет собой основной источник ПАУ, присутствующих в сыром кокосовом масле, которое может включать уровни ПАУ, превышающие 2000 мкг/кг. Очистка масла понижает содержание индивидуальных ПАУ до уровня мкг/кг.
Определение и регулирование ПАУ в пищевых маслах и жирах очень важно, так как многие ПАУ представляют собой сильные канцерогены. FEDIOL (Federation del'Industrie d'Huilerie de la Communaute Europeene) утвердило предел в 25 ppb (25 мкг/кг) для суммы ПАУ, 5 ppb для тяжелых ПАУ (пять и более колец) и 1 ppb для БаП (бензо[a]пирен) в пищевых жирах и маслах.
Указанные масла могут также содержать моноциклические ароматические углеводороды (например, бензол, толуол и ксилолы) вследствие загрязнения жидким топливом, которое также обычно содержит значительные уровни (примерно 10000 м.д.) низших ПАУ (нафталин, метилнафталин, фенантрен и аценафтен). Обычно загрязнение жидким топливом определяют с помощью ГХ/МС (газовая хроматография/масс-спектрометрия) определения алифатических углеводородов. Однако определенный процент данных алифатических углеводородов естественным образом уже присутствует в пищевых маслах. Соответственно, определение уровней жидкого топлива с помощью анализа ароматических углеводородов, которые не присутствуют в пищевом масле, но представляют порядка 35% большинства жидких топлив, как ожидается, даст более правильные результаты.
Предлагалось много способов для анализа бензо[a]пирена (Б[a]П или БаП) и других полициклических ароматических углеводородов (ПАУ) в пищевых маслах и жирах. Они обычно включают в себя одну или более стадий экстракции, обогащения образца и/или очистки с последующим количественным анализом, используя ГХ (газовую хроматографию) или ВЭЖХ. Способы экстракции, обычно применяемые для отделения ПАУ от липидов, включают в себя распределение в растворителе, комплексообразование с кофеином и омыление, за которым часто следует "очистка" для удаления других потенциально мешающих компонентов на колонке с силикагелем (см. обзор Moret и Conte, 2000, и ссылки в нем). См. также, например, Sengupta et al. 1093; Moret et al. 1996, 1998, 2002; Perrin et al. 1993; Vaessen et al. 1988; Myojyo et al/ 1995; Germuska et al. 2000; и Cejpek et al/ 1995; все упомянутые выше. Протокол, утвержденный FEDIOL, для определения БаП в пищевых маслах дан в примерах.
Большинство из указанных способов являются длительными (до 24 часов или более), дорогими и часто приводят к потере анализируемого вещества и/или загрязнению образца, давая плохую воспроизводимость. Количество времени, требуемого для анализа, также приводит к необходимости длительного хранения большого количества материала при ожидании результатов анализа.
Соответственно, существует необходимость обеспечения более эффективных средств анализа таких материалов с точки зрения времени, стоимости и использования материала так же, как и способов, которые воспроизводимы и точны при низких уровнях обнаружения.
Сущность изобретения
В первом аспекте настоящее изобретение обеспечивает способ для определения уровня, по меньшей мере, одного полициклического ароматического углеводорода (ПАУ) в образце, выбранном из пищевых масел, пищевых жиров и их компонентов, например, жирных кислот. Данный способ включает стадии:
получение образца в первом растворителе, в котором ПАУ растворим/мы;
нанесение образца на колонку для гельпроникающей хроматографии (ГПХ) и элюирование образца ГПХ элюирующим растворителем, эффективным для получения фракции, содержащей ПАУ, которая, по существу, свободна от таких компонентов образца, как триглицерид и свободная жирная кислота;
введение фракции, без выделения, в ГПХ/ВЭЖХ систему, где к фракции добавляется растворитель, в котором ПАУ имеют низкую растворимость;
перенос фракции, без выделения, на колонку для высокоэффективной жидкостной хроматографии (ВЭЖХ) с обращенной фазой;
элюирование фракции вначале растворителем, в котором ПАУ имеют низкую растворимость;
отдельное элюирование каждого детектируемого ПАУ из ВЭЖХ колонки ВЭЖХ элюирующим растворителем;
детектирование, по меньшей мере, одного указанного ПАУ обычно посредством флуоресцентного детектирования при длине/ах волны, характерной для указанного ПАУ, и
определение уровня, по меньшей мере, одного указанного ПАУ в образце.
Используемый здесь термин "растворитель" может быть смесью растворителей, например ТГФ/ацетонитрил или вода/ацетонитрил. "Растворитель, в котором ПАУ имеют низкую растворимость," представляет собой, предпочтительно, растворитель, в котором они растворимы менее чем на 5%. Такие растворителя включают в себя от 95:5 до 100:0 вода/ацетонитрил.
Предпочтительно, данный способ осуществляют автоматическим образом. В частности, стадии введения и переноса, предпочтительно, начинают автоматически при программном регулировании механизма переключения клапана.
В одном варианте осуществления данного способа стадия элюирования включает прокачку ГПХ растворителя через ГПХ колонку с помощью первого насоса с выходом к источнику при атмосферном давлении, который может быть детектором по индексу рефракции (ИР), и, отдельно, прокачку ВЭЖХ растворителя или смеси растворителей, обычно используя отдельный (второй) насос, через петлю для введения пробы и оттуда через ВЭЖХ колонку; стадия введения включает прокачку ГПХ растворителя, содержащего ПАУ, используя первый насос, и растворителя, в котором ПАУ имеют низкую растворимость, обычно используя второй насос, через смешивающий тройник в петлю для введения пробы с выходом на ИР детектор или другой источник при атмосферном давлении с обводом ВЭЖХ колонки; и стадии переноса и элюирования включают прокачку растворителя, в котором ПАУ имеют низкую растворимость, и затем ВЭЖХ растворителя, обычно используя второй насос, через петлю для введения пробы и оттуда через ВЭЖХ колонку.
ПАУ могут быть выбраны из группы, состоящей из нафталина, метилнафталина, флуорена, аценафтена, аценафтилена, фенантрена, антрацена, флуорантена, пирена, бензо[a]антрацена, хризена, бензо[a]флуорантена, бензо[b]флуорантена, бензо[k]флуорантена, бензо[a]пирена, бензо[ghi]перилена, дибензо[ah]антрацена, индено[1,2,3-cd]пирена, бензо[е]пирена, перилена, бензоперилена, антантрена, коронена и их комбинации. В отдельных вариантах осуществления ПАУ выбирают из бензо[b]флуорантена, бензо[k]флуорантена, бензо[a]пирена, бензо[ghi]перилена, дибензо[ah]антрацена, индено[1,2,3-cd]пирена, бензо[е]пирена, перилена, антантрена, коронена и их комбинации. В одном варианте осуществления определяют единственный ПАУ, например бензо[a]пирен.
Первая смесь растворителей, предпочтительно, содержит тетрагидрофуран (ТГФ); пример представляет собой смесь ТГФ и ацетонитрила, предпочтительно, в соотношении 70:30 или больше, например примерно от 70:30 до 75:25. Элюирующий ГПХ растворитель, предпочтительно, представляет собой ТГФ. "Растворитель, в котором ПАУ имеют низкую растворимость," представляет собой, предпочтительно, от 95:5 до 100:0 вода/ацетонитрил. ВЭЖХ элюирующий растворитель обычно представляет собой градиент растворителя, содержащего изменяющиеся соотношения воды и ацетонитрила.
Извлечение ПАУ из образца составляет обычно, по меньшей мере, 99%. Данный способ может быть использован для детектирования ПАУ, предпочтительно, бензо[a]пирена, присутствующего в образце при уровне менее чем 1 ppb, предпочтительно, при уровнях менее чем 0,5 ppb, и более предпочтительно, при уровнях менее чем 0,1 ppb (0,1 мкг на кг).
В одном варианте осуществления для детектирования множества ПАУ детектирование включает переключение флуоресцентного детектора на длины волн детектирования, характерные для каждого детектируемого ПАУ, при заданном ВЭЖХ времени удерживания для ПАУ автоматическим образом. Данный способ может быть использован для определения, по меньшей мере, 10 разных ПАУ в образце или, в других вариантах осуществления, для определения, по меньшей мере, 20 разных ПАУ в образце.
В соответствующем аспекте данное изобретение обеспечивает быстрый способ "по отпечаткам пальцев" для определения уровня бензо[a]пирена в образце, выбранном из пищевых масел, пищевых жиров и их компонентов, причем данный способ включает:
получение образца в смеси растворителей, содержащей ТГФ, ацетонитрил или их смесь;
нанесение образца на колонку для гельпроникающей хроматографии (ГПХ);
элюирование образца с помощью ТГФ, эффективного для получения фракции, содержащей ароматический углеводород, которая, по существу, свободна от таких компонентов образца, как триглицерид и свободная жирная кислота; и
измерение флуоресцентного поглощения данной фракции при длине(ах) волны, характерной для бензо[а]пирена, например 378 нм возбуждение/ 403 нм испускание. Данный способ может быть использован для детектирования бензо[а]пирена в образце при уровнях менее чем 10 ppb и, предпочтительно, менее чем 5 ppb. Извлечение бензо[а]пирена из указанного образца составляет предпочтительно, по меньшей мере, 99%.
Данное изобретение также обеспечивает способ для определения уровня ароматических углеводородов в таком образце, причем данный способ включает:
получение образца в первом растворителе, содержащем ТГФ, ацетонитрил, или их смесь;
нанесение образца на колонку для гельпроникающей хроматографии (ГПХ);
элюирование образца с помощью ТГФ, эффективного для получения фракции, содержащей ароматический углеводород, которая, по существу, свободна от таких компонентов образца, как триглицерид и свободная жирная кислота; и детектирование уровня ароматических углеводородов в данной фракции с помощью УФ-поглощения. Обычно данный способ дополнительно содержит стадию оценки уровня загрязнения жидким топливом в образце, основанную на отдельно определенной корреляции между уровнем жидкого топлива и интенсивностью УФ поглощения фракции.
Когда первый растворитель представляет собой ацетонитрил, данный способ дополнительно включает экстракцию образца ацетонитрилом, и экстракт образца наносят на ГПХ колонку. Элюирующий растворитель обычно представляет собой ТГФ. Фракция ароматических углеводородов может содержать один или больше компонентов, выбранных из бензола, толуола, этилбензола, ксилолов, нафталина, метилнафталинов, фенантрена и аценафтена. Предпочтительно, уровень указанных ароматических углеводородов во фракции составляет меньше, чем 5 м.д.
Эти и другие цели и признаки данного изобретения станут более очевидными после прочтения последующего подробного описания изобретения наряду с соответствующими чертежами.
Фиг.1 показывает результат ГПХ (гельпроникающая хроматография) анализа образца сырого кокосового масла с уровнем БаП 55 мкг/кг с элюированием бензо[а]пирена (и всех ПАУ) в течение примерно 9,7 минут.
Фиг.2 показывает калибровочную кривую для БаП в модели кокосового масла, приготовленной по семи стандартам, отличающимся по концентрации от 12 до 123 мкг/кг (ppb).
Фиг.3 показывает ГПХ хроматограммы (наложенные), использованные для анализа бензо[а]пирена в трех образцах кокосового масла.
Фиг.4 показывает наложение ГПХ хроматограмм семи стандартов жидкого топлива, приготовленных загрязнением пальмового масла чистым дизельным топливом в концентрациях, меняющихся от 2 до 85 мкг/г (ppm).
Фиг.5 представляет собой линейную калибровочную кривую м.д. жидкого топлива от поглощения при 226 нм, полученную с помощью данных фиг.4.
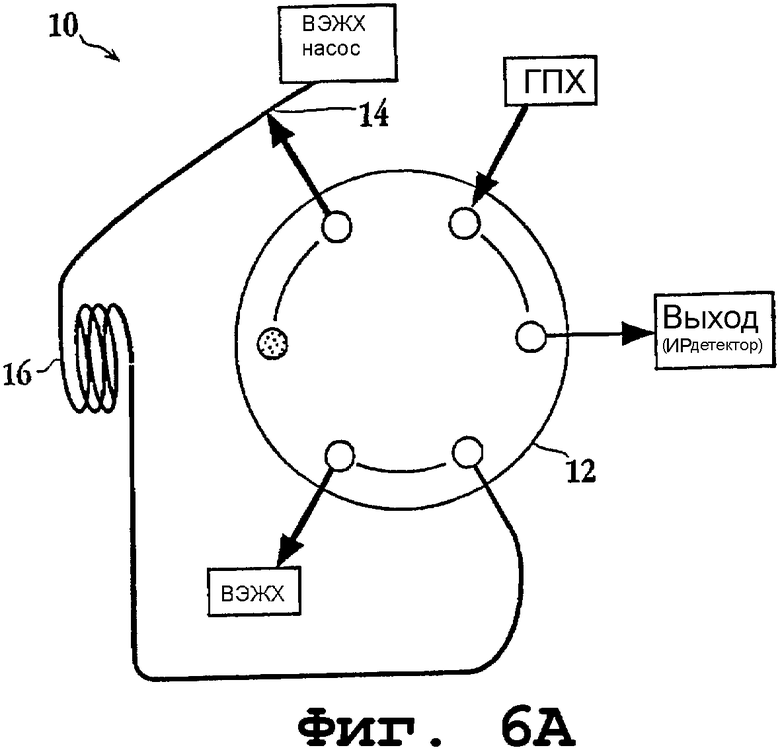
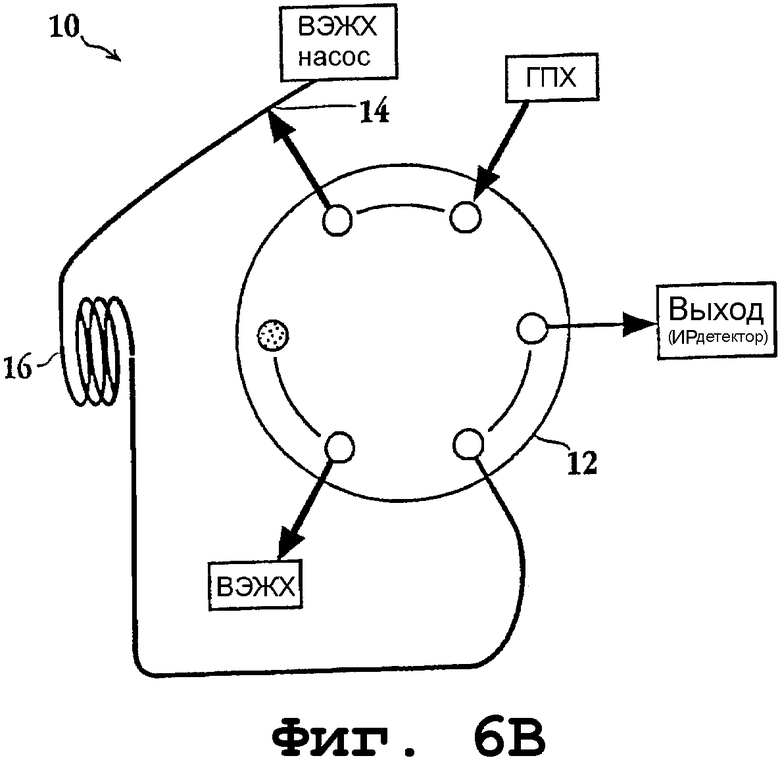
Фиг.6А-В представляют собой схематичные диаграммы переключающего растворитель интерфейса в рабочем положении и в положении введения пробы соответственно.
Фиг.6С представляет собой схематичную диаграмму расположенной линейно ГПХ/ВЭЖХ системы с переключающим растворитель интерфейсом в рабочем положении (согласно фиг.6А).
Фиг.7 представляет собой график, сравнивающий уровни бензо[a]пирена, измеренные в нескольких образцах, определенные двумя коммерческими лабораториями и в соответствии с вариантом осуществления данного изобретения.
Фиг.8 представляет собой ВЭЖХ хроматограмму, показывающую разделение разных ПАУ в образце сырого кокосового масла, полученную с помощью расположенной линейно ГПХ/ВЭЖХ.
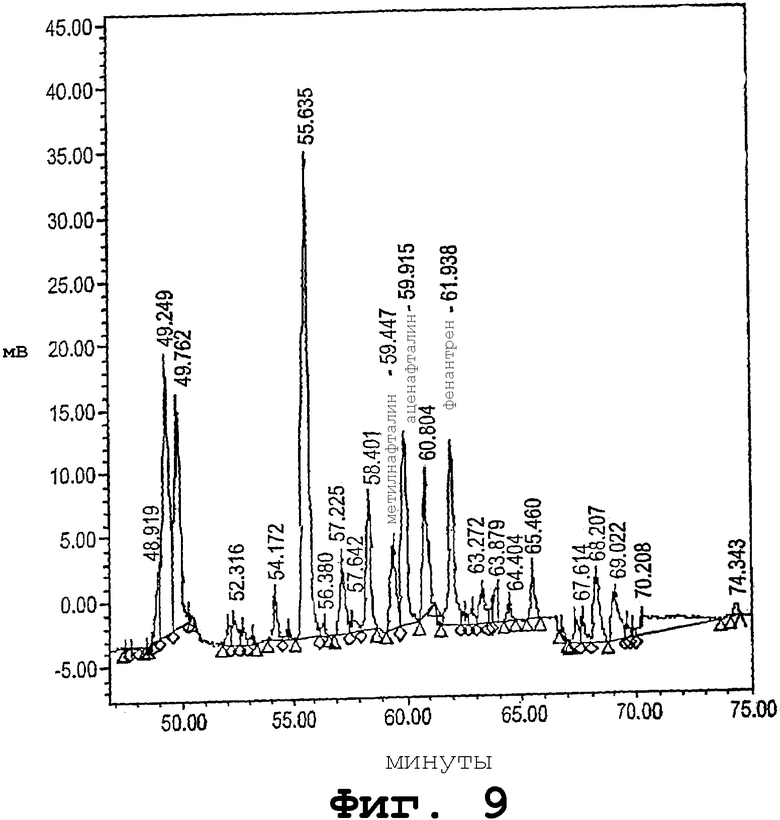
Фиг.9 представляет собой ВЭЖХ хроматограмму стандарта, содержащего 34 м.д. жидкого топлива в сыром пальмовом масле, полученную с помощью расположенной линейно ГПХ/ВЭЖХ, используя один набор частот детектирования для детектирования БаП.
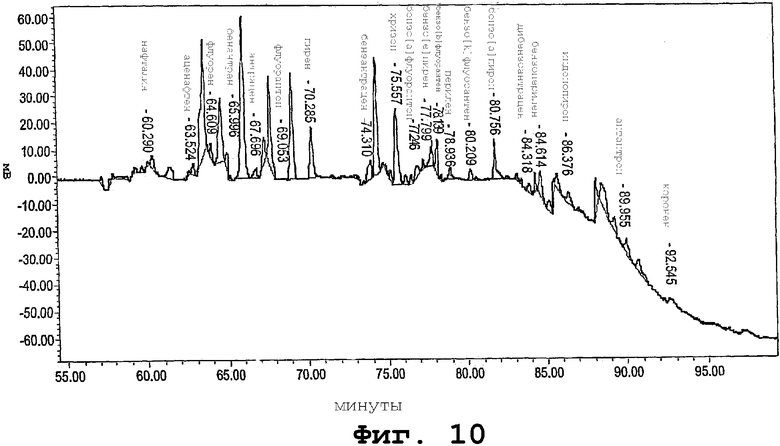
Фиг.10 представляет собой ВЭЖХ хроматограмму, показывающую разделение множества ПАУ в образце пищевого масла, полученную с помощью расположенной линейно ГПХ/ВЭЖХ, используя программное переключение частоты детектирования для каждого компонента ПАУ.
Подробное описание изобретения
Настоящее изобретение обеспечивает способы детектирования низких уровней ароматических углеводородов, в частности бензо[a]пирена и/или других ПАУ, в сырых и очищенных пищевых маслах и жирах так же, как и в родственных продуктах, таких как жирные кислоты, полученные из таких масел и жиров. Данные способы используют гельпроникающую хроматографию (ГПХ), одну или в комбинации с высокоэффективной жидкостной хроматографией с обращенной фазой (ОФ-ВЭЖХ).
I. Анализируемые соединения
Полициклические ароматические углеводороды (ПАУ) представляют собой органические соединения, содержащие два или больше конденсированных карбоциклических ароматических колец. Указанные соединения представляют собой результат геохимических процессов и являются также частыми побочными продуктами неполного сгорания или пиролиза органического вещества. Многие известны как канцерогены. Их можно классифицировать как легкие ПАУ, имеющие от двух до четырех, обычно три или четыре, ароматических кольца, или тяжелые ПАУ, имеющие пять или более конденсированных колец. Первый класс включает в себя, например, нафталин, флуорен, аценафтен, аценафтилен, фенантрен, антрацен, флуорантен, пирен, бензо[a]антрацен и хризен. Последний класс включает в себя, например, бензо[a]флуорантен, бензо[b]флуорантен, бензо[k]флуорантен, бензо[a]пирен, бензо[ghi]перилен, дибензо[ah]антрацен, индено[1,2,3-cd]пирен, бензо[е]пирен, перилен, антантрен и коронен. Сообщалось, что бензо[a]пирен является самым канцерогенным из известных ПАУ.
Среди указанных соединений следующие появились в списке FEDIOL:
• Фенантрен
• Антрацен
• Флуорантен
• Пирен
• Бензо[a]антрацен
• Хризен
• Бензо[е]пирен
• Перилен
• Бензо[a]пирен
• Дибензо[ah]антрацен
• Бензоперилен
• Антантрен
• Коронен
Любые другие ПАУ, которые желательно детектировать, также могут быть детектированы с помощью способов, описанных здесь, если время удерживания и длина(ны) волны детектирования известны или определены для выбранного соединения. Данный способ может быть использован для детектирования алкилзамещенных ПАУ, таких как метилнафталин.
Жидкие топлива представляют собой сложные смеси алканов, алкенов, циклоалканов и ароматических углеводородов и также включают в себя небольшой процент серо-, азот- и кислородсодержащих соединений. Ароматические соединения представляют по оценке 35% жидких топлив и обычно включают в себя бензол, толуол, этилбензол и ксилолы, известные, в целом, как БТЭК. Жидкие топлива также содержат примерно 15000 м.д. (1,5%) ПАУ, из которых нафталин, метилнафталины, фенантрен и аценафтен составляют примерно 10000 м.д. (1,0%). Так как БТЭК, ПАУ и алкилированные ПАУ, все присутствующие в жидких топливах, являются опасными компонентами, оценка токсичности и подтверждение загрязнения жидким топливом оптимально базировались бы на анализе указанных ароматических соединений лучше, чем на анализе насыщенных углеводородов, как в текущей практике. Кроме того, как указано выше, указанные ароматические компоненты не присутствуют естественным образом в пищевых маслах в отличие от насыщенных углеводородов.
II. Матрицы
Материалы, анализируемые способами, описанными здесь, обычно представляют собой пищевые жиры или масла, которые могут быть растительного происхождения, включая например, кукурузное масло, кокосовое масло, подсолнечное масло, пальмовое масло, сафлоровое масло и продукты какао, или животного происхождения, включая например, сало, жир или рыбий жир. Указанные материалы, в основном, состоят из различных смешанных триглицеридов (ТГ); т.е. жирных алкиловых сложных триэфиров глицерина, где жирные алкильные компоненты включают такие группы, как пальмитил, стеарил, миристил и т.д., и обычно также включают фракцию свободных жирных кислот (СЖК). Пищевые масла, пищевые жиры и их компоненты такие, как СЖК, могут называться здесь вместе как "продукты, содержащие пищевые масла".
В сыром кокосовом масле, которое представляет собой типичное пищевое масло, средняя молекулярная масса триглицеридного компонента равна 674, и средняя молекулярная масса компонента свободных жирных кислот (СЖК), которые, в первую очередь, представляют собой С12 жирные кислоты, равна 200. Средняя молекулярная масса триглицеридных компонентов других типичных пищевых масел равна следующему: пальмовое масло, 850; соевое масло, 875; подсолнечное масло, 879; рапсовое масло, 880; хлопковое масло, 860; и кукурузное масло, 887.
Описанные здесь способы являются приемлемыми для любой матрицы, которая достаточно растворима в растворителе(ях), используемом(ых) для выделения ароматического углеводородного компонента от оставшихся компонентов матрицы с помощью ГПХ, как описано ниже, и чьи компоненты достаточно отделяются от ароматического компонента посредством описанного ГПХ способа. Матрицы, имеющие неполную растворимость в данном растворителе, также могут быть использованы, как описано в разделе IIIC ниже, где анализируемое соединение экстрагируют из матрицы. Такие типичные матрицы могут включать в себя, например, компоненты пищевых масел, такие как жирные кислоты, и другие пищевые продукты, которые могут быть предварительно обработаны для удаления белков или любых других мешающих компонентов. Другие углеводородсодержащие матрицы, такие как непищевые масла, топлива и смазочные материалы, также рассматриваются.
III. Аналитические способы: ГПХ
А. Выделение ароматических углеводородов из матриц посредством ГПХ
Гельпроникающая хроматография (ГПХ) представляет собой разновидность жидкостной хроматографии, в которой молекулы разделяются посредством повторяющегося обмена между растворителем подвижной фазы и растворителем в неподвижной жидкой фазе в порах наполнителя колонки. Диапазон размера пор заполняющего материала определяет диапазон молекулярных размеров, в котором может проходить разделение. В общем, большие молекулы исключаются из некоторых или всех пористых матриц наполнителя вследствие их физического размера, и элюируются из колонки раньше более мелких молекул, которые имеют возможность проникать в больший процент пор заполненной растворителем матрицы. ГПХ разделение также зависит от реального трехмерного размера или формы молекулы; таким образом, молекулы, имеющие близкие молекулярные массы, но разные формы, часто могут быть разделены, и молекулы, имеющие разные молекулярные массы, но близкие формы, могут элюироваться вместе.
В случае пищевых масел полное разделение между триглицеридами, СЖК и ароматическими углеводородами может быть достигнуто при помощи ГПХ, как описано здесь. Так как ароматические соединения схожи по форме, они обычно элюируются вместе, несмотря на разницу в молекулярной массе.
ГПХ колонки коммерчески доступны в разнообразии характеристик по молекулярной массе. Для настоящих применений разделение проводят на аналитической колонке, имеющей относительно низкий эффективный диапазон по молекулярной массе, например от 0 до 1000. Предпочтительный материал наполнителя колонки представляет собой сшитый полистирол или стирол-дивинилбензольный сополимер (СДВБ). Одной из таких колонок является колонка Waters Styragel®-HR 0,5 (4,3 мм внутренний диаметр · 300 мм; 5 мк размер частиц). Другие подходящие колонки доступны из различных источников, например Polymer Laboratoies Inc. или Jasco Corporation.
Было обнаружено, что работа при слегка повышенной постоянной температуре улучшает воспроизводимость результатов ГПХ, и также приводит к лучшей растворимости образцов и меньшему давлению в колонке. Предпочтительно поддерживать температуру колонки примерно 40°С во время разделения посредством применения термостата колонки.
В. Быстрый анализ "по отпечаткам пальцев" при помощи ГПХ
Согласно одному варианту осуществления изобретения анализ "по отпечаткам пальцев" одного ПАУ, предпочтительно бензо[a]пирена, в сыром масле может проводиться за примерно 15 минут или меньше с пределом обнаружения примерно 5 мкг/кг. В типичном анализе масло растворяют в соответствующем растворителе, например смеси ТГФ/ацетонитрил, фильтруют через 0,20 мкм шприц-фильтр, вводят в систему колонки ГПХ и элюируют, предпочтительно ТГФ.
Для растворения образца и для элюирования используют растворители или смеси растворителей, в которых все анализируемые вещества легко растворяются. Типичным растворителем является ТГФ. Было найдено, что использование смеси ТГФ:ацетонитрил в соотношении примерно 5:2 по объему для приготовления образца и ТГФ для элюирования увеличивает разрешение и резкость пика ПАУ относительно образца, приготовленного в одном ТГФ. Данное соотношение, предпочтительно, лежит между примерно 70:30 и 75:25. Могут быть использованы более высокие доли ТГФ, например 80% или 90%, до 100% ТГФ, хотя резкость пика может уменьшиться. Большие количества ацетонитрила не рекомендуются из-за пониженной растворимости анализируемых соединений.
Флуоресцентное детектирование предпочтительно для детектирования ПАУ, так как данные соединения имеют тенденцию быть сильно флуоресцентными в отличие от компонентов матрицы. Отдельное детектирование по индексу рефракции может быть использовано для определения суммарного введенного образца, так как выходной сигнал ИР детектора зависит только от количества образца. Поэтому использование внутреннего стандарта не является необходимым. Предпочтительно, когда компоненты матрицы также легко растворимы в растворителях образца и элюирования.
Как указано выше, ПАУ обычно элюируются вместе в ГПХ процессе пищевых масел или подобных матриц. Так как каждый ПАУ имеет различные максимумы длин волн возбуждения и испускания, флуоресцентное детектирование может быть установлено для конкретного соединения, такого как БаП, как показано на фиг.1.
Было найдено, что примерно восемь других ПАУ соединений дают некоторый уровень помех на БаП при данной установке, как описано в примере 1 ниже. Антрацен представляет собой единственное соединение из них, дающее потенциально значительное количество помех при данных длинах волн.
Фиг.1 показывает результаты ГПХ анализа образца сырого кокосового масла, имеющего уровень БаП 55 мкг/кг, с элюированием БаП (и всех ПАУ) при приблизительно 9,7 минут. Первичные компоненты пищевого масла, ТГ и СЖК, не детектируются флуоресцентным детектором, как указано выше. Однако было замечено, что при использовании детектора по индексу рефракции они элюируются при приблизительно 6,7 и 7,4 минут соответственно.
Чтобы получить калибровочную кривую для матрицы кокосового масла, были приготовлены семь БаП стандартов в диапазоне концентраций от 12 до 123 мкг/кг. Калибровочная кривая (полученная с использованием программы Cargill Instrument Performance Monitoring) показана на фиг.2.
Три образца сырого кокосового масла были проанализированы на БаП с использованием настоящего ГПХ способа. Были сделаны двенадцать дубликатных пробегов, и результаты сравнивали с анализами независимых лабораторий. Результаты, приведенные в таблице 1, показывают низкое стандартное отклонение для ГПХ способа и приемлемое согласие с внешними анализами.
По желанию, может быть получена отдельная БаП калибровочная кривая для разных матриц в практике настоящего ГПХ анализа, так как разные матрицы могут содержать различные ПАУ в разных пропорциях. Однако было показано, что калибровочная кривая, полученная для матрицы кокосового масла, дает точные результаты при анализе сырого подсолнечного масла. Анализ трех образцов подсолнечного масла на БаП с уровнями ниже примерно 10 мкг/кг с использованием калибровочной кривой, полученной для кокосового масла, показал хорошую корреляцию с количественными данными внешней лаборатории. Фиг.3 показывает наложенные хроматограммы для данных трех образцов, где данные образцы по определению внешней лаборатории содержат, соответственно, 5,3, 6,3 и 8,9 мкг/кг БаП. Определение с помощью настоящего метода с использованием калибровочной кривой, полученной для матрицы кокосового масла, дало уровни 5,7, 6,4 и 8,1 мкг/кг соответственно.
Показано, что указанный способ быстрого анализа имеет высокую воспроизводимость, хотя определение БаП может зависеть от присутствия антрацена. Предел обнаружения для БаП при использовании данного способа составляет примерно 5 ppb (мкг/кг).
С. ГПХ анализ загрязнения жидким топливом детектированием низших ароматических углеводородов
Для анализа низших ароматических углеводородов таких, как БТЭК (бензол, толуол, этилбензол и ксилолы), используют УФ детектирование в диапазоне длин волн 200-750 нм. Указанные соединения обычно элюируются примерно вместе в ГПХ анализе и могут детектироваться при длине волны примерно 226 нм.
Для усиления детектирования указанных соединений в пищевой масляной матрице может быть желательно увеличить их концентрацию экстракцией матрицы ацетонитрилом. Триглицериды слабо растворимы в ацетонитриле, тогда как различные ароматические соединения в жидком топливе (и свободные жирные кислоты) растворимы. Экстракцию проводят взбалтыванием смеси сырого масла и ацетонитрила (например, один грамм масла на 6 мл растворителя) в течение нескольких секунд и отстаиванием смеси. Ацетонитрильную (верхнюю) фазу отделяют, фильтруют (например, через 0,45 мкм шприцевой фильтр) в пробоотборную пробирку и используют для введения в ГПХ систему. Данная обработка обычно увеличивает концентрацию анализируемых соединений в матрице пищевого масла примерно в 25 раз. ТГФ предпочтителен для элюирования образца.
Чистое дизельное топливо (B.C.R. Standard № 106, Community Bureau of Reference, Bruxelles) использовали для приготовления семи стандартов жидкого топлива в сыром пальмовом масле в диапазоне концентраций от 2 до 85 мкг/г. Данный диапазон концентраций включает в себя жидкое топливо в концентрации 25 м.д., определенной по соглашению между производителями как максимальный уровень загрязнения жидким топливом, приемлемым для производства пищевого масла. Указанные стандарты анализировали после отработки, описанной выше (взбалтывание с ацетонитрилом), использованной для приготовления образцов.
В сыром пальмовом масле, использованном для приготовления стандартов, было найдено с помощью внешней коммерческой лаборатории согласно AOCS способу 6 мкг/г (6 м.д.) алифатических углеводородов. Так как незагрязненное пальмовое масло содержит примерно от 4 до 20 м.д. алифатических углеводородов, это масло посчитали свободным от загрязнения жидким топливом на основе данного определения.
Фиг.4 показывает наложение ГПХ хроматограмм семи стандартов с УФ детектированием при 226 нм. В условиях анализа ароматические соединения элюировались при примерно 12,2 минуты.
Линейная калибровочная кривая м.д. жидкого топлива от поглощения при 226 нм (фиг.5) была получена по данным стандартам с использованием Cargill Instrument Performance Monitoring software. Такая калибровочная кривая дает корреляцию между уровнем ароматических углеводородов, определяемым по УФ поглощению, и м.д. жидкого топлива для жидкого топлива состава, подобного использованному для приготовления стандартов.
Воспроизводимость ГПХ способа для загрязнения жидким топливом тестировали, используя шесть повторов трех разных стандартов. Результаты даны в таблице 2. Было найдено, что предел обнаружения данного способа составляет примерно 2 м.д.
IV. Аналитические способы: расположенная линейно ГПХ/ВЭЖХ
А. Уровень техники, аппаратура и общий способ
Разделение соединений с помощью ВЭЖХ так же, как и с помощью других разновидностей жидкой хроматографии, основано на взаимодействии между соединениями, растворенными в подвижной фазе, и неподвижной фазой, т.е. твердым наполнителем колонки. Движущая сила разделения заключается в разнице энтальпий взаимодействия разных компонентов (соединений, подвижной фазы и неподвижной фазы). Хроматография с обращенной фазой (ОФ), которая использует неполярную (гидрофобную) неподвижную фазу и полярную подвижную фазу, является предпочтительной для настоящих разделений. В ОФ-ВЭЖХ первичные взаимодействия отвечают за удерживание и разделение не ковалентных ассоциаций неполярных компонентов (анализируемых соединений или их неполярных компонентов и неподвижной фазы) в полярной среде. Типичные подвижные фазы, используемые в ОФ-ВЭЖХ, представляют собой водные растворы замещающих агентов, таких как ацетонитрил или 1-пропанол. Обычно анализируемые вещества элюируют градиентом подвижной фазы, в которой концентрация замещающего агента постепенно увеличивается.
Наиболее широко используемые ОФ-ВЭЖХ адсорбенты в данной области основаны на диоксиде кремния, модифицированном углеводородом, обычно диоксиде кремния, модифицированном октадецильными (С18) группами. Такие колонки могут быть обозначены как ОДК (октадецил диоксид кремния) колонки, и много таких колонок коммерчески доступно; например, Waters Bondapack C18. Колонки, содержащие диоксид кремния, связанный с алкилфенилом, также описаны как подходящие для разделения химических соединений, включая ПАУ (например, Faizy et al., патент США № 5993653).
Для элюирования используют градиент растворителей, состоящий из полярных растворителей. Типичный градиент содержит ацетонитрил и воду, хотя другие полярные элюирующие растворители, например метанол или этилацетат, также могут быть использованы. Ввиду сильной флуоресценции, демонстрируемой большинством анализируемых ПАУ, предпочтителен спектрофлуорометрический детектор.
ПАУ фракция, полученная посредством ГПХ отделения от матричных компонентов, таких как ТГ и СЖК, в матрице пищевого масла, как описано выше, по существу, свободна от триглицеридов и СЖК. "По существу, свободна" означает, что фракция свободна от любого детектируемого (например, спектрофотометрическими детекторами, соединенными с аппаратом) ТГ или СЖК компонента. Указанную фракцию линейно переносят, то есть без выделения фракции или удаления из аппарата, в ВЭЖХ систему посредством ГПХ-ВЭЖХ интерфейса.
Типичный интерфейс, такой как обозначен 10 на фиг.6А-В, включает в себя переключающий механизм 12 для введения пробы, такой как Rheodyne автоматический шестипозиционный поточный процессор, смешивающий тройник 14 и петлю 16 для введения пробы, предпочтительно имеющую объем 2 мл. Схематичное изображение компонентов расположенной линейно ГПХ-ВЭЖХ системы с интерфейсом в режиме разделения (как описано ниже) показано на фиг.6С.
Одной из функций, выполняемых интерфейсом, является переключение растворителей между ГПХ и ВЭЖХ системами. Как описано выше, растворители, в которых ПАУ хорошо растворимы, такие как ТГФ, являются предпочтительными для ГПХ отделения от других компонентов матрицы. В типичном ГПХ отделении следовых количеств ПАУ в образце пищевого масла фракцию ПАУ получают в примерно 0,3 мл ТГФ. Прямое введение указанной фракции в ВЭЖХ колонку обычно приводит к быстрому элюированию ПАУ, по существу, одним пиком. Для разделения на колонке для ВЭЖХ с обращенной фазой применяют, как указано выше, градиент полярного растворителя.
Спаренная ГПХ-ВЭЖХ система описана в литературе. Некоторые применяют подобные растворители в двух системах (например, Winkle 1990; De Vries 1989), так что переключение растворителя не требуется. В случаях, когда применяются разные растворители, контакт ГПХ растворителя с ВЭЖХ колонкой описывают как проблематичное. Смотри, например, Kraak et al. 1986 или van Stijn et al. 1996, которые отмечают подобную проблему в ДАКХ (донорно-акцепторная комплексная хроматография)-ВЭЖХ спаренной системе. Kraak et al. решили данную проблему в системе для удаления белков из образцов плазмы введением предварительной колонки для адсорбции анализируемых соединений из ГПХ растворителя и затем высвобождения их в ВЭЖХ подвижную фазу. Williams et al. (1989) описывают способ, в котором ГПХ элюат в ТГФ непрерывно разбавляется водой, и выбранная фракция переносится в ОФ-ВЭЖХ колонку в воде. Данная система описана, как имеющая пределы обнаружения примерно 50 ppb.
В настоящей системе, как указано выше, ГПХ осуществляется в органическом растворителе, таком как ТГФ, тогда как для ВЭЖХ разделения обычно применяется система водного растворителя. Соответственно, водный растворитель (например, растворитель, состоящий преимущественно из воды) добавляют к образцу в интерфейсе, который содержит устройство переключения клапанов. Указанный растворитель представляет собой растворитель, в котором детектируемые ПАУ имеют низкую растворимость (также называемый "не-растворитель"), например, от 95:5 до 100:0 вода/ацетонитрил. В режиме введения пробы, как показано на фиг.6В, фракция ПАУ в ТГФ (обычно имеющая объем примерно 0,3 мл, как указано выше) смешивается с таким растворителем при, по существу, таком же объеме и скорости потока посредством смешивающего тройника 14 и переносится в петлю 16 для введения пробы.
Другой функцией интерфейса является защита ГПХ колонки от быстрых изменений давления, когда образец вводится в ВЭЖХ-систему. Во время введения пробы, как показано на фиг.6В, и ГПХ ТГФ поток, и поток ВЭЖХ вода/ацетонитрил поступают на ИР детектор, который работает при атмосферном давлении. Соответственно, давление на ГПХ колонке остается, по существу, постоянным.
После введения пробы (примерно 1 минута) установка клапанов возвращается в обычное положение (фиг.6А) и содержимое петли 16 для введения пробы переносится в ВЭЖХ колонку. Из-за присутствия добавленной воды в образце анализируемые ПАУ больше не являются растворимыми и осаждаются в верхней части ВЭЖХ колонки. ПАУ сначала элюируют, используя "не-растворитель", как описано выше, с последующим программируемым градиентом растворителя, эффективным для раздельного элюирования каждого детектируемого ПАУ из ВЭЖХ колонки.
Таким образом, последовательность операций в типичном переключении расположенного линейно ГПХ-ВЭЖХ интерфейса, которое, предпочтительно, осуществляется автоматическим способом, является следующей.
(1) ГПХ фаза (фиг.6А): ГПХ растворитель прокачивают через ГПХ колонку (ГПХ насос, не показан) с выходом на ИР детектор или другой источник при атмосферном давлении; отдельно ВЭЖХ градиент или "не-растворитель" прокачивают (ВЭЖХ насос) через петлю 16 для введения пробы и ВЭЖХ колонку.
(2) Фаза введения пробы (фиг.6В): ГПХ растворитель, содержащий анализируемые соединения (ГПХ насос) и "не-растворитель" (ВЭЖХ насос), прокачивают через смешивающий тройник 14 в петлю 16 для введения пробы с выходом на ИР детектор или другой источник при атмосферном давлении; ВЭЖХ колонку обходят. Введение пробы, предпочтительно, осуществляется в течение программируемого или заданного периода времени, например одну минуту.
(3) Разделяющая фаза (фиг.6А): "не-растворитель" и затем ВЭЖХ градиент прокачивают через петлю 16 для введения пробы (ВЭЖХ насос), перенося содержимое в ВЭЖХ колонку для элюирования.
Переключение от фазы (1) к (2) и от (2) к (3), предпочтительно, выполняется автоматически (т.е. без необходимости действий оператора) посредством программного регулирования механизма 12 переключения введения пробы. Данное устройство программируется таким образом, чтобы переключать в режим введения пробы (фиг.6) после заданного времени после введения пробы; это заданное время основано на заданном времени(ах) удерживания ГПХ анализируемых соединений. Данное устройство затем автоматически переключается в режим разделения (фиг.6А) после заданного времени введения пробы, например одна минута.
В. Количественный анализ бензо[а]пирена с помощью ГПХ-ВЭЖХ
В одном аспекте данное изобретение обеспечивает способ точного определения единственного ПАУ, такого как бензо[а]пирен, в сложных матрицах, таких как пищевые масла и жиры. Данный способ применяет тандемную, расположенную линейно ГПХ-ВЭЖХ для выделения и/или количественного определения анализируемого вещества. Стадию ГПХ разделения такую, как описана выше для быстрого "по отпечаткам пальцев" анализа БаП, использовали как стадию предварительной очистки в данном способе. Применение ВЭЖХ дает возможность обнаружить "тяжелые" ПАУ, которые обычно не могут быть обнаружены с помощью способов газовой хроматографии (ГХ) из-за термического разложения. Данный способ имеет предел обнаружения примерно 0,01 мкг/кг и может быть осуществлен за примерно 45 минут или меньше.
Как дополнительно описано ниже, данное изобретение также обеспечивает способ точного определения множества ПАУ в одном анализе. Определение 20 разных ПАУ выполняется за примерно 100 минут или меньше, как описано ниже в разделе D.
В иллюстрации ГПХ-ВЭЖХ способа для количественного определения БаП готовили стандарты, содержащие БаП (Alltech Chemie) с уровнями в диапазоне от 1 до 80 ppb в очищенном кокосовом масле. Условия, описанные ниже в примере 3, включая программу градиента, найденную особенно эффективной для выделения бензо[а]пирена, применили для ВЭЖХ разделения.
Калибровочная кривая была получена для разных стандартов с последующими десятью повторными измерениями 30 ppb стандарта. Среднее значение концентрации БаП, полученное из десяти повторных измерений 30 ppb стандарта, составило 29,61 ppb со стандартным отклонением 0,58 ppb.
В дополнительной иллюстрации способа уровни БаП в нескольких естественных образцах проанализировали в тех же условиях и результаты сравнили с анализами двух независимых лабораторий. Предполагалось, что данные лаборатории применят обычный протокол, утвержденный для определения уровней БП в пищевых маслах, который представлен ниже как сравнительный пример. Как отмечалось выше, указанный обычный протокол гораздо менее эффективен по времени, труду и материалам, чем настоящий описанный способ.
Как показано в таблице 3 ниже и графически на фиг.7, способ данного изобретения давал хорошее соответствие с коммерческим тестированием. Образцы с №1-12 были образцами кокосового масла, тогда как образцы от 13 до 15 были подсолнечными маслами, показывая, что настоящий способ может быть использован с различными матрицами пищевых масел.
Указанная таблица также показывает величины, полученные только при ГПХ, которые часто находятся в хорошем соответствии с более количественным способом.
№
описание
В таблице 4 представлены дополнительные сравнительные данные, в этот раз образцы очищенного кокосового масла для анализа имели уровень БаП меньший, чем 3,0 ppb.
На фиг. 8 показано разделение различных ПАУ в образце сырого кокосового масла с использованием ГПХ/ВЭЖХ, как описано выше, с флуоресцентным детектором при 378 нм/403 нм, как описано в примере 3. ВЭЖХ градиент растворителя, показанный в примере 3, оптимизировали для отделения БаП от других компонентов. В данном примере получали хорошее разделение с элюированием БаП в 51,3 минуты. Суммарное время анализа, включая подготовку образца, составило примерно 80 минут. При желании, градиент растворителя можно варьировать, чтобы оптимизировать выделение других отдельных ПАУ соединений.
С. ГПХ-ВЭЖХ анализ сложной смеси ПАУ: установка простого детектирования
Ароматические соединения, выделенные из матрицы пищевого масла с помощью ГПХ для определения загрязнений жидким топливом, как описано выше в разделе IIIC, могут быть дополнительно проанализированы расположенной линейно ВЭЖХ. Для иллюстрации данного способа фракции ГПХ, содержащие ароматические углеводороды, полученные, как описано в разделе IIIC, анализировали на метилнафталин, аценафтен и фенантрен, которые представляют собой доминирующие ПАУ в жидком топливе. Интерфейс и ВЭЖХ аппаратура были такие же, как описаны выше в материалах и способах. Использовали следующую программу градиентного элюирования:
Определяемые вещества детектировали методом флуоресценции при 244/375 нм (возбуждение/испускание).
Семь стандартов, полученных, как описано в разделе IIIC, имеющих от 2 до 85 м.д. жидкого топлива в сыром пальмовом масле, анализировали с помощью ГПХ/ВЭЖХ. Фиг. 9 показывает выход флуоресцентного детектирования фракции, содержащей 34 м.д. жидкого топлива. Как показано, ВЭЖХ времена удерживания метилнафталина, аценафтена и фенантрена составили 59,5 мин, 60,0 мин, и 62,0 мин соответственно.
Получили калибровочную кривую м.д. жидкого топлива от уровня данных трех ПАУ, и кривую использовали для установления м.д. жидкого топлива в нескольких коммерческих образцах при анализе данных трех ПАУ расположенной линейно ГПХ/ВЭЖХ. Результаты, включая результаты, полученные только ГПХ, представлены в таблице 5.
Как показано, при данных низких уровнях коммерческие результаты, полученные при анализе алифатических углеводородов, имеют тенденцию быть значительно более высокими, чем результаты, полученные при анализе ароматических. Как отмечено выше, это, вероятно, обусловлено присутствием в пищевых маслах природных алифатических углеводородов.
(пальмовое масло)
(три ПАУ)
D. ГПХ-ВЭЖХ анализ сложной смеси ПАУ: установка множественного детектирования
Для оптимального детектирования сложной смеси ПАУ флуоресцентный детектор может быть включен на специфическую длину волны, как наиболее подходящую. Данный способ дает возможность быстро определять уровни в сложной смеси ПАУ в образце в одном анализе.
Калибровочные стандарты, приготовленные введением чистого масла с известным количеством каждого ПАУ, который следует определять, могут быть использованы для определения времени удерживания и отклика детектора для каждого ПАУ с данной установленной колонкой и с данными условиями. Анализируемый образец точно взвешивают и приготавливают, как описано выше, например, растворением в 5:2 ТГФ/ацетонитрил, фильтрацией и вводом в ГПХ колонку. Образец элюируют ТГФ, затем вводят в дозировочную петлю, как описано выше (см. фиг. 6В), где образец смешивается с растворителем, в котором ПАУ имеет низкую растворимость («не-растворитель», как описано выше) например, 95:5 вода/ацетонитрил. Затем образец переносят в колонку ВЭЖХ (переключением назад к режиму работы; фиг. 6А), и начинается градиентная ВЭЖХ. Элюирование обычно начинается с «не-растворителя», как показано в примере 4 ниже.
Флуоресцентный детектор программируют на переключение соответствующей для каждого компонента (ПАУ) длины волны детектирования при определенном заранее времени удерживания компонента. Одна такая программа показана в примере 4 ниже. (Аценафтилен не детектируется флуоресценцией, он может быть определен встроенным в систему УФ детектором). Соединения идентифицируют сравнением времен удерживания с предварительно введенным стандартом и количественно определяют по измерению площади пика.
Как иллюстрация образец, содержащий двадцать ПАУ, которые были найдены в пищевых маслах, включая тринадцать ПАУ из списка FEDIOL, анализировали за примерно 100 минут, как описано в примере 4 ниже.
Хроматограмма типичного анализа сложной смеси ПАУ с использованием нескольких установленных детекторов показана на фиг. 10.
В анализе, описанном здесь, преодолены многие неудобства, представленные в традиционных способах, например процедуры, требующие много материалов и времени, и риск потери или загрязнений во время приготовления образца. Упрощение стадии очистки образца при использовании ГПХ перед ВЭЖХ анализом уменьшает риск потери анализируемого вещества или загрязнения. Автоматический ввод и для сложной анализируемой смеси переключение установок детектора дает возможность проводить анализ быстро и удобно. Полностью автоматизированным, аналитическим, расположенным линейно способом 20 различных ПАУ (включая в себя 13 FEDIOL ПАУ) могут быть проанализированы за 100 минут, как показано выше. Расположенная линейно ГПХ-ВЭЖХ технология резко уменьшает время анализа и объем расходуемых растворителей и может применяться в качестве рутинного анализа на непрерывной основе.
Примеры
Следующие примеры имеют целью проиллюстрировать, но не ограничить изобретение.
Материалы и способы
ГПХ выполняли на Waters Styragel®-HR 0,5 ГПХ колонке (4,3 мм внутренний диаметр х 300 мм; 5 мкм размер частиц) с использованием ВЭЖХ-насоса, модель 515, автосамплера, модель 717, дифференциального рефрактометра, модель 410, детектора с набором диодов, модель 996 (или другой УФ детектор) и флуоресцентного детектора. Для области «отпечатков пальцев» при анализе жидкого топлива использовали только детектор с набором фотодиодов.
Для ГПХ/ВЭЖХ (количественного) анализа применяли ВЭЖХ насос, модель 515, автосамплер, модель 717 с 250 мкм петлей для образца, дифференциальный рефрактометр, модель 410, детектор с набором диодов, модель 996, сканирующий флуоресцентный детектор, модель 474, градиентный насос, модель 600, Rheodyne 6-позиционный потоковый процессор и термостат для колонки. A Waters Millennium Chromatography manager использовали для получения, обработки и управления хроматографической информации. RP-ВЭЖХ используемая колонка была BESTER Analytical PAK (ODS) колонкой 5 мкм, 250 х 3,0 мм, с Phenomenex® Security Guard C18 (ODS) предколонкой 4 х 3,0 мм.
Пример 1. Быстрый анализ «отпечатков пальцев» Б[а]П в кокосовом масле с помощью ГПХ
Образец (примерно 8-12 капель) сырого кокосового масла растворяли в 7 мл 5:2 ТГФ/ацетонитрил, и раствор фильтровали через 0,20 мкм шприцевой фильтр и вводили в Waters Styragel®-HR 0,5 ГПХ колонку, (4,3 мм внутренний диаметр х 300 мм; 5 мкм размер частиц). Образец элюировали с помощью ТГФ при скорости потока, равной 0,30 мл/мин, и фракцию, элюированную в примерно 9,7 минуты детектировали с помощью флуоресценции. Флуоресцентное детектирование проводили при 378 нм возбуждение/403 нм испускание, специфической для бензо[а]пирена. Суммарное количество введенного образца определяли одновременно по индексу рефракции детектирования.
Типичная хроматограмма представлена на фиг.1. Калибровочная кривая интенсивности флуоресценции от ppb Б[а]П, полученная при проведении аналогичного анализа семи приготовленных стандартов с использованием Cargill Instrument Performance Monitoring software, представлена на фиг.2.
Флуоресценцию некоторых других ПАУ при 378нм/403нм исследовали для определения возможных помех при Б[а]П детектировании.
В таблице 6 показана высота пика относительно количества соединения для серии ПАУ (введенных индивидуально) с детектированием при 378 нм/403 нм (оптимизированным для детектирования БаП). Как можно видеть, антрацен представляет собой единственное соединение, дающее помеху потенциально значительной величины при указанных длинах волн. (Хотя бензо[k]флуорантен поглощает при указанной длине волны сильнее, чем антрацен, он обычно присутствует в пренебрежимых количествах по сравнению с антраценом).
введенного
(нг)
378нм/403нм
Пример 2. Быстрый анализ жидкого топлива в пальмовом масле с помощью ГПХ
Один грамм образца сырого пальмового масла смешивали с 6 мл ацетонитрила, и смесь взбалтывали в течение нескольких секунд и давали возможность отстояться. Смесь фильтровали через 0,45 мкм шприцевой фильтр в пробоотборную пробирку, отделяли ацетонитрил как (верхнюю) фазу и вводили в колонку ГПХ, как описано выше в примере 1. Образец элюировали ТГФ при скорости потока, равной 30 мл/мин, фракцию с временем элюирования, равным примерно 12,2 мин, детектировали по УФ поглощению при 226 нм.
На фиг.4 показана схема ГПХ хроматограмм семи образцов, введенных с различным количеством чистого дизельного топлива и проанализированных данным способом. Калибровочная кривая поглощения от м.д. дизельного топлива, полученная с использованием Cargill Instrument Perfomance Monitoring software, показана на фиг. 5.
Пример 3. Количественный анализ бензо[а]пирена в пищевом масле с помощью ГПХ-ВЭЖХ
Раствор ПАУ в ТГФ получали с помощью ГПХ разделения компонентов из матрицы кокосового масла, как описано выше (пример 1). Данную фракцию (приблизительно 0,3 мл) переносили в расположенную линейно ВЭЖХ систему (Bester Analytical PAK ODS колонка (5 мкм размер частиц, 259 х 3,0 мм) с предколонкой Phenomenex® Security Gard C18 (ODS) (4 х 3,0 мм) введением с помощью переключающего интерфейса, состоящего из Rheodyne автоматического шестипозиционного потокового процессора, тройника для смешения и петли для введения пробы, имеющей объем 2 мкл. Во время нормальной операции, как показано схематически на фиг.6А, ВЭЖХ растворитель (ACN/вода) прокачивали через тройник для смешения и петлю для ввода. Во время ввода, как показано схематически на фиг.6В, фракция ПАУ в ТГФ смешивалась с ВЭЖХ растворителем в тройнике для смешения. Выходящий поток растворителя во время ввода проходил RI детектор, который работал при атмосферном давлении. Соответственно, давление в ГПХ колонке оставалось, по существу, постоянным.
После приблизительно одной минуты интерфейс переключался назад к рабочему режиму (Фиг.6А) и образец элюировали, используя градиентную программу, представленную ниже:
Ацетонитрил(%)
5:95 ACN:вода(%)
В данных условиях бензо[а]пирен элюировали за примерно 51,3 мин и детектировали по флуоресценции при 378 нм/403 нм. Калибровочную кривую получали по нескольким стандартам очищенного кокосового масла, введенного с бензо[а]пиреном на уровнях 1-80 ppb.
Пример 4.Детектирование сложной смеси ПАУ с помощью ГПХ-ВЭЖХ при использовании программируемого детектирования
Калибровочные образцы готовили введением стандартной смеси, содержащей 16 ПАУ (Restek; product M-610-QC в ацетонитриле), в чистое масло. Стандарт содержал аценафтен, аценафтилен, антрацен, бензантрацен, бензо[а]пирен, бензо[b]флуорантен, бензоперилен, бензо[k]флуорантен, хризен, дибензантрацен, флуорантен, флуорен, инденопирен, нафталин, фенантрен и пирен. Бензо[а]флуорантен, бензо[е]пирен, перилен и коронен получали от Alltech Chemie. Стандарты готовили при концентрации Б[а]П в интервале от 0,2 до 4,2 ppb (мкг/кг). Данные образцы использовали для определения времени удерживания и отклика детектора для каждого анализируемого компонента.
Образцы точно взвешивали и растворяли в 6 мл 5:2 ТГФ/ацетонитрил. Раствор фильтровали через 0,45 мкм шприцевой фильтр в пробоотборную пробирку и использовали для ввода. Предпочтительные количества образца и объем ввода для образцов различных типов даны ниже:
Используемая аппаратура описана выше в разделе описания материалов и способов. ГПХ и ВЭЖХ колонки поддерживали при 40°С в течение всей процедуры.
Объем 100 мкл образца вводили в ГПХ колонку и элюировали ТГФ при скорости потока, равной 0,30 мл/мин. После, примерно, 11 минут интерфейс переключали на режим ввода (Фиг.6В) в течение одной минуты. Образец затем переносили в ВЭЖХ колонку (при переключении назад в режим работы; Фиг.6А) и начинали ВЭЖХ градиент, показанный в таблице 8 ниже.
Флуоресцентный детектор программировали на переключение на подходящую для детектирования длину волны для каждого компонента (ПАУ) при заранее определенном времени удерживания данного компонента. Одна такая программа показана в таблице 9 ниже. (Поскольку аценафтилен не детектируется флуоресценцией, он может быть определен встроенным УФ детектором). Соединения идентифицировали сравнением времен удерживания с предварительно введенными стандартами и количественно определяли по измерению площади пика.
Градиент растворителя
Программа время-длина волны для флуоресцентного детектирования
мин
Сравнительный пример: официальный протокол определения БаП в пищевых маслах
Следующая процедура взята из "Code of Practice on Polycyclic Aromatic Hydrocarbons" of French Society for Fat Science (FEDIOL).
Принцип: подходящее количество масла или жира в легком петролейном эфире добавляли на верх 22 г колонки с окисью алюминия активности 4 (способной вместить или удержать примерно 600/мг масла или жира) и бензо[а]пирен элюировали из колонки 75 мл легкого петролейного эфира. Окончательный анализ проводили с помощью высокоэффективной жидкостной хроматографии с обращенной фазой, используя флуорометрический детектор.
Реагенты
• Легкий петролейный эфир или гексан аналитического качества, перегнанный над гранулами КОН (4 г/л).
• Ацетонитрил и ТГФ, LiChrsolv® (Merk).
• Сульфат натрия аналитического качества, гранулированный, безводный.
• Окись алюминия, активность 4 степени: нейтральная окись алюминия, активность супер I, полученная у Woelm, Eschwege, G.F.R., деактивированная добавлением 10 мл воды к 90 г окиси алюминия. Приведение к равновесию в течение 24 часов перед использованием и хранение в закрытом сосуде при комнатной температуре.
• Бензо[а]пирен, полученный у Bureau Communautaire des References (BCR), Brussel, Belgium. Приготовление стандартного раствора примерно 0,1 мкг/мл в тетрагидрофуране.
Аппаратура
• Стеклянная хроматографическая колонка: 30 см х 20 мм внутренний диаметр, заполненная спеченными дисками и верхушками PTEF.
• Жидкостной хроматограф высокого давления с флуорометрическим детектором.
Очистка
• Получить 20% мас./об. раствора образца масла в легком петролейном эфире.
• Заполнить хроматографическую колонку до половины легким петролейным эфиром. Быстро взвесить 22 г окиси алюминия активностью 4 степени в лабораторном стакане и немедленно перенести ее в колонку. Способствовать распределению окиси алюминия слабым постукиванием по колонке.
• Добавить безводный сульфат натрия на верх колонки слоем примерно 3 см.
• Открыть верхнюю часть и довести уровень легкого петролейного эфира до вершины слоя соли.
• Поместить 10 мл мерную колбу под колонку.
• Ввести из пипетки 2,0 мл раствора масла или жира на колонку с минимальным разбавлением, давая возможность слою растворителя войти в слой сульфата натрия между добавлениями.
• Элюировать колонку легким петролейным эфиром и отбросить первые 10 мл элюата.
• Собрать последующие 75 мл элюата в 100 мл круглодонную колбу.
• Концентрировать элюат на роторном испарителе до примерно 0,5-1 мл и перенести раствор в изгиб верхней части минипробирки (объем 2 мл).
• Продолжить испарение на водяной бане при 35°С в потоке азота до высушивания.
• Растворить осадок в 25 мкл тетрагидрофурана. Закрыть минипробирку слоем Teflon®, поместить в алюминиевую капсулу и сохранить для ВЭЖХ с флуорометрическим детектором.
ВЭЖХ анализ
ВЭЖХ оборудование состоит из насоса для жидкости (например, Waters модель 510), устройства для ввода (например, Waters U6K); колонки с обращенной фазой; флуорометрического детектора (например, Perkin Elmer 204A) и интегратора (например, HP-3390A).
Условия ВЭЖХ следующие:
Елюент: ацетонитрил, скорость потока 1 мл/мин.
Колонка: колонка с обращенной фазой для ВЭЖХ, Vydoc TP-RP, длиной 25 см, внутренним диаметром 4,6 мм, размером частиц 10 мкм (ex Chrompack).
Детектор: длина волны возбуждения 381 нм, длина волны испускания 403 нм.
• Ввод 15 мкл стандартного раствора бензо[a]пирена.
• Ввод 15 мкл образца.
Расчет
При количестве образца, равном 400 мг, конечный объем фракции бензо[a]пирена равен 25 мкл, используют равные объемы (15 мкл) образца и стандарта, и:
h1 = высоте пика образца
h2 = высоте пика стандарта
с = количеству бензо[a]пирена (нг) в 15 мкл стандарта
p = уровню бензо[a]пирена мкг/кг в образце

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ ОБЩИХ И ПОЛИЦИКЛИЧЕСКИХ АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ В КОМПОНЕНТАХ ЭКОСИСТЕМЫ | 2015 |
|
RU2589897C1 |
| СПОСОБ КАЧЕСТВЕННОГО И КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ В СЛОЖНЫХ СМЕСЯХ И ЭКСТРАКТАХ НИТРОПРОИЗВОДНЫХ ПОЛИЦИКЛИЧЕСКИХ АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ, ИМЕЮЩИХ ФОСФОРЕСЦЕНЦИЮ В ЗАМОРОЖЕННЫХ РАСТВОРАХ | 1997 |
|
RU2122199C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПОЛИЦИКЛИЧЕСКИХ АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ В ПОЧВАХ И ДОННЫХ ОТЛОЖЕНИЯХ | 2019 |
|
RU2719578C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ БЕНЗ(А)ПИРЕНА В МОЧЕ МЕТОДОМ ЖИДКОСТНОЙ ХРОМАТОГРАФИИ | 2011 |
|
RU2466406C1 |
| Способ подготовки проб цельного и сухого молока для определения в них химических загрязнителей | 2021 |
|
RU2774814C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ БЕНЗ(А)ПИРЕНА В КРОВИ МЕТОДОМ ЖИДКОСТНОЙ ХРОМАТОГРАФИИ | 2014 |
|
RU2546530C1 |
| Способ определения содержания полициклических ароматических углеводородов в маслах-пластификаторах | 2016 |
|
RU2630854C1 |
| Способ подготовки проб для определения алифатических и полициклических ароматических углеводородов в донных отложениях | 2017 |
|
RU2646402C1 |
| СПОСОБ УДАЛЕНИЯ ПОЛИЦИКЛИЧЕСКИХ АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ | 2009 |
|
RU2516556C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ ТРУДНОЛЕТУЧИХ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ В ГАЗООБРАЗНОЙ СРЕДЕ, КОМПОЗИЦИЯ В КАЧЕСТВЕ СОРБЕНТА, ПРИМЕНЕНИЕ СОРБЕНТА | 2012 |
|
RU2510501C2 |








Изобретение относится к пищевой промышленности. Способ включает: приготовление указанного образца в растворителе, в котором каждый указанный полициклический ароматический углеводород (ПАУ) растворим (например, тетрагидрофуран (ТГФ), ацетонитрил или их смесь), нанесение указанного образца на колонку для гельпроникающей хроматографии (ГПХ), элюирование указанного образца элюирующим растворителем для получения фракции, содержащей указанный ПАУ, ввод указанной фракции без выделения в систему гель проникающая хроматография/высокоэффективная жидкостная хроматография, причем растворитель, в котором каждый указанный ПАУ имеет низкую растворимость, добавляют к указанной фракции, перенос указанной фракции, без выделения, на колонку для высокоэффективной жидкостной хроматографии (ВЭЖХ) с обращенной фазой, первоначальное элюирование указанной фракции растворителем, в котором каждый указанный ПАУ имеет низкую растворимость, отдельное элюирование каждого указанного ПАУ, который подлежит детектированию, из указанной ВЭЖХ колонки ВЭЖХ элюирующим растворителем, детектирование указанного, по меньшей мере, одного ПАУ, определение уровня указанного, по меньшей мере, одного ПАУ в указанном образце. 3 н.п. и 23 з.п. ф-лы, 12 ил., 9 табл.
Приоритеты по пунктам:
| WO 9206758 A, 04.01.1995 | |||
| СПОСОБ ОПРЕДЕЛЕНИЯ ПОЛИЦИКЛИЧЕСКИХ АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ В БИОЛОГИЧЕСКИХ ОБЪЕКТАХ | 2000 |
|
RU2187106C1 |
| Способ определения состава и содержания ароматических углеводородов в нефтепродуктах | 1987 |
|
SU1523972A1 |
Авторы
Даты
2008-11-27—Публикация
2004-05-13—Подача