Изобретение относится к биотехнологии, в частности к созданию на основе коллагеназы микробного происхождения субстанции для лекарственных средств.
Известна группа микробных коллагеназ, которая широко используется в биотехнологии и для лабораторных целей, например, коллагеназы, синтезируемые бактерией Clostridium histolyticum. Продуцентами коллагеназ являются также насекомые Hypoderma lineatum и камчатские крабы [1].
Известными аналогами предлагаемого изобретения могут быть препараты, полученные из бактерий Clostridium histolyticum и крабовая коллагеназа [1]. Бактерия Clostridium histolyticum является возбудителем газовой гангрены, строгим анаэробом, требующим особых условий выращивания. Технология получения препарата из этой бактерии сложная и дорогостоящая. Крабовая коллагеназа уступает по свойствам бактериальной, так как неполностью нейтрализует коллаген. Кроме того, присущий препарату фибренолитические и тромболитические свойства могут вызывать нежелательное воздействие при нанесении на кожу.
Наиболее близким прототипом предлагаемого биологически активного ультрафильтрата является коллагеназа, выделенная из культуральной жидкости штамма Streptomyces lavendulae ВКПМ S-910 [2].
Недостатком указанного изобретения является низкая коллагенолитическая активность, более сложный и дорогостоящий способ получения названного фермента, а также ограниченная область использования в медицинской биотехнологии.
Технической задачей данного изобретения является получение высокоэффективного биологически активного ультрафильтрата, содержащего коллагеназу и протеазу микробного происхождения, предназначенного для использования в качестве субстанции для лекарственных средств в различных ранозаживляющих препаратах, препаратах для лизиса послеоперационного или посттравматического гемоторакса, для лизиса послеоперационных спаек, в косметологии.
Техническая задача решается тем, что заявленная биологически активная субстанция содержит коллагеназу и протеазу из Streptomyces lavendulae ВКПМ S-910 при следующих ферментативных активностях:
- коллагенолитическая активность 1800-2500 КЕА/мл,
- протеолитическая активность 120-200 ПЕ/мл.
Для получения заявленной субстанции-ультрафильтрата используют штамм Streptomyces lavendulae ВКПМ S-910, который выращивают на плотной питательной среде - на картофельном агаре, а затем на ферментационной питательной среде следующего состава (г/л): кукурузная мука - 20; пептон - 0,5; сухие кормовые дрожжи - 0,05; MgSO4·7H2O - 0,4; желатин - 0,5; вода водопроводная рН 6,4-6,8. Выращивание проводят в колбах Эрленмейера объемом 250 мл на качалке (200 об/мин) при температуре 28 градусов Цельсия в течение 72-96 часов. Мицелий отделяют центрифугованием. Процедуру получения биологически активного ультрафильтрата из фильтрата культуральной жидкости начинают с ее концентрирования при одновременном отделении низкомолекулярных веществ и белковых фракций при температуре 15-20 градусов Цельсия и давлении 760-800 мм рт.ст. Фильтрат культуральной жидкости помещают в ультрафильтрационную лабораторную установку с рабочей поверхностью 2 квадратных дециметра. Приемная емкость заполняется фильтратом. Ультрафильтрацию нативного раствора проводят под давлением 0,4±0,02 МПа. Для получения биологически активного ультрафильтрата в работе используют мембрану с низкой проницаемостью по протеазе. Полученный биологически активный ультрафильтрат хранят при температуре+1-+20 градусов Цельсия в присутствии стабилизатора.
Субстанция для дерматологических лекарственных средств «Ультрализин» соответствует требованиям разработанных технических условий ТУ 9336-001-11684510-03, введенных в действие с 01.07.2003 года, с соблюдением санитарных норм и правил, действующих на предприятиях микробиологической промышленности Российской Федерации.
По своим физико-химическим характеристикам «Ультрализин» соответствует следующим показателям:
- раствор имеет цвета от светло-коричневого до темно-коричневого;
- обладает специфическим запахом;
- растворяется в воде, 95-процентном спирте, хлороформе;
- рН водного раствора составляет 5,0-7,0;
- коллагенолитическая активность составляет от 1800 до 2500 коллагенолитических единиц активности на 1 мл;
- общая протеалитическая активность составляет от 150 до 200 протеолитических единиц на 1 мл;
- нетоксичен, неаллергенен;
- по микробиологической чистоте соответствует требованиям Га XI, вып.2, стр.193.
Коллагенолитическая активность определяется по методу Розена [4]. Протеолитическая активность определялась по Кунитцу [3].
Определение коллагенолитической активности.
За единицу коллагенолитической активности (КЕА) принимается такое количество фермента, при воздействии которого на коллаген выделяются продукты гидролиза, равноценные 1 мкг L-лицина в стандартных условиях опыта.
В 5 пробирок вместимостью по 20 мл вносят пипеткой по 2 мл суспензии коллагена в фосфатном буфере рН 7,4. В 1, 2 и 3 пробирки (опытные) прибавляют по 2 мл испытуемого раствора ультрализина (перед анализом содержимое ампулы или флакона осторожно взболтать). В пробирки 4 и 5 (контрольные) прибавляют по 2 мл воды. Все пробирки закрывают пробками и помещают в термостат при 37±0,5 градусов Цельсия на 18 часов. Охлаждают.
Из каждой опытной и контрольной пробирки отбирают по 1 мл раствора, вносят в 5 конических пробирок вместимостью 10 мл и прибавляют по 1 мл двухпроцентного раствора нингедрина в ацетоне. Пробирки помещают на 10 минут в водяную баню при 50 градусах Цельсия. Охлаждают и после испарения ацетона (определяют по отсутствию запаха ацетона), доводят объем раствора водой до 10 мл.
Определяют величины оптической плотности на спектрофотометре при длине волны 600 нм в кюветах с толщиной слоя 10 мм. В качестве раствора сравнения используют воду. По калибровочному графику находят значения концентрации L-лицина в опытных и контрольных пробирках, вычисляют средние арифметические величины. Из величины опытной концентрации вычитают величину контрольной. Эту величину используют для расчета активности ультрализина. Активность субстанции (Ак) в коллагенолитических единицах (КЕА) вычисляют по формуле:
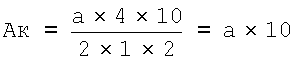
где а - количество L-лицина в мг, найденное по графику.
Определение протеолитической активности по Кунитцу
Приготовление двухпроцентного раствора казеина: реактив А 0,2 М Na·H2PO4·H2O-27,8 г/л.
Реактив Б: 0,2 М Na2HPO4·7H2О - 53,65 г/л. Взять 81 мл реактива Б.
К 4 г казеина прилить 81 мл реактива Б, выдержать 5 минут при комнатной температуре, перенести в кипящую водяную баню, остудить. Добавить 19 мл реактива А и 100 мл дистиллированной воды.
Опытные и контрольные пробирки, содержащие по 2 мл двухпроцентного казеина термостатируют 10 минут при температуре 30 градусов Цельсия. В контроль вносят по 2,5 мл трихлоруксусной кислоты (ТХУ). В опытные и контрольные пробирки вносят по 0,5 мл ультрафильтрата. Инкубируют 10 минут. Затем в опыт вносят по 2,5 мл ТХУ, через 30 секунд в каждую пробирку. Определяют оптическую плотность (ОП) ультрафильтрата при 280 нм. Полученный показатель умножают на разведение.
Ферментативная активность ультраконцентрата варьировала в следующих диапазонах:
Пример 1
Ультраконцентрат имел следующие характеристики:
Коллагенолитическая активность - 1800 КЕА/мл
Протеалитическая активность - 120 ПЕ/мл.
Пример 2
Коллагенолитическая активность - 2000 КЕА/мл,
протеолитическая активность - 150 ПЕ/мл.
Пример 3
Коллагенолитическая активность - 2500 КЕА/мл,
протеолитическая активность - 200 ПЕ/мл.
Изучение острой токсичности субстанции проводилось на белых мышах (самцы и самки с массой тела 19-21 г).
Эксперименты выполнены в соответствии с "Методическими рекомендациями по изучению общетоксического действия фармакологических средств", 1997 [5].
«Ультрализин» вводили мышам внутривенно, однократно, в объеме 0,2-0,5 мл, со скоростью 0,1 мл/с.
Длительность наблюдения за мышами составляла 10-15 дней. В ходе эксперимента следили за поведением, внешним видом, двигательной активностью, реакцией животных на внешние раздражители. В случаях летального исхода фиксировались клиническая картина и проводилось вскрытие погибших мышей.
При внутривенном введении препарата мышам в дозах до 3500-4000 ЕД/кг признаков интоксикации не наблюдалось. Животные оставались подвижными, нормально реагировали на окружающую среду. При дальнейшем увеличении дозы введенного вещества отмечалась гибель отдельных животных. Были установлены среднесмертельные дозы (LD50) для мышей при однократном внутривенном введении субстанции: LD50=12400±2500 ЕД/кг.
Максимально переносимая доза вещества при внутривенном введении мышам составляла ≈4500 ЕД/кг. В этих случаях при наблюдении за животными в течение 2 недель гибели не отмечено.
Были также проведены исследования на микробиологическую чистоту и пирогенность заявленной композиции.
Были проведены исследования на наличие пирогенных примесей в препарате. Испытание проводили на кроликах породы Шиншилла, содержащихся на стандартном рационе вивария.
Так как данный препарат применяется только наружно в качестве мази, установить четкую терапевтическую дозу сложно. Поэтому для подбора тест-дозы для испытания на пирогенность мы использовали дозу на коллагеназный препарат - от 50 ЕД/кг.
Установлено, что этот препарат тест-доза выше 5000 ЕД на кг массы животного - пирогенен.
Отмечена тенденция снижения пирогенной реакции с уменьшением вводимого объема.
Установление четкой терапевтической дозы позволит более надежно подобрать тест-дозу на пирогенность. Проведение дополнительных испытаний с новыми образцами билогически активного ультрафильтрата, в минимальном объеме разбавителя, в обоснованной тест-дозе, возможно, позволит получить результаты, свидетельствующие об отсутствии пирогенности.
Таким образом, биологически активный ультрафильтрат на основе коллагеназы, выделенного из штамма Streptomyces lavendulae ВКПМ S-910 с коллагенолитической активностью 1800-2500 КЕА/мл и протеалитической активностью 120-200 ПЕ/мл, является высокоэффективным, нетоксичным, неаллергенным средством. Имея в своем составе коллагеназу и усиливающую ее действие протеазу, предлагаемый биологически активный ультрафильтрат может быть использован в составе различных ранозаживляющих препаратов и дерматологии.
Источники информации
1. Демина Н.С., Лысенко С.В. Коллагенолитические ферменты, синтезируемые микроорганизмами. Журнал «Микробиология», 1996 год, том 65, №3, стр.293-304.
2. Демина Н.С., Лысенко С.В. Фармацевтическая композиция на основе коллагеназы микробного происхождения. Патент РФ №2075219, публ. 03.10.1997 г.
3. Kunits J./ The method of defection proteolytic enzyme. J. Gen. Physiol, 1947, v.30, №4 р.291-310.
4. Rozen H. Amodified ninhydryn colorimetric analysis for amino acids. Arch. Biohem. Biophys., 1957, v.67, p 10-15.
5. "Методическими рекомендациями по изучению общетоксического действия фармакологических средств", 1997 год.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ОСНОВЕ КОЛЛАГЕНАЗЫ МИКРОБНОГО ПРОИСХОЖДЕНИЯ | 2000 |
|
RU2166950C1 |
| ФЕРМЕНТНЫЙ РАНОЗАЖИВЛЯЮЩИЙ ПРЕПАРАТ | 2011 |
|
RU2484811C2 |
| СПОСОБ ПОЛУЧЕНИЯ КОЛЛАГЕНОЛИТИЧЕСКОГО ФЕРМЕНТА | 2020 |
|
RU2758788C1 |
| КОСМЕТИЧЕСКОЕ СРЕДСТВО НА ОСНОВЕ КОЛЛАГЕНАЗЫ МИКРОБНОГО ПРОИСХОЖДЕНИЯ | 2007 |
|
RU2355383C2 |
| Препарат-реагент для очистки поверхностей от биологического обрастания | 1991 |
|
SU1794795A1 |
| Способ получения протеолитических ферментов для обработки кожевенного сырья | 1990 |
|
SU1788010A1 |
| Способ получения коллагеназы | 1991 |
|
SU1822879A1 |
| Штамм Clostridium sporogenes B-14642 - продуцент коллагеназы | 2024 |
|
RU2835110C1 |
| Штамм актиномицета SтRертомUсеS LaVeNDULae - продуцент протеолитических ферментов | 1989 |
|
SU1735364A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОТЕОЛИТИЧЕСКОГО ПРЕПАРАТА ДЛЯ ГИДРОЛИЗА СТРУКТУРНЫХ БЕЛКОВ | 2003 |
|
RU2244741C1 |
Субстанция для дерматологических лекарственных средств на основе коллагеназы микробного происхождения представляет собой ультрафильтрат, выделенный из культуральной жидкости штамма Streptomyces lavendulae ВКПМ S-910 с коллагенолитической активностью 1800-2500 КЕА/мл и протеолитической активностью 120-200 ПЕ/мл. Изобретение обеспечивает получение биологически активного ультрафильтрата с высокой коллагенолитической и протеолитической активностью, предназначенного для эффективного использования в составе различных ранозаживляющих препаратов и дерматологии.
Субстанция для дерматологических лекарственных средств на основе коллагеназы микробного происхождения, характеризующая собой ультрафильтрат, выделенный из культуральной жидкости штамма Streptomyces lavendulae ВКПМ S-910 с коллагенолитической активностью 1800-2500 КЕА/мл и протеолитической активностью 120-200 ПЕ/мл.
| RU 2075219 С1, 10.03.1997 | |||
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ОСНОВЕ КОЛЛАГЕНАЗЫ МИКРОБНОГО ПРОИСХОЖДЕНИЯ | 2000 |
|
RU2166950C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОЛЛАГЕНАЗЫ | 1999 |
|
RU2180002C2 |
| Способ получения коллагеназы | 1991 |
|
SU1822879A1 |
| Штамм актиномицета SтRертомUсеS LaVeNDULae - продуцент протеолитических ферментов | 1989 |
|
SU1735364A1 |
| US 5989888, 23.11.1999. | |||
Авторы
Даты
2008-12-10—Публикация
2007-06-19—Подача