ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение касается новых терапевтических лекарственных препаратов; композиций, которые включают новые терапевтические лекарственные препараты; и способов введения и использования новых терапевтических лекарственных препаратов и композиций.
УРОВЕНЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
Возможность вводить биологически эффективные лекарства, которые плохо растворимы в биосовместимых растворителях, млекопитающим представляет собой главное препятствие в области фармацевтической и медицинской химии. В частности, трудности возникают, когда активное лекарство либо нерастворимо в воде, либо нестабильно в других биосовместимых растворителях.
Путь повысить растворимость медицинских агентов заключается в том, чтобы их химически модифицировать или соединить их с другой молекулой, чтобы изменить профиль растворимости в конкретном растворителе. Связанные активные лекарства, часто называемые пролекарства, включают химические производные биологически активных исходных соединений, которые превращаются в исходные соединения in vivo. Освобождение активного исходного лекарства из пролекарства может происходить в результате таких процессов, как гидролиз или ферментативный гидролиз. Скорость освобождения зависит от нескольких факторов, включая тип химической связи, соединяющей активное исходное лекарство с сопряженным фрагментом.
Внедрение водорастворимого фрагмента (например, полиэтиленгликоля, полиглутамата или полимера) для увеличения растворимости и времени циркуляции лекарства исследовано другими. Использование жирных кислот для соединения с активными лекарствами с целью определения опухолей также исследовали, как способ улучшения терапевтического индекса.
Многие сильнодействующие лекарства, такие как камптотецин и его аналоги (например, 10-гидроксикамптотецин и 7-этил-10-гидроксикамптотецин), таксаны (например, паклитаксел, додетаксел), кандесартан, амфотерицин В, азатиоприн, циклоспорин, энтакапон, даназол, элетриптан и бозентан, называя некоторые, плохо растворимы или имеют плохую клеточную проницаемость. Проблемы растворимости потенциальных терапевтических агентов обычны и часто вызывают задержки при разработке лекарства. Несколько технологий разработано для облегчения доставки плохо растворимых и нерастворимых соединений пациентам. Примеры технологий, специально разработанных для решения проблем растворимости, включают комплексообразующие агенты, наночастицы, микроэмульсии, увеличивающие растворимость рецептуры, пролекарства и новые полимерные системы.
Паклитаксел (смотри структуру ниже), природный продукт, найденный в лубе тихоокеанского тиса, представляет собой пример важного химиотерапевтического агента с широким спектром активности против солидных опухолей, первичного рака груди, рака яичника, толстой кишки и рака немалых клеток легких.
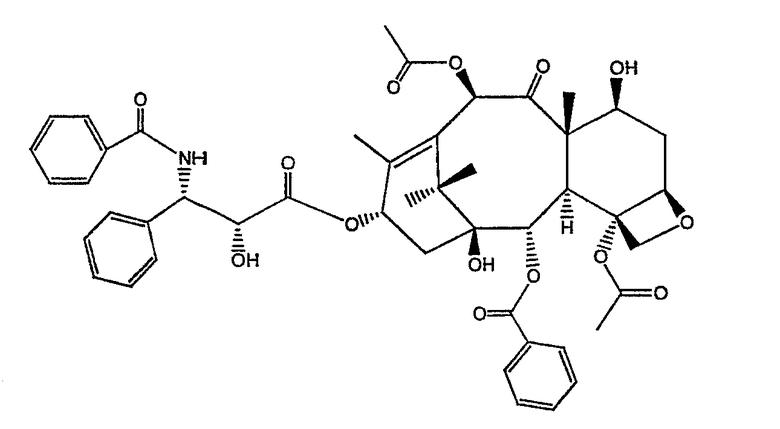
Паклитаксел оказывает противоопухолевую активность посредством связывания с тубулином и стабилизации микротрубочек и, таким образом, блокирования митоза клеток. Однако паклитаксел, подобно многим другим сильнодействующим биологически активным молекулам, имеет очень ограниченную водную растворимость.
Камптотецин (КПТ) (смотри структуру ниже) представляет собой другой пример плохо растворимого и трудного для рецептур противоракового лекарства.
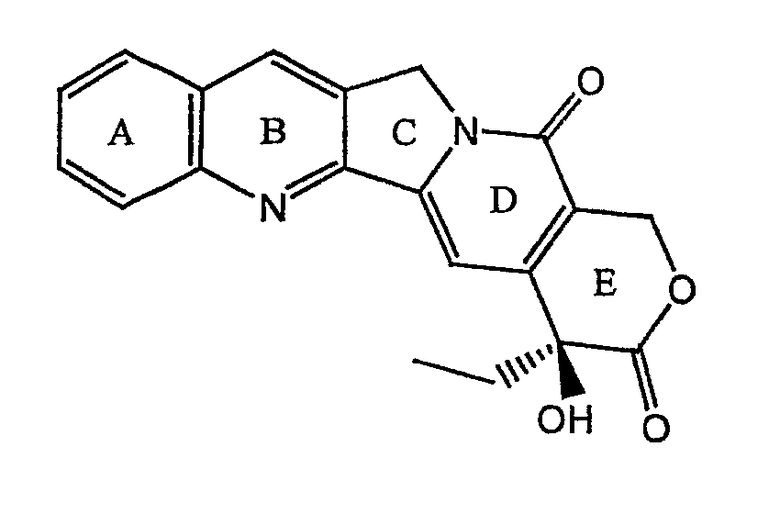
КПТ представляет собой алкалоид на основе хинолина, найденный в коре китайского camptotheca и азиатского nothapodytes. КПТ включает четыре плоских кольца (ABCD) и одно кольцо в конформации лодка (Е). Обнаружено, что КПТ имеет широкий спектр противоопухолевой активности, особенно в солидных опухолях человека. Однако лактон (кольцо Е) камптотецина и его производных полностью подвижен в щелочных условиях и физиологическом рН. Раскрытие данного кольца с образованием частиц кислой соли или карбоксилата приводит к существенной потере противораковой активности. С начала 1960-тых, когда Wall и Wani открыли КПТ, предпринимали усилия улучшить противораковую активность камптотецина и его аналогов и снизить нежелательную токсичность. До настоящего времени не было разработано успешной рецептуры камптотецина из-за его плохой растворимости в воде и органических растворителях. Однако водорастворимые аналоги камптотецина, гидрохлорид иринотекана (CAMPTOSAR) и гидрохлорид топотекана (HYCAMPTIN) разработаны и представляют собой единственные аналоги камптотецина, одобренные в настоящее время Администрацией по контролю за продуктами питания и лекарствами.
Недавно была разработана технология рецептуры эмульсии витамина Е на основе α-токоферола для доставки лекарства паклитаксел. В данной рецептуре паклитаксел растворяют в α-токофероле и получают в виде эмульсии масло-в-воде. Однако, хотя паклитаксел растворим в α-токофероле, растворимость других активных фрагментов (включая камптотецин и другие таксаны) в α-токофероле ограничена. Поэтому сохраняется необходимость в новых способах, которые безопасны и эффективны, растворения и доставки молекул плохо растворимого активного лекарства.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В одном аспекте настоящее изобретение предлагает терапевтические лекарственные соединения, которые были модифицированы для увеличения их липофильности. Соединения изобретения включают один или более терапевтических лекарственных фрагментов и один или более липофильных фрагментов. Терапевтический лекарственный фрагмент ковалентно связан с липофильным фрагментом непосредственно или с помощью связующего фрагмента. Способы изготовления модифицированных терапевтических лекарств также предлагаются.
В другом аспекте изобретения предлагаются композиции, которые включают соединения изобретения. В одном варианте осуществления данные композиции включают соединение изобретения, возможно один или более других терапевтических агентов и липофильную среду. Способы изготовления композиций также предлагаются.
В дополнительном аспекте изобретение предлагает рецептуры эмульсии и мицелл, которые включают соединение изобретения. Рецептура эмульсии включает масляную фазу и водную фазу. Масляная фаза включает соединение изобретения и липофильную среду. Эмульсия может быть эмульсией типа масло-в-воде или эмульсией типа вода-в-масле. Рецептура мицелл включает соединение изобретения и водную фазу. Способы изготовления рецептур эмульсии и мицелл также предлагаются.
В других аспектах также предлагаются способы введения соединений изобретения к нуждающемуся в них субъекту и способы создания условий, пригодных для лечения с помощью введения соединения изобретения.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Вышеупомянутые аспекты и многие сопутствующие преимущества данного изобретения будет легче оценить и лучше понять со ссылкой на последующее детальное описание, взятое в комбинации с сопутствующими чертежами, где:
ФИГУРА 1 схематически иллюстрирует реакцию d-α-токоферола и терапевтического лекарства, содержащего карбонильную группу, с получением токоферол-модифицированного терапевтического лекарственного соединения.
ФИГУРА 2 схематически иллюстрирует функционализацию токоферола хлоркарбонильной группой (-C(=O)Cl) и хлорфосфорильной группой (-P(=O)OR1Cl) и реакцию полученного хлорангидрида кислоты и соответствующего функционализированного терапевтического лекарственного соединения с получением токоферол-модифицированного терапевтического лекарственного соединения.
ФИГУРА 3 схематически иллюстрирует функционализацию токоферола дикарбоновым ангидридом (янтарный ангидрид) и реакцию полученной карбоновой кислоты и соответствующего функционализированного терапевтического лекарственного соединения с получением токоферол-модифицированного терапевтического лекарственного соединения.
ФИГУРА 4 схематически иллюстрирует приготовление токоферолсукцината камптотецина.
ФИГУРА 5 схематически иллюстрирует приготовления токоферолсукцината 10-гидроксикамптотецина и токоферолсукцината 7-этил-10-гидроксикамптотецина.
ФИГУРА 6 схематически иллюстрирует приготовление 10,20-ди(токоферолсукцинат) 7-этил-10-гидроксикамптотецина.
ФИГУРА 7 схематически иллюстрирует приготовление токоферолсукцината камптотецина, содержащего группу полиэтиленоксида.
ФИГУРА 8 схематически иллюстрирует приготовление токоферолсукцината паклитаксела.
ФИГУРА 9 схематически иллюстрирует приготовление токоферолсукцината доцетаксела.
ФИГУРА 10 схематически иллюстрирует приготовление токоферолтерефталата камптотецина.
ФИГУРА 11 схематически иллюстрирует приготовление токоферолциклогексан-1,2-дикарбоксилата 7-этил-10-гидроксикамптотецина.
ФИГУРА 12 представляет собой график, сравнивающий in vivo стабильность лактонной формы камптотецина и двух типичных токоферол-модифицированных терапевтических лекарственных соединений изобретения (SN2300, токоферолсукцинат камптотецина и SN2310, токоферолсукцинат 7-этил-10-гидроксикамптотецина).
ФИГУРА 13 представляет собой график, сравнивающий величины GI50, представленные NCI, для камптотецина, гидрохлорида иринотекана (иринотекан) и гидрохлорида топотекана (топотекан) с величинами GI50, полученными для двух типичных токоферол-модифицированных терапевтических лекарственных соединений изобретения (SN2300 и SN2310) для линий клеток: Н460, НСТ-116, НТ29 и OVCAR-3.
ФИГУРЫ 14А и 14В представляют собой графики величин концентрация-время после внутривенной инъекции 13,8 мг/кг двух типичных токоферол-модифицированных терапевтических лекарственных соединений изобретения (ФИГУРА 14А, SN2300; и ФИГУРА 14В, SN2310).
ФИГУРЫ 15А и 15В представляют собой графики, иллюстрирующие рост опухоли (мм3) по прошествии времени в ксенорентгенографах, обработанной солевым раствором, иринотеканом и двумя типичными токоферол-модифицированными терапевтическими лекарственными соединениями изобретения (SN2300 и SN2310) для двух разных опухолевых моделей (ФИГУРА 15А, NCI-H460 и ФИГУРА 15В, НТ-29).
ПОДРОБНОЕ ОПИСАНИЕ ПРЕДПОЧТИТЕЛЬНОГО ВАРИАНТА ОСУЩЕСТВЛЕНИЯ
В одном аспекте настоящее изобретение предлагает терапевтические лекарственные соединения, которые модифицированы для увеличения их липофильности. Соединения изобретения представляют собой модифицированные терапевтические лекарства. Соединения изобретения включают терапевтический лекарственный фрагмент и липофильный фрагмент.
В некоторых вариантах осуществления соединения изобретения включают больше, чем один терапевтический лекарственный фрагмент. В некоторых вариантах осуществления соединения изобретения включают больше, чем один липофильный фрагмент. В других вариантах осуществления соединения изобретения включают больше, чем один терапевтический лекарственный фрагмент, и больше, чем один липофильный фрагмент.
В некоторых вариантах осуществления терапевтический лекарственный фрагмент ковалентно связан с липофильным фрагментом через связующий фрагмент. В других вариантах осуществления терапевтический лекарственный фрагмент непосредственно ковалентно связан с липофильным фрагментом без связующего фрагмента.
В одном варианте осуществления липофильный фрагмент представляет собой фрагмент токоферола, и соединение представляет собой токоферол-модифицированное терапевтическое лекарственное соединение. Токоферол-модифицированное терапевтическое лекарственное соединение (или "токоферольное" терапевтическое лекарственное соединение) имеет один или более фрагментов токоферола, ковалентно связанных с терапевтическим лекарственным фрагментом, или фрагмент токоферола, ковалентно связанный с одним или более терапевтическим лекарственным фрагментом. Как указано выше, фрагмент токоферола ковалентно связан с терапевтическим лекарственным фрагментом непосредственно или через связующий фрагмент.
В одном варианте осуществления токоферол-модифицированные терапевтические лекарственные соединения изобретения можно представить общей формулой (1):
(T-L)n(T)mD (1)
в которой Т представляет собой фрагмент токоферола (т.е. типичный липофильный фрагмент); L представляет собой связующий фрагмент; n равно 0, 1, 2 или 3; m равно 0, 1, 2 или 3; n+m равно 1, 2 или 3; и D представляет собой терапевтический лекарственный фрагмент. В указанном варианте осуществления данное соединение включает n T-L фрагментов (т.е. токоферол-связующие фрагменты) и m фрагментов токоферола с условием, что n+m равно 1, 2 или 3. Каждый T-L фрагмент включает фрагмент токоферола, ковалентно связанный с терапевтическим лекарственным фрагментом через связующий фрагмент. Каждый из n T-L фрагментов ковалентно связан с терапевтическим лекарственным фрагментом через связующий фрагмент T-L фрагмента. В указанном варианте осуществления каждый из m фрагментов токоферола непосредственно связан с терапевтическим лекарственным фрагментом без связующего фрагмента.
Типичные соединения, имеющие формулу (1), включают соединения, в которых n равно 0 и m равно 1, 2 или 3. Данные соединения имеют общую формулу:
TmD (2)
В указанном варианте осуществления один, два или три фрагментам токоферола непосредственно ковалентно связаны с терапевтическим лекарственным фрагментом.
Типичные соединения, имеющие формулу (1), включают соединения, в которых m равно 0 и n равно 1, 2 или 3. Данные соединения имеют общую формулу:
(T-L)nD (3)
В указанном варианте осуществления один, два или три T-L фрагмента токоферола ковалентно связаны с терапевтическим лекарственным фрагментом через связующий фрагмент T-L фрагмента.
Типичные соединения, имеющие формулу (1), включают соединения, в которых m равно 1 или 2 и n равно 1 или 2. Данные соединения имеют общие формулы:
(T-L)(T)D (4)
(T-L)(T)2D (5)
(T-L)2(T)D (6)
В указанных вариантах осуществления соединения изобретения имеют фрагменты токоферола, которые непосредственно ковалентно связаны с терапевтическим лекарственным фрагментом без связующего, и фрагменты токоферола, которые непосредственно ковалентно связаны с терапевтическим лекарственным фрагментом через связующее (т.е. T-L фрагменты).
Описанные выше соединения изобретения включают один терапевтический лекарственный фрагмент и один или более липофильных фрагментов (например, фрагментов токоферола). В других вариантах осуществления соединения изобретения включают больше, чем один терапевтический лекарственный фрагмент. В одном варианте осуществления соединения изобретения включают два терапевтических лекарственных фрагмента. В другом варианте осуществления данные соединения включают три терапевтических лекарственных фрагмента. Для соединений, которые включают больше, чем один терапевтический лекарственный фрагмент, терапевтические лекарственные фрагменты могут быть одинаковыми или разными.
Для соединений, которые включают больше, чем один терапевтический лекарственный фрагмент, терапевтические лекарственные фрагменты могут быть внедрены в соединение любым подходящим способом. В некоторых вариантах осуществления терапевтические лекарственные фрагменты могут быть непосредственно ковалентно спарены (например, соединение включает -D-D- или -D-D фрагмент). В других вариантах осуществления терапевтические лекарственные фрагменты разделены в соединении связующим фрагментом (например, соединение включает -D-L-D- или -D-L-D фрагмент), липофильным фрагментом (например, соединение включает -D-Т-D- или -D-Т-D фрагмент) или липофильно-связующим фрагментом (например, соединение включает -D-Т-L-D-, -D-T-L-D или -D-L-Т-D фрагмент; или -D-L-T-L-D- или -D-L-Т-L-D фрагмент).
Типичные соединения, включающие два или три терапевтических лекарственных фрагмента, имеют общую формулу:
(T-L)(D)p (7)
в которой р равно 2 или 3. В указанном варианте осуществления два или три терапевтических лекарственных фрагмента ковалентно связаны со связующим фрагментом. В данном случае связующее включает множество мест для присоединения терапевтического лекарственного соединения (или модифицированного терапевтического лекарственного соединения). Как ясно из формулы (7), связующий фрагмент также ковалентно связан с липофильным фрагментом (например, фрагментом токоферола). Как отмечено выше, соединения изобретения, включающие больше, чем один терапевтический лекарственный фрагмент, могут иметь формулы иные, чем показано выше в формуле (7). Например, такое соединение может включать больше, чем один (например, два или три) липофильных фрагментов (например, токоферола).
Соединения изобретения включают один или более липофильных фрагментов и один или более терапевтических лекарственных фрагментов, которые либо непосредственно ковалентно соединены, либо ковалентно соединены через связующие фрагменты.
Используемый здесь термин "липофильный фрагмент" означает химический фрагмент, имеющий липофильные или гидрофобные характеристики и который увеличивает растворимость терапевтического лекарственного соединения в липофильном растворителе или окружении, когда он ковалентно связан с терапевтическим лекарственным соединением с образованием соединения изобретения. Описание типичных липофильных фрагментов, пригодных для изготовления соединений изобретения, приводится ниже.
Используемый здесь термин "терапевтический лекарственный фрагмент" означает химический фрагмент, производный от терапевтического лекарственного соединения. Описание типичных терапевтических лекарственных соединений, пригодных для изготовления соединений изобретения, приводится ниже.
Используемый здесь термин "связующий фрагмент" означает атом или группу атомов, которые ковалентно связывают, например, липофильный фрагмент с терапевтическим лекарственным фрагментом. Описание типичных связующих, пригодных для изготовления соединений изобретения, приводится ниже.
Липофильное модифицирование терапевтических лекарственных соединений. Терапевтическое лекарственное соединение может иметь одну или более подходящих функциональных групп или может быть модифицировано таким образом, чтобы включать одну или более подходящих функциональных групп для ковалентного связывания с липофильным фрагментом. Подходящие функциональные группы включают, например, следующие группы: гидроксильная группа (-ОН), аминогруппа (первичная аминогруппа -NH2 или вторичная аминогруппа -NHR1, где R1 независимо выбирают из Н, С1-6 н-алкила, С3-12 разветвленного алкила, замещенного или незамещенного С3-6 циклоалкила, замещенного или незамещенного арила или аралкила), тиольная группа (-SH), карбоксильная группа (-СООН), альдегидная группа (-СНО), изоцианатная группа (-N=C=O), сульфогруппа (-SO3H), сернокислая группа (-OSO3H), фосфорнокислая группа (-ОРО3Н), фосфоновокислая группа (-РО3Н2), галогеналлильная группа, галогенбензильная группа, замещенная галогенбензильная группа и эпоксиранилгруппа (-СН(О)СН2).
Терапевтическое лекарственное соединение может быть непосредственно соединено с липофильным фрагментом (например, фрагментом токоферола) через сложноэфирную группу (-С(=О)О-), карбаматную группу (-ОС(=О)NH-), сульфонатную группу (-SO3-), сульфатную группу (-OSO3-), фосфатную группу (-OPO3R1-, где R1 независимо выбирают из Н, С1-6 н-алкила, С3-12 разветвленного алкила, замещенного или незамещенного С3-6 циклоалкила, замещенного или незамещенного арила или аралкила), фосфонатную группу (-PO3R1-, где R1 независимо выбирают из Н, С1-6 н-алкила, С3-12 разветвленного алкила, замещенного или незамещенного С3-6 циклоалкила, замещенного или незамещенного арила или аралкила) или эфирную группу (-О-).
Соединение токоферола, типичное липофильное соединение, подходящее для изготовления соединений изобретения, включает гидроксильную группу (-ОН). После модифицирования соединение токоферола может быть ковалентно связано со связующим соединением, которое включает одну или более реакционно-способных функциональных групп. Подходящие реакционно-способные функциональные группы включают следующие группы: гидроксильная группа (-ОН), аминогруппа (первичная аминогруппа -NH2 или вторичная аминогруппа -NHR1, где R1 независимо выбирают из Н, С1-6 н-алкила, С3-12 разветвленного алкила, замещенного или незамещенного С3-6 циклоалкила, замещенного или незамещенного арила или аралкила), тиольная группа (-SH), карбоксильная группа (-С(=О)ОН), альдегидная группа (-СНО), изоцианатная группа (-N=C=O), сульфогруппа (-SO3H), сернокислая группа (-OSO3H), фосфорнокислая группа (-ОРО3Н), фосфоновокислая группа (-РО3Н2), галогеналлильная группа, галогенбензильная группа, замещенная галогенбензильная группа и эпоксигруппа (-СН(О)СН2).
Связующие фрагменты. Как отмечено выше, в некоторых вариантах осуществления соединения изобретения включают липофильный фрагмент (например, фрагмент токоферола), ковалентно связанный с терапевтическим лекарственным фрагментом посредством связующего фрагмента. В добавление к вариантам осуществления, описанным выше, токоферол-модифицированные терапевтические лекарственные соединения изобретения могут быть представлены общей формулой (8):
T-A-R-A'-D (8)
где Т представляет собой фрагмент токоферола (т.е. типичный липофильный фрагмент), D представляет собой терапевтический лекарственный фрагмент и A-R-A' представляет собой связующий фрагмент. Следует принять во внимание, что для формул (1) и от (3) до (7) выше, каждая из которых включает связующий фрагмент L, указанный связующий фрагмент L в данных соединениях может быть связующим фрагментом A-R-A'.
В формуле 8 группы А и A' независимо выбирают из O, S, SO, SO2, NR1, карбоксилатной группы (-С(=О)О-), амидной группы (-C(=O)NR1-), ангидридной группы (-С(=О)ОС(=О)-), карбаматной группы (-OC(=O)NH-), карбонилдиокси группы (-ОС(=О)О)-), уреиленовой группы (-NR1C(=O)NR2-), фосфатной группы (-OP(=O)(OR1)O-), фосфамидной группы (-OP(=O)(NR1)O-), фосфонатной группы (-OP(OR1)O-), фосфонамидной группы (-OP(=O)NR1-), сульфатной группы (-OSO2O-), сульфамидной группы (-SO2NR1-), сульфонатной группы (-SO3-), сульфонамидной группы (-SO2NR1-) и дикарбонильной группы -C(=O)R3C(=O)-, где R3 отсутствует или представляет собой двухвалентный алкил (например, -(СН2)n-, n=1-12), замещенный алкил, разветвленный алкил, циклоалкил, замещенный циклоалкил, арил, замещенный арил. Для вышеуказанных групп R представляет собой двухвалентную группу, выбранную из следующих групп: алкил; замещенный алкил, разветвленный алкил; циклоалкил; замещенный циклоалкил; гетероалкил; замещенный гетероалкил; арил; замещенный арил; аралкил; замещенный аралкил; аминокислота; пептид; полипептид; белок; моно-, ди- или полисахарид; олигомер этиленгликоля, полиэтиленгликоль; полиалкиленоксидные полимеры, такие как полиэтиленоксид и полипропиленоксид; и сополимер полиэтиленоксид-полипропиленоксид. Для вышеуказанных групп R1 и R2 независимо выбирают из Na+, K+, H, С1-6 н-алкила, С3-12 разветвленного алкила, замещенного или незамещенного С3-6 циклоалкила, замещенного или незамещенного арила и замещенного или незамещенного аралкила.
Используемый здесь термин "арил" означает моноциклические или полициклические ароматические соединения, имеющие от 6 до 14 атомов углерода или гетероатомов, и включает карбоциклические арильные группы и гетероциклические арильные группы. Типичные арильные группы включают фенил, нафтил, пиридинил, пиримидинил, тиазолил, индолил, имидазолил, фуранил и подобные. Термин "аралкил" означает алкильную группу, которая замещена арильной группой.
Следующие соединения (соединения от 9 до 32) представляют собой типичные примеры соединений, имеющих формулу 8.
Связующий фрагмент (L) и терапевтический лекарственный фрагмент (D) могут быть ковалентно соединены через сложноэфирную группу. В одном варианте осуществления терапевтический лекарственный фрагмент включает гидроксильную группу, которая связана с карбоксильной группой связующего фрагмента. Связующий фрагмент может быть соединен с фрагментом токоферола через простую эфирную группу (соединение 9), сложноэфирную группу (соединение 10), аминогруппу (соединение 11) или амидную группу (соединение 12).
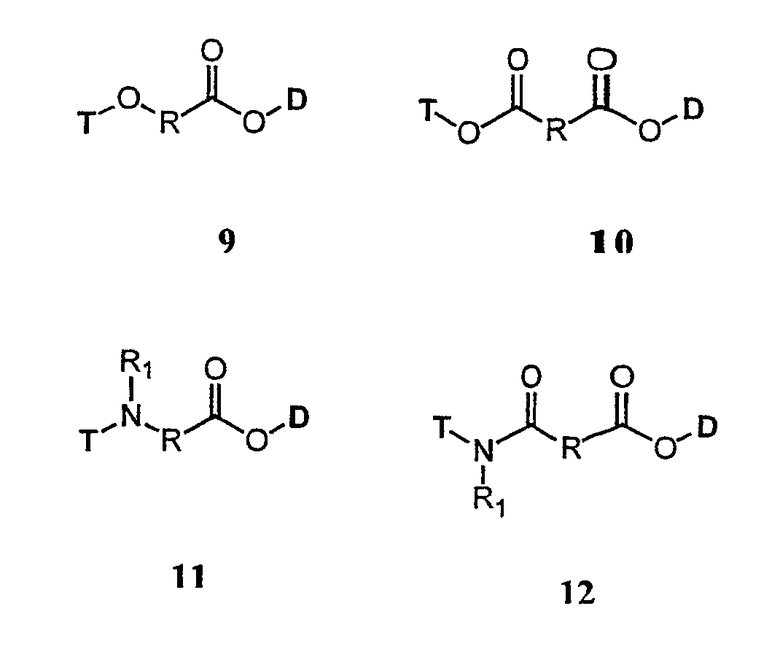
В другом варианте осуществления терапевтический лекарственный фрагмент (D) включает карбоксильную группу, которая соединена с гидроксильной группой связующего фрагмента (L). Связующий фрагмент может быть связан фрагментом токоферола через простую эфирную группу (соединение 13), сложноэфирную группу (соединение 14), аминогруппу (соединение 15) или амидную группу (соединение 16).
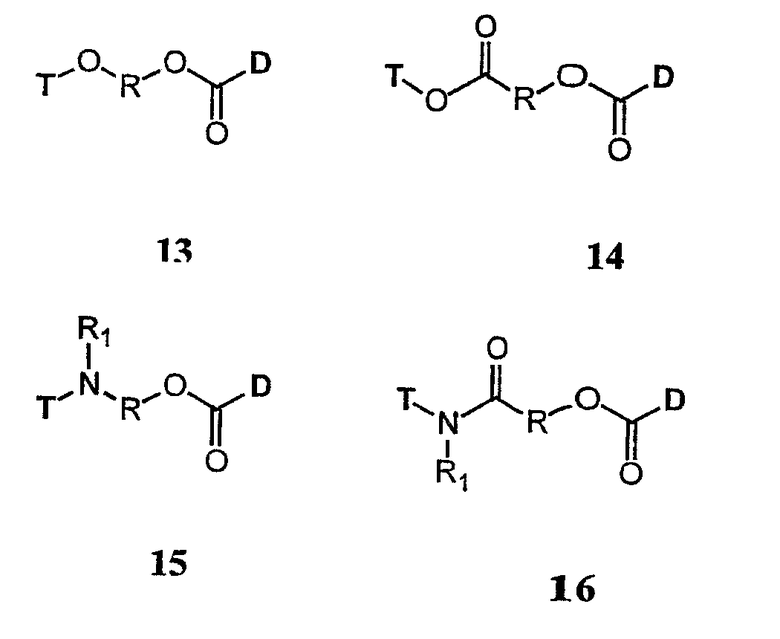
В вышеуказанных соединениях двухвалентную группу R выбирают из алкила; замещенного алкила; разветвленного алкила; циклоалкила; замещенного циклоалкила; гетероалкила; замещенного гетероалкила; арила; замещенного арила; аралкила; замещенного аралкила; аминокислоты; пептида; полипептида; белка; моно-, ди- или полисахарида; олигомера этиленгликоля, полиэтиленгликоля; полиалкиленоксидных полимеров, таких как полиэтиленоксид и полипропиленоксид; и сополимера полиэтиленоксид-полипропиленоксид. В вышеуказанных соединениях двухвалентную группу R1 выбирают из H, С1-6 н-алкила, С3-12 разветвленного алкила, замещенного или незамещенного С3-6 циклоалкила, замещенного или незамещенного арила и замещенного или незамещенного аралкила.
Хотя предпочтительный вариант осуществления изобретения проиллюстрирован и описан, следует принять во внимание, что в нем могут быть сделаны различные изменения без отклонения от духа и объема изобретения. Связующий фрагмент (L) и терапевтический лекарственный фрагмент (D) могут быть ковалентно связаны через амидную группу. В одном варианте осуществления терапевтический лекарственный фрагмент включает аминогруппу, которая связана с карбоксильной группой связующего фрагмента. Связующий фрагмент может быть соединен с фрагментом токоферола через простую эфирную группу (соединение 17), сложноэфирную группу (соединение 18), аминогруппу (соединение 19) или амидную группу (соединение 20).
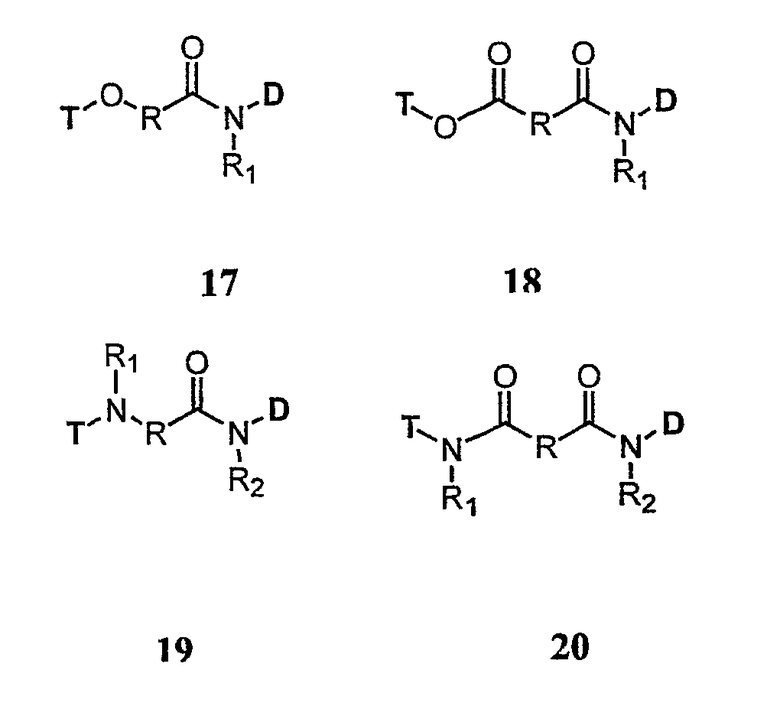
В вышеуказанных соединениях двухвалентную группу R выбирают из алкила; замещенного алкила; разветвленного алкила; циклоалкила; замещенного циклоалкила; гетероалкила; замещенного гетероалкила; арила; замещенного арила; аралкила; замещенного аралкила; аминокислоты; пептида; полипептида; белка; моно-, ди- или полисахарида; олигомера этиленгликоля, полиэтиленгликоля; полиалкиленоксидных полимеров, таких как полиэтиленоксид и полипропиленоксид; и сополимера полиэтиленоксид-полипропиленоксид. В вышеуказанных соединениях R1 и R2 независимо выбирают из H, С1-6 н-алкила, С3-12 разветвленного алкила, замещенного или незамещенного С3-6 циклоалкила, замещенного или незамещенного арила и замещенного или незамещенного аралкила.
Связующий фрагмент (L) и терапевтический лекарственный фрагмент (D) могут быть ковалентно соединены через простую эфирную группу (соединение 21) или аминогруппу (соединение 22). В одном варианте осуществления терапевтический лекарственный фрагмент включает гидроксильную группу и в другом варианте осуществления терапевтический лекарственный фрагмент включает аминогруппу.
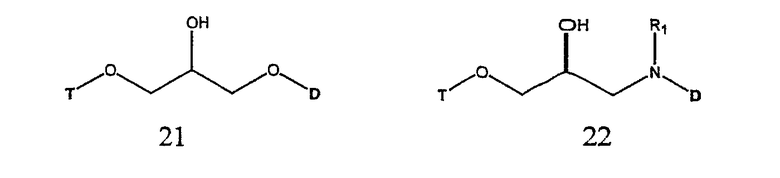
В вышеуказанных соединениях R1 выбирают из H, С1-6 н-алкила, С3-12 разветвленного алкила, замещенного или незамещенного С3-6 циклоалкила, замещенного или незамещенного арила или аралкила.
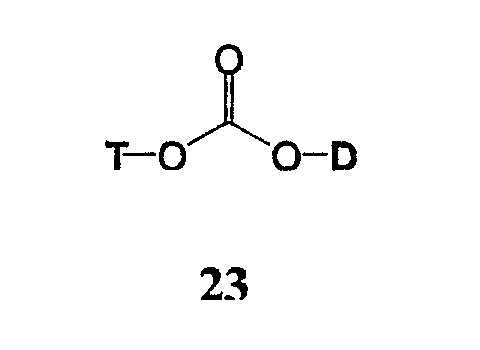
Фрагмент токоферола (Т) и терапевтический лекарственный фрагмент (D) могут быть ковалентно соединены через карбонилдиоксигруппу (-ОС(=О)О-) (соединение 23). В данном случае связующий фрагмент представляет собой карбонилдиоксигруппу и терапевтический лекарственный фрагмент включает гидроксильную группу.
Фрагмент токоферола (Т) и терапевтический лекарственный фрагмент (D) могут быть ковалентно соединены через ангидридную группу (-С(=О)ОС(=О)-). В одном варианте осуществления терапевтический лекарственный фрагмент включает карбоксильную группу, которая соединена с карбоксильной группой связующего фрагмента. Связующий фрагмент может быть соединен с фрагментом токоферола через простую эфирную группу (соединение 24), сложноэфирную группу (соединение 25), аминогруппу (соединение 26) или амидную группу (соединение 27).
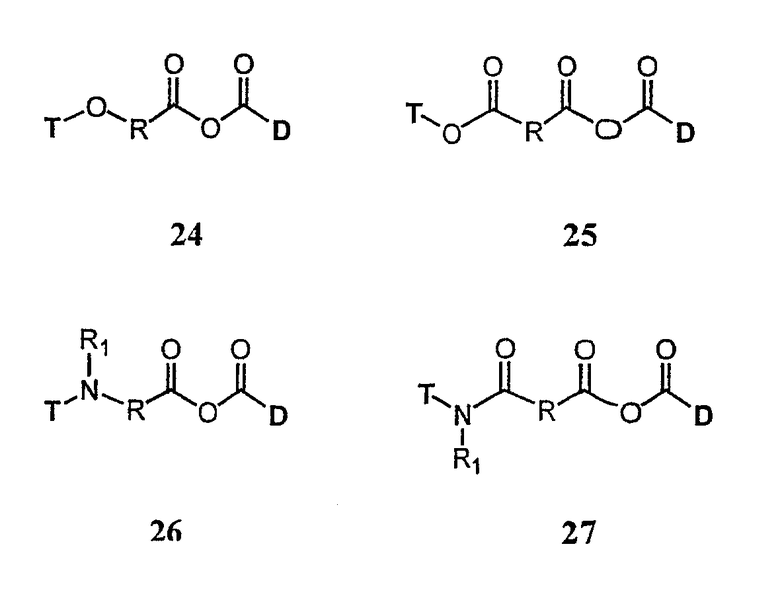
В вышеуказанных соединениях двухвалентную группу R выбирают из алкила; замещенного алкила; разветвленного алкила; циклоалкила; замещенного циклоалкила; гетероалкила; замещенного гетероалкила; арила; замещенного арила; аралкила; замещенного аралкила; аминокислоты; пептида; полипептида; белка; моно-, ди- или полисахарида; олигомера этиленгликоля, полиэтиленгликоля; полиалкиленоксидных полимеров, таких как полиэтиленоксид и полипропиленоксид; и сополимера полиэтиленоксид-полипропиленоксид. В вышеуказанных соединениях R1 выбирают из H, С1-6 н-алкила, С3-12 разветвленного алкила, замещенного или незамещенного С3-6 циклоалкила, замещенного или незамещенного арила и замещенного или незамещенного аралкила.
Фрагмент токоферола (Т) и терапевтический лекарственный фрагмент (D) могут быть ковалентно соединены через фосфатную, фосфорамидную или тиофосфатную группу (соединение 28).
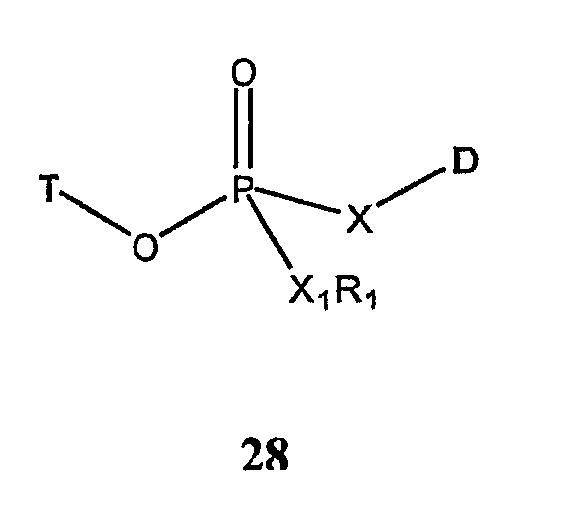
В вышеуказанных соединениях Х представляет собой О, NR2 или S; X1 представляет собой О, NR3 или S; R1 выбирают из Na+, K+, H, С1-6 н-алкила, С3-12 разветвленного алкила, замещенного или незамещенного С3-6 циклоалкила, замещенного или незамещенного арила или аралкила; и R2 и R3 независимо выбирают из С1-6 н-алкила, С3-12 разветвленного алкила, замещенного или незамещенного С3-6 циклоалкила, замещенного или незамещенного арила или аралкила.
Фрагмент токоферола (Т) и терапевтический лекарственный фрагмент (D) могут быть ковалентно соединены через сульфатную, тиосульфатную или сульфонамидную группу (соединение 29).

В вышеуказанных соединениях Х представляет собой О, NR1 или S; и R1 выбирают из H, С1-6 н-алкила, С3-12 разветвленного алкила, замещенного или незамещенного С3-6 циклоалкила, замещенного или незамещенного арила или аралкила.
Фрагмент токоферола (Т) и терапевтический лекарственный фрагмент (D) могут быть ковалентно соединены через уреиленовую группу (-NHC(=O)NH-) (соединение 30).
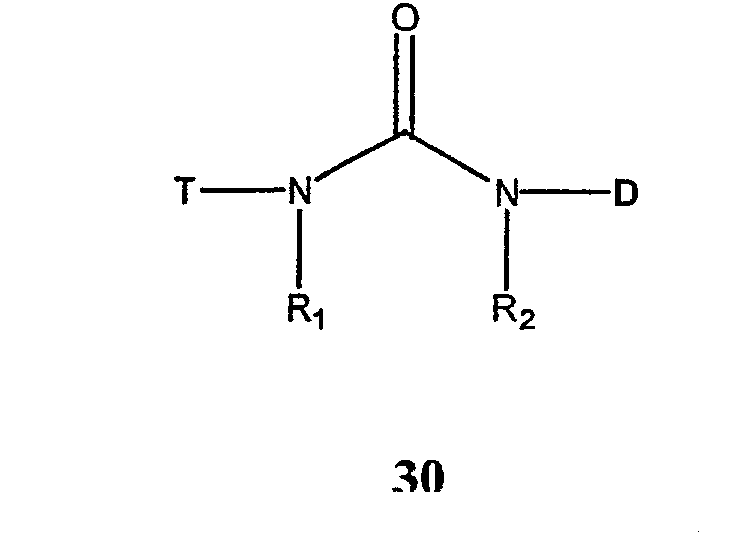
В вышеуказанном соединениях R1 и R2 независимо выбирают из H, С1-6 н-алкила, С3-12 разветвленного алкила, замещенного или незамещенного С3-6 циклоалкила, замещенного или незамещенного арила или аралкила.
Фрагмент токоферола (Т) и терапевтический лекарственный фрагмент (D) могут быть ковалентно соединены через карбаматную группу (-NR1C(=O)O- или -OC(=O)NR2-, соединения 31 и 32 соответственно).
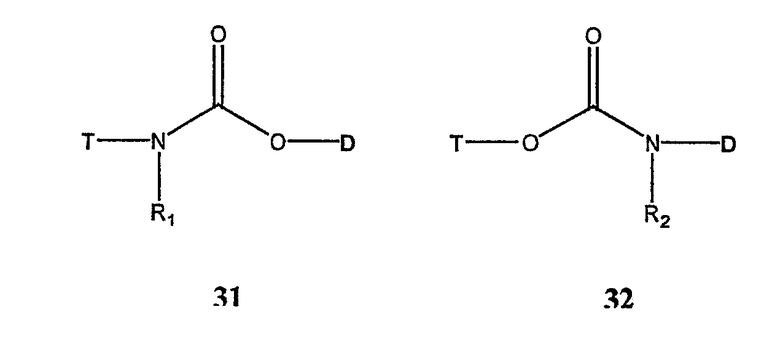
В вышеуказанных соединениях R1 и R2 независимо выбирают из H, С1-6 н-алкила, С3-12 разветвленного алкила, замещенного или незамещенного С3-6 циклоалкила, замещенного или незамещенного арила или аралкила.
Связующий фрагмент. Соединения изобретения включают один или более липофильных фрагментов. Липофильный фрагмент или фрагменты увеличивают растворимость соединения в липофильном растворителе или окружении. В одном варианте осуществления липофильный фрагмент представляет собой фрагмент токоферола.
Используемый здесь термин "фрагмент токоферола" означает химический фрагмент, который является производным от семейства природных или синтетических соединений, также известных по их родовым именам токол или витамин Е. В добавление к соединениям токоферола, соединения токотриенола включены в данное семейство. Указанные соединения включают хромановую голову, имеющую фенольный спирт (С-6), и фитильный хвост (С-2). Указанные соединения имеют следующую общую формулу:

Токоферолы составляют ряд родственных бензпиранолов (или метилтоколов), в которых С-2 фитильная (шестнадцать углеродов) боковая цепь С-2 является насыщенной. Типичные токоферолы включают α-токоферол, (d-форма, dl-форма, l-форма), β-токоферол (d-форма, dl-форма, l-форма), γ-токоферол (d-форма, dl-форма, l-форма) и δ-токоферол (d-форма, dl-форма, l-форма). Среди токоферолов преобладает α-токоферол. Токотриенолы подобны по структуре токоферолам за исключением того, что триенолы имеют три двойных связи в С-2 фитильной боковой цепи.
Соединения токоферола и токотриенола, пригодные для изготовления соединений изобретения, включают соединения, показанные ниже.
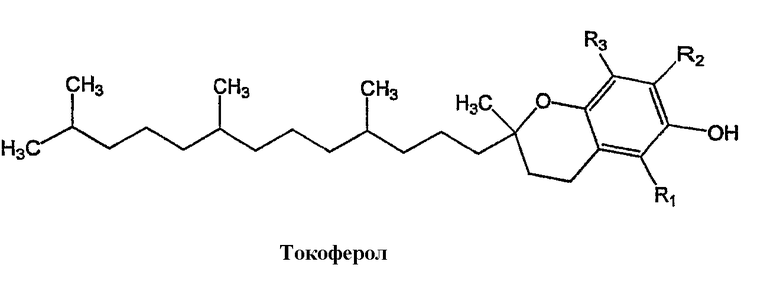
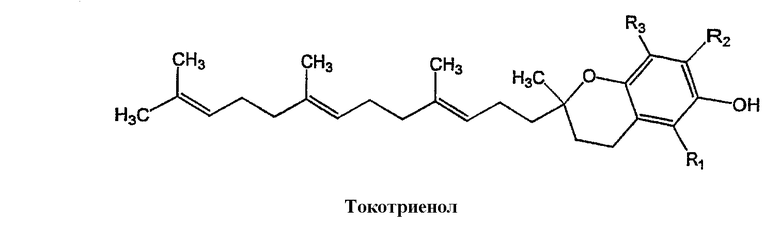
Используемый здесь термин "токоферол" относится к любому члену семейства токоферола, указанному выше.
Терапевтический лекарственный фрагмент. Соединения изобретения включают один или более терапевтических лекарственных фрагментов. Фактически любое терапевтическое лекарственное соединение, имеющее подходящую функциональную группу или которое можно модифицировать включением подходящей функциональной группы, может быть ковалентно соединено с липофильным соединением с образованием соединения изобретения. Типичные функциональные группы включают, например, гидроксильные группы (-ОН), аминогруппы (первичные аминогруппы -NH2 и вторичные аминогруппы -NHR), тиольные группы (-SH), карбоксильные группы (-СООН), альдегидные группы (-СНО), изоцианатные группы (-N=C=O), группы сульфоновой кислоты (-SO3H), группы серной кислоты (-OSO3H), группы фосфорной кислоты (-ОРО3Н), фосфонатные группы (-РО3OR1R2), и R1 и R2 независимо выбирают из H, С1-6 н-алкила, С3-12 разветвленного алкила, замещенного или незамещенного С3-6 циклоалкила, замещенного или незамещенного арила или аралкила, галогеналлильные группы, галогенбензильные группы, замещенные галогенбензильные группы и эпоксигруппы (-СН(О)СН2).
Терапевтические лекарственные соединения, пригодные для изготовления соединений изобретения, не должны быть, по существу, водонерастворимыми, хотя модифицирование токоферолом согласно настоящему изобретению особенно хорошо подходит для получения и доставки таких водонерастворимых соединений.
В одном варианте осуществления терапевтический лекарственный фрагмент получают из терапевтического соединения, которое, по существу, нерастворимо в воде. В другом варианте осуществления терапевтический лекарственный фрагмент получают из терапевтического соединения, которое, по существу, нерастворимо в органических растворителях. В другом варианте осуществления терапевтический лекарственный фрагмент получают из терапевтического соединения, которое, по существу, нерастворимо в воде и, по существу, нерастворимо в органических растворителях. В одном варианте осуществления терапевтическое лекарственное соединение имеет растворимость в воде при комнатной температуре меньше, чем примерно 1000 мкг/мл. В одном варианте осуществления терапевтическое лекарственное соединение имеет растворимость в воде при комнатной температуре меньше, чем примерно 500 мкг/мл. В одном варианте осуществления терапевтическое лекарственное соединение имеет растворимость в воде при комнатной температуре меньше, чем примерно 100 мкг/мл. В одном варианте осуществления терапевтическое лекарственное соединение имеет растворимость в воде при комнатной температуре меньше, чем примерно 25 мкг/мл.
Типичные терапевтические лекарственные соединения, пригодные для изготовления соединений изобретения, включают противораковые соединения (например, паклитаксел и его производные, включая доцетаксел, камптотецин и его производные, включая 7-этил-10-гидроксикамптотецин (SN38) и 10-гидроксикамптотецин, и доксорубицин и его производные), противогрибковые соединения (например, флуканазол), антибактериальные соединения (например, пенициллин G, пенициллин V), антигипертензивные соединения (например, гидралазин, кандесартан и карведиол), противовоспалительные соединения (например, изоксикам), противодиабетические соединения (например, метформин), противовирусные соединения (например, ламивудин), антидепрессантные соединения (например, флуоксетин), антигистаминные соединения (например, гидроксизин), антиаритмические соединения (например, гидрохлорид прокаинамида), антигиперлипопротеиновые соединения (например, пробукол) и соединения для репродуцивного здоровья (например, даназол) и лечения болезни Паркинсона (например, лазабемид) и иммунодепрессивных (например, азатиоприн и циклоспорин) и респираторных (например, бозентан) заболеваний и условий. Другие терапевтически полезные биологические материалы, которые могут быть модифицированы согласно изобретению, включают биологически активные белки, энзимы и пептиды.
В одном варианте осуществления терапевтический лекарственный фрагмент получают из противоракового соединения. Типичные противораковые терапевтические соединения включают таксаны. Таксаны включают любой антимитотический таксан, производное таксана или аналог. Используемый здесь термин "таксан" относится к таксанам, таксинам и таксоидам так же, как и их производным или аналогам.
Паклитаксел и его производные и аналоги являются членами семейства таксанов. Производные паклитаксела включают, например, бензоатные производные паклитаксела, такие как 2-дебензоил-2-ароил и С-2-ацетокси-С-4-бензоат паклитаксела, 7-деокситаксол, С-4 азиридинпаклитаксел так же, как и различные соединения паклитаксела с природными и синтетическими полимерами, особенно с жирными кислотами, фосфолипидами и глицеридами, и 1,2-диацилоксипропан-3-амином. Другие производные паклитаксела включают доцетаксел; спикатин; таксан-2,13-дион, 5β,9β,10β-тригидрокси-, циклический 9,10-ацеталь с ацетоном, ацетат; таксан-2,13-дион, 5β,9β,10β-тригидрокси-, циклический 9,10-ацеталь с ацетоном; таксан-2β,5β,9β,10β-тетрол, циклический 9,10-ацеталь с ацетоном; таксан; цефаломаннин-7-ксилосид; 7-эпи-10-деацетилцефаломаннин; 10-деацетилцефаломаннин; цефаломаннин; таксол В; 13-(2',3'-дигидрокси-3'-фенилпропионил)баккатин III; юннанксол; 7-(4-азидобензоил)баккатин III; N-дебензоилтаксол А; О-ацетилбаккатин IV; 7-(триэтилсилил)баккатин III; 7,10-ди-О-[(2,2,2-трихлороэтокси)карбонил]баккатин III; баккатин III 13-О-ацетат; баккатин диацетат; баккатин; баккатин VII; баккатин VI; баккатин IV; 7-эпи-баккатин III; баккатин V; баккатин I; баккатин III; баккатин A; 10-деактил-7-эпитаксол; эпитаксол; 10-деацетилтаксол С; 7-ксилосил-10-деацетилтаксол; 10-деацетилтаксол-7-ксилосид; 7-эпи-10-деацетилтаксол; 10-деацетилтаксол; или 10-деацетилтаксол В.
Другие противораковые соединения, пригодные для изготовления соединений изобретения, включают камптотецин и его производные, включая 7-этил-10-гидроксикамптотецин (SN38) и 10-гидроксикамптотецин, и доксорубицин и его производные.
В некоторых вариантах осуществления терапевтический лекарственный фрагмент получают из паклитаксела, доцетаксела, камптотецина или их производных.
Для соединений изобретения, имеющих формулу (2) с m=1, формулу (3) с n=1 и формулу 8, определенные соединения исключаются и не входят в объем изобретения. Когда связующий фрагмент представляет собой 2-гидроксипропилен (-СН2СН(ОН)СН2-), терапевтический лекарственный фрагмент не является α-аминокислотой (например, глицином, аланином, пролином, цистеином, аминомасляной кислотой, аспарагиновой кислотой, глутаминовой кислотой), ω-аминокислотой (например, β-аланином, γ-аминомасляной кислотой, ε-аминокапроновой кислотой, 2-аминоэтансульфоновой кислотой (таурин)) или пептидом, содержащим цистеиновый остаток, связанный через его N-конец или тиольную группу (например, -глутатион). Когда связующий фрагмент представляет собой сукцинат, терапевтический лекарственный фрагмент не является S-связанным аминосоединением или аминокислотой, соединенным с одним из алифатических углеродов сукцината. Когда связующий фрагмент представляет собой сукцинат, терапевтический лекарственный фрагмент не является феруловой кислотой или ее сложным эфиром.
В другом аспекте предлагаются способы изготовления соединений изобретения. Есть много способов ковалентно связать липофильное соединение (например, соединение токоферола) с терапевтическим лекарственным соединением с образованием соединения изобретения. В одном варианте осуществления типичный токоферол, d-α- токоферол, включает гидроксильную группу, которая может быть непосредственно связана с карбонильной группой терапевтического лекарственного средства с образованием токоферол-модифицированного терапевтического лекарственного соединения. Приготовление типичного токоферол-модифицированного терапевтического соединения изобретения из терапевтического лекарственного соединения, содержащего карбоновую кислоту, показано на ФИГУРЕ 1.
В другом варианте осуществления токоферол может быть функционализирован по гидроксильной группе реагентом для введения активной группы, таким как фосфорный хлорангидрид (-P(O)OR1Cl), фосфоновый хлорангидрид (-P(O)R1Cl), сульфохлорид (-SO2Cl) или карбонилхлорид (-COCl). Полученный хлорангидрид кислоты может затем реагировать с соответствующим функционализированным терапевтическим лекарственным соединением с получением токоферол-модифицированного терапевтического лекарственного соединения.
На ФИГУРЕ 2 Х обозначает O, S или NH; и R1 независимо выбирают из H, С1-6 н-алкила, С3-12 разветвленного алкила, замещенного или незамещенного С3-6 циклоалкила, замещенного или незамещенного арила и замещенного или незамещенного аралкила.
В другом варианте осуществления токоферол может быть функционализирован по гидроксильной группе дикарбоновой кислотой, сложным эфиром или ангидридом. Подходящие реагенты включают ангидрид янтарной кислоты, 1,2-циклогександикарбоновый ангидрид, 2,3-диметилянтарный ангидрид, 3,3-тетраметиленглутаровый ангидрид, глутаровый ангидрид, ангидрид малеиновой кислоты, ангидрид фталевой кислоты, терефталевую кислоту или изофталевую кислоту для введения карбоксильной группы (-СООН). Полученная карбоксильная группа затем может непосредственно реагировать с соответствующим функционализированным терапевтическим лекарственным средством, или карбоксильная группа может превращаться в более реакционно-способную карбонилхлоридную группу (-COCl), и затем карбонилхлоридная группа может соединяться с функциональной группой терапевтического лекарственного средства с образованием токоферол-модифицированного терапевтического лекарственного соединения, как показано на ФИГУРЕ 3. На ФИГУРЕ 3 Х обозначает O, S, NH или С(=О)О.
В другом варианте осуществления связующее может быть связано с гидроксильной группой токоферола, и затем терапевтическое лекарственное средство может быть присоединено к доступной функциональной группе связующего. Функциональная группа может быть, например, но не ограничена, карбоксильной группой (-СООН), полиэтиленоксидной группой (-(СН2СН2О)n-H), альдегидной группой (-СНО), изоцианатной группой (-N=C=O), фосфорнокислой группой (-ОРО3Н2) или фосфорнохлорангидридной группой (-OPO2R1Cl, где R1 представляет собой замещенный или незамещенный алкил или циклоалкил, замещенный или незамещенный арил или аралкил), фосфоновохлорангидридной группой (-PO2R1Cl, где R1 представляет собой замещенный или незамещенный алкил или циклоалкил, замещенный или незамещенный арил или аралкил), сернокислотной группой (-OSO3H2), хлорсульфоновой группой (-SO3Cl) или эпоксигруппой (-СН(О)СН2).
Синтезы типичных токоферол-модифицированных терапевтических лекарственных соединений изобретения показаны на ФИГУРАХ от 4 до 11 и описаны в примерах от 1 до 13.
ФИГУРА 4 иллюстрирует приготовление соединения токоферолсукцината камптотецина. Токоферолянтарная кислота (витамин Е янтарная кислота) имеет свободную карбоксильную группу, которая может соединяться с гидроксильной группой, аминогруппой, тиольной группой или карбонилхлоридной группой с получением токоферол-модифицированного терапевтического лекарственного препарата, имеющего сукцинатную группу в качестве связующего. На ФИГУРЕ 4 карбоксильная группа токоферолянтарной кислоты соединена с гидроксильной группой камптотецина. Приготовление токоферолсукцината камптотецина описано в примере 1.
ФИГУРА 5 иллюстрирует приготовление токоферолсукцината 10-гидроксикамптотецина и токоферолсукцината 7-этил-10-гидроксикамптотецина (SN38). Токоферолянтарная кислота превращается в соответствующий хлорид и затем реагирует с 10-гидроксикамптотецином или 7-этил-10-гидроксикамптотецином (SN38). Приготовления токоферолсукцината 10-гидроксикамптотецина и токоферолсукцината 7-этил-10-гидроксикамптотецина описаны в примерах 2 и 3 соответственно.
ФИГУРА 6 иллюстрирует приготовление 10,20-ди(токоферолсукцината) SN38, который содержит один терапевтический лекарственный (SN38) фрагмент, два фрагмента токоферола и два связующих фрагмента (сукцинильные группы). Приготовление 10,20-ди(токоферолсукцината) SN38 описано в примере 4.
Подходящие связующие фрагменты могут включать олигомер или полимер, такой как пептид, полипептид, белок, моно-, ди- или полисахарид, олигомер этиленгликоля, полиэтиленгликоль, полиалкиленоксид, такой как полиэтиленоксид и полипропиленоксид; и сополимер полиэтиленоксид-полипропиленоксид.
ФИГУРА 7 иллюстрирует приготовление токоферол-модифицированного камптотецина, содержащего связующий фрагмент, который включает группу полиэтиленоксида. Приготовление токоферолсукцината камптотецина, имеющего связующий фрагмент, который включает группу полиэтиленоксида, описано в примере 5.
ФИГУРА 8 иллюстрирует приготовление токоферолсукцината паклитаксела. В ходе данного приготовления токоферолянтарная кислота превращается в соответствующий хлорангидрид и затем реагирует с паклитакселом. Приготовление токоферолсукцината паклитаксела описано в примере 6.
ФИГУРА 9 иллюстрирует приготовление токоферолсукцината доцетаксела. Приготовление токоферолсукцината доцетаксела описано в примере 7.
ФИГУРА 10 иллюстрирует приготовление токоферолтерефталата камптотецина. В ходе данного приготовления токоферол сначала соединяется с терефталатом с образованием токоферолтерефталата (пример 9) и затем соединяется с камптотецином с образованием токоферолтерефталата камптотецина. Приготовление токоферолтерефталата камптотецина описано в примере 10.
ФИГУРА 11 иллюстрирует приготовление токоферолциклогексан-1,2-дикарбоксилата SN38. Приготовление токоферолциклогексан-1,2-дикарбоксилата SN38 описано в примере 11.
Приготовление токоферолсукцината доксорубицина и токоферолсукцината гидроксизина описано в примерах 12 и 13 соответственно.
В другом аспекте настоящее изобретение предлагает композиции, которые включают соединения изобретения. Данные композиции включают одно или более соединений изобретения, возможно один или более дополнительных терапевтических агентов и липофильную среду. В одном варианте осуществления токоферол-модифицированное терапевтическое лекарственное соединение растворяют в липофильной среде. Благодаря липофильному фрагменту данное соединение имеет улучшенную липофильность по сравнению с немодифицированным терапевтическим лекарственным соединением. Липофильная среда (или носитель) композиции может быть любой средой из множества липофильных сред, включая, например, масла. В одном варианте осуществления липофильная среда включает токоферол (например, α-токоферол). Типичные масла, пригодные в качестве липофильной среды, включают следующее:
Жирные кислоты и их сложные эфиры, включая карбоновые кислоты с различной длиной цепи, главным образом прямой цепью, но которая может быть разветвленной, примеры которых включают каприновую, каприловую, капроновую, лауриновую, миристиновую, стеариновую, олеиновую, линолевую, бегеновую, так же, как и насыщенные и ненасыщенные жирные кислоты и сложные эфиры.
Жирные кислоты, этерифицированые глицерином с образованием моно-, ди- или триглицеридов, которые могут быть синтетическими или производными из природных источников, включая, но не ограниченно, например, глицериды, такие как соевое масло, хлопковое масло, рапсовое масло, рыбий жир, касторовое масло, Capmul MCM, Captex 300, Miglyol 812, моноолеат глицерила, триацетин, ацетилированный моноглицерид, тристеарин, бегенат глицерила и сложные эфиры диацетилвинной кислоты и моноглицеридов.
Глицериды, связанные с другими фрагментами, такие как полиэтиленгликоль (например, Labrasol, Labrafac, Cemophor EL).
Фосфолипиды, природные или синтетические, такие как димиристилфосфатидилхолин, яичный лецитин и pegylated фосфолипиды.
Другие жирные сложные эфиры, включая жирные спирты (миристилмиристат, изопропилпальмиат) или сахара (сорбитмоноолеат, SPAN 80, Tween 80, лаурат сахарозы).
Жирные спирты, такие как стеариловый спирт, лауриловый спирт, бензиловый спирт или их сложные или простые эфиры, такие как бензилбензоат.
Жирорастворимые витамины и производные, например, витамин Е (включая все токоферолы и токотриенолы и производные токоферола и токотриенола, такие как сукцинат витамина Е, ацетат витамина Е и витамин Е сукцинатполиэтиленгликоль (ТПГС)).
Органические со-растворители также могут использоваться в композициях, возможно в комбинации с водой, включая, например, этанол, полиэтиленгликоль, пропиленгликоль, глицерин, N-метилпирролидон и диметилсульфоксид.
Растворимости двух типичных токоферол-модифицированных соединений камптотецина по изобретению в нескольких средах сравниваются с камптотецином в примере 14.
В дополнительном аспекте изобретение предлагает рецептуры эмульсии, микроэмульсии и мицелл, которые включают соединение изобретения. Также предлагаются способы приготовления рецептур эмульсии, микроэмульсии и мицелл.
Используемый здесь термин "эмульсия" относится к коллоидной дисперсии двух несмешивающихся жидкостей, таких как масло и вода, в форме капель, чей диаметр, в основном, находится между 0,1 и 3,0 мкм, и которые обычно оптически непрозрачны, если только показатели преломления дисперсной и непрерывной фаз не совпадают. Такие системы обладают ограниченной стабильностью, обычно определяемой применением или значимой эталонной системой, которая может быть усилена добавлением амфифильных молекул или усилителей вязкости.
Термин "микроэмульсия" относится к термодинамически стабильной, изотропно прозрачной дисперсии двух несмешивающихся жидкостей, таких как масло или вода, стабилизированных поверхностной пленкой молекул поверхностно-активных веществ. Микроэмульсия имеет основной диаметр капель меньше, чем 200 нм, обычно от 10 до 50 нм. В отсутствие воды смеси масла(сел) и неионогенного поверхностно-активного вещества(ств) образуют прозрачные и изотропные растворы, которые известны как самоэмульгирующиеся системы доставки лекарства (СЭСДЛ) и могут быть использованы для улучшения растворения липофильного лекарства и орального поглощения.
Рецептуры эмульсии и микроэмульсии включают масляную фазу и водную фазу. Эмульсия или микроэмульсия может быть эмульсией типа масло-в-воде или эмульсией типа вода-в-масле. Масляная фаза включает одно или более соединений изобретения и липофильную среду, как описано выше. В одном варианте осуществления данное соединение присутствует в рецептуре в количестве от примерно 0,005 до примерно 3,0 массовых процентов от суммарной массы рецептуры. В одном варианте осуществления данное соединение присутствует в рецептуре в количестве от примерно 0,01 до примерно 2,5 массовых процентов от суммарной массы рецептуры. В одном варианте осуществления данное соединение присутствует в рецептуре в количестве от примерно 0,1 до примерно 1,5 массовых процентов от суммарной массы рецептуры. В одном варианте осуществления липофильная среда присутствует в рецептуре в количестве от примерно 2 до примерно 20 массовых процентов от суммарной массы рецептуры. В одном варианте осуществления липофильная среда присутствует в рецептуре в количестве от примерно 4 до примерно 12 массовых процентов от суммарной массы рецептуры. В одном варианте осуществления липофильная среда присутствует в рецептуре в количестве от примерно 6 до примерно 10 массовых процентов от суммарной массы рецептуры.
В одном варианте осуществления эмульсии или микроэмульсии данное соединение представляет собой токоферол-модифицированное терапевтическое лекарственное соединение, липофильная среда включает токоферол и водная среда представляет собой воду.
В добавление к соединениям изобретения рецептуры эмульсии или микроэмульсии могут включать другие компоненты, обычно используемые в эмульсиях и микроэмульсиях и особенно используемые в фармацевтических эмульсиях и микроэмульсиях. Указанные компоненты включают, среди прочего, поверхностно-активные вещества и со-растворители. Типичные поверхностно-активные вещества включают неионогенные поверхностно-активные вещества, такие как поверхностно-активные производные токоферола и поверхностно-активные полимеры.
Подходящие поверхностно-активные производные токоферола включают производные токоферолполиэтиленгликоля, такие как витамин Е сукцинат полиэтиленгликоля (например, d-α-токоферолполиэтиленгликоль 1000 сукцинат, ТПГС), который представляет собой производное витамина Е, в котором полиэтиленгликоль присоединен с помощью эфира янтарной кислоты к гидроксилу кольца витамина Е. Используемый здесь термин "витамин Е сукцинат полиэтиленгликоля" включает витамин Е сукцинат полиэтиленгликоля и производные витамина Е сукцинат полиэтиленгликоля, имеющие различные связи сложных и простых эфиров. ТПГС представляет собой неионогенное поверхностно-активное вещество (HLB=16-18). Сообщается, что ТПГС ингибирует Р-гликопротеин, белок, который способствует развитию устойчивости к многим лекарствам. Варианты осуществления рецептур изобретения, которые включают ТПГС, поэтому включают ингибитор Р-гликопротеина. Поверхностно-активные производные токоферола (например, ТПГС) могут присутствовать в рецептурах изобретения в количестве от примерно 1 до примерно 10 массовых процентов, от примерно 2 до примерно 6 массовых процентов или примерно 5 массовых процентов от суммарной массы рецептуры.
Подходящие неионогенные поверхностно-активные вещества включают блок-сополимеры этиленоксида и пропиленоксида, известные как POLOXAMERS и PLUROINICS. Указанные синтетические блок-сополимеры имеют общую структуру: H(OCH2CH2)a(OC3H6CH2)b(OCH2CH2)aOH. Следующие варианты на основе величин а и b коммерчески доступны от BASF Performance Chemicals (Parsippany, New Jersey) под торговой аркой PLURONIC и состоят из группы поверхностно-активных веществ, обозначенных CTFA названием POLOXAMER 108, 188, 217, 237, 238, 288, 338, 407, 101, 105, 122, 123, 124, 181, 182, 183, 184, 212, 231, 282, 331, 401, 402, 185, 215, 234, 235, 284, 333, 334, 335 и 403. Для наиболее обычно используемых POLOXAMERS 124, 188, 237, 338 и 407 величины а и b составляют 12/20, 79/28, 64/37, 141/44 и 101/56 соответственно. В одном варианте осуществления неионогенные поверхностно-активные вещества присутствуют в рецептуре в количестве от примерно 0,5 до примерно 5 массовых процентов от суммарной массы рецептуры.
Со-растворители, пригодные для рецептур, включают, среди прочего, этанол, полиэтиленгликоль, пропиленгликоль, глицерин, N-метилпирролидон, диметиламид и диметилсульфоксид. Полиэтиленгликоль (ПЭГ) представляет собой гидрофильную полимеризованную форму этиленгликоля, состоящую из повторяющихся звеньев, имеющих химическую структуру: (-СН2СН2О-). Общая формула полиэтиленгликоля Н(ОСН2СН2)nОН. Молекулярная масса варьируется от 200 до 10000. Такие различные формы описывают по их молекулярной массе, например, ПЭГ-200, ПЭГ-300, ПЭГ-400 и подобные.
Эмульсии паклитексела и их компоненты описаны в патенте США №6458173 и патенте США №6660286, каждый из которых определенно включен здесь в качестве ссылки.
Типичные эмульсии, включающие токоферол-модифицированные терапевтические лекарственные соединения (например, токоферолсукцинат доцетаксела, токоферолсукцинат паклитаксела, токоферолсукцинат камптотецина, токоферолсукцинат 7-этил-10-гикроксикамптотецина и токоферолсукцинат 10-гидроксикамптотецина), описаны в примере 15. In vitro цитотоксичности типичных токоферол-модифицированных терапевтических лекарственных соединений (например, токоферолсукцинат 7-этил-10-гикроксикамптотецина и токоферолсукцинат камптотецина) описаны в примере 16.
В дополнительном аспекте изобретение предлагает рецептуры мицелл, которые включают соединение изобретения и водную фазу. Мицеллы представляют собой организованные агрегаты одного или более поверхностно-активных веществ в растворе. В одном варианте осуществления данное соединение присутствует в рецептуре в количестве от примерно 0,005 до примерно 3,0 массовых процентов от суммарной массы рецептуры. В одном варианте осуществления данное соединение присутствует в рецептуре в количестве от примерно 0,01 до примерно 2,5 массовых процентов от суммарной массы рецептуры. В одном варианте осуществления данное соединение присутствует в рецептуре в количестве от примерно 0,1 до примерно 1,0 массовых процентов от суммарной массы рецептуры. Подходящие поверхностно-активные вещества включают вышеуказанные поверхностно-активные вещества и в количествах, указанных выше. В одном варианте осуществления рецептуры мицелл данное соединение представляет собой токоферол-модифицированное терапевтическое лекарственное соединение, и поверхностно-активное вещество представляет собой токоферолполиэтиленгликольсукцинат (ТПГС). Типичные рецептуры мицелл, включающие токоферол-модифицированные терапевтические лекарственные соединения, описаны в примере 15.
Рецептуры мицелл могут также включать дополнительные компоненты, такие как со-растворители, включающие вышеуказанные со-растворители. В одном варианте осуществления рецептура мицелл включает полиэтиленгликоль и низший алкиловый спирт (например, этанол). В одном варианте осуществления со-растворители присутствуют в количестве от примерно 2 до примерно 20 массовых процентов от суммарной массы рецептуры. Рецептуры мицелл, эмульсий и микроэмульсий включают водную фазу. В одном варианте осуществления водная фаза включает деионизированную воду. В другом варианте осуществления водная фаза включает соляной раствор. В другом варианте осуществления водная фаза представляет собой солевой раствор, буферизованный органической кислотой (например, сукцинат, цитрат).
Изобретение также предлагает применение соединений изобретения при производстве медикаментов. Например, для соединения изобретения, которое включает терапевтический лекарственный фрагмент, полученный от терапевтического лекарственного соединения, эффективного при лечении пролиферативного заболевания клеток, изобретение предлагает применение таких соединений при производстве медикамента для лечения пролиферативного заболевания клеток.
В других аспектах также предлагаются способы введения соединения изобретения к нуждающемуся в них субъекту и способы лечения состояния, которое подлежит лечению введением терапевтически эффективного количества соединения изобретения. Указанные способы включают введение соединений, композиций, рецептур эмульсий, рецептур микроэмульсий и рецептур мицелл, описанных здесь.
В одном варианте осуществления изобретение предлагает способ лечения состояния, которое подлежит лечению исходным, немодифицированным терапевтическим лекарственным соединением (например, пролиферативного заболевания клеток, такого как рак). В данном способе терапевтически эффективное количество соединения изобретения применяют к нуждающемуся в нем объекту.
В одном варианте осуществления изобретение предлагает способ лечения пролиферативного заболевания клеток введением соединения изобретения, имеющего терапевтический лекарственный фрагмент, полученный от терапевтического лекарственного средства, эффективного при лечении пролиферативного заболевания клеток. Типичные пролиферативные заболевания клеток, подлежащие лечению соединениями изобретения, включают виды гематологического рака, такие как лейкемия, лимфома и миелома; и виды негематологического рака, такие как твердоопухолевые карциномы (например, груди, яичников, двенадцатиперстной кишки, толстой кишки, прямой кишки, немалых клеток легких и мочевого пузыря), саркомы и глиомы.
Терапевтически эффективные количества указанных соединений обычно варьируют вплоть до максимально допустимой дозы, но данные концентрации не являются критичными и могут меняться в широких пределах. Точные количества, назначаемые лечащим врачом, меняются, конечно, в зависимости от соединения, способа введения, физического состояния пациента и других факторов. Ежедневную дозу можно применять как одноразовую дозу или ее можно разделять на множество доз для введения.
Реально применяемое количество данного соединения является терапевтически эффективным количеством, термином, используемым здесь для обозначения количества, необходимого для получения существенного благоприятного эффекта. Эффективные дозы можно экстраполировать по кривым доза-эффект, полученным из in vitro или животных модельных тестовых систем. Животные модели также обычно используют для определения желаемого диапазона доз и способа введения. Такую информацию можно затем использовать для определения приемлемых доз и способов введения для людей и других млекопитающих. Определение эффективной дозы понятно для специалистов в данной области техники. Таким образом, реально вводимое количество зависит от индивида, подвергаемого лечению, и предпочтительно, представляет собой оптимальное количество, такое, чтобы желаемый эффект достигался без заметных побочных эффектов.
Терапевтическая эффективность и возможная токсичность соединения изобретения могут быть определены по стандартным фармацевтическим процедурам на клеточных культурах или экспериментальных животных (например, ED50, доза, терапевтически эффективная для 50% популяции; и LD50, смертельная доза для 50% популяции). Соотношение доз между терапевтическим и токсичным эффектами представляет собой терапевтический индекс и может быть выражено как отношение LD50 к ED50. Модифицированные терапевтические лекарственные соединения, которые имеют большие терапевтические индексы, особенно пригодны в практике способов изобретения. Данные, полученные по анализам клеточных культур и исследованиям животных, могут быть использованы при определении диапазона доз для применения к людям и другим млекопитающим. Дозировка таких соединений, предпочтительно, лежит внутри диапазона концентраций, которые включают ED50 с малой токсичностью или без нее. Дозировка обычно варьируется внутри указанного диапазона в зависимости от дозировки применяемой формы, чувствительности пациента и способа введения. Таким образом, оптимальные количества будут изменяться со способом введения и обычно находятся в соответствии с количествами обычных медикаментов, вводимых в той же или подобной форме.
Соединения изобретения могут быть введены в одиночку или в комбинации с одним или более дополнительным терапевтическим агентом. Например, при лечении рака указанные соединения могут быть введены в комбинации с терапевтическими агентами, включая, но не ограничиваясь, андрогенные ингибиторы, такие как флутамид и лапролид; антиэстрогены, такие как томоксифен; антиметаболиты и цитотоксические агенты, такие как даунорубицин, флуороурацил, флоксуридин, альфа интерферон, метотрексат, пликамицин, мекаптопурин, тиогуанин, адриамицин, кармустин, ломустин, цитарабин, циклофосфамид, доксорубицин, эстрамустин, алтретамин, гидроксимочевина, ифосфамид, прокарбазин, мутамицин, бусульфан, митоксантрон, карбоплатин, цисплатин, стрептозорин, блеомицин, дактиномицин и идамицин; гормоны, такие как медроксипрогестерон, эстрамустин, этинилэстрадиол, эстрадиол, леупролид, мегестрол, октреотид, диэтилстилбестрол, хлортрианизен, этопосид, подофиллотоксин и госерелин; производные азотной горчицы, такие как мелфалан, хлорамбуцил, метлоретамин и тиотепа; стероиды, такие как бетаметазон; и другие противоопухолевые агенты, такие как живые Mycobacterium bovis, дикарбазин, аспарагиназа, лейковорин, митотан, винкристин, винбластин и таксотер. Соответствующие количества в каждом случае будут меняться с конкретным агентом и либо хорошо известны специалистам в данной области техники, либо легко определяются с помощью обычных экспериментов.
Введение соединений изобретения выполняют любым эффективным способом, например, парентерально, местным образом или орально. Способы введения включают ингаляционное, буккальное, внутримозговое, внутривенное, внутриносовое, внутрипрямокишечное, внутриглазное, внутрибрюшное, внутриартериальное, внутрисуставное, интрацервикальнное, внутричерепное, интрадуктальное, интрадуральное, интралезиональное, внутримышечное, внутрипоясничное, внутристеночное, внутриглазное, интраоперационное, внутристенное, внутрибрюшное, внутриплевральное, внутрилегочное, внутрипозвоночное, внутригрудное, внутритрахеальное, внутрибарабанное, внутриматочное, внутрисосудистое и внутрижелудочковое введение и другие обычные способы. Соединения изобретения, имеющие противоопухолевую активность, можно вводить непосредственно в опухоль, в окрестность опухоли или в кровеносный сосуд, который подает кровь в опухоль.
Рецептуры эмульсий, микроэмульсий и мицелл изобретения можно распылять, используя аэрозольные пропелленты, которые известны в области легочной доставки соединений.
Из соединений изобретения можно составлять композиции, которые дополнительно содержат подходящие фармацевтически приемлемые носители, включая наполнители и другие соединения, которые облегчают введение соединения к субъекту. Дополнительные детали технологий приготовления и введения можно найти в последней редакции "Remington's Pharmaceutical Sciences" (Maack Publishing Co., Easton, PA).
Композиции для орального введения можно готовить, используя фармацевтически приемлемые носители, хорошо известные в технике, в дозировке, подходящей для орального применения. Такие носители позволяют готовить композиции, содержащие соединения изобретения, в виде таблеток, пилюль, драже, капсул, жидкостей, гелей, сиропов, суспензий, подходящих для приема объектом. Композиции для орального введения можно готовить, например, в комбинации с твердыми наполнителями, возможно перемешивая полученную смесь и изготавливая смесь гранул после добавления подходящих дополнительных соединений, если необходимо, с получением таблеток или ядер драже. Подходящие наполнители включают углеводные или белковые наполнители. Они включают, но не ограничены, сахара, включая лактозу, сахарозу, маннит или сорбит, крахмал из кукурузы, пшеницы, риса, картофеля или других растений; целлюлозу, такую как метилцеллюлоза, гидроксипропилметилцеллюлоза или натрийкарбоксиметилцеллюлоза; и смолы, включая гуммиарабик и трагакант; так же, как и белки, такие как желатин и коллаген. При желании, можно добавлять дезинтегрирующие или растворяющие агенты, такие как сшитый поливинилпирролидон, агар, альгиновая кислота или ее соли, такие как альгинат натрия.
Ядра драже обеспечивают подходящими покрытиями, такими как концентрированные растворы сахара, которые могут содержать гуммиарабик, тальк, поливинилпирролидон, карбопол гель, полиэтиленгликоль и/или диоксид титана, лаковые растворы и подходящие органические растворители или смеси растворителей. Красители или пигменты можно добавлять в таблетки или покрытия драже для идентификации продукта или обозначения количества активного компонента (т.е. дозировки).
Соединения для орального введения можно готовить, например, в виде плотных капсул, сделанных из желатина, или в виде мягких герметичных капсул, сделанных из желатина и покрытия, такого как глицерин или сорбит. Плотные капсулы могут содержать соединения, смешанные с наполнителем или связующим, таким как лактоза или крахмалы, смазочными материалами, такими как тальк или стеарат магния, и, возможно стабилизаторами. В мягких капсулах ковалентные соединения могут быть растворены или суспендированы в подходящих жидкостях, таких как жирные масла, жидкий парафин или жидкий полиэтиленгликоль, с или без стабилизаторов.
Для местного или носового введения в рецептуре обычно используют проникающие агенты, соответствующие конкретному барьеру, который надо преодолевать. Их примеры представляют собой 2-пирролидон, N-метил-2-пирролидон, диметилацетамид, диметилформамид, пропиленгликоль, метиловый или изопропиловый спирт, диметилсульфоксид и озон. Дополнительные агенты могут дополнительно включаться, чтобы сделать рецептуру косметически приемлемой. Их примеры представляют собой жиры, воски, масла, краски, ароматизаторы, консерванты, стабилизаторы и поверхностно-активные вещества. Кератолитические агенты, такие как агенты, известные в данной области техники, также могут быть включены. Примеры представляют собой салициловую кислоту и серу. Для местного введения композиция может быть в форме трансдермальной мази или повязки для системной доставки соединения и может быть приготовлена обычным образом (смотри, например, Barry, Dermatological Formulations (Drugs and the Pharmaceutical Sciences-Dekker); Harry's Cosmeticology (Leonard Hill Books).
Для ректального введения композиции можно применять в форме суппозиториев или удерживающих клизм. Такие композиции можно готовить смешением соединений с подходящим нераздражающим наполнителем, который является твердым при обычных температурах, но жидким при ректальной температуре, и поэтому плавится в прямой кишке с освобождением лекарства. Подходящие наполнители включают, но не ограничены, масло какао и полиэтиленгликоли.
Количества каждого из указанных разных типов добавок легко видны специалистам в данной области техники, причем оптимальные количества такие же, как в других известных рецептурах, разработанных для того же типа введения.
Композиции, содержащие соединения изобретения, можно изготовить способами, подобными известным в данной области техники (например, с помощью способов обычного смешения, растворения, гранулирования, изготовления драже, растирания в порошок, эмульгирования, инкапсулирования, включения или лиофилизации). Композиции можно также модифицировать, чтобы обеспечить соответствующие характеристики освобождения, замедленного высвобождения или целевого высвобождения, обычными способами (например, покрытием). Как указано выше, в одном варианте осуществления соединения готовят в виде эмульсии.
Композиции, содержащие соединения, могут быть приготовлены в виде соли и могут быть образованы со многими кислотами, включая, но не ограничиваясь, соляную, серную, уксусную, молочную, винную, яблочную и янтарную. Соли имеют тенденцию к большей растворимости в водных и других протонных растворителях, чем соответствующие формы свободных оснований.
После того, как композиции, разработанные для содержания соединения и приемлемого носителя, приготовлены, они могут быть помещены в соответствующий контейнер и помечены для использования. Таким образом, в другом аспекте изобретение предоставляет наборы.
Токоферол-модифицированные терапевтические лекарственные соединения по изобретению подходят для введения как в виде эмульсий масло-в-воде, так и в виде рецептур мицелл. Соединения обеспечивают высокую нагрузку лекарственным веществом, что дает возможность введения небольших объемов.
Эмульсии, содержащие токоферол-модифицированные камптотециновые соединения по изобретению, обеспечивают увеличенную стабильность лактоновых соединений по сравнению с обычными способами введения камптотециновых соединений. Длинный период полупревращения плазмы достигается для токоферол-модифицированных камптотециновых соединений благодаря продолжительному воздействию соединения на опухоль. Токоферол-модифицированные соединения достигают высокого проникания через липоидные мембраны клеток опухоли. Больший антиопухолевый эффект без увеличения токсичности может быть обеспечен токоферол-модифицированными камптотециновыми соединениями по изобретению по сравнению с немодифицированным камптотецином и доступными в настоящее время аналогами каптотецина.
Хотя соединения по изобретению, имеющие формулу (2) с m=1, формулу (3) с n=1 или формулу (8), не включают соединения, специфически не допустимые, как описано выше, следует оценить, что композиции, рецептуры эмульсий, рецептуры микроэмульсий и рецептуры мицелл включают соединения по изобретению, имеющие формулы (1)-(8) без подобных ограничений. Способы введения композиций, рецептур эмульсий, рецептур микроэмульсий и рецептур мицелл и способы подготовки условий для подвергающегося лечению при введении композиций, рецептур эмульсий, рецептур микроэмульсий и рецептур мицелл также не ограничены при рассмотрении соединений по изобретению.
Следующие примеры иллюстрируют, но не ограничивают изобретение.
ПРИМЕРЫ
ПРИМЕР 1
Приготовление типичного токоферол-модифицированного соединения камптотецина: токоферолсукцинат камптотецина
В колбу объемом 500 мл загружали 10,6 грамма d-α-токоферол янтарной кислоты, 6,9 грамма камптотецина, 6,13 грамма 2-хлор-1-метилпиридинийиодида (ХМПИ), 5,86 грамма 4-(диметиламино)пиридина (ДМАП) и 200 мл сухого N,N-диметилацетамида. Смесь перемешивали при комнатной температуре в течение 24 часов и затем нагревали при 50°С в течение 4 часов. Смесь охлаждали до комнатной температуры и затем фильтровали для удаления осадка и фильтрат собирали. К фильтрату прибавляли 250 мл хлороформа и 150 мл деионизированной воды для экстракции продукта в хлороформ и водную фракцию удаляли, используя делительную воронку. Фракцию с хлороформом промывали деионизированной водой (3·150 мл) в делительной воронке, собирали, сушили над безводным MgSO4 в течение ночи. MgSO4 удаляли фильтрацией и хлороформ удаляли с помощью роторного испарителя при пониженном давлении, получая темно-желтое твердое вещество. Продукт очищали колоночной хроматографией на силикагеле. (Выход: 9,5 грамма, 55,2%).
1Н ЯМР (300 МГц, CDCl3): δ 8,318(с, 1Н), 8,163-8,135(д, J=8,4 Гц, 1Н), 7,927-7,901(д, J=7,8 Гц, 1Н), 7,842-7,787(м, 1Н), 7,682-7,632(м, 1Н), 7,263-7,242(д, J=6,3 Гц, 1Н), 5,702-5,410(Abкв, J1=17,4 Гц, J2=70 Гц, 2Н), 5,190(с, 2Н), 3,014-2,938(м, 4Н), 2,368-0,809(м, 54Н).
Элементный анализ. Рассчитано для C53H68N2O8: C, 73,92; H, 7,96; N 3,25. Найдено С, 73,61; Н, 7,90; N, 3,17.
ПРИМЕР 2
Приготовление типичного токоферол-модифицированного соединения камптотецина: токоферолсукцинат 10-гидроксикамптотецина
Способ 1. В колбу объемом 100 мл загружали 1,06 грамма d-α-токоферол янтарной кислоты, 0,476 грамма тионилхлорида и 50 мл толуола. Смесь перемешивали при комнатной температуре в течение ночи. Растворитель удаляли с помощью роторного испарителя при 50°С и остаток собирали. К остатку прибавляли 0,728 грамма 10-гидроксикамптотецина и 40 мл сухого тетрагидрофурана при перемешивании. Затем 0,404 грамма триэтиламина в 10 мл тетрагидрофурана прибавляли по каплям в реакционную смесь. Смесь перемешивали при комнатной температуре в течение ночи. Смесь фильтровали, и белый порошок промывали этилацетатом (3·10 мл). Фильтрат собирали. Растворитель удаляли с помощью роторного испарителя. Остаток собирали и очищали колоночной хроматографией на силикагеле с подвижной фазой, состоящей из ацетона и хлороформа (1:4, об./об.). (Выход: 0,85 грамма, 48,4%).
МС (ES положительная ионизация): m/z 877 (M)+.
Анализ. Рассчитано для C53H68N2O9: C, 72,58; H, 7,81; N, 3,19. Найдено: С, 72,52; Н, 7,84; N, 3,21.
Альтернативно, токоферолсукцинат 10-гидроксикамптотецина может быть получен, как описано ниже.
Способ 2. В колбу объемом 100 мл загружали 2,65 грамма d-α-токоферолсукцината, 0,89 г тионилхлорида и 20 мл толуола. Смесь перемешивали при комнатной температуре в течение 24 часов. Толуол и избыток тионилхлорида удаляли отгонкой в вакууме при 50°С. Остаток растворяли в 15 мл хлорметана для получения раствора А. В колбу объемом 100 мл прибавляли при перемешивании 0,9 грамма 10-гидроксикамптотецина, 0,5 мл триэтиламина и 25 мл свежевысушенного N,N-диметилацетамида. Далее 15 мл раствора А медленно прибавляли в смесь через капельную воронку в течение 5 минут. Реакционную смесь перемешивали при комнатной температуре в течение 24 часов. Смесь концентрировали отгонкой в вакууме. К остатку прибавляли 150 мл этилацетата. Смесь промывали насыщенным водным раствором NaCl (3·100 мл). Смесь сушили над безводным MgSO4. MgSO4 удаляли фильтрацией и затем этилацетат удаляли отгонкой в вакууме. Сырой продукт очищали колоночной хроматографией на силикагеле. (Выход: 1,14 грамма, 52,5%).
ПРИМЕР 3
Приготовление типичного токоферол-модифицированного соединения камптотецина: токоферолсукцинат 7-этил-10-гидроксикамптотецина
Способ 1. В колбу объемом 500 мл загружали 22,5 грамма d-α-токоферолсукцината, 7,6 г тионилхлорида и 200 мл толуола. Смесь перемешивали при комнатной температуре в течение 24 часов. Толуол и избыток тионилхлорида удаляли отгонкой в вакууме. Остаток растворяли в 100 мл хлорметана для получения раствора А. Раствор А использовали сразу же и не выдерживали на воздухе. В колбу объемом 500 мл загружали при перемешивании 7,8 грамма 7-этил-10-гидроксикамптотецина, 7 мл триэтиламина и 250 мл свежевысушенного N,N-диметилацетамида. 100 мл раствора А медленно прибавляли в смесь через капельную воронку в течение 30 минут. Реакционную смесь перемешивали при комнатной температуре в течение 24 часов. Смесь концентрировали вакуумной отгонкой. К остатку прибавляли 500 мл этилацетата. Смесь промывали насыщенным водным раствором NaCl (3·200 мл). Смесь сушили над безводным MgSO4. MgSO4 удаляли фильтрацией и затем этилацетат удаляли отгонкой в вакууме. Сырой продукт очищали перекристаллизацией из ацетона. (Выход: 15,18 грамма, 83,9%).
Температура плавления 171-173°С.
1Н ЯМР (300 МГц, CDCl3): δ 8,236-8,206(д, J=9 Гц, 1Н), 7,809-7,801(д, J=2,4 Гц, 1Н), 7,648(с, 1Н), 7,572-7,533(дд, J1=2,7 Гц, J2=9,3 Гц, 1Н), 5,781-5,280(Abкв, J1=16,2 Гц, J2=134,0 Гц, 2Н), 5,253(с, 2Н), 3,863(с, 1Н), 3,136-3,113(м, 6Н), 2,588(т, 2Н), 2,091(с, 3Н), 2,037(с, 3Н), 1,994(с, 3Н), 1,970-1,852(м, 2Н), 1,821-1,725(м, 2Н), 1,654-0,833(м, 42Н).
МС (ES-положительная ионизация): m/z 905(M)+, 928(M+Na)+.
Анализ. Вычислено для С55Н72N2O9: C 72,98; H 8,02; N 3,09.
Найдено: С 72,87; H 8,01; N 2,88.
Альтернативно токоферолсукцинат 7-этил-10-гидроксикамптотецина может быть получен, как описано ниже.
Способ 2. В колбу объемом 500 мл загружали 8,48 грамма d-α-токоферол сукцината, 3,81 грамма тионилхлорида и 250 мл толуола. Смесь перемешивали при комнатной температуре в течение ночи. Толуол и избыток тионилхлорида удаляли с помощью роторного испарителя при 50°С и остаток собирали. К остатку прибавляли при перемешивании 6,27 грамма 7-этил-10-гидроксикамптотецина и 250 мл высушенного натрием тетрагидрофурана. Далее к смеси по каплям прибавляли 3,23 грамма триэтиламина в 50 мл тетрагидрофурана. Смесь перемешивали при комнатной температуре в течение ночи. Смесь фильтровали и белый порошок промывали этилацетатом (3·50 мл). Фильтрат собирали. Растворитель удаляли с помощью роторного испарителя. Сырой продукт очищали перекристаллизацией в ацетоне. (Выход: 8,28 грамма, 57,2%).
ПРИМЕР 4
Получение типичного токоферол-модифицированного соединения камптотецина: 10,20-ди(токоферолсукцинат) 7-этил-10-гидроксикамптотецина
В колбу объемом 100 мл загружали 0,905 грамма токоферолсукцината 7-этил-10-гидроксикампотецина, 0,53 грамма d-α-токоферолянтарной кислоты, 0,255 г 2-хлор-1-метилпиридинийиодида, 0,244 грамма 4-(диметиламино)пиридина и 50 мл диоксана. Смесь перемешивали при комнатной температуре в течение 24 часов. Тонкослойная хроматография показала, что реакция прошла. Смесь фильтровали для удаления твердой фазы и фильтрат собирали. Растворитель удаляли вакуумной отгонкой. Сырой продукт очищали колоночной хроматографией на силикагеле с 30% этилацетатом в циклогексане. (Выход: 0,64 грамма, 44,82%).
1Н ЯМР (300 МГц, CDCl3): δ 8,168-8,138(д, J=9 Гц, 1Н), 7,813-7,805(д, J=2,4 Гц, 1Н), 7,754-7,536(дд, J1=2,1 Гц, J2=11,4 Гц, 1Н), 7,197(с, 1Н), 5,703-5,409(Abкв, J1=17,4 Гц, J2=71,0, 2Н), 5,243-5,088(м, 2Н), 3,113-2,857(м, 10Н), 2,606-2,564(т, J=6 Гц, 2Н), 2,383-2,184(м, 2Н), 2,090-1,723(м, 22Н), 1,588-0,785(м, 80Н).
МС (ES-положительная ионизация): m/z 1418(M+H)+.
Элементный анализ. Рассчитано для C88H124N2O13: C 74,54; H 8,81; N 1,98. Найдено: C 74,31; H 8,96; N 1,75.
ИКνмакс KBrсм-1: 2925, 2867, 1751, 1665, 1615, 1657, 1510, 1458, 1413, 1376, 1330, 1218, 1128, 1075, 1060, 1035, 992, 943, 923, 829, 812, 758, 724, 668.
ПРИМЕР 5
Приготовление типичного токоферол-модифицированного соединения камптотецина: токоферол-камптотецин, сопряженный с гекса(этиленгликоль)связующим
Получение гекса(этиленгликоль)токоферолсукцината. В колбе объемом 250 мл растворяли при перемешивании 2,65 грамма d-α-токоферол янтарной кислоты и 2,82 грамма гекса(этиленгликоля) в 100 мл толуола. Толуол удаляли с помощью роторного испарителя (сушка азеотропной дистилляцией). К смеси прибавляли 100 мл хлороформа, 1,08 грамма N,N-дициклогексилкарбодиимида и 100 мг 4-(диметиламино)пиридина. Смесь перемешивали в течение ночи. Тонкослойная хроматография с 40% ацетона в гексане показала, что реакция завершилась. Смесь промывали три раза деионизированной водой (3·100 мл), фракцию хлороформа собирали и сушили над безводным MgSO4 в течение двух часов. После фильтрации хлороформ удаляли с помощью роторного испарителя. Сырой продукт очищали колоночной хроматографией на силикагеле, используя последовательно растворители 30% этилацетата в гексане, 50% этилацетата в гексане и 30% ацетона в гексане. (Выход: 0,53 грамма, 13,33%).
Получение токоферолсукцинилгекса(этиленгликоль)янтарной кислоты. В колбу объемом 100 мл загружали 1,42 грамма гекса(этиленгликоль)токоферолсукцината, полученного выше, 0,2 грамма ангидрида янтарной кислоты, 2 капли олово(II)этилгексаноата и 25 мл ксилола. Смесь кипятили с обратным холодильником в течение 4 часов. После завершения реакции растворитель удаляли с помощью роторного испарителя. Сырой продукт очищали колоночной хроматографией на силикагеле. (Выход: 0,864 грамма, 54%).
Получение токоферолсукцината камптотецина с гекса(этиленгликоль)связующим. В колбу объемом 100 мл загружали 0,822 грамма токоферолсукцинилгекса(этиленгликоль)янтарной кислоты, полученной выше, 0,3 грамма камптотецина, 0,47 грамма 2-хлор-1-метилпиридинийиодида, 0,45 грамма 4-(диметиламино)пиридина и 40 мл сухого N,N-диметилацетамида. Реакционную смесь перемешивали при комнатной температуре в течение ночи. После завершения реакции растворитель удаляли вакуумной отгонкой и остаток собирали. К остатку прибавляли 100 мл этилацетата. После перемешивания в течение 30 минут смесь фильтровали для удаления осадка, и фильтрат собирали и концентрировали. Сырой продукт очищали колоночной хроматографией на силикагеле. (Выход: 0,342 грамма, 30,4%).
1Н ЯМР (300 МГц, CDCl3): δ 8,388(с, 1Н), 8,240-8,213(д, J=8,1 Гц, 1Н), 7,951-7,923(д, J=8,4 Гц, 1Н), 7,861-7,805(дт, J1=1,5 Гц, J2=8,4 Гц, 1Н), 7,694-7,640(дт, J1=1,2 Гц, J2=8,1 Гц, 1Н), 7,269(с, 1Н), 5,708-5,365(Abкв, J1=17,1 Гц, J2=85,8 Гц, 2Н), 5,283(с, 2Н), 4,273-4,169(м, 4Н), 3,705-3,673(т, 2Н), 3,631-3,550(м, 18Н), 2,926-2,654(м, 8Н), 2,597-2,552(т, J=6,9 Гц, 2Н), 2,381-2,113(м, 2Н), 2,074(с, 3Н), 2,004(с, 3Н), 1,964(с, 3Н), 1,827-1,683(м, 2Н), 1,655(с, 3Н), 1,544-0,964(м, 24Н), 0,875-0,830(м, 12Н).
МС(ES-положительная ионизация)m/z 1225(M)+.
Элементный анализ. Вычислено для С88Н124N2O13: С 67,62; H 7,90; N 2,29. Найдено C 67,08; H 8,04; N 2,07.
ИКνмакс KBr см-1: 2925, 2867, 1735, 1667, 1618, 1563, 1500, 1457, 1405, 1366, 1349, 1232, 1204, 1141, 1107, 1060, 994, 945, 859, 813, 787, 761, 723, 707.
ПРИМЕР 6
Получение типичного токоферол-модифицированного соединения паклитаксела: токоферолсукцинат паклитаксела
В колбу объемом 250 мл загружали 5,83 грамма токоферолянтарной кислоты, 2,38 грамма тионилхлорида и 50 мл толуола. Смесь перемешивали при комнатной температуре в течение ночи. Растворитель удаляли с помощью роторного испарителя при 50°С и остаток собирали. К остатку при перемешивании прибавляли 8,54 грамма паклитаксела и 100 мл сухого тетрагидрофурана. Далее 1,52 грамма триэтиламина в 50 мл тетрагидрофурана прибавляли по каплям к реакционной смеси. Смесь перемешивали при комнатной температуре в течение ночи. Смесь фильтровали и белый порошок промывали этилацетатом (3·10 мл). Фильтрат собирали. Растворитель удаляли с помощью роторного испарителя. Осадок собирали и очищали перекристаллизацией в ацетоне и гексане. (Выход: 11,56 грамма, 84,6%).
Анализ. Вычислено для C80H103NO18: C, 70,31; H, 7,59; N, 1,02. Найдено: C, 70,02; H, 7,83; N, 0,93.
ПРИМЕР 7
Получение типичного токоферол-модифицированного соединения доцетаксела: токоферолсукцинат доцетаксела
В колбу объемом 250 мл загружали 9,86 грамма d-α-токоферолянтарной кислоты, 5,0 грамм доцетаксела, 3,83 грамма сухого N,N-дициклогексилкарбодиимида, 500 мг 4-(диметиламино)пиридина и 150 мл хлороформа. Смесь перемешивали при комнатной температуре в течение ночи. Смесь фильтровали для удаления осадка и фильтрат собирали. Растворитель удаляли с помощью роторного испарителя и остаток собирали. Сырой продукт очищали колоночной хроматографией на силкагеле.
ПРИМЕР 8
Получение моно-токоферолфталата
В колбу объемом 100 мл загружали 8,61 грамма dl-α-токоферола, 2,96 грамма фталиевого ангидрида, 50 мг олово(II) 2-этилгексаноата и 50 мл сухого N,N-диметилацетамида. Смесь перемешивали при примерно 140°С в течение 24 часов. После охлаждения смеси до комнатной температуры смесь выливали в 150 мл этилацетата. Смесь промывали три раза насыщенным водным NaCl (3·100 мл) и сушили над безводным MgSO4 в течение ночи. Сырой продукт очищали колоночной хроматографией на силикагеле с 30% этилацетата в гексане. (Выход: 3,6 грамма, 31,1%).
1Н ЯМР (300 МГц, CDCl3): δ ppm 10,80(шир.с, 1Н), 8,119-8,063(м, 1Н), 7,883-7,828(м, 1Н), 7,678-7,616(м, 2Н), 2,627-2,582(т, 2Н), 2,123(с, 3Н), 2,112(с, 3Н), 2,081(с, 3Н), 1,868-1,702(м, 2Н), 1,616-1,020(м, 24Н), 0,874-0,834(м, 12Н).
Анализ. Вычислено для C37H54O5: C, 76,78; H, 9,40. Найдено: С, 76,57; Н, 9,29.
ИК νмакс KBr см-1: 3073, 2919, 2858, 1737, 1701, 1578, 1455, 1409, 1373, 1276, 1230, 1107, 1071, 913, 738.
ПРИМЕР 9
Получение моно-токоферолтерефталата
В колбу объемом 100 мл загружали 4,30 грамма dl-α-токоферола, 3,32 грамма терефталиевой кислоты, 2,55 грамма 2-хлор-1-метилпиридинийиодида, 0,244 грамма 4-(диметиламино)пиридина и 50 мл сухого N,N-диметилацетамида. Смесь перемешивали при 50°С в течение 4 часов. Тонкослойная хроматография показала, что реакция завершилась. После охлаждения смеси до комнатной температуры смесь выливали в 150 мл этилацетата. Смесь промывали три раза насыщенным водным NaCl (3·100 мл) и сушили над безводным MgSO4 в течение ночи. Сырой продукт очищали колоночной хроматографией на силикагеле с 30% этилового эфира в гексане. (Выход: 1,60 грамма, 27,6%).
1Н ЯМР (300 МГц, CDCl3): δ ppm 11,80(шир.с, 1Н), 8,374-8,259(кв, J1=8,4 Гц, J2=26,1 Гц, 4Н), 2,650-2,607(т, 2Н), 2,130(с, 3Н), 2,066(с, 3Н), 2,024(с, 3Н), 1,895-1,783(м, 2Н), 1,532-1,083(м, 24Н), 0,878-0,839(м, 12Н).
Анализ. Вычислено для C37H54O5: С 76,78; Н 9,40. Найдено: С 76,64; Н 9,39.
ИК νмакс KBr см-1: 3062, 2924, 2858, 1737, 1696, 1573, 1460, 1424, 1373, 1276, 1240, 1097, 928, 774, 723.
ПРИМЕР 10
Приготовление типичного токоферол-модифицированного соединения камптотецина: токоферолтерефталат камптотецина
В колбу объемом 100 мл загружали 1,16 грамма моно-токоферола, приготовленного выше, 0,70 грамма камптотецина, 0,511 грамма 2-хлор-1-метилпиридинийиодида и 0,489 грамма 4-(диметиламино)пиридина. Смесь перемешивали при 50°С в течение ночи. Тонкослойная хроматография показала, что реакция завершилась. После охлаждения смеси до комнатной температуры реакционную смесь выливали в 150 мл этилацетата. Смесь фильтровали и фильтрат собирали. Фильтрат промывали насыщенным водным NaCl (3·100 мл) и сушили над безводным MgSO4 в течение ночи. Сырой продукт очищали колоночной хроматографией на силикагеле. (Выход: 0,560 грамма, 30,8%).
1Н ЯМР (300 МГц, CDCl3): δ ppm 8,387(с, 1Н), 8,370-8,242(кв, J1=8,4 Гц, J2=30,3 Гц, 4Н), 8,167-8,139(д, J=8,4 Гц, 1Н), 7,937-7,910(д, J=8,1 Гц, 1Н), 7,823-7,774(т, 1Н), 7,672-7,625(т, 1Н), 7,260(с, 1Н), 5,823-5,462(Abкв, J1=17,4 Гц, J2=90,9 Гц, 2Н), 5,302(с, 2Н), 2,461(т, 2Н), 2,559-2,312(м, 2Н), 2,123(с, 3Н), 2,056(с, 3Н), 2,015(с, 3Н), 1,844-1,801(м, 2Н), 1,629-1,085(м, 27Н), 0,938-0,789(м, 12Н).
Анализ. Вычислено для C57H68N2O8: С 75,30; Н 7,54; N 3,08. Найдено: С 74,91; Н 7,56; N 3,02.
ИК νмаксKBrсм-1: 3057, 2924, 2858, 1757, 1737, 1675, 1614, 1558, 1450, 1399, 1266, 1235, 1163, 1102, 1020, 723.
ПРИМЕР 11
Приготовление типичного токоферол-модифицированного соединения камптотецина: токоферолциклогексан-1,2-дикарбоксилат 7-этил-10-гидроксикамптотецина
Приготовление токоферолциклогексан-1,2-дикарбоновой кислоты. Смесь 1,54 грамма ангидрида 1,2-циклогександикарбоновой кислоты, 8,6 грамма d-α-токоферола, 1,34 грамма треххлористого алюминия и 100 мл циклогексана кипятили с обратным холодильником в 250 мл колбе в течение примерно 30 минут. После охлаждения смеси до комнатной температуры ее фильтровали. Фильтрат промывали разбавленным водным раствором соляной кислоты и затем сушили над безводным MgSO4. Смесь концентрировали и сырой продукт очищали колоночной хроматографией на силикагеле. (Выход: 3,325 грамма, 56,9%).
Приготовление токоферолциклогексан-1,2-дикарбоксилата 7-этил-10-камптотецина. Смесь 1,08 грамма токоферолциклогексан-1,2-дикарбоновой кислоты, приготовленной выше, 0,44 грамма тионилхлорида и 20 мл толуола перемешивали в атмосфере азота в течение ночи. Толуол и избыток тионилхлорида удаляли вакуумной отгонкой и остаток растворяли в 10 мл дихлорметана для получения раствора А. В 100 мл колбе растворяли 0,350 грамма SN38 в 25 мл сухого N,N-диметилацетамида для получения раствора В. Раствор А и 0,186 г триэтиламина добавляли к раствору В. Смесь перемешивали в течение ночи при комнатной температуре. Сырой продукт очищали колоночной хроматографией на силикагеле. (Выход 0,59 грамма, 68,9%).
ПРИМЕР 12
Приготовление типичного токоферол-модифицированного соединения доксорубицина: токоферолсукцинат доксорубицина
В колбу объемом 100 мл загружали эквивалентные моли (1 ммоль) токоферолянтарной кислоты, доксорубицина, N,N-дициклогексилкарбодиимида и 50 мл сухого N,N-диметилацетамида. Смесь перемешивали при комнатной температуре до завершения реакции. Смесь фильтровали для удаления белого осадка и фильтрат собирали. Растворитель удаляли с помощью роторного испарителя и остаток собирали. Продукт очищали или перекристаллизацией, или колоночной хроматографией на силикагеле.
ПРИМЕР 13
Приготовление типичного токоферол-модифицированного соединения гидроксизина: токоферолсукцинат гидроксизина
В колбу объемом 100 мл загружали эквивалентные моли (1 ммоль) токоферолянтарной кислоты и тионилхлорида и 50 мл толуола. Смесь перемешивали при комнатной температуре в течение ночи. Растворитель удаляли с помощью роторного испарителя при 50°С и остаток собирали. К остатку при перемешивании прибавляли 1 ммоль гидроксизина и 40 мл хлороформа. Затем к реакционной смеси при 0-5°С по каплям прибавляли 1 ммоль триэтиламина в 10 мл хлороформа. Смесь затем перемешивали при комнатной температуре в течение ночи. Смесь промывали насыщенным водным раствором NaHCO3 (3·50 мл). Органическую фазу собирали и сушили над безводным MgSO4. Растворитель удаляли с помощью роторного испарителя после удаления MgSO4. Остаток собирали и сырой продукт очищали или перекристаллизацией, или колоночной хроматографией на силикагеле.
ПРИМЕР 14
Растворимость типичного токоферол-модифицированного терапевтического лекарственного соединения
В данном примере растворимость типичных токоферол-модифицированных терапевтических лекарственных соединений по изобретению, токоферолсукцинат камптотецина и токоферолсукцинат 7-этил-10-гидроксикамптотецина сравнивали с растворимостью камптотецина в различных растворителях.
Растворимость камптотецина, токоферолсукцината камптотецина и токоферолсукцината 7-этил-10-гидроксикамптотецина определяли в нескольких растворителях. Соединения растворяли в каждом растворителе при постоянном перемешивании и температуре до насыщения. Полученные растворы центрифугировали и надосадочную жидкость анализировали с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ).
Сравнительная растворимость (мг/г) камптотецина, токоферолсукцината камптотецина и токоферолсукцината 7-этил-10-гидроксикамптотецина в различных растворителях представлена в таблице 1.
Сравнение растворимости камптотецина и токоферолсукцината камптотецина
(мг/г)
мг/г)
(мг/г)
(°С)
NF
температура
USP/NF
USP
температура
EP
температура
NF
температура
денатурат
температура
температура
температура
температура
температура
дихлорид
температура
температура
USP/EP/BP/
JP
температура
Результаты в таблице 1 иллюстрируют, что токоферолсукцинат камптотецина и токоферолсукцинат 7-этил-10-гидроксикамптотецина оба имеют существенную растворимость в маслах и имеют особенно высокую растворимость в витамине Е (α-токоферол).
ПРИМЕР 15
Эмульсии, содержащие типичные токоферол-модифицированные терапевтические лекарственные соединения
В данном примере описаны типичные эмульсии, содержащие токоферол-модифицированные терапевтические лекарственные соединения.
А. Эмульсия токоферолсукцинат 7-этил-10-гидроксикамптотецина.
Токоферолсукцинат 7-этил-10-гидроксикамптотецин, полученный как описано в примере 3, растворяли в витамине Е и затем эмульгировали с использованием микрофлюидизатора (М110Y Microfluidics) в присутствии d-α-токоферолполиэтиленгликоль 1000 сукцината (TPGS), полоксамера 407 и солевого раствора для получения эмульсии, имеющей следующую композицию (мас.%):
Эмульсию фильтровали через фильтр 0,2 мкм и разливали в стерильные стеклянные пузырьки. Средний размер частиц составлял приблизительно 50 нМ, как определяли субмикронным определителем размера (Nicomp Model 370), с 99% частиц меньшими, чем 80 нм. Никаких признаков образования осадка или уменьшения концентрации при измерении с помощью ВЭЖХ не наблюдали в течение, по меньшей мере, 3 месяцев при хранении при 4°С.
B. Эмульсия токоферолсукцинат 7-этил-10-гидроксикамптотецина.
Токоферолсукцинат 7-этил-10-гидроксикамптотецин, полученный как описано в примере 3, растворяли в витамине Е и затем эмульгировали с использованием микрофлюидизатора (М110Y Microfluidics) в присутствии TPGS и солевого раствора для получения эмульсии, имеющей следующую композицию (мас.%):
Данная рецептура образовывала более желтую и крупнозернистую эмульсию, чем эмульсия, полученная как описано выше, которая включала Полоксамер 407. Эмульсию фильтровали через фильтр 0,2 мкм и разливали в стерильные стеклянные пузырьки. Средний размер частиц составлял приблизительно 75 нм, как определяли субмикронным определителем размера (Nicomp Model 370), с 99% частиц меньшими, чем 170 нм. Никаких признаков образования осадка или уменьшения концентрации при измерении с помощью ВЭЖХ не наблюдали в течение, по меньшей мере, 3 месяцев при хранении при 4°С.
С. Эмульсия токоферолсукцината камптотецина.
Токоферолсукцинат камптотецина, полученный как описано в примере 1, растворяли в витамине Е и затем эмульгировали с использованием микрофлюидизатора (М110Y Microfluidics) в присутствии TPGS, полоксамера 407 и солевого раствора для получения эмульсии, имеющей следующую композицию (мас.%):
Эмульсию фильтровали через фильтр 0,2 мкм и разливали в стерильные стеклянные пузырьки. Средний размер частиц составлял приблизительно 40 нм, как определяли субмикронным определителем размера (Nicomp Model 370), с 99% частиц меньшими, чем 75 нм. Никаких признаков образования осадка или уменьшения концентрации при измерении ВЭЖХ не наблюдали в течение, по меньшей мере, 3 месяцев при хранении при 4°С.
D. Эмульсия токоферолсукцината камптотецина.
Токоферолсукцинат камптотецина, полученный как описано в примере 1, растворяли в витамине Е и затем эмульгировали с использованием микрофлюидизатора (М110Y Microfluidics) в присутствии TPGS, полоксамера 407 и солевого раствора для получения эмульсии, имеющей следующую композицию (мас.%):
Эмульсию фильтровали через фильтр 0,2 мкм и разливали в стерильные стеклянные пузырьки. Средний размер частиц составлял приблизительно 30 нм, как определяли субмикронным определителем размера (Nicomp Model 370), с 99% частиц меньшими, чем 100 нм. Никаких признаков образования осадка или уменьшения концентрации при измерении ВЭЖХ не наблюдали в течение, по меньшей мере, 3 месяцев при хранении при 4°С.
Е. Эмульсия токоферолсукцината 7-этил-10-гидроксикамптотецина.
Токоферолсукцинат 7-этил-10-гидроксикамптотецина, полученный как описано в примере 3, растворяли в витамине Е и затем эмульгировали с использованием микрофлюидизатора (М110Y Microfluidics) в присутствии TPGS и буферного солевого раствора лимонной кислоты для получения эмульсии, имеющей следующую композицию (мас.%):
Эмульсию фильтровали через фильтр 0,2 мкм и разливали в стерильные стеклянные пузырьки. Средний размер частиц составлял приблизительно 60 нм, как определяли субмикронным определителем размера (Nicomp Model 370), с 99% частиц меньшими, чем 150 нМ. Никаких признаков образования осадка или уменьшения концентрации при измерении ВЭЖХ не наблюдали в течение, по меньшей мере, 3 месяцев при хранении при 4°С и 25°С.
F. Эмульсия токоферолсукцината 7-этил-10-гидроксикамптотецина.
Токоферолсукцинат 7-этил-10-гидроксикамптотецина, полученный как описано в примере 3, растворяли в витамине Е и затем эмульгировали с использованием микрофлюидизатора (М110Y Microfluidics) в присутствии TPGS и буферного солевого раствора сукцината для получения эмульсии, имеющей следующую композицию (мас.%):
Эмульсию фильтровали через фильтр 0,2 мкм и разливали в стерильные стеклянные пузырьки. Средний размер частиц составлял приблизительно 70 нм, как определяли субмикронным определителем размера (Nicomp Model 370), с 99% частиц меньшими, чем 170 нм. Никаких признаков образования осадка или уменьшения концентрации при измерении ВЭЖХ не наблюдали в течение, по меньшей мере, 3 месяцев при хранении при 4°С и 25°С.
Эмульсию фильтровали через фильтр 0,2 мкм и разливали в стерильные стеклянные пузырьки. Средний размер частиц составлял приблизительно 70 нм, как определяли субмикронным определителем размера (Nicomp Model 370), с 99% частиц меньшими, чем 170 нм. Никаких признаков образования осадка или уменьшения концентрации при измерении ВЭЖХ не наблюдали в течение, по меньшей мере, 1 месяца при хранении при 4°С, 25°С и 40°С.
Эмульсию фильтровали через фильтр 0,2 мкм и разливали в стерильные стеклянные пузырьки. Средний размер частиц составлял приблизительно 95 нм, как определяли субмикронным определителем размера частиц (Nicomp Model 370), с 99% частиц меньшими, чем 220 нм. Никаких признаков образования осадка или уменьшения концентрации при измерении ВЭЖХ не наблюдали в течение, по меньшей мере, 1 месяца при хранении при 4°С, 25°С и 40°С.
G. Рецептура мицелл токоферолсукцината 7-этил-10-гидроксикамптотецина (VESA-SN38)
Токоферолсукцинат 7-этил-10-гидроксикамптотецина растворяли в смеси, содержащей TPGS, ПЭГ(300) и этанол при, примерно, от 50°С до, примерно, 60°С с перемешиванием в течение, примерно, часа, до образования прозрачного раствора. К данному раствору прибавляли деионизированную воду (ДИ-вода), полоксамер 407 и ДИ-воду, полоксамер 188 и ДИ-воду или 0,9% водного раствора NaCl для образования рецептур 1-5 соответственно, ниже. Рецептуры перемешивали в течение нескольких минут для образования прозрачных мицелльных растворов, имеющих следующие композиции (мас.%):
Рецептуру раствора фильтровали через фильтр 0,2 мкм и разливали в стерильные стеклянные пузырьки. Никаких признаков образования осадка или уменьшения концентрации при измерении ВЭЖХ не наблюдали в течение, по меньшей мере, 11 недель при хранении при 4°С.
Раствор рецептуры фильтровали через фильтр 0,2 мкм и разливали в стерильные стеклянные пузырьки. Никаких признаков образования осадка или уменьшения концентрации при измерении ВЭЖХ не наблюдали в течение, по меньшей мере, 11 недель при хранении при 4°С.
Раствор рецептуры фильтровали через фильтр 0,2 мкм и разливали в стерильные стеклянные пузырьки. Никаких признаков образования осадка или уменьшения концентрации при измерении ВЭЖХ не наблюдали в течение, по меньшей мере, 11 недель при хранении при 4°С И 25°С.
Раствор рецептуры фильтровали через фильтр 0,2 мкм и разливали в стерильные стеклянные пузырьки. Никаких признаков образования осадка или уменьшения концентрации при измерении ВЭЖХ не наблюдали в течение, по меньшей мере, 1 недели при хранении при 4°С, 25°С и 40°С.
Раствор рецептуры фильтровали через фильтр 0,2 мкм и разливали в стерильные стеклянные пузырьки. Никаких признаков образования осадка или уменьшения концентрации при измерении ВЭЖХ не наблюдали в течение, по меньшей мере, 3 недель при хранении при 4°С.
Н. Рецептура мицелл токоферолсукцината 7-этил-10-гидроксикамптотецина (VESA-SN38)
Токоферолсукцинат 7-этил-10-гидроксикамптотецина растворяли в смеси, содержащей TPGS, ПЭГ(300) и этанол при примерно от 50°С до примерно 60°С с перемешиванием в течение, примерно, 1 часа до образования прозрачного раствора. К данному раствору прибавляли буферный солевой раствор сукцината для образования рецептур 1 и 2 ниже. Рецептуры перемешивали в течение нескольких минут для образования прозрачных мицелльных растворов, имеющих следующие композиции (мас.%):
Раствор рецептуры фильтровали через фильтр 0,2 мкм и разливали в стерильные стеклянные пузырьки.
сукцината, pH 4,0
Раствор рецептуры фильтровали через фильтр 0,2 мкм и разливали в стерильные стеклянные пузырьки.
ПРИМЕР 16
In vitro стабильность лактона типичного токоферол-модифицированного терапевтического лекарственного соединения в присутствии человеческого альбумина
В данном примере in vitro стабильность в присутствии человеческого альбумина лактоновой формы типичного токоферол-модифицированного терапевтического лекарственного соединения по изобретению, токоферолсукцината камптотецина и токоферолсукцината 7-этил-10-гидроксикамптотецина сравнивали in vitro со стабильностью лактоновой формы камптотецина.
Поскольку лактон (цикл Е) представляет собой критический фрагмент для активности камптотецина и, сообщается, что он не стабилен при физиологических условиях (pH 7,4), была определена стабильность лактона токоферолсукцината камптотецина и токоферолсукцината 7-этил-10-гидроксикамптотецина. Предпологалось, что солюбилизация токоферолсукцината камптотецина и токоферолсукцината 7-этил-10-гидроксикамптотецина в масляной фазе защищает лактон от гидролиза и, таким образом, обеспечивает улучшенную стабильность лактона в физиологических условиях. Для оценки стабильности лактона, солевой буферный раствор, (10 мМ, pH 7,4) содержащий 4% сыворотки альбумина человека, инкубировали при 37°С в присутствии камптотецина (растворенный в ДМСО), эмульсии токоферолсукцината камптотецина (полученной, как описано в примере 15С, обозначенной здесь как "SN2300 эмульсия") или эмульсии токоферолсукцината 7-этил-10-гидроксикамптотецина (полученной, как описано в примере 15А, обозначенной здесь как "SN2310 эмульсия"). Высокоэффективную жидкостную хроматографию с флуоресцентным детектором использовали для анализа уменьшения концентрации лактоновой формы со временем.
Фигура 12 иллюстрирует процентное изменение концентрации лактоновой формы от времени для камптотецина, токоферолсукцината камптотецина (SN2300) и токоферолсукцината 7-этил-10-гидроксикамптотецина (SN2310) в присутствии сыворотки альбумина человека. Устойчивость лактона токоферолсукцината камптотецина и токоферолсукцината 7-этил-10-гидроксикамптотецина больше, чем устойчивость камптотецина. Это резкое увеличение в устойчивости лактона может приводить к увеличенной активности по сравнению с немодифицированным исходным соединением камптотецина.
ПРИМЕР 17
In vitro цитотоксичность типичных токоферол-модифицированных терапевтических лекарственных соединений
В данном примере, in vitro цитотоксичность типичных токоферол-модифицированных терапевтических лекарственных соединений по изобретению, токоферолсукцината каптотецина и токоферолсукцината 7-этил-10-гидроксикамптотецина сравнивали с in vitro цитотоксичностью камптотецина, 10-гидроксикаптотецина, SN38, иринотекана и топотекана.
In vitro цитотоксичность, измеренную по значениям РИ50 (50% рост ингибирования) для токоферолсукцината камптотецина и токоферолсукцината 7-этил-10-гидроксикамптотецина, исследовали и сравнивали со значениями РИ50 в National Cancer Institute (NCI) для камптотецина, 10-гидроксикамптотецина, SN-38, иринотекана и топотекана в следующих колониях раковых клеток: NCI-H460(ATCC #HTB-177) (немалые легочные клетки), HCT-15 (ATCC #CCL-225) (ректальные), HT-116 (ATCC #CCL-247) (ректальные), HT-29 (ATCC #HTB-38) (ректальные), MCF-7 (ATCC #HTB-22) (грудные) и OVCAR-3 (ATCC #HTB-161) (яичниковые).
Изучение проводили с использованием рецептур эмульсий токоферолсукцината 7-этил-10-гидроксикамптотецина (описанных в примере 15А) и токоферолсукцината камптотецина (описанных в примере 15С), разбавленных в соответствующей клеточной среде. Клетки находились в контакте с различными концентрациями тестовых соединений в течение 48 часов. После окончания 48 часов проводили окрашивание с помощью ALamar Blue для определения числа жизнеспособных клеток и расчета уровня ингибирования клеточного роста при сравнении с контрольной группой. Процент ингибирования от концентрации рассчитывали с помощью уравнения Хилла для определения концентрации, которая вызывает 50% рост ингибирования (РИ50).
Чувствительность тестируемых клеточных линий к токоферолсукцинату камптотецина (SN2300) и токоферолсукцинату 7-этил-10-гидроксикамптотецина (SN2310), камптотецину, иринотекану и топотекану иллюстрируется в таблице 2 и фигуре 13.
Сравнительная концентрация препарата, которая вызывает 50% рост ингибирования (РИ50)
клеток
(NCl)
CPT
(NCl)
(NCl)
(NCl)
(NCl)
CPT
SN38
(NSCLC)
(толстый
кишечник)
(яичники)
актив-
ность
(толстый
кишечник)
(толстый
кишечник)
(грудь)
Результаты в таблице 2 иллюстрируют, что рецептуры токоферол-модифицированных терапевтических лекарственных соединений по изобретению обеспечивают эффективную противоопухолевую активность.
ФИГУРА 13 представляет собой диаграмму значений РИ50 (концентрация, которая вызывает 50% рост ингибирования), определенных для токоферолсукцината камптотецина и для токоферолсукцината 7-этил-10-гидроксикамптотецина в четырех тестируемых колониях клеток. Значения, сообщенные NCI для тех же самых колоний клеток для камптотецина, иринотецкана и топотекана, также включены для сравнения. Высокое значение РИ50 соответствует низкой концентрации препарата, вызывающей 50% ингибирование. Из диаграммы ясно, что соединения по изобретению токоферолсукцинат камптотецина и токоферолсукцинат 7-этил-10-гидроксикамптотецина показывают высокий уровень цитотоксичной активности, аналогично камптотецину.
ПРИМЕР 18
Фармакокинетика типичных токоферол-модифицированных терапевтических лекарственных соединений
В данном примере фармакокинетика типичных токоферол-модифицированных терапевтических лекарственных соединений по изобретению токоферолсукцината камптотецина и токоферолсукцината 7-этил-10-гидроксикамптотецина сравнивают с камптотецином, иринотеканом и топотеканом.
Фармакокинетические профили токоферолсукцината камптотецина и токоферолсукцината 7-этил-10-гидроксикамптотецина исследовали на Sprague-Dowley крысах после пилюль, внутривенного введения рецептур эмульсий лекарственных соединений (SN2300 эмульсия и SN2310 эмульсия) через латеральную хвостовую вену дозой, приблизительно, 14 мг лекарственного вещества/кг массы тела. Образцы крови отбирали до 120 часов после дозирования через яремную вену. Концентрацию каждого производного камптотецина в плазме определяли высокоэффективной жидкостной хроматографией (ВЭЖХ) с флуоресцентным детектором. Общий анализ проводили с использованием WinNonlin (v 4.1).
Фармакокинетические профили токоферолсукцината камптотецина (SN2300) и токоферолсукцината 7-этил-10-гидроксикамптотецина (SN2310) показаны на ФИГУРАХ 14А и 14B соответственно. На ФИГУРАХ 14А и 14В показаны значения концентрация-время после внутривенной инъекции 13,8 мг лекарственного соединения/кг массы тела для токоферолсукцината камптотецина (SN2300 эмульсия) и токоферолсукцината 7-этил-10-гидроксикамптотецина (SN2310 эмульсия) соответственно. С ссылкой на ФИГУРЫ 14А и 14В показан пролонгированный полупериод превращения плазмы после внутривенного введения, особенно для токоферолсукцината камптотецина.
Рассчитанный полупериод элиминирования плазмы, среднее время удерживания и выведение токоферолсукцината камптотецина (SN2300), токоферолсукцината 7-этил-10-гидроксикамптотецина (SN2310), камптотецина, иринотекана и топотекана представлены в Таблице 3.
Термин «полупериод элиминирования плазмы» относится ко времени, необходимому для уменьшения концентрации препарата в плазме до 50% после достижения равновесия. Термин «константа скорости элиминирования» относится к доле препарата, элиминированного в единицу времени. При первом порядке элиминирования скорость элиминирования прямо пропорциональна концентрации препарата в сыворотке. Имеется линейная зависимость между скоростью элиминирования и концентрацией препарата в сыворотке. Хотя количество препарата, элиминированного в процессе первого порядка, изменяется с концентрацией, доля элиминированного препарата остается постоянной.
Термин «очистка» относится к измерению способности тела вывести лекарственный препарат и представляет собой гипотетический объем распределения препарата, который выводится за единицу времени (т.е. мл/мин) любым путем удаления препарата. Важно прояснить, что очистка не показывает, как много препарата было удалено, скорее объем биологической жидкости, такой как кровь или плазма, который должен был бы быть свободным от препарата за счет выведения. Термин «объем распределения» относится к рассчитанному объему жидкости тела, который потребовался бы, чтобы растворить суммарное количество препарата с той же самой концентрацией, которая найдена в крови. Это представляет собой константу пропорциональности, связывающую количество препарата в теле с измеренной концентрацией в биологической жидкости (кровь, плазма, сыворотка).
Сравнительные фармакокинетические параметры после внутривенного введения крысам токоферолсукцината камптотецина (SN2300) и токоферолсукцината 7-этил-10-гидроксикамптотецина (SN2310) в сравнении с камптотецином, иринотеканом и топотеканом
(элиминирование)
(часы)
(л/час/кг)
Таблица 3 иллюстрирует, что рассчитанный полупериод элиминирования токоферолсукцината камптотецина (SN2300) и токоферолсукцината 7-этил-10-гидроксикамптотецина (SN2310) приблизительно в 30 раз и в 3 раза соответственно больше, чем коммерчески доступных аналогов. Более высокое среднее время удерживания (СВУ) и меньшая скорость очистки предполагает большее время обработки опухоли указанными новыми производными, что может указывать на возможность увеличения хемотерапевтического эффекта.
Через липофильную модификацию терапевтических лекарственных соединений полупериод элиминирования плазмы исходного терапевтического лекарственного соединения может быть увеличен. Соединения по изобретению, благодаря достоинствам липофильного фрагмента (например, фрагмента токоферола), имеют увеличенный полупериод элиминирования плазмы по сравнению с исходными терапевтическими препаратами. Как показано выше, для токоферолсукцината камптотецина и токоферолсукцината 7-этил-10-гидроксикамптотецина полупериод элиминирования плазмы значительно возрастает по сравнению с исходными соединениями.
ПРИМЕР 19
In vivo противоопухолевая активность типичных токоферол-модифицированных терапевтических лекарственных соединений в ксенотрансплантатах опухоли человека
В данном примере in vivo противоопухолевую активность типичных токоферол-модифицированных терапевтических лекарственных соединений по изобретению токоферолсукцинат камптотецина и токоферолсукцинат 7-этил-10-гидроксикамптотецина сравнивали с противоопухолевым эффектом иринотекана.
NCI-H460 ксенотрансплантат опухоли человека. Атимичным мышам подкожно имплантировали клеточную суспензию (107 клеток/мышь). Когда опухоли достигали соответствующего размера, животных рандомизировали в группы по восемь и внутривенно вводили следующие соединения с дозой 15 мг лекарственного соединения/кг массы тела по схеме q1dx5 в течение двух последующих недель:
Солевая-контрольная группа
Иринотекан
SN2300 эмульсия
SN2310 эмульсия
HT-29 ксенотрансплантат опухоли человека. Атимичным мышам подкожно имплантировали 30-40 мг фрагментов опухоли с использованием троакарных игл 12-размера. Достаточное количество мышей, имплантированных фрагментами опухоли в узком весовом интервале (100-200 мг), выбрали для испытания в установочный день (УД). Животные, отобранные с опухолями в соответствующем интервале по размеру, рандомизировали в шесть групп по 10 животных и им подкожно ввели следующие тестовые соединения:
В обоих исследованиях ксенотрансплантации массу тела животного и опухоли измеряли дважды в неделю после дозирования. Измерения опухоли проводили с использованием циркуля (миллиметры); объем опухоли рассчитывали на основании формулы: (длина × ширина2)/2 = объем (мм3).
Противоопухолевый эффект SN2300 и SN2310 эмульсий, введенных атимичным мышам с имплантированными NCI-H460 клетками опухоли человека и HT-29 клетками опухоли человека, графически представлен на ФИГУРАХ 15А и 15В соответственно. Хотя эмульсия SN2300 показала в данной модели слабый противоопухолевый эффект или его отсутствие, эмульсия SN2310 показала существенный противоопухолевый эффект по сравнению как с солевым контрольным раствором, так и с иринотеканом.
Рассчитанные параметры отклика для HT-29 изучения ксенотрансплантации представлены в Таблице 4. Через пятьдесят пять дней после введения дозы 30% мышей контрольной группы были умерщвлены по причине размера опухоли (>4000 мм3) и средний размер опухоли составил 3136 мм3. В это же самое время у 80% мышей в группе SN2310 (q3dx10) оказались неизмеримые опухоли. Кроме того, группа SN2310(q1dx5) имела средний размер опухоли 126 мм3 с 40% имеющих неизмеримые опухоли. В то же самое время в группе иринотекана средний размер опухоли составил 1637 мм3. Результаты показывают на то, что введение SN2310 вызывает значительную противоопухолевую активность.
Рассчитанные параметры опухолевого отклика из изучения HT-29 ксенотрансплантации
(дни)
роста
опухоли
(%Т/С)
животных с неизмеримой опухолью
на 55 день
(2 недели)
(2 недели)
(2 недели)
(2 недели)
В то время как был проиллюстрирован и описан предпочтительный вариант осуществления изобретения, следует иметь в виду, что различные изменения могут быть проведены без выхода за рамки идеи и рамки изобретения.
Варианты осуществления изобретения, в которых заявляются исключительная собственность или преимущество, определены как следующее.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОМЕЖУТОЧНОЕ СОЕДИНЕНИЕ КОНЪЮГАТА АНТИТЕЛО-ЛЕКАРСТВЕННОЕ СРЕДСТВО, СОДЕРЖАЩЕЕ SN38, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2022 |
|
RU2840789C2 |
| ПРОИЗВОДНЫЕ КАМПТОТЕЦИНА И ИХ ПРИМЕНЕНИЕ | 2007 |
|
RU2411244C2 |
| КАРБОЦИКЛИЧЕСКИЕ АНАЛОГИ 20(S)-КАМПТОТЕЦИНА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ЛЕЧЕНИЯ | 1997 |
|
RU2200163C2 |
| НАЦЕЛЕННЫЕ НА БЕЛКИ СОЕДИНЕНИЯ, ИХ КОМПОЗИЦИИ, СПОСОБЫ И ПРИМЕНЕНИЯ | 2016 |
|
RU2694895C2 |
| СИСТЕМЫ ДОСТАВКИ ДЛЯ КОНТРОЛИРУЕМОГО ВЫСВОБОЖДЕНИЯ ЛЕКАРСТВЕННОГО СРЕДСТВА | 2016 |
|
RU2748992C2 |
| ИНГИБИТОРЫ ПРОЛИЛГИДРОКСИЛАЗЫ | 2010 |
|
RU2518071C2 |
| ПРОИЗВОДНЫЕ ТЕТРАГИДРОНАФТАЛИНА И ТЕТРАГИДРОИЗОХИНОЛИНА В КАЧЕСТВЕ РАЗРУШИТЕЛЕЙ ЭСТРОГЕНОВОГО РЕЦЕПТОРА | 2017 |
|
RU2797244C2 |
| КОНЪЮГАТЫ ЭТОПОЗИДА И ДОКСОРУБИЦИНА ДЛЯ ДОСТАВКИ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2009 |
|
RU2531591C2 |
| СОЕДИНЕНИЯ ДЛЯ ЛЕЧЕНИЯ ОПОСРЕДОВАННЫХ КОМПЛЕМЕНТОМ НАРУШЕНИЙ | 2015 |
|
RU2703995C2 |
| НОВЫЙ КЛАСС ПРОТИВОВИРУСНЫХ СРЕДСТВ | 2021 |
|
RU2827993C2 |

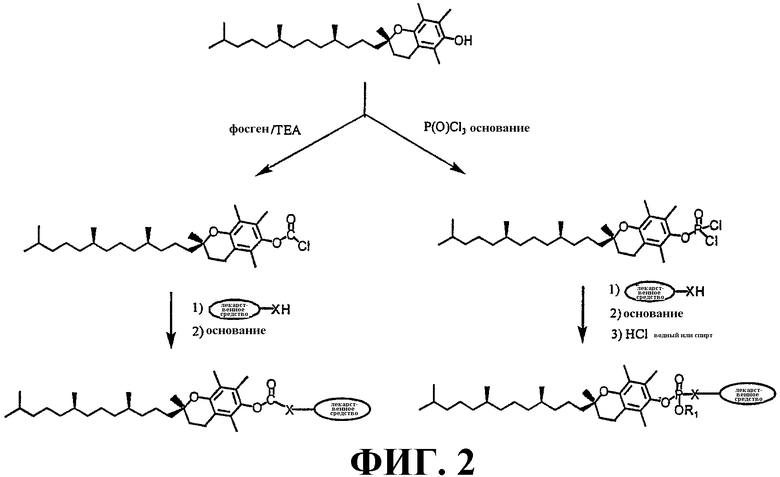

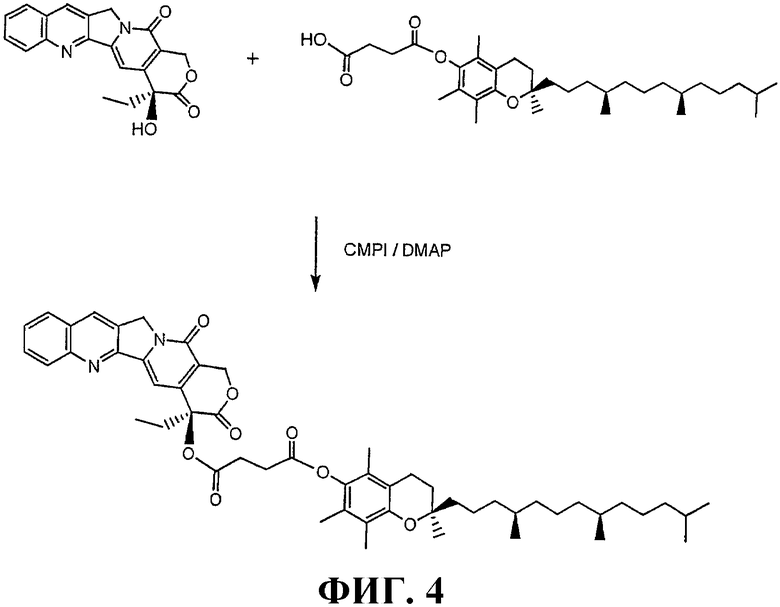
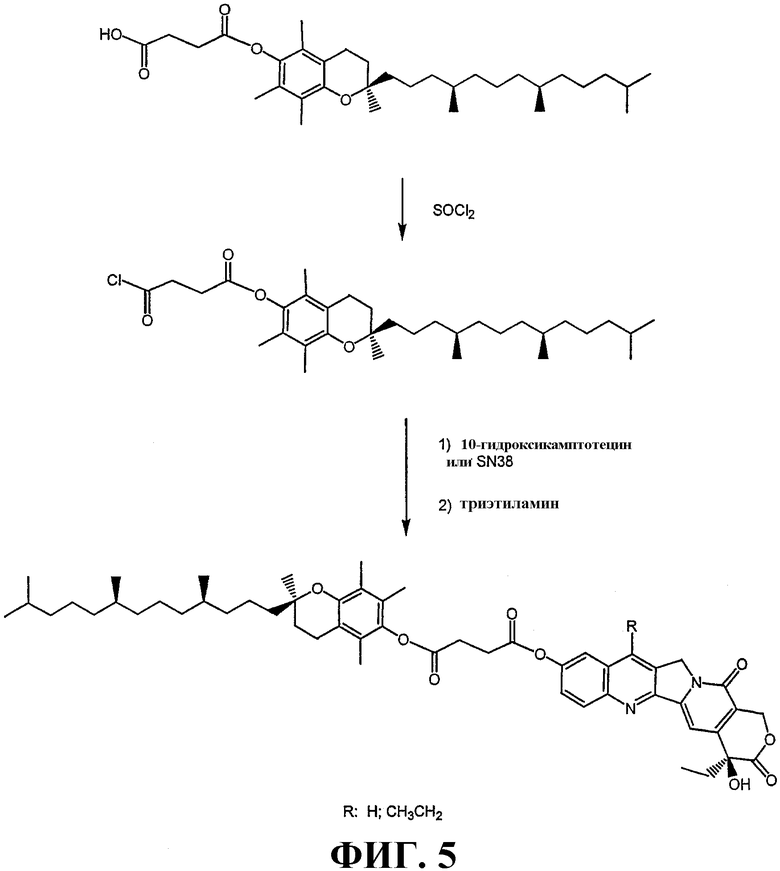
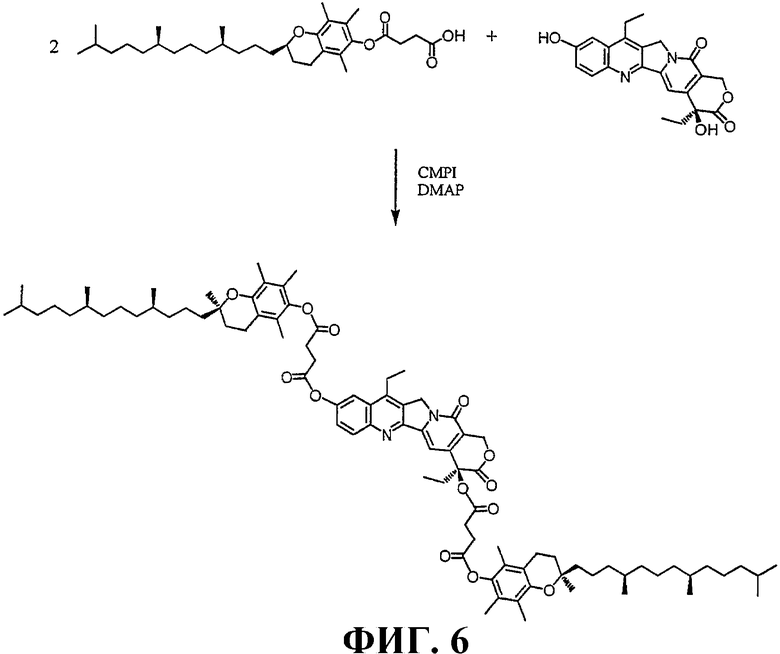
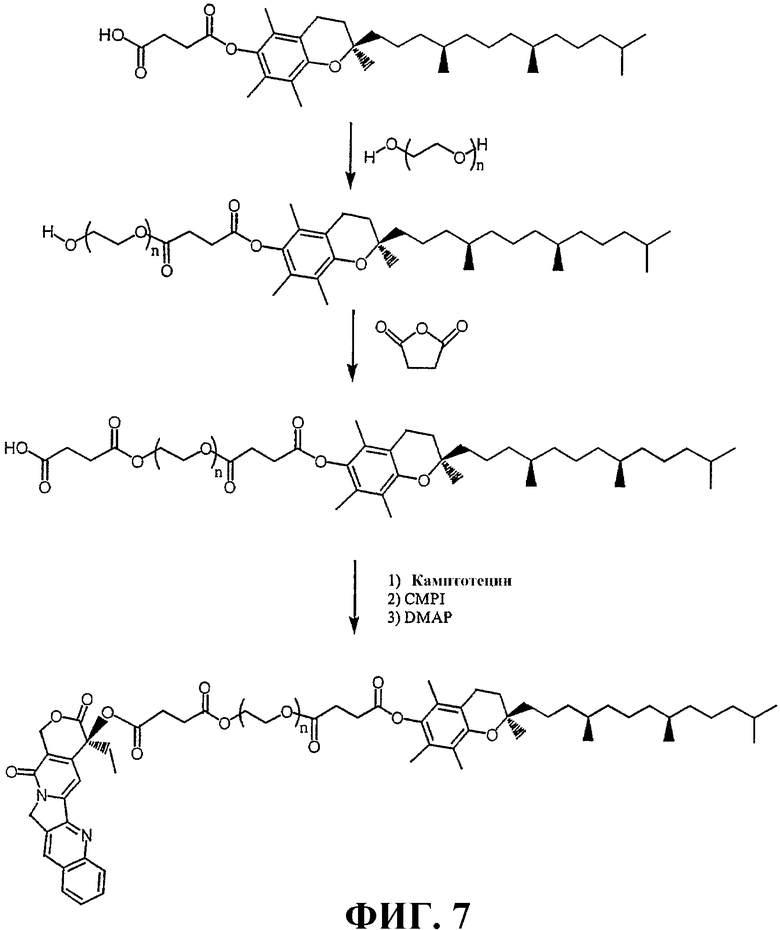

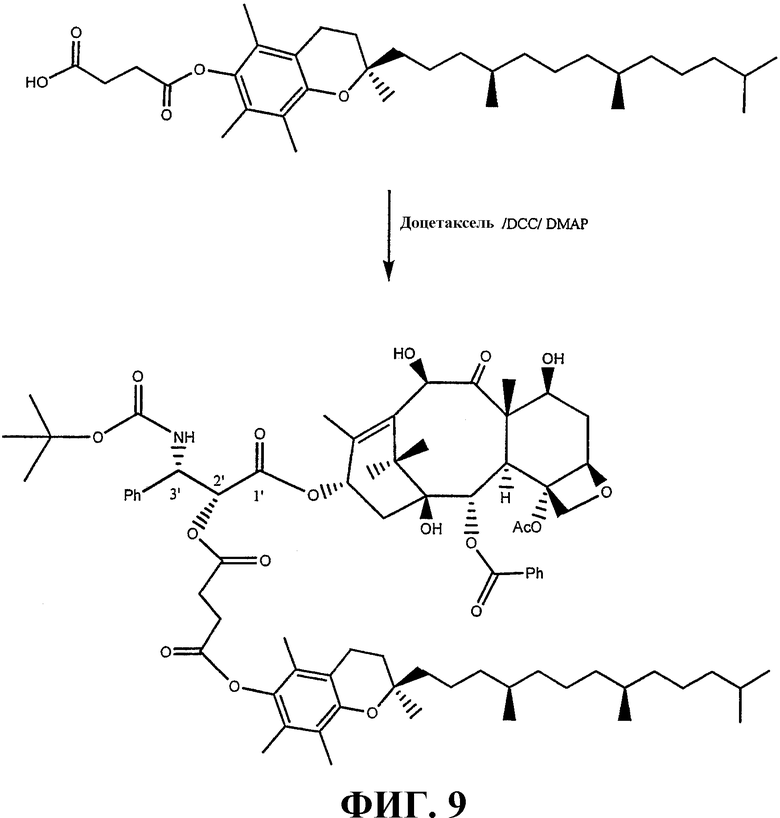



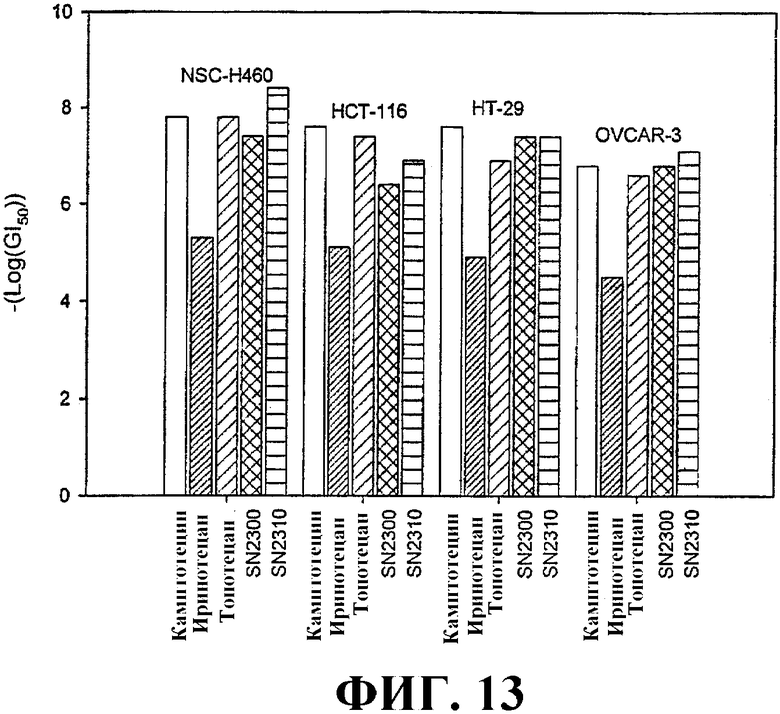
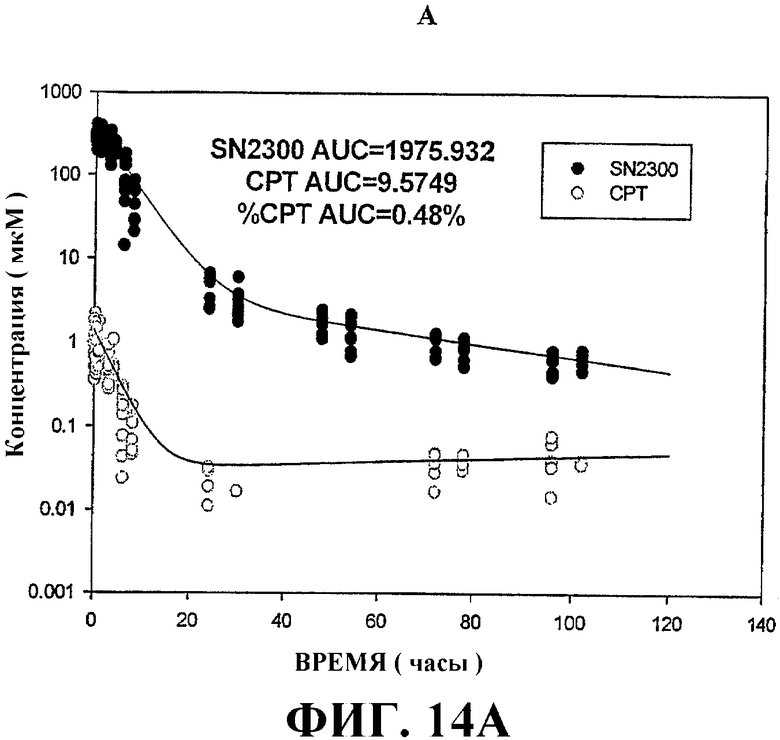

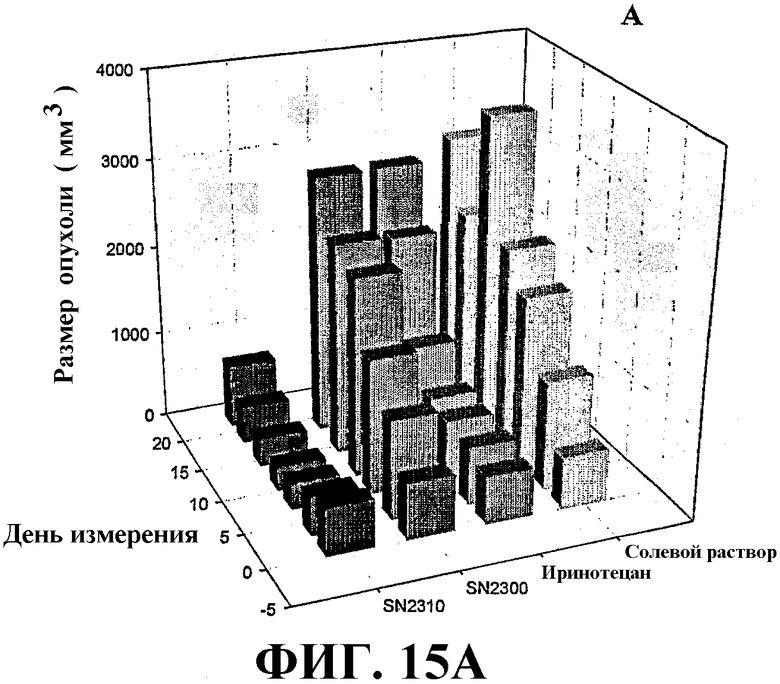
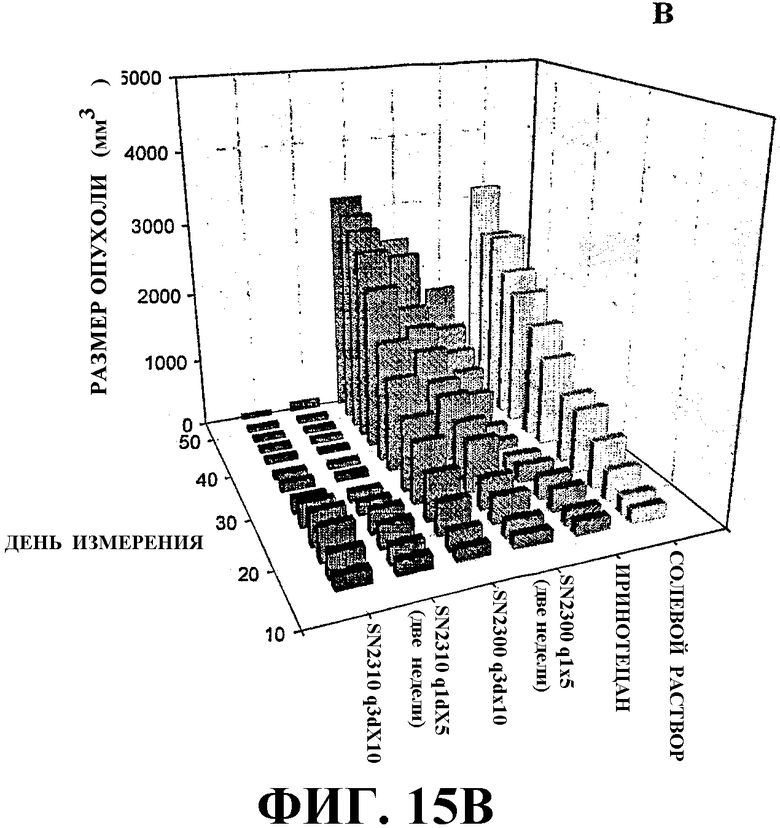
Изобретение относится к новым токоферол-модифицированным терапевтическим лекарственным соединениям формулы 1 T-L-D, в которой Т представляет собой токоферол, L представляет собой сукцинат, и D представляет собой камптотецин или его производное, где все три фрагмента ковалентно соединены. Изобретение также относится к эмульсиям на основе этих соединений, рецептурам мицелл, которые включают эти соединения, способам лечения клеточной пролиферативной болезни с использованием этих соединений и рецептур, а также к применению этих соединений для получения лекарственного средства для лечения клеточной пролиферативной болезни. 12 н. и 6 з.п. ф-лы, 17 ил., 4 табл.
T-L-D,
в которой Т представляет собой токоферол,
L представляет собой сукцинат, и
D представляет собой камптотецин или его производное,
где все три фрагмента ковалентно соединены.
(а) масляную фазу, содержащую
(i) соединение, имеющее формулу
T-L-D,
в которой Т представляет собой токоферол,
L представляет собой сукцинат, и
D представляет собой камптотецин или его производное,
где все три фрагмента ковалентно соединены,
(ii) липофильную среду; и
(b) водную фазу.
(a) соединение, имеющее формулу
T-L-D,
в которой Т представляет собой токоферол,
L представляет собой сукцинат, и
D представляет собой камптотецин или его производное,
где все три фрагмента ковалентно соединены, и
(b) водную фазу.
T-L-D,
в которой Т представляет собой токоферол,
L представляет собой сукцинат, и
D представляет собой камптотецин или его производное,
где все три фрагмента ковалентно соединены.
T-L-D,
в которой Т представляет собой токоферол,
L представляет собой сукцинат, и
D представляет собой доцетаксел,
где токоферол ковалентно соединен с доцетакселом через сукцинатный фрагмент.
(a) масляную фазу, содержащую
(i) соединение, имеющее формулу
T-L-D,
в которой Т представляет собой токоферол,
L представляет собой сукцинат, и
D представляет собой доцетаксел,
где токоферол ковалентно соединен с доцетакселом через сукцинатный фрагмент,
(ii) липофильную среду; и
(b) водную фазу.
T-L-D,
в которой Т представляет собой токоферол,
L представляет собой сукцинат, и
D представляет собой доцетаксел,
где токоферол ковалентно соединен с доцетакселом через сукцинатный фрагмент.
Приоритет от 29.10.2003 по пп.1-9, 11, 14-18
от 26.10.2004 по пп.10 и 13.
| Способ соединения электрических проводов | 1947 |
|
SU71163A1 |
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ПЛОСКОЙ УПЛОТНИТЕЛЬНОЙ ПРОКЛАДКИ ИЗ РАСШИРЕННОГО ГРАФИТА | 1994 |
|
RU2076970C1 |
| Бесколесный шариковый ход для железнодорожных вагонов | 1917 |
|
SU97A1 |
| Оправка для изготовления стеклопластиковых труб | 1961 |
|
SU140961A1 |
| Электрический нагревательный прибор для размягчения сургуча | 1927 |
|
SU8573A1 |
| XINLI LIU ET AL, JACS, 2002, v.124, p.7650-7651 | |||
| ОПТИЧЕСКИ АКТИВНЫЕ ПРОИЗВОДНЫЕ БЕНЗОПИРАНА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И СПОСОБ ЛЕЧЕНИЯ ЧУВСТВИТЕЛЬНЫХ К ЭСТРОГЕНАМ ЗАБОЛЕВАНИЙ | 1996 |
|
RU2220143C2 |
Авторы
Даты
2008-12-10—Публикация
2004-10-29—Подача