Изобретение относится к области медицины и фармацевтической промышленности и касается состава и способа получения комбинированного средства для лечения заболеваний суставов на основе растительного экстракта, местного анестетика и раствора димексида.
Болезни суставов (артриты различной этиологии, артрозы, остеохондрозы, спондилезы и др.) широко распространены и трудноизлечимы. В основе этих заболеваний лежит нарушение обмена веществ и воспалительный процесс в суставах, сопровождающийся разрушением суставного хряща, обнажением костной ткани, нарушением конгруэнтности суставных поверхностей и болевым синдромом.
Современный арсенал лекарственных средств, применяемых при этих заболеваниях, направлен на подавление воспаления, восстановление разрушенной хрящевой ткани, нормализацию обменных процессов в синовиальной жидкости, а также общую и местную анальгезию болевого синдрома.
Известны средства для лечения заболеваний суставов, полученные на основе диметилсульфооксида (ДМСО), а также его фармацевтического аналога (более высокой степени очистки) - димексида. ДМСО используется в качестве средо- и формообразующего вещества, а также как мембранопротекторное, трансдермальное средство. В качестве активного компонента в таких препаратах применяют биогенные глюкозамины [Патент RU №2271811] и их смеси с хондроитин сульфатом [Патент RU №2271812]; комбинацию хонсурида с даларгином [Патент RU №2088239]; лактоферрины женского молока [Патент RU №2088238], а также сочетание противомикробных и противовоспалительных (кортикостероидных) веществ [Патент RU №2088216]. Средства, обладающие противовоспалительным, репаративным и местноанестезирующим действием, получают, комбинируя ДМСО с новокаином [Патент RU №2142811], а также смесью прополиса с новокаином и анестезином [Патент RU №2261720].
Наиболее близким техническим решением задачи является изобретение, описанное в патенте RU №2271811 от 2006 года, поскольку оно также направлено на лечение той же патологии - заболеваний суставов - и взято нами за прототип. Содержит глюкозамина соль, диметилсульфоксид и различные типы основ, используемых для получения мазей, гелей, линиментов, кремов, паст. В качестве основ применяется смесь безводного ланолина и вазелина, низко- и высокомолекулярные полиэтиленоксиды, натрийкарбоксиметилцеллюлоза, карбопол-940.
Недостатками прототипа являются следующие положения:
1. В препарате отсутствуют компоненты, обладающие целенаправленным обезболивающим и противовоспалительным действием. Слабый анальгетический и противовоспалительный эффект обусловлен присутствием в препарате только диметилсульфоксида в концентрации 1-20%.
2. Препарат не содержит компонентов, обладающих Р-витаминным действием (растительных фенолов - флавоноидов, катехинов, кумаринов), нормализующих сосудистый тонус артерий и вен, а также улучшающих кровоснабжение сустава.
3. В качестве основного действующего вещества в препарате используется хлористоводородные и сернокислые соли глюкозамина, которые создают кислую среду (рН 1,5-4,0), для нейтрализации которой необходимо использовать щелочные компоненты (натрия гидроксид или замещенные алкиламины).
4. В изобретении отсутствуют селективные методы анализа компонентов препарата при совместном присутствии.
Задачей изобретения является состав и способ получения средства для лечения заболеваний суставов, компонентами которого являются растительный экстракт, местный анестетик и димексид.
Задача достигается тем, что в качестве растительного источника биологически активных веществ используются сухие экстракты из растений семейства Норичниковые (Scrophulariaceae) - очанки коротковолосистой и зубчатки обыкновенной, полученные в одинаковых условиях по разработанному нами способу [Патент RU №2220735]. Экстракты очанки коротковолосистой и зубчатки обыкновенной содержат большой набор биологически активных веществ (флавоноиды, иридоиды, фенолокислоты и др.) и обладают довольно сильным противовоспалительным и Р-витаминным действием, что делает их целесообразными компонентами для включения в комплексный препарат [Петриченко В.М., Сухинина Т.В., Шрамм Н.И. и др. Технология получения и фармакологические свойства сухого экстракта из травы очанки коротковолосистой В.М.Петриченко, Т.В.Сухинина, Н.И.Шрамм, Л.К.Бабиян, В.В.Юшков // Химико-фармацевтический журнал, 2005, Т. 39, №3. - с.33-36., Патент RU №2160598].
Обезболивающий эффект в препарате обуславливается анестетиком отечественного производства - анилокаином, сочетающим в себе высокую анестезирующую активность с умеренным противовоспалительным действием [Панцуркин В.В., Алексеева И.В. Анилокаин, поиск, свойства. Начальный опыт применения лекарственных форм в медицинской практике / В.В.Панцуркин, И.В.Алексеева. - Пермь: ГОУ ВПО «ПГФА Росздрава», 2006. - 174 с.].
В качестве растворителя и средообразующего вещества используется смесь димексида и воды очищенной (1:1) в терапевтической концентрации [Машковский М.Д. Лекарственные средства. - М.: Медицина, 1993, T.1, с.222], что позволяет сразу получать препарат, готовый к употреблению. Димексид является универсальным растворителем, растворяющим как липофильные, так и гидрофильные вещества, обладает проводниковой активностью и способствует проведению биологически активных веществ, содержащихся в растительных экстрактах, и анилокаина внутрь сустава. Кроме того, он обладает умеренным противовоспалительным и анальгезирующим действием.
Сущность изобретения: 10 г сухого экстракта из травы растений семейства Норичниковые, полученного по способу [Патент RU 2220735], растворяют в 85 г смеси димексида (ФС 42-2980-98) и воды очищенной, в соотношении 1:1 в плоскодонной колбе при температуре 100°С в течение 15 мин, при перемешивании. Раствор охлаждают до комнатной температуры, добавляют 5 г анилокаина (ВФС 42-2846-97) и растворяют в течение 5 мин, при легком перемешивании. Жидкость процеживают через три слоя марли и получают готовый препарат. Изобретение иллюстрируют следующими примерами:
Пример 1. 10 г сухого экстракта из травы очанки коротковолосистой (Euphrasia brevipila Bumat et Gremli) растворяют в 85 г смеси димексида и воды очищенной, взятых в соотношении 1:1, в плоскодонной колбе при температуре 100°С в течение 15 мин, при перемешивании. Раствор охлаждают до комнатной температуры, добавляют 5 г анилокаина и растворяют в течение 5 мин, при легком перемешивании. Жидкость процеживают через три слоя марли и получают готовый препарат.
Пример 2. 10 г сухого экстракта из травы зубчатки обыкновенной (Odontites vulgaris Moench) растворяют в 85 г смеси димексида и воды очищенной, взятых в соотношении 1:1, в плоскодонной колбе при температуре 100°С в течение 15 мин, при перемешивании. Раствор охлаждают до комнатной температуры, добавляют 5 г анилокаина и растворяют в течение 5 мин, при легком перемешивании. Жидкость процеживают через три слоя марли и получают готовый препарат.
Препараты, полученные способом, описанным в примерах 1 и 2, представляют собой прозрачную жидкость, коричневого цвета, специфического запаха (запах ДМСО), смешивается с водой и спиртом этиловым в любых соотношениях.
Параметры стандартизации препаратов
Подлинность препаратов подтверждается качественными реакциями (табл.1), хроматографическими пробами (табл.2) и УФ-спектральными характеристиками (табл.3).
1. Реакции подлинности на содержание биологически активных веществ растений и анилокаина:
а) Флавоноидов
К 1 мл препарата добавляют 1 мл воды очищенной, 10 мг кристаллического магния и 5 капель кислоты хлористоводородной концентрированной, нагревают на кипящей водяной бане 3 мин, появляется черно-синее или черно-коричневое окрашивание (проба Синода).
б) Иридоидов
К 1 мл препарата добавляют 1 мл воды очищенной и 5 капель реактива Трим-Хилла (смесь, состоящая из 5 мл концентрированной кислоты хлористоводородной, 10 мл 0,2% раствора меди сульфата и 100 мл кислоты уксусной ледяной), нагревают на кипящей водяной бане в течение 10 мин, появляется темно-синее окрашивание.
К 1 мл препарата добавляют 1 мл воды очищенной и 5 капель реактива Шталя (смесь 1 г п-диметиламинобензальдегида, 5 г кислоты фосфорной и 50 г кислоты уксусной ледяной, разбавленная водой до 100 мл), доводят до кипения на водяной бане, появляется синее окрашивание.
в) Фенолкарбоновых кислот
К 1 мл препарата добавляют 1 мл воды очищенной и 5 капель 1% водного раствора квасцов железоаммониевых, нагревают на кипящей водяной бане в течение 5 мин, появляется осадок темно-коричневого цвета.
г) Анилокаина
К 1 мл препарата добавляют 1 мл воды очищенной и 5 капель 10% водного раствора натрия гидроксида, нагревают на кипящей водяной бане 1 мин, выпадает осадок темно-коричневого цвета.
Специфичность проб подлинности подтверждается реакциями на модельной смеси, состоящей из водного раствора димексида с анилокаином, взятых в одинаковых с препаратом пропорциях (табл.1).
2. Хроматографическая характеристика флавоноидов
На лист хроматографической бумаги марки «Ленинградская - С» размером 30×40 см наносят 0,1 мл препарата и хроматографируют в стеклянной камере восходящим методом в системе растворителей бутанол - кислота уксусная - вода (4:1:2) в течение 17 часов (первое направление). Хроматограмму вынимают из камеры, высушивают, поворачивают на 90° таким образом, чтобы флавоноиды, распределившиеся в первом направлении, были внизу, помещают в камеру с 15% раствором кислоты уксусной, где выдерживают в течение 8 часов (второе направление). По истечении времени хроматограмму вынимают из камеры, высушивают и просматривают в УФ-свете до и после обработки парами аммиака, а также обрабатывают хромогенными реактивами - 1% спиртовым раствором алюминия хлорида и 3% спиртовым раствором цирконила нитрата. Результаты хроматографического анализа представлены в таблице 2.
На основании люминесцентно-хроматографических свойств и реакций с хромогенными реактивами установлено, что в препарате с экстрактом очанки коротковолосистой содержится семь, а с экстрактом зубчатки обыкновенной шесть веществ флавоноидной природы. Значение коэффициентов распределения (Rf) этих веществ служит показателем подлинности препаратов.
3. УФ-спектральная характеристика
УФ-спектры препаратов в разведении 1:2000 представлены в таблице 3. Как следует из полученных данных, в УФ-спектрах препаратов с экстрактами очанки и зубчатки присутствует по два максимума - общий коротковолновый 226 нм и длинноволновые 326 и 320 нм соответственно. При добавлении хромогенного реактива (AlCl3) наблюдается батохромный сдвиг обоих максимумов поглощения, причем в коротковолновой области он незначителен, а в длинноволновой более существенен - в препарате с экстрактом очанки λмакс составляет 332 нм, а с экстрактом зубчатки - 331 нм. Изменения в УФ-спектрах подтверждают наличие флавоноидов в препаратах и участие их в реакциях комплексообразования.
Совместное добавление комплексообразующего (AlCl3) и ионизирующего (CH3COONa) агентов за счет сольватационных эффектов приводит к еще более значительному батохромному сдвигу длинноволнового максимума.
В дифференциальных спектрах препаратов с алюминия хлоридом и натрия ацетатом присутствует также по два максимума. Длинноволновые максимумы 387 (препарат с экстрактом очанки) и 382 нм (препарат с экстрактом зубчатки) находятся в области спектра, свободной от поглощения простых фенольных соединений (простых фенолов, гидроксикоричных кислот, кумаринов и др.), и могут использоваться как для подтверждения подлинности, так и для разработки методов количественного определения флавоноидов в препаратах.
4. Количественное определение флавоноидов
В мерную колбу вместимостью 100 мл помещают 0,5 г препарата (точная навеска), доводят до метки водой очищенной (раствор А). 5 мл раствора А помещают в мерную колбу вместимостью 50 мл, добавляют 2 мл 2% спиртового раствора алюминия хлорида и 2 мл 8% спиртового раствора натрия ацетата, доводят объем раствора до метки водой очищенной, через 30 мин измеряют оптическую плотность на спектрофотометре СФ-2000 (или другой марки) при длине волны 387 нм (препарат с экстрактом очанки) или 382 нм (препарат с экстрактом зубчатки) в кювете с толщиной слоя 10 мм. В качестве раствора сравнения используют раствор, состоящий из 5 мл раствора А, доведенного водой очищенной до метки в мерной колбе объемом 50 мл.
Содержание флавоноидов в % (X) в пересчете на цинарозид вычисляют по формуле:
 ,
,
где D - оптическая плотность исследуемого раствора; Е1% 1см - удельный показатель поглощения комплекса цинарозида с реактивами при λ387=403; при λ382=357; а - точная навеска препарата, г.
Содержание флавоноидов в препарате с экстрактом очанки коротковолосистой составляет 1,04±0,01%, а с экстрактом зубчатки обыкновенной 0,50±0,08%.
5. Содержание димексида
Концентрация димексида в препаратах определяется по значению плотности. Нами установлена линейная зависимость плотности от концентрации димексида в модельной смеси и препаратах, включающих сухие экстракты с влажностью 5%, в интервале 20-60% (табл.4). Рассчитаны уравнения линейной регрессии, описывающие эти зависимости. Учитывая одинаковые значения угловых коэффициентов (0,0015) в уравнениях, рассчитана формула для количественной оценки содержания димексида в препаратах. Для расчета использовалось среднее значение плотности препаратов, приготовленных на основе сухих экстрактов очанки коротковолосистой и зубчатки обыкновенной.
Количественное содержание димексида в % (X) в препаратах с экстрактами очанки коротковолосистой и зубчатки обыкновенной находят по формуле:
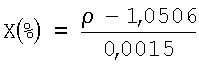 ,
,
где ρ - плотность препарата, г/см3.
Содержание димексида в препаратах составляет 50,0±5,0%
6. Физико-химические параметры
Значение плотности, показателя преломления и сухого остатка препаратов устанавливаются по методикам ГФ XI [Государственная фармакопея СССР, вып.1, М., 1987, 336 с.] и представлены в таблице 5.
7. Фармакологическая активность
Оценку противовоспалительной активности препаратов проводили на беспородных крысах обоего пола, массой 180-200 г, по общепринятой методике [Методические рекомендации по экспериментальному (доклиническому) изучению нестероидных противовоспалительных фармакологических веществ. Одобрено фармакологическим комитетом МЗ СССР, 1982].
Асептическое воспаление конечностей вызывали субплантарным введением в правую заднюю лапу крысы 0,1 мл 1% раствора карагенина. Препараты вводили перорально и внутрибрюшинно, в дозе 50 мл/кг в 1 мл воды, очищенной за один час до моделирования воспаления. В качестве препарата сравнения использовали индометацин в дозе 10 мг/кг. Животным контрольной группы в равном объеме вводили воду очищенную. Через 1 и 3 часа после введения карагенина определяли величину отека онкометрическим методом, по разности между объемами воспаленной и невоспаленной лапок животных. Статистическую обработку данных фармакологического эксперимента проводили по критерию Стьюдента. Эффект считали достоверным при р≤0,05 [Беленький М.Л. Элементы количественной оценки фармакологического эффекта, 2-е изд.. Л.: Медицинская литература, 1963]. Для подтверждения фармакологической активности заявленного состава на противовоспалительную активность испытаны модельные растворы димексида и его смеси с анилокаином в концентрациях, идентичных препаратам.
Как следует из полученных данных (табл.6), препараты с экстрактами растений семейства Норичниковые проявляют противовоспалительное действие. Наибольший эффект наблюдается при внутрибрюшинном введении у препарата с экстрактом зубчатки. Препарат вызывает статистически достоверное торможение отека через 1 час на 39%, а через 3 часа на 42%. У препарата с экстрактом очанки эффект несколько ниже - 10 и 30%, через 1 и 3 часа соответственно. При пероральном введении также наблюдается противовоспалительное действие, однако эффект не достоверен и на пике воспаления составляет примерно 25%.
Модельные препараты в аналогичных условиях вызывают незначительное торможение воспалительного отека. Противовоспалительный эффект раствора димексида (50%) с анилокаином при внутрибрюшинном и пероральном введении находится в пределах 7-14% и является статистически не достоверным. Раствор димексида в воде (50%) на данной модели воспаления практически не проявляет антиотечного действия при обоих путях введения.
8. Сравнение с прототипом
Сравнительная характеристика заявленного состава средства и способа его получения с прототипом представлена в таблице 7.
Состав средства существенно отличается от прототипа, так как содержит компоненты, обладающие целенаправленным обезболивающим и Р-витаминным действием. Противовоспалительный эффект средства обусловлен комбинированным действием всех компонентов (растительных экстрактов, анилокаина, димексида - 50%).
Способ получения средства исключает стадию нейтрализации кислых продуктов. Селективные методы стандартизации средства позволяют контролировать технологические стадии получения и стандартизовать целевой продукт.
Технический результат от использования изобретения заключается в повышении эффективности средства за счет включения в состав растительных экстрактов, местного анестетика и димексида.
Вышеуказанные преимущества в сочетании с простой схемой получения, исключающей загрязнение окружающей среды отходами производства, способствуют рациональному использованию лекарственного растительного сырья, расширяют ассортимент лекарственных средств для лечения заболеваний суставов и открывают перспективу внедрения данного средства в фармацевтическую промышленность.
Компоненты, обладающие противовоспалительным действием
Необходимость нейтрализации кислых продуктов
| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИМИКРОБНЫМ, ПРОТИВОВОСПАЛИТЕЛЬНЫМ И АНЕСТЕЗИРУЮЩИМ ДЕЙСТВИЕМ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2008 |
|
RU2396971C2 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО ПРОТИВОВОСПАЛИТЕЛЬНОЙ И ГИПОТЕНЗИВНОЙ АКТИВНОСТЬЮ | 2002 |
|
RU2220735C1 |
| УНИФИЦИРОВАННЫЙ СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ФЛАВОНОИДОВ В ТРАВЕ И ЭКСТРАКЦИОННЫХ ПРЕПАРАТАХ ОЧАНКИ | 2003 |
|
RU2266544C2 |
| СПОСОБ ПОЛУЧЕНИЯ РАСТИТЕЛЬНОГО СРЕДСТВА, ОБЛАДАЮЩЕГО АНТИКОАГУЛЯНТНЫМ, ГИПОТЕНЗИВНЫМ И ДИУРЕТИЧЕСКИМ ДЕЙСТВИЕМ | 2011 |
|
RU2504391C2 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО ЖЕЛЧЕГОННОЙ И ПРОТИВОВОСПАЛИТЕЛЬНОЙ АКТИВНОСТЬЮ | 1999 |
|
RU2160598C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО ГЕПАТОЗАЩИТНОЙ АКТИВНОСТЬЮ | 2008 |
|
RU2366445C1 |
| СПОСОБ ПОЛУЧЕНИЯ РАСТИТЕЛЬНОГО СРЕДСТВА ИЗ ТРАВЫ ЯРУТКИ ПОЛЕВОЙ, ОБЛАДАЮЩЕГО АНТИОКСИДАНТНОЙ, ПРОТИВОВОСПАЛИТЕЛЬНОЙ, АНТИКОАГУЛЯЦИОННОЙ И АНТИАГРЕГАЦИОННОЙ АКТИВНОСТЬЮ | 2024 |
|
RU2834024C1 |
| РАСТИТЕЛЬНЫЙ СБОР "ЭУФРАЗИН", ОБЛАДАЮЩИЙ АНТИОКСИДАНТНОЙ И НООТРОПНОЙ АКТИВНОСТЬЮ | 2014 |
|
RU2560077C1 |
| ГЕЛЬ ДИМЕКСИДА, ОБЛАДАЮЩИЙ ПРОТИВОВОСПАЛИТЕЛЬНЫМ ДЕЙСТВИЕМ | 2024 |
|
RU2838731C1 |
| Способ получения средства, обладающего желчегонной, противовоспалительной и антиоксидантной активностью | 2017 |
|
RU2665968C1 |
Изобретение относится к области медицины и фармацевтической промышленности и касается состава и способа получения препарата для лечения заболеваний суставов. В состав препарата входят сухие экстракты очанки коротковолосистой или зубчатки обыкновенной, местный анестетик анилокаин, средообразующее вещество и растворитель смесь димексида и воды очищенной в соотношении 1:1 при следующем соотношении компонентов: сухой экстракт 10: анилокаин 5: смесь (1:1) димексида и воды очищенной 85. Препарат получают растворением сухих экстрактов при перемешивании в смеси димексида и воды очищенной, взятых в соотношении 1:1 при температуре 100°С в течение 15 мин, а анилокаин растворяют в охлажденном до комнатной температуры растворе. Полученный состав обладает целенаправленным обезболивающим и Р-витаминным действием. 2 н.п. ф-лы, 7 табл.
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНЕЙ СУСТАВОВ | 2004 |
|
RU2271811C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНЕЙ СУСТАВОВ | 2004 |
|
RU2271812C1 |
| ПРЕПАРАТ "АНИКСИД" ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ МАСТИТА КРУПНОГО РОГАТОГО СКОТА | 1995 |
|
RU2091070C1 |
| ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 1993 |
|
RU2089205C1 |
Авторы
Даты
2009-01-10—Публикация
2007-04-09—Подача