Настоящее изобретение относится к новым производным N-[2-(2-пиридинил)этил]бензамида, к способу их получения, к их применению в качестве фунгицидов, в особенности в виде фунгицидных композиций, и к способам борьбы с фитопатогенными грибами растений с применением указанных соединений или их композиций.
В международной заявке на патент WO 01/11965 раскрыто широкое семейство фунгицидных соединений, в которых 2-пиридильная группа замещена, по крайней мере, одной галогеналкильной группой.
Для сельского хозяйства всегда представляет большой интерес применение новых пестицидов для предупреждения или для борьбы с возникновением линий грибов, устойчивых к действию применяемых земледельцем активных ингредиентов. Для сельского хозяйства также представляет большой интерес применение новых соединений, более активных по сравнению с уже известными соединениями, с целью снижения количеств необходимого для применения земледельцем активного вещества, и в то же время поддержание эффективности, по крайней мере, эквивалентной уже известным соединениям.
Авторами было обнаружено новое семейство соединений, которые обладают приведенными выше характеристиками.
Таким образом, настоящее изобретение относится к производному N-[2-(2-пиридинил)этил]бензамида общей формулы (I):
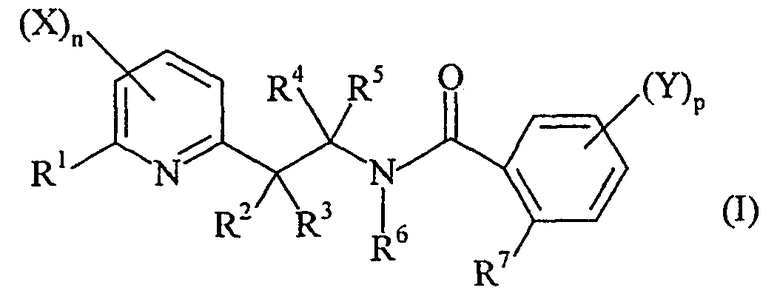
в которой:
n равно 1, 2 или 3;
X является одинаковым или различным и представляет собой атом водорода, атом галогена, нитрогруппу, цианогруппу,
гидроксигруппу, аминогруппу, сульфанильную группу,
пентафтор-λ6-сульфанильную группу, формильную группу,
формилоксигруппу, формиламиногруппу, карбоксигруппу,
карбамоильную группу, N-гидроксикарбамоильную группу,
карбаматную группу, гидроксиимино-C1-C6алкильную группу,
C1-C8алкил, C2-C8алкенил, C2-C8алкинил, C1-C8алкиламиногруппу,
ди-C1-C8алкиламиногруппу, C1-C8алкоксигруппу,
содержащую 1-5 атомов галогена C1-C8галогеналкоксигруппу,
C1-C8алкилсульфанил,
содержащий 1-5 атомов галогена C1-C8галогеналкилсульфанил,
C2-C8алкенилоксигруппу,
содержащую 1-5 атомов галогена C2-C8галогеналкенилоксигруппу,
C3-C8алкинилоксигруппу,
содержащую 1-5 атомов галогена C3-C8галогеналкинилоксигруппу,
C3-C8-циклоалкил,
содержащий 1-5 атомов галогена C3-C8-галогенциклоалкил,
C1-C8алкилкарбонил,
содержащий 1-5 атомов галогена C1-C8галогеналкилкарбонил,
C1-C8алкилкарбамоил, ди-C1-C8алкилкарбамоил,
(N-C1-C8алкил)оксикарбамоил, C1-C8алкоксикарбамоил,
(N-C1-C8алкил)-C1-C8алкоксикарбамоил, C1-C8алкоксикарбонил,
содержащий 1-5 атомов галогена C1-C8галогеналкоксикарбонил,
C1-C8алкилкарбонилоксигруппу,
содержащую 1-5 атомов галогена C1-C8галогеналкилкарбонилоксигруппу,
C1-C8алкилкарбониламиногруппу,
содержащую 1-5 атомов галогена C1-C8галогеналкилкарбониламиногруппу,
C1-C8алкиламинокарбонилоксигруппу,
ди-C1-C8алкиламинокарбонилоксигруппу,
C1-C8алкилоксикарбонилоксигруппу, C1-C8алкилсульфенил,
содержащий 1-5 атомов галогена C1-C8галогеналкилсульфенил,
C1-C8алкилсульфинил,
содержащий 1-5 атомов галогена C1-C8галогеналкилсульфинил,
C1-C8алкилсульфонил,
содержащий 1-5 атомов галогена C1-C8галогеналкилсульфонил,
(C1-C6алкоксиимино)-C1-C6алкил, (C1-C6алкенилоксиимино)-C1-C6алкил,
(C1-C6алкинилоксиимино)-C1-C6алкил, (бензилоксиимино)-C1-C6алкил,
бензилоксигруппу, бензилсульфанил, бензиламиногруппу,
феноксигруппу, фенилсульфанил или фениламиногруппу;
R1 представляет собой атом водорода, атом галогена, нитрогруппу, цианогруппу, гидроксигруппу, аминогруппу,
сульфанильную группу, пентафтор-λ6-сульфанильную группу,
формильную группу, формилоксигруппу, формиламиногруппу,
карбоксигруппу, карбамоильную группу,
N-гидроксикарбамоильную группу, карбаматную группу,
(гидроксиимино)-C1-C6алкильную группу, C1-C8алкил, C2-C8алкенил,
C2-C8алкинил, C1-C8алкиламиногруппу, ди-C1-C8алкиламиногруппу,
C1-C8алкоксигруппу,
содержащую 1-5 атомов галогена C1-C8галогеналкоксигруппу,
C1-C8алкилсульфанил,
содержащий 1-5 атомов галогена C1-C8галогеналкилсульфанил,
C2-C8алкенилоксигруппу,
содержащую 1-5 атомов галогена C2-C8галогеналкенилоксигруппу,
C3-C8алкинилоксигруппу,
содержащую 1-5 атомов галогена C3-C8галогеналкинилоксигруппу,
C3-C8циклоалкил,
содержащий 1-5 атомов галогена C3-C8галогенциклоалкил,
C1-C8алкилкарбонил,
содержащий 1-5 атомов галогена C1-C8галогеналкилкарбонил,
C1-C8алкилкарбамоил,
ди-C1-C8алкилкарбамоил, N-C1-C8алкилоксикарбамоил,
C1-C8алкоксикарбамоил, N-C1-C8алкил-C1-C8алкоксикарбамоил,
C1-C8алкоксикарбонил,
содержащий 1-5 атомов галогена C1-C8галогеналкоксикарбонил,
C1-C8алкилкарбонилоксигруппу,
содержащую 1-5 атомов галогена C1-C8галогеналкилкарбонилоксигруппу,
C1-C8алкилкарбониламиногруппу,
содержащую 1-5 атомов галогена C1-C8галогеналкилкарбониламиногруппу,
C1-C8алкиламинокарбонилоксигруппу,
ди-C1-C8алкиламинокарбонилоксигруппу,
C1-C8алкилоксикарбонилоксигруппу, C1-C8алкилсульфенил,
содержащий 1-5 атомов галогена C1-C8галогеналкилсульфенил,
C1-C8алкилсульфинил,
содержащий 1-5 атомов галогена C1-C8галогеналкилсульфинил,
C1-C8алкилсульфонил,
содержащий 1-5 атомов галогена C1-C8галогеналкилсульфонил,
(C1-C6алкоксиимино)-C1-C6алкил, (C1-C6алкенилоксиимино)-C1-C6алкил,
(C1-C6алкинилоксиимино)-C1-C6алкил, (бензилоксиимино)-C1-C6алкил,
бензилоксигруппу,
необязательно замещенный 1-5 атомами галогена бензилсульфанил,
бензиламиногруппу, феноксигруппу,
необязательно замещенный 1-5 атомами галогена фенилсульфанил или
фениламиногруппу;
при условии, что X и R1 оба не являются атомом водорода;
R2 и R3 являются одинаковыми или различными и представляют собой атом водорода, атом галогена, цианогруппу, гидроксигруппу, C1-C6алкил, содержащий 1-5 атомов галогена C1-C6галогеналкил, C2-C6алкенил, C1-C6алкоксигруппу, C1-C6алкилсульфанил, C1-C6алкилсульфенил, C1-C6алкилсульфинил, C1-C6алкоксикарбонил, C1-C6алкилкарбонилоксигруппу или C1-C6алкилкарбониламиногруппу;
или R2 и R3 могут вместе образовывать 3-, 4-, 5- или 6-членный карбоцикл;
R4 и R5 являются одинаковыми или различными и представляют собой атом водорода, атом галогена, цианогруппу, C1-C6алкил или содержащий 1-5 атомов галогена C1-C6галогеналкил;
или R4 и R5 могут вместе образовывать 3-, 4-, 5- или 6-членный карбоцикл;
R6 представляет собой атом водорода, цианогруппу, формильную группу, гидроксигруппу, C1-C6алкил, содержащий 1-5 атомов галогена C1-C6галогеналкил, C1-C6алкоксигруппу, содержащую 1-5 атомов галогена C1-C6галогеналкоксигруппу, C3-C6-циклоалкил, содержащий 1-5 атомов галогена C3-C6-галогенциклоалкил, C2-C6алкенил, C2-C6алкинил, C1-C6алкокси-C1-C6алкил, C1-C6-цианоалкил, C1-C6-аминоалкил, C1-C6алкиламино-C1-C6алкил, ди-C1-C6алкиламино-C1-C6алкил, C1-C6алкилкарбонил, содержащий 1-5 атомов галогена C1-C6галогеналкилкарбонил, C1-C6алкилоксикарбонил, C1-C6-бензилоксикарбонил, C1-C6алкокси-C1-C6алкилкарбонил, C1-C6алкилсульфонил или содержащий 1-5 атомов галогена C1-C6галогеналкилсульфонил;
p равно 1, 2, 3 или 4;
Y является одинаковым или различным и представляет собой атом водорода, атом галогена, нитрогруппу, цианогруппу,
гидроксигруппу, аминогруппу, сульфанильную группу,
пентафтор-λ6-сульфанильную группу, формильную группу,
формилоксигруппу, формиламиногруппу, карбоксигруппу, C1-C8алкил,
содержащий 1-5 атомов галогена C1-C8галогеналкил, C2-C8алкенил,
C2-C8алкинил, C1-C8алкиламиногруппу, ди-C1-C8алкиламиногруппу,
C1-C8алкоксигруппу,
содержащую 1-5 атомов галогена C1-C8галогеналкоксигруппу,
C1-C8алкокси-C2-C8алкенил, C1-C8алкилсульфанил,
содержащий 1-5 атомов галогена C1-C8галогеналкилсульфанил,
C1-C8алкоксикарбонил,
содержащий 1-5 атомов галогена C1-C8галогеналкоксикарбонил,
C1-C8алкилкарбонилоксигруппу,
содержащую 1-5 атомов галогена C1-C8галогеналкилкарбонилоксигруппу,
C1-C8алкилсульфенил,
содержащий 1-5 атомов галогена C1-C8галогеналкилсульфенил,
C1-C8алкилсульфинил,
содержащий 1-5 атомов галогена C1-C8галогеналкилсульфинил,
C1-C8алкилсульфонил,
содержащий 1-5 атомов галогена C1-C8галогеналкилсульфонил или
C1-C8алкилсульфонамид; и
R7 представляет собой атом галогена, нитрогруппу,
цианогруппу, аминогруппу, сульфанильную группу,
пентафтор-λ6-сульфанильную группу, формильную группу,
формилоксигруппу, формиламиногруппу, карбоксигруппу, C1-C8алкил,
содержащий 1-5 атомов галогена C1-C8галогеналкил, C2-C8алкенил,
C2-C8алкинил, C1-C8алкиламиногруппу, ди-C1-C8алкиламиногруппу,
C1-C8алкоксигруппу,
содержащую 1-5 атомов галогена C1-C8галогеналкоксигруппу,
C1-C8алкокси-C2-C8алкенил, C1-C8алкилсульфанил,
содержащий 1-5 атомов галогена C1-C8галогеналкилсульфанил,
C1-C8алкоксикарбонил,
содержащий 1-5 атомов галогена C1-C8галогеналкоксикарбонил,
C1-C8алкилкарбонилоксигруппу,
содержащую 1-5 атомов галогена C1-C8галогеналкилкарбонилоксигруппу,
C1-C8алкилсульфенил,
содержащий 1-5 атомов галогена C1-C8галогеналкилсульфенил,
C1-C8алкилсульфинил,
содержащий 1-5 атомов галогена C1-C8галогеналкилсульфинил,
C1-C8алкилсульфонил,
содержащий 1-5 атомов галогена C1-C8галогеналкилсульфонил или
C1-C8алкилсульфонамид;
а также к его солям, N-оксидам, металлосодержащим и металлоидсодержащим комплексам.
В контексте настоящего изобретения:
- «галоген» означает фтор, бром, хлор или йод;
- «карбокси» означает -C(=O)OH, «карбонил» означает -C(=O)-, «карбамоил» означает -C (=O)NH2, «N-гидроксикарбамоил» означает -C(=O)NHOH;
- алкильная группа, алкенильная группа и алкенильная группа, а также фрагменты, включающие эти термины, могут быть неразветвленными или разветвленными.
В контексте настоящего изобретения также следует понимать, что в случае дизамещенных амино- и дизамещенных карбамоильных радикалов два заместителя вместе с атомом азота, на котором они находятся, могут образовывать насыщенное гетероциклическое кольцо, содержащее 3-7 атомов.
Любое соединение по настоящему изобретению может существовать в одной или нескольких формах оптических или хиральных изомеров, в зависимости от числа асимметрических центров в соединении. Поэтому настоящее изобретение в равной степени относится ко всем оптическим изомерам и к их рацемическим или scalemic смесям (термин «scalemic» обозначает смесь энантиомеров в различных пропорциях), и к смесям всех возможных стереоизомеров во всех пропорциях. Диастереоизомеры и/или оптические изомеры могут быть разделены в соответствии с методами, известными per se обычному специалисту в данной области.
Любое соединение по настоящему изобретению может также существовать в одной или нескольких формах геометрических изомеров, в зависимости от числа двойных связей в соединении. Поэтому настоящее изобретение в равной степени относится ко всем геометрическим изомерам и ко всем возможным смесям во всех пропорциях. Геометрические изомеры могут быть разделены в соответствии с общими методами, известными per se обычному специалисту в данной области техники.
Любое соединение общей формулы (I), в которой R1 представляет собой гидроксигруппу или сульфанильную группу, и/или X представляет собой гидроксигруппу, сульфанильную группу или аминогруппу, может быть обнаружено в своей таутомерной форме, полученной в результате сдвига протона в указанной гидроксигруппе, сульфанильной группе или аминогруппе. Такие таутомерные формы указанных соединений также составляют часть настоящего изобретения. В более общем смысле, все таутомерные формы соединений общей формулы (I), в которой R1 представляет собой гидроксигруппу или сульфанильную группу, и/или X представляет собой гидроксигруппу, сульфанильную группу или аминогруппу, а также все таутомерные формы соединений, которые могут быть необязательно использованы в качестве промежуточных продуктов в способах получения и определения которых будут представлены в описании этих способов, также составляют часть настоящего изобретения.
В соответствии с настоящим изобретением 2-пиридил замещен R1 в положении 6 и может быть замещен (X)n в любом другом положении, где значения X и n определены выше. Предпочтительно, настоящее изобретение относится к производному N-[2-(2-пиридинил)этил]бензамида общей формулы (I), в которой различные характеристики могут быть выбраны по отдельности или в комбинации, а именно:
- что касается R1, то R1 представляет собой атом водорода или атом галогена;
- что касается n, то n равно 1 или 2;
- что касается X, то X представляет собой атом галогена или C1-C8алкил;
- что касается положений, в которых 2-пиридильный фрагмент замещен X, то 2-пиридильный фрагмент замещен X в положении 3 и/или 5.
В соответствии с настоящим изобретением фенил замещен R7 в ортоположении и может быть замещен (Y)p в любом другом положении, где значения Y и p определены выше. Предпочтительно, настоящее изобретение относится к производному N-[2-(2-пиридинил)этил]бензамида общей формулы (I), в которой различные характеристики могут быть выбраны по отдельности или в комбинации, а именно:
- что касается R7, то R7 представляет собой атом галогена, C1-C8алкил или содержащий 1-5 атомов галогена C1-C8галогеналкил;
- что касается p, то p равно 1 или 2; более предпочтительно p равно 1;
- что касается Y, то Y представляет собой атом водорода, атом галогена или C1-C8алкил; более предпочтительно Y представляет собой атом водорода;
- что касается положений, в которых фенильный радикал замещен Y, то фенильный радикал замещен Y предпочтительно сначала в параположении.
Настоящее изобретение также относится к способу получения соединения общей формулы (I). Поэтому, в соответствии с дополнительным аспектом настоящее изобретение относится к способу A получения соединения общей формулы (Ia)

где:
R1, R2, R7, X, Y, n и p определены выше;
R3 представляет собой C1-C6алкил;
который включает:
- первую стадию в соответствии со схемой реакции A-1:
Схема А-1
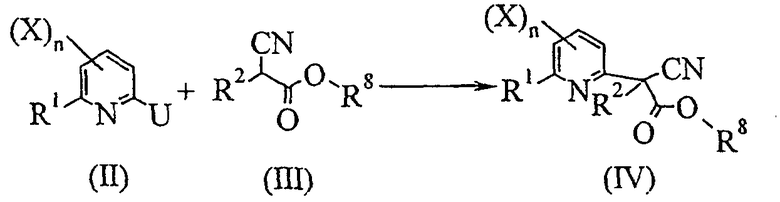
где:
R1, R2, X и n определены выше;
R8 представляет собой C1-C6алкил, C1-C6галогеналкил, бензил, 4-метоксибензил или пентафторфенил;
U представляет собой уходящую группу, выбранную из галогена, C1-C6алкилсульфоната или C1-C6галогеналкилсульфоната;
включающую арилирование производного цианоацетата общей формулы (III) производным пиридина общей формулы (II) в присутствии основания при температуре от 0°C до 200°C с получением производного 2-пиридилцианоацетата общей формулы (IV);
- вторую стадию в соответствии со схемой реакции A-2:
Схема А-2

где:
R1, R2, X, n определены выше;
R3 представляет собой атом водорода;
R8 представляет собой C1-C6алкил, C1-C6галогеналкил, бензил, 4-метоксибензил или пентафторфенил;
включающую гидролиз в щелочной среде, гидролиз в кислой среде или замещение галогенидом соединения общей формулы (IV) в том же самом или другом сосуде при нагревании при температуре от 40°C до температуры дефлегмации с получением производного 2-пиридилацетонитрила общей формулы (Va);
- третью стадию в соответствии со схемой реакции A-3:
Схема А-3

где:
R1, R2, X, n определены выше;
R3 представляет собой C1-C6алкил;
W представляет собой атом галогена, C1-C6алкилсульфонат, C1-C6галогеналкилсульфонат или 4-метилфенилсульфонат,
включающую алкилирование соединения общей формулы (Va) реагентом общей формулы (XVII) с получением соединений общей формулы (Vb);
- четвертую стадию в соответствии со схемой реакции A-4:
Схема А-4
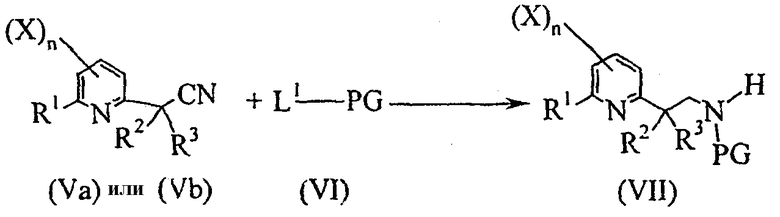
где:
R1, R2, X, n определены выше;
R3 представляет собой атом водорода и C1-C6алкил;
L1 представляет собой уходящую группу, выбранную из -OR8-группы или -OCOR8-группы, где R8 представляет собой C1-C6алкил, C1-C6галогеналкил, бензил, 4-метоксибензил или пентафторфенил;
PG представляет собой защитную группу, которой может являться -COOR8-группа или -COR8-группа, где R8 представляет собой C1-C6алкил, C1-C6галогеналкил, бензил, 4-метоксибензил или пентафторфенил;
включающую восстановление соединения общей формулы (Va) или (Vb) путем гидрирования или обработки гидридным донором в присутствии катализатора и в присутствии соединения общей формулы (VI) при температуре от 0°C до 150°C и при давлении от 1 бар до 100 бар с получением соединения общей формулы (VII);
- пятую стадию в соответствии со схемой реакции A-5:
Схема А-5

где:
R1, R2, X, n определены выше;
R3 представляет собой C1-C6алкил;
PG представляет собой защитную группу, которой может являться -COOR8-группа или -COR8-группа, где R8 представляет собой C1-C6алкил, C1-C6галогеналкил, бензил, 4-метоксибензил или пентафторфенил;
включающую реакцию снятия защиты с соединения общей формулы (VII) в кислой или в щелочной среде с получением производного амина общей формулы (VIIIa) или одной из его солей;
- шестую стадию в соответствии со схемой реакции A-6:
Схема А-6
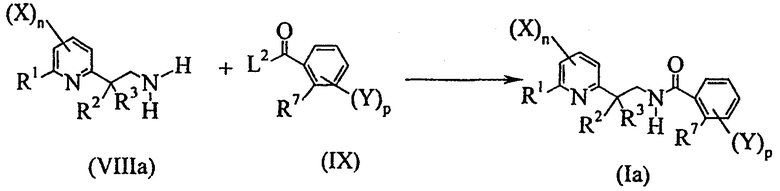
где:
R1, R2, R7, X, Y, n и p определены выше;
R3 представляет собой C1-C6алкил;
L2 представляет собой уходящую группу, выбранную из атома галогена, гидроксильной группы, -OR8-группы, -OCOR8, где R8 представляет собой C1-C6алкил, C1-C6галогеналкил, бензил, 4-метоксибензил или пентафторфенил, или группы формулы 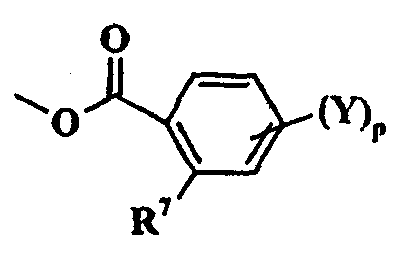 ,
,
включающую реакцию сочетания производного амина общей формулы (VIIIa) или одной из его солей с производным карбоновой кислоты формулы (IX) с получением соединения общей формулы (Ia).
Первую стадию (схема A-1) способа A по настоящему изобретению проводят в присутствии основания. Предпочтительно, основание выбирают из неорганического или органического основания. Подходящими примерами таких оснований могут являться, например, гидриды, гидроксиды, амиды, алкоголяты, карбонаты или гидрокарбонаты, ацетаты щелочноземельных или щелочных металлов, или третичные амины.
Первую стадию (схема A-1) способа A по настоящему изобретению проводят при температуре от 0°C до 200°C. Предпочтительно, первую стадию (схема A-1) проводят при температуре от 0°C до 120°C, более предпочтительно при температуре от 0°C до 80°C.
Первая стадия (схема A-1) способа A по настоящему изобретению может быть проведена в присутствии растворителя. Предпочтительно, растворитель выбирают из воды, органического растворителя или их смеси. Подходящим органическим растворителем может, например, являться алифатический, алициклический или ароматический растворитель.
Первая стадия (схема A-1) способа A по настоящему изобретению может быть также проведена в присутствии катализатора. Предпочтительно, катализатор выбирают из солей и комплексов палладия. Более предпочтительно, катализатор выбирают из комплексов палладия. Подходящий катализатор на основе комплекса палладия может быть, например, получен непосредственно в реакционной смеси путем раздельного добавления к реакционной смеси соли палладия и комплексообразующего лиганда. Подходящими лигандами могут, например, являться большей частью фосфиновые или арсиновые лиганды, такие как (R)-(-)-1-[(S)-2-(дициклогексилфосфино)ферроценил]этилдициклогексилфосфин и его соответствующий энантиомер или их смесь; (R)-(-)-1-[(S)-2-(дициклогексилфосфино)ферроценил]этилдифенилфосфин и его соответствующий энантиомер или их смесь; (R)-(-)-1-[(S)-2-(дициклофенилфосфино)ферроценил]этилди-трет-бутилфосфин и его соответствующий энантиомер или их смесь; или (R)-(-)-1-[(S)-2-(дициклофенилфосфино)ферроценил]этилдициклогексилфосфин и его соответствующий энантиомер или их смесь.
Четвертую стадию (схема A-4) способа A по настоящему изобретению проводят в присутствии гидридного донора. Предпочтительно, гидридный донор выбирают из гидридов металлов или металлоидов, таких как LiAlH4, NaBH4, KBH4, B2H6.
Четвертую стадию (схема A-4) способа A по настоящему изобретению проводят в присутствии катализатора. Предпочтительно, катализатор выбирают из хлорида Co(II), хлорида Ni(II), аммиака или одной из его солей, палладия на угле, никеля Ренея, кобальта Ренея или платины.
Четвертую стадию (схема A-4) способа A по настоящему изобретению проводят при температуре от 0°C до 150°C. Предпочтительно, температура составляет от 10°C до 120°C. Более предпочтительно, температура составляет от 10°C до 80°C.
Четвертую стадию (схема A-4) способа A по настоящему изобретению проводят при давлении от 1 бар до 100 бар. Предпочтительно, давление составляет от 1 бар до 50 бар.
Четвертая стадия (схема A-4) способа A по настоящему изобретению может быть проведена в присутствии органического растворителя, воды или их смеси. Предпочтительно, растворитель выбирают из эфира, спирта, карбоновой кислоты или их смеси с водой, или чистой воды.
Настоящее изобретение также относится к другому способу получения соединения общей формулы (I). Поэтому, в соответствии с дополнительным аспектом настоящее изобретение относится ко второму способу B получения соединения общей формулы (Ia)

в которой:
R1, R2, R7, X, Y, n и p определены выше;
R3 представляет собой C1-C6алкил;
который включает:
- первую стадию в соответствии со схемой реакции B-1:
Схема В-1
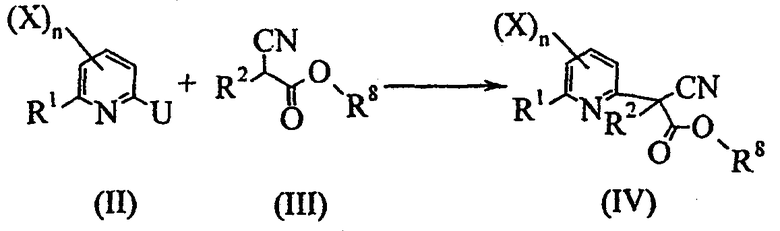
где:
R1, R2, X и n определены выше;
R8 представляет собой C1-C6алкил, C1-C6галогеналкил, бензил, 4-метоксибензил или пентафторфенил;
U представляет собой уходящую группу, выбранную из атома галогена, C1-C6алкилсульфоната или C1-C6галогеналкилсульфоната;
включающую арилирование производного цианоацетата общей формулы (III) производным пиридина общей формулы (II) с получением производного 2-пиридилцианоацетата общей формулы (IV);
- вторую стадию в соответствии со схемой реакции B-2:
Схема В-2

где:
R1, R2, X, n определены выше;
R8 представляет собой C1-C6алкил, C1-C6галогеналкил, бензил, 4-метоксибензил или пентафторфенил;
включающую гидролиз в щелочной среде, гидролиз в кислой среде или замещение галогенидом соединения общей формулы (IV) в том же самом или другом сосуде при нагревании при температуре от 40°C до температуры дефлегмации с получением производного 2-пиридилацетонитрила общей формулы (Va);
- третью стадию в соответствии со схемой реакции B-3:
Схема В-3

где:
R1, R2, X, n определены выше;
R3 представляет собой C1-C6алкил;
W представляет собой атом галогена, C1-C6алкилсульфонат, C1-C6галогеналкилсульфонат или 4-метилфенилсульфонат,
включающую алкилирование соединения общей формулы (Va) реагентом общей формулы (XVII) с получением соединения общей формулы (Vb);
- четвертую стадию в соответствии со схемой реакции B-4:
Схема В-4

где:
R1, R2, R7, X, Y, n и p определены выше;
R3 представляет собой C1-C6алкил;
L3 представляет собой уходящую группу, выбранную из -OCOR8, где R8 представляет собой C1-C6алкил, C1-C6галогеналкил, бензил, 4-метоксибензил или пентафторфенил; -OCHO, -SCSN(Me)2 или группы формулы
 ,
,
включающую восстановление соединения общей формулы (Va) или соединения общей формулы (Vb) путем гидрирования или обработки гидридным донором в присутствии катализатора и в присутствии соединения общей формулы (IX) при температуре от 0°C до 150°C и при давлении от 1 бар до 100 бар с получением соединения общей формулы (Ia).
Соединение общей формулы (Ia) по настоящему изобретению может быть получено в соответствии со способом B.
Предпочтительные условия, в которых проводят стадию B-1 способа B, аналогичны условиям, в которых проводят стадию A-1 приведенного выше способа A.
Предпочтительные условия, в которых проводят стадию B-2 способа B, аналогичны условиям, в которых проводят стадию A-2 приведенного выше способа A.
Предпочтительные условия, в которых проводят стадию B-3 способа B, аналогичны условиям, в которых проводят стадию A-3 приведенного выше способа A.
Предпочтительные условия, в которых проводят стадию B-4 способа B, аналогичны условиям, в которых проводят стадию A-4 приведенного выше способа A.
Настоящее изобретение также относится к другому способу получения соединения общей формулы (I). Поэтому, в соответствии с дополнительным аспектом настоящее изобретение относится к третьему способу C получения соединения общей формулы (Ia)

в которой:
R1, R2, R3, R7, X, Y, n и p определены выше;
который включает:
- первую стадию в соответствии со схемой реакции C-1:
Схема С-1
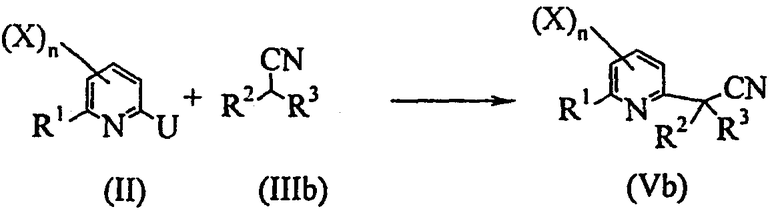
где:
R1, R2, R3, X и n определены выше;
U представляет собой уходящую группу, выбранную из атома галогена, C1-C6алкилсульфоната или C1-C6галогеналкилсульфоната;
включающую арилирование соединения общей формулы (IIIb) производным пиридина общей формулы (II) в присутствии основания при температуре от -100°C до 200°C с получением производного 2-пиридилацетонитрила общей формулы (Vb);
- вторую стадию в соответствии со схемой реакции C-2:
Схема С-2
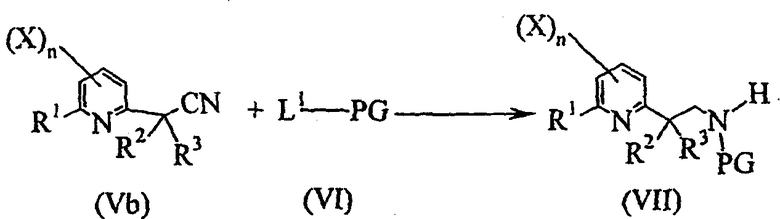
где:
R1, R2, R3, X и n определены выше;
L1 представляет собой уходящую группу, выбранную из -OR8-группы или -OCOR8-группы, где R8 представляет собой C1-C6алкил, C1-C6галогеналкил, бензил, 4-метоксибензил или пентафторфенил;
PG представляет собой защитную группу, которой может являться -COOR8-группа или -COR8-группа, где R8 представляет собой C1-C6алкил, C1-C6галогеналкил, бензил, 4-метоксибензил или пентафторфенил;
включающую восстановление соединения общей формулы (Va) или (Vb) путем гидрирования или обработки гидридным донором в присутствии соединения общей формулы (VI) с получением соединения общей формулы (VII);
- третью стадию в соответствии со схемой реакции C-3:
Схема С-3

где:
R1, R2, R3, X и n определены выше;
PG представляет собой защитную группу, которой может являться -COOR8-группа или -COR8-группа, где R8 представляет собой C1-C6алкил, C1-C6галогеналкил, бензил, 4-метоксибензил или пентафторфенил;
включающую реакцию снятия защиты с соединения общей формулы (VII) в кислой или в щелочной среде с получением производного амина общей формулы (VIIIa) или одной из его солей;
- четвертую стадию в соответствии со схемой реакции C-4:
Схема С-4

где:
R1, R2, R3, R7, X, Y, n и p определены выше;
L4 представляет собой уходящую группу, выбранную из атома галогена, гидроксильной группы, -OCHO, -SCSN(Me)2, -OR8-группы, -OCOR8, где R8 представляет собой C1-C6алкил, C1-C6галогеналкил, бензил, 4-метоксибензил или пентафторфенил, или группы формулы  ,
,
включающую реакцию сочетания производного амина общей формулы (VIIIa) или одной из его солей с производным карбоновой кислоты формулы (IX) с получением соединения общей формулы (Ia).
Первую стадию (схема C-1) способа C по настоящему изобретению проводят при температуре от -100°C до 200°C. Предпочтительно, первую стадию (схема C-1) проводят при температуре от -80°C до 120°C, более предпочтительно при температуре от -80°C до 80°C.
Первую стадию (схема C-1) способа C по настоящему изобретению проводят в присутствии основания. Предпочтительно, основание выбирают из неорганического или органического основания. Подходящими примерами таких оснований могут являться, например, гидриды, гидроксиды, амиды, алкоголяты, карбонаты или гидрокарбонаты, ацетаты щелочноземельных или щелочных металлов, или третичные амины.
Первая стадия (схема C-1) способа C по настоящему изобретению может быть проведена в присутствии растворителя. Предпочтительно, растворитель выбирают из воды, органического растворителя или их смеси. Подходящим органическим растворителем может, например, являться алифатический, алициклический или ароматический растворитель.
Первая стадия (схема C-1) способа C по настоящему изобретению может быть также проведена в присутствии катализатора. Предпочтительно, катализатор выбирают из солей и комплексов палладия. Более предпочтительно, катализатор выбирают из комплексов палладия. Подходящий катализатор на основе комплекса палладия может быть, например, получен непосредственно в реакционной смеси путем раздельного добавления к реакционной смеси соли палладия и комплексообразующего лиганда. Подходящими лигандами могут, например, являться большей частью фосфиновые или арсиновые лиганды, такие как (R)-(-)-1-[(S)-2-(дициклогексилфосфино)ферроценил]этилдициклогексилфосфин и его соответствующий энантиомер или их смесь; (R)-(-)-1-[(S)-2-(дициклогексилфосфино)ферроценил]этилдифенилфосфин и его соответствующий энантиомер или их смесь; (R)-(-)-1-[(S)-2-(дициклофенилфосфино)ферроценил]этилди-трет-бутилфосфин и его соответствующий энантиомер или их смесь; или (R)-(-)-1-[(S)-2-(дициклофенилфосфино)ферроценил]этилдициклогексилфосфин и его соответствующий энантиомер или их смесь.
Предпочтительные условия, в которых проводят стадию C-2 способа C, аналогичны условиям, в которых проводят стадию A-4 приведенного выше способа A.
Предпочтительные условия, в которых проводят стадию C-3 способа C, аналогичны условиям, в которых проводят стадию A-5 приведенного выше способа A.
Предпочтительные условия, в которых проводят стадию C-4 способа C, аналогичны условиям, в которых проводят стадию A-6 приведенного выше способа A.
Настоящее изобретение также относится к другому способу получения соединения общей формулы (I). Поэтому, в соответствии с дополнительным аспектом настоящее изобретение относится к четвертому способу D получения соединения общей формулы (Ia)

в которой:
R1, R2, R7, X, Y, n и p определены выше;
R3 представляет собой C1-C6алкил;
который включает:
- первую стадию в соответствии со схемой реакции D-1:
Схема D-1

где:
R1, R2, R3, X и n определены выше;
U представляет собой уходящую группу, выбранную из атома галогена, C1-C6алкилсульфоната или C1-C6галогеналкилсульфоната;
включающую арилирование соединения общей формулы (IIIb) производным пиридина общей формулы (II) в присутствии основания при температуре от -100°C до 200°C с получением производного 2-пиридилацетонитрила общей формулы (Vb);
- вторую стадию в соответствии со схемой реакции D-2:
Схема D-2

где:
R1, R2, R7, X, Y, n и p определены выше;
R3 представляет собой C1-C6алкил;
L3 представляет собой уходящую группу, выбранную из -OCOR8, где R8 представляет собой C1-C6алкил, C1-C6галогеналкил, бензил, 4-метоксибензил или пентафторфенил; -OCHO, -SCSN(Me)2 или группы формулы
 ,
,
включающую восстановление соединения общей формулы (Va) или соединения общей формулы (Vb) путем гидрирования или обработки гидридным донором в присутствии соединения общей формулы (IX) с получением соединения общей формулы (Ia).
Соединение общей формулы (Ia) по настоящему изобретению может быть получено в соответствии со способом D.
Предпочтительные условия, в которых проводят стадию D-1 способа D, аналогичны условиям, в которых проводят стадию C-1 приведенного выше способа C.
Предпочтительные условия, в которых проводят стадию D-2 способа D, аналогичны условиям, в которых проводят стадию A-4 приведенного выше способа A.
Настоящее изобретение также относится к другому способу получения соединения общей формулы (I). Поэтому, в соответствии с дополнительным аспектом настоящее изобретение относится к пятому способу E получения соединения общей формулы (Ia)

в которой:
R1, R2, R3, R7, X, Y, n и p определены выше;
R4 представляет собой атом водорода, C1-C6алкил или C1-C6галогеналкил;
R5 представляет собой C1-C6алкил или C1-C6галогеналкил;
L4 представляет собой уходящую группу, выбранную из атома галогена, гидроксильной группы, -OCHO, -SCSN(Me)2, -OR8-группы, -OCOR8, где R8 представляет собой C1-C6алкил, C1-C6галогеналкил, бензил, 4-метоксибензил или пентафторфенил, или группы формулы 
которая включает:
- первую стадию в соответствии со схемой реакции E-1:
Схема E-1
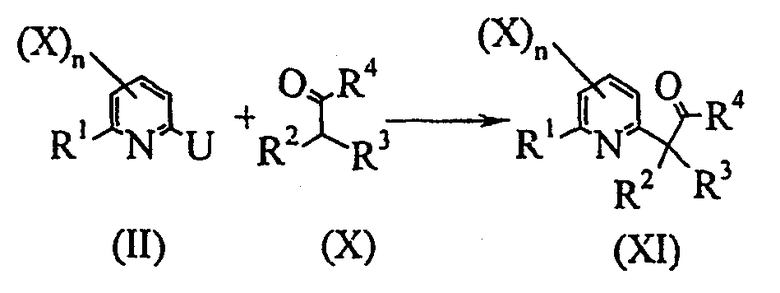
где:
R1, R2, R3, X и n определены выше;
R4 представляет собой атом водорода, C1-C6алкил или C1-C6галогеналкил;
U представляет собой уходящую группу, выбранную из атома галогена, C1-C6алкилсульфоната или C1-C6галогеналкилсульфоната;
включающую арилирование соединения общей формулы (X) производным пиридина общей формулы (II) с получением соединения общей формулы (XI);
- вторую стадию в соответствии со схемой реакции E-2:
Схема E-2
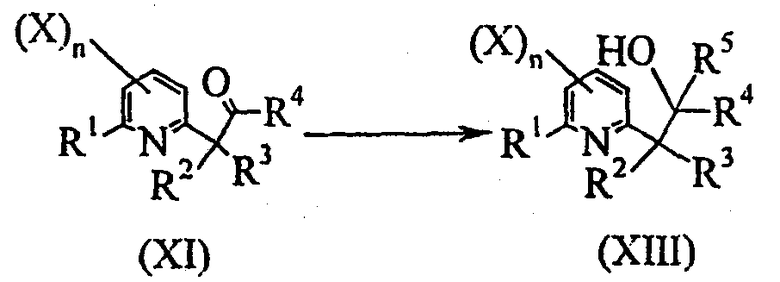
где:
R1, R2, R3, X и n определены выше;
R4 представляет собой атом водорода, C1-C6алкил или C1-C6галогеналкил;
включающую преобразование соединения общей формулы (XI) в соединение общей формулы (XIII) путем добавления соединения общей формулы R5-M, в которой R5 представляет собой C1-C6алкил или C1-C6галогеналкил и M является частицей металла;
- третью стадию в соответствии со схемой реакции E-3:
Схема E-3

где:
R1, R2, R3, X и n определены выше;
R4 представляет собой атом водорода, C1-C6алкил или C1-C6галогеналкил;
R5 представляет собой C1-C6алкил или C1-C6галогеналкил;
W представляет собой уходящую группу, выбранную из атома галогена, C1-C6алкилсульфоната, C1-C6галогеналкилсульфоната или 4-метилфенилсульфоната;
включающую активацию соединения общей формулы (XIII) путем преобразования его в соединение общей формулы (XIV);
- четвертую стадию в соответствии со схемой реакции E-4:
Схема E-4
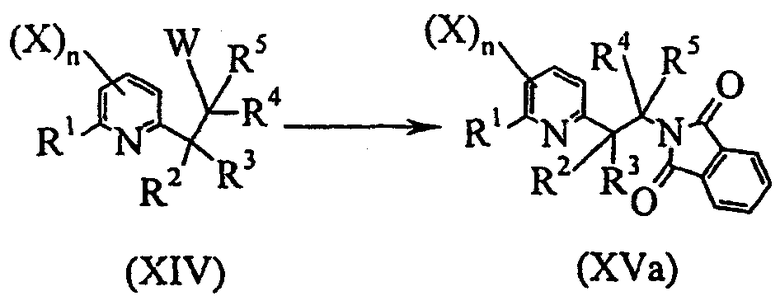
где:
R1, R2, R3, X и n определены выше;
R4 представляет собой атом водорода, C1-C6алкил или C1-C6галогеналкил;
R5 представляет собой C1-C6алкил или C1-C6галогеналкил;
W представляет собой уходящую группу, выбранную из атома галогена, C1-C6алкилсульфоната, C1-C6галогеналкилсульфоната или 4-метилфенилсульфоната;
включающую замещение соединения общей формулы (XIV) производным фталимида или одной из его солей с получением соединения общей формулы (XVa);
- пятую стадию в соответствии со схемой реакции E-5:
Схема E-5
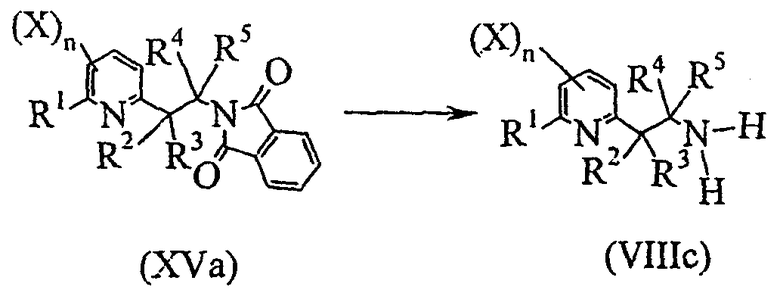
где:
R1, R2, R3, X и n определены выше;
R4 представляет собой атом водорода, C1-C6алкил или C1-C6галогеналкил;
R5 представляет собой C1-C6алкил или C1-C6галогеналкил;
включающую реакцию снятия защиты с соединения общей формулы (XVa) путем его взаимодействия с гидразингидратом или солью гидразина с получением производного амина общей формулы (VIIIc) или одной из его солей;
- шестую стадию в соответствии со схемой реакции E-6:
Схема E-6
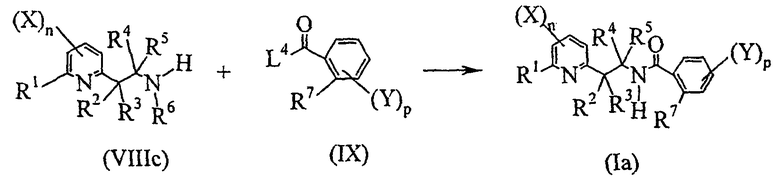
где:
R1, R2, R3, R7, X, Y, n и p определены выше;
R4 представляет собой атом водорода, C1-C6алкил или C1-C6галогеналкил;
R5 представляет собой C1-C6алкил или C1-C6галогеналкил;
L4 представляет собой уходящую группу, выбранную из атома галогена, гидроксильной группы, -OCHO, -SCSN(Me)2, -OR8-группы, -OCOR8, где R8 представляет собой C1-C6алкил, C1-C6галогеналкил, бензил, 4-метоксибензил или пентафторфенил, или группы формулы  ,
,
включающую реакцию сочетания производного амина общей формулы (VIIIb) или одной из его солей с производным карбоновой кислоты формулы (IX) с получением соединения общей формулы (Ia).
Соединение общей формулы (I) по настоящему изобретению может быть получено в соответствии со способом E.
Предпочтительные условия, в которых проводят стадию E-6 способа E, аналогичны условиям, в которых проводят стадию A-6 приведенного выше способа A.
Настоящее изобретение также относится к другому способу получения соединения общей формулы (I). Поэтому, в соответствии с дополнительным аспектом настоящее изобретение относится к шестому способу F получения соединения общей формулы (Ia)

в которой:
R1, R7, X, Y, n и p определены выше;
R2, R4 и R5 независимо друг от друга выбирают из атома водорода, C1-C6алкила или C1-C6галогеналкила;
который включает:
- первую стадию в соответствии со схемой реакции F-1:
Схема F-1

где:
R1, X и n определены выше;
U представляет собой уходящую группу, выбранную из атома галогена, C1-C6алкилсульфоната или C1-C6галогеналкилсульфоната;
R2, R4 и R5 независимо друг от друга выбирают из атома водорода, C1-C6алкила или C1-C6галогеналкила;
M является частицей металла или металлоида;
включающую реакцию сочетания производного пиридина общей формулы (II) с винильным производным общей формулы (XVI) при температуре от 0°C до 200°C с получением соединения общей формулы (XVII);
- вторую стадию в соответствии со схемой реакции F-2:
Схема F-2

где:
R1, X и n определены выше;
R2, R4 и R5 независимо друг от друга выбирают из атома водорода, C1-C6алкила или C1-C6галогеналкила;
включающую добавление фталимида или одной из его солей к соединению общей формулы (XVII) с получением соединения общей формулы (XVb);
- третью стадию в соответствии со схемой реакции F-3:
Схема F-3

где:
R1, X и n определены выше;
R2, R4 и R5 независимо друг от друга выбирают из атома водорода, C1-C6алкила или C1-C6галогеналкила;
включающую реакцию снятия защиты с соединения общей формулы (XVb) гидразингидратом или с солью гидразина с получением производного амина общей формулы (VIIId) или одной из его солей;
- четвертую стадию в соответствии со схемой реакции F-4:
Схема F-4

где:
R1, R7, X, Y, n и p определены выше;
R2, R4 и R5 независимо друг от друга выбирают из атома водорода, C1-C6алкила или C1-C6галогеналкила;
L4 представляет собой уходящую группу, выбранную из атома галогена, гидроксильной группы, -OCHO, -SCSN(Me)2, -OR8-группы, -OCOR8, где R8 представляет собой C1-C6алкил, C1-C6галогеналкил, бензил, 4-метоксибензил или пентафторфенил, или группы формулы  ,
,
включающую реакцию сочетания производного амина общей формулы (VIIIb) или одной из его солей с производным карбоновой кислоты формулы (IX) с получением соединения общей формулы (Ia).
Первую стадию (схема F-1) способа F по настоящему изобретению проводят в присутствии винильного производного общей формулы (XVI), в которой M является частицей металла или металлоида. Предпочтительно, M представляет собой производное олова или производное бора. Более предпочтительно, M представляет собой группу три-н-бутилолова.
Первую стадию (схема F-1) способа F по настоящему изобретению проводят при температуре от 0°C до 200°C. Предпочтительно, стадию G-1 проводят при температуре от 60°C до 160°C, более предпочтительно при температуре от 80°C до 140°C.
Первая стадия (схема F-1) способа F по настоящему изобретению может быть проведена в присутствии растворителя. Предпочтительно, растворитель выбирают из воды, органического растворителя или их смеси. Подходящим органическим растворителем может, например, являться алифатический, алициклический или ароматический растворитель.
Первая стадия (схема F-1) способа F по настоящему изобретению может быть также проведена в присутствии катализатора. Предпочтительно, катализатор выбирают из солей и комплексов палладия. Более предпочтительно, катализатор выбирают из комплексов палладия. Подходящий катализатор на основе комплекса палладия может быть, например, получен непосредственно в реакционной смеси путем раздельного добавления к реакционной смеси соли палладия и комплексообразующего лиганда. Подходящими лигандами могут, например, являться большей частью фосфиновые или арсиновые лиганды, такие как (R)-(-)-1-[(S)-2-(дициклогексилфосфино)ферроценил]этилдициклогексилфосфин и его соответствующий энантиомер или их смесь; (R)-(-)-1-[(S)-2-(дициклогексилфосфино)ферроценил]этилдифенилфосфин и его соответствующий энантиомер или их смесь; (R)-(-)-1-[(S)-2-(дициклофенилфосфино)ферроценил]этилди-трет-бутилфосфин и его соответствующий энантиомер или их смесь; или (R)-(-)-1-[(S)-2-(дициклофенилфосфино)ферроценил]этилдициклогексилфосфин и его соответствующий энантиомер или их смесь.
Первую стадию (схема F-1) способа F по настоящему изобретению проводят в присутствии основания. Предпочтительно, основание выбирают из неорганического или органического основания. Подходящими примерами таких оснований могут являться, например, гидриды, гидроксиды, амиды, алкоголяты, карбонаты или гидрокарбонаты, ацетаты щелочноземельных или щелочных металлов, или третичные амины.
Предпочтительные условия, в которых проводят стадию F-3 способа F, аналогичны условиям, в которых проводят стадию E-5 приведенного выше способа E.
Предпочтительные условия, в которых проводят стадию F-4 способа F, аналогичны условиям, в которых проводят стадию A-6 приведенного выше способа A.
Любой из описанных выше способов A-F может необязательно включать дополнительную стадию в соответствии со схемой реакции G:
Схема G
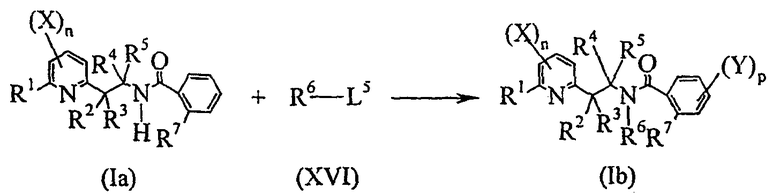
где:
R1, R2, R3, R4, R5, R6, R7, X, Y, n and p определены выше;
L5 представляет собой уходящую группу, выбранную из атома галогена, 4-метилфенилсульфонилоксигруппы, метилсульфонилоксигруппы;
включающую взаимодействие соединения общей формулы (Ia) с соединением общей формулы (XVI) с получением соединения общей формулы (Ib).
Настоящее изобретение также относится к другому способу получения соединения общей формулы (I). Поэтому, в соответствии с дополнительным аспектом настоящее изобретение относится к седьмому способу H получения соединения представленной выше общей формулы (I),
который включает:
- первую стадию в соответствии со схемой реакции H-1:
Схема H-1

где:
R1, R2, R3, X и n определены выше;
R4 представляет собой атом водорода, C1-C6алкил или C1-C6галогеналкил;
U представляет собой уходящую группу, выбранную из атома галогена, C1-C6алкилсульфоната или C1-C6галогеналкилсульфоната;
включающую арилирование соединения общей формулы (X) производным пиридина общей формулы (II) в присутствии основания при температуре 0°C до 200°C с получением соединения общей формулы (XI);
- вторую стадию в соответствии со схемой реакции H-2:
Схема H-2
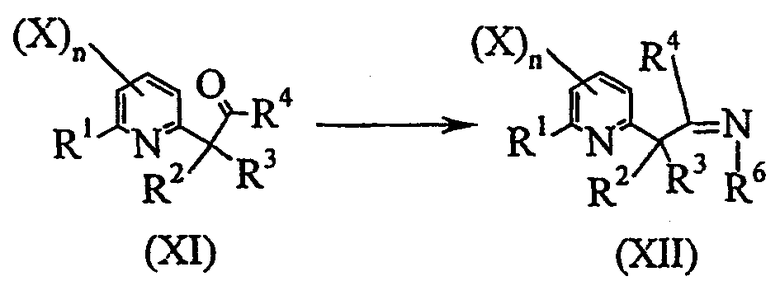
где:
R1, R2, R3, X и n определены выше;
R4 представляет собой атом водорода, C1-C6алкил или C1-C6галогеналкил;
R6 представляет собой атом водорода, C1-C6алкил или C1-C6галогеналкил, C1-C6алкоксигруппу или C3-C7-циклоалкил;
включающую взаимодействие соединения общей формулы (XI) с амином формулы R6-NH2 с получением иминопроизводного общей формулы (XII);
- третью стадию в соответствии со схемой реакции H-3:
Схема H-3
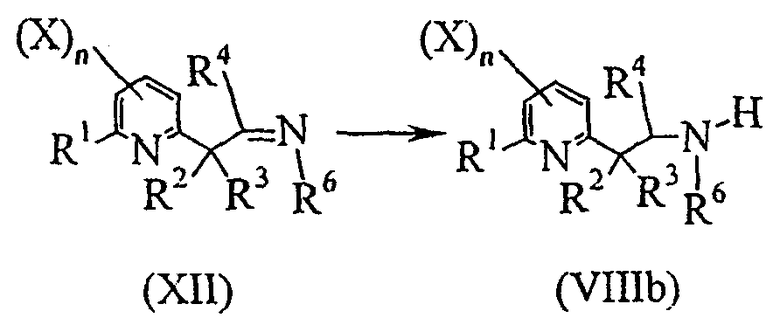
где:
R1, R2, R3, X и n определены выше;
R4 представляет собой атом водорода, C1-C6алкил или C1-C6галогеналкил;
R6 представляет собой атом водорода, C1-C6алкил, C1-C6галогеналкил, C1-C6алкоксигруппу или C3-C7-циклоалкил;
включающую восстановление иминопроизводного общей формулы (XII) путем гидрирования или обработки гидридным донором в том же самом или другом сосуде с получением производного амина общей формулы (VIIIb) или одной из его солей;
- четвертую стадию в соответствии со схемой реакции H-4:
Схема H-4

где:
R1, R2, R3, R7, X, Y, n и p определены выше;
R4 представляет собой атом водорода, C1-C6алкил или C1-C6галогеналкил;
R6 представляет собой атом водорода, C1-C6алкил, C1-C6галогеналкил, C1-C6алкоксигруппу или C3-C7-циклоалкил;
L4 представляет собой уходящую группу, выбранную из атома галогена, гидроксильной группы, -OCHO, -SCSN(Me)2, -OR8-группы, -OCOR8, где R8 представляет собой C1-C6алкил, C1-C6галогеналкил, бензил, 4-метоксибензил или пентафторфенил, или группы формулы  ,
,
включающую реакцию сочетания производного амина общей формулы (VIIIb) или одной из его солей с производным карбоновой кислоты формулы (IX) с получением соединения общей формулы (I).
Соединение общей формулы (I) по настоящему изобретению может быть получено в соответствии со способом H.
Предпочтительные условия, в которых проводят стадию H-1 способа H, аналогичны условиям, в которых проводят стадию A-1 приведенного выше способа A.
Третью стадию (схема H-3) способа H по настоящему изобретению проводят в присутствии гидридного донора. Предпочтительно, гидридный донор выбирают из гидридов металлов или металлоидов, таких как LiAlH4, NaBH4, KBH4, B2H6.
Соединение по настоящему изобретению могут быть получены в соответствии с описанными выше общими способами получения. Тем не менее, следует понимать, что специалист в данной области сможет адаптировать указанный способ в соответствии с особенностями каждого из соединений, которые необходимо синтезировать, основываясь на общем знании и доступных публикациях.
Настоящее изобретение также относится к фунгицидной композиции, содержащей эффективное количество активного вещества общей формулы (I). Таким образом, настоящее изобретение относится к фунгицидной композиции, содержащей эффективное количество определенного выше активного вещества общей формулы (I) в качестве активного ингредиента и пригодную для применения в сельском хозяйстве основу, носитель или наполнитель.
В описании настоящего изобретения термин «основа» означает встречающееся в природе или синтетическое, органическое или неорганическое вещество, с которым объединяют активное вещество для его более легкого нанесения, а именно на части растения. Поэтому, указанная основа является, как правило, инертной и должна быть приемлема с точки зрения сельского хозяйства. Основа может быть твердой или жидкой. Примеры приемлемых основ включают глины, встречающиеся в природе, или синтетические силикаты, двуокись кремния, смолы, воски, твердые удобрения, воду, спирты, в частности, бутанол, органические растворители, минеральные и растительные масла и их производные. Также могут применяться смеси указанных основ.
Композиция может также содержать дополнительные компоненты. В частности, композиция может дополнительно содержать поверхностно-активное вещество. Поверхностно-активное вещество может быть эмульгатором, диспергирующим веществом или смачивающим веществом ионогенного или неионогенного типа, или смесью указанных поверхностно-активных веществ. Например, могут быть приведены соли полиакриловой кислоты, соли лигносульфоновой кислоты, соли фенолсульфоновой или нафталинсульфоновой кислоты, поликонденсаты этиленоксида с жирными спиртами или с жирными кислотами или с жирными аминами, замещенные фенолы (в частности, алкилфенолы или арилфенолы), соли сложных эфиров сульфоянтарной кислоты, производные таурина (в частности, алкилтаураты), сложные эфиры фосфорной кислоты и полиоксиэтилированных спиртов или фенолов, сложные эфиры жирных кислот и полиолов, и производные указанных выше соединений, содержащие сульфатные, сульфонатные и фосфатные функциональные группы. Присутствие, по крайней мере, одного поверхностно-активного вещества, как правило, важно в том случае, когда активное вещество и/или инертная основа являются нерастворимыми в воде и когда агент-переносчик представляет собой воду. Предпочтительно, содержание поверхностно-активного вещества может составлять от 5 мас.% до 40 мас.% композиции.
Также могут быть включены другие необязательные компоненты, например, защитные коллоиды, адгезивы, загустители, тиксотропные вещества, способствующие проникновению вещества, стабилизаторы, связывающие агенты. В более общем смысле, активные вещества могут быть объединены с твердой или жидкой добавкой, которая соответствует требованиям обычных способов приготовления составов.
Композиция по настоящему изобретению может содержать, как правило, от 0,05 до 99 мас.% активного вещества, предпочтительно 10-70 мас.%.
Композиции по настоящему изобретению могут применяться в различных формах, таких как аэрозольный распылитель, микрокапсулированная суспензия, концентрат для холодного аэрозольного орошения, распыляемый порошок, эмульгирующийся концентрат, эмульсия типа «вода в масле», эмульсия типа «масло в воде», заключенная в капсулу гранула, мелкодисперсная гранула, жидкий концентрат для обработки семян, газ (под давлением), газогенерирующий продукт, гранула, концентрат для горячего аэрозольного орошения, макрогранула, микрогранула, диспергируемый в масле порошок, смешивающийся с маслом жидкий концентрат, смешивающая с маслом жидкость, паста, для намазывания растений, порошок для сухой обработки семян, покрытые пестицидом семена, растворимый концентрат, растворимый порошок, раствор для обработки семян, концентрат суспензий (жидкий концентрат), жидкость сверхнизкого объема, суспензия сверхнизкого объема, диспергируемые в воде гранулы или таблетки, диспергируемый в воде порошок для обработки во взвешенном состоянии, растворимые в воде гранулы или таблетки, растворимый в воде порошок для обработки семян и смачивающийся порошок.
Эти композиции включают не только композиции, готовые для нанесения на растение или семена, обрабатываемые при помощи подходящего устройства, такого как разбрызгивающее устройство или распылитель, а также концентрированные коммерческие композиции, которые должны быть разбавлены перед применением по отношению к культуре.
Соединения по настоящему изобретению могут также быть смешаны с одним или несколькими инсектицидами, фунгицидами, бактерицидами, аттрактантами-акарицидами или феромонами или другими биологически активными соединениями. Полученные таким образом смеси обладают расширенным спектром активности. Особенно эффективными являются смеси с другими фунгицидами.
Фунгицидные композиции по настоящему изобретению могут применяться для лечебного или профилактического контроля роста фитопатогенных грибов на сельскохозяйственных культурах. Поэтому в соответствии с дополнительным аспектом настоящее изобретение относится к способу лечебного или профилактического контроля роста фитопатогенных грибов на сельскохозяйственных культурах, характеризуемого тем, что определенную выше композицию наносят на семена, растение и/или на плод растения или на почву, на которой растение произрастает или на которой его требуется вырастить.
Композиция, применяемая для борьбы с фитопатогенными грибами на сельскохозяйственных культурах, содержит эффективное и нетоксичное в отношении растения количество активного вещества общей формулы (I).
Выражение «эффективное и нетоксичное в отношении растения количество» означает количество композиции по настоящему изобретению, которое эффективно контролирует рост или разрушает грибы, которыми сельскохозяйственные культуры поражены или которые склонны на них появиться, и которые не вызывают какого-либо заметного проявления фитотоксичности в отношении указанных сельскохозяйственных культур. Такое количество может варьировать в широком диапазоне в зависимости от вида гриба, чей рост необходимо контролировать, климатических условий и соединений, включенных в состав фунгицидной композиции по настоящему изобретению.
Это количество может быть определено путем планомерных полевых испытаний, которые способен провести специалист в данной области техники.
Способ обработки по настоящему изобретению полезен для обработки репродуктивного материала, такого как клубни или корневища, а также семян, саженцев или пикированных саженцев и растений или пикированных растений. Этот способ обработки может также применяться для обработки корней. Способ обработки по настоящему изобретению также может применяться для обработки надземных частей растения, таких как стволы, стебли или черенки, листья, цветы или плоды рассматриваемого растения.
Растениями, которые могут быть защищены по способу по настоящему изобретению, может являться хлопчатник, лен, виноград, плодовые и овощные культуры, такие как Rosaceae sp. (например, семечковые плоды, такие как яблоки и груши, а также косточковые плоды, такие как абрикосы, миндаль и персики), Ribesioidae sp., Juglandaceae sp., Betulaceae sp., Anacardiaceae sp., Fagaceae sp., Moraceae sp., Oleaceae sp., Actinidaceae sp., Lauraceae sp., Musaceae sp. (например, банановые деревья и саженцы), Rubiaceae sp., Theaceae sp., Sterculiceae sp., Rutaceae sp. (например, лимоны, апельсины и грейпфруты); бобовые культуры, такие как Solanaceae sp. (например, томаты), Liliaceae sp., Asteraceae sp. (например, латуки), Umbelliferae sp., Cruciferae sp., Chenopodiaceae sp., Cucurbitaceae sp., Papilionaceae sp. (например, гороховые), Rosaceae sp. (например, земляники); высокоурожайные, такие как Graminae sp. (такие как кукуруза, газонные культуры или злаковые, такие как пшеница, рис, ячмень и тритикале), Asteraceae sp. (например, подсолнечник), Cruciferae sp. (например, кольза), Papilionaceae sp. (например, соя), Solanaceae sp. (например, картофель), Chenopodiaceae sp. (например, столовая свекла), садоводческие культуры и насаждения, а также генетически модифицированные гомологи этих сельскохозяйственных культур.
В качестве растений и возможных болезней этих растений, для защиты от которых может применяться способ по настоящему изобретению, могут быть приведены:
- пшеница, в отношении борьбы со следующими болезнями семян: фузариозом (Microdochium nivale и Fusarium roseum), твердой головней пшеницы (Tilletia caries, Tilletia controversa или Tilletia indica), септориозом злаков (Septoria nodorum) и пыльной головней;
- пшеница, в отношении борьбы со следующими болезнями надземных частей растения: глазковой пятнистостью злаков (Tapesia yallundae, Tapesia acuiformis), выпреванием (Gaeumannomyces graminis), увяданием нижней части растения (F. culmorum, F. graminearum), черной паршой картофеля (Rhizoctonia cerealis), истинной мучнистой росой (Erysiphe graminis forma specie tritici), ржавчиной злаков (Puccinia striiformis и Puccinia recondita) и септориозом злаков (Septoria tritici и Septoria nodorum);
- пшеница и ячмень, в отношении борьбы с бактериальными и вирусными заболеваниями, например, с желтой мозаичной болезнью ячменя;
- ячмень, в отношении борьбы со следующими болезнями семян: сетчатой пятнистостью (Pyrenophora graminea, Pyrenophora teres и Cochliobolus sativus), пыльной головней (Ustilago nuda) и фузариозом (Microdochium nivale и Fusarium roseum);
- ячмень, в отношении борьбы со следующими болезнями надземных частей растения: глазковой пятнистостью злаков (Tapesia yallundae), сетчатой пятнистостью (Pyrenophora teres и Cochliobolus sativus), истинной мучнистой росой (Erysiphe graminis forma specie hordei), карликовой ржавчиной ячменя (Puccinia hordei) и окаймленной пятнистостью зерновых (Rhynchosporium secalis);
- картофель, в отношении борьбы с болезнями клубней (в особенности, вызываемых Helminthosporium solani, Phoma tuberosa, Rhizoctonia solani, Fusarium solani), ложной мучнистой росой (Phytopthora infestans) и конкретными вирусами (вирус Y);
- картофель, в отношении борьбы со следующими болезнями листвы: бурой пятнистостью пасленовых (Alternaria solani), ложной мучнистой росой (Phytophthora infestans);
- хлопчатник, в отношении борьбы со следующими болезнями проращенных из семян саженцев: выпреванием и ризоктониозной гнилью (Rhizoctonia solani, Fusarium oxysporum) и черной корневой гнилью (Thielaviopsis basicola);
- высокобелковых культур, например, гороховых, в отношении борьбы со следующими болезнями семян: антракнозом (Ascochyta pisi, Mycosphaerella pinodes), фузариозом (Fusarium oxysporum), серой гнилью (Botrytis cinerea) и ложной мучнистой росой (Peronospora pisi);
- масленичные сельскохозяйственные культуры, например, рапс, в отношении борьбы с болезнями семян, вызываемыми Phoma lingam, Alternaria brassicae и Sclerotinia sclerotiorum;
- кукуруза, в отношении борьбы с болезнями семян, вызываемыми Rhizopus sp., Penicillium sp., Trichoderma sp., Aspergillus sp. и Gibberella fujikuroi;
- лен, в отношении борьбы с болезнью семян, вызываемой Alternaria linicola;
- высокоствольные деревья, в отношении борьбы с выпреванием (Fusarium oxysporum, Rhizoctonia solani);
- рис, в отношении борьбы со следующими болезнями надземных частей растения: пирикуляриозом (Magnaporthe grisea), ризоктониозной гнилью (Rhizoctonia solani);
- бобовые культуры, в отношении борьбы со следующими болезнями семян и проращенных из семян саженцев: выпреванием и ризоктониозной гнилью (Fusarium oxysporum, Fusarium roseum, Rhizoctonia solani, Pythium sp.);
- бобовые культуры, в отношении борьбы со следующими болезнями надземных частей растения: серой гнилью (Botrytis sp.), истинной мучнистой росой (в особенности, вызываемой Erysiphe cichoracearum, Sphaerotheca fuliginea и Leveillula taurica), фузариозом (Fusarium oxysporum, Fusarium roseum), пятнистостью листьев (Cladosporium sp.), альтернариозом листьев (Alternaria sp.), антракнозом (Colletotrichum sp.), септориозной пятнистостью (Septoria sp.), черной паршой картофеля (Rhizoctonia solani), ложной мучнистой росой (например, вызываемыми Bremia lactucae, Peronospora sp., Pseudoperonospora sp., Phytophthora sp.);
- фруктовые деревья, в отношении борьбы с болезнями надземных частей: монилиальным ожогом яблони (Monilia fructigenae, M. laxa), паршой яблок (Venturia inaequalis), истинной мучнистой росой (Podosphaera leucotricha);
- виноград, в отношении борьбы с болезнями листвы: в особенности, серой гнилью (Botrytis cinerea), истинной мучнистой росой (Uncinula necator), черной гнилью (Guignardia biwelli) и ложной мучнистой росой (Plasmopara viticola);
- столовая свекла, в отношении борьбы со следующими болезнями надземных частей растения: церкоспорозом (Cercospora beticola), истинной мучнистой росой (Erysiphe beticola), пятнистостью листьев (Ramularia beticola).
Фунгицидная композиция по настоящему изобретению может также применяться для борьбы с грибковыми болезнями, способными возникать на поверхности или внутри строевого леса. Термин «строевой лес» означает все типы видов дерева и все типы полученных из этого строевого леса конструкционных лесоматериалов, например, массива дерева, плотной древесины, слоистой (клееной) древесины и фанеры. Способ обработки строевого леса по настоящему изобретению состоит, главным образом, из контакта строевого леса с одним или несколькими соединениями по настоящему изобретению или с композицией по настоящему изобретению; он включает, например, непосредственное нанесение, распыление, погружение в состав, инъекцию или любые другие подходящие способы.
Для способов нанесения с обработкой листвы эффективная доза активного вещества, обычно применяемая для обработки по настоящему изобретению, как правило, составляет от 10 до 800 г/га, предпочтительно от 50 до 300 г/га. В случае обработки семян эффективная доза наносимого активного вещества, как правило, составляет от 2 до 200 г на 100 кг семян, предпочтительно от 3 до 150 г на 100 кг семян. Следует ясно понимать, что указанные выше дозы представлены в качестве иллюстративных примеров настоящего изобретения. Специалисту в данной области известно, каким образом можно скорректировать наносимые дозы в соответствии с природой обрабатываемой культуры.
Фунгицидная композиция по настоящему изобретению может также применяться для обработки генетически модифицированных микроорганизмов соединениями по настоящему изобретению или агрохимическими композициями по настоящему изобретению. Генетически модифицированные растения представляют собой растения, в геном которых может быть устойчиво введен гетерологичный ген, кодирующий интересующий белок. Выражение «гетерологичный ген, кодирующий интересующий белок», по существу означает гены, которые придают трансформированному растению новые агрономические свойства, или гены, улучшающие агротехнические качества трансформированного растения.
Композиции по настоящему изобретению могут также применяться для приготовления композиции, пригодной для лечения или профилактики у человека или животного грибковых заболеваний, таких как, например, микозы, дерматозы, трихофитии и кандидозы, или заболеваний, вызываемых Aspergillus spp., например, Aspergillus fumigatus.
Далее будут проиллюстрированы аспекты настоящего изобретения со ссылкой на следующие таблицы соединений и примеры. Следующая таблица в неограничивающей манере иллюстрирует примеры фунгицидных соединений по настоящему изобретению. В последующих примерах M+1 (или M-1) означает полученное в ходе масс-спектрометрии значение пика молекулярного иона плюс/минус 1 а.е.м. (атомная единица массы), соответственно, и M (ApcI+) означает значение пика молекулярного иона, полученного путем масс-спектрометрии с химической ионизацией при повышенном атмосферном давлении.



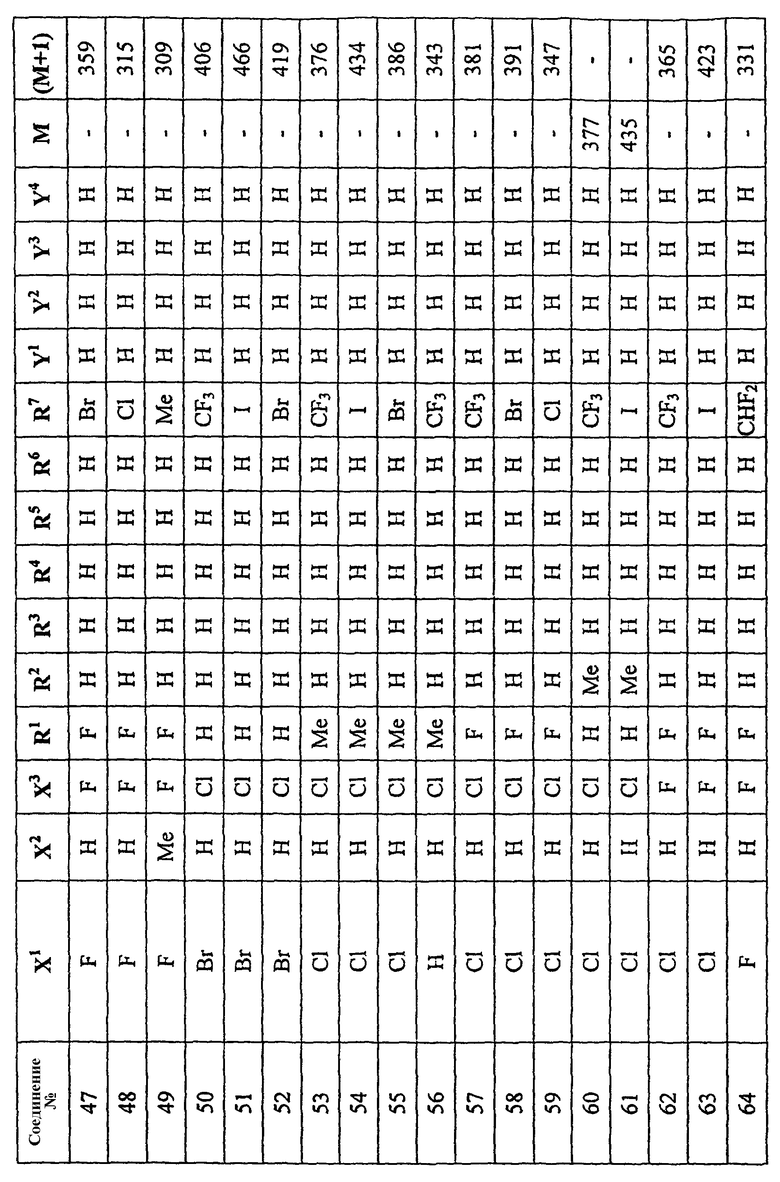

Примеры способа получения соединения общей формулы (I)
Пример способа A: Получение N-[2-(3,5-дихлор-2-пиридинил)этил]-2-йодбензамида (соединение 5)
Стадия 1: Получение трет-бутилциано(3,5-дихлор-2-пиридинил)ацетата
К 50 мл диметоксиэтана при 0°C медленно порциями добавляли 8,8 г (0,22 моль) гидрида натрия (60% дисперсия в минеральном масле).
К этой суспензии при 5°C по каплям дополнительно добавляли 17 г (0,12 моль) трет-бутилцианоацетата в 50 мл диметоксиэтана. Суспензию перемешивали в течение 45 минут при комнатной температуре.
К суспензии последовательно добавляли 20 г (0,11 моль) 2,3,5-трихлорпиридина, 0,59 г (1,1 ммоль) (S)-(+)-1-[(R)-2- (дифенилфосфино)ферроценил]этил-трет-бутилфосфина и 1,2 г (2,2 ммоль) бис(дибензилиденацетон)палладия(0).
Черную смесь кипятили с обратным холодильником в течение 5 часов. После охлаждения реакционную смесь вливали в 100 мл 1н. хлористоводородной кислоты. Водную фазу фильтровали на supersel и экстрагировали этилацетатом (3×200 мл). Органическую фазу промывали насыщенным раствором соли и сушили над сульфатом магния. Растворитель выпаривали при пониженном давлении с получением 38,5 г неочищенного продукта в виде коричневого масла.
Неочищенный продукт очищали флэш-хроматографией на силикагеле (элюент: гептан/хлороформ=6/4) с получением 13 г (41%) трет-бутилциано(3,5-дихлор-2-пиридинил)ацетата в виде желтого масла; данные масс-спектрометрии: 287(M+1).
Стадия 2: Получение (3,5-дихлор-2-пиридинил)ацетонитрила
К раствору 12 г (0,042 моль) трет-бутилциано(3,5-дихлор-2-пиридинил)ацетата в 50 мл смеси диметилсульфоксид/вода=25/1 добавляли 1,2 г (0,021 моль) хлорида натрия.
Смесь перемешивали в течение 3 часов при 130°C. После охлаждения реакционную смесь вливали в воду со льдом. Водную фазу экстрагировали этилацетатом (3×250 мл), органическую фазу промывали насыщенным раствором соли и сушили над сульфатом магния. Растворитель выпаривали при пониженном давлении с получением 8,2 г неочищенного продукта в виде коричневого масла.
Неочищенный продукт очищали флэш-хроматографией на силикагеле (элюент: гептан/этилацетат=7/3) с получением 5,9 г (76%) (3,5-дихлор-2-пиридинил)ацетонитрила в виде оранжевого масла; данные масс-спектрометрии: 185(M-1).
Стадия 3: Получение трет-бутил-2-(3,5-дихлор-2-пиридинил)этилкарбамата
К раствору 2,8 г (0,015 моль) (3,5-дихлор-2-пиридинил)ацетонитрила в 40 мл метанола быстро добавляли 3,9 г (0,0165 моль) гексагидрата хлорида кобальта(II) и 6,5 г (0,03 моль) ди-трет-бутилдикарбоната.
Темный раствор охлаждали до -5°C и при 0°C порциями добавляли 3,96 г (0,1 моль) боргидрида натрия. Реакционную смесь перемешивали при комнатной температуре в течение 18 часов.
Реакционную смесь нейтрализовали добавлением 1 н. хлористоводородной кислоты и удаляли метанол при пониженном давлении. Водную фазу повторно экстрагировали дихлорметаном, органическую фазу промывали насыщенным раствором соли и сушили над сульфатом магния. Растворитель выпаривали при пониженном давлении с получением 4 г неочищенного продукта в виде коричневого масла.
Неочищенный продукт очищали флэш-хроматографией на силикагеле (элюент: гептан/этилацетат=5/1) с получением 2,0 г (46%) трет-бутил-2-(3,5-дихлор-2-пиридинил)этилкарбамата в виде желтого масла; данные масс-спектрометрии: 192 (M+1-101 (boc)).
Стадия 4: Получение гидрохлорида 2-(3,5-дихлор-2-пиридинил)этанамина
К раствору 2,4 г (8, 2 ммоль) трет-бутил-2-(3,5-дихлор-2-пиридинил)этилкарбамата в 100 мл дихлорметана добавляли 5 мл трифторуксусной кислоты.
Смесь перемешивали в течение 1 часа при комнатной температуре. Растворитель выпаривали при пониженном давлении с получением 4,7 г неочищенного желтого масла.
Неочищенное масло повторно растворяли в 10 мл этилового эфира и по каплям добавляли 5,2 мл 2н. хлористоводородной кислоты с выпадением в осадок гидрохлорида.
Твердое вещество собирали фильтрованием, промывали этиловым эфиром и сушили в вакууме с получением 1,3 г (70%) 2-(3,5-дихлор-2-пиридинил)этанамина в виде его гидрохлорида.
Стадия 5: Получение N-[2-(3,5-дихлор-2-пиридинил)этил]-2-йодбензамида (соединение 5)
К суспензии 60 мг (0,26 ммоль) гидрохлорида 2-(3,5-дихлор-2-пиридинил)этанамина в 1 мл дихлорметана последовательно добавляли 81 мкл (0,58 ммоль) триэтиламина и 85 мг (0,32 ммоль) 2-йодбензоилацетата. Смесь перемешивали в течение 18 часов при комнатной температуре.
Реакционную смесь вливали в воду и доводили pH до 4. Водную фазу экстрагировали этилацетатом, органическую фазу промывали насыщенным раствором соли и сушили над сульфатом магния.
Растворитель выпаривали и очищали остаток флэш-хроматографией на силикагеле (элюент: гептан/этилацетат=8/2) с получением 47 мг (43%) N-[2-(3,5-дихлор-2-пиридинил)этил]-2-йодбензамида в виде коричневого твердого вещества; т.пл.=133єC.
В соответствии со способом, идентичным получению соединения 5, получали следующие соединения формулы (I), также иллюстрирующие настоящее изобретение: 2, 3, 4, 13, 16, 17, 21, 22, 23, 25 и 26.
Пример способа B: Получение N-[2-(3,5-дихлор-2-пиридинил)этил]-2-(трифторметил)бензамида (соединение 1)
Стадия 1: Получение метилциано(3,5-дихлор-2-пиридинил)ацетата
К 100 мл 1-метил-2-пирролидинона при 0°C медленно порциями добавляли 24,8 г (0,62 моль) гидрида натрия (60% дисперсия в минеральном масле).
К этой суспензии при 5°C по каплям дополнительно добавляли 32,7 г (0,33 моль) метилцианоацетат в 50 мл 1-метил-2-пирролидинона.
Суспензию перемешивали в течение 30 минут при 5°C. Затем к охлажденной суспензии быстро добавляли 70 г (0,3 моль) 2-бром-3,5-дихлорпиридина и нагревали смесь при 130°C в течение 5 часов. После охлаждения реакционную смесь вливали в воду со льдом. Водную фазу экстрагировали этиловым эфиром (3×·300 мл), органическую фазу промывали насыщенным раствором соли и сушили над сульфатом магния.
Растворитель выпаривали при пониженном давлении и перекристаллизовывали неочищенный продукт из метанола с получением 24,8 г (34%) метилциано(3,5-дихлор-2-пиридинил)ацетата в виде коричневых кристаллов; т.пл.=109-110°C.
Стадия 2: Получение (3,5-дихлор-2-пирдинил)ацетонитрила
К раствору 14,45 г (0,06 моль) метилциано(3,5-дихлор-2-пиридинил)ацетата в 70 мл смеси диметилсульфоксид/вода=25/1 добавляли 1,75 г (0,03 моль) хлорида натрия.
Смесь перемешивали в течение 4 часов при 130°C. После охлаждения реакционную смесь вливали в воду со льдом. Водную фазу экстрагировали этиловым эфиром (3×250 мл), органическую фазу промывали насыщенным раствором соли и сушили над сульфатом магния. Растворитель выпаривали при пониженном давлении с получением 11,2 г неочищенного продукта в виде коричневого масла.
Неочищенный продукт очищали флэш-хроматографией на силикагеле (элюент: гептан/этилацетат=7/3) с получением 8,65 г (77%) (3,5-дихлор-2-пиридинил)ацетонитрила в виде желтого масла; данные масс-спектрометрии: 185 (M-1).
Стадия 3: Получение N-[2-(3,5-дихлор-2-пиридинил)этил]-2-трифторметилбензамида (соединение 1)
К раствору 1 г (5,4 ммоль) (3,5-дихлор-2-пиридинил)ацетонитрила в 15 мл метанола быстро добавляли 1,3 г (5,9 ммоль) гексагидрата хлорида кобальта(II) и 3,9 г (10,8 ммоль) 2-трифторметилбензойного ангидрида.
Темно-зеленый раствор охлаждали до -5°C и при 0°C порциями добавляли 1,4 г (37,4 ммоль) боргидрида натрия.
Реакционную смесь перемешивали при комнатной температуре в течение 18 часов. Реакционную смесь нейтрализовали добавлением 1н. хлористоводородной кислоты и удаляли метанол при пониженном давлении. Водную фазу повторно экстрагировали дихлорметаном, органическую фазу промывали насыщенным раствором соли и сушили над сульфатом магния. Растворитель выпаривали при пониженном давлении с получением 2,6 г неочищенного продукта в виде коричневого масла.
Неочищенный продукт очищали флэш-хроматографией на силикагеле (элюент: гептан/этилацетат=7/3) с получением 0,80 г (41%) N-[2-(3,5-дихлор-2-пиридинил)этил]-2-трифторметилбензамида в виде белых кристаллов; т.пл.=118°C.
В соответствии со способом, идентичным получению соединения 1, получали следующие соединения формулы (I), также иллюстрирующие настоящее изобретение: 10, 11, 12 и 15.
Пример способа C/D: Получение N-[2-(3-хлор-2-пиридинил)этил]-2-(трифторметил)бензамида (соединение 6)
Стадия 1: Получение (3-хлор-2-пиридинил)ацетонитрила
К раствору 55,5 мл (0,138 моль) 2,5M бутиллития в 400 мл безводного тетрагидрофурана при -78°C добавляли 6,22 г (0,153 моль) ацетонитрила. Реакционную смесь перемешивали в течение 45 минут при -78°C до образования суспензии.
К полученной суспензии при -78°C медленно добавляли раствор 3 г (0,02 моль) 2,3-дихлорпиридина в 50 мл безводного тетрагидрофурана и дополнительно перемешивали реакционную смесь при -78°C в течение 2 часов.
Реакционную смесь вливали в 50 мл воды. Водную фазу экстрагировали дихлорметаном, органическую фазу промывали водой и сушили над сульфатом магния.
Растворитель выпаривали при пониженном давлении и очищали остаток флэш-хроматографией на силикагеле (элюент: дихлорметан) с получением 1,2 г (40%) (3-хлор-2-пиридинил)ацетонитрила в виде масла; данные масс-спектрометрии: 153 (M+1).
Стадия 2: Получение N-[2-(3-хлор-2-пиридинил)этил]-2-(трифторметил)бензамида (соединение 6)
К раствору 0,152 г (1 ммоль) (3-хлор-2-пиридинил)ацетонитрила в 4 мл метанола последовательно добавляли 0,238 г (1 ммоль) гексагидрата хлорида никеля(II), 0,724 г (2 ммоль) 2-трифторметилбензойного ангидрида и при 0°C медленно добавляли 0,265 г (7 ммоль) боргидрида натрия.
Реакционную смесь перемешивали при комнатной температуре в течение 18 часов. Растворитель выпаривали и очищали остаток флэш-хроматографией на силикагеле (элюент: гептан/этилацетат=9/1) с получением 90 мг (27%) N-[2-(3-хлор-2-пиридинил)этил]-2-(трифторметил)бензамида в виде масла; данные масс-спектрометрии: 329 (M+1).
В соответствии со способом, идентичным получению соединения 6, получали следующие соединения формулы (I), также иллюстрирующие настоящее изобретение: 7, 8 и 9.
Пример способа G: Получение N-[2-(5-метил-2-пиридинил)этил]-2-йодбензамида (соединение 14)
Стадия 1: Получение 5-метил-2-винилпиридина
К раствору 3 г (17,4 ммоль) 2-бром-5-метилпиридина в 30 мл диметилформамида последовательно добавляли 2 г (1,7 ммоль) тетракис(трифенилфосфин)палладия и 5,52 г (17,4 ммоль) трибутил(винил)олова. Реакционную смесь перемешивали при 120°C в течение 18 часов. После охлаждения реакционную смесь вливали в 50 мл воды, насыщенной фторидом калия, и перемешивали в течение 1 часа.
Смесь фильтровали на supersel и экстрагировали водную фазу этиловым эфиром. Органическую фазу дважды промывали насыщенной фторидом калия водой, один раз водой и сушили над сульфатом магния. Растворитель выпаривали при пониженном давлении с получением 3,5 г неочищенной смеси в виде желтого масла.
Смесь очищали флэш-хроматографией на силикагеле (элюент: гептан/этилацетат=4/1) с получением 0,9 г (43%) 5-метил-2-винилпиридина в виде желтого масла; данные масс-спектрометрии: 120 (M+1).
Стадия 2: Получение 2-[2-(5-метил-2-пиридинил)этил]-1H-изоиндол-1,3(2H)-диона
К 0,5 мл гидроксида бензилтриметиламмония (Troton B™) добавляли 0,5 г (4,2 ммоль) 5-метил-2-винилпиридина и 0,618 г (4,2 ммоль) фталимида и нагревали смесь при 200°C в течение 3 часов.
Смесь оставляли остывать до комнатной температуры и непосредственно очищали флэш-хроматографией на силикагеле (элюент: гептан/этилацетат=5/1) с получением 0,680 г (59%) 2-[2-(5-метил-2-пиридинил)этил]-1H-изоиндол-1,3(2H)-диона в виде белых кристаллов; данные масс-спектрометрии: 267 (M+1).
Стадия 3: Получение 2-(5-метил-2-пиридинил)этанамина
К раствору 0,5 г (1,88 ммоль) 2-[2-(5-метил-2-пиридинил)этил]-1H-изоиндол-1,3(2H)-диона в 5 мл метанола добавляли 0,45 г (7,5 моль) гидразингидрата. Реакционную смесь кипятили с обратным холодильником в течение 1 часа до завершения реакции.
Растворитель удаляли в вакууме и подкисляли раствор добавлением 1н. хлористоводородной кислоты. Твердый фталгидразид удаляли фильтрованием. Фильтрат подщелачивали добавлением гидроксида натрия и экстрагировали хлороформом. Органическую фазу промывали водой и сушили над сульфатом магния.
Растворитель выпаривали с получением 0,240 г (94%) чистого 2-(5-метил-2-пиридинил)этанамина в виде желтого масла; данные масс-спектрометрии: 137 (M+1).
Стадия 4: Получение N-[2-(5-метил-2-пиридинил)этил]-2-йодбензамида (соединение 14)
К раствору 0,06 мг (0,44 ммоль) 2-(5-метил-2-пиридинил)этанамина в 3 мл ацетонитрила последовательно добавляли 0,117 мг (0,44 ммоль) 2-йодбензоилхлорида и 0,078 мг (0,44 ммоль) карбоната калия.
Реакционную смесь перемешивали при комнатной температуре в течение 18 часов. Реакционную смесь вливали в водный карбонат калия и экстрагировали водную фазу этилацетатом. Органическую фазу промывали насыщенным раствором соли и сушили над сульфатом магния.
Растворитель выпаривали при пониженном давлении с получением 0,08 г (53%) чистого N-[2-(5-метил-2-пиридинил)этил]-2-йодбензамида в виде бежевых кристаллов; данные масс-спектрометрии: 367 (M+1).
В соответствии со способом, идентичным получению соединения 14, получали соединения 18, 19, 20 и 24, также иллюстрирующие настоящее изобретение.
Примеры биологической активности соединения общей формулы (I)
Пример A: Тест in vivo на Alternaria brassicae (пятнистость листьев крестоцветных)
Тестируемый активный ингредиент в концентрации 100 г/л приготавливали в виде концентрированного состава типа суспензии путем гомогенизации в герметизированном сосуде. Затем эту суспензию разбавляли водой с получением требуемой концентрации активного вещества.
Саженцы редиса (сорта Pernot) в пересадочных горшках, культивируемые на смеси торфяного грунта и вулканического туфа (50/50) при 18-20°C, обрабатывали на стадии семядоли путем опрыскивания описанной выше водной суспензией.
Саженцы, применяемые в качестве контроля, обрабатывали водным раствором, не содержащим активного вещества.
Через 24 часа саженцы заражали путем опрыскивания водной суспензией спор Alternaria brassicae (40000 спор в см3). Споры отбирали из 12-13-суточной культуры.
Зараженные саженцы редиса инкубировали в течение 6-7 суток приблизительно при 18°C во влажной атмосфере.
Оценку качества проводили через 6-7 суток после заражения при сравнении с контрольными саженцами.
В указанных условиях хорошую (по крайней мере, 50%) или полную защиту наблюдали для следующих соединений (взятых в дозе 330 ч./млн): 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 24, 25, 26, 27, 28, 30, 31, 32, 34, 35, 36, 37, 38, 40, 41, 43, 45, 47, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 67 и 68.
Пример B: Тест in vivo на Erysiphe graminis f. sp. tritici (истинная мучнистая роса пшеницы)
Тестируемый активный ингредиент в концентрации 100 г/л приготавливали в виде концентрированного состава типа суспензии путем гомогенизации в герметизированном сосуде. Затем эту суспензию разбавляли водой с получением требуемой концентрации активного вещества.
Саженцы пшеницы (сорта Audace) в пересадочных горшках, культивируемые на смеси торфяного грунта и вулканического туфа (50/50) при 12°C, обрабатывали на стадии одного листа (высотой 10 см) путем опрыскивания описанной выше водной суспензией.
Саженцы, применяемые в качестве контроля, обрабатывали водным раствором, не содержащим активного вещества.
Через 24 часа саженцы заражали путем опыления спорами Erysiphe graminis f. sp. tritici, используя для опыления зараженные растения.
Оценку качества проводили через 7-14 суток после заражения при сравнении с контрольными саженцами.
В указанных условиях хорошую (по крайней мере, 50%) или полную защиту наблюдали для следующих соединений (взятых в дозе 330 ч./млн): 1, 3, 4, 5, 6, 8, 9, 10, 11, 12, 13, 18, 38, 50, 43 и 45.
Пример C: Тест in vivo на Botrytis cinerea (серая гниль огурцов)
Тестируемый активный ингредиент в концентрации 100 г/л приготавливали в виде концентрированного состава типа суспензии путем гомогенизации в герметизированном сосуде. Затем эту суспензию разбавляли водой с получением требуемой концентрации активного вещества.
Саженцы огурцов (сорта Marketer) в пересадочных горшках, культивируемые на смеси торфяного грунта и вулканического туфа (50/50) при 18-20°C, обрабатывали на стадии семядоли Z11 путем опрыскивания описанной выше водной суспензией. Саженцы, применяемые в качестве контроля, обрабатывали водным раствором, не содержащим активного вещества.
Через 24 часа саженцы заражали путем капельного нанесения водной суспензии спор Botrytis cinerea (150000 спор в 1 мл) на верхнюю поверхность листьев. Споры отбирали из 15-суточной культуры и суспендировали в питательном растворе, содержащем 20 г/л желатина, 50 г/л тростникового сахара, 2 г/л NH4NO3 и 1 г/л KH2PO4.
Зараженные саженцы огурцов выращивали в течение 5-7 суток в камере искусственного климата при 15-11°C (день/ночь) и при относительной влажности 80%.
Оценку качества проводили через 5-7 суток после заражения при сравнении с контрольными саженцами. В указанных условиях хорошую (по крайней мере, 50%) или полную защиту наблюдали для следующих соединений (взятых в дозе 330 ч./млн): 1, 2, 3, 4, 5, 6, 9, 10, 13, 18, 21, 22, 23, 25, 26, 27, 28, 29, 32, 34, 35, 38, 40, 43, 44, 45, 46, 47, 50, 51, 52, 53, 57 и 62.
Пример D: Тест in vivo на Pyrenophora teres (сетчатая пятнистость ячменя)
Тестируемый активный ингредиент в концентрации 100 г/л приготавливали в виде концентрированного состава типа суспензии путем гомогенизации в герметизированном сосуде. Затем эту суспензию разбавляли водой с получением требуемой концентрации активного вещества.
Саженцы ячменя (сорта Express) в пересадочных горшках, культивируемые на смеси торфяного грунта и вулканического туфа (50/50) при 12°C, обрабатывали на стадии одного листа (высотой 10 см) путем опрыскивания описанной выше водной суспензией. Саженцы, применяемые в качестве контроля, обрабатывали водным раствором, не содержащим активного вещества.
Через 24 часа саженцы заражали путем опрыскивания водной суспензией спор Pyrenophora teres (12000 спор в 1 мл). Споры отбирали из 12-дневной культуры. Зараженные саженцы ячменя инкубировали в течение 24 часов приблизительно при 20°C и при относительной влажности 100%, и затем в течение 12 суток при относительной влажности 80%.
Оценку качества проводили через 12 суток после заражения при сравнении с контрольными саженцами. В указанных условиях хорошую (по крайней мере, 50%) или полную защиту наблюдали для следующих соединений (взятых в дозе 330 ч./млн): 1, 2, 3, 4, 5, 9, 10, 11, 12, 13, 16, 18, 19, 21, 28, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 45, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 65, 67 и 68.
Раскрытый в патентной заявке WO 01/11965 N-{1-метилкарбамоил-2-[3-хлор-5-(трифторметил)-2-пиридинил]этил}-4-фенилбензамид (см. соединение 316 в таблице D) показал плохую эффективность в отношении Alternaria brassicae и нулевую эффективность в отношении Botrytis cinerea в дозе 330 ч./млн; раскрытый также в патентной заявке WO 01/11965 N-{1-этилкарбамоил-2-[3-хлор-5-(трифторметил)-2-пиридинил]этил}-3-нитробензамид (см. соединение 307 в таблице D) показал плохую эффективность в отношении Alternaria brassicae и нулевую эффективность в отношении Botrytis cinerea в дозе 330 ч./млн; раскрытые также в патентной заявке WO 01/11965 N-{1-этилкарбамоил-2-[3-хлор-5-(трифторметил)-2-пиридинил]этил}бензамид и N-{1-метилкарбамоил-2-[3-хлор-5-(трифторметил)-2-пиридинил]этил}бензамид (см. соединения 304 и 314 в таблице D) показали нулевую эффективность в отношении Botrytis cinerea в дозе 330 ч./млн; и раскрытые в патентной заявке WO 01/11965 N-{1-этилкарбамоил-2-[3-хлор-5-(трифторметил)-2-пиридинил]этил}-4-хлорбензамид, N-{1-этилкарбамоил-2-[3-хлор-5-(трифторметил)-2-пиридинил]этил}-2-бромбензамид и N-{1-метилкарбамоил-2-[3-хлор-5-(трифторметил)-2-пиридинил]этил}-4-метоксибензамид (см. соединения 306, 310 и 315 в таблице D) показали нулевую эффективность в отношении Botrytis cinerea в дозе 330 ч./млн.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ ФЕНИЛУКСУСНОЙ КИСЛОТЫ, ПРОМЕЖУТОЧНЫЕ ПРОДУКТЫ ДЛЯ ИХ ПОЛУЧЕНИЯ И СОДЕРЖАЩИЕ ИХ СРЕДСТВА | 1995 |
|
RU2165411C2 |
| НЕМАТОЦИДНЫЕ СУЛЬФОНАМИДЫ | 2010 |
|
RU2531317C2 |
| ПРОИЗВОДНЫЕ ФЕНИЛУКСУСНОЙ КИСЛОТЫ И СРЕДСТВО БОРЬБЫ ПРОТИВ НАСЕКОМЫХ И ПАУКООБРАЗНЫХ И ПРОТИВ ВРЕДОНОСНЫХ ГРИБОВ | 1995 |
|
RU2162075C2 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ АМИНЫ И ИХ ПРИМЕНЕНИЕ | 2011 |
|
RU2632900C2 |
| НОВЫЕ СОЕДИНЕНИЯ НА ОСНОВЕ ОКСАДИАЗОЛА ДЛЯ КОНТРОЛЯ ФИТОПАТОГЕННЫХ ГРИБОВ ИЛИ ПРЕДУПРЕЖДЕНИЯ ПОРАЖЕНИЯ ИМИ | 2020 |
|
RU2818085C2 |
| КАРБОКСАМИДНЫЕ СОЕДИНЕНИЯ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНГИБИТОРОВ КАЛЬПАИНА | 2010 |
|
RU2540856C2 |
| АМИДЫ N-СУЛЬФОНИЛ- И N-СУЛЬФИНИЛАМИНОКИСЛОТ В КАЧЕСТВЕ МИКРОБИЦИДОВ | 1995 |
|
RU2140411C1 |
| ФУНГИЦИДНЫЕ ФЕНИЛПИРИМИДИНИЛАМИНО ПРОИЗВОДНЫЕ | 2008 |
|
RU2459819C2 |
| МОЛЕКУЛА, ПЕСТИЦИДНАЯ КОМПОЗИЦИЯ НА ЕЕ ОСНОВЕ (ВАРИАНТЫ) И СПОСОБ ПРИМЕНЕНИЯ МОЛЕКУЛЫ (ВАРИАНТЫ) | 2010 |
|
RU2543806C2 |
| НОВЫЕ СОЕДИНЕНИЯ, КОТОРЫЕ ЯВЛЯЮТСЯ ИНГИБИТОРАМИ ERK | 2013 |
|
RU2660429C2 |
Изобретение описывает новые 2-пиридинилэтилбензамидные соединения общей формулы (I) 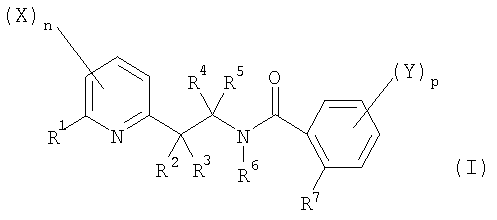
в которой: n равно 1, 2 или 3; X является одинаковым или различным и представляет собой атом водорода, атом галогена, С1-С8алкил; R1 представляет собой атом водорода, атом галогена, пентафтор-λ6-сульфанильную группу, С1-С8алкил; при условии, что Х и R1 оба не являются атомом водорода; R2 и R3 являются одинаковыми или различными и представляют собой атом водорода, C1-С6алкил; или R2 и R3 могут вместе образовывать 3-, 4-, 5- или 6-членный карбоцикл; R4 и R5 являются одинаковыми или различными и представляют собой атом водорода; R6 представляет собой атом водорода, C1-С6алкил, p равно 1, 2, 3 или 4; Y является одинаковым или различным и представляет собой атом водорода, атом галогена; и R7 представляет собой атом галогена, С1-С8алкил, содержащий 1-5 атомов галогена С1-С8галогеналкил, а также его соли, N-оксиды, металлосодержащие и металлоидсодержащие комплексы. А также способ получения этого соединения и фунгицидная композиция, содержащая соединение общей формулы (I), способ обработки растений путем нанесения соединения общей формулы (I) или содержащей его композиции. Технический результат: получены новые соединения, которые могут найти свое применение в сельском хозяйстве. 10 н. и 11 з.п. ф-лы, 1 табл.
1. Соединение общей формулы (I):
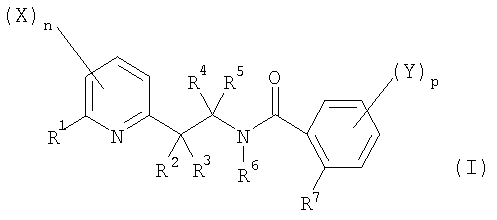
в которой
n равно 1, 2 или 3;
X является одинаковым или различным и представляет собой атом водорода, атом галогена, С1-С8алкил;
R1 представляет собой атом водорода, атом галогена,
пентафтор-λ6-сульфанильную группу, С1-С8алкил;
при условии, что Х и R1 оба не являются атомом водорода;
R2 и R3 являются одинаковыми или различными и представляют собой атом водорода, C1-С6алкил;
или R2 и R3 могут вместе образовывать 3-, 4-, 5- или 6-членный карбоцикл;
R4 и R5 являются одинаковыми или различными и представляют собой атом водорода;
R6 представляет собой атом водорода, С1-С6алкил,
p равно 1, 2, 3 или 4;
Y является одинаковым или различным и представляет собой атом водорода, атом галогена; и
R7 представляет собой атом галогена, С1-С8алкил,
содержащий 1-5 атомов галогена С1-С8галогеналкил,
а также его соли, N-оксиды, металлосодержащие и металлоидсодержащие комплексы.
2. Соединение по п.1, отличающееся тем, что R1 представляет собой атом водорода или атом галогена.
3. Соединение по п.1 или 2, отличающееся тем, что n равно 1 или 2.
4. Соединение по п.1, отличающееся тем, что Х представляет собой атом галогена или С1-С8алкил.
5. Соединение по п.1, отличающееся тем, что 2-пиридил замещен Х в 3-м и/или в 5-м положении.
6. Соединение по п.1, отличающееся тем, что R7 представляет собой атом галогена, С1-С8алкил или содержащий 1-5 атомов галогена С1-С8галогеналкил.
7. Соединение по п.1, отличающееся тем, что p равно 1 или 2.
8. Соединение по п.7, отличающееся тем, что p равно 1.
9. Соединение по п.1, отличающееся тем, что Y представляет собой атом водорода, атом галогена.
10. Соединение по п.9, отличающееся тем, что Y представляет собой атом водорода.
11. Соединение по п.1, отличающееся тем, что фенил замещен Y предпочтительно сначала в параположении.
12. Способ А получения соединения общей формулы (Ia)
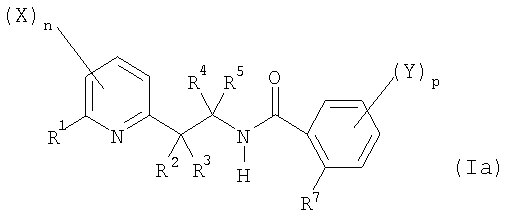
в которой
R1, R2, R7, X, Y, n и p определены в п.1;
R3 представляет собой C1-С6алкил;
который включает:
- первую стадию в соответствии со схемой реакции А-1:
Схема А-1
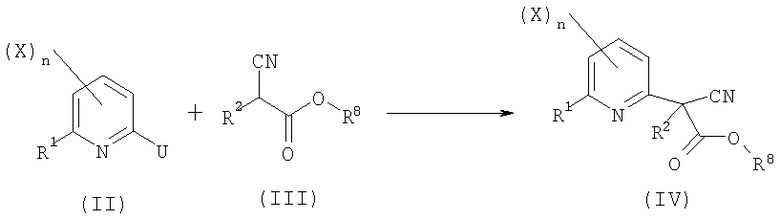
где
R1, R2, Х и n определены в п.1;
R8 представляет собой C1-С6алкил, C1-С6галогеналкил, бензил, 4-метоксибензил или пентафторфенил;
U представляет собой уходящую группу, выбранную из галогена, C1-С6алкилсульфоната или C1-С6галогеналкилсульфоната;
включающую арилирование производного цианоацетата общей формулы (III) производным пиридина общей формулы (II) в присутствии основания при температуре от 0 до 200°С с получением производного 2-пиридилцианоацетата общей формулы (IV);
вторую стадию в соответствии со схемой реакции А-2:
Схема А-2

где
R1, R2, X, n определены в п.1;
R8 представляет собой C1-С6алкил, C1-С6галогеналкил, бензил, 4-метоксибензил или пентафторфенил;
включающую гидролиз в щелочной среде, гидролиз в кислой среде или замещение галогенидом соединения общей формулы (IV) в том же самом или другом сосуде при нагревании при температуре от 40°С до температуры дефлегмации с получением производного 2-пиридилацетонитрила общей формулы (Va);
третью стадию в соответствии со схемой реакции А-3:
Схема А-3

где
R1, R2, X, n определены в п.1;
R3 представляет собой С1-С6алкил;
W представляет собой атом галогена, C1-С6алкилсульфонат, С1-С6галогеналкилсульфонат или 4-метилфенилсульфонат, включающую алкилирование соединения общей формулы (Va) реагентом общей формулы (XVII) с получением соединений общей формулы (Vb);
четвертую стадию в соответствии со схемой реакции А-4:
Схема А-4
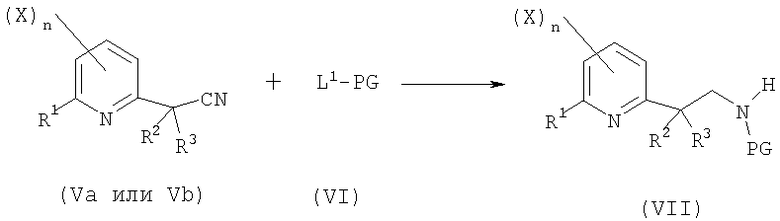
где
R1, R2, X, n определены в п.1;
R3 представляет собой атом водорода и C1-С6алкил;
L1 представляет собой уходящую группу, выбранную из -OR8-группы или -OCOR8-группы, где R8 представляет собой C1-С6алкил, C1-С6галогеналкил, бензил, 4-метоксибензил или пентафторфенил;
PG представляет собой защитную группу, которой может являться -COOR8-группа или -COR8-группа, где R8 представляет собой C1-С6алкил, C1-С6галогеналкил, бензил, 4-метоксибензил или пентафторфенил;
включающую восстановление соединения общей формулы (Va) или (Vb) путем гидрирования или обработки гидридным донором в присутствии катализатора и в присутствии соединения общей формулы (VI) при температуре от 0 до 150°С и при давлении от 1 до 100 бар с получением соединения общей формулы (VII);
пятую стадию в соответствии со схемой реакции А-5:
Схема А-5
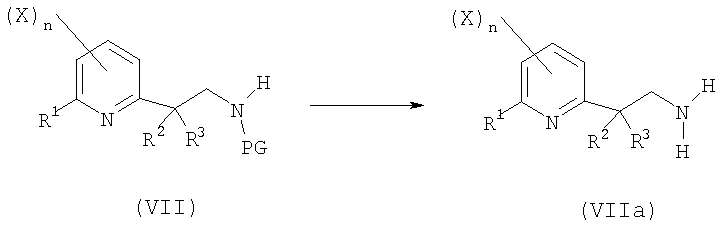
где
R1, R2, X, n определены в п.1;
R3 представляет собой C1-С6алкил;
PG представляет собой защитную группу, которой может являться -COOR8-группа или -COR8-группа, где R8 представляет собой C1-С6алкил, C1-С6галогеналкил, бензил, 4-метоксибензил или пентафторфенил;
включающую реакцию снятия защиты с соединения общей формулы (VII) в кислой или в щелочной среде с получением производного амина общей формулы (VIIIa) или одной из его солей;
шестую стадию в соответствии со схемой реакции А-6:
Схема А-6
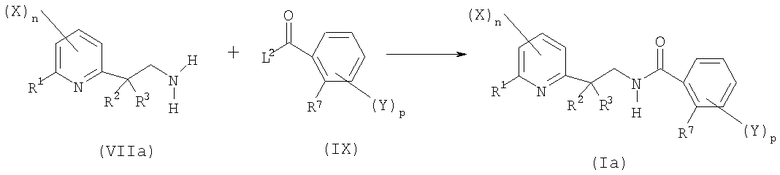
где
R1, R2, R7, X, Y, n и р определены в п.1;
R3 представляет собой C1-С6алкил;
L2 представляет собой уходящую группу, выбранную из атома галогена, гидроксильной группы, -OR8-группы, -OCOR8, где R8 представляет собой C1-С6алкил, C1-С6галогеналкил, бензил, 4-метоксибензил или пентафторфенил, или группы формулы 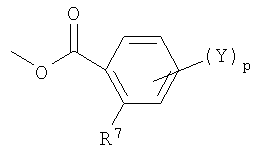 ,
,
включающую реакцию сочетания производного амина общей формулы (VIIIa) или одной из его солей с производным карбоновой кислоты формулы (IX) с получением соединения общей формулы (Ia).
13. Способ В получения соединения общей формулы (Ia)
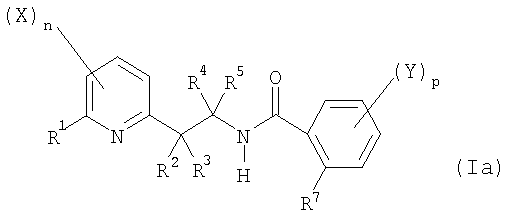
в которой
R1, R2, R7, X, Y, n и р определены в п.1;
R3 представляет собой C1-С6алкил;
который включает:
первую стадию в соответствии со схемой реакции В-1:
Схема В-1
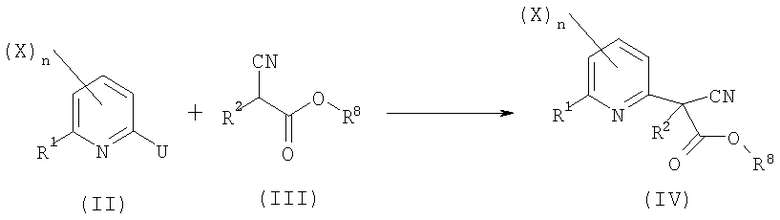
где
R1, R2, X и n определены выше;
R8 представляет собой C1-С6алкил, C1-С6галогеналкил, бензил, 4-метоксибензил или пентафторфенил;
U представляет собой уходящую группу, выбранную из атома галогена, С1-С6алкилсульфоната или С1-С6галогеналкилсульфоната;
включающую арилирование производного цианоацетата общей формулы (III) производным пиридина общей формулы (II) с получением производного 2-пиридилцианоацетата общей формулы (IV);
вторую стадию в соответствии со схемой реакции В-2:
Схема В-2
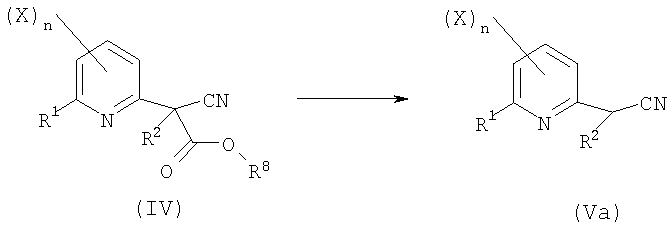
где
R1, R2, X, n определены в п.1;
R8 представляет собой C1-С6алкил, С1-С6галогеналкил, бензил, 4-метоксибензил или пентафторфенил;
включающую гидролиз в щелочной среде, гидролиз в кислой среде или замещение галогенидом соединения общей формулы (IV) в том же самом или другом сосуде при нагревании при температуре от 40°С до температуры дефлегмации с получением производного 2-пиридилацетонитрила общей формулы (Va);
третью стадию в соответствии со схемой реакции В-3:
Схема В-3
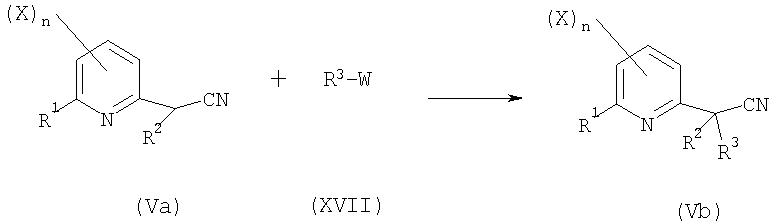
где
R1, R2, X, n определены в п.1;
R3 представляет собой C1-С6алкил;
W представляет собой атом галогена, С1-С6алкилсульфонат, C1-С6галогеналкилсульфонат или 4-метилфенилсульфонат,
включающую алкилирование соединения общей формулы (Va) реагентом общей формулы (XVII) с получением соединения общей формулы (Vb);
четвертую стадию в соответствии со схемой реакции В-4:
Схема В-4
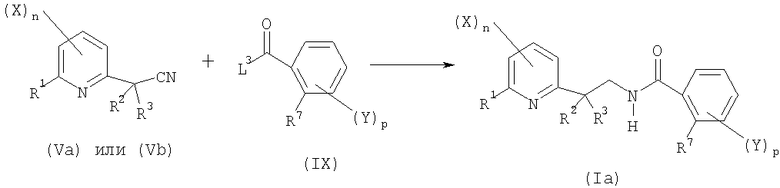
где
R1, R2, R7, X, Y, n и р определены в п.1;
R3 представляет собой C1-С6алкил;
L3 представляет собой уходящую группу, выбранную из -OCOR8, где R8 представляет собой C1-С6алкил, С1-С6галогеналкил, бензил, 4-метоксибензил или пентафторфенил; -ОСНО, -SCSN(Me)2 или группы формулы  ,
,
включающую восстановление соединения общей формулы (Va) или соединения общей формулы (Vb) путем гидрирования или обработки гидридным донором в присутствии катализатора и в присутствии соединения общей формулы (IX) при температуре от 0 до 150°С и при давлении от 1 до 100 бар с получением соединения общей формулы (Ia).
14. Способ С получения соединения общей формулы (Ia)

в которой
R1, R2, R3, R7, X, Y, n и р определены в п.1;
который включает:
первую стадию в соответствии со схемой реакции С-1:
Схема С-1

где
R1, R2, R3, X и n определены в п.1;
U представляет собой уходящую группу, выбранную из атома галогена, C1-С6алкилсульфоната или С1-С6галогеналкилсульфоната;
включающую арилирование соединения общей формулы (IIIb) производным пиридина общей формулы (II) в присутствии основания при температуре от -100 до 200°С с получением производного 2-пиридилацетонитрила общей формулы (Vb);
- вторую стадию в соответствии со схемой реакции С-2:
Схема С-2
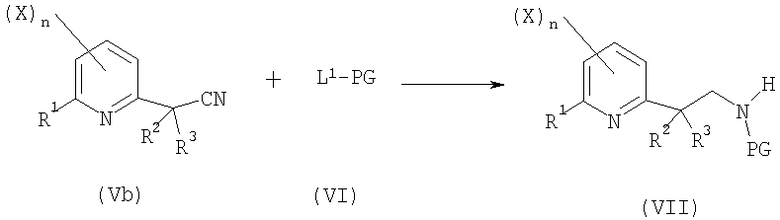
где
R1, R2, R3, Х и n определены в п.1;
L1 представляет собой уходящую группу, выбранную из -OR -группы или -OCOR8-группы, где R8 представляет собой C1-С6алкил, С1-С6галогеналкил, бензил, 4-метоксибензил или пентафторфенил;
PG представляет собой защитную группу, которой может являться -COOR8-группа или -COR8-группа, где R8 представляет собой C1-С6алкил, C1-С6галогеналкил, бензил, 4-метоксибензил или пентафторфенил;
включающую восстановление соединения общей формулы (Va) или (Vb) путем гидрирования или обработки гидридным донором в присутствии соединения общей формулы (VI) с получением соединения общей формулы (VII);
третью стадию в соответствии со схемой реакции С-3:
Схема С-3

где
R1, R2, R3, Х и n определены в п.1;
PG представляет собой защитную группу, которой может являться -COOR8-группа или -COR8-группа, где R8 представляет собой C1-С6алкил, C1-С6галогеналкил, бензил, 4-метоксибензил или пентафторфенил;
включающую реакцию снятия защиты с соединения общей формулы (VII) в кислой или в щелочной среде с получением производного амина общей формулы (VIIIa) или одной из его солей;
четвертую стадию в соответствии со схемой реакции С-4:
Схема С-4
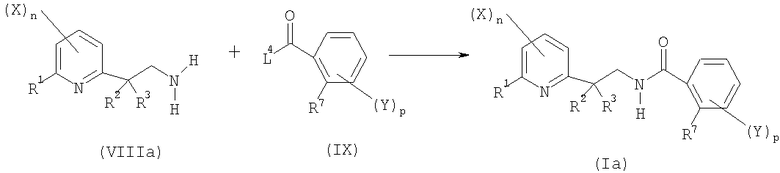
где
R1, R2, R3, R7, X, Y, n и p определены в п.1;
L4 представляет собой уходящую группу, выбранную из атома галогена, гидроксильной группы, -ОСНО, -SCSN(Me)2, -OR8-группы, -OCOR8, где R8 представляет собой C1-С5алкил, C1-С6галогеналкил, бензил, 4-метоксибензил или пентафторфенил, или группы формулы 
включающую реакцию сочетания производного амина общей формулы (VIIIa) или одной из его солей с производным карбоновой кислоты формулы (IX) с получением соединения общей формулы (Ia).
15. Способ D получения соединения общей формулы (Ia)

в которой
R1, R2, R7, X, Y, n и p определены в п.1;
R3 представляет собой С1-С6алкил;
который включает:
первую стадию в соответствии со схемой реакции D-1:
Схема D-1

где
R1, R2, R3, Х и n определены в п.1;
U представляет собой уходящую группу, выбранную из атома галогена, C1-С6алкилсульфоната или C1-С6галогеналкилсульфоната;
включающую арилирование соединения общей формулы (IIIb) производным пиридина общей формулы (II) в присутствии основания при температуре от -100 до 200°С с получением производного 2-пиридилацетонитрила общей формулы (Vb);
вторую стадию в соответствии со схемой реакции D-2:
Схема D-2

где
R1, R2, R7, X, Y, n и р определены в п.1;
R3 представляет собой C1-С6алкил;
L3 представляет собой уходящую группу, выбранную из -OCOR8, где R8 представляет собой С1-С6алкил, C1-С6галогеналкил, бензил, 4-метоксибензил или пентафторфенил; -ОСНО, -SCSN(Me)2 или группы формулы  ,
,
включающую восстановление соединения общей формулы (Va) или соединения общей формулы (Vb) путем гидрирования или обработки гидридным донором в присутствии соединения общей формулы (IX) с получением соединения общей формулы (Ia).
16. Способ Е получения соединения общей формулы (Ia)
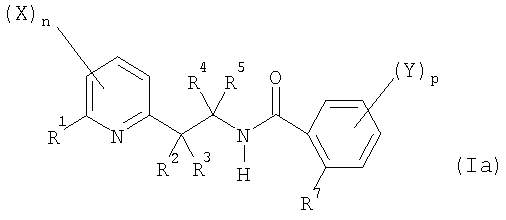
в которой
R1, R2, R3, R7, X, Y, n и р определены в п.1;
R4 представляет собой атом водорода, C1-С6алкил или C1-С6галогеналкил;
R5 представляет собой C1-С6алкил или С1-С6галогеналкил;
L4 представляет собой уходящую группу, выбранную из атома галогена, гидроксильной группы, -ОСНО, -SCSN(Me)2, -OR8-группы, -OCOR8, где R8 представляет собой C1-С6алкил, C1-С6галогеналкил, бензил, 4-метоксибензил или пентафторфенил, или группы формулы  ,
,
который включает:
первую стадию в соответствии со схемой реакции Е-1:
Схема Е-1

где
R1, R2, R3, Х и n определены в п.1;
R4 представляет собой атом водорода, C1-С6алкил или C1-С6галогеналкил;
U представляет собой уходящую группу, выбранную из атома галогена, С1-С6алкилсульфоната или С1-С6галогеналкилсульфоната;
включающую арилирование соединения общей формулы (X) производным пиридина общей формулы (II) с получением соединения общей формулы (XI);
вторую стадию в соответствии со схемой реакции Е-2:
Схема Е-2

где
R1, R2, R3, Х и n определены в п.1;
R4 представляет собой атом водорода, С1-С6алкил или C1-С6галогеналкил;
включающую преобразование соединения общей формулы (XI) в соединение общей формулы (XIII) путем добавления соединения общей формулы R5-M, в которой R5 представляет собой C1-С6алкил или С1-С6галогеналкил и М является частицей металла;
третью стадию в соответствии со схемой реакции Е-3:
Схема Е-3

где
R1, R2, R3, Х и n определены в п.1;
R4 представляет собой атом водорода, C1-С6алкил или C1-С6галогеналкил;
R5 представляет собой C1-С6алкил или C1-С6галогеналкил;
W представляет собой уходящую группу, выбранную из атома галогена, C1-С6алкилсульфоната, C1-С6галогеналкилсульфоната или 4-метилфенилсульфоната;
включающую активацию соединения общей формулы (XIII) путем преобразования его в соединение общей формулы (XIV);
четвертую стадию в соответствии со схемой реакции Е-4:
Схема Е-4

где
R1, R2, R3, Х и n определены в п.1;
R4 представляет собой атом водорода, С1-С6алкил или C1-С6галогеналкил;
R5 представляет собой C1-С6алкил или C1-С6галогеналкил;
W представляет собой уходящую группу, выбранную из атома галогена, C1-С6алкилсульфоната, C1-С6галогеналкилсульфоната или 4-метилфенилсульфоната;
включающую замещение соединения общей формулы (XIV) производным фталимида или одной из его солей с получением соединения общей формулы (XVa);
пятую стадию в соответствии со схемой реакции Е-5:
Схема Е-5
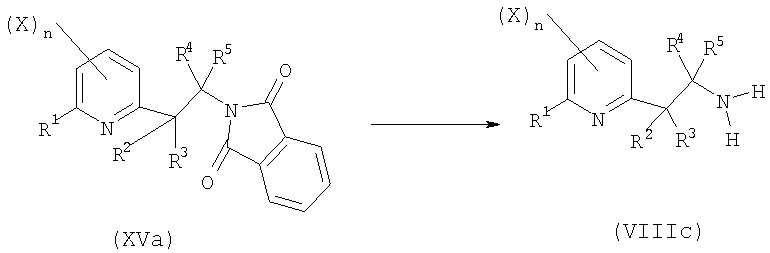
где
R1, R2, R3, Х и n определены в п.1;
R4 представляет собой атом водорода, C1-С6алкил или C1-С6галогеналкил;
R5 представляет собой C1-С6алкил или C1-С6галогеналкил;
включающую реакцию снятия защиты с соединения общей формулы (XVa) путем его взаимодействия с гидразингидратом или солью гидразина с получением производного амина общей формулы (VIIIc) или одной из его солей;
шестую стадию в соответствии со схемой реакции Е-6:
Схема Е-6
 где
где
R1, R2, R3, R7, X, Y, n и р определены в п.1;
R4 представляет собой атом водорода, С1-С6алкил или C1-С6галогеналкил;
R5 представляет собой С1-С6алкил или C1-С6галогеналкил;
L4 представляет собой уходящую группу, выбранную из атома галогена, гидроксильной группы, -ОСНО, -SCSN(Me)2, -OR8-группы, -OCOR8, где R8 представляет собой C1-С6алкил, C1-С6галогеналкил, бензил, 4-метоксибензил или пентафторфенил, или группы формулы  ,
,
включающую реакцию сочетания производного амина общей формулы (VIIIb) или одной из его солей с производным карбоновой кислоты формулы (IX) с получением соединения общей формулы (Ia).
17. Способ F получения соединения общей формулы (Ia)

в которой
R1, R7, X, Y, n и р определены в п.1;
R2, R4 и R5 независимо друг от друга выбирают из атома водорода, C1-С6алкила или С1-С6галогеналкила;
который включает:
первую стадию в соответствии со схемой реакции F-1:
Схема F-1

где
R1, Х и n определены в п.1;
U представляет собой уходящую группу, выбранную из атома галогена, C1-С6алкилсульфоната или C1-С6галогеналкилсульфоната;
R2, R4 и R5 независимо друг от друга выбирают из атома водорода, С1-С6алкила или C1-С6галогеналкила;
М является частицей металла или металлоида;
включающую реакцию сочетания производного пиридина общей формулы (II) с винильным производным общей формулы (XVI) при температуре от 0 до 200°С с получением соединения общей формулы (XVII);
вторую стадию в соответствии со схемой реакции F-2:
Схема F-2

где
R1, Х и n определены в п.1;
R2, R4 и R5 независимо друг от друга выбирают из атома водорода, C1-С6алкила или C1-С6галогеналкила;
включающую добавление фталимида или одной из его солей к соединению общей формулы (XVII) с получением соединения общей формулы (XVb);
третью стадию в соответствии со схемой реакции F-3:
Схема F-3

где
R1, Х и n определены в п.1;
R2, R4 и R5 независимо друг от друга выбирают из атома водорода, C1-С6алкила или C1-С6галогеналкила;
включающую реакцию снятия защиты с соединения общей формулы (XVb) гидразингидратом или с солью гидразина с получением производного амина общей формулы (VIIId) или одной из его солей;
четвертую стадию в соответствии со схемой реакции F-4:
F-4
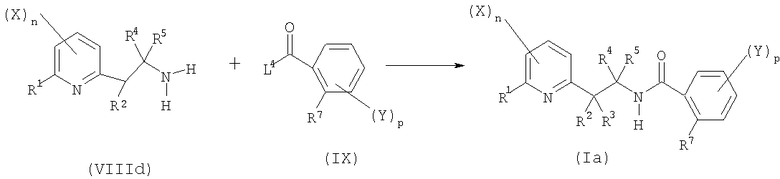
где
R1, R7, X, Y, n и p определены в п.1;
R2, R и R5 независимо друг от друга выбирают из атома водорода, C1-С6алкила или C1-С6галогеналкила;
L4 представляет собой уходящую группу, выбранную из атома галогена, гидроксильной группы, -ОСНО, -SCSN(Me)2, -OR8-группы, -OCOR8, где R8 представляет собой C1-С6алкил, C1-С6галогеналкил, бензил, 4-метоксибензил или пентафторфенил, или группы формулы  ,
,
включающую реакцию сочетания производного амина общей формулы (VIIIb) или одной из его солей с производным карбоновой кислоты формулы (IX) с получением соединения общей формулы (Ia).
18. Способ по любому из пп.12-17, который дополнительно включает дополнительную стадию в соответствии со схемой реакции G:
Схема G

где
R1, R2, R3, R4, R5, R6, R7, X, Y, n и р определены в п.1;
L5 представляет собой уходящую группу, выбранную из атома галогена, 4-метилфенилсульфонилоксигруппы, метилсульфонилоксигруппы;
включающую взаимодействие соединения общей формулы (Ia) с соединением общей формулы (XVI) с получением соединения общей формулы (Ib).
19. Способ получения соединения общей формулы (I) по п.1, который включает:
первую стадию в соответствии со схемой реакции Н-1:
Схема Н-1
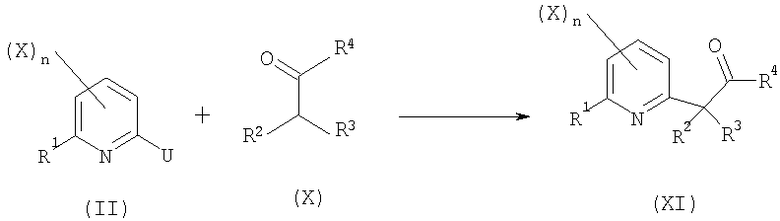
где
R1, R2, R3, X и n определены в п.1;
R4 представляет собой атом водорода, C1-С6алкил или C1-С6галогеналкил;
U представляет собой уходящую группу, выбранную из атома галогена, C1-С6алкилсульфоната или C1-С6галогеналкилсульфоната;
включающую арилирование соединения общей формулы (X) производным пиридина общей формулы (II) в присутствии основания при температуре от 0 до 200°С с получением соединения общей формулы (XI);
вторую стадию в соответствии со схемой реакции Н-2:
Схема Н-2
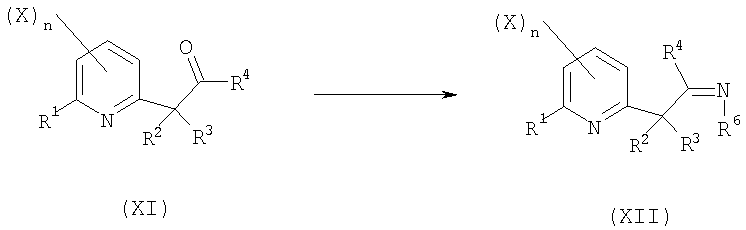
где
R1, R2, R3, X и n определены в п.1;
R4 представляет собой атом водорода, С1-С6алкил или С1-С6галогеналкил;
R6 представляет собой атом водорода, C1-С6алкил или С1-С6галогеналкил, C1-С6алкоксигруппу или С3-С7-циклоалкил;
включающую взаимодействие соединения общей формулы (XI) с амином формулы R6-NH2 с получением иминопроизводного общей формулы (XII);
третью стадию в соответствии со схемой реакции Н-3:
Схема Н-3

где
R1, R2, R3, Х и n определены в п.1;
R4 представляет собой атом водорода, C1-С6алкил или C1-С6галогеналкил;
R6 представляет собой атом водорода, C1-С6алкил, C1-С6галогеналкил, C1-С6алкоксигруппу или С3-С7-циклоалкил;
включающую восстановление иминопроизводного общей формулы (XII) путем гидрирования или обработки гидридным донором в том же самом или другом сосуде с получением производного амина общей формулы (VIIIb) или одной из его солей;
четвертую стадию в соответствии со схемой реакции Н-4:
Схема Н-4
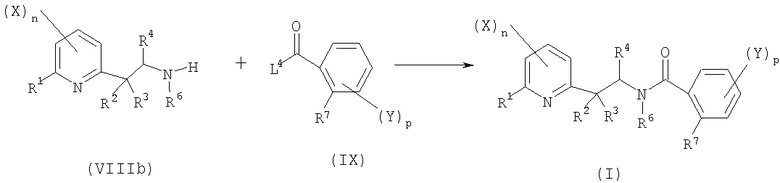
где
R1, R2, R3, R7, X, Y, n и р определены в п.1;
R4 представляет собой атом водорода, C1-С6алкил или C1-С6галогеналкил;
R6 представляет собой атом водорода, C1-С6алкил, C1-С6галогеналкил, C1-С6алкоксигруппу или С3-С7-циклоалкил;
L4 представляет собой уходящую группу, выбранную из атома галогена, гидроксильной группы, -ОСНО, -SCSN(Me)2, -OR8-группы, -OCOR8, где R8 представляет собой С1-С6алкил, C1-С6галогеналкил, бензил, 4-метоксибензил или пентафторфенил, или группы формулы  ,
,
включающую реакцию сочетания производного амина общей формулы (VIIIb) или одной из его солей с производным карбоновой кислоты формулы (IX) с получением соединения общей формулы (I).
20. Фунгицидная композиция, содержащая эффективное количество соединения по п.1 и приемлемую с точки зрения сельского хозяйства основу.
21. Способ профилактического или лечебного контроля роста фитопатогенных грибов на сельскохозяйственных культурах, отличающийся тем, что эффективное и нетоксичное количество композиции по п.20 наносят на семена растения, на листья растения и/или на плоды растений или на почву, на которой растение произрастает или на которой его требуется вырастить.
| 0 |
|
SU284174A1 | |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
| US 3995044 A, 30.11.1976 | |||
| US 4006239 A, 01.02.1977 | |||
| Способ получения производных алкилендиамина | 1988 |
|
SU1563594A3 |
| Способ получения производных 2(3-пиридил)-2-фениламиноуксусной кислоты (его варианты) | 1984 |
|
SU1316557A3 |
Авторы
Даты
2009-04-20—Публикация
2004-07-19—Подача