Изобретение относится к области электрохимического синтеза алкоголятов тантала. Интерес к этим продуктам базируется на перспективе их использования как предшественников высокочистых и высокодисперсных моно- и смешанных оксидных композиций для нанотехнологических процессов. Керамические материалы на их основе обладают высокой диэлектрической проницаемостью и низким тангенсом угла диэлектрических потерь, что привело к созданию добротных диэлектрических резонаторов для целей современной СВЧ-микроэлектроники. Оксид тантала (Ta2O5) используют в качестве диэлектрика в прецизионных кондесаторах, интегральных схемах.
Широкому использованию алкоголятов тантала особенно в крупном масштабе препятствует несовершенство их синтеза - трудность осуществления реакций и очистки конечных продуктов, малая доступность исходных реагентов.
Известные способы получения алкоголятов тантала в большинстве своем основаны на реакции между галогенидом Та (V) и соответствующим алкильным спиртом в присутствии газообразного аммиака (NH3), необходимого для связывания галогенсодержащей кислоты, выделяющейся в ходе реакции. Это многостадийные и весьма трудоемкие процессы, не отвечающие современным требованиям экологии. Так, согласно патенту Японии (№1045325, 1989 г.) для получения соответствующего алкоголята тантала галогенид Та (V) подвергают многоступенчатой очистке, включающей его экстракцию смешанным органическим растворителем из водного раствора HF+H2SO4, последующую экстракцию, осаждение галогенида смесью KOH+KF, растворение осадка при контролируемом рН и, наконец, извлечение целевого галогенида тантала растворителем эфирного типа и отделение растворителя.
Известны способы получения алкоголятов металлов, в том числе и тантала, с относительно высокой молекулярной массой, которые основаны на реакции переэтерификации более низкомолекулярных алкоголятов, например изопропокси- и бутокситантала из метокси- или этокситантала по схемам:
Та(ОСН3)5+5С3Н7OH→Та(ОС3Н7)5+5СН3ОН
Та(ОС2Н5)5+5С3Н7OH→Та(ОС3Н7)5+5С4Н9OH
Та(ОС2Н5)5+5С4Н9OH→Та(ОС4Н9)5+5С4Н9OH
Та(ОСН3)5+5С4Н9OH→Та(ОС4Н9)5+5СН3ОН
(D.C.Bradley, R.C.Mehrotra, D.P.Gaur, Metal Press, London, 1978).
Существенным недостатком этих известных способов является недоступность низкомолекулярных алкоголятов тантала (метокси- и этокси-) из-за отсутсвия их производства.
Перспективным направлением получения изопропокситантала и бутокситантала, а также более низкомолекулярных алкоголятов, которые могут быть использованы в указанных реакциях переэтерификации, является применение эелектрохимических способов синтеза этих соединений, основанных на анодном растворении тантала в соответствующих C1-C4 алифатических спиртах.
Известные способы получения алкоголятов тантала электрохимическим способом касаются, в основном, электросинтеза этокситантала. Так, по способу, изложенному в пат. Англии №1307581 (1973), электрохимическое растворение тантала проводили в этанольном растворе, содержащем электропроводную добавку типа [N(R)4]X, где R - алкил или водород, Х - галоген. Электролиз вели при температуре кипения растворителя, напряжении 40-60 В и силе постоянного тока 0,5-2,0 А. Выход алкоголята по току составил 91%. Плотность тока и выход по веществу продукта не указаны.
Недостатком способа являются его низкая эффективность, связанная с уменьшением в ходе процесса токовой нагрузки с 2,0 А до 0,7 А и ростом напряжения в процессе электролиза до 80 В.
Также с выходом по току, равным 91%, получен этокситантал в работе V.A.Shreider et al, Direct Electrochemical Synthesis of Metal Alkoxides (Inorg. Chimica Acta, 53, pp.73-76, 1981). Процесс вели при токовой нагрузке 0,2 А и общем напряжении 30 В, в качестве электропроводящей добавки использовали тетрабутиламмонийбромид (Bu)4NBr. После 10 часов электролиза было получено 5,5 г этокситантала Та(ОС2Н5)5, который очищали вакуумной дистилляцией.
Недостаток способа - высокая энергоемкость процесса (рассчитанный расход электроэнергии на основании данных, приведенных в работе, составил ~11,0 кВт·ч/кг; в качестве электропроводной добавки используют малодоступный и трудноочищаемый (Bu)4NBr.
Известен способ получения этокситантала с выходом по току 97% (Пат. США №3730857, 1973). Электролиз вели в горячем этаноле, насыщенном хлористым аммонием. Постоянный ток силой 0,25-0,4 А подавали на электроды после их предварительной переменнотоковой поляризации в течение 20 минут. После пропускания 6 ампер-часов при напряжении 50 В электролизный раствор содержал 17,6 г Та(ОС2Н5)5.
Недостаток способа - сложность электрохимической стадии, связанная с необходимостью предварительной переменнотоковой поляризации электродов, высокая энергоемкость процесса, обусловленная, по-видимому, малой растворимостью NH4Cl в этаноле (рассчитанный расход электроэнергии составляет ~17,0 кВт·ч/кг), невозможность по предлагаемому способу получить прямым электрохимическим методом изопропокси- бутокситантал из-за практической нерастворимости хлористого аммония в изопропаноле и бутаноле.
Известен способ (авт. свид. №1008282, 1981) получения алкоголятов тантала под действием переменного тока промышленной частоты в C1-C4-алкиловых спиртах, содержащих инертный разбавитель (ацетонитрил, диметилсульфоксид, диметилформамид) и электропроводную добавку общей формулы КХ, где К - катион щелочного металла, аммония или четвертичного аммонийного основания, Х - галоген, ClO4-, BF- в количестве 2-20%. Электролиз вначале вели постоянным током до прекращения осаждения окислов металлов, а затем переменным током силой 0,5 А и напряжением 220 В. Выход этокситантала по току и веществу составил 68% и 71% соответственно.
Недостатком способа является сложная система электролиза, высокий расход электроэнергии, обусловленный высоким напряжением и низкими выходами по току и веществу целевого продукта. При этом использование различных по своей природе растворителей и повышение концентрации электропроводящей добавки являются дополнительными источниками загрязнения целевого продукта.
Наиболее близкий по своему содержанию к предлагаемому изобретению способ изложен в работе (N.Ya.Turova, A.V.Korolev, D.E.Tchebukov and A.I.Belokon, Tantalum (V) Alkoxides: Electrochemical Synthesis, Mass-spectral Investigation and oxoalkoxocomplexes. Polyhedron, Vol.15, No.21, pp.3869-3880, 1996).
По этому способу электрохимический синтез алкоголятов тантала проводили в стеклянной ячейке, снабженной термостатирующей рубашкой и обратным холодильником, с электродным пакетом из тантала и катодом из платины или нержавеющей стали. В качестве электролизного раствора использовали соответствующий спирт с растворенным в нем хлоридом лития, который предварительно сушили в вакууме при 80-100°С, а спирты обезвоживали на Al(OR)3 и цеолитами до содержания влаги 0,01-0,03 мас.%. Электролиз вели постоянным током (U=110-220 V, I=0,05-0,20 А) при средней плотности 0,05 А/см2 с возвратом паров растворителя и удалением водорода, образующегося на катоде. После завершения электролиза (10-20 часов) спирт отгоняли при пониженном давлении, алкоголяты экстрагировали гексаном или толуолом и таким образом отделяли от LiCl, который практически нерастворим в углеводородах. После центрифугирования экстрагент отделяли от алкоголятов тантала упариванием при пониженном давлении. В некоторых случаях для очистки алкоголятов тантала от следовых количеств LiCl их подвергали вакуумной дистилляции или, как в случае с Та(ОС2Н5)5 экстрагировали гексаном. Кроме того, было отмечено, что электросинтез бутокситантала протекал со скоростями значительно меньшими, чем в случае других алкоголятов, а в конце электролиза поверхность Та-анода покрывалась слоем смолоподобных продуктов.
Недостаток способа - высокая энергоемкость процесса, использование в качестве электропроводной добавки LiCl, загрязняющего целевой продукт соединениями лития, низкая эффективность, особенно в случае электросинтеза бутокситантала.
Таким образом, анализ вышеуказанных способов получения алкоголятов тантала показывает, что химические способы малоэффективны либо из-за своей многостадийности, трудоемкости и экологии, не отвечающей современным требованиям, либо из-за отсутствия приемлемых методов получения исходных продуктов, как в случае переэтерификации метокси- и этокси- производных тантала изопропиловым и бутиловым спиртами. В свою очередь, электрохимический способ позволяет получать рассматриваемые алкоголяты, но характеризуется высокой энергоемкостью и низкой эффективностью при синтезе относительно высокомолекулярных алкоголятов тантала, а также использованием в качестве электропроводной добавки малодоступных и загрязняющих целевой продукт соединений.
Цель предлагаемого изобретения - снижение энергоемкости электрохимического синтеза алкоголятов тантала и упрощение технологической схемы этого процесса.
Поставленная цель достигается тем, что синтез алкоголята осуществляют при электролизе раствора соответствующего спирта в метаноле с использованием NH4Cl в качестве электропроводной добавки. Это позволяет провести в одном реакционном пространстве электросинтез целевого продукта как за счет электрохимической реакции анодного растворения тантала, так и реакции переэтерификации образующегося в этом процессе метокситантала.
Применительно к электросинтезу изопропокситантала и бутокситантала сущность предлагаемого способа заключается в том, что электролизу подвергали метанольно-изопропанольный или метанольно-бутанольный раствор при содержании спиртов в них в интервале 30-70 об.% в присутствии NH4Cl в количестве 1,0-2,0 мас.% при температуре 60-70°С в первом случае и 70-75°С - во втором. Затем из реакционных масс, полученных в первом или во втором случаях, с помощью эффективной ректификации сначала при атмосферном давлении полностью удаляли метанол, а потом при пониженном давлении - избыток изопропанола или бутанола. В результате получали кубовые остатки с составом, представляющим собой соответствующий алкоголят с примесью электропроводной добавки. К полученному остатку добавляли гексан и экстрагировали алкоголят, при этом NH4Cl, нерастворимый в углеводородах, выпадал в осадок. Экстракт декантировали из него, при пониженном давлении отгоняли растворитель, а полученный изопропокситантал или бутокситантал очищали перекристаллизацией или дистилляцией соответственно.
При этом существенно, что если при одной и той же плотности тока электролиз в изопропиловом или бутиловом спиртах в присутствии электропроводной добавки протекает с высокими напряжением и энергозатратами, то электролиз раствора, содержащего 30-70 об.% изопропанола или бутанола в метаноле, идет при существенно более низких напряжениях и удельных энергозатратах. Также существенно, что в этом случае в качестве электропроводной добавки вместо относительно дорогого и гигроскопического хлорида лития, к тому же загрязняющего целевой продукт соединениями лития, оказалось возможным использовать дешевый и доступный, легко поддающийся очистке и осушке хлорид аммония.
Концентрация NH4Cl в интервале 1,0-2,0 мас.% для растворов соответсвующего спирта является оптимальной. При его содержании в электролизном растворе менее 1,0 мас.% заметно возрастают удельные энергозатраты. Верхняя граница концентрации электропроводной добавки обусловнена растворимостью NH4Cl в метанольно-спиртовом растворе указанного состава.
Количества изопропанола или бутанола, входящие в состав электролизного раствора, также оптимальны. Использование растворов, содержащих более 70 об.% изопропанола или бутанола, является нецелесообразным вследствие существенного роста удельных энергозатрат. Применение этих спиртов в количествах менее 30 об.% также нецелесообразно, так как в этом случае удельные энергозатраты практически не снижаются, а эффективность реакции переэтерификации падает, что приводит к уменьшению выхода соответствующего алкоголята.
Предлагаемое изобретение иллюстрируется следующими примерами
Пример 1.
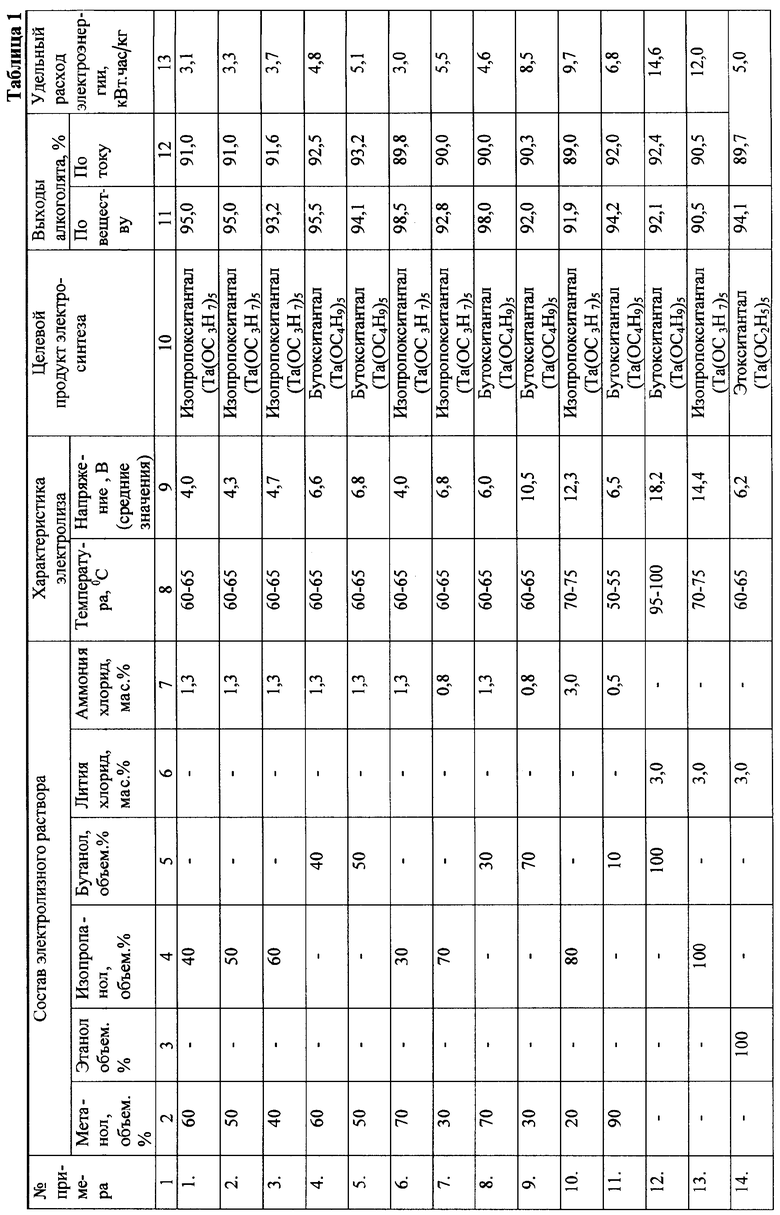
В стеклянный электролизер с Та-анодом и катодом из нержавеющей стали, снабженный рубашкой для охлаждения, обратным холодильником, термометром и устройством для подачи инертного газа, загружали 200 мл электролизного раствора, содержащего соответствующие спирты и до 2,0 мас.% NH4Cl. Электролиз вели при токовой нагрузке 1,5 А и средней плотности тока 5 А/дм2. Режим электролиза - гальваностатический. После пропускания 20 А·час электролиз прекращали. Затем из послеэлектролизного раствора на ректификационной колонке сначала при атмосферном давлении отгоняли метанол, а после этого при пониженном давлении - избыток изопропанола или бутанола. К остатку, представляющему собой изопропокситантал или бутокситантал, добавляли ~100 мл гексана, которым экстрагировали соответствующий алкоголят и отделяли NH4Cl, нерастворимый в гексане. Экстракт декантировали, из него при пониженном давлении на роторно-пленочном испарителе отделяли гексан. В результате получили алкоголяты с выходами по току 91%, по веществу - 95%. При этом удельный расход электроэнергии составил 3,0 кВт ч/кг.
Примеры 2-11 проводили в аналогичных условиях, но при различном соотношении метанола и изопропанола, метанола и бутанола, а также при различном содержании электропроводной добавки NH4Cl.
Результаты синтезов приведены в Таблице 1.
Примеры 12-14 сравнительные по прототипу.
Таким образом, предлагаемое изобретение позволяет упростить процесс электрохимического синтеза алкоголятов тантала при значительном снижении энергоемкости этого процесса.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПЕНТАБУТОКСИДОВ НИОБИЯ И ТАНТАЛА | 2008 |
|
RU2381231C2 |
| СПОСОБ ЭЛЕКТРОХИМИЧЕСКОГО СИНТЕЗА АЛКОКСИДОВ ЦИРКОНИЯ | 2009 |
|
RU2399608C1 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКОКСОПРОИЗВОДНЫХ ЖЕЛЕЗА (III) | 1991 |
|
RU2017712C1 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКОКСИДОВ ТИТАНА | 1995 |
|
RU2079503C1 |
| Способ получения алкоголятов металлов | 1980 |
|
SU953008A1 |
| Способ получения алкоголятов металлов | 1981 |
|
SU1008282A1 |
| Способ получения алкоголятов металлов | 1983 |
|
SU1237658A1 |
| Способ получения вторичного бутилового спирта | 1977 |
|
SU734182A1 |
| СПОСОБ ЭЛЕКТРОХИМИЧЕСКОГО ПОЛУЧЕНИЯ ФОСФИНА ИЗ НЕВОДНОГО РАСТВОРА БЕЛОГО ФОСФОРА | 2011 |
|
RU2469130C1 |
| СПОСОБ ВЫДЕЛЕНИЯ АЛКОКСИДОВ ТИТАНА | 1995 |
|
RU2076106C1 |
Изобретение относится к электрохимическому синтезу алкоголятов тантала, которые являются перспективными предшественниками высокочистых и высокодисперсных моно- и смешанных оксидных композиций для нанотехнологических процессов. Способ заключается в электрохимическом растворении тантала при его анодной поляризации постоянным током при повышенной температуре в растворе изопропилового или бутилового спирта в присутствии электропроводной добавки, с последующим выделением изопропокситантала или бутокситантала из соответствующего электролизного раствора экстракцией. При этом синтез осуществляют при электролизе раствора изопропилового или бутилового спирта в метаноле, в качестве электропроводной добавки используют аммоний хлорид в количестве 1,0-2,0 мас.%, а содержание соответствующего спирта в метаноле составляет 30-70 об.%. Предлагаемое изобретение позволяет упростить процесс электрохимического синтеза алкоголятов тантала при значительном снижении энергоемкости этого процесса. 1 табл.
Способ получения алкоголятов тантала методом электролиза путем электрохимического растворения тантала при его анодной поляризации постоянным током при повышенной температуре в растворе изопропилового или бутилового спирта, в присутствии электропроводной добавки, с последующим выделением изопропокситантала или бутокситантала из соответствующего электролизного раствора экстракцией, отличающийся тем, что синтез осуществляют при электролизе раствора изопропилового или бутилового спирта в метаноле, а в качестве электропроводной добавки используют аммоний хлорид в количестве 1,0-2,0 мас.%, при этом содержание соответствующего спирта в метаноле составляет 30-70 об.%.
| N.Y.TUROVA et al., Tantalum (V) alkoxides: electrochemical synthesis, mass-spectral investigation and oxoalkoxocomplexes | |||
| Polyhedron, 1996, т.15, №21, с.3869-3880 | |||
| Подвесной крановый путь для сооружений с арочными несущими конструкциями | 1986 |
|
SU1460026A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| Березкин М.Ю | |||
| и др | |||
| Электрохимический синтез этилата ниобия (V) | |||
| ЖПХ, 2006, т.79, вып.5, с.752-756. | |||
Авторы
Даты
2009-05-27—Публикация
2007-09-21—Подача