Область техники, к которой относится изобретение
Изобретение относится к области медицины, фармакологии, биотехнологии, генной инженерии, генной терапии, а именно к лечению заболеваний, требующих стимуляции регенераторных процессов, включая повреждения тканей человека различной этиологии, с помощью фармацевтической композиции или препарата для генной терапии на основе синтетического модифицированного гена инсулиноподобного фактора роста человека первого типа.
Настоящее изобретение также относится к использованию вектора для генной терапии, несущего синтетический модифицированный ген инсулиноподобного фактора роста человека.
Уровень техники
Пептидные ростовые факторы представляют собой группу низкомолекулярных белков, влияющих на рост и функции отдельных клеток и тканей организма. К общим функциям пептидных ростовых факторов относятся: стимуляция митоза, влияние на процессы дифференцировки и роста клеток, участие в процессах эмбриогенеза, регенерации тканей.
Процессы регенерации являются одним из важнейших механизмов поддержания гомеостаза организма, особенно при повреждениях различной этиологии. К ним можно отнести травмы механические, включая операционные, химические, термические, радиационные, ишемические и др. Регенерация поврежденных тканей зависит, в основном, от пролиферации в зоне поражения клеток различных типов и синтеза клетками как собственных элементов, так и компонентов межклеточного вещества.
Ускорение заживления ран и лечение прочих повреждений путем стимуляции регенерации является одной из важнейших задач практической медицины. В качестве стимуляторов регенерации используются различные агенты: 2'-дезоксирибонуклеотиды (патент №2115410), липосомы, содержащие альфа-токоферол (патент №2036637), масло авокадо и минеральные частицы (патент №2173982), фетальная хрящевая ткань, вводимая внутрисуставно для регенерации суставного хряща (патент №2195940), биоантиоксидантный раствор тиофана на основе масляного раствора альфа-токоферола (патент №2297217), экстракты личинок комнатной мухи для омоложения кожи с группой минералов (патент №2289412), физиологический раствор поваренной соли (патент №2053775), смесь витаминов с экстрактом вытяжки коры свиных или фетальных надпочечников человека (патент №2185835), одновременное облучение высокочастотными полями и низкоинтенсивным квазимонохроматическим излучением видимого и ближнего инфракрасного диапазона (патент №2259216), местное введение гиалуроновой кислоты (патент №2284768), донорская кровь и ее компоненты (патент №2191585), смесь масла подсолнечного, масла облепихового, масла лавандового (№2097017), четвертичная аммонийная соль конидина (патент №2020933), 5-(2-пиразинил)-4-метил-1, 2-дитиол-3тион (патент №2291696), синтетические пептиды для регенерации печени (патенты №2297239, №2286794), нейротрофические факторы AF-1 и AF-2 (патент №2157223), кондиционированная культуральная среда, полученная при культивировании эукариотических клеток в трех измерениях (патент №2280459). Регенераторный эффект большинства этих средств и веществ связан либо с опосредованным, либо с трофическим действием. Именно поэтому многие пептидные ростовые факторы, действующие в качестве непосредственных митогенов, могут рассматриваться в качестве наиболее перспективных лекарственных средств. Они могут применяться в составе различных биологических экстрактов (например, из плаценты) или путем получения рекомбинантных белков с использованием продуцентов на основе различных организмов. К таковым относят различные бактериальные продуценты, дрожжи и другие эукариотические клетки.
Однако при использовании рекомбинантных белков имеется ряд недостатков. В частности, требуется частое введение белков вследствие их быстрой биодеградации в организме, происходят значительные колебания уровня введенного белка в организме, рекомбинантные белки могут не иметь естественного гликозилирования и других посттрансляционных модификаций, очистка рекомбинантных белков требует использования сложных методов очистки, рефолдинга.
В этом смысле более перспективным направлением является использование генной терапии, когда применяются различные векторы, несущие гены факторов роста и соответствующие регуляторные элементы. По сравнению с применением рекомбинантных белков у генной терапии имеется целый ряд значительных преимуществ:
- при применении генной терапии не требуются частые инъекции препарата, поскольку экспрессия целевых генов в организме пациента может продолжаться, в зависимости от типа используемой конструкции и целей терапии, от нескольких дней до многих лет и даже пожизненно;
- уровни образующегося в организме целевого белка более постоянны, не наблюдается значительных колебаний;
- образующиеся с помощью векторов в клетках пациента человеческие белки совершенно не отличаются от природных, поскольку проходят все этапы естественных посттрансляционных изменений;
- очистка препаратов для генной терапии в целом проще и легче может быть стандартизирована;
- не требуется рефолдинг терапевтических конструкций в отличие от рекомбинантных белков, вырабатываемых продуцентами.
Для генной терапии используется целый ряд векторов, прежде всего вирусных. Однако последние имеют целый ряд недостатков, таких как возникающий иммунный ответ на вирусный вектор (например, аденовирусный), риск опухолевой трансформации (ретровирусные векторы) и др. В этом смысле наиболее безопасными векторами являются плазмиды. Одной из наиболее серьезных проблем генной терапии при использовании в качестве векторов плазмид является нерешенность вопроса их высокоэффективной доставки в клетки, что определяет зачастую недостаточный для достижения терапевтического эффекта уровень экспрессии гена и синтеза целевого белка.
Генная терапия может использоваться для лечения ран. Так, молекула ДНК, включенная в состав биосовместимой матрицы и несущая какой-либо генный продукт, может быть доставлена в репаративные клетки в области раны (патент №2170104). В числе таких генов рассматриваются, в том числе, различные ростовые факторы, включая инсулиноподобный фактор роста (не указан тип данного фактора).
Инсулиноподобный фактор роста человека первого типа (ИФР-1, IGF-1) является пептидным ростовым фактором, опосредующим ростостимулирующие эффекты соматотропного гормона (СТГ). Он представляет собой полипептид, состоящий из 153 аминокислот, с молекулярной массой примерно 17 кДа. Под влиянием СТГ ИФР-1 образуется в печени и других тканях. В свою очередь ИФР-1 тормозит секрецию СТГ по механизму отрицательной обратной связи.
ИФР-1 присутствует в крови в основном в комплексе со связывающими белками, модулирующими действие инсулиноподобных факторов роста (Clemmons D.R. et al., 1993; Krywicki R.F., 1992). Он участвует в развитии плода и постэмбриональном развитии. ИФР-1 стимулирует пролиферацию клеток большинства тканей, прежде всего костных, хрящевых и мышечных. Наряду с гормоном роста ИФР-1 определяет рост человека и размеры его органов (Kahn C.R. et al., 1981).
ИФР-1 in vitro способен вызывать метаболические эффекты, принципиально сходные с инсулином, реализуя их путем перекрестного взаимодействия с рецепторами инсулина (Le Roith D. et al., 1993). Рецепторы инсулина и рецепторы ИРФ-1 - трансмембранные гликопротеины (класс тирозиновые протеинкиназы) тетрамерной структуры (две экстраклеточные лигандсвязывающие альфа-субъединицы и две трансмембранные эффекторные бета-субъединицы с тирозинкиназным цитоплазматическим доменом), стабилизированной двумя видами дисульфидных связей. Оба протеинкиназных рецептора обладают сходным принципом передачи гормонального сигнала: фосфорилирование по тирозину каскада белков-посредников под действием протеинкиназы бета-субъединицы, которая после связывания соответствующего пептидного лиганда с экстраклеточной альфа-субъединицей активируется в результате автофосфорилирования (Le Roith еt аl. 1993). ИРФ-1 является анаболическим агентом, для которого было продемонстрировано улучшение метаболизма (Meyer N.A. et al., 1996) [35], функции слизистой кишечника (Huang K.F. et al., 1993) [42] и снижение белковых потерь (Strock L.L. et al., 1990) [43] после различных типов повреждения. ИРФ-1 опосредует активности гормона роста при гиперметаболическом состоянии за счет ослабления потерь безжировой массы тела, нарушенного иммунного ответа, острой фазы ответа и за счет улучшения заживления раны (Zaizen Y. et al., 1990; Clemmons D.R. 1994; Lo H.C. et al., 1995; Guler et al., 1988; Walker J.L et al., 1991) [35, 38, 44-47]. Обработка ИРФ-1 улучшает заживление тканей (Martin P.1997; Steenfos H. 1994; Pierre et al., 1997) [40, 41, 48]. ИРФ-1 использовался для снижения проявлений токсической невропатии (патент №2120803). Имеются неблагоприятные побочные эффекты, такие как гипогликемия, изменения психического состояния, отек, утомление и головные боли, которые ограничивают терапевтическое применение пептида ИРФ-1 (Jabri N. et al., 1994) [49, 50]. Указанные неблагоприятные побочные проявления обусловливаются сверхфизиологическими дозами свободного ИРФ-1, которые необходимы для достижения биологической эффективности и стимуляции процессов регенерации в конкретном локальном месте при системном введении (Bondy С.А. et al., 1994) [49, 50]. В связи с этим разработка системы локальной доставки пептида ИФР-1 к месту повреждения является важным условием для проведения полноценной и безопасной терапии травматических повреждений различной этиологии и лечения других заболеваний, требующих стимуляции регенераторных процессов. Одним из решений проблемы является применение генной терапии, использующей различные векторы, несущие целевой терапевтический ген. Такая конструкция, включенная в состав биосовместимой матрицы и несущая какой-либо генный продукт, в том числе различные ростовые факторы, включая инсулиноподобный фактор роста (не указан тип данного фактора), может быть использована для лечения ран (патент №2170104).
На данный момент в мире разрабатывается множество систем доставки ДНК в клетки-мишени, например липосомы или различные вирусные системы. Было показано, что с повышением эффективности доставки падает ее специфичность. Так, липосомы разносят ДНК по всему организму и доставляют ее в различные органы, включая сердце, печень, селезенку, легкие и т.д. (Thierry A.R. et al., 1996). Вирусные векторы имеют ряд недостатков - они дорогостоящи и часто обладают ограниченной клонирующей емкостью, что не позволяет регулировать экспрессию «терапевтического гена» с помощью тканеспецифичных последовательностей. Кроме того, вирусные белки могут вызывать воспалительную реакцию, что исключает повторное введение вектора. Существуют и другие опасности применения вирусных векторов.
Таких недостатков лишены векторы на основе плазмидных ДНК, которые не вызывают иммунной реакции. Было показано, что при внутримышечной иньекции обычной, «голой» плазмидной ДНК она встречает диффузионный тканевой барьер и трансформирует лишь клетки, находящиеся около места инъекции. Безусловно, величина этого диффузионного барьера зависит от состояния тканей и межклеточного матрикса, однако дальше места инъекции, по всему организму, значительного распространения не происходит (Jiao et.al., 1990; Davis et.al, 1993).
Несмотря на указанные достоинства, одним из недостатков использования «голой» плазмидной ДНК является сравнительно низкая частота трансформации клеток ткани в месте введения. Из всего количества введенной плазмидной ДНК в процессе трансформации клеток участвует 0,01-1% плазмид. Таким образом, действующая часть дозы подобного лекарственного препарата невелика. Одним из путей решения данной проблемы является усиление экспрессии генов, входящих в состав терапевтической плазмиды. При таком подходе, несмотря на низкий уровень трансформации клеток поврежденной и прилегающей к зоне повреждения ткани, возможно достижение необходимого терапевтического эффекта без увеличения дозы препарата.
Модуляция экспрессии генов представляет собой такую проблему, как влияние нуклеотидного состава генов на их экспрессию (Duret, 2000; Naya et.al., 2001). В настоящее время изучается влияние различий в составе кодонов на стабильность матричной РНК, ее процессинг и нуклеоцитоплазматический транспорт в различных клеточных системах (Graf et.al., 2000; Koresawa et.al., 2000; Liu et.al., 2002; Stratford et.al., 2000; Uchijima et.al., 1998; Yang et.al., 1996; Zhang et.al., 1999).
Раскрытие изобретения
Приведенные выше недостатки вирусных векторов обусловили включение в основу разработанной нами фармакологической композиции в качестве вектора плазмиды ("голой" ДНК). Именно такой вектор для генной терапии является наиболее безопасным.
Кроме того, ограничение распространения плазмиды по всему организму от точки инъекции в ткани из-за тканевого диффузионного барьера, являющееся недостатком с точки зрения генной терапии всего организма, - одновременно является достоинством при необходимости локальной стимуляции регенераторных процессов. Такое локальное действие может быть необходимо при различных заболеваниях, в частности, при повреждении тканей. Данное очень важное свойство также свидетельствовало в пользу включения именно «голой» плазмидной ДНК (а не в составе липосом или вирусных систем доставки) в разрабатываемый нами препарат для местной регенерации тканей. Таким образом, важным элементом нашего изобретения является локальное действие фактором ИФР-1 и отсутствие его значимого влияния на организм в целом, что позволяет избежать упомянутых выше неблагоприятных воздействий, которые имеют место при употреблении белковых форм препарата ИФР-1.
Одним из возможных решений проблемы низкой эффективности генной терапии на основе плазмидных конструкций из-за сложности доставки достаточного их количества в клетки является повышение экспрессии целевых генов в клетке. Такой эффект значительного повышения экспрессии целевых генов в клетке в процессе генной терапии может быть достигнут разными путями, в частности изменением регуляторных элементов вектора, а также созданием синтетических генов. При использовании синтетических генов их экспрессия в клетках пациента может быть значительно повышена без изменения первичной структуры терапевтического белка.
Нами было обнаружено, что матричная РНК гена ИФР-1 при изменении ее нуклеотидного состава делается более стабильной в клетках млекопитающих и культуре человеческих клеток. На основе полученных данных мы разработали модифицированный ген ИФР-1 (ФГсинтИФР-1, PGsyntIGF-1) с оптимизированным нуклеотидным составом без изменения аминокислотной последовательности транслируемого белка и синтезировали его (см. перечень последовательностей).
Данный синтетический ген был клонирован в рекомбинантные плазмидные ДНК для эукариотической экспрессии. Нуклеотидная последовательность синтетического гена ФГсинтИФР-1 обеспечила увеличение стабильности мРНК в клетках млекопитающих, что позволило при использовании стандартных плазмидных векторов для эукариотической экспрессии в клетках человека повысить уровень трансляции кодируемого белка до 100 и более раз по сравнению с использованием в аналогичных условиях нативного, природного гена.
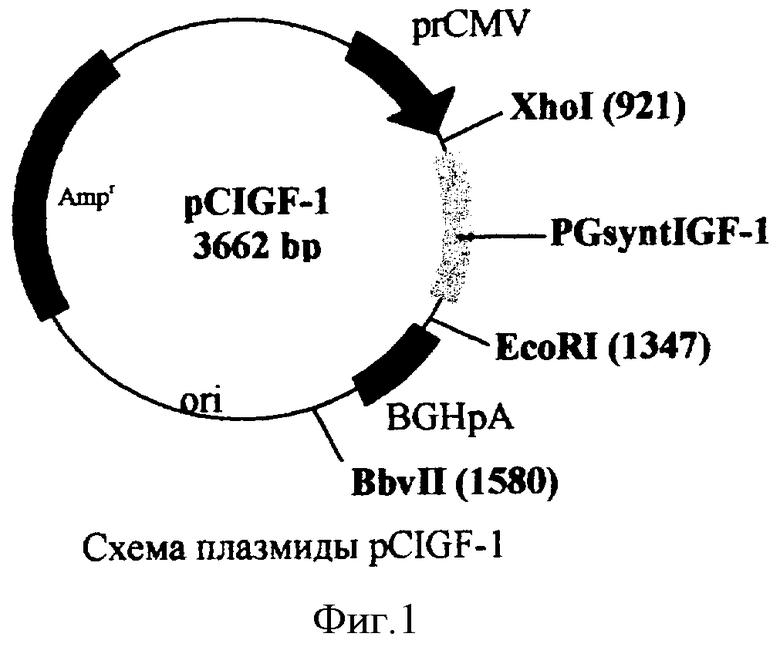
Разработанный нами препарат для генной терапии или включающая его фармацевтическая композиция представляет собой плазмидную ДНК (рС), несущую модифицированный синтетический ген ФГсинтИФР-1, кодирующей и экспрессирующей в организме человека пептидный фактор роста - ИФР-1 (см. материалы, поясняющие сущность изобретения, фиг.1).
Нами показано, что при использовании синтетического гена ФГсинтИФР-1 с оптимизированной нуклеотидной последовательностью для генной терапии могут вводиться более низкие количества плазмидной ДНК, от 4 до 100 раз меньшие по сравнению с системами, описанными в других патентах №205114367, 200110435, 2001129537, 2004129332 и др. Это делает применение фармакологического препарата на основе разработанной нами плазмидной ДНК более экономичным, эффективным и безопасным.
Идентичность образуемого пептида природному ИФР-1 при экспрессии синтетического гена и последующей трансляции обеспечивает безопасность и эффективность применения препарата с точки зрения использования природных механизмов его метаболизма и катаболизма без образования токсичных продуктов. Это свойство выделяет данный препарат как среди обычных химических фармацевтических средств, так и среди белковых препаратов, полученных с помощью прокариотических или эукариотических продуцентов in vitro. Причина заключается в том, что в первом случае, при использовании прокариотических продуцентов, не работают многие природные механизмы фолдинга (сворачивания) белков и их посттрансляционных модификаций. Во втором случае, при использовании любых эукариотических продуцентов (за исключением клеток человека), процессы фолдинга и посттрансляционных модификаций могут отличаться от процессов, происходящих в клетках человека. Использование же в качестве продуцента клеток человека опасно с точки зрения распространения вирусов, в том числе онкогенных. Кроме того, использование данного препарата для генной терапии, обеспечивающей синтез целевого полипептида in vivo, позволит избежать сложностей производства и процессов очистки белка in vitro. Производство же, очистка и хранение ДНК-препаратов экономически выгоднее, чем белковых, так как первые значительно более стабильны и их можно нарабатывать в больших количествах и с меньшими затратами, а очистка плазмидной ДНК проще, чем белка. Более того, при производстве препарата на основе плазмидной ДНК, в отличие от белковых препаратов, не требуются этапы фолдинга.
Таким образом, разработанная конструкция была использована в фармацевтической композиции в качестве препарата для генной терапии заболеваний различной этиологии, требующих стимуляции регенераторных процессов в широком спектре тканей человека, включая в себя мышечную, костную, все виды соединительной, эпидермальную, хрящевую и нервную ткани.
Краткое описание чертежей
(см. материалы, поясняющие сущность изобретения).
Фиг.1 - плазмидная ДНК рС, несущая модифицированный синтетический ген ФГсинтИФР-1, кодирующей и экспрессирующей в организме человека пептидный фактор роста ИФР-1 (плазмида pCIGF-1).
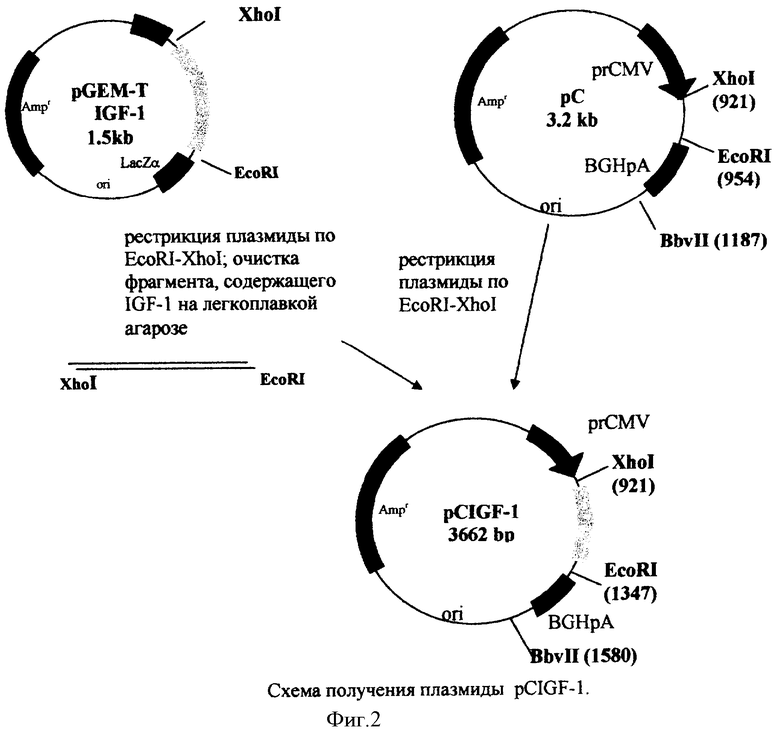
Фиг.2 - схема получения плазмиды pCIGF-1.
Фиг.3 - вестерн-блоттинг лизата клеток 293Т, трансформированных плазмидами pCIGF-1 (2-я дорожка), pCIGF-Isynt (3-я дорожка), несущими нативный ген ИФР-1 и ФГсинтИФР-1 соответственно. 1-я дорожка - лизат нетрансформированных клеток, 4-я дорожка - белковый маркер (Fermentas, Литва).
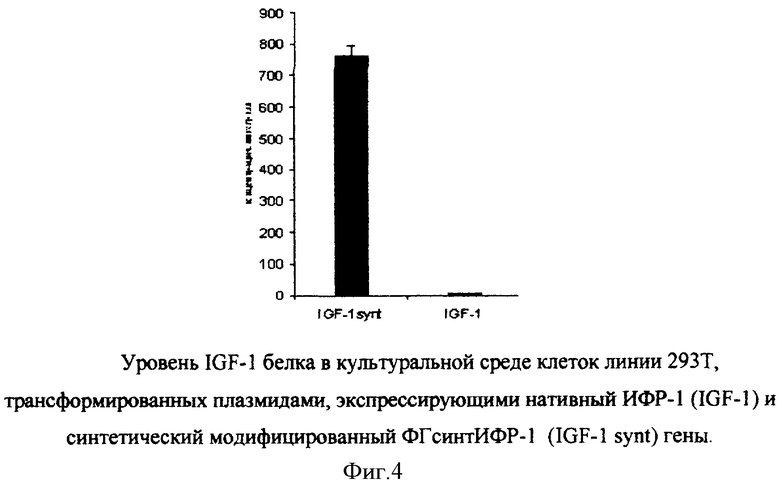
Фиг.4 - уровень IGF-1 белка в культуральной среде клеток линии 293Т, трансформированных плазмидами, экспрессирующими нативный ИФР-1 (IGF-1) и синтетический модифицированный ФГсинтИФР-1 (IGF-1 synt) гены.
Фиг.5 - сроки эпителизации полнослойных ран кожи в зависимости от используемой плазмидной ДНК.
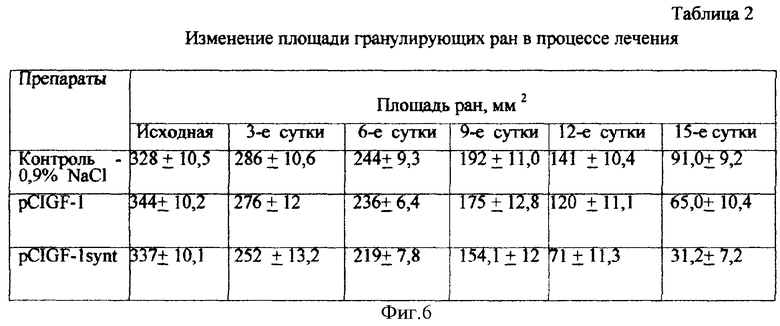
Фиг.6 - изменение площади гранулирующих ран в процессе лечения.
Осуществление изобретения
Синтез гена ФГсинтИФР-1 осуществляли путем удлинения взаимоперекрывающихся олигонуклеотидов (праймеров) согласно описанным методам (Majumder, 1992). Олигонуклеотады представляли собой фрагменты гена длиной около 60-70 нуклеотидов со взаимоперекрывающимися участками длиной около 20 нуклеотидов. Основные требования к праймерам заключались в том, что их длина не должна была превышать 70 нуклеотидов, а участки гибридизации должны были быть не меньше 20 нуклеотидов. Кроме того, на концах олигонуклеотидов не должно было быть длинных участков с повторяющимися G или С. В ряде случаев подбор оптимальных праймеров осуществляли эмпирически, путем сдвига праймера по отношеню к матрице или изменения длины праймера на 3-6 нуклеотидов. В общей сложности для синтеза гена длиной 462 нуклеотида было использовано 36 праймеров. Синтезированные фрагменты длиной около 100 нуклеотидов выделялись с помощью гель-электрофореза и клонировались в плазмидный вектор pGEM-T Easy. Клонирование осуществляли с использованием рестрикционных сайтов Kpnl, SacII, EcoRV, BamHI или посредством „тупых" концов. После секвенирования фрагменты вырезали из вектора с помощью соответствующих рестрикционных ферментов или амплифицировали, после чего соединяли в нуклеотидную последовательность ИФР-1 путем их сплавления методом полимеразной цепной реакции (ПЦР). После заключительного этапа синтеза ФГсинтИФР-1 путем лигирования фрагментов искусственный ген клонировали в вектор pGEM-T по рестрикционным сайтам Kpnl и Sacl. Синтетический ген был фланкирован дополнительными рестрикционными сайтами EcoRI на 5'-конце и Xhol на 3'-конце. Далее искусственный ген переклонировали в экспрессионный вектор рС под контроль цитомегалловирусного промотора. Вектор рС предназначен для экспрессии генов в эукариотических клетках. Он содержит основные необходимые регуляторные элементы: промотор предранних белков цитомегаловируса, сайт терминации транскрипции, полиаденилирования и ориджин репликации ColEl из высококопийной плазмиды pBR322. Данный вектор был сконструирован в ООО «Фарма Ген» авторами данного патента. Схема получения плазмиды представлена на чертеже (см. материалы, поясняющие сущность изобретения, фиг.2).
Для переклонирования последовательность гена ФГсинтИФР-1 (462 нуклеотида) выделили из геля и дотировали в экспрессионный вектор рС по сайтам рестрикции Xhol и EcoRI. Реакцию лигирования проводили с помощью "DNA Ligation Kit" (Sigma, США) в следующих условиях: буфер для лигирования (25 мМ Трис-HCl рН 7,8; 10 мМ MgCl2; 1 мМ ДТТ; 0,5 мМ АТФ), 400 нг подготовленных фрагментов, 100 нг рестрицированной векторной ДНК, 1 ед. ДНК-лигазы фага Т4. Реакцию проводили в течение 8 часов при 16°С. Лигазную смесь диализовали на нитроцеллюлозных фильтрах (Millipore) с использованием буфера для диализа (глицерин 0,5%; ЭДТА 5 тМ).
Лигазная смесь была трансформирована с помощью тепловой Са2++-трансформации в клетки бактерий. В работе использовали клетки E.coli DH10B/R (Gibko BRL, США) с генотипом F-mcrA Δ(mrr-hsdRMS-mcrBC) φ80dlacZΔM 15 ΔlacX74 deoR recA1 endA1 araD139 Δ(ara, leu)769 galU galKλ- rpsL nupG. Для приготовления компетентных клеток брали отдельную колонию, выращенную на LB-aгape (Gibko BRL, США) в чашке Петри, и помещали в 5 мл LB-среды (Gibko BRL, США). Клетки растили в течение восьми часов при 37°С в режиме постоянного перемешивания (250 об/мин). 2 мл полученной культуры помещали в 200 мл LB-среды. Клетки растили при 37°С при постоянном перемешивании (250 об/мин) до ОП600=0,6, после чего осаждали центрифугированием в течение 10 минут на 4000g при 4°С. Клетки отмывали в деионизованной воде с последующим центрифугированием. Процедура отмывки повторялась трижды. После отмывки осадок клеток ресуспендировали в малом объеме деионизованной воды и центрифугировали 30 сек при 12000 об/мин на микроцентрифуге. К осадку клеток добавляли 3 объема (от объема клеточного осадка) 15%-ного глицерина, осадок ресуспендировали и быстро замораживали в жидком азоте. Готовые к трансформации клетки хранили при температуре - 70°С.
Высев трансформированных клеток осуществляли на твердую среду LB. Для быстрого скрининга клонов, содержащих плазмиду с клонированной вставкой, использовали метод ПЦР. Реакцию проводили в объеме 25 мкл в тонкостенных полипропиленовых пробирках объемом 650 мкл, содержащих 10 мМ Трис-HCl рН 8,3; 1,25 мМ MgCl2; 50 мМ KCl; 200 мкМ каждого из дНТФ; 200 нМ каждого из праймеров; 1,5-2 мкг клеточной ДНК и 2,5 ед. Taq-полимеразы (Литех, Россия). Реакционную смесь прогревали 1 минуту при 95°С для денатурации клеточной ДНК. Для предотвращения испарения на реакционную смесь объемом 25 мкл наслаивали 15 мкл Bayol F (Sigma, США). Реакцию амплификации проводили в термоциклере Терцик (ДНК-технология, Россия) при следующих условиях - 32 цикла: 10 секунд при 95°С; 15 секунд при Топж (°С); 60 секунд при Тештгеза 72°С. В качестве матрицы использовали биомассу одной колонии размером около 1 мм. Для достройки образовавшихся цепей ДНК проводили дополнительный цикл: 5 минут при 72°С.
Было отобрано три клона. Из клонов выделили плазмидную ДНК. Выделение плазмидной ДНК проводили для рестрикционного анализа исследуемых плазмид, трансформации эукариотических клеток с целью анализа экспрессии гена ИФР-1, а также при анализе рекомбинантных клонов на наличие требуемой вставки. Для мини-выделения плазмидной ДНК брали отдельную колонию, выращенную на LB-агаре, и помещали ее в 5-10 мл LB-среды с ампициллином (50 мкг/мл). Клетки растили в течение восьми часов при 37°С в условиях постоянного перемешивания (250 об/мин). Полученную культуру бактериальных клеток осаждали при 4000 g в течение 10 минут при 4°С. Супернатант отбрасывали, а из осадка клеток выделяли плазмидную ДНК с помощью набора "Wizard Minipreps DNA Purification System" (Promega, США) по инструкции, прилагаемой к набору. Выделенную плазмидную ДНК анализировали электрофорезом в 0,8%-ном агарозном геле, измеряли ее концентрацию и хранили при - 20°С.
В ходе дальнейшей работы провели рестрикционный анализ полученных плазмид на наличие фрагмента, содержащего ген ФГсинтИФР-1.
Наработанную плазмиду использовали для трансформации эукариотических клеток 293Т. За день до трансформации эукариотические клетки пересевали при плотности 104/см. На следующий день меняли среду культивирования на свежую, содержащую 10%-ную фетальную телячью сыворотку. Через 3 часа добавляли кальций-фосфатный преципитат ДНК. Для флакона 25 см2, содержащего 5 мл среды, преципитат готовили следующим образом: в одну пробирку вносили раствор, содержащий 5 мкг ДНК, затем 31 мкл 2М CaCl2 и доводили суммарный объем водой до 0.25 мл; в другую пробирку вносили 0,25 мл 2×HBS (1,64% NaCl (по весу); 1,13% HEPES (по весу); 0,04% Na2HPO4 (по весу) и рН 7.12). Раствор ДНК по каплям добавляли к HBS. Преципитат наносили на клетки, слегка наклоняя чашку и добавляя его в среду. Клетки инкубировали в течение 4 часов и промывали средой без сыворотки. Чтобы повысить эффективность трансформации на этой стадии, клетки подвергали глицериновому шоку. Для этого во флакон с клетками добавляли 0,5 мл 15%-ного раствора глицерина в HBS и инкубировали при 37°С в течение 2 минут. «Шок-раствор» удаляли до того момента, когда клетки начинали сжиматься. Затем клетки отмывали и заливали свежей средой. Через 3 дня клетки снимали с подложки и проводили анализ на экспрессию трансформированных генов. Перенос предварительно фракционированных в геле ПААГ в денатурирующих условиях белков клеточного лизата трансформированных эукариотических клеток на нитроцеллюлозную мембрану (Bio-Rad, США) проводили по методу Вестерн-блота (Нго Т.Т и др., 1988) с некоторыми модификациями. Перед началом переноса гель с фракционированными белками клеточного лизата 293Т и нитроцеллюлозную мембрану вымачивали в буфере для переноса (0,025 М Трис; 0,193 М глицин; 20%-ный этанол) в течение 10 минут. Перенос белков из геля осуществляли электропереносом (напряженность эл. поля 7,5 В/см) в течение 1,5 часов в специально предназначенной для этого ячейке (Bio-Rad, США). После окончания переноса блот промывали 5 минут в растворе ФСБ-твин (0,01 М Na2HPO4/NaH2PO4 рН 7,2; 0.15 М NaCl; 0,3% твин-20) при комнатной температуре. Прокрашивали зону блота, соответствующую смеси стандартных белков, красителем амидочерным (Sigma, США). Блот высушивали при комнатной температуре и хранили в герметичных пакетах при 4°С до выявления белков. Для выявления белка ИФР-1 использовали моноклональные антитела. Для предотвращения неспецифического связывания антител с блотом проводили блокировку неспецифических сайтов связывания 2,5%-ным раствором Skim Milk (Fluka) при комнатной температуре в течение 40 минут. После трех отмывок по 10 минут при комнатной температуре в ФСБ-твин с 1%-ным раствором Skim Milk (Fluka) блот инкубировали с моноклональными антителами в течение восьми часов при комнатной температуре, осторожно перемешивая на ротационной качалке. После трех отмывок по 10 минут при комнатной температуре в ФСБ-твин с 0,1%-ным Skim Milk (Fluka) блот инкубировали 2 часа с аккуратным встряхиванием в ФСБ-твин с 0,1%-ным раствором Skim Milk (Fluka), содержащим вторичные антитела, коньюгированные с пероксидазой хрена. После промывки блота в ФСБ-твин с 0,1%-ным раствором Skim Milk (Fluka) блот помещали в раствор субстрата (3,3-диаминобензидин (Sigma, США); 0,003% Н2O) на 5 минут. Реакцию останавливали, промывая блот водой. Проявленный блот высушивали и сканировали. Экспрессию белков оценивали с помощью Вестерн-блоттинга лизата трансформированных клеток. Для приготовления клеточного лизата использовали одинаковое количество клеток, получаемых после трансформации плазмидами pCIGF-1 и pCIGF-lsynt (для трансформации использовали по 50000 нг плазмиды). Клетки осаждали из культуральной среды центрифугированием при 800 g и ресуспендировали в лизирующем буфере. На электрофорез наносили одинаковое количество клеточного лизата.
Результаты Вестерн-блоттинга представлены на чертеже (см. материалы, поясняющие сущность изобретения, фиг.3). С помощью денситометрического анализа было установлено, что яркость полосы, соответствующей экспрессии синтетического гена ФГсинтИФР-1, выше в 47 раз яркости полосы, образующейся при экспрессии нативного генаИФР-1.
Нижеследующие примеры даны для цели иллюстрирования различных вариантов воплощения изобретения и не призваны в чем бы то ни было ограничить настоящее изобретение.
Пример 1
Экспрессионные плазмиды pCIGF-1 и pCIGF-lsynt использовали для трансформации эукариотических клеток 293Т. После трансформации клетки инкубировали в 3 мл культуральной среды в течение 48 часов. Был выполнен иммуноферментный анализ культуральной среды клеток 293Т, трансформированных данными плазмидами и экспрессирующих нативный и синтетический гены ИФР-1. С помощью метода иммуноферментного анализа в культуральной среде клеток был обнаружен антиген - белок ИФР-1. Концентрация этого белка соответствовала уровню экспрессии нативного и синтетического генов ИФР-1. В случае плазмиды pCIGF-lsynt, несущей ФГсинтИФР-1, наблюдалось максимальная концентрация белка. Результаты иммуноферментного анализа представлены на чертеже (см. материалы, поясняющие сущность изобретения, фиг.4).
Интенсивность экспрессии белка ИФР-1 при использовании двух вариантов гена можно примерно оценить следующим образом: ИФР-1 - 1, ФГсинтИФР-1 - 100. Таким образом, ФГсинтИФР-1 может быть эффективно использован как для генной терапии, так для продукции ИФР-1 в составе эукариотического продуцента.
Пример 2
Экспериментальные животные - крысы.
Крысы являются хорошо исследованной моделью для экспериментальных исследований травм. Каждая из 30 крыс получала 2 полнослойные раны под наркозом и с обезболиванием. Каждый раневой участок имел круглую форму при приблизительном диаметре 2 см, при расстоянии между участками приблизительно 5 см, и находился в области верхней части боков и на спине. Сразу после индукции раны у 10 животных ее обкалывали раствором плазмиды, несущей ген ФГсинтИФР-1. Другие 10 животных получали иньекцию плазмиды, несущей нативный, более слабо экспрессируемый ген. Оставшиеся 10 животных с нанесенными ранениями представляли собой контрольную группу. У крыс, получавших конструкцию pCIGF-lsynt и pCIGF-1, имелось подтверждение того, что мРНК ИФР-1 находится в коже поблизости от сайтов трансфекции, но только не в контрольных тканях. В случае использования плазмидной конструкции pCIGF-lsynt наблюдалось статистически достоверное увеличение количества мРНК в 14 раз.
Концентрации белка ИФР-1 определяли с помощью ИФА в кожных биоптатах, полученных из участков, окружающих рану.
Во всех взятых кожных биопсиях у животных, которым вводили конструкции pCIGF-lsynt и pCIGF-1, определялись концентрации белка ИФР-1 по периметру раны по сравнению с биопсиями, взятыми у животных, которым вводили пустые плазмиды или физиологический раствор (р<0,01). Концентрации белка ИФР-1 статистически достоверно были выше в 12 раз при использовании плазмидной конструкции pCIGF-lsynt. Отсутствовали различия между группами по концентрации белка ИФР-1 в сыворотке, печени, селезенке или почках. В динамике во всех группах животных изучали состояние дна и краев раны, используя полуколичественную шкалу. Для оценки эффективности регенерационной активности используемых препаратов измеряли скорость эпителизации. С этой целью до начала лечения точно определяли площадь раны. Для этого на рану накладывали стерильный лист полиэтиленовой пленки и переносили на нее контуры кожного дефекта. Затем полученное изображение раны накладывали на лист миллиметровой бумаги, после чего подсчитывали количество квадратных сантиметров и миллиметров, заключенных внутри границ контура. Повторное измерение площади раны осуществляли через каждые 10-15 дней проводимой локальной и общей терапии. Процентное уменьшение площади раны в процессе лечения определяли по формуле Л.Н.Поповой (1942) (Теория и практика местного лечения гнойных ран. / Е.П.Безуглая, С.Г.Белов, В.Г.Гунько и др. / Под ред. Б.М.Даценко. - К.: Здоров'я, 1995. - 384 с.). Кроме того, при каждой перевязке измерялся максимальный размер язвы и производилось ее фотографирование на цифровую камеру (Canon 350D). Результаты представлены в таблицах (см. материалы, поясняющие сущность изобретения, фиг.5 и фиг.6).
Литературные ссылки
1. Firedmann T. Scientific American. 1997. 6: 96-101.
2. Feigner P.L. Scientific American. 1997. 6: 102-106.
3. Feigner, P.L. Annals of the New York Academy of Sciences. 1995. 772: 126-139.
4. Feigner, P.L. Human Gene Therapy. 1996. 7: 1791-1793.
5. Wheeler, C.J. et al. Proc Nati Acad Sciec 1996. 93 (21): 11454-11459.
6. Sharata et al. Intern J Dermatalogy. 1996. 35 (11): 761-769.
7. Fey G. & Gauldie J. The acute phase response of the liver in inflammation. In Popper, H., Schaffher, F. (Eds.). 89-116.
8. Rotheschild M.A. et al. Hepatology. 1988. 8: 385-401.
9. MoshageHJ. Pathol. 1997. 181: 257-266.
10. Seizman C.H. et al. Shock 1998; 10: 309-318.
11. Gilpin D.A. et al. Surgery. 1996. 119 (6): 664-673.
12. Jarrar D. et al. Arch. Surg 1997. 132: 1171-1176.
13. Xia Z.F. et al. Surgery. 1996. 119: 664-673.
15. Hemdon D.M. et al. J. Surg. Res. 1978. 25: 394-403.
16. Beutler B. & Cerami A. Adv Immunol. 1988. 42: 213-231.
17. Moldawer L.L. et al. Ann Rev Nutr. 1988. 8: 585-609.
18. Frost R.A. et al. Endo. 1997. 138 (10): 4153-4159.
19. Marano M. et al. Am Bum Assoc Ann Proc. 1988. 20: 18.
20. Yamada Y. et al. Bums. 1996. 22 (8): 587-593,
21. Balteskard L. et al. Scand J Infect Dis. 1997. 29: 393-399.
22. Gore D.C. et al. Arch Surg. 1991. 126: 38-43.
23. Chrysopoulo M.T. et al. Arch Surg. 1998. (in press).
24. Pennanen N. et al. Pharm Res. 1995. 12: 916-922.
25. Aramaki Y. et al. Biochem Biophys Res Corn. 1996. 220: 1-6.
26. Aramaki Y. et al. Biochem Biophys Res Corn. 1997. 231: 827-830.
27. Mulsch A. et al. Biochem Biophys Res Corn. 1993. 191: 1301-1308.
28. Sambrand et al. Proc Nati Acad Sci USA. 1995. 92: 1396-1400.
29. Shackelford R.E. et al. J Biol Chem. 1995. 270: 3745-3478.
30. Mulsch A. etal. FEBS Lett. 1993. 321: 215-218.
31. Brisseau G.F., et al. Antimicrobial Agents and Chemotherapy. 1994. 38: 2671-2675.
32. Xiao B.G. et al. Neurosci Lett. 1998. 249: 17-20.
33. Amush M. et al. J Clin Invest. 1998. 102: 516-526.
34. Pierre, El. Growth hormone therapy in the treatment of bums. In: M.H. Torosian, ed. Growth hormone in critical illness: research and clinical studies. R.G.Lan-des. 1996. Pp.105-116
35. Meyer N.A. et al. 1996. J. Trauma 31 (6): 1008-1012.
36. Hemdon, D.N. et al. 1989. Ann. Surg. 209 (5): 547-553.
37. Rodriguez, J.L. et al. 1993. J. Trauma 34: 684-694.
38. Zaizen, Y. et al. 1990. J Ped Surg (25): 70.
39. Hemdon, D.N., et al. 1990. Ann. Surg. 212: 424.
40. Martin, P. 1997. Science 276: 75-81. 1997.
41. Steenfos H. 1994. Scand J Plast Reconstr Hand Surg 28: 95-105.
42. Huang K.F. et al. 1993. Arch Surg 128: 47-54.
43. Strock. L.L. et al. 1990. Surgery 108 (2): 161-164.
44. Clemmons D.R. 1994. Arm Intern Med 120: 596-597.
45. Lo H.C. et al. 1995. Am J Physiol 269: E368-E376.
46. Guler et al. 1988. Proc-Nati Acad Sci USA 85: 4889-4893.
47. Walker J.L. et al. 1991. N Engi J Med 324: 1483-1488.
48. Pierre et al. 1997. J Bum Care Rehab 18 (4): 287-291.
49. Jabri N. et al. 1994. Diabetes 43: 369-374.
50. Bondy C.A. et al. 1994. Ann Int Med 120: 593-601.
51. Filion, & Philips. BrJ Pharmacol 122: 551-557. 1997.
52. Noguchi A. et al. FEBS Lett; 433: 169-173. 1998.
53. Caplen N.J. et al. Nat Med; 1: 39-46. 1995.
54. Alexander, & Akhurst. 1995. Human Molecular Genetics 4 (12). 2279-2285.
55. O'Connor & Culp. Biotechniques; 17: 502-509. 1994.
56. Lasic D.D. Liposomes in gene delivery. CRC Press, New York.
57. IGF-I APR
58. Kupper T.S. et al. Surgery 100: 409-414. 1986.
59. Gamer W.L. et al. Surgery; 116: 42-48. 1994.
60. Hemdon D.N. et al. 1978. J. Surg. Res.; 25: 394-403.
61. Hoekstra M.J. et al., 1994. Bums 20: S43-47.
62. Van Baare J. et al., 1994. Bums 20: S77-80.
63. Hettich R. et al., 1994. Bums 20: 871-76.
64. Richters C.D. et al., 1997. J. Bum Care Rehabil. 18: 228-233.
65. Патент США №4361552, выданный Baur Jr.
66. Патент США №5002071, выданный Harrell.
67. Thierry A.R. et al., 1996. Ferns Immunol. Med. Microbiol. V.14. P.221-230.




Изобретение относится к области медицины, а именно к генной терапии, и касается нуклеотидной последовательности, кодирующей инсулиноподобный фактор роста человека, IGF-1, представленную синтетическим геном, включающим последовательность SEQ ID NO:1, рекомбинантной плазмидной ДНК, содержащей эту последовательность, эукариотической клетки, содержащей рекомбинантную плазмидную ДНК, конструкции для генной терапии и фармацевтической композиции для генной терапии, обладающей регенеративным и ранозаживляющим действием. Преимущество изобретения заключается в снижении доз инъекционных препаратов и частоты их введения. 5 н.п. ф-лы, 6 ил.
1. Нуклеотидная последовательность синтетического гена инсулиноподобного фактора роста-1 (IGF-1) человека, представленная в перечне последовательности SEQ ID NO:1.
2. Рекомбинантная плазмидная ДНК, содержащая нуклеотидную последовательность синтетического гена инсулиноподобного фактора роста-1 (IGF-1) человека по п.1.
3. Эукариотическая клетка, содержащая рекомбинантную плазмидную ДНК по п.2 - продуцент инсулиноподобного фактора роста-1 (IGF-1) человека.
4. Конструкция для генной терапии, содержащая цитомегаловирусный промотор, нуклеотидную последовательность синтетического гена инсулиноподобного фактора роста-1 (IGF-1) человека по п.1, сайт полиаденилирования, ген устойчивости к ампициллину, общим размером 3662 нуклеотида.
5. Фармацевтическая композиция для генной терапии, обладающая регенераторным и ранозаживляющим действием, характеризующаяся тем, что содержит конструкцию по п.4 и фармацевтически приемлемый носитель.
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| US 5077276 A, 31.12.1991 | |||
| US 5612198 A, 18.03.1997. | |||
Авторы
Даты
2009-11-20—Публикация
2007-07-02—Подача