Изобретение относится к медицине, в частности к лучевой диагностике, и может быть использовано для исследования больных опухолями головного мозга.
Известен способ диагностики опухолей головного мозга методом однофотонной эмиссионной компьютерной томографии с 99mTc-метоксиизобутилизонитрилом [Conti P.S. Introduction to imaging brain tumor metabolism with positron emission tomography /P.S.Conti // Cancer Invest. - 1995. - Vol.13. - P.244-259; Scotti G. Tumors of the brain / G.Scotti // Abstr. 10 Th. European. Congress of Radiology. Venna, Austria, March 2-7. - 1997. - P.118].
В ряду основных факторов, ограничивающих возможности радионуклидного выявления опухолей, по мнению многих исследователей, на первом месте стоит низкий уровень накопления радиофармпрепарата в некоторых опухолевых образованиях или малые (менее 1,5-2 см в диаметре) их размеры [Saha G.B. Radiofarmaceuticals for brain imaging / G.B.Saha, W.J.Maclntyre, R.T.Go // Seminars in Nucl. Med. - 1994. - Vol.24, №5 - P.324-349; Soler C. Technetium-99m sestamibi brain single-photon emission computed tomography for detection of recurrent gliomas after radiation therapy / C.Soler, P.Beauchesne, K.Maatougui et al. // EJNM. - 1998. - Vol.25, №12. - P.1649-1657; Soler С. Technetium-99m sestamibi brain single-photon emission computed tomography for detection of recurrent gliomas after radiation therapy / C.Soler, P.Beauchesne, K.Maatougui et al. // EJNM. - 1998. - Vol.25, №12. - P.1649-1657]. Так, по данным ряда авторов, визуализация низкозлокачественных глиальных опухолей головного мозга с применением однофотонной эмиссионной томографии с 99mTc-метоксиизобутилизонитрилом затруднительна и, таким образом, не является информативным методом в дифференциальной диагностике высоко- и низкозлокачественных глиальных опухолей [Henze M. Detection of tumour progression in the follow-up of irradiated low-grade astrocytomas: comparison of 3-[123I]iodo-α-methyl-L-tyrosine and 99mTc-MIBI SPET / M.Henze, A.Mohammed, H.Schlemmer, et al. // EJNM. - 2002. - Vol.29, №11. - P.1455-1461].
Цель изобретения - повышение информативности метода однофотонной эмиссионной компьютерной томографии головного мозга в диагностике и определении степени злокачественности глиальных опухолей.
Цель достигается тем, что проводят два исследования после однократного внутривенного введения радиофармпрепарата 99mTc-метоксиизобутилизонитрила: первичное раннее (через 1 час) и повторное отсроченное (через 4 часа), и на основании времени появления очагов гиперфиксации препарата и их интенсивности дифференцируются глиальные опухоли высокой и низкой степени злокачественности.
Способ реализуется путем исследования с использованием однофотонной эмиссионной компьютерной томографии после внутривенного введения радиофармпрепарата и отличается тем, что проводят раннее через 1 час и повторное исследование через 4 часа, при выявлении на томосцинтиграммах через 1 час после введения препарата очага интенсивного патологического накопления, который сохраняется и при повторном исследовании через 4 часа, диагностируется опухоль высокой степени злокачественности, при отсутствии патологического накопления препарата при исследовании через 1 час и появлении очагов накопления при повторном исследовании диагностируется глиальная опухоль низкой степени злокачественности.
Для глиальных опухолей высокой степени злокачественности (grade III-IV по классификации ВОЗ, 2001) характерным является быстрый захват препарата тканью опухоли и появление ранних очагов гиперфиксации радиофармпрепарата в опухолевом узле уже при первичном раннем исследовании. Интенсивность накопления РФП в опухоли высокой степени злокачественности к четырем часам исследования может как возрастать, так и несколько снижаться в зависимости от активности внутриклеточных систем элиминации препарата из клеток, вместе с тем характерным является относительное снижение активности накопления РФП в мягких тканях головы и в сосудистых сплетениях боковых желудочков. Опухоли низкой степени злокачественности (grade I-II по классификации ВОЗ, 2001) отличаются более медленным и постепенным накоплением радиофармпрепарата в течение 3-4 часов и появлением очагов повышенного его накопления в опухолевом узле при отсроченном (через 4 часа) сканировании при полном отсутствии или незначительно выраженном накоплении его на ранних томосцинтиграммах.
Различия в характере и динамике накопления радиофармпрепарата в глиальных опухолях головного мозга различной степени злокачественности основаны на механизме накопления препарата и особенностях метаболизма и функции опухолевых клеток с различной степенью анаплазии. Используемый радиофармпрепарат проникает внутрь клеток путем пассивного переноса, активность и скорость которого зависит от величины трансмембранного потенциала и активности мембранной K-Na АТФ-азы, а накапливается и фиксируется препарат внутриклеточно на мембранах митохондрий. Количество накопленного радиофармпрепарата внутри клетки зависит от количества и активности митохондрий, которые в клетках с высокой степенью анаплазии гораздо выше, чем в клетках, имеющих гистологическую активность, близкую к доброкачественной.
Однофотонная эмиссионная компьютерная томография с целью дифференциальной диагностики глиальных опухолей проводится пациентам после выполнения магнитно-резонансной или рентгеновской компьютерной томографии, при которых у них выявлены новообразования. Результаты томосцинтиграфии подтверждены данными гистологического исследования послеоперационного материала или материала, полученного путем стереотаксической биопсии.
Клинические примеры.
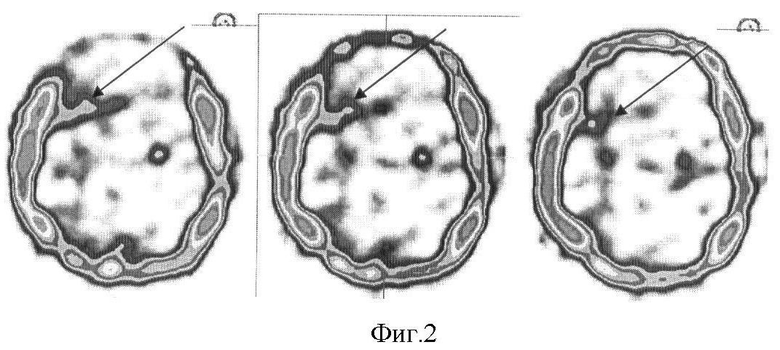
1. Пациент С., 53 лет (гистологическое заключение: фибриллярно-протоплазматическая астроцитома, grade II по классификации ВОЗ, 2001). При лучевом обследовании выявлено объемное образование правой височной доли головного мозга. На томосцинтиграммах головного мозга через 1 час после внутривенного введения РФП в передних отделах правой височной доли отмечается незначительно повышенное накопление РФП (см. фиг.1). На отсроченных томосцинтиграммах определяется участок повышенного накопления РФП, значительно превышающий по интенсивности накопление РФП в окружающей ткани мозга, а также накопление препарата на ранних томограммах в данном месте (см. фиг.2).
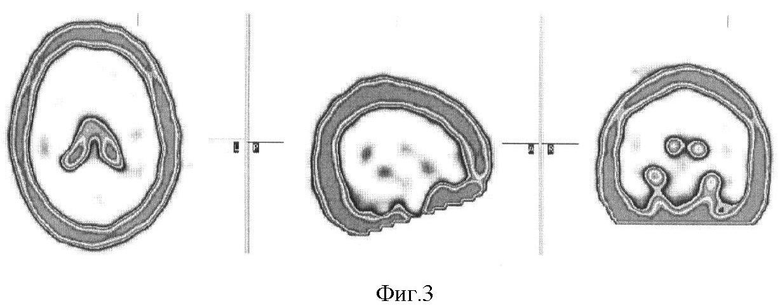
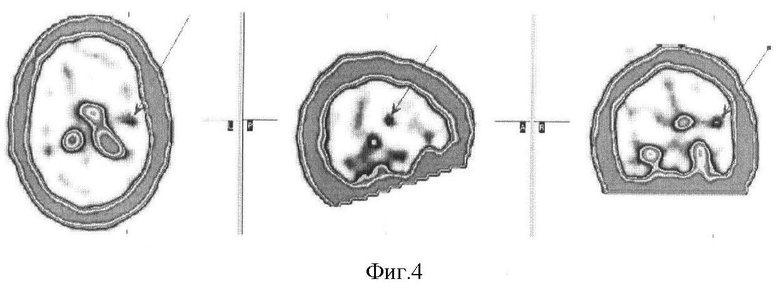
2. Пациент К., 34 года (гистологическое заключение: фибриллярная астроцитома, grade II по ВОЗ, 2001). По данным МРТ у пациента имеется новообразование левой височной области, вероятнее всего глиального ряда, незначительно смещающее срединные структуры в противоположную сторону, без выраженного отека окружающей ткани мозга, не накапливающее контрастное вещество при внутривенном усилении. При ОФЭКТ через 1 час после введения РФП очагов патологического накопления РФП не определяется (см. фиг.3), отмечается характерная для нормального распределения РФП в ткани мозга неоднородность накопления, вместе с тем имеется незначительная деформация левого бокового желудочка. При отсроченном сканировании через 4 часа в левой височной области отчетливо визуализируется округлый участок патологического накопления препарата (см. фиг.4).
3. Пациент С., 50 лет (гистологическое заключение: анапластическая астроцитома, grade III по ВОЗ, 2001). В правой височной доле головного мозга визуализируется очаг раннего интенсивного патологического накопления РФП с неровными контурами, неоднородной структуры, значительно превышающее накопление в окружающей мозговой ткани. Очаг визуализируется как при раннем сканировании через 1 час после внутривенного введения РФП (см. фиг.5), так и через 4 часа при отсроченном сканировании (см. фиг.6).
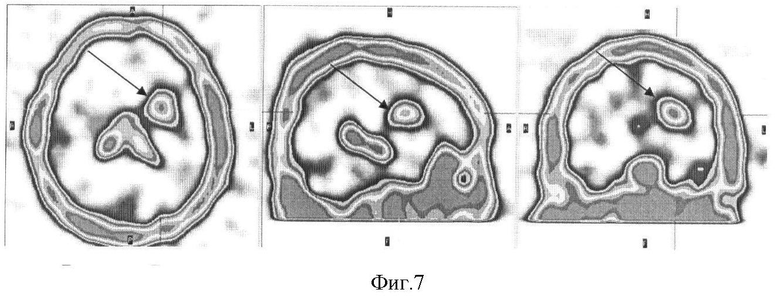
4. Больная Ж., 48 лет (гистологическое заключение: глиобластома, grade IV по ВОЗ, 2001). При лучевом обследовании выявлено объемное патологическое образование левой лобно-височной области с перифокальным отеком и накапливающее контрастное вещество после внутривенного его введения. При ОФЭКТ на томосцинтиграммах как через 1 час (см. фиг.7), так и через 4 часа после внутривенного введения визуализируется очаг интенсивного значительно повышенного накопления РФП в левой лобно-височечной области с четкими неровными контурами (см. фиг.8). Интенсивность накопления препарата на фоне снижения его накопления в сосудистых сплетениях боковых желудочков и мягких тканях головы к 4 часам исследования не снижалась.
Разграничение опухолей по степени злокачественности имеет ключевое значение, как в плане прогноза заболевания, так и для выбора способа лечения. При высокозлокачественных глиальных опухолях головного мозга 50% выживаемость составляет лишь 9-10 месяцев, а при опухолях низкой степени злокачественности 50-75% больных достигает 5-летней выживаемости [Grossman S.A. Thymidine, leucine and 2-deoxyglucose incorporation in brain tumors and abscess: a quantitative autoradiographic (QAR) study with implications for PET scans / S.A.Grossman, S.Eller, J. Dick et al. // Ann. Proc. Am. Assos. Cancer Res. - 1998. - Vol.29, №3. - P.516].
Значительным шагом в этом направлении явилась разработка и внедрение в клиническую практику методов ядерной медицины, таких как однофотонная эмиссионная компьютерная и позитронно-эмиссионная (двухфотонная) томография (ПЭТ) [Корсаков М.В. Руководство по ПЭТ радиохимии / М.В.Корсаков. - СПб., 2002. - 180 с.; Медведев Н.П. Позитронная эмиссионная томография в диагностике объемных образований головного мозга / Н.П.Медведев, Н.П.Бехтерева, Н.А.Костеников и др. // Вопр. нейрохирургии. - 1996. - №1. - С.21-26]. Эти методы позволили визуализировать функциональные процессы, протекающие в нормальных условиях, и при возникновении неопластической патологии проводить своего рода неинвазивную биопсию, что в значительной мере приблизило лучевых диагностов к гистологическому заключению [Костеников Н.А. Позитронная эмиссионная томография - новые возможности в онкологии / Н.А.Костеников, М.М.Власова, Е.Е.Кузнецова // Тезисы докладов научной сессии: «Современные возможности лучевой диагностики повреждений и заболеваний у военнослужащих». - СПб., 1997. - С.36-37; Тютин Л.А. Комлексная лучевая диагностика опухолей головного мозга (МРТ, МРА, МРС, ПЭТ) / Л.А.Тютин, А.В.Поздняков, Н.А.Костеников // Материалы VI международного симпозиума: «Современные минимально-инвазивные технологии (нейрохирургия, вертебрология, неврология, нейрофизиология). - СПб., 2001. - С.103-104]. Однако, несмотря на проводимые исследования и последние работы в этой области, определение роли и места методов ядерной медицины в общем алгоритме лучевой диагностики опухолей головного мозга, уточнение роли и информативности применяемых радиофармацевтических препаратов были и остаются ключевыми проблемами ядерной нейроонкологии [Бродская З.Л. Позитронно-эмиссионная томография в предоперационной дифференциальной диагностике церебральных астроцитом / З.Л.Бродская, Т.Ю.Скворцова, М.С.Рудас и др. // III съезд нейрохирургов в России. - СПб., 2002. - С.653-654; Костеников Н.А. Однофотонная эмиссионная томография в диагностике продолженного роста злокачественных опухолей головного мозга / Н.А.Костеников, Н.П.Фадеев, Л.А.Тютин, P.M.Жабина // Материалы научной конференции: «Актуальные вопросы лучевой диагностики и интервенционной радиологии». - СПб., 1997. - С.57; Лишманов Ю.Б. Радионуклидная диагностика для практических врачей / Ю.Б.Лишманов, В.И.Чернов. - Томск, 2004. - 387 с.; Скворцова Т.Ю. ПЭТ диагностика астроцитарных опухолей головного мозга: Дисс. … канд. мед. наук / Т.Ю.Скворцова. - СПб., 2004. - 173 с.].
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ДИАГНОСТИКИ ОБЪЕМНЫХ ОБРАЗОВАНИЙ ГОЛОВНОГО МОЗГА | 1998 |
|
RU2138991C1 |
| Способ дифференциальной диагностики глиом высоких грейдов | 2022 |
|
RU2786003C1 |
| Способ радионуклидной диагностики опухолей головного мозга | 2017 |
|
RU2692451C2 |
| Способ оценки степени злокачественности опухолей головного мозга | 2022 |
|
RU2786824C1 |
| СПОСОБ ВЫЯВЛЕНИЯ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ МОЛОЧНОЙ ЖЕЛЕЗЫ | 1998 |
|
RU2134546C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ОПУХОЛЕЙ ЩИТОВИДНОЙ ЖЕЛЕЗЫ | 2008 |
|
RU2386398C1 |
| СПОСОБ РАДИОНУКЛИДНОЙ ДИАГНОСТИКИ РАКА ЛЕГКОГО | 2008 |
|
RU2397704C2 |
| Способ радионуклидной диагностики рака гортани и гортаноглотки | 2017 |
|
RU2679298C1 |
| СПОСОБ ВЫЯВЛЕНИЯ ПАТОЛОГИЧЕСКИХ СОСТОЯНИЙ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ | 1998 |
|
RU2134545C1 |
| Способ радионуклидной диагностики операбельного рака молочной железы с гиперэкспрессией Her2/neu | 2019 |
|
RU2702294C1 |




Изобретение относится к медицине и предназначено для дифференциальной диагностики высоко- и низкозлокачественных глиальных опухолей головного мозга. После внутривенного введения радиофармпрепарата проводят однофотонную эмиссионную компьютерную томографию. Исследование осуществляют через 1 час и через 4 часа. При выявлении на томосцинтиграммах через 1 час после введения препарата очага интенсивного патологического накопления, который сохраняется и при повторном исследовании через 4 часа, диагностируют опухоль высокой степени злокачественности. При отсутствии патологического накопления препарата при исследовании через 1 час и появлении очагов накопления при повторном исследовании диагностируют глиальные опухоли низкой степени злокачественности. Предлагаемый способ позволяет поставить дифференциальный диагноз на основании однофотонной эмиссионной компьютерной томографии головного мозга. 8 ил.
Способ дифференциальной диагностики высоко- и низкозлокачественных глиальных опухолей головного мозга путем исследования с использованием однофотонной эмиссионной компьютерной томографии после внутривенного введения радиофармпрепарата, отличающийся тем, что проводят исследование через 1 ч и повторное исследование через 4 ч, при выявлении на томосцинтиграммах через 1 ч после введения препарата очага интенсивного патологического накопления, который сохраняется и при повторном исследовании через 4 ч, диагностируют опухоль высокой степени злокачественности, при отсутствии патологического накопления препарата при исследовании через 1 ч и появлении очагов накопления при повторном исследовании диагностируют глиальные опухоли низкой степени злокачественности.
| CONTI PSl | |||
| Introduction to imaging brain tumor metabolism with positron emission tomography (PET) | |||
| Review | |||
| Cancer Invest | |||
| Топка с качающимися колосниковыми элементами | 1921 |
|
SU1995A1 |
| СПОСОБ ДИАГНОСТИКИ ДОБРОКАЧЕСТВЕННЫХ И ЗЛОКАЧЕСТВЕННЫХ ГЛИАЛЬНЫХ ОПУХОЛЕЙ | 1999 |
|
RU2154830C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АНГИОГЕНЕЗА ГЛИОМЫ | 2001 |
|
RU2203620C1 |
| ДЕКАН В | |||
| и др | |||
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
Авторы
Даты
2009-12-20—Публикация
2007-07-09—Подача