Изобретение относится к медицине, в частности к способам оценки степени злокачественности опухолей головного мозга.
Первичные опухоли центральной нервной системы (ЦНС), по данным Министерства здравоохранения РФ, составляют 2% в структуре онкологической заболеваемости (Каприн А.Д., 2019). Ежегодно в России регистрируется около 32100 новых случаев заболевания опухолями ЦНС. Наряду с этим в отчете CBTRUS (The Central Brain Tumor Registry of the United State - Центральный реестр опухолей головного мозга Соединенных Штатов), являющемся крупнейшим популяционным реестром, ориентированным исключительно на первичные опухоли центральной нервной системы, говорится, что показатель заболеваемости опухолями ЦНС составляет 23,4 на 100 тысяч населения (QuinnT., 2019). Более тридцати процентов (30,2%) всех опухолей ЦНС являются злокачественными. При этом в 14,6% случаев опухоль представлена глиобластомой головного мозга, которая составляет практически половину (48,3%) от всех первичных злокачественных опухолей ЦНС. Показатель смертности при злокачественных опухолях ЦНС равен в среднем 4,42 на 100 тысяч населения. В развитых странах пятилетняя выживаемость пациентов с опухолями головного мозга не превышает 35,8%. Самые низкие показатели пятилетней выживаемости пациентов со злокачественными новообразованиями ЦНС наблюдаются в возрастной группе ≥40 лет, всего 21,3%, а это самый активный в социальном отношении возраст.
В настоящее время основными методами лучевой диагностики опухолей головного мозга являются магнитно-резонансная томография (МРТ) и рентгеновская компьютерная томография (КТ) (Ideguchi М., 2015). В случае со злокачественными опухолями головного мозга МРТ в различных последовательностях имеет основополагающее значение для структурной характеристики опухоли, определения хирургической стратегии, планирования и оценки результатов лучевого и химиолучевого лечения. По данным разных исследователей, чувствительность МРТ с контрастным усилением в диагностике первичных опухолей головного мозга составляет 70-93% (van Dijken В., 2017). Показатели специфичности магнитно-резонансной томографии в диагностике объемных образований головного мозга весьма вариабельны и зависят от различных факторов и их сочетаний. В большей степени на специфичность МРТ в визуализации опухолей головного мозга влияют размер образования, его локализация, гистологический тип и степень злокачественности, выраженность сосудистого компонента и, как следствие, уровень кровотока в опухоли (European Association for Neuro-Oncology (EANO), 2017). Кроме того, специфичность метода нередко зависит от правильности выбора режима и последовательности проведения магнитно-резонансной томографии. Усредненные показатели специфичности МРТ в диагностике всех типов опухолей головного мозга составляют 81-90% (Okuchi S., 2019). Наряду с магнитно-резонансной томографией для диагностики опухолей головного мозга сегодня применяется спиральная компьютерная томография (СКТ). Особое значение СКТ имеет в тех случаях, когда существует подозрение на вовлечение в патологический процесс костных структур, а при невозможности выполнения пациенту МРТ компьютерная томография становится единственным методом диагностики опухолей головного мозга. Ключевую роль в визуализации опухолей головного мозга методом СКТ играет применение перфузионных технологий. Так, многочисленные исследования свидетельствуют, что чувствительность и специфичность КТ-перфузии в диагностике глиом высокой степени злокачественности составляют 85,7% и 100% соответственно (Caras А., 2020).
Безусловно, СКТ и МРТ являются эффективными методами, позволяющими с высокой степенью детализации визуализировать как нормальные органы и анатомические структуры организма, так и патологические изменения в них. Несмотря на применение различных современных методик, позволяющих косвенно судить об уровне метаболизма опухоли, МРТ и СКТ по-прежнему остаются в первую очередь методами точной анатомо-топографической визуализации опухолевого поражения той или иной локализации. Гораздо больший интерес с позиции изучения метаболических процессов в опухоли и окружающих тканях в настоящее время представляют методы ядерной медицины и молекулярной визуализации. Методы ядерной медицины достаточно широко применяются в онкологии уже на протяжении многих десятков лет. Они отличаются функциональностью, то есть способностью отражать течение физиологических и патологических процессов в организме в целом и в отдельных органах в частности. Основными методами ядерной медицины являются однофотонная эмиссионная компьютерная томография (ОФЭКТ, SPECT) и позитронно-эмиссионная томография (ПЭТ, PET).
Особенное значение методы ядерной медицины имеют в диагностике злокачественных опухолей головного мозга. Безоговорочное лидерство среди методов ядерной медицины в диагностике опухолей головного мозга в последние годы удерживает позитронно-эмиссионная томография с различными радиофармацевтическими лекарственными препаратами (РФЛП) (Suchorska В., 2014). Считается, что ПЭТ с 11С-МЕТ является сегодня эталонным методом в диагностике опухолей головного мозга. По данным разных авторов, усредненные показатели чувствительности и специфичности ПЭТ с 11С-МЕТ в визуализации опухолей головного мозга различной степени злокачественности составляют 89-90% и 94-100% соответственно (Takenaka S., 2014; Не Q.,2019).
Несмотря на доказанную высокую диагностическую эффективность позитронно-эмиссионной томографии с различными препаратами, широкое применение этого метода по-прежнему ограничено из-за высокой стоимости оборудования, диагностической процедуры и сложного цикла изготовления циклотронных РФЛП.
Следует отметить, что такой метод ядерной медицины, как ОФЭКТ, сегодня значительно доступнее для населения, чем ПЭТ, как в мире, так и в нашей стране. Наиболее часто используемым радионуклидом для ОФЭКТ является технеций-99 м. В свою очередь главным достоинством РФЛП на основе производных глюкозы, меченных технецием-99м, является то, что визуализация опухолевой ткани с их применением может быть произведена с помощью гамма-камеры, а это значительно снижает стоимость диагностической процедуры. Использование РФЛП на основе производных глюкозы, меченных технецием-99м, позволит на молекулярном уровне изучать биохимические процессы, протекающие в организме, за счет включения производных глюкозы в нормальные и патологические метаболические процессы и получать информацию, по уникальности и достоверности не уступающую ПЭТ-исследованиям (Dapueto R., 2015; Stasyuk Е., 2020).
Наиболее близким способом диагностики опухолей головного мозга различной степени злокачественности является способ с применением метода позитронной эмиссионной томографии ПЭТ с 11С-МЕТ (Kawai N, Kagawa М, Hatakeyama Т, Tamiya Т, Noshiyama Y, Yamamoto Y, Miki A, Ichikawa Т. 11C-methionine positron emission tomography in brain tumor. No Shinkei Geka. 2008 Oct;36(10):847-59. Japanese. PMID: 18975560).
Новый технический результат - повышение доступности, эффективности, точности и информативности оценки степени злокачественности опухолей головного мозга. Для достижения нового технического результата в способе оценки степени злокачественности опухолей головного мозга включающем внутривенное введение радиофармацевтического препарата и последующее проведение сцинтииграфических исследований, вводят радиофармацевтический лекарственный препарат «99mTc-1-тио-D-глюкоза» в дозе 500 МБк, через 40 минут выполняют ОФЭКТ исследование и при визуализации очагов метаболической гиперфиксации препарата в проекции головного мозга выполняют расчет показателя опухоль/фон и при значении опухоль/фон <4,425 диагностируют опухоль головного мозга со степенью злокачественности Grade II, при значении опухоль/фон 4,425-8,205 - опухоль головного мозга со степенью злокачественности Grade III, и при значении опухоль/фон >8,205 - опухоль головного мозга со степенью злокачественности Grade IV.
Способ осуществляют следующим образом.
Пациенту с опухолью головного мозга вводят внутривенно радиофармацевтический лекарственный препарат «99mTc-1-тио-D-глюкозу», через 40 минут после внутривенного введения препарата в дозе 500 МБк выполняют ОФЭКТ исследование и при визуализации очагов метаболической гиперфиксации препарата в проекции головного мозга выполняют расчет показателя опухоль/фон и при значении опухоль/фон <4,425 диагностируют опухоль головного мозга со степенью злокачественности Grade II, при значении опухоль/фон 4,425-8,205 - опухоль головного мозга со степенью злокачественности Grade III, и при значении опухоль/фон >8,205 - опухоль головного мозга со степенью злокачественности Grade IV.
Способ основан на анализе результатов экспериментальных клинических исследований. Для подтверждения эффективности способа в оценке степени злокачественности опухолей головного мозга были выполнены экспериментальные клинические исследования по изучению накопления радиофармацевтического препарата «99mTc-l-тио-D-глюкоза» у 70 пациентов с верифицированным диагнозом злокачественной опухоли головного мозга Grade II-IV. Всем пациентам внутривенно вводили радиофармацевтический препарат на основе меченной технецием-99m производной глюкозы «99mTc-1-тио-D-глюкоза» в дозе 500 МБк. Радиофармацевтический препарат на основе меченной технецием-99m производной глюкозы «99mTc-1-тио-D-глюкоза» готовили непосредственно перед введением согласно разработанной инструкции по применению: 4 мл раствора натрия пертехнетата (Na99mTcO4) из генератора в асептических условиях вводили с помощью шприца во флакон с реагентом путем прокалывания резиновой пробки иглой. При необходимости предварительно проводили разбавление элюата изотоническим раствором натрия хлорида до требуемой величины объемной активности. Содержимое флакона перемешивали встряхиванием и инкубировали при комнатной температуре в течение 30 минут до полного растворения реагента. Стерильность препарата достигалась путем применения бактериального фильтра. Состав радиофармацевтического препарата «99mTc-1-тио-D-глюкоза» представлен в таблице 1. Анализ качества препарата «99mTc-1-тио-D-глюкоза» осуществляли путем измерения радиохимической чистоты с помощью мгновенной тонкослойной радиохроматографии.
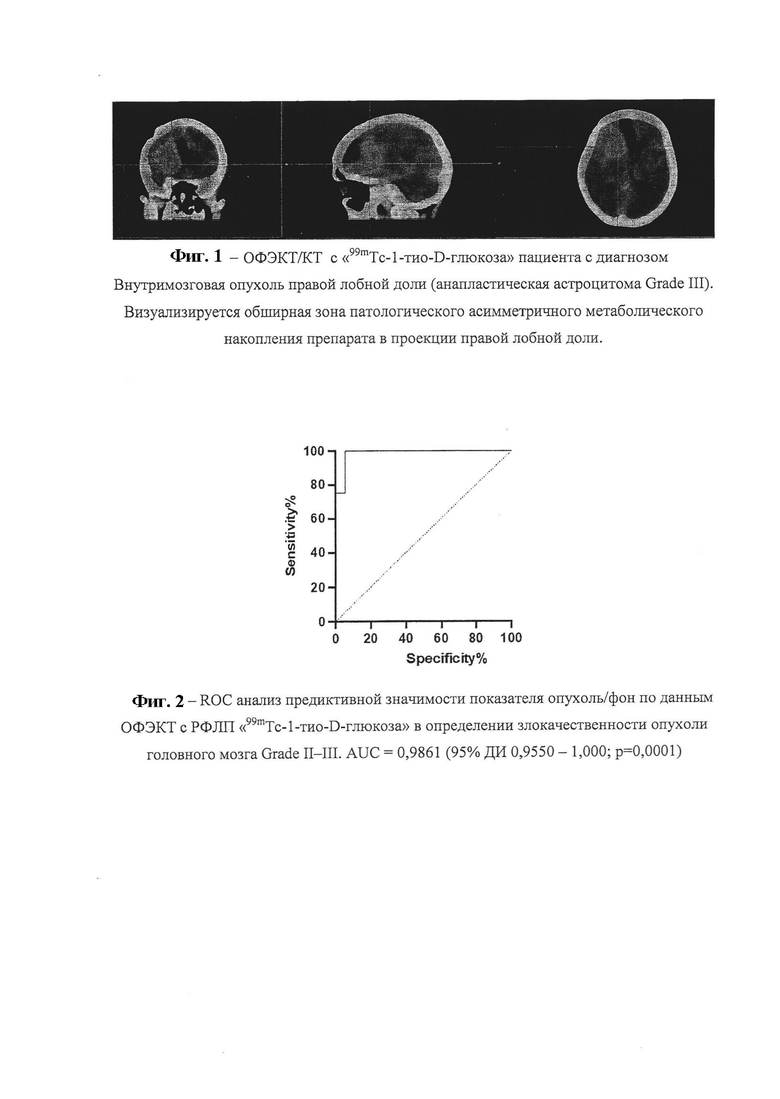
Через 40 минут после внутривенного введения препарата пациентам выполняли однофотонную эмиссионную компьютерную томографию головного мозга. Патологическими считались участки метаболической гиперфиксации препарата в проекции головного мозга (Фиг. 1) Приложения. Вместе с этим производили расчет показателя опухоль/фон для каждого клинического случая. Полученные результаты сопоставляли с результатами патоморфологического и иммуногистохимического исследования в каждом клиническом случае. Особое значение предавалось изучению зависимости уровня показателя опухоль/фон и значений пролиферативного маркера Ki 67, отражающего степень злокачественности опухоли Grade II-IV. На основании статистического анализа полученного массива данных была установлена положительная корреляционная взаимосвязь изучаемых показателей в общей группе пациентов со степенью злокачественности опухоли головного мозга Grade II-IV. Коэффициент корреляции для показателя опухоль/фон с уровнем пролиферативного маркера Ki 67 составил 0,8516 (0,7680-0,9067). На следующем этапе обработки и анализа полуколичественных показателей ОФЭКТ головного мозга с РФЛП «99mTc-1-тио-D-глюкоза» был проведен ROC анализ с целью получения достоверной информации о предиктивной значимости показателя опухоль/фон в определении степени злокачественности опухоли головного мозга, то есть, Grade опухоли по ВОЗ.
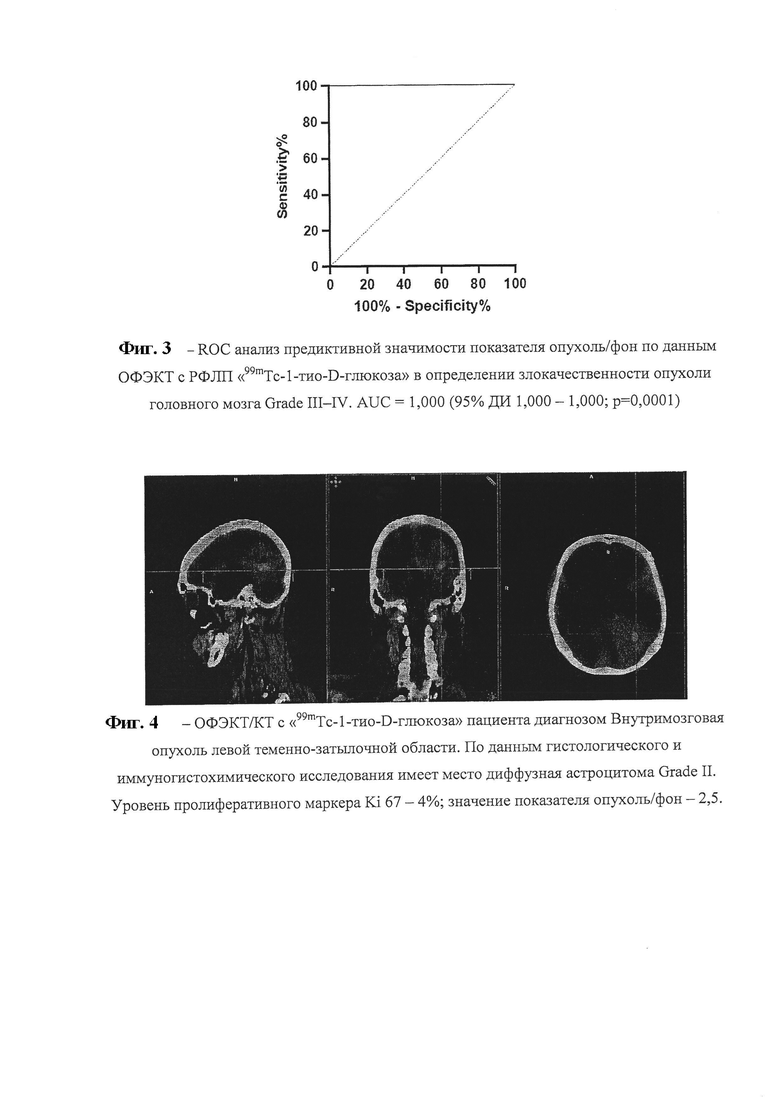
При этом было установлено, что пороговое значение показателя опухоль/фон <4,425 характерно для опухолей головного мозга Grade II, а значения показателя опухоль/фон >4,425 свидетельствует о наличии у пациента опухоли Grade III. Площадь под кривой (AUC) составила 0,9861 (95% ДИ 0,9550 - 1,000; р=0,0001). Чувствительность и специфичность - 100 и 94,4% соответственно (Фиг. 2а, 2б) Приложения. Выполненный ROC-анализ с целью определения предиктивной значимости показателя опухоль/фон в отнесении опухоли головного мозга к Grade III-IV по данным ОФЭКТ с РФЛП «99mTc-1-тио-D-глюкоза» продемонстрировал, что для опухолей головного мозга Grade III характерно значение опухоль/фон <8,205, а для опухолей Grade IV> 8,205. Площадь под кривой (AUC) составила 1,000 (95% ДИ 1,000 - 1,000; р=0,0001), при этом значения чувствительности и специфичности находились на уровне 100% (Фиг. 3).
Таким образом, полученные результаты свидетельствуют о возможности использования количественного показателя опухоль/фон при ОФЭКТ с РФЛП «99mTc-1-тио-D-глюкоза» у пациентов со злокачественными новообразованиями головного мозга в качестве маркера степени злокачественности опухоли головного мозга, а его количественные пороговые значения позволяют с высокой чувствительностью (100%) и специфичностью (94,4-100%) производить дифференциальную диагностику и устанавливать степень злокачественности опухоли Grade II-IV на дооперационном этапе по данным ОФЭКТ с РФЛП «99mTc-1-тио-D-глюкоза». В качестве пороговых значений показателя опухоль/фон при опухолях головного мозга Grade II следует считать значения не превышающие <4,425. Для опухолей со степенью злокачественности Grade III по данным ОФЭКТ с РФЛП «99mTc-1-тио-D-глюкоза» значения показателя опухоль/фон находятся в интервалах 4,425-8,205, а для опухолей головного мозга со степенью злокачественности Grade IV характерны высокие значения опухоль/фон >8,205.
Таким образом, предлагаемый способ оценки степени злокачественности опухолей головного мозга с применением радиофармацевтического лекарственного препарата «99mTc-1-тио-D-глюкоза», позволяет с высокой чувствительностью и специфичностью установить степень злокачественности (Grade II-IV) опухоли головного мозга на дооперационном этапе неинвазивным методом ОФЭКТ. Применение предлагаемого способа позволит на этапе диагностики определить степень злокачественности опухоли, спрогнозировать вариант течения заболевания и поможет составить индивидуальный план лечения пациентов с опухолями головного мозга.
Клинические примеры
Пример 1. Пациент Б., 45 лет, Ds.: Внутримозговая опухоль левой теменно-затылочной области. На этапе первичной диагностики наряду со стандартными методами исследования пациенту выполнена ОФЭКТУКТ головного мозга с «99mTc-l-тио-D-глюкоза», при которой определялся очаг патологической гиперфиксации препарата в проекции левой теменно-затылочной области (фиг. 4). При расчете показателя опухоль/фон получено значение 2,5. По данным иммуногистохимического исследования постоперационного материала верифицирована диффузная астроцитома со степенью злокачественности Grade II. Уровень пролиферативного маркера Ki 67-4%. Согласно предлагаемому методу оценки степени злокачественности опухоли головного мозга значение опухоль/фон - 2,5 также соответствует Grade II (<4,425).
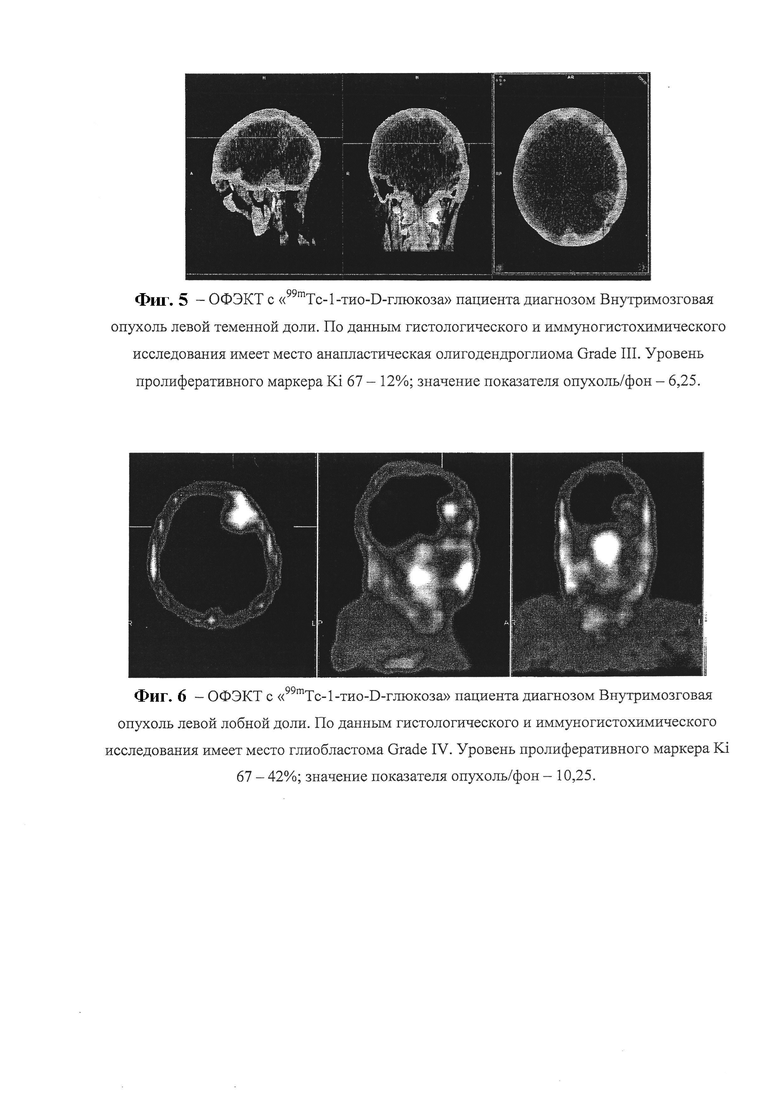
Пример 2. Пациент Г., 62 года, Ds.: Внутримозговая опухоль левой теменной доли. На этапе первичной диагностики пациенту выполнена ОФЭКТУКТ головного мозга с «99mTc-l-тио-D-глюкоза» в качестве дополнительного метода, при которой определялся очаг патологической гиперфиксации препарата в проекции левой теменной доли (фиг. 5). При расчете показателя опухоль/фон получено значение 6,25, которое находилось в пределах 4,425-8,205, что согласно предлагаемому способу соответствует степени злокачественности опухоли Grade III. По данным иммуногистохимического исследования постоперационного материала верифицирована анапластическая олигодендроглиома со степенью злокачественности Grade III. Уровень пролиферативного маркера Ki 67-12%.
Пример 3. Пациент Е., 28 лет, Ds.: Внутримозговая опухоль левой лобной доли. На этапе первичной диагностики в дополнение к стандартным методам пациенту выполнена ОФЭКТ головного мозга с «99mTc-l-тио-D-глюкоза». При этом был выявлен гиперинтенсивный очаг патологического метаболического накопления препарата в проекции левой лобной доли (фиг. 6). При расчете показателя опухоль/фон получено достаточно высокое значение - 10,25, которое, в соответствии с предлагаемым способом определения степени злокачественности опухоли, превышало пороговое значение >8,205 и соответствовало степени злокачественности Grade IV. Данные иммуногистохимического исследования постоперационного материала свидетельствовали о наличии у пациента глиобластомы Grade IV. Уровень пролиферативного маркера Ki 67-42%.

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ радионуклидной диагностики опухолей головного мозга | 2017 |
|
RU2692451C2 |
| Способ радионуклидной диагностики рака легкого | 2020 |
|
RU2751103C1 |
| Способ диагностики рака ободочной кишки | 2021 |
|
RU2755010C1 |
| СПОСОБ ПРОВЕДЕНИЯ ОДНОФОТОННОЙ ЭМИССИОННОЙ КОМПЬЮТЕРНОЙ ТОМОГРАФИИ ГОЛОВНОГО МОЗГА В ДИАГНОСТИКЕ И ОПРЕДЕЛЕНИИ СТЕПЕНИ ЗЛОКАЧЕСТВЕННОСТИ ГЛИАЛЬНЫХ ОПУХОЛЕЙ | 2007 |
|
RU2375961C2 |
| Способ радионуклидной диагностики рака молочной железы | 2017 |
|
RU2682880C1 |
| Способ радионуклидной диагностики рака гортани и гортаноглотки | 2017 |
|
RU2679298C1 |
| Способ радионуклидной диагностики рака предстательной железы | 2021 |
|
RU2776234C1 |
| Способ радионуклидной диагностики злокачественных лимфом | 2018 |
|
RU2706602C1 |
| СПОСОБ ДИАГНОСТИКИ РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ С ГИПЕРЭКСПРЕССИЕЙ HER2/NEU | 2022 |
|
RU2800818C1 |
| Способ радионуклидной диагностики операбельного рака молочной железы с гиперэкспрессией Her2/neu | 2019 |
|
RU2702294C1 |
Изобретение относится к медицине, а именно к лучевой диагностике, и может быть использовано для оценки степени злокачественности опухолей головного мозга. Вводят радиофармацевтический лекарственный препарат (РФЛП) «99mTc-1-тио-D-глюкоза» в дозе 500 МБк. Через 40 минут после введения препарата выполняют однофотонную эмиссионную томографию (ОФЭКТ). При визуализации очагов метаболической гиперфиксации препарата в проекции головного мозга выполняют расчет показателя опухоль/фон. При значении опухоль/фон <4,425 диагностируют опухоль головного мозга со степенью злокачественности Grade II, при значении опухоль/фон 4,425-8,205 - опухоль головного мозга со степенью злокачественности Grade III и при значении опухоль/фон>8,205 - опухоль головного мозга со степенью злокачественности Grade IV. Способ обеспечивает повышение доступности, эффективности, точности и информативности оценки степени злокачественности опухолей головного мозга за счет использования количественного показателя опухоль/фон при ОФЭКТ с РФЛП «99mTc-1-тио-D-глюкоза». 1 табл., 6 ил., 3 пр.
Способ оценки степени злокачественности опухолей головного мозга, включающий внутривенное введение радиофармацевтического препарата и последующее проведение сцинтиграфических исследований, отличающийся тем, что вводят радиофармацевтический лекарственный препарат «99mТс-1-тио-D-глюкоза» в дозе 500 МБк, через 40 минут выполняют однофотонную эмиссионную томографию и при визуализации очагов метаболической гиперфиксации препарата в проекции головного мозга выполняют расчет показателя опухоль/фон, при значении опухоль/фон <4,425 диагностируют опухоль головного мозга со степенью злокачественности Grade II, при значении опухоль/фон 4,425-8,205 - опухоль головного мозга со степенью злокачественности Grade III и при значении опухоль/фон >8,205 - опухоль головного мозга со степенью злокачественности Grade IV.
| СПОСОБ ПРОВЕДЕНИЯ ОДНОФОТОННОЙ ЭМИССИОННОЙ КОМПЬЮТЕРНОЙ ТОМОГРАФИИ ГОЛОВНОГО МОЗГА В ДИАГНОСТИКЕ И ОПРЕДЕЛЕНИИ СТЕПЕНИ ЗЛОКАЧЕСТВЕННОСТИ ГЛИАЛЬНЫХ ОПУХОЛЕЙ | 2007 |
|
RU2375961C2 |
| Способ радионуклидной диагностики опухолей головного мозга | 2017 |
|
RU2692451C2 |
| СПОСОБ ДИАГНОСТИКИ ОБЪЕМНЫХ ОБРАЗОВАНИЙ ГОЛОВНОГО МОЗГА | 1998 |
|
RU2138991C1 |
| ЗЕЛЬЧАН И | |||
| Г | |||
| и др | |||
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
| Медицинская радиология и радиационная безопасность | |||
| Способ регенерирования сульфо-кислот, употребленных при гидролизе жиров | 1924 |
|
SU2021A1 |
| Парный автоматический сцепной прибор для железнодорожных вагонов | 0 |
|
SU78A1 |
| ЗЕЛЬЧАН И | |||
| Г | |||
| и др | |||
| Возможность | |||
Авторы
Даты
2022-12-26—Публикация
2022-03-29—Подача