Изобретение относится к области биотехнологии, а именно к генно-инженерным конструкциям для экспрессии трансгенов в клетках млекопитающих с целью их применения в клеточной инженерии и в генной терапии, а именно к модификации последовательности гена для трансфекции клеток печени in vivo с целью экспрессии в них металлопротеиназы 8.
Металлопротеиназы представляют собой ферменты, расщепляющие белки, которые находят широкое применение в пищевой и легкой промышленности, в сельском хозяйстве, а также в медицине. В частности, матриксные металлопротеиназы обладают способностью расщеплять коллаген - основной компонент внеклеточного матрикса, и расщепление коллагена под действием этих ферментов приводит к уменьшению степени фиброза и к улучшению кровоснабжения клеток печени (Siller-Lopez F, et al. Gastroenterology 2004; 126: 1122-1133; IredaleJP, Gastroenterology. 2004 126(4): 1199-201). Для продуцирования ММР8 используют ДНК, содержащую природный ген металлопротеиназы 8 человека (Garcia-Bañuelos J, et al. Gene Theraphy. 2002 Jan; 9(2): 127-34).
Технической задачей, решаемой авторами настоящего изобретения, являлось создание гена металлопротеиназы 8, при включении которого в состав эукариотического вектора обеспечивался бы более высокий уровень экспрессии названного белка в клетках, трансфицированных названным вектором.
Технический результат достигался созданием гена MMP8opt путем модификации природной последовательности гена ММР 8 таким образом, чтобы триплет нуклеотидов, кодирующий каждую из аминокислот белковой последовательности ММР 8, встречался в генах человека наиболее часто.
На фиг.1. показана последовательность нуклеотидов гена MMP8opt, а также последовательность аминокислот кодируемого белкового продукта - матриксной металлопротеиназы 8 человека.
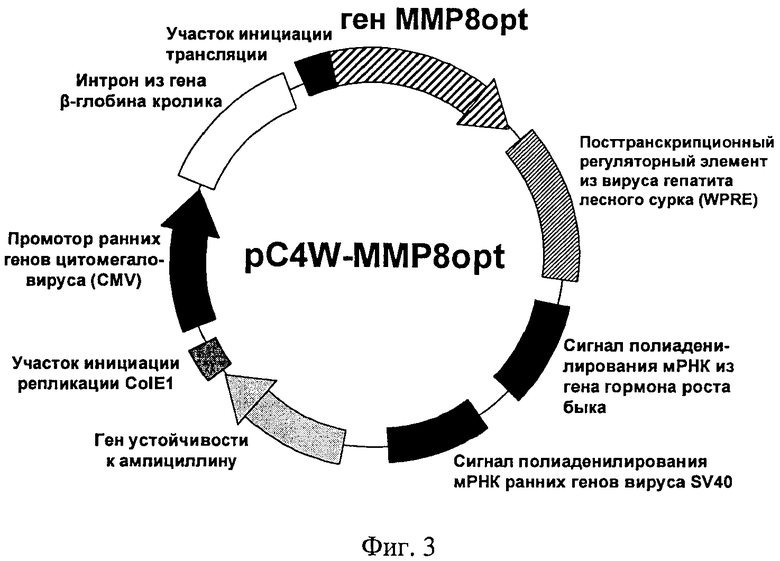
На фиг.2 показан предназначенный для клонирования участок ДНК вектора рВА, а на фиг.3 - функциональная карта плазмиды pC4W-MMP8opt
Синтез гена и плазмиды осуществляли с помощью стандартной технологии и оборудования, применяемых для решения подобных задач в генной инженерии (Watson, J.D., Gilman, M., Witkowski, J., Zoller, M. - Recombinant DNA, Scientific American Books, New York, 1992). Дизайн оптимизированной последовательности нуклеотидов, кодирующей матриксную металлопротеиназу человека ММР 8, производили, основываясь на вырожденности генетического кода. Для каждой аминокислоты белковой последовательности ММР 8 выбирали кодирующий ее триплет нуклеотидов, наиболее часто встречающийся в генах человека. При этом использовали частоты встречаемости кодонов, приведенные на вэб-сайте http://del.mediaglyphs.org/mg/bf/nucs_aa.html. Полученная таким образом последовательность нуклеотидов представлена на фиг.1.
Плазмиду pC4W-MMP8opt, несущую оптимизированный ген MMP8opt, получали методом генно-инженерного конструирования в 6 стадий.
На первой стадии изготавливали вектор для клонирования рВА. Для этого химически синтезированные пары олигонуклеотидов
VEC-89 (AAGCTTGGCATTCCGGTACTGTTGGTAAAGCCAC) и
VEC-90 (CCATGGTGGCTTTACCAACAGTACCGGAATGCCA),
VEC-91 (CATGGAGATCTCGTCTCTGGCCATCCCGGG) и
VEC-92 (CGGAACCCGGGATGGCCAGAGACGAGATCTC),
VEC-93 (TTCCGGATGTCTTCGATATCTGCAGGATCCT) и
VEC-94(CTAGAGGATCCTGCAGATATCGAAGACATC),
отжигали, смешивали и клонировали в расщепленный рестриктазами HindIII и XbaI вектор pBluescriptII-SK+. В результате вектор рВА имеет предназначенный для клонирования участок ДНК, представленный на фиг.2.
На второй стадии:
- в вектор рВА, расщепленный рестриктазами NcoI и ВаmHI, клонировали химически синтезированные пары олигонуклеотидов
ММР-101 (CATGTTCTCCCTGAAAACCCTGCCCTTCCTGC) и
MMP-102(GCAGCAGCAGGAAGGGCAGGGTTTTCAGGGAGAA),
ММР-103 (TGCTGCTGCACGTGCAGATCTCCAAGGCCTTC) и
ММР-104 (CACGGGGAAGGCCTTGGAGATCTGCACGTGCA),
ММР-105m (CCCGTGTCCTCCAAGGAGAAGAACACCAAGACCGTGCAATGTCTTCG) и
MMP-106m(GATCCGAAGACATTGCACGGTCTTGGTGTTCTTCTCCTTGGAGGA)
с получением промежуточной плазмиды pBD-MMP8-N1-D2;
- в вектор рВА, расщепленный рестриктазами BsmBI и ВаmHI, клонировали химически синтезированные пары олигонуклеотидов ММР-107 m
(GATCCGAAGACATTGCAGGACTACCTGGAGAAGTTCTACCAGCTGCCCAG) и ММР-108 m
(TGGTTGCTGGGCAGCTGGTAGAACTTCTCCAGGTAGTCCTGCAATGTCTTCG),
ММР-109 (CAACCAGTACCAGTCCACCAGGAAGAACGGCACCAAC) и
ММР-110 (GATCACGTTGGTGCCGTTCTTCCTGGTGGACTGGTAC),
ММР-111 (GTGATCGTGGAGAAGCTGAAGGAGATGCAGCGGTTCTTC) и
ММР-112 (GGCCGAAGAACCGCTGCATCTCCTTCAGCTTCTCCAC) с получением промежуточной плазмиды pBD-MMP8-D2-B3;
- в вектор рВА, расщепленный рестриктазами BsmBI и BbsI, клонировали химически синтезированные пары олигонуклеотидов
ММР-113 (GGCCTGAACGTGACCGGCAAGCCCAACGAGGAGACCCTGGACATGA) и
ММР-114 (TCTTCATCATGTCCAGGGTCTCCTCGTTGGGCTTGCCGGTCACGTTCA),
MMP-115 (TGAAGAAGCCTCGCTGCGGCGTGCCCGACAGCGGCGGCTTCATGCT) и
ММР-116 (GGGGTCAGCATGAAGCCGCCGCTGTCGGGCACGCCGCAGCGAGGCT),
MMP-117 (GACCCCAGGCAACCCCAAGTGGGAGCGCACCAACCTGACCTACAGAAT) и
ММР-118 (CCGGATTCTGTAGGTCAGGTTGGTGCGCTCCCACTTGGGGTTGCCT)
с получением промежуточной плазмиды рВА-ММР8-В3-А4;
- в вектор рВА, расщепленный рестриктазами BsmBI и BbsI, клонировали химически синтезированные пары олигонуклеотидов
ММР-119 (CCGGAACTACACCCCACAGCTGTCCGAGGCCGAGGTG) и
MMP-120(TCTCTCCACCTCGGCCTCGGACAGCTGTGGGGTGTAGTT),
ММР-121 (GAGAGAGCCATCAAGGACGCCTTCGAGCTGTGGA) и
ММР-122 (CCACGCTCCACAGCTCGAAGGCGTCCTTGATGGC),
MMP-123 (GCGTGGCCTCCCCTCTGATCTTCACCAGGATCTCCCAGGGCGA) и
ММР-124 (GGCCTCGCCCTGGGAGATCCTGGTGAAGATCAGAGGGGAGG) с получением промежуточной плазмиды рВА-ММР8-А4-В5;
- в вектор рВА, расщепленный рестриктазами BsmBI и BbsI, клонировали химически синтезированные пары олигонуклеотидов
ММР-125 (GGCCGACATCAACATCGCCTTCTACCAGAG) и
ММР-126 (TGGTCTCTCTGGTAGAAGGCGATGTTGATGTC),
ММР-127 (AGACCACGGCGACAACTCCCCCTTCGACGG) и
ММР-128 (TTGGGGCCGTCGAAGGGGGAGTTGTCGCCG),
ММР-129 (CCCCAACGGCATCCTGGCCCACGCCTTCCAGC) и
ММР-130 (CCGGGCTGGAAGGCGTGGGCCAGGATGCCG) с получением промежуточной плазмиды рВА-ММР8-В5-А6;
- в вектор рВА, расщепленный рестриктазами BsmBI и BbsI, клонировали химически синтезированные пары олигонуклеотидов
ММР-131 (CCGGCCAGGGCATCGGCGGCGACGCCCACTTCGACGCC) и
ММР-132 (CTCCTCGGCGTCGAAGTGGGCGTCGCCGCCGATGCCCTGG),
ММР-133 (GAGGAGACCTGGACCAACACCTCCGCCAACTACAACCTGT) и
ММР-134 (CCAGGAACAGGTTGTAGTTGGCGGAGGTGTTGGTCCAGGT),
MMP-135 (TCCTGGTGGCCGCCCACGAGTTCGGCCACTCCCTGGGCCT) и
MMP-136 (GGCCAGGCCCAGGGAGTGGCCGAACTCGTGGGCGGCCA)
с получением промежуточной плазмиды рВА-ММР8-А6-В7;
- в вектор рВА, расщепленный рестриктазами BsmBI и BbsI, клонировали химически синтезированную пару олигонуклеотидов
MMP-137 (GGCCCACTCCTCTGACCCTGGCGCCCTGATGTACCCCAACTACGC) и
MMP-138 (CTGAAGGCGTAGTTGGGGTACATCAGGGCGCCAGGGTCAGAGGAGTG),
MMP-139 (CTTCAGGGAGACCAGCAACTACTCCCTGCCTCAGGACGACATCGA) и
MMP-140 (ATGCCGTCGATGTCGTCCTGAGGCAGGGAGTAGTTGCTGGTCTCC),
MMP-141 (CGGCATCCAGGCCATCTACGGCCTGTCCAGCAACCCCATCCAGCCCA) и
MMP-142 (CCGGTGGGCTGGATGGGGTTGCTGGACAGGCCGTAGATGGCCTGG) с получением промежуточной плазмиды рВА-ММР8-В7-А8;
- в вектор рВА, расщепленный рестриктазами HindIII и BbsI, клонировали химически синтезированные пары олигонуклеотидов
ММР-143 (CCGGCCCCAGCACCCCCAAGCCCTGCGACCCCAGCCTG) и
MMP-144 (GAAGGTCAGGCTGGGGTCGCAGGGCTTGGGGGTGCTGGGG),
ММР-145 (ACCTTCGACGCCATCACCACCCTGCGGGGCGAGATCCTG) и
MMP-146 (GAAGAACAGGATCTCGCCCCGCAGGGTGGTGATGGCGTC),
MMP-147m (TTCTTCAAGGACAGGTACTTCTGGAGAAGGCACCCCCAGCTGCAAGAGACGA) и MMP-148m (AGCTTCGTCTCTTGCAGCTGGGGGTGCCTTCTCCAGAAGTACCTGTCCTT) с получением промежуточной плазмиды pDA-MMP8-A8-D9;
- в вектор рВА, расщепленный рестриктазами BsmBI и BamHI, клонировали химически синтезированные пары олигонуклеотидов
MMP-149m (GATCCGAAGACATTGCAGAGAGTGGAGATGAACTTCATCTCTCTGTTCTGGC) и
ММР-150 m (GGGAGGGCCAGAACAGAGAGATGAAGTTCATCTCCACTCTCTGCAATGTCTTCG),
ММР-151 (CCTCCCTGCCCACCGGCATCCAGGCCGCCTACGAGGACTTC) и
ММР-152 (TCTGTCGAAGTCCTCGTAGGCGGCCTGGATGCCGGTGGGCA),
MMP-153 (GACAGAGACCTGATCTTCCTGTTCAAGGGCAACCAGTACTG) и
ММР-154 (GGCCCAGTACTGGTTGCCCTTGAACAGGAAGATCAGGTC)
с получением промежуточной плазмиды pBD-MMP8-D9-B10;
- в вектор рВА, расщепленный рестриктазами BsmBI и BamHI, клонировали химически синтезированные пары олигонуклеотидов
ММР-155 (GGCCCTGAGCGGCTACGACATCCTGCAGGGCTACC) и
ММР-156 (CTTGGGGTAGCCCTGCAGGATGTCGTAGCCGCTCAG),
ММР-157m (CCAAGGACATCTCCAACTACGGCTTCCCCAGCAGCGTGCAATGTCTTCG) и
ММР-158m (GATCCGAAGACATTGCACGCTGCTGGGGAAGCCGTAGTTGGAGATGTC)
с получением промежуточной плазмиды pBD-MMP8-B10-Dl 1;
- в вектор рВА, расщепленный рестриктазами HindIII и BbsI, клонировали химически синтезированные пары олигонуклеотидов
ММР-159 m (AGCTTCGTCTCTTGCAGGCCATCGACGCCGCCGTGTTCTACAGAAGCAAGACCTA) и ММР-160 m
(AAGAAGTAGGTCTTGCTTCTGTAGAACACGGCGGCGTCGATGGCCTGCAAGAGAC GA),
ММР-161 (CTTCTTCGTGAACGACCAGTTCTGGAGATACGACAACCAGAGAC) и
ММР-162 (TGAACTGTCTCTGGTTGTCGTATCTCCAGAACTGGTCGTTCACG),
ММР-163 (AGTTCATGGAGCCCGGCTACCCCAAGAGCATCTCCGGCGCCTTCC) и
ММР-164 (CCGGGGAAGGCGCCGGAGATGCTCTTGGGGTAGCCGGGCTCCA)
с получением промежуточной плазмиды pDA-MMPS-D11-A12;
- в вектор рВА, расщепленный рестриктазами BsmBI и BbsI, клонировали химически синтезированные пары олигонуклеотидов
ММР-165 (CCGGCATCGAGAGCAAGGTGGACGCCGTGTTCCAGC) и
ММР-166 (GCTCCTGCTGGAACACGGCGTCCACCTTGCTCTCGATG),
ММР-167 (AGGAGCACTTCTTCCACGTGTTCAGCGGCCCCAGATAC) и
ММР-168 (GGCGTAGTATCTGGGGCCGCTGAACACGTGGAAGAAGT),
MMP-169 (TACGCCTTCGACCTGATCGCCCAGAGAGTGACCAGAGT) и
ММР-170 (GGCCACTCTGGTCACTCTCTGGGCGATCAGGTCGAA)
с получением промежуточной плазмиды рВА-ММР8-А12-В13;
- в вектор рВА, расщепленный рестриктазами BsmBI и EcoRV, клонировали химически синтезированную пару олигонуклеотидов
ММР-171 (GGCCAGAGGCAACAAGTGGCTGAACTGCAGATACGGCTGAT) и
ММР-172 (ATCAGCCGTATCTGCAGTTCAGCCACTTGTTGCCTCT) с получением промежуточной плазмиды рВА-ММР8-В13-Е14.
Встраивание соответствующих последовательностей ДНК подтверждали секвенированием.
На третьей стадии;
- Bbsl - BsmBI фрагмент плазмиды pBD-MMP8-D2-B3 и BsmBI - XbaI фрагмент плазмиды рВА-ММР8-В3-А4 клонировали в плазмиду pBD-MMP8-Nl-D2, расщепленную рестриктазами BbsI и XbaI, с получением новой промежуточной плазмиды рВА-ММР8-Н1-А4;
- BsmBI - Bbsl фрагмент плазмиды рВА-ММР8-В5-А6 и BamHI - BsmBI фрагмент плазмиды рВА-ММР8-А4-В5 клонировали в плазмиду рВА-ММР8-А6-В7, расщепленную рестриктазами BbsI и BamHI, с получением новой промежуточной плазмиды рВА-ММР8-А4-В7;
- ВаmHI - BsmBI фрагмент плазмиды pDA-MMP8-A8-D9 клонировали в плазмиду pBD-MMP8-D9-B10, расщепленную рестриктазами Bbsl и ВаnHI, с получением новой промежуточной плазмиды
рВА-ММР8-А8-В10;
- XhoI - BbsI фрагмент плазмиды pBD-MMP8-B10-D11 клонировали в плазмиду pDA-MMP8-D11-A12, расщепленную рестриктазами XhoI и BsmBI, с получением новой промежуточной плазмиды рВА-ММР8-В10-А12;
- ВаmHI - BsmBI фрагмент плазмиды рВА-ММР8-А12-В13 и BsmBI - EcoRV фрагмент плазмиды рВА-ММ81-В13-Е14 клонировали в плазмиду рВА, расщепленную рестриктазами BglII и EcoRV, с получением новой промежуточной плазмиды рВА-ММР8-А12-Е14.
Встраивание соответствующих последовательностей ДНК подтверждали рестриктным анализом полученных плазмид.
На четвертой стадии Bbsl - ВаmHI фрагмент плазмиды рВА-ММР8-А12-Е14 клонировали в плазмиду рВА-ММР8-В10-А12, расщепленную рестриктазами BbsI и ВаmHI, с получением новой промежуточной плазмиды рВА-ММР8-В10-Е14. Встраивание соответствующих последовательностей ДНК подтверждали рестриктным анализом полученной плазмиды.
На пятой стадии:
- BbsI - BglII фрагмент плазмиды рВА-ММР8-А4-В7 клонировали в плазмиду рВА-ММР8-Н1-А4, расщепленную рестриктазами BbsI и ВаmHI, с получением новой промежуточной плазмиды рВА-ММР8-Н1-В7;
- BbsI - BsmBI фрагмент плазмиды рВА-ММР8-А8-В10 и BsmBI - ВаmHI фрагмент плазмиды рВА-ММР8-В10-Е14 клонировали в плазмиду рВА-ММР8-В7-А8, расщепленную рестриктазами BbsI и ВаmHI, с получением новой промежуточной плазмиды рВА-ММР8-В7-Е14;
Встраивание соответствующих последовательностей ДНК подтверждали рестриктным анализом полученных плазмид.
На шестой стадии HindIII - BsmBI фрагмент плазмиды рВА-ММР8-Н1-В7 и BsmBI - XbaI фрагмент плазмиды рВА-ММР8-В7-Е14 клонировали в экспрессионный вектор pC4W, расщепленный рестриктазами HindIII и XbaI, с получением конечной плазмиды pC4W-MMP8opt. Встраивание соответствующих последовательностей ДНК подтверждали рестриктным анализом и секвенированием полученной плазмиды.
Функциональная карта плазмиды pC4W-MMP8opt, несущей ген MMP8opt и предназначенной для экспрессии гена матриксной металлопротеиназы 8 в клетках млекопитающих, представлена на фиг.3.
Эффективность заявляемого изобретения иллюстрируется следующим примером.
Пример. Клетки НЕК293, высеянные в лунки 24-луночной плашки (50000 клеток на лунку) в среде DMEM, содержащей 2% эмбриональной телячьей сыворотки, трансфицировали плазмидой pC4W-MMP8opt, несущей оптимизированный ген матриксной металлопротеиназы 8 человека MMP8opt. Трансфекцию проводили с использованием 1 мкг ДИК и 1 мкл реагента Липофектамин 2000 (Invitrogen) в соответствии с протоколом производителя. Через 24 ч после трансфекции культуральную среду заменяли на свежую. Анализировали накопление ММР8 в культуральной среде за следующие 48 часов. Концентрацию ММР8 в культуральной среде измеряли при помощи набора "Quantikine Human MMP-8 (total) Immunoassay" компании R&D Systems (США) в соответствии с протоколом производителя. Согласно этим измерениям концентрация ММР 8 в культуральной среде составляла 8.5 мкг/мл, что в 6 раз быше чем при использовании аналогичной ДНК, содержащей немодифицированный ген.
| название | год | авторы | номер документа |
|---|---|---|---|
| ГЕН ММР1opt МЕТАЛЛОПРОТЕИНАЗЫ 1 | 2008 |
|
RU2378377C1 |
| ГЕН HGFopt ФАКТОРА РОСТА ГЕПАТОЦИТОВ | 2008 |
|
RU2385936C1 |
| ГЕН AGРopt АНГИОПОЭТИНА-1 | 2008 |
|
RU2385938C1 |
| ГЕН VEGFopt ФАКТОРА РОСТА ЭНДОТЕЛИЯ СОСУДОВ ЧЕЛОВЕКА | 2008 |
|
RU2385937C1 |
| ЭКСПРЕССИОННЫЙ ВЕКТОР ДЛЯ СИНТЕЗА БЕЛКОВ В КЛЕТКАХ МЛЕКОПИТАЮЩИХ | 2007 |
|
RU2364627C2 |
| СПОСОБ СТИМУЛЯЦИИ АНГИОГЕНЕЗА В ИШЕМИНИЗИРОВАННЫХ ТКАНЯХ И КОМБИНИРОВАННОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ОСУЩЕСТВЛЕНИЯ СПОСОБА | 2015 |
|
RU2628706C2 |
| Лекарственное средство для лечения фиброза печени, способ его получения и способ лечения фиброза печени | 2015 |
|
RU2615445C2 |
| СПОСОБ НЕЙТРАЛИЗАЦИИ ВИРУСА ГЕПАТИТА С, ПОЛНОСТЬЮ ЧЕЛОВЕЧЕСКОЕ МОНОКЛОНАЛЬНОЕ АНТИТЕЛО ПРОТИВ ВИРУСА ГЕПАТИТА С (ВАРИАНТЫ), КОМПОЗИЦИЯ ПОЛНОСТЬЮ ЧЕЛОВЕЧЕСКИХ МОНОКЛОНАЛЬНЫХ АНТИТЕЛ ПРОТИВ ВИРУСА ГЕПАТИТА С И ГИБРИДНАЯ МЫШЬ/ЧЕЛОВЕК КЛЕТОЧНАЯ ЛИНИЯ - ПРОДУЦЕНТ ПОЛНОСТЬЮ ЧЕЛОВЕЧЕСКИХ МОНОКЛОНАЛЬНЫХ АНТИТЕЛ ПРОТИВ ВИРУСА ГЕПАТИТА С (ВАРИАНТЫ) | 2013 |
|
RU2539770C1 |
| СИНТЕТИЧЕСКИЙ ГЕН, КОДИРУЮЩИЙ ЗЕЛЕНЫЙ ФЛУОРЕСЦЕНТНЫЙ БЕЛОК, СПОСОБ ПОЛУЧЕНИЯ ГЕНА, ЭКСПРЕССИРУЮЩИЙ ВЕКТОР, СПОСОБ ПОЛУЧЕНИЯ КУЛЬТУРЫ КЛЕТОК | 1997 |
|
RU2233329C2 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕННО-ИНЖЕНЕРНОГО ГЛЮКАГОНА ЧЕЛОВЕКА, РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК pER-Gl, КОДИРУЮЩАЯ ГИБРИДНЫЙ БЕЛОК, СПОСОБНЫЙ К АВТОКАТАЛИТИЧЕСКОМУ РАСЩЕПЛЕНИЮ С ОБРАЗОВАНИЕМ ГЛЮКАГОНА ЧЕЛОВЕКА, И ШТАММ Escherichia coli ER-2566/pER-Gl - ПРОДУЦЕНТ УКАЗАННОГО БЕЛКА | 2005 |
|
RU2302465C2 |




Изобретение относится к биотехнологии и представляет собой ген металлопротеиназы 8 с последовательностью нуклеотидов, приведенной на чертеже. Изобретение позволяет при включении данного гена в состав вектора экспрессии обеспечивать высокий уровень экспрессии металлопротеиназы 8 в клетках. 3 ил.
Оптимизированный для экспрессии в клетках млекопитающего ген металлопротеиназы 8, обладающий последовательностью нуклеотидов, приведенной на фиг.1.
| SILLER-LOPEZ F et.al | |||
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
| GARCIA-BANUELOS et.al | |||
| Cirrhotic rat liver with extensive fibrosis can be safely transduced with clinical-garde adenoviral vectors | |||
| Evidence of cirrhosis reversion, gene Theraphy, 2002 Jan, 9(2), 127-34 | |||
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК pBANP 464, КОДИРУЮЩАЯ МЕТАЛЛОПРОТЕИНАЗУ BACILLUS AMYLOLIQUEFACIENS A-50 И ШТАММ БАКТЕРИЙ BACILLUS AMYLOLIQUEFACIENS - ПРОДУЦЕНТ МЕТАЛЛОПРОТЕИНАЗЫ. | 1989 |
|
RU1679800C |
Авторы
Даты
2010-01-10—Публикация
2008-06-25—Подача