Изобретение относится к области биотехнологии, а именно к генно-инженерным конструкциям для экспрессии трансгенов в клетках млекопитающих с целью их применения в клеточной инженерии и в генной терапии, а именно к модификации последовательности гена для трансфекции клеток печени in vivo с целью экспрессии в них металлопротеиназы 1 (ММР 1).
Металлопротеиназы представляют собой ферменты, расщепляющие белки, которые находят широкое применение в пищевой и легкой промышленности, в сельском хозяйстве, а также в медицине. В частности, матриксные металлопротеиназы обладают способностью расщеплять коллаген - основной компонент внеклеточного матрикса, и расщепление коллагена под действием этих ферментов приводит к уменьшению степени фиброза и к улучшению кровоснабжения клеток печени (Iimuro Y, et al., Gastroenterology. 2003 Feb; 124(2):445-458.; Yang С, et al., Zhonghua Gan Zang Bing Za Zhi. 1999 Dec; 7(4):230-232).
Для синтеза ММР 1 использовали, в частности, рекомбинантную плазмидную ДНК pBANP 463, которая содержит природную последовательность гена ММР 1 и кодирует синтез ММР 1 микроорганизма B.amyloliquefaciens A-50 (RU 1679800).
Технической задачей, решаемой авторами настоящего изобретения, являлась модификация последовательности гена металлопротеиназы 1 таким образом, чтобы при ее включении в состав эукариотического вектора обеспечивался более высокий уровень экспрессии названного белка в клетках, трансфицированных названным вектором.
Технический результат достигался получением гена MMPlopt, структура которого представлена на фиг.1 модификацией природной последовательности гена ММР1 таким образом, чтобы триплет нуклеотидов, кодирующий каждую из аминокислот белковой последовательности ММР1, встречался в генах человека наиболее часто.
На фиг.1 показана последовательность нуклеотидов гена MMPl opt, а также последовательность аминокислот кодируемого белкового продукта - матриксной металлопротеиназы 1 человека.
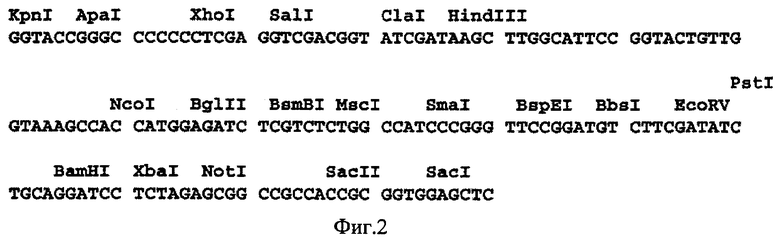
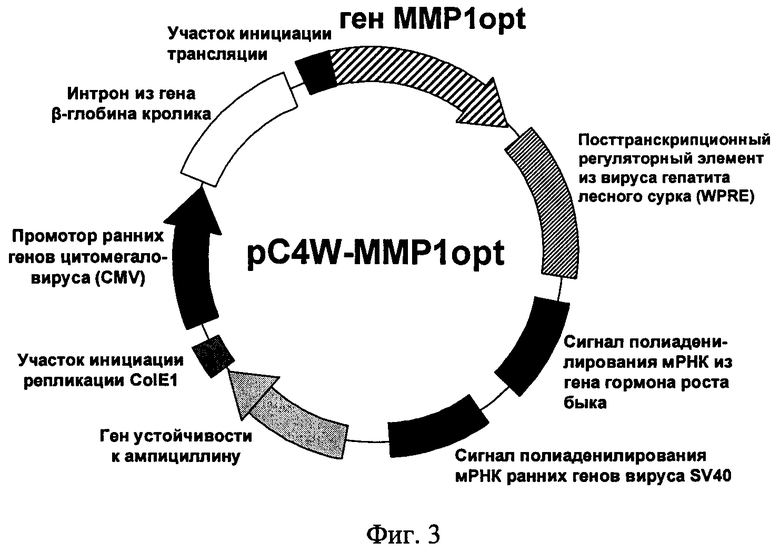
На фиг.2 показан предназначенный для клонирования участок ДНК вектора рВА, а на фиг.3 - функциональная карта плазмиды pC4W-MMPl opt.
Синтез гена и плазмиды осуществляли с помощью стандартной технологии и оборудования, применяемых для решения подобных задач в генной инженерии.
Дизайн оптимизированной последовательности нуклеотидов, кодирующей матриксную металлопротеиназу ММР1, производили, основываясь на вырожденности генетического кода. Для каждой аминокислоты белковой последовательности ММР1 выбирали кодирующий ее триплет нуклеотидов, наиболее часто встречающийся в генах человека. При этом использовали частоты встречаемости кодонов, приведенные на вэб-сайте http://del.mediaglyphs.org/mg/bf/nucs_aa.html. Полученная таким образом последовательность нуклеотидов представлена на фиг.1, структура плазмиды pC4W-MMPl opt с использованием данного гена - на фиг.3.
Плазмиду pC4W-MMPlopt, несущую оптимизированный ген MMPl opt, получали методом генно-инженерного конструирования.
На первой стадии изготавливали вектор для клонирования рВА. Для этого химически синтезированные пары олигонуклеотидов
VEC-89 (AAGCTTGGCATTCCGGTACTGTTGGTAAAGCCAC) и
VEC-90 (CCATGGTGGCTTTACCAACAGTACCGGAATGCCA),
VEC-91 (CATGGAGATCTCGTCTCTGGCCATCCCGGG) и
VEC-92 (CGGAACCCGGGATGGCCAGAGACGAGATCTC),
VEC-93 (TTCCGGATGTCTTCGATATCTGCAGGATCCT) и
VEC-94 (CTAGAGGATCCTGCAGATATCGAAGACATC),
отжигали, смешивали и клонировали в расщепленный рестриктазами HindIII и XbaI вектор pBluescripfII-SK+. В результате вектор рВА получает предназначенный для клонирования участок ДНК, представленный на фиг.2.
На второй стадии:
- в вектор рВА, расщепленный рестриктазами NcoI и ВаmHI, клонировали химически синтезированные пары олигонуклеотидов
ММР-1 (CATGCACAGCTTCCCTCCACTGCTGCTGCTGCT) и
MMP-2 (CAGAACAGCAGCAGCAGCAGTGGAGGGAAGCTGTG),
ММР-3 (GTTCTGGGGCGTGGTGTCCCACAGCTTCCCAGCC) и
MMP-4 (CAGGGTGGCTGGGAAGCTGTGGGACACCACGCCC),
ММР-5 (ACCCTGGAGACCCAGGAGCAGGACGTATGTCTTCG) и
MMP-6 (GATCCGAAGACATACGTCCTGCTCCTGGGTCTC)
с получением промежуточной плазмиды pBC-MMP1-N1-C2;
- в вектор рВА, расщепленный рестриктазами BsmBI и ВamHI, клонировали химически синтезированные пары олигонуклеотидов
ММР-7 (GATCCGAAGACATACGTGGACCTGGTGCAGA) и
MMP-8 (GGTACTTCTGCACCAGGTCCACGTATGTCTTCG),
ММР-9 (AGTACCTGGAGAAGTACTACAACCTGAAGAAC) и
ММР-10 (GCCGTCGTTCTTCAGGTTGTAGTACTTCTCCA),
ММР-11 (GACGGCAGGCAGGTGGAGAAGCGGAGAAACAGC) и
MMP-12 (GGCCGCTGTTTCTCCGCTTCTCCACCTGCCT)
с получением промежуточной плазмиды рВС-ММР1-С2-В3;
- в вектор рВА, расщепленный рестриктазами BsmBI и BbsI, клонировали химически синтезированные пары олигонуклеотидов
ММР-13 (GGCCCCGTGGTGGAGAAGCTGAAGCAG) и
ММР-14 (TGCATCTGCTTCAGCTTCTCCACCACGG),
ММР-15 (ATGCAGGAGTTCTTCGGCCTGAAGGTGA) и
MMP-16 (CCGGTCACCTTCAGGCCGAAGAACTCC)
с получением промежуточной плазмиды рВА-ММР1-В3-А4;
- в вектор рВА, расщепленный рестриктазами HindIII и BbsI, клонировали химически синтезированные пары олигонуклеотидов
ММР-17 (CCGGGAAGCCCGACGCCGAGACCCTGAAGGTG) и
ММР-18 (CTTCATCACCTTCAGGGTCTCGGCGTCGGGCTTC),
ММР-19 (ATGAAGCAGCCCAGATGCGGCGTGCCCGACGTGG) и
MMP-20 (ACTGGGCCACGTCGGGCACGCCGCATCTGGGCTG),
ММР-21 (CCCAGTTCGTGCTGACCGAGGGCAACAGAGACGA) и
MMP-22 (AGCTTCGTCTCTGTTGCCCTCGGTCAGCACGA)
с получением промежуточной плазмиды pGA-MMP1-A4-G5;
- в вектор рВА, расщепленный рестриктазами BsmBI и ВаmHI, клонировали химически синтезированные пары олигонуклеотидов
ММР-23 (GATCCGAAGACATCAACCCCCGCTGGGAGCAGAC) и
MMP-24 (AGGTGGGTCTGCTCCCAGCGGGGGTTGATGTCTTCG),
ММР-25 (CCACCTGACCTACAGGATCGAGAACTACACCCCCGA) и
MMP-26 (GGCAGGTCGGGGGTGTAGTTCTCGATCCTGTAGGTC),
ММР-27 (CCTGCCCAGAGCCGACGTGGACCACGCCATCGAGAA) и
MMP-28 (GGCCTTCTCGATGGCGTGGTCCACGTCGGCTCTG) с получением промежуточной плазмиды pBG-MMP1-G5-B6;
- в вектор рВА, расщепленный рестриктазами BsmBI и BbsI, клонировали химически синтезированные пары олигонуклеотидов
ММР-29 (GGCCTTCCAGCTGTGGAGCAACGTGACCCCT) и
MMP-30 (GGTCAGAGGGGTCACGTTGCTCCACAGCTGGAA),
ММР-31 (CTGACCTTCACCAAGGTGTCTGAGGGCCAGGC) и
MMP-32 (ATGTCGGCCTGGCCCTCAGACACCTTGGTGAA),
ММР-33 (CGACATCATGATCTCCTTCGTGAGGGGCGACCA) и
MMP-34 (CCGGTGGTCGCCCCTCACGAAGGAGATCATG)
с получением промежуточной плазмиды рВА-ММР1-В6-А7;
- в вектор рВА, расщепленный рестриктазами BsmBI и BbsI, клонировали химически синтезированную пару олигонуклеотидов
ММР-35 (CCGGGACAACTCTCCTTTCGAC) и
ММР-36 (GGCCGTCGAAAGGAGAGTTGTC)
с получением промежуточной плазмиды рВА-ММР1-А7-В8;
- в вектор рВА, расщепленный рестриктазами BsmBI и BbsI, клонировали химически синтезированные пары олигонуклеотидов
ММР-37 (GGCCCCGGCGGCAACCTGGCCCACGCCTTCCAGCCAG) и
MMP-38 (CTGGGCCTGGCTGGAAGGCGTGGGCCAGGTTGCCGCCGG),
ММР-39 (GCCCAGGCATCGGCGGCGACGCCCACTTCGACGAGGA) и
ММР-40 (CTCTCGTCCTCGTCGAAGTGGGCGTCGCCGCCGATGC),
ММР-41 (CGAGAGGTGGACCAACAACTTCAGAGAGTACAACCTGCA) и
MMP-42 (CCGGTGCAGGTTGTACTCTCTGAAGTTGTTGGTCCAC)
с получением промежуточной плазмиды рВА-ММР1-В8-А9;
- в вектор рВА, расщепленный рестриктазами BsmBI и BbsI, клонировали химически синтезированные пары олигонуклеотидов
ММР-43 (CCGGGTGGCCGCCCACGAGCTGGGCCACTCCCTGGG) и
MMP-44 (GACAGGCCCAGGGAGTGGCCCAGCTCGTGGGCGGCCAC),
ММР-45 (CCTGTCCCACTCCACCGACATCGGCGCCCTGAT) и
MMP-46 (GGGTACATCAGGGCGCCGATGTCGGTGGAGTGG),
ММР-47 (GTACCCCAGCTACACCTTCAGCGGCGACGTGCAGCT) и
MMP-48 (GGCCAGCTGCACGTCGCCGCTGAAGGTGTAGCTG) с получением промежуточной плазмиды рВА-ММР1-А9-В10;
- в вектор рВА, расщепленный рестриктазами BsmBI и BbsI, клонировали химически синтезированные пары олигонуклеотидов
ММР-49 (GGCCCAGGACGACATCGACGGCATCCAGGCCATCTACGGCC) и
MMP-50 (GGGACCGGCCGTAGATGGCCTGGATGCCGTCGATGTCGTCCTG),
ММР-51 (GGTCCCAGAACCCCGTGCAGCCCATCGGCCCACAGACCCCAA) и
MMP-52 (AGGCCTTTGGGGTCTGTGGGCCGATGGGCTGCACGGGGTTCT),
ММР-53 (AGGCCTGCGACAGCAAGCTGACCTTCGACGCCATCACCACCAT) и
MMP-54 (CCGGATGGTGGTGATGGCGTCGAAGGTCAGCTTGCTGTCGC)
с получением промежуточной плазмиды pBA-MMPl-B10-A11;
- в вектор рВА, расщепленный рестриктазами BsmBI и BbsI, клонировали химически синтезированные пары олигонуклеотидов
ММР-55 (CCGGGGCGAGGTGATGTTCTTCAAGGACAGATTCTACA) и
MMP-56 (TGCGCATGTAGAATCTGTCCTTGAAGAACATCACCTCGCC),
ММР-57 (TGCGCACCAACCCCTTCTACCCCGAGGTGGAGCTGAACT) и
MMP-58 (AGATGAAGTTCAGCTCCACCTCGGGGTAGAAGGGGTTGG),
ММР-59 (TCATCTCCGTGTTCTGGCCCCAGCTGCCAAACGGCCTGGA) и
MMP-60 (GGCCTCCAGGCCGTTTGGCAGCTGGGGCCAGAACACGG)
с получением промежуточной плазмиды pBA-MMP1-A11-B12;
- в вектор рВА, расщепленный рестриктазами BsmBI и BamHI, клонировали химически синтезированные пары олигонуклеотидов
ММР-61 (GGCCGCCTACGAGTTCGCCGACAGGGACGAG) и
MMP-62 (CCGCACCTCGTCCCTGTCGGCGAACTCGTAGGC),
ММР-63 (GTGCGGTTCTTCAAGGGCAACAAGTACTGGGC) и
MMP-64 (TGCACGGCCCAGTACTTGTTGCCCTTGAAGAA),
ММР-65 (CGTGCAGGGCCAGAACGTGCTGCAATGTCTTCG) и
MMP-66 (GATCCGAAGACATTGCAGCACGTTCTGGCCC) с получением промежуточной плазмиды pBD-MMP1-B12-D13;
- в вектор рВА, расщепленный рестриктазами HindIII и BbsI, клонировали химически синтезированные пары олигонуклеотидов
ММР-67 (AGCTTCGTCTCTTGCACGGCTACCCCAAGGAC) и
MMP-68 (GTAGATGTCCTTGGGGTAGCCGTGCAAGAGACGA),
ММР-69 (ATCTACAGCTCCTTCGGCTTCCCCAGAACCGTG) и
ММР-70 (GTGCTTCACGGTTCTGGGGAAGCCGAAGGAGCT),
ММР-71 (AAGCACATCGACGCCGCCCTGTCTGAGGAGAACA) и
MMP-72 (CCGGTGTTCTCCTCAGACAGGGCGGCGTCGAT)
с получением промежуточной плазмиды pDA-MMP1-D13-A14;
- в вектор рВА, расщепленный рестриктазами BsmBI и BbsI, клонировали химически синтезированные пары олигонуклеотидов
ММР-73 (CCGGCAAGACCTACTTCTTCGTGGCCAACAAGTACT) и
MMP-74 (ACCTCCAGTACTTGTTGGCCACGAAGAAGTAGGTCTTG),
ММР-75 (GGAGGTACGACGAGTACAAGCGGTCCATGGACCCAG) и
MMP-76 (GGTAGCCTGGGTCCATGGACCGCTTGTACTCGTCGT),
ММР-77 (GCTACCCCAAGATGATCGCCCACGACTTCCCTGGCATC) и
MMP-78 (GGCCGATGCCAGGGAAGTCGTGGGCGATCATCTTGG)
с получением промежуточной плазмиды рВА-ММР1-А14-В15;
- в вектор рВА, расщепленный рестриктазами BsmBI и EcoRV, клонировали химически синтезированные пары олигонуклеотидов
ММР-79 (GGCCACAAGGTGGACGCCGTGTTCATGAAGGACGGCTTCTTCTACTT) и
MMP-80 (TGGAAGAAGTAGAAGAAGCCGTCCTTCATGAACACGGCGTCCACCTTGT)
ММР-81 CTTCCACGGCACCAGACAGTACAAGTTCGACCCCAAGACCAAGAGAATC) и
ММР-82 (GGTCAGGATTCTCTTGGTCTTGGGGTCGAACTTGTACTGTCTGGTGCCG),
MMP-83 (CTGACCCTGCAGAAGGCCAACAGCTGGTTCAACTGCAGGAAGAACTGAT) и
ММР-84 (ATCAGTTCTTCCTGCAGTTGAACCAGCTGTTGGCCTTCTGCAG)
с получением промежуточной плазмиды рВА-ММР1-В15-Е16.
Встраивание соответствующих последовательностей ДНК подтверждали секвенированием.
На третьей стадии:
- Bbsl - BsmBI фрагмент плазмиды рВС-ММР1-С2-В3 и BsmBI - XbaI фрагмент плазмиды рВА-ММР1-В3-А4 клонировали в плазмиду pBC-MMP1-N1-C2, расщепленную рестриктазами BbsI и XbaI, с получением новой промежуточной плазмиды рВА-ММР1-Н1-А4;
- ВamHI - BsmBI фрагмент плазмиды pGA-MMP1-A4-G5 клонировали в плазмиду pBGMMP1-G5-B6, расщепленную рестриктазами Bbsl и ВаmHI, с получением новой промежуточной плазмиды рВА-ММР1-А4-В6;
- Bbsl - BsmBI фрагмент плазмиды рВА-ММР1-А7-В8 и BsmBI-ВаmHI фрагмент плазмиды рВА-ММР1-В8-А9 клонировали в плазмиду рВА-ММР1-В6-А7, расщепленную рестриктазами BbsI и ВаmHI, с получением новой промежуточной плазмиды рВА-ММР1-В6-А9;
- BsmBI - BbsI фрагмент плазмиды рВА-ММР1-В10-А11 и ВаmHI - BsmBI фрагмент плазмиды рВА-ММР1-А9-В10 клонировали в плазмиду pBA-MMP1-A11-B12, расщепленную рестриктазами BbsI и ВаmHI, с получением новой промежуточной плазмиды рВА-ММР1-А9-В12;
- Xhol - Bbsl фрагмент плазмиды pBD-MMP1-В12-D13 клонировали в плазмиду pDA-MMP1-D13-A14, расщепленную рестриктазами XhoI и BsmBI, с получением новой промежуточной плазмиды рВА-ММР1-В12-А14;
- ВаmHI - BsmBI фрагмент плазмиды рВА-ММР1-А14-В15 и BsmBI - EcoRV фрагмент плазмиды рВА-ММР1-В15-Е16 клонировали в плазмиду рВА, расщепленную рестриктазами BglII и EcoRV, с получением новой промежуточной плазмиды рВА-ММР1-А14-Е16.
Встраивание соответствующих последовательностей ДНК подтверждали рестриктным анализом полученных плазмид.
На четвертой стадии BbsI - BsmBI фрагмент плазмиды pBA-MMPI-A14-B15 и HindIII - BbsI фрагмент плазмиды рВА-ММР1-В12-А14 клонировали в плазмиду рВА-ММР1-В15-Е16, расщепленную рестриктазами HindIII и BsmBI, с получением новой промежуточной плазмиды рВА-ММР1-В12-Е16. Встраивание соответствующих последовательностей ДНК подтверждали рестриктным анализом полученной плазмиды.
На пятой стадии:
- BbsI - BsmBI фрагмент плазмиды рВС-ММР1-А4-В6 и BsmBI - ВаmHI фрагмент плазмиды рВА-ММР1-В6-А9 клонировали в плазмиду рВС-ММР1-Н1-А4, расщепленную рестриктазами BbsI и ВаmHI, с получением новой промежуточной плазмиды рВА-ММР1-Н1-А9;
- ВаmHI - BsmBI фрагмент плазмиды рВА-ММР1-А9-В12 клонировали в плазмиду рВА-ММР1-В12-Е16, расщепленную рестриктазами BsmBI и BglII, с получением новой промежуточной плазмиды рВА-ММР1-А9-Е16.
Встраивание соответствующих последовательностей ДНК подтверждали рестриктным анализом полученных плазмид.
На шестой стадии HindIII - BbsI фрагмент плазмиды рВА-ММР1-Н1-А9 и BbsI - ВаmHI фрагмент плазмиды рВА-ММР1-А9-Е16 клонировали в экспрессионный вектор pC4W, расщепленный рестриктазами HindIII и BamHI, с получением конечной плазмиды pC4W-MMPl opt. Встраивание соответствующих последовательностей ДНК подтверждали рестриктным анализом и секвенированием полученной плазмиды.
Функциональная карта плазмиды pC4W-MMPl opt, несущей ген MMPl opt и предназначенной для экспрессии гена матриксной металлопротеиназы 1 в клетках млекопитающих, представлена на фиг.3.
Эффективность заявляемого изобретения иллюстрируется следующим примером. Пример. Клетки НЕК293, высеянные в лунки 24-луночной плашки (50000 клеток на лунку) в среде DMEM, содержащей 2% эмбриональной телячьей сыворотки, трансфицировали плазмидой pC4W-MMPlopt, несущей оптимизированный ген матриксной металлопротеиназы человека MMPl opt. Трансфекцию проводили с использованием 1 мкг ДНК и 1 мкл реагента Липофектамин 2000 (Invitrogen) в соответствии с протоколом производителя. Через 24 ч после трансфекции культуральную среду заменяли на свежую. В течение последующих 48 часов анализировали накопление ММР 1 в культуральной среде и его функциональную активность. Концентрацию ММР 1 в культуральной среде измеряли при помощи набора "Amersham Matrix Metalloproteinase-1 (MMP-1), Biotrak Activity Assay System" компании GE Healthcare (США). По данным проведенных измерений, концентрация ММР 1 в культуральной среде составляла 16 мкг/мл, что в 3 раза превышает данный показатель при использовании плазмиды с немодифицированной генной последовательностью.
| название | год | авторы | номер документа |
|---|---|---|---|
| ГЕН MMP8opt МЕТАЛЛОПРОТЕИНАЗЫ 8 | 2008 |
|
RU2378376C1 |
| ГЕН HGFopt ФАКТОРА РОСТА ГЕПАТОЦИТОВ | 2008 |
|
RU2385936C1 |
| ГЕН AGРopt АНГИОПОЭТИНА-1 | 2008 |
|
RU2385938C1 |
| ГЕН VEGFopt ФАКТОРА РОСТА ЭНДОТЕЛИЯ СОСУДОВ ЧЕЛОВЕКА | 2008 |
|
RU2385937C1 |
| ЭКСПРЕССИОННЫЙ ВЕКТОР ДЛЯ СИНТЕЗА БЕЛКОВ В КЛЕТКАХ МЛЕКОПИТАЮЩИХ | 2007 |
|
RU2364627C2 |
| СПОСОБ СТИМУЛЯЦИИ АНГИОГЕНЕЗА В ИШЕМИНИЗИРОВАННЫХ ТКАНЯХ И КОМБИНИРОВАННОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ОСУЩЕСТВЛЕНИЯ СПОСОБА | 2015 |
|
RU2628706C2 |
| Лекарственное средство для лечения фиброза печени, способ его получения и способ лечения фиброза печени | 2015 |
|
RU2615445C2 |
| СПОСОБ НЕЙТРАЛИЗАЦИИ ВИРУСА ГЕПАТИТА С, ПОЛНОСТЬЮ ЧЕЛОВЕЧЕСКОЕ МОНОКЛОНАЛЬНОЕ АНТИТЕЛО ПРОТИВ ВИРУСА ГЕПАТИТА С (ВАРИАНТЫ), КОМПОЗИЦИЯ ПОЛНОСТЬЮ ЧЕЛОВЕЧЕСКИХ МОНОКЛОНАЛЬНЫХ АНТИТЕЛ ПРОТИВ ВИРУСА ГЕПАТИТА С И ГИБРИДНАЯ МЫШЬ/ЧЕЛОВЕК КЛЕТОЧНАЯ ЛИНИЯ - ПРОДУЦЕНТ ПОЛНОСТЬЮ ЧЕЛОВЕЧЕСКИХ МОНОКЛОНАЛЬНЫХ АНТИТЕЛ ПРОТИВ ВИРУСА ГЕПАТИТА С (ВАРИАНТЫ) | 2013 |
|
RU2539770C1 |
| СИНТЕТИЧЕСКИЙ ГЕН, КОДИРУЮЩИЙ ЗЕЛЕНЫЙ ФЛУОРЕСЦЕНТНЫЙ БЕЛОК, СПОСОБ ПОЛУЧЕНИЯ ГЕНА, ЭКСПРЕССИРУЮЩИЙ ВЕКТОР, СПОСОБ ПОЛУЧЕНИЯ КУЛЬТУРЫ КЛЕТОК | 1997 |
|
RU2233329C2 |
| ИСКУССТВЕННЫЙ БЕЛОК-ИММУНОГЕН TCI, СОДЕРЖАЩИЙ МНОЖЕСТВЕННЫЕ CTL-ЭПИТОПЫ ОСНОВНЫХ АНТИГЕНОВ ВИЧ-1, ИСКУССТВЕННЫЙ ГЕН TCI, КОДИРУЮЩИЙ ПОЛИЭПИТОПНЫЙ БЕЛОК-ИММУНОГЕН TCI | 2002 |
|
RU2238946C2 |



Изобретение относится к области биотехнологии и представляет собой ген металлопротеиназы 1 с последовательностью нуклеотидов, приведенной на фиг.1. Изобретение позволяет при включении данного гена в состав вектора экспрессии обеспечивать высокий уровень экспрессии металлопротеиназы 1 в клетках. 3 ил.
Ген металлопротеиназы 1, обладающий последовательностью нуклеотидов, приведенной на фиг.1.
| IIMURO Y., NISHIO Т., MORIMOTO Т., NITTA Т., STEFANOVIC В., CHOI S.K., BRENNER D.A., YAMAOKA Y | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Gastroenterology | |||
| Способ и приспособление для нагревания хлебопекарных камер | 1923 |
|
SU2003A1 |
| TEMPLETON NS, BROWN PD, LEVY AT, MARGULIES IM, LIOTTA LA, STETLER-STEVENSON WG | |||
| Cloning and characterization of human | |||
Авторы
Даты
2010-01-10—Публикация
2008-06-25—Подача