Изобретение относится к области органической химии, а именно к способу получения индолинов с аминоалкильными заместителями у атома азота.
Изобретение может быть использовано в различных органических синтезах для получения болеутоляющих, противовоспалительных лекарств и средств лечения заболеваний центральной нервной системы (Международный патент WO 03/053945, 2003; H.Rami et al. Bioorganic and Medicinal Chemistry Letters, 2006, 16, 3287-3291; S. Shapiro et al., J.Am.Chem.Soc., 1959, 81, 3083-3088).
1-(Аминоалкил)индолины могут также представлять интерес как радиопротекторы в связи с тем, что близкие по структуре индолилалкиламины при сравнительно низкой токсичности часто проявляют высокую радиозащитную активность (П.Г.Жеребченко. «Противолучевые свойства индолилалкиламинов». М., Атомиздат, 1971 г., стр.6-31; Н.Н.Суворов, B.C.Шашков. «Химия и фармакология средств профилактики радиационных поражений». М., Атомиздат, 1975 г., стр.122-139).
Известен способ получения 1-(2-аминоэтил)индолина (выход ~65%) восстановлением 1-(2-аминоэтил)индола под действием бис(трифторацетокси)борана в среде тетрагидрофурана при 0-5°С (В.Maryanoff et al., J.Org.Chem., 1981, 46, 355-360).
Недостатком способа является образование побочного продукта - 3-трифторацетил-1-(2-аминоэтил)индола, который загрязняет целевое соединение, а также труднодоступность исходного соединения. Последний получается с низким выходом (от 4 до 20%) 2-аминоэтилированием индола под действием тетрафторбората азиридиния из-за конкурирующего образования триптамина (Е.Pfiel et al., Angew.Chem.Int.Ed., 1967, 6, 178).
Известен способ получения 1-(2-аминоэтил)индолина нагреванием индолина с β-бромэтилфталимидом при 100°С в течение 3,5 часов при соотношении реагентов 2:1 и последующим кипячением N-β-фталимидоэтилиндолина с гидразингидратом в спирте в течение 1 часа (Н.Н.Суворов, B.C.Мурашева в кн. «Химия гетероциклических соединений», сборник 1, 1967 г., стр.25-27/ из-во «Зинатне», Рига).
Недостатками способа являются многостадийность и необходимость использования двойного избытка индолина (для связывания образующегося НВr).
Известно получение 1-(2-аминоэтил)индолина кипячением смеси индолина, хлорацетонитрила и карбоната натрия в толуоле, содержащем 0,1% воды в течение 11 часов, с последующим восстановлением полученного (1-индолинил)ацетонитрила (выход 27%) литийалюминийгидридом в эфире, выход целевого соединения 51% (R.Mull, F.Park, Пат. США 3093632; 1963).
Недостатками способа являются многостадийность, длительность процесса и низкий выход 1-(2-аминоэтил)индолина: в расчете на индолин он составляет всего 14%.
Известен способ получения 1-(3-аминопропил)индолина цианэтилированием индолина под действием акрилонитрила в среде уксусной кислоты при 145°С в течение 12 часов с последующим восстановлением полученного N-(β-цианоэтил)индолина (выход 87%) до целевого соединения (выход 83%; в расчете на индолин его выход составляет 72%) (S.Shapiro et al., J. Am.Chem.Soc, 1959, 81, 3083-3088; В. Astill, V. Boekelheide, J.Org.Chem., 1958, 23, 316-318).
Недостатками способа являются многостадийность, длительность процесса и использование токсичного акрилонитрила.
Известен способ получения 1-(2-аминоэтил)индолина кипячением индолина с бромгидратом β-бромэтиламина в толуоле в течение 18 часов при соотношении реагентов 2:1 с последующим удалением толуола в вакууме, растворением остатка в воде, подщелачиванием водным карбонатом калия и экстрагированием метиленхлоридом. Целевой продукт выделяли из остатка (после удаления растворителя) с помощью колоночной хроматографии на силикагеле с выходом 26,7% (Международный патент WO 03/053945, 2003).
Этот способ выбран нами в качестве прототипа как наиболее близкий по технической сущности.
Недостатками способа являются низкий выход (26,7%), необходимость использования двойного избытка индолина (для связывания образующегося НВr), длительность процесса, а также необходимость отгонки толуола и проведения трудоемкой колоночной хроматографии для выделения продукта, что усложняет процесс.
Задачей настоящего изобретения является разработка технологичного и эффективного способа получения 1-(аминоалкил)индолинов с хорошими выходами и высокой степенью чистоты.
Поставленная задача решается путем взаимодействия индолина с бромгидратами аминоалкилбромидов в водной среде с использованием бикарбоната натрия в качестве акцептора бромистого водорода при молярном соотношении реагентов индолин:бромгидрат аминоалкилбромида:бикарбонат натрия, равном 1:1,2-1,4:1-1,4 при температуре 95-100°С, с последующим выделением конечного продукта путем подщелачивания водным NaOH, экстракции органическими растворителями и перегонки в вакууме.
Схема синтеза 1-(аминоалкил)индолинов(I-II)
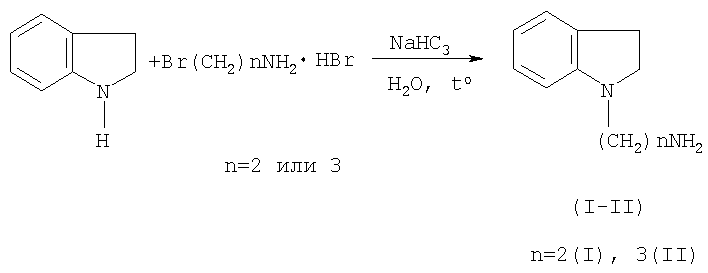
В качестве исходных соединений в синтезе целевых соединений (I-II) использованы индолин (99%-ный) фирмы «Acros», а также отечественные реактивы: бромгидрат β-бромэтиламина (ч., Союзглавреактив, завод «РИАП», ТУ КРЗ №299-06), 3-бромпропиламин гидробромид (ч., Реахим, ТУ 6-09-37-112-83) и натрий углекислый кислый (хч, Реахим, ГОСТ 4201-79).
Растворителем реакции является вода; бикарбонат натрия прибавляют к смеси индолина, бромгидрата и воды или в сухом виде (примеры 1 и 3), или в водном растворе (пример 2).
Указанное соотношение реагентов является оптимальным для завершения алкилирования (длительность нагревания устанавливают ТСХ-методом). После обработки реакции и перегонки в вакууме получают целевые продукты (I-II) с выходами 65-70%, которые по данным ПМР- и масс-спектров имеют чистоту не менее 97%.
При эквимолярном соотношении реагентов (1:1:1) не удается достичь полной конверсии индолина, примесь которого загрязняет целевые продукты (I-II), и их выходы снижаются. Использование большого избытка бромгидрата амина и NаНСО3 (более 1,4 моля на 1 моль индолина) нецелесообразно, так как это не приводит к увеличению выходов соединений (I-II). Алкилирование индолина бромгидратом 3-бромпропиламина идет труднее, чем с бромгидратом β-бромэтиламина, и для завершения реакции требуются повышенный избыток бромгидрата и бикарбоната натрия и более длительное нагревание (пример 3).
Изобретение иллюстрируется следующими примерами.
Пример 1.
В трехгорлую колбу объемом 1 л, снабженную мешалкой и обратным холодильником, помещают 49,41 г (0,415 моля) индолина, 102,14 г (0,498 моля) бромгидрата β-бромэтиламина и 100 мл воды. Реакционную смесь нагревают при перемешивании до 95°С (в бане), затем постепенно прибавляют 34,88 г (0,415 моля) бикарбоната натрия при этой температуре. Смесь перемешивают при 95°С еще ~15 мин, затем водяную баню заменяют на колбонагреватель и кипятят при перемешивании до окончания реакции (~1 час 45 мин; ТСХ-анализ в системе ацетон - CCl4=1:3). Температуру смеси доводят до комнатной, прибавляют 40%-ный NaOH (75 мл) и воду до растворения осадка (~250 мл). Органический слой собирают, водный экстрагируют эфиром, затем CH2Cl2 (2 раза). Объединенные органические слои промывают насыщенным раствором NaCl и сушат над MgSO4. После фракционирования в вакууме получают 47,08 г (70%) 1-(2-аминоэтил)индолина (I) в виде бледно-желтого масла с т.кип. 103-108°/2 мм и nD 20 1,5830 [лит.данные: т.кип. 154-160°/17 мм (R.Mull, F.Park, Пат. США 3093632; 1963)], чистого по ТСХ-анализу и ПМР- и масс-спектрам.
Найдено: С 74,04%; Н 8,81%; N 17,33%; М+ 162. С10Н14N2. Вычислено: С 74,07%; Н 8,64%; N 17,28%; М 162. Спектр ЯМР 1Н (CDCl3, δ, м.д.): 1,35 (с, 2Н, NH2); 3,01 (м, 4Н, 2-СН2+3-СН2); 3,18 (т, 2Н, CH 2NH2, J=7,2 Гц); 3,42 (т, 2Н, >NCH2, J=7,2 Гц); 6,59 (д, 1Н, Аr, J=7,8 Гц); 6,74 (т, 1Н, Аr, J=7,4 Гц); 7,14 (т, 2Н, Аr, J=7,8 Гц).
Пример 2.
Смесь 11,9 г (0,1 моля) индолина, 24,6 г (0,12 моля) бромгидрата β-бромэтиламина и 12 мл воды нагревают при перемешивании до 95°С (в бане), затем прибавляют в течение 30 мин горячий раствор 10,08 г (0,12 моля) NаНСО3 в 45 мл воды. Через 10 минут (при 95°С) реакционную смесь кипятят на колбонагревателе при перемешивании до окончания реакции (~2,5 часа). После обработки реакционной смеси (аналогично примеру 1) перегонкой выделено 11,34 г (70%) продукта (I).
Пример 3.
Смесь 9,52 г (0,08 моля) индолина, 24,51 г (0,112 моля) бромгидрата 3-бромпропиламина и 20 мл воды нагревают при перемешивании до 95°С (в бане), затем прибавляют в течение 30 мин 9,4 г (0,112 моля) NаНСО3. Через 15 минут (при 95°С) реакционную смесь кипятят на колбонагревателе при перемешивании до окончания реакции (5-6 часов; ТСХ-анализ в системе ацетон - ССl4=1:3). После обработки реакции (аналогично примеру 1) перегонкой выделено 9,15 г (65%) 1-(3-аминопропил)индолина (II) в виде светло-желтого масла с т.кип. 105-109°/1 мм и nD 21 1,5729 [лит.данные: т.кип. 92-100°/0,07 мм (S.Shapiro et al., J. Am.Chem.Soc, 1959, 81, 3083-3088)], чистого по ТСХ-анализу и ПМР- и масс-спектрам.
Найдено: С 74,75%; Н 9,04%; N 15,72%; М+ 176. C11H16N2. Вычислено: С 75,00%; Н 9,09%; N 15,91%; М 176. Спектр ЯМР 1Н (CDCl3, δ, м.д.): 1,24 (с, 2Н, NH2); 1,82 (м, 2Н, С-СН2-С); 2,89 (т, 2Н, CH 2NH2, J=6,95 Гц); 3,02 (т, 2Н, 3-СН2, J=8,24 Гц); 3,19 (т, 2Н, >NCH2, J=7,14 Гц); 3,40 (т, 2Н, 2-СН2, J=8,23 Гц); 6,56 (д, 1Н, Аr, J=8,06 Гц); 6,71 (т, 1Н, Аr, J=7,32 Гц); 7,13 (м, 2Н, Аr).
Таким образом, предлагаемый способ является одностадийным, в отличие от способов-аналогов. Благодаря введению в реакцию третьего компонента - бикарбоната натрия и замене растворителя (вода вместо толуола) предлагаемый способ имеет следующие существенные преимущества перед прототипом:
- повышение выходов (~ в 2,6 раза);
- сокращение времени реакции в 9 раз (с 18 до 2 часов при синтезе I);
- экономия индолина: на 1 моль бромгидрата требуется не 2, а 0,7-0,8 моля индолина;
- технологичность: не нужно удалять растворитель реакции и осуществлять трудоемкую колоночную хроматографию для выделения продуктов.
Высокая технологичность предлагаемого способа позволяет успешно применять его в промышленном масштабе. Кроме того, метод является экологически и пожаробезопасным, так как процесс проводят не в толуоле, а в воде.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНОГО ПОЛИЕНОВОГО СПИРТА (ВАРИАНТЫ), СУЛЬФОНОВОЕ СОЕДИНЕНИЕ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1998 |
|
RU2196133C2 |
| АГОНИСТЫ TRPV1, СОДЕРЖАЩИЕ ИХ ПРЕПАРАТЫ И ИХ ПРИМЕНЕНИЕ | 2005 |
|
RU2379282C2 |
| РОДСТВЕННОЕ ВИТАМИНУ A СОЕДИНЕНИЕ И СПОСОБЫ ЕГО ПОЛУЧЕНИЯ | 1998 |
|
RU2188193C2 |
| Способ получения пуриновых нуклеозидов ряда β-D-арабинофуранозы | 2015 |
|
RU2624023C2 |
| Соединения формул (I) и (A), фармацевтическая композиция, лекарственное средство, применение и способ получения соединения формулы (I) | 2018 |
|
RU2822758C2 |
| СПОСОБ ПОЛУЧЕНИЯ ВТОРИЧНЫХ НИТРАМИНОВ | 2008 |
|
RU2378251C1 |
| N, N', N'-ТРИЗАМЕЩЕННЫЕ ИЗОСЕЛЕНОМОЧЕВИНЫ | 2010 |
|
RU2434852C1 |
| СОЛИ ЯБЛОЧНОЙ КИСЛОТЫ И ПОЛИМОРФЫ (3S,5S)-7-[3-АМИНО-5-МЕТИЛПИПЕРИДИНИЛ]-1-ЦИКЛОПРОПИЛ-1,4-ДИГИДРО-8-МЕТОКСИ-4-ОКСО-3-ХИНОЛИНКАРБОНОВОЙ КИСЛОТЫ | 2007 |
|
RU2417222C2 |
| СОЛИ 9-ω-АРИЛОКСИАЛКИЛ-2,3-ДИГИДРОИМИДАЗО[1,2-А]БЕНЗИМИДАЗОЛА, ОБЛАДАЮЩИЕ МЕСТНОАНЕСТЕЗИРУЮЩИМ ДЕЙСТВИЕМ | 2003 |
|
RU2233279C1 |
| СПОСОБ ПОЛУЧЕНИЯ α,β,β-ТРИФТОРСТИРОЛА | 2023 |
|
RU2811553C1 |
Изобретение относится к усовершенствованному способу получения 1-(аминоалкил)индолинов, который заключается в том, что индолин взаимодействует с бромгидратом аминоалкилбромида в водной среде с использованием бикарбоната натрия в качестве акцептора бромистого водорода при молярном соотношении реагентов индолин:бромгидрат аминоалкилбромида:бикарбонат натрия, равном 1:1,2-1,4:1-1,4 при температуре 95-100°С, с последующим выделением целевого продукта подщелачиванием водным NaOH, экстракцией органическими растворителями и перегонкой в вакууме. Способ позволяет повысить выход и чистоту целевого продукта, сократить время его получения.
Способ получения 1-(аминоалкил)индолинов путем взаимодействия индолина с бромгидратами аминоалкилбромидов в среде растворителя при нагревании, отличающийся тем, что реакцию проводят в водной среде с использованием бикарбоната натрия в качестве акцептора бромистого водорода при молярном соотношении реагентов индолин:бромгидрат аминоалкилбромида:бикарбонат натрия, равном 1:1,2-1,4:1-1,4 при температуре 95-100°С, с последующим выделением конечного продукта путем подщелачивания водным NaOH, экстракции органическими растворителями и перегонки в вакууме.
| Способ и приспособление для нагревания хлебопекарных камер | 1923 |
|
SU2003A1 |
| Bioorganic & Medicinal Chemistry Letters, 16 (2006), 3287-3291 | |||
| ES 531414, 09.04.1984 | |||
| Ж.: ХГС, 1, 1967, с | |||
| Видоизменение пишущей машины для тюркско-арабского шрифта | 1923 |
|
SU25A1 |
Авторы
Даты
2010-04-27—Публикация
2008-09-18—Подача