Изобретение относится к области органической химии и может найти применение в аналитической химии и биологических исследованиях.
При изучении физиологически активных соединений необходимы их меченые аналоги.
Известно, что замена атомов соединений на их меченые аналоги не приводит к изменению каких-либо свойств исходного соединения (Evans Е.А. - Tritium and its compounds London Butterworths, 1974, p.48) [1].
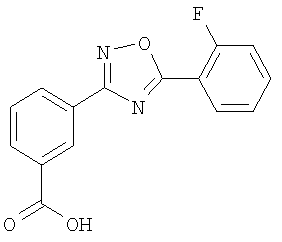
Известна 3-[5-(2-фторфенил)-1,2,4-оксадиазол-3-ил]бензойная кислота формулы I:
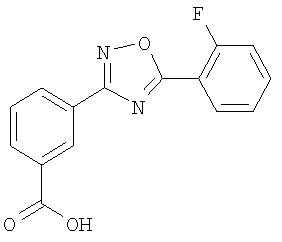
Данное соединение является одним из самых интенсивно изучаемых низкомолекулярных сапрессоров кодонов, позволяющих восстановить процесс синтеза нефункционирующих белков, нарушенный из-за наличия преждевременного кодона в m-РНК вследствие мутации, и является одним из многообещающих препаратов для коррекции ряда генетических нарушений (Welch E.M. и др. "РТС124 targets genetic disorders caused by nonsense mutations". Nature 447 (7140): 87-91 [2]).
Однако его меченный тритием аналог не описан.
Техническим результатом, достигаемым настоящим изобретением, является расширение ассортимента меченых аналогов физиологически активных соединений.
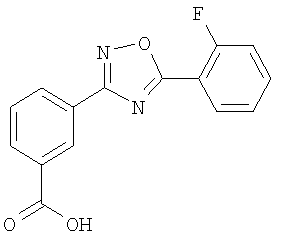
Достигается указанный технический результат получением меченной тритием 3-[5-(2-фторфенил)-1,2,4-оксадиазол-3-ил]бензойная кислоты формулы I:
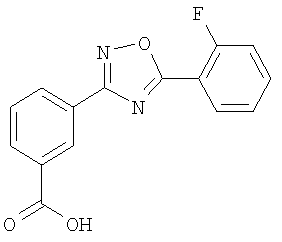
Ниже приведен пример реализации изобретения.
Пример I.
Раствор 2 мг 3-[5-(2-фторфенил)-1,2,4-оксадиазол-3-ил]бензойная кислоты в 0.34 мл смеси хлороформа с метанолом (3:1) добавляли к 55 мг Al2O3 (5 мкм), упарили и лиофилизировали. Остаток смешали с 25 мг 5% Pd/BaSO4, перетерли в ступке и вновь лиофилизировали. Сухую смесь переносили в реакционную ампулу. Затем ампулу вакуумировали до давления 0.1 Па, заполняли газообразным тритием до давления 400 гПа и выдерживали при температуре 265°C 5 мин. Избыток газообразного трития удаляли вакуумированием. Вещество с катализатора отделяли фильтрованием, экстракцию проводили метанолом (5×1 мл). Лабильный тритий удаляли несколько раз, растворяя вещество в метаноле (5×1 мл) и упаривая последний. Радиоактивность выделенного реакционной массы - около 1.25 Ки. После удаления летучих продуктов радиоактивность выделенного реакционной массы упала до 60 мКи.
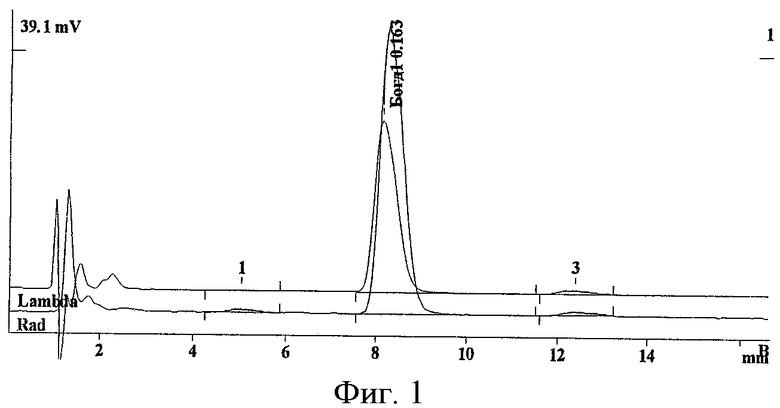
Хроматография на Милихроме А-02 колонка ProntoSIL-120-5-C18 AQ DB-2003, 2.0×75 мм, 5 мкм, 0.2 мл/мин, 35°С, детекция - 210 нм, А - 0.2 М LiClO4 + 0.005 М HClO4 буфер, Б - метанол, градиент Б→(0-100) за 16,5 мин, время удерживания - 16.02 мин, градиент Б→(50-100), время удерживания - 10.53 мин, градиент Б→(70-100), время удерживания - 4.95 мин. Распределение радиоактивности в продуктах реакции определяли с использованием колонки Reprosil pur C18aq, 5 мкм, 4×150 мм, в системе 70% метанол с 0.1% уксусной кислоты и 0.01% трифторуксусной кислоты, скорость потока - 1 мл/мин (фиг.1).
Фиг.1 - Распределение радиоактивности при анализе реакционной смеси после обработки исходного соединения тритием при 265°С.
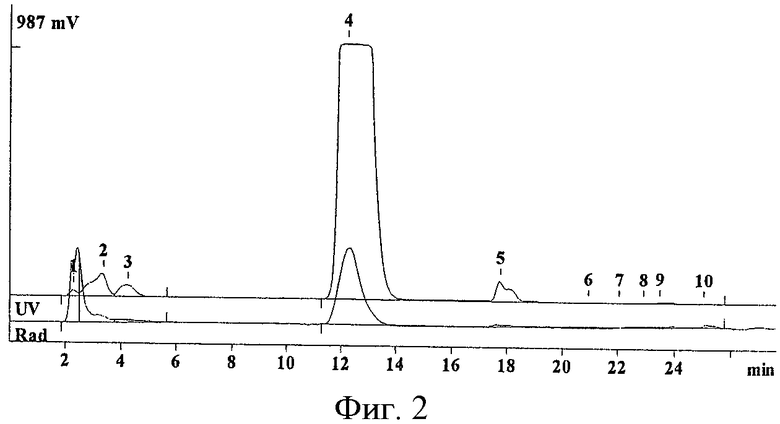
Фиг.2 - Распределение радиоактивности при препаративной хроматографии меченной тритием 3-[5-(2-фторфенил)-1,2,4-оксадиазол-3-ил]бензойная кислоты.
Препаративную хроматографию проводили на колонке Kromasil 100C18, 8×150 мм, 7 мкм, в системе 70% метанол с 0.1% уксусной кислоты и 0.01% трифторуксусной кислоты, скорость потока - 2 мл/мин, время удерживания - 12.56 мин (фиг.2).
После очистки методом ВЭЖХ радиохимическая чистота меченого препарата - 98%, выход - 25-30%, молярная радиоактивность - 6.5 Ки/ммоль.
Таким образом получено новое меченное тритием соединение.
| название | год | авторы | номер документа |
|---|---|---|---|
| РАВНОМЕРНО МЕЧЕННЫЙ ТРИТИЕМ 4,4-ДИФТОР-N-{(1S)-3-[3-(3-ИЗОПРОПИЛ-5-МЕТИЛ-4Н-1,2,4-ТРИАЗОЛ-4-ИЛ)-8-АЗАБИЦИКЛО[3.2.1]ОКТ-8-ИЛ]-1-ФЕНИЛПРОПИЛ}ЦИКЛОГЕКСАН КАРБОДИИМИД | 2008 |
|
RU2368613C1 |
| ВЫСОКОМЕЧЕННЫЙ ТРИТИЕМ [H]-(E)-N-[(4-ГИДРОКСИ-3-МЕТОКСИФЕНИЛ)МЕТИЛ]-8-МЕТИЛ-6-НОНЕНАМИД | 2004 |
|
RU2268256C1 |
| Равномерномеченный дейтерием и тритием 3-(1-метилпирролидин-2-ил)пиридин | 2014 |
|
RU2620190C2 |
| МЕЧЕННЫЙ ТРИТИЕМ АЦИЛКОЕНЗИМ А | 2006 |
|
RU2305104C1 |
| РАВНОМЕРНО МЕЧЕННЫЙ ДЕЙТЕРИЕМ ИЛИ ТРИТИЕМ 4-(2-АМИНОЭТИЛ)ПИРОКАТЕХОЛ С ИСПОЛЬЗОВАНИЕМ НАНОАЛМАЗНОГО ПОРОШКА | 2010 |
|
RU2422436C1 |
| РАВНОМЕРНО МЕЧЕННЫЙ ТРИТИЕМ (R)-(+)-[5-МЕТИЛ-3-(4-МОРФОЛИНИЛМЕТИЛ)-2,3-ДИГИДРО-[1,4]ОКСАЗИНО [2,3,4-hi]-6-ИНДОЛИЛ]-1-НАФТАЛИНИЛМЕТАНОН АЦЕТАТ | 2009 |
|
RU2404185C1 |
| РАВНОМЕРНО МЕЧЕННЫЙ ТРИТИЕМ 5-(1,1-ДИМЕТИЛГЕПТИЛ)-2-[5-ГИДРОКСИ-2-(3-ГИДРОКСИПРОПИЛ)ЦИКЛОГЕКСИЛ]ФЕНОЛ | 2009 |
|
RU2398755C1 |
| РАВНОМЕРНО МЕЧЕННЫЙ ТРИТИЕМ ТИЛОЗИН | 2008 |
|
RU2360896C1 |
| РАВНОМЕРНОМЕЧЕННАЯ ТРИТИЕМ [H]ТРАНС-3,7-ДИМЕТИЛ-9-(2,6,6-ТРИМЕТИЛ-3-ОКСО-1-ЦИКЛОГЕКСЕН-1-ИЛ)-2,4,6,8-НОНАТЕТРАЕНОВАЯ КИСЛОТА | 2006 |
|
RU2318806C1 |
| ВЫСОКОМЕЧЕННЫЙ ТРИТИЕМ 2-МЕТИЛ-3-ФИТИЛ-1,4-НАФТОХИНОН | 2001 |
|
RU2190591C1 |
Изобретение относится к области органической химии, а именно к меченной тритием 3-[5-(2-фторфенил)-1,2,4-оксадиазол-3-ил]бензойной кислоте формулы I.
Технический результат - получение меченного тритием аналога физиологически активного соединения, которое используется для коррекции ряда генетических нарушений. 2 ил.
Меченная тритием 3-[5-(2-фторфенил)-1,2,4-оксадиазол-3-ил]бензойная кислота формулы I
| US 20040204461 A1, 14.10.2004 | |||
| ПРОИЗВОДНЫЕ ОКСАДИАЗОЛА | 1997 |
|
RU2182905C2 |
Авторы
Даты
2010-09-10—Публикация
2009-03-27—Подача