Изобретение относится к области органической химии и может найти применение в аналитической химии и биологических исследованиях.
При изучении физиологически активных соединений необходимы их меченые аналоги.
Известно, что замена атомов соединений на их меченые аналоги не приводит к изменению каких-либо свойств исходного соединения (Evans Е.А. - Tritium and its compounds London Butterworths, 1974, p.48) [I].
Известен 4-(2-аминоэтил)пирокатехол формулы I:

Данное соединение является эндогенным катехоламином с α- и β-адренергической активностью (Мерк 3479) (J. F. Dasta, M. G. Kirby // Pharmacotherapy 6, 304 (1986) [2]).
Известен способ получения его меченного тритием аналога (C.N.Filer, D.Orphanos, R.J.Seguin "Synthesis of [Ring-3H]dopamine and fluoro analogues at high specific activity" // Synthetic Communications. 2006. Vol. 36. P.975-978 [3]). Полученный препарат содержал метку только в ароматическом кольце (44 Ки/ммоль), при этом содержание изотопа водорода в среднем равнялось около 1.5 атомов на молекулу 4-(2-аминоэтил)пирокатехола.
Техническим результатом, достигаемым настоящим изобретением, является получение равномерномеченного дейтерием и тритием 4-(2-аминоэтил)пирокатехола с использованием наноалмазного порошка (НАП), что расширит ассортимент меченых аналогов физиологически активных соединений.
Достигается указанный технический результат получением меченного изотопами водорода 4-(2-аминоэтил)пирокатехола формулы I:

Ниже приведен пример реализации изобретения.
Пример I.
20 мг НАП смешивали с раствором 2 мг солянокислого 4-(2-аминоэтил)пирокатехола в 30 мкл метанола, растворитель упарили, а остаток лиофилизировали. Остаток смешали с 60 мг катализатора Линдлара, механически растерли и снова лиофилизировали.
Высушенный остаток помещали в ампулу. Ампулу вакуумировали и заполняли дейтерием или тритием. Реакцию вели при 180°С в течение 15 мин. Ампулу снова вакуумировали, катализатор наносили на фильтр, вещество экстрагировали смесью метанола с уксусной кислотой (5×0.5 мл метанола с 1% уксусной кислотой). Экстракты упаривали, остаток растворяли в метаноле (3×1 мл) и вновь упаривали для удаления лабильного дейтерия или трития.
Анализ проводили на Милихроме А-02, колонка ProntoSIL-120-5-C18 AQ DB-2003, 2.0×75 мм, 5 мкм, 0.2 мл/мин, 35°С, детекция - 210 нм, А - 0.2 М LiClO4+0.005М НСlO4 буфер, Б - метанол, градиент Б→(0-100) за 12.5 мин, время удерживания 4-(2-аминоэтил)пирокатехола - 4.27 мин. Время удерживания 4-(2-аминоэтил)пирокатехола при анализе в тех же условиях, но при использовании воды, содержащей 0.1% трифторуксусной кислоты, в качестве системы А равнялось 3.83 мин.
Меченый 4-(2-аминоэтил)пирокатехол очищали также методом высокоэффективной жидкостной хроматографии. Хроматографию проводили на колонке Kromasil 100C18, 8×150 мм, 7 мкм, система: метанол-вода-уксусная кислота-трифторуксусная кислота (20:80:0.1:0.01), скорость потока - 2 мл/мин, время удерживания - 11 мин, содержание меченого препарата не менее - 98%, выход - 7-10%.
а) В случае использования дейтерия в молекулу 4-(2-аминоэтил)пирокатехола включалось в среднем 4.8 атома детерия. Причем распределение дейтерия доходило до семи атомов в молекулу допамина (14%), а изотопомер, содержащий 5 атомов дейтерия, образовывался с наибольшим выходом (31%). Таким образом, при использовании наноматериалов распределение метки в полученном соединении и прототипе существенно отличалось, т.е. получено новое меченое соединение с другими характеристиками.
б) В случае использования трития получен меченый 4-(2-аминоэтил)пирокатехол с молярной радиоактивностью до 130-135 Ки/ммоль, что в три раза выше, чем в прототипе.
Таким образом получено равномерномеченное изотопами водорода соединение.
| название | год | авторы | номер документа |
|---|---|---|---|
| РАВНОМЕРНОМЕЧЕННЫЙ ДЕЙТЕРИЕМ ИЛИ ТРИТИЕМ His-Phe-Arg-Trp-Pro-Gly-Pro | 2014 |
|
RU2544016C1 |
| Равномерномеченный дейтерием и тритием 3-(1-метилпирролидин-2-ил)пиридин | 2014 |
|
RU2620190C2 |
| РАВНОМЕРНОМЕЧЕННЫЙ ТРИТИЕМ АЛЬФА-ХЕДЕРИН | 2006 |
|
RU2326889C1 |
| РАВНОМЕРНО МЕЧЕННЫЙ ТРИТИЕМ 5-(1,1-ДИМЕТИЛГЕПТИЛ)-2-[5-ГИДРОКСИ-2-(3-ГИДРОКСИПРОПИЛ)ЦИКЛОГЕКСИЛ]ФЕНОЛ | 2009 |
|
RU2398755C1 |
| РАВНОМЕРНО МЕЧЕННЫЙ ТРИТИЕМ [H]-14-ГИДРОКСИДАУНОМИЦИН АДРИАМИЦИНОНА | 2006 |
|
RU2305103C1 |
| РАВНОМЕРНОМЕЧЕННЫЙ ТРИТИЕМ ПИРО-Glu-His-Pro-NH | 2013 |
|
RU2513852C1 |
| РАВНОМЕРНОМЕЧЕННЫЙ ТРИТИЕМ [Н]АМФОТЕРИЦИН В | 2006 |
|
RU2323224C1 |
| РАВНОМЕРНОМЕЧЕННАЯ ТРИТИЕМ [H]ТРАНС-3,7-ДИМЕТИЛ-9-(2,6,6-ТРИМЕТИЛ-3-ОКСО-1-ЦИКЛОГЕКСЕН-1-ИЛ)-2,4,6,8-НОНАТЕТРАЕНОВАЯ КИСЛОТА | 2006 |
|
RU2318806C1 |
| РАВНОМЕРНО МЕЧЕННЫЙ ТРИТИЕМ (R)-(+)-[5-МЕТИЛ-3-(4-МОРФОЛИНИЛМЕТИЛ)-2,3-ДИГИДРО-[1,4]ОКСАЗИНО [2,3,4-hi]-6-ИНДОЛИЛ]-1-НАФТАЛИНИЛМЕТАНОН АЦЕТАТ | 2009 |
|
RU2404185C1 |
| РАВНОМЕРНОМЕЧЕННЫЙ ТРИТИЕМ 4-ИОДО-N-[4-МЕТОКСИ-3-(4-МЕТИЛ-1-ПИПЕРАЗИНИЛ)ФЕНИЛ]БЕНЗЕНСУЛЬФОНАМИД | 2012 |
|
RU2491281C1 |
Изобретение относится к равномерномеченному дейтерием или тритием 4-(2-аминоэтил)пирокатехолу формулы (I), применяемому в аналитической химии и биологических исследованиях. Равномерномеченный дейтерием или тритием 4-(2-аминоэтил)пирокатехол получают с использованием наноалмазного порошка (НАП). Технический результат - равномерномеченный дейтерием или тритием 4-(2-аминоэтил)пирокатехол.
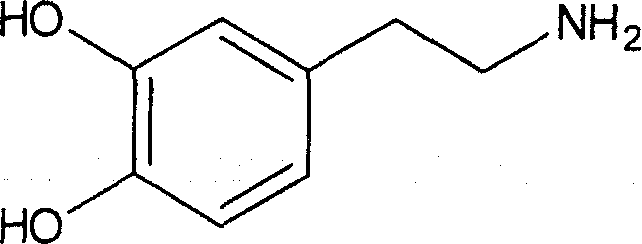
Равномерно меченный дейтерием или тритием 4-(2-аминоэтил)пирокатехол формулы I:

| PAJAK, M.; KANSKA, M.: «Enzymatic synthesis of dopamine ring labeled with hydrogen isotopes» JOURNAL OF RADIOANALYTICAL AND NUCLEAR CHEMISTRY | |||
| POL., 2009, vol | |||
| АППАРАТ ДЛЯ ОБОГАЩЕНИЯ РУД ПО МЕТОДУ ВСПЛЫВАНИЯ | 1915 |
|
SU279A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| СПОСОБ ПОЛУЧЕНИЯ 4-(2-АМИНОЭТИЛ)ФЕНОЛА | 2001 |
|
RU2218326C2 |
| FARNUM MARTIN, PALCIC MONICA, KLINMAN JUDITH P.: «pH Dependence of deuterium isotope effects and tritium exchange in the bovine | |||
Авторы
Даты
2011-06-27—Публикация
2010-04-15—Подача