Изобретение относится к области ветеринарной вирусологии и биотехнологии и может быть использовано при изготовлении средств специфической профилактики и диагностики вирусной геморрагической болезни кроликов.
Вирусная геморрагическая болезнь кроликов - ВГБК (некротический гепатит, геморрагическая пневмония кроликов) - остропротекающая высококонтагиозная болезнь вирусной этиологии, наносящая значительный экономический ущерб кролиководству.
ВГБК характеризуется явлениями геморрагического диатеза во всех органах кроликов, в особенности в легких и печени. Поражаются кролики старше 1,5-месячного возраста. О заболевании этим вирусом животных других видов и человека не сообщалось. При ВГБК заболеваемость достигает 70-80%, а летальность - 90-100%. Болезнь широко распространена в мире, где есть восприимчивые животные, европейские кролики (Oryctolagus cuniculus).
Экономический ущерб, наносимый ВГБК, складывается из-за высокого процента гибели взрослых особей и молодых кроликов с момента отъема.
Вакцинопрофилактика ВГБК занимает основное место в комплексе противоэпизоотических мер, направленных на борьбу с этим заболеванием. Для вакцинопрофилактики вирусной геморрагической болезни кроликов применяют инактивированные моно- и ассоциированные вакцины. Рекомбинантные вакцины против ВГБК в настоящее время тоже получены, но коммерчески широко не применяются.
Молекулярно-генетические исследования зарубежных ученых за последнее десятилетие показывают, что все штаммы ВГБК (в тех областях, где болезнь была диагностирована) принадлежат к одному серотипу [1-2]. Сравнительное секвенирование выделенных изолятов показывает, что в консервативных областях генома они имеют отличия по аминокислотному составу в пределах от 2 до 5%. Однако выделенные в последнее время температурозависимые изоляты вируса ГБК в Германии, Италии значительно отличаются по гемагглютинирующим свойствам при более низкой температуре +4°С и по аминокислотному составу от ранее известных вирусов ГБК в области Е генома, где у представителей калицивирусов представлены основные антигенные детерминанты.
Известен штамм «Воронежский-87», официально депонированный в коллекциях ФГУ «ВГНКИ» (регистрационный №1652) и ГНУ ВНИИВВИМ для изготовления инактивированных вакцин против ВГБК [3-5].
Однако кролики, привитые вакциной, приготовленной из ранее выделенных изолятов, имеют более низкую степень защиты против выделенных изолятов ВГБК. Поэтому в России необходимо не только вести генетический мониторинг и сравнение гемагглютинирующих и иммунобиологических свойств вновь появляющихся изолятов ВГБК в очагах инфекции, но и иметь в музейных коллекциях штаммы вируса геморрагической болезни кроликов, позволяющих изготавливать из них более эффективные средства специфической профилактики против ВГБК, исходя из эпизоотической ситуации.
Целью настоящего изобретения явилось получение нового производственного и диагностического штамма вируса геморрагической болезни кроликов, сохраняющего свои иммунобиологические свойства после инактивации и пригодного для изготовления высокоиммуногенных вакцинных препаратов, диагностических систем (из неконцентрированного вируса), способных защитить поголовье европейского кролика (Oryctolagus cuniculus) от эпизоотического возбудителя геморрагической болезни кроликов и идентифицировать его при заносе на территорию Российской Федерации.
Технический результат от использования предлагаемого изобретения заключается в расширении арсенала штаммов вируса геморрагической болезни кроликов, отличающихся геномом и иммунобиологическими свойствами, обладающих высокой биологической антигенной и иммуногенной активностью, сохраняющих свои нативные иммунобиологические свойства после инактивации и пригодных для изготовления высокоэффективных вакцинных, лечебных и диагностических препаратов.
Данный технический результат достигнут получением штамма «Манихино-09» вируса геморрагической болезни кроликов. Штамм «Манихино-09» является новым и ранее неизвестным.
Полученный штамм депонирован во Всероссийской государственной коллекции штаммов микроорганизмов, используемых в ветеринарии и животноводстве, Всероссийского Государственного Центра Качества и Стандартизации Лекарственных Средств для Животных и Кормов РОССЕЛЬХОЗНАДЗОРА (ФГУ «ВГНКИ») 19 ноября 2009 года под регистрационным шифром Штамм «Манихино-09».
Штамм «Манихино-09» отличается от ранее депонированного штамма ВГБК «Воронежский-87» на 7% по нуклеотидным последовательностям консервативной области гена VP-60 длинной 398 пар нуклеотидов и на 6% от штамма вируса ГБК «Белгородский-03». Вышеуказанные штаммы, основываясь на результатах филогенетического анализа, относятся к разным геногруппам.
Штамм «Манихино-09» обеспечивает проведение серологической диагностики вирусной геморрагической болезни кроликов и производство эффективной инактивированной вакцины против ВГБК, создающей надежную защиту диких и домашних европейских кроликов от указанного возбудителя заболевания.
Штамм «Манихино-09» вируса геморрагической болезни кроликов характеризуется следующими признаками и свойствами.
Таксономическая характеристика заключается в том, что штамм «Манихино-09» имеет форму и размеры, типичные для калицивирусов. В серологических реакциях (РЗГА, РСК, ИФА, РДП) выявляются антигены, общие для всех штаммов вируса геморрагической болезни кроликов. Основные маркерные характеристики штамма «Манихино-09» вируса геморрагической болезни кроликов приведены в таблице.


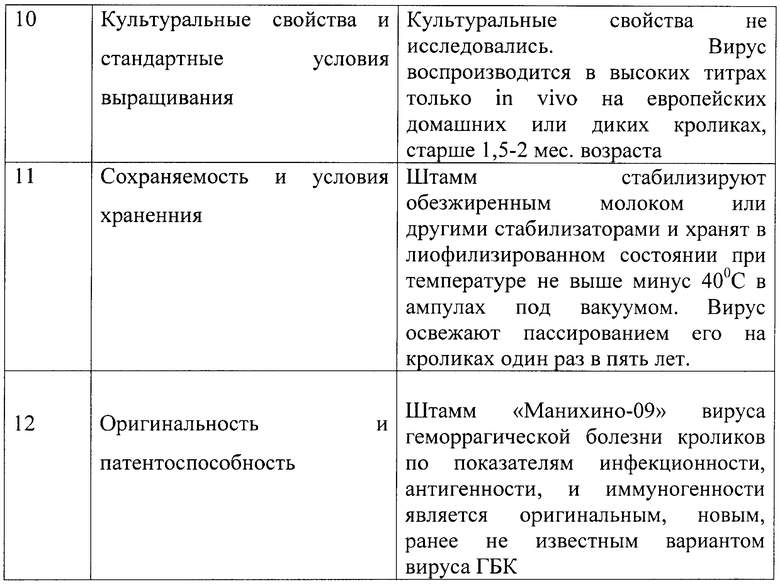
Сущность предлагаемого изобретения поясняется примерами его исполнения.
Пример 1
Для получения вируса геморрагической болезни кроликов штамм «Манихино-09» используют три ампулы с вирусом, на уровне первого пассажа на кроликах, павших от введения им 10% суспензии печени от кроликов, павших в Московской области в марте 2009 года (инфекционная активность не ниже 104,0 ЛД50/см3). В каждую ампулу вносят стерильный растворитель (дистиллированная вода или физиологический раствор, pH 7,0-7,4) до объема, указанного на этикетке. Затем содержимое ампул объединяют и из общей пробы готовят разведение вируса на физиологическом растворе таким образом, чтобы в конечном разведении содержалось 100 ЛД50/см3. Указанное разведение вируса вводят внутримышечно 5 кроликам в объеме 1,0 см3. Инфицированных кроликов содержат в оборудованном инфекционном виварии в индивидуальных металлических клетках.
У инфицированных кроликов через 15-25 ч отмечают характерные клинические признаки болезни: угнетение, отказ от корма, повышение температуры тела до 40,7°C, носовое кровотечение и гибель в течение 24-96 ч. Трупы животных погружают на 5-10 мин в раствор марганцевокислого калия (1:10000), затем во вскрывочной комнате инфекционного вивария подвешивают на вешалки, снимают шкурки, обрабатывают брюшную полость раствором марганцевокислого калия (1:10000), разрезают брюшные мышцы по белой линии, извлекают печень, отделяют желчный пузырь. Печень используют только от трупов, при вскрытии которых обнаружены специфические патолого-анатомические изменения, свойственные ВГБК: геморрагии в трахее, геморрагическая пневмония, кровоизлияния под капсулой почек, селезенки, печень дряблой консистенции, которая легко рвется и имеет желто-коричневый цвет, местами с красноватым оттенком. Некроз печени и увеличение селезенки - первичные поражения. Острое поражение легких - результат венозного тромбоза, вызывающего острый отек, пенистый серозный или с примесью крови транссудат, который заполняет пеной трахею и выделяется постоянно из ноздрей. Инфаркты наблюдают почти во всех органах, а почки - полностью инфарктны и имеют темно-коричневый цвет.
Материал помещают в стерильные флаконы, плотно укупоривают, снаружи дезинфицируют 5%-ным раствором хлорамина, помещают в термос со льдом и доставляют в стерильный бокс.
Каждый образец печени готовят отдельно, используя отдельную стерильную посуду. Образец печени измельчают ножницами, добавляют стерильный ФСБ (соотношение 1:10 - вес/объем), гомогенизируют в блендере при охлаждении в течение 10 мин. Отбирают в отдельную стерильную пробирку типа «Eppendorf» для идентификации в ПЦР. В оставшийся материал вносят хлороформ (конечная концентрация 2%) и помещают в камеру бытового холодильника на 18 ч при 4°C. После чего суспензию печени центрифугируют в течение 1 ч при 6000 g при 4°C. Супернатант ультрацентрифугируют при 80000 g в течение 2 ч при 4°C, через 20%-й раствор сахарозы. Осадок ресуспендируют в ФСБ 1/100 от начального объема.
Для получения результатов молекулярно-генетической характеристики штамма «Манихино-09» вируса геморрагической болезни кроликов было проведено нуклеотидное секвенирование консервативной области гена VP-60, длинной 398 пар нуклеотидов.
Нуклеотидное секвенирование участков гена VP60 вируса геморрагической болезни кроликов проводят с использованием типоспецифических праймеров, разработанных для обнаружения вируса методом ПЦР. Выделение специфических продуктов амплификации из агарозного геля или реакционной смеси осуществляют коммерческим набором для выделения нуклеиновых кислот «DNA purification kit» (Fermentas, Латвия), с последующей реамплификацией фрагментов при помощи компонентов «BigDye v.3.1. Terminator» (Applied Biosystems, США). Реакцию с дефектными трифосфатами проводят в параллелях с прямым и обратным праймерами при следующих температурных режимах: 95°C - 10 с, 50°C - 20 с, 60°C - 4 мин - всего 25 циклов. По окончании реакции к смеси добавляют 45 мкл 96% этилового спирта и 2,5 мкл 125 мМ ЭДТА, перемешивают и оставляют при комнатной температуре на 10-15 минут. Затем центрифугируют в течение 10-15 минут при 10000 g, надосадочную жидкость выбрасывают, а осадок промывали 75% этиловым спиртом по той же схеме с 10-15 мин экспозицией при комнатной температуре. Осадок после центрифугирования подсушивают, аккуратно растворяют в 10-12 мкл формамида. Полученную смесь денатурируют при 94°C в течение нескольких минут и резко охлаждают во льду. Секвенирование проводят в автоматическом анализаторе Genetic Analyzer 3130XL (Applied Biosystems, США).
Вируссодержащий материал всесторонне исследуют в соответствии с рекомендациями МЭБ по стандартным диагностическим методам и вакцинам (2004) на отсутствие контаминации микоплазмами, бактериями и грибами путем посева на чувствительные питательные среды. Отсутствие контаминации посторонними вирусами и идентификацию вируса геморрагической болезни кроликов определяют методом негативного контрастирования электронной микроскопией. Определяют инфекционную активность на кроликах, гемагглютинирующую активность в РГА, антигенную активность в ТФ ИФА, специфичность в ТФ ИФА и РЗГА и на уровне 2 пассажа на кроликах вирус был расфасован, лиофилизирован и запаян в ампулы под вакуумом и заложен на хранение при температуре не выше минус 40°C в качестве Master seed (M.s.) с титром инфекционной активности не ниже 5,0 lg LD50/см3. Полученному штамму вируса геморрагической болезни кроликов присвоено авторское название «Манихино-09».
Пример 2
С целью определения биологической, антигенной и иммунологической активности вируса геморрагической болезни кроликов штамма «Манихино-09» проводят гипериммунизацию клинически здоровых кроликов из благополучных по инфекционным и инвазионным болезням хозяйств, живой массой не менее 2,5 кг, согласно 2-ой схеме получения специфической сыворотки для лечения, диагностики и профилактики ВГБК (патент №2077340 от 06 августа 1993 года). Для гипериммунизации кроликов используют тканевую инактивированную вакцину, изготовленную из штамма вируса геморрагической болезни кроликов штамм «Манихино-09» в дозе 0,5 мл на голову. Путь введения препарата животным - внутримышечно. Кратность введения - двукратно, с интервалом 14 дней. Через 14 дней после второй иммунизации от гипериммунизированных животных получают сыворотку крови. Специфическую сыворотку проверяют на активность и специфичность в реакции задержки гемагглютинации. Результаты исследований приведены в таблице 1.
Приведенные в таблице 1 данные, характеризуют высокую биологическую, антигенную и иммуногенную активность штамма «Манихино-09» вируса геморрагической болезни кроликов при введении в организм лабораторным животным.
Пример 3
Для получения вируса, используемого при изготовлении тканевой инактивированной гидроокисьалюминиевой вакцины против ВГБК из штамма «Манихино-09», используют полученную и охарактеризованную матровую расплодку Master seed (M.s.) вируса геморрагической болезни кроликов из вышеуказанного штамма. Изначально готовят разведение вируса на физиологическом растворе таким образом, чтобы в конечном разведении содержалось 100 ЛД50/см3. Указанное разведение вируса вводят внутримышечно кроликам в объеме 1,0 см3. Предварительно сыворотку крови кроликов исследуют на наличие антител к вирусу ВГБК «Манихино-09» в РЗГА при +(4±2)°C и при +(20±2)°C с эритроцитами крови человека 0(I) группы. При наличии специфических антител к указанному вирусу в титре 1:4 и выше кроликов в опыт не берут. Инфицированных кроликов содержат в оборудованном инфекционном виварии в индивидуальных металлических клетках.
Из полученной от павших кроликов печени готовят 10%-ную вирусную суспензию на забуференном физрастворе (pH 7,0-7,4). В материал вносят хлороформ (конечная концентрация 2%) и помещают в холодильник при 4°C на 18 часов. Затем суспензию печени центрифугируют в течение 1 ч при 6000 g при 4°C. Вирусная суспензия, используемая для изготовления тканевой инактивированной вакцины, должна иметь активность в РГА при +(4±2)°C не менее 1:1280-1:2560 ГАЕ.
Инактивацию вируса проводят с помощью 4%-ного раствора формалина. Исходя из концентрации формальдегида готовят 4%-ный раствор формалина (т.е. 1,1-1,4% раствор формальдегида) на стерильной дистиллированной воде. Раствор формалина готовят в стеклянных бутылях в день составления сырья для вакцины и вносят в вирусную суспензию до конечной концентрации 0,14-0,1% формальдегида.
Инактивируют вирус при температуре 27-28°C в течение 3-х суток с периодическим перемешиванием (1 раз в час в течение 5 мин).
Началом инактивации считают время после доведения температуры в емкости до 27-28°C и добавления формалина. После инактивации формалином к суспензии при постоянном перемешивании добавляют метабисульфит натрия (1М раствор) до полной нейтрализации остаточного формальдегида.
Из инактивированного материала брали пробу для проверки стерильности, активности и полноты инактивации. Для проверки полноты инактивации двум кроликам массой 2,5-3,0 кг, не имеющих антител к вирусу геморрагической болезни кроликов, вводят по 3,0 см3 внутримышечно инактивированный материал. Животные в течение 7 суток наблюдения оставались здоровыми.
После окончания инактивации вируссодержащей суспензии в емкость с вирусной суспензией добавляют гель гидрата окиси алюминия (ГОА) с 3% сухого остатка после размола из расчета на 1000 см3 суспензии 150 см3 ГОА (20%) при pH 7,2-7,4 и температуре 4-8°C (патент РФ №2039570 от 20 июля 1995 года). Сорбцию проводят в течение 1-2 часов с периодическим перемешиванием. Вакцину хранят при 8°C до получения результатов контроля препарата. Смесь перед фасовкой перемешивают при температуре 10-12°C в течение 1 часа.
Содержание антигена при +(4±2)°C в дозе вакцины на уровне 640-1280 ГАЕ является его оптимальным количеством в препарате, обеспечивающим достижение технического результата.
Полученную вакцину проверяют на внешний вид, стерильность, уровень pH, полноту инактивации вируса, иммуногенность и безвредность.
Вакцина представляет собой прозрачную жидкость серо-коричневого цвета с рыхлым осадком, образующимся при хранении, который при встряхивании легко разбивается в гомогенную взвесь.
Стерильность вакцины определяют в соответствии с ГОСТ 28085-89. Безвредность препарата определяют путем его введения четырем кроликам внутримышечно по 3 см3. Вакцина считается безвредной, если она не вызывает гибель или заболевания кроликов, а также изменений некротического характера на месте введения в течение 14 суток наблюдения.
Полноту инактивации вируса в вакцине проверяют на 4 кроликах, которым вводят внутримышечно в область средней трети бедра по 3,0 см3.
За кроликами ведут наблюдение в течение 10 дней. Вакцину считают не содержащей инфекционного вируса, если она не вызывает гибели кроликов от вирусной геморрагической болезни в течение 10 суток после введения препарата.
В используемых флаконах с вакциной определяют pH, средняя величина показателей должна быть в пределах 7,2-7,4.
Гемагглютинирующую активность антигена каждой серии вакцины определяют в реакции гемагглютинации (РГА) при +(4±2)°C, с эритроцитами человека 0(I) группы и выражают в гемагглютинирующих единицах. Гемагглютинирующий титр в вакцине должен быть не ниже 8,0 log2, что соответствует разведению 1:256 ГАЕ.
Результаты, приведенные в таблице 2, свидетельствуют о том, что тканевая инактивированная гидроокисьалюминиевая вакцина против ВГБК из штамма «Манихино-09» обладает высокой гемагглютинирующей активностью.
При изучении иммуногенной активности тканевой инактивированной гидроокисьалюминиевой вакцины против ВГБК из штамма «Манихино-09» установлено, что у кроликов старше 1,5-2 мес. возраста, привитых однократно внутримышечно в дозе 0,5 мл уже на 5 день после введения препарата индуцируется иммунный ответ, обеспечивающий 90-100% образование гуморальных антител и защиту от заболевания. Экспериментально показано, что одна прививная доза в объеме 0,5 мл содержит не менее 640-1280 ГАЕ. Результаты исследований, представленные в таблице 3, подтверждают высокую эффективность инактивированной вакцины против ВГБК из штамма «Манихино-09».
Таким образом, штамм «Манихино-09», полученный в соответствии с предлагаемым изобретением, обладает высокой инфекционной, антигенной и иммуногенной активностью и пригоден для изготовления вакцинных препаратов против ВГБК.
Источники информации
1. Molecular epidemiology of Rabbit haemorrhagic disease virus. Moss S.R., Turner S.L., Trout R.C., White P.J., Hudson P.J., Desai A., Armesto M., Forrester N.L., Gould E.A.; J. Gen. Virol. - 2002. - Vol.83. - P.2461-2467.
2. Manual of standards Diagnostic Tests and Vaccines 2004; PART 2; SECTION 2.8.; CHAPTER 2.8.3. RABBIT HAEMORRHAGIC DISEASE.
3. Патент РФ №2077340 от 06 августа 1993 г.
4. Патент РФ №2039570 от 20 июля 1995 г.
5. Авторское свидетельство №294945 от 22.08.1989 г.
| название | год | авторы | номер документа |
|---|---|---|---|
| Штамм "Шевченко-2014" вируса геморрагической болезни кроликов для изготовления вакцинных, диагностических и лечебных препаратов | 2015 |
|
RU2631925C2 |
| ШТАММ "БЕЛГОРОДСКИЙ-03" ВИРУСА ГЕМОРРАГИЧЕСКОЙ БОЛЕЗНИ КРОЛИКОВ ДЛЯ ИЗГОТОВЛЕНИЯ ВАКЦИННЫХ И ДИАГНОСТИЧЕСКИХ ПРЕПАРАТОВ | 2010 |
|
RU2417262C1 |
| Ассоциированная вакцина против миксоматоза, пастереллёза и вирусной геморрагической болезни кроликов 1 и 2 типов | 2020 |
|
RU2741643C1 |
| ШТАММ "АС-21/07" ВИРУСА АУЕСКИ ДЛЯ ИЗГОТОВЛЕНИЯ ВАКЦИННЫХ И ДИАГНОСТИЧЕСКИХ ПРЕПАРАТОВ | 2010 |
|
RU2439150C1 |
| ВАКЦИНА АССОЦИИРОВАННАЯ ПРОТИВ ПАРАГРИППА-3, ИНФЕКЦИОННОГО РИНОТРАХЕИТА И ВИРУСНОЙ ДИАРЕИ КРУПНОГО РОГАТОГО СКОТА ЭМУЛЬСИОННАЯ ИНАКТИВИРОВАННАЯ | 2012 |
|
RU2504400C1 |
| Ассоциированная вакцина против чумы плотоядных, парвовирусного и коронавирусного энтеритов, аденовирусной инфекции собак | 2022 |
|
RU2806164C1 |
| Ассоциированная вакцина против панлейкопении, калицивироза и вирусного ринотрахеита кошек | 2023 |
|
RU2812330C1 |
| ШТАММ "ЛЕНИНГРАДСКИЙ" ВИРУСА ТРАНСМИССИВНОГО ГАСТРОЭНТЕРИТА СВИНЕЙ ДЛЯ ИЗГОТОВЛЕНИЯ ДИАГНОСТИЧЕСКИХ И ВАКЦИННЫХ ПРЕПАРАТОВ | 2004 |
|
RU2266326C1 |
| ШТАММ "ИЛЬИНОГОРСКИЙ" ВИРУСА ТРАНСМИССИВНОГО ГАСТРОЭНТЕРИТА СВИНЕЙ ДЛЯ ИЗГОТОВЛЕНИЯ ДИАГНОСТИЧЕСКИХ И ВАКЦИННЫХ ПРЕПАРАТОВ | 2004 |
|
RU2266328C1 |
| ВАКЦИНА ПРОТИВ ВИРУСНОЙ ДИАРЕИ КРУПНОГО РОГАТОГО СКОТА | 2011 |
|
RU2457859C1 |
Изобретение относится к ветеринарной вирусологии и биотехнологии. Показана антигенная и иммуногенная эффективность нового штамма «Манихино-09», используемого для приготовления инактивированной вакцины против ВГБК. Вакцина содержит антигенный материал из штамма «Манихино-09» вируса геморрагической болезни кроликов, формалин, метабисульфит натрия, гель гидроокиси алюминия в эффективных соотношениях. Штамм депонирован в коллекции ВГНКИ под регистрационным наименованием «Манихино-09» - ДЕП вирус геморрагической болезни кроликов. Вирус репродуцируется in vivo на европейском кролике (Oryctolagus cuniculus) старше 1,5 мес возраста, свободных от антител против этого заболевания или имеющих титр антител против ВГБК ниже 1:4. В качестве инактиванта используют 4%-ный раствор формалина (т.е. 1,1-1,4% раствор формальдегида). Для приготовления сорбированной вакцины из адъювантов используют гель гидроокиси алюминия (ГОА). Вакцина обладает высокой антигенной и иммуногенной активностью. 4 табл.
Штамм вируса геморрагической болезни кроликов, семейства Caliciviridae, род Lagovirus, коллекция ВГНКИ, регистрационное наименование «Манихино-09» - ДЕП для изготовления вакцинных и диагностических препаратов.
| СПОСОБ ПОЛУЧЕНИЯ СПЕЦИФИЧЕСКОЙ СЫВОРОТКИ ДЛЯ ЛЕЧЕНИЯ, ДИАГНОСТИКИ И ПРОФИЛАКТИКИ ВИРУСНОЙ ГЕМОРРАГИЧЕСКОЙ БОЛЕЗНИ КРОЛИКОВ И НАБОР ДЛЯ ДИАГНОСТИКИ БОЛЕЗНИ | 1993 |
|
RU2077340C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ИНАКТИВИРОВАННОЙ ВАКЦИНЫ ПРОТИВ ВИРУСНОЙ ГЕМОРРАГИЧЕСКОЙ БОЛЕЗНИ КРОЛИКОВ | 1992 |
|
RU2039570C1 |
| ВАКЦИНА ПРОТИВ ВИРУСНОЙ ГЕМОРРАГИЧЕСКОЙ БОЛЕЗНИ КРОЛИКОВ | 2002 |
|
RU2229895C1 |
Авторы
Даты
2011-04-20—Публикация
2010-02-09—Подача