Введение
Настоящее изобретение относится к новым соединениям 3-цианонафталин-1-карбоновой кислоты и пергидроксиалкилметилпиперазина формулы I, которые являются антагонистами рецепторов тахикинина. Кроме того, настоящее изобретение относится к фармацевтическим композициям, включающим такие соединения, к способам получения таких соединений и к промежуточным продуктам для получения соединений по указанным способам.
Предпосылки создания изобретения
Тахикинины включают природные нейропептиды, такие как вещество Р, нейрокинин А и нейрокинин В. Тахикинины действуют в качестве агонистов рецепторов, присутствующих в организме крупных млекопитающих и в организме человека, такие как рецепторы нейрокинина NK1, NK2 и NK3. Синтетические соединения, которые являются антагонистами рецепторов тахикинина, обычно классифицируются по их относительной способности связываться с одним или более вышеуказанных трех подтипов рецептора. В физиологическом процессе тахикинины играют важную роль в передаче сигналов боли, рвоты, нейрогенного воспаления, воспаления мочевого пузыря, воспалительных заболеваний суставов или приступов астмы.
Производные пиперазина, которые действуют в качестве антагонистов рецептора NK1, описаны в WO 2004/033428 А1.
Производные пиперазина, которые действуют в качестве антагонистов рецептора NK2, описаны в ЕР 1293506 А1.
Другие производные пиперазина, которые действуют в качестве антагонистов рецепторов тахикинина, описаны в WO 96/10568.
Объектом настоящего изобретения является разработка новых активных соединений, которые являются антагонистами рецепторов тахикинина NK1 и NK2 и характеризуются улучшенным профилем действия и которые являются прежде всего пригодными для лечения и/или профилактики респираторных заболеваний, прежде всего астмы, бронхита, кашля и ринита, кожных заболеваний, прежде всего воспалительных кожных реакций, аллергических кожных реакций и псориаза, артропатических заболеваний, прежде всего артрита, васкулитов и системной красной волчанки, функциональных или воспалительных нарушений в желудочно-кишечном тракте, прежде всего псевдомембранозного колита и диареи, буллезных заболеваний, таких как цистит и интерстициальный цистит, и мигрень. Соединения по настоящему изобретению прежде всего пригодны для лечения периферических нарушений, таких как функциональные и воспалительные нарушения в желудочно-кишечном тракте, такие как IBS.
В настоящее время неожиданно установлено, что группа новых соединений 3-цианонафталин-1-карбоновой кислоты и пергидроксиалкилметилпиперазина обладает антагонистическим действием на рецепторы тахикинина, прежде всего на рецепторы NK1 и NK2, и прежде всего заметной активностью в периферической области организма. Следовательно, группа соединений по изобретению прежде всего пригодна для лечения периферических нарушений, при которых переносчиками сигнала являются тахикинины, прежде всего нейрокинин А, например, для лечения и/или профилактики респираторных заболеваний, прежде всего астмы, бронхита, кашля и ринита, кожных заболеваний, прежде всего воспалительных кожных реакций, аллергических кожных реакций и псориаза, артропатических заболеваний, прежде всего артрита, васкулитов и системной красной волчанки, функциональных или воспалительных нарушений в желудочно-кишечном тракте, прежде всего псевдомембранозного колита и диареи, буллезных заболеваний, таких как цистит и интерстициальный цистит, и мигрень.
Другим преимуществом соединений по настоящему изобретению является их свойство эффективно поддерживать баланс комбинированного NK1- и NK2-профиля.
Еще одним преимуществом соединений по настоящему изобретению является синергитическое действие на профиль NK1 и NK2.
Краткое изложение сущности изобретения
Объектом изобретения являются новые соединения 3-цианонафталин-1-карбоновой кислоты и пергидроксиалкилметилпиперазина общей формулы I

где
R1 выбирают из группы, включающей водород и С1-С4алкил,
R2 означает галоген,
R3 означает галоген,
R4 выбирают из группы, включающей 2-фуранил, 3-фуранил, 2-тиофен, 3-тиофен, фенил, бензил, 2-бензофуранил, 3-бензофуранил, 5-хлор-2-тиофен, 4-метилфенил, 3,4-метилендиоксифенил, 2-метоксифенил, 4-метоксифенил, 2-пиридинил, 3-пиридинил, 1-бензо[с]тиофен, 4-бензо[с]тиофен, 5-бензо[с]тиофен, 2-бензо[b]тиофен, 3-бензо[b]тиофен, 4-бензо[b]тиофен, 5-бензо[b]тиофен, 6-бензо[b]тиофен, 7-бензо[b]тиофен, 1-бензо[1,3]диоксол, 4-бензо[1,3]диоксол и 5-бензо[1,3]диоксол,
R5 выбирают из группы, включающей водород и R6,
R6 означает подгруппу общей формулы

где
R7 выбирают из группы, включающей водород или С1-С4алканоил, или R7 вместе с другим заместителем, выбранным из группы, включающей R8, R9, R10 и R11, образует 5- или 6-членный цикл с карбонильным мостиком или метиленовым мостиком, необязательно замещенным группой С1-С4алкил или С4-С5алкилен,
R8 выбирают из группы, включающей водород или С1-С4алканоил, или R8 вместе с другим заместителем, выбранным из группы, включающей R7, R9, R10 и R11, образует 5- или 6-членный цикл с карбонильным мостиком или метиленовым мостиком, необязательно замещенным группой С1-С4алкил или С4-С5алкилен,
R9 выбирают из группы, включающей водород или С1-С4алканоил, или R9 вместе с другим заместителем, выбранным из группы, включающей R7, R8, R10 и R11, образует 5- или 6-членный цикл с карбонильным мостиком или метиленовым мостиком, необязательно замещенным группой С1-С4алкил или С4-С5алкилен,
R10 выбирают из группы, включающей водород или С1-С4алканоил, или R10 вместе с другим заместителем, выбранным из группы, включающей R7, R8, R9 и R11, образует 5- или 6-членный цикл с карбонильным мостиком или метиленовым мостиком, необязательно замещенным группой С1-С4алкил или С4-С5алкилен,
R11 выбирают из группы, включающей водород или С1-С4алканоил, или R11 вместе с другим заместителем, выбранным из группы, включающей R7, R8, R9 и R10, образует 5- или 6-членный цикл с карбонильным мостиком или метиленовым мостиком, необязательно замещенным группой С1-С4алкил или С4-С5алкилен,
k равно 0 или 1,
l равно 0 или 1,
m равно 0 или 1,
n равно 0 или 1,
или их физиологически совместимые кислотно-аддитивные соли.
Кроме того, объектами изобретения являются фармацевтические композиции, включающие соединения формулы I. Кроме того, объектами изобретения являются способы получения соединений формулы I и промежуточных продуктов для получения соединений по указанным способам.
Подробное описание предпочтительных вариантов осуществления изобретения
Термин фармацевтические композиции, используемый в настоящем изобретении, означает фармацевтические композиции, включающие фармакологически эффективное количество соединения по настоящему изобретению и фармацевтические вспомогательные вещества и/или носители, обычно используемые в составе фармацевтических композиций.
Объектом изобретения являются новые соединения 3-цианонафталин-1-карбоновой кислоты и пергидроксиалкилметилпиперазина общей формулы I, указанной выше. Если заместители в соединениях формулы I означают галоген, то пригодными являются фтор, хлор или бром, а предпочтителен хлор. Подразумевается, что термин (гетеро)арил в описании настоящего изобретения включает радикалы арил и гетероарил.
В предпочтительном варианте настоящего изобретения R1 означает метил.
В другом предпочтительном варианте настоящего изобретения R2 и R3 каждый означает хлор.
В другом предпочтительном варианте настоящего изобретения R4 выбирают из группы, включающей 2-фуранил, 3-фуранил, 2-тиофен, 3-тиофен, фенил, бензил, 2-бензофуранил, 5-хлор-2-тиофен, 4-метилфенил, 3,4-метилендиоксифенил, 2-метоксифенил и 4-метоксифенил.
В другом предпочтительном варианте настоящего изобретения R4 выбирают из группы, включающей 2-фуранил, 3-фуранил, 2-тиофен и 3-тиофен.
В другом предпочтительном варианте настоящего изобретения R5 означает водород.
В другом предпочтительном варианте настоящего изобретения R7 и R11 каждый означает водород, k равно 1, а l, m, n каждый равен 0.
В другом предпочтительном варианте настоящего изобретения R7, R8 и R11 каждый означает водород, k и l каждый равен 1, а m и n каждый равен 0.
В другом предпочтительном варианте настоящего изобретения R7, R8, R9 и R11 каждый означает водород, k, l и m каждый равен 1, а n равен 0.
В другом предпочтительном варианте настоящего изобретения R7-R11 каждый означает водород, k, l и m каждый равен 1, а n равно 0.
В другом предпочтительном варианте настоящего изобретения хиральный центр *С находится в S конфигурации.
Если заместитель в подгруппе R6, включающей группы R7, R8, R9, R10 и R11, вместе с другим заместителем, выбранным из указанной группы, означает 5- или 6-членный цикл, содержащий метиленовый мостик, необязательно замещенный группой С1-С4алкил или С4-С5алкилен, прежде всего 5- или 6-членные циклы с метиленовым мостиком, то пригодными являются 1,1-диметилметилен, 1,1-спиро-тетраметиленметилен или 1,1-спиро-пентаметиленметилен. Соответствующие 5- или 6-членные карбонильные мостики можно рассматривать как циклические карбонаты, k предпочтительно равно 1, n предпочтительно равно 0. Таким образом, R6 предпочтительно означает необязательно замещенный радикал 1,2-диола, 1,2,3-триола или 1,2,3,4-тетрола. Атомы углерода, замещенные группами R8, R9, R10 и R11, представляют собой центры асимметрии и каждый из них может присутствовать в двух различных конфигурациях. Благодаря этому R7 может присутствовать в нескольких стереоизомерных формах. Наряду с соединениями формулы I, которые представляют собой смеси стереоизомерных форм по подгруппе R7, настоящее соединение включает соединения формулы I, в которых подгруппы R7 присутствуют в изомерно чистой форме. Предпочтительными подгруппами R7 являются ксило-1,2,3,4-тетрагидроксибутил, ликсо-1,2,3,4-тетрагидроксибутил, арабино-1,2,3,4-тетрагидроксибутил, трео-1,2,3-тригидроксипропил, эритро-1,2,3-тригидроксипропил и глицеро-1,2-дигидроксиэтил. Наиболее предпочтительные результаты получают при включении в состав молекулы углеводородов, выбранных из D-углеводородов, включающих главным образом подгруппы R7. Предпочтительны диастереоизомерно чистые подгруппы R7.
Более предпочтительны соединения формулы I выбирают из группы, включающей
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1R,2S)-1-(2-фурил)-2,3-дигидроксипропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
(2S,3R)-2-(ацетилокси)-3-{4-[(3S)-4-[3-циано-1-нафтоил)(метил)амино]-3-(3,4-дихлорфенил)бутил]пиперазин-1-ил}-3-(2-фурил)пропилацетат,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[1-(2-фурил)-2-гидроксиэтил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1R,2S,3R,4R)-1-(2-фурил)-2,3,4,5-тетрагидроксипентил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1R,2S,3S,4R)-1-(2-фурил)-2,3,4,5-тетрагидроксипентил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1S,2S,3S,4R)-2,3,4,5-тетрагидрокси-1-(3-тиенил)пентил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1S,2S,4R,4R)-2,3,4,5-тетрагидрокси-1-(3-тиенил)пентил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[1-(2-фурил)-2-гидрокси-1-(гидроксиметил)этил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[1-(2-фурил)-2-гидрокси-1-(гидроксиметил)этил]пиперазин-1-ил}бутил]-R-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1S,2S)-2,3-дигидрокси-1-(3-тиенил)пропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1R,2S)-2,3-дигидрокси-1-(2-тиенил)пропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(S)-[(4S)-2-оксо-1,3-диоксолан-4-ил](3-тиенил)метил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-(4-{(R)-2-фурил[(4S)-2-оксо-1,3-диоксолан-4-ил]метил}пиперазин-1-ил)бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1S,2S)-1-(3-фурил)-2,3-дигидроксипропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[1-(2-фурил)-2,3-дигидроксипропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1S,2S)-2,3-дигидрокси-1-фенилпропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2)-2-(3,4-дихлорфенил)-4-{4-[(1S,2S)-2,3-дигидрокси-1-(4-метоксифенил)пропил]пиперазин-1-ил}бутил]-метил-1-нафтамид,
N-[(2S)-4-{4-[(1R,2S)-1-(1-бензофуран-2-ил)-2,3-дигидроксипропил]пиперазин-1-ил}-2-(3,4-дихлорфенил)бутил]-3-циано-N-метил-1-нафтамид,
N-[(2S)-4-(4-[(1R,2S)-1-(5-хлор-2-тиенил)-2,3-дигидроксипропил]пиперазин-1-ил}-2-(3,4-дихлорфенил)бутил]-3-циано-N-метил-1-нафтамид,
N-[(2S)-4-{4-[(1S,2S)-1-(1,3-бензодиоксол-5-ил)-2,3-дигидроксипропил]пиперазин-1-ил}-2-(3,4-дихлорфенил)бутил]-3-циано-N-метил-1-нафтамид и
N-[(2S)-4-{4-[(1R,2S)-1-(1-бензотиен-2-ил)-2,3-дигидроксипропил]пиперазин-1-ил}-2-(3,4-дихлорфенил)бутил]-3-циано-N-метил-1-нафтамид.
Способ 1
Соединения по настоящему изобретению получают по реакции соединения формулы II
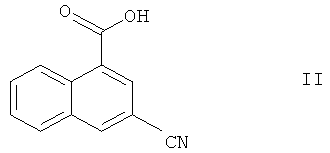
с хлор-содержащим реагентом, предпочтительно с оксалилдихлоридом, с образованием соединения формулы III

Соединение формулы III вводят в реакцию с соединением общей формулы IV

с образованием соединения общей формулы V
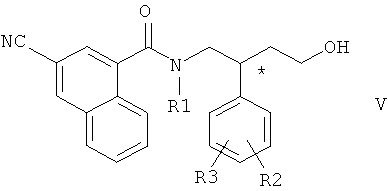
где R1, R2 и R3 имеют значения, указанные выше. Соединение общей формулы V вводят в реакцию с метансульфонилхлоридом с образованием соединения общей формулы VI

где R1, R2 и R3 имеют значения, указанные выше. Соединение общей формулы VI сначала вводят в реакцию с галогенидом щелочного металла MX, где М означает щелочной металл, предпочтительно натрий, а Х означает галоген, предпочтительно иод, а затем вводят в реакцию с соединением общей формулы XIX

где SG означает отщепляемую защитную группу, предпочтительно трет-бутоксикарбонил, с образованием соединения общей формулы VIa,

где R1, R2 и R3 имеют значения, указанные выше. Соединение общей формулы VIa гидролизуют в кислотной среде с образованием соединения общей формулы VII
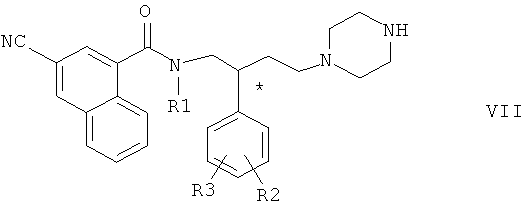
где R1, R2 и R3 имеют значения, указанные выше. Соединение общей формулы VII вводят в реакцию с соединением общей формулы VIII

и соединением общей формулы IX

с образованием соединения общей формулы I, которое необязательно превращают в его физиологически совместимую кислотно-аддитивную соль, где R1, R2, R3, R4, R5 и R6 имеют значения, указанные выше.
Способ 2
Соединения по настоящему изобретению можно также получить по реакции соединения общей формулы Х

с соединением общей формулы VIII

и с соединением общей формулы IX

с образованием соединения общей формулы XI
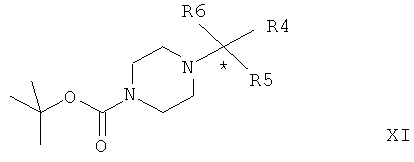
где R4, R5 и R6 имеют значения, указанные выше. Затем соединение общей формулы XI гидролизуют в кислотной среде с образованием соединения общей формулы XII
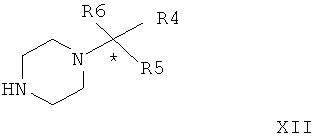
где R4, R5 и R6 имеют значения, указанные выше. Соединение общей формулы XII вводят в реакцию с соединением общей формулы XIII

с образованием соединения общей формулы XIV

где R1, R2, R3, R4, R5 и R6 имеют значения, указанные выше. Затем соединение общей формулы XIV гидролизуют в кислотной среде с образованием соединения общей формулы XV

где R1, R2, R3, R4, R5 и R6 имеют значения, указанные выше. Затем соединение общей формулы XV вводят в реакцию с соединением формулы III с образованием соединения общей формулы I, которое необязательно превращают в его физиологически совместимую кислотно-аддитивную соль, где R1, R2, R3, R4, R5 и R6 имеют значения, указанные выше.
Способ 2 можно модифицировать за счет того, что соединение общей формулы XII

вводят в реакцию с соединением общей формулы XVI

с образованием соединения общей формулы XIV, где R1, R2, R3, R4, R5 и R6 имеют значения, указанные выше. Затем соединение общей формулы XVI

модифицируют, как описано выше.
Способ 3
Соединения по настоящему изобретению можно также получить по реакции соединения общей формулы II

с хлор-содержащим реагентом с образованием соединения формулы III

Затем соединение формулы III вводят в реакцию с соединением общей формулы IV

с образованием соединения общей формулы V

Соединение общей формулы V окисляют с образованием соединения общей формулы VI
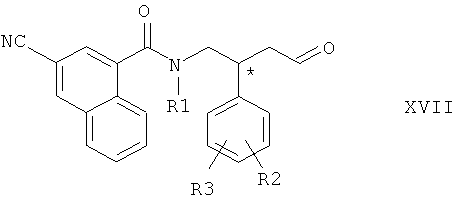
Соединение общей формулы XVII вводят в реакцию с соединением общей формулы XII

с образованием соединения общей формулы I, которое необязательно превращают в его физиологически совместимую кислотно-аддитивную соль.
В способах I и III, соответственно, реакцию, в которой соединение общей формулы VII или X, соответственно, взаимодействует с соединением общей формулы VIII и IX с образованием соединения общей формулы I, проводят в известных условиях реакции бороновых кислот Манниха (см., например, N.A. Petasis и др., Journal of the American Chemical Society, 120, 11798-11799 (1998), WO 98/00398 или WO 00/24510). Соответственно, соединение формулы VII или Х можно вводить в реакцию в одном реакторе с бороновой кислотой формулы VIII и углеводом формулы IX, необязательно защищенным пригодными защитными группами, в растворителе, который является инертным в условиях проведения реакции. Пригодные защитные группы углеводов известны в данной области, см., например, J.A.W. McOmie, "Protective Groups in Organic Chemistry", Plenum Press (1973), или T.W. Green, P.G. Wuts," Protective Groups in Organic Synthesis", Wiley and Sons (1999). Пригодными растворителями являются диполярные протонные органические растворители, такие как низшие спирты, например С1-С4Спирты с прямой или разветвленной цепью, предпочтительно этанол, или смеси вышеуказанных растворителей с водой или диполярными апротонными растворителями, такими как галоген(низш.)алканы, предпочтительно дихлорметан. Реакцию проводят при температуре от комнатной температуры до температуры кипения растворителя или смеси растворителей. В этом способе синтеза предпочтительно последовательно комбинируют соединения формул VII, X, VIII и IX. Аналогичным образом можно также на первой стадии комбинировать соединение формулы VII с соединением формулы IX, а затем с соединением формулы VII или X. Подгруппы R4, R5 и R6, включающие хиральный центр, образовавшиеся в результате такой конденсации в соединении формулы I, обычно обеспечивают получение "анти" продукта с высокой степенью диастереоспецифичности.
Соединения формулы I, содержащие в подгруппе R6 по меньшей мере одну свободную гидроксильную группу, при необходимости можно затем ввести в реакцию с карбоновыми кислотами R12COOH формулы XVII, где R12 означает C1-С3алкил с прямой или разветвленной цепью, с целью ацилирования свободных гидроксигрупп в подгруппе R6. Обычно при этом происходит перацилирование свободных гидроксигрупп в подгруппе R6. В качестве ацилирующих агентов используются кислоты формулы XVII или их реакционноспособные производные. Пригодными реакционноспособными производными являются прежде всего ангидриды и галогенангидриды карбоновых кислот. Ацилирование проводят в органическом растворителе, который является инертным в условиях проведения реакции, предпочтительно при температуре от -20°С до комнатной температуры. Пригодными растворителями являются прежде всего ароматические углеводороды, такие как бензол или толуол, циклические или алифатические ди(низш.)алкиловые эфиры, такие как диэтиловый эфир, тетрагидрофуран (ТГФ) или диоксан, частично галогенированные (низш.)углеводороды, такие как дихлорметан, или смеси указанных растворителей. Если в качестве ацилирующего агента используется ангидрид и галогенангидрид карбоновой кислоты формулы XVII, ацилирование проводят в присутствии связывающего кислоту реагента. Пригодными реагентами являются ненуклеофильные органические основания, растворимые в реакционной смеси, такие как пиридин, триэтиламин или 4-диметиламинопиридин. Органические основания, которые используются в избытке, могут также выполнять функцию растворителя.
Соединения формулы I, содержащие в подгруппе R6 по меньшей мере две свободных гидроксильных группы, при необходимости после их получения, как описано выше, вместо реакции с соединением формулы XVII можно также ввести в реакцию с реакционноспособным карбонилирующим соединением, при этом происходит карбонилирование подгруппы R6. Реакцию проводят в известных условиях. Например, соединение формулы I вводят в реакцию в органическом растворителе, который является инертным в условиях проведения реакции. Пригодными реакционноспособными карбонилирующими соединениями являются, например, фосген или подобные ему карбонилирующие реагенты, такие как бис(трихлорметил)карбонат (трифосген), трихлорметилхлорформиат (дифосген) или прежде всего карбонилдиимидазол. В реакционную смесь обычно добавляют реагент, связывающий кислоту. Пригодными реагентами являются реагенты, указанные выше для реакции соединения формулы I с соединением формулы XVII. Реакцию обычно проводят при температуре от приблизительно -20°С до комнатной температуры.
Соединения формулы I, содержащие в подгруппе R6 по меньшей мере две свободных гидроксильных группы, при необходимости после их получения, как описано выше, вместо реакции с соединением формулы XVII или вместо реакции с реакционноспособным карбонилирующим соединением, можно также модифицировать по реакции с ди(низш.)алкилкетоном или C5-С6циклоалкилкетоном в подгруппе R6 с образованием 5-6-членного циклического производного, включающего мостиковую метиленовую группу, необязательно замещенную группой (низш.)алкил, или С4-С5алкилен. В качестве ди(низш.)алкилкетона предпочтительно используют ацетон. В качестве C5-Сбциклоалкилкетонов предпочтительно используют циклопентанон и циклогексанон.
Если необходимо получить соединения формулы I, в которых заместители, присутствующие в подгруппе R6, R7, R8, R9, R10 и/или R11, не означают водород, в качестве исходного соединения предпочтительно используют углеводородные соединения формулы IX, содержащие свободные гидроксильные группы по меньшей мере в α-положении к альдегидной группе. Предпочтительно в качестве исходных соединений следует использовать соединения формулы IX, где R7, R8, R9, R10 и R11 означают водород. При необходимости свободные гидроксильные группы можно ацилировать, карбонилировать или вводить в реакцию с пригодным кетоном, как указано выше.
Соединения формулы VII являются новыми соединениями, которые прежде всего пригодны в качестве промежуточных продуктов для получения новых активных соединений, например для получения соединений формулы I, которые являются антагонистами рецепторов тахикинина.
Соединения формулы VII можно получить по реакции соединения общей формулы VI

где R2 и R3 имеют значения, указанные выше, с галоидом щелочного металла MX, где М означает щелочной металл, предпочтительно натрий, а Х означает галоген, предпочтительно иод, и защищенным производным пиперазина общей формулы XIX

где SG означает отщепляемую защитную группу, прежде всего трет-бутоксикарбонил, с образованием соединения общей формулы VIa, при последующем отщеплении защитной группы SG известным способом, с образованием соединения общей формулы VII. Реакцию проводят в органическом растворителе, инертном в условиях проведения реакции, таком как ароматический углеводород, прежде всего толуол, или в циклическом или алифатическом ди(низш.)алкиловом эфире, прежде всего ТГФ, или предпочтительно в смеси вышеуказанных растворителей, и в присутствии основания. Пригодными основаниями являются ненуклеофильные органические азотистые основания, такие как трет-(низш.)алкиламины, например триэтиламин. Реакцию проводят при температуре от 50°С до 100°С, предпочтительно приблизительно от 70°С до 90°С.
Соединения формулы VI можно получить по реакции соединения общей формулы V

где R1, R2 и R3 имеют значения, указанные выше, с метансульфонилхлоридом. Соединения формулы VI и их стереоизомерные формы являются известными соединениями, например описаны в ЕР 0474561 А1, и их можно получить способами, описанными в указанных документах или аналогичными способами.
Соединения формулы XIII можно получить по реакции соединения общей формулы IV
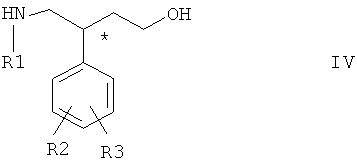
с трет-бутилоксикарбонилангидридом с образованием соединения общей формулы XX

где R1, R2 и R3 имеют значения, указанные выше. Затем соединения общей формулы XX вводят в реакцию с метансульфонилхлоридом с образованием соединения общей формулы XXI
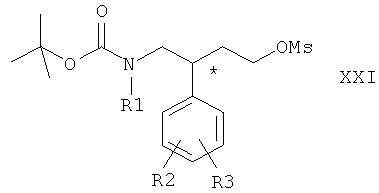
где R1, R2 и R3 имеют значения, указанные выше. Затем соединения общей формулы XXI вводят в реакцию с галоидом щелочного металла MX, где М означает щелочной металл, предпочтительно натрий, а Х означает галоген, предпочтительно иод, с образованием соединения общей формулы XIII
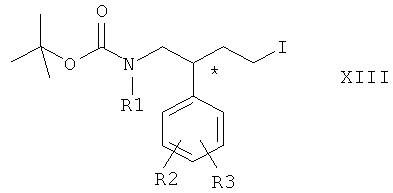
где R1, R2 и R3 имеют значения, указанные выше.
Соединение общей формулы XVI можно получить при окислении соединения XX любым известным способом, например, диметилсульфоксидом, активированным оксалилхдоридом (окисление по Сверну).
Соединения формул VIII, IX и XIX известны или специалист в данной области может их получить из известных соединений известными методами. Соединения формулы IX, которые являются предпочтительными, включают D-ксилозу, D-ликсозу, D-арабинозу, D-треозу, D-эритрозу и D- и L-глицеральдегид.
Соединения формулы I можно выделить из реакционной смеси и очистить известным способом. Кислотно-аддитивные соли можно превратить в свободные основания обычным способом, и из оснований при необходимости можно получить физиологически совместимые кислотно-аддитивные соли. Физиологически совместимые соли соединений формулы I представляют собой обычные соли неорганических кислот, например серной кислоты, фосфорной кислоты или галогенводородных кислот, предпочтительно соляной кислоты, или органических кислот, например (низш.)алифатических монокарбоновых, дикарбоновых или трикарбоновых кислот, таких как малеиновая кислота, фумаровая кислота, молочная кислота, винная кислота, лимонная кислота, или сульфоновых кислот, например (низш.)алкансульфоновых кислот, таких как метансульфоновая кислота или трифторметансульфоновая кислота, или бензолсульфоновые кислоты, необязательно замещенные в бензольной цикле группой галоген или (низш.)алкил, такие как пара-толуолсульфоновая кислота.
Соединения формулы I содержат в α-положении к атому азота в положении 4 пиперазинового цикла асимметрический атом углерода, а именно атом углерода *С, к которому присоединен фенильный цикл, замещенный группами R2 и R3. Благодаря присутствию указанного асимметрического атома углерода и присутствию асимметрического атома углерода, к которому присоединены подгруппы R4, R5 и R6, и необязательно благодаря присутствию асимметрических атомов углерода в подгруппе R6, соединения формулы I могут присутствовать с нескольких стереоизомерных формах. Настоящее изобретение включает как смеси оптических изомеров, так и изомерно чистые соединения формулы I. Предпочтительны соединения формулы I, в которых атом углерода *С, к которому присоединен фенил, замещенный группами R2 и R3, находится в S-конфигурации. Если в синтезе соединения формулы I используются смеси оптических изомеров исходного соединения, например соединения формулы VII или соединения формулы IX, то соединения формулы I также образуются в форме смесей оптических изомеров. Если в синтезе используются индивидуальные изомеры исходного соединения, то соединения формулы I также образуются в стереохимически индивидуальной форме. Стереохимически индивидуальные формы соединения формулы I можно получить из смеси оптических изомеров известным способом, например хроматографией на хиральных материалах или по реакции с пригодной оптически чистой кислотой, например винной кислотой или 10-камфорсульфоновой кислотой, и последующим разделением на их оптически активные антиподы фракционной кристаллизацией полученных диастереомерных солей.
Соединения формулы I и их кислотно-аддитивные соли обладают антагонистическим действием на рецепторы тахикинина и, следовательно, могут использоваться для лечения патологических состояний у крупных млекопитающих, прежде всего человека, при которых передача сигнала производится с участием тахикининов. Группа соединений по изобретению характеризуется благоприятным профилем действия, т.е. указанные соединения обладают высокоселективным сродством к рецепторам NK1 и NK2. Кроме того, группа соединений по изобретению характеризуется высокой совместимостью при продолжительном введении и высокой доступностью при пероральном введении. Благодаря благоприятному профилю действия соединения формулы I прежде всего пригодны для подавления процессов, в которых принимают участие тахикинины, такие как нейрокинин А, которые связываются с рецепторами NK1 и NK2. Благодаря действию, которое преимущественно направлено на периферические области, соединения формулы I прежде всего пригодны для лечения и/или профилактики респираторных заболеваний, прежде всего астмы, бронхита, кашля и ринита, кожных заболеваний, прежде всего воспалительных кожных реакций, аллергических кожных реакций и псориаза, артропатических заболеваний, прежде всего артрита, васкулитов и системной красной волчанки, функциональных или воспалительных нарушений в желудочно-кишечном тракте, прежде всего псевдомембранозного колита и диареи, буллезных заболеваний, таких как цистит и интерстициальный цистит, и мигрень, у крупных млекопитающих, прежде всего человека обоих полов, включая также заболевания, которые связаны с повышенной чувствительностью к боли и/или с задержкой стула в отделе ободочной кишки. Функциональные нарушения в желудочно-кишечном тракте, которые излечиваются соединениями по изобретению, включают прежде всего нарушения в нижних отделах кишечника, известные под названием "синдром раздраженного кишечника" (IBS). Типичные симптомы для диагностики IBS описаны, например, в статьях W.G. Thompson и др., Gastroenterology International, 2, 92-95 (1989) или W.G. Thompson и др., GUT, 45/11, II43-II47 (1999), и известны специалистам под названием "Rome Criteria". Соответственно, главные симптомы IBS включают боли в нижних отделах кишечника, которые возникают благодаря гиперчувствительности висцеральной афферентной нервной системы и аномалиям в подвижности кишечника, таким как запор, диарея или чередованием запора и диареи. Другими воспалительными нарушениями в желудочно-кишечном тракте, на которые оказывает лечебное действия группа соединений по изобретению, являются, например, воспалительные нарушения в области тонкого и толстого кишечника, известные под названием "воспалительное заболевание кишечника" (IBD), например язвенный колит или болезнь Крона. Кроме того, благодаря механизму действия соединения по изобретению пригодны для лечения других нарушений, при которых тахикинины и прежде всего нейрокинин А принимают участие в качестве агентов передачи сигнала. Указанные нарушения включают, например, нейрогенные воспаления, воспалительные заболевания суставов, такие как ревматоидный артрит, приступы астмы, аллергические нарушения, нарушения иммунной регуляции, воспаление мочевого пузыря, а также функциональная диспепсия.
Описание методов фармакологических испытаний
Номера соединений формулы I, использованных при проведении указанных ниже фармакологических испытаний, соответствуют примерам получения соединений, описанным ниже.
1. Определение связывания анализируемых соединений с рецепторами NK1 in vitro
В Нидерландах сродство анализируемых соединений к рецепторам NK1 человека оценивали in vitro. Ингибирование связывания физиологического нейрокинина (вещества Р) с рецепторами нейрокинина-1 определяли в Нидерландах, (ред).
Исследование связывания проводили с использованием в качестве лиганда [3Н]-вещества Р. Для анализа связывания различные образцы мембранных препаратов клеток СНО (клетки яичника китайского хомячка, ооциты китайского хомячка), экспрессирующих рецептор NK1 человека ("кат.номер" соответствующей нуклеотидной последовательности М74290, "кат.номер" соответствующей аминокислотной последовательности Р25103, см. статью Takeda Y., Chou K.В., Takeda J., Sachais B.S. и Krause J.E, Biochemical and Biophysical Research Communications, 179(3), 1232-1240 (1991)), инкубировали в присутствии меченого лиганда в реакционной смеси, не содержащей анализируемое соединение, или содержащей различные концентрации анализируемого соединения. Затем в каждом образце отделяли несвязанный лиганд фильтрованием на стекловолоконном фильтре, остаток на фильтре несколько раз промывали буферным раствором и измеряли радиактивность остатка на фильтре с использованием β-сцинтилляционного счетчика.
Для соединений, описанных в примерах 1-14, определяли концентрацию, при которой связывание меченого лиганда ингибируется на 50% от максимального значения и представляли в виде величины IC50, характеризующей анализируемое соединение. Затем рассчитывали соответствующую константу ингибирования (Ki) анализируемого соединения, которую представляли в виде отрицательного логарифма ki(pKi). Величина pKi отражает степень сродства анализируемых соединений к рецепторам NK1 человека. В указанной модели испытаний анализируемые соединения характеризуются величинами pKi, указанными в таблице 1.
В указанной модели испытаний все вышеуказанные анализируемые соединения характеризуются величинами pKi по меньшей мере 7,0. Соединения, описанные в примерах 1-14, характеризуются величинами pKi по меньшей мере 7,9.
2. Определение связывания анализируемых соединений к рецепторам NK2 in vitro
Сродство анализируемых соединений с рецепторами NK2 человека оценивали in vitro. Сродство анализируемых соединений определяли по конкуренции связывания с антагонистом SR 48968 (саредутант), селективным в отношении рецептора NK2, который использовали в качестве стандартного лиганда.
Исследование связывания проводили с использованием в качестве
радиоактивно меченного лиганда соединения [3H]-SR 48968 (фирма Amersham). Для анализа связывания различные образцы мембранных препаратов клеток СНО (клетки яичника китайского хомячка, ооциты китайского хомячка), экспрессирующих рецептор NK2 человека (получение см. N.P. Gerard и др., Journal of Biological Chemistry, 265/33, 20455-20462 (1990)), инкубировали в течение 90 мин в присутствии меченого лиганда в реакционной смеси, не содержащей анализирумое соединение, или содержащей различные концентрации анализирумого соединения. Затем в каждом образце отделяли несвязанный лиганд фильтрованием, остаток на фильтре несколько раз промывали буферным раствором и измеряли радиоактивность остатка на фильтре с использованием сцинтилляционного счетчика.
Концентрацию, при которой наблюдается ингибирование связывания меченого лиганда на 50% от максимального значения, представляли в виде величины IC50, характеризующей анализируемое соединение. Затем по величине IC50 рассчитывали соответствующую константу ингибирования (Ki) анализируемого соединения, которую представляли в виде отрицательного логарифма ki(pKi).
Для соединений, описанных в примерах 1-14, сродство к рецепторам NK2 человека в каждом случае определяли по меньшей мере при трех повторах в интервале концентраций анализируемых соединений от 10-6 до 10-10 моль/л. Если проводили несколько измерений, то каждый раз определяли среднее значение. Величина pKi отражает степень сродства анализируемых соединений к рецепторам NK2 человека. В указанной модели испытаний анализируемые соединения характеризуются величинами pKi, указанными в таблице 2.
В указанной модели испытаний все вышеуказанные анализируемые соединения характеризуются величинами pKi по меньшей мере 7,0. Соединения, описанные в примерах 1-14, характеризуются величинами pKi по меньшей мере 6,9.
3. Определение функционального антагонизма анализируемых соединений в отношении рецептора NK1 на изолированной ткани морских свинок in vitro
В Нидерландах антагонистическое действие анализируемых соединений в отношении рецепторов NK1 измеряли in vitro на изолированных кольцевых препаратах аорты морских свинок (Pirbright-White), содержащихся в оксигенированном питательном растворе. При этом определяли ингибирование анализируемыми соединениями релаксации тонуса препаратов аорты после стимулирования веществом Р (агонистом NK1).
Для измерения сокращения мышц сосудов препараты фиксировали на крючке, соединенном нитью с динамометром, и в каждом случае сокращения регистрировали на самописце. Препараты аорты тонизировали фенилэфрином. Затем до и после введения анализирумого соединения стимулировали рецепторы NK1 препаратов аорты при добавлении 0,01 ммоль вещества Р, которое вызывало релаксацию тонуса. Релаксацию до и после введения анализируемых соединений рассчитывали в процентах. Затем рассчитывали эффективную концентрацию, обеспечивающую ингибирование релаксации тонуса на 50% от максимума (ЕС50). Результаты представляли в виде отрицательного логарифма ЕС50 (рЕС50). Величина рЕС50 является мерой функциональной эффективности действия анализируемых соединений на рецепторы NK1. В указанной модели испытаний анализируемые соединения характеризуются величинами рЕС50, указанными в таблице 3.
4. Определение функционального антагонизма анализируемых соединений на изолированной ткани морских свинок in vitro
Антагонистическое действие анализируемых соединений в отношении рецепторов NK2 измеряли in vitro на изолированных препаратах желчного пузыря морских свинок (Pirbright-White), содержащихся в насыщенном кислородом питательном растворе. Для этого препараты с одной стороны закрепляли в фиксаторах органа в питательном растворе и с другой стороны соединяли с динамометром.
В указанном испытании рецепторы NK2, присутствующие в препаратах желчного пузыря, стимулировали природным агонистом рецептора NK2 нейрокинином A (NKA, 0,1 мкмоль/л), сокращение препаратов измеряли и представляли в виде сократительной способности в мН (предварительная оценка). Затем NKA в препаратах отмывали раствором, не содержащим NKA, и добавляли анализируемые соединения в концентрации 10-7 моль/л. Через 2 ч инкубации препаратов с анализируемыми соединениями измеряли сокращения, вызываемые новой порцией NKA, и полученные результаты представляли в процентах относительно первоначально измеренного сокращения, вызываемого добавлением только NKA. Концентрацию анализируемых соединений в последующих экспериментах увеличивали в несколько раз в логарифмической или полулогарифмической шкале до определения по меньшей мере одной концентрации, вызывающей приблизительно (выше или ниже) 50% ингибирование сокращения (вплоть до 10-5 моль/л). Для каждой концентрации рассчитывали среднее значение ингибирования сокращения для 2-4 препаратов. В каждом случае рассчитывали концентрацию анализирумого соединения, вызывающую 50% ингибирование от максимальной величины (IC50). В каждом случае результаты представляли в виде логарифма IC50 анализирумого соединения, т.е. в виде pIC50 (моль/л). В указанной модели испытаний анализируемые соединения характеризуются величинами pIC50, указанными в таблице 4.
5. Функциональные испытания антагонизма в отношении NK1 и NK2 на клетках
Функциональные испытания антагонистического действия соединений по настоящему изобретению на рецепторы тахикинина в организме человека проводили с использованием клеток СНО, экспрессирующих рекомбинантный рецептор NK1 или NK2 человека. В указанных испытаниях определяли ингибирование лиганд-индуцированного повышения мобилизации внутриклеточного кальция и ингибирование лиганд-индуцированного фосфорилирования МАРK, которые можно использовать для оценки функциональной активности антагонистов тахикинина. Кроме того, для сравнения характеризовали антагонистические свойства стандартных соединений на различные рецепторы тахикинина.
Действие анализируемых оценивали с использованием фибробластов яичника китайского хомячка (СНО), стабильно экспрессирующих клонированные рецепторы NK1 или NK2 человека. Рецептор NK сопряжен с Gq белком. Активация Gq белка при связывании рецептора с лигандом приводит к мобилизации внутриклеточного кальция и фосфорилированию МАРK. Для определения функционального действия анализируемых соединений использовали обе системы анализа.
Измерение уровня Са2+ с использованием анализа FLIPR для определения активности NK1 и NK2
За 24 ч до проведения эксперимента клетки высевали в черные 96-луночные микропланшеты с плотностью 2,2×104 клеток/лунка. Все стадии эксперимента проводили в стерильных условиях. Для наблюдения за изменениями уровня внутриклеточного кальция клетки нагружали кальций-чувствительным красителем FLUO-4 (фирма Molecular Probes), который характеризуется поглощением при 488 нм и испусканием в области 500-560 нм только в виде комплекса с кальцием. Для этого питательную среду удаляли из лунок, не нарушая конфлюентного сплошного слоя клеток, и в каждую лунку добавляли 100 мкл среды, содержащей краситель (HBSS, 4 мкМ FLUO-4, 0,005% (мас./об.) плюроновая кислота, 2,5 мМ пробенецид, 20 мМ HEPES, рН 7,4) с использованием автоматической пипетки (Multidrop, фирма Labsystems). Плюроновую кислоту добавляли для повышения растворимости красителя и захвата клетками, а пробенецид, ингибитор анионообмена, добавляли в среду для усиления удерживания красителя в клетках. Клетки инкубировали в инкубаторе в атмосфере 5% СО2 при 37°С в течение 40 мин. После захвата красителя клетки трижды промывали буферным раствором для промывки (HBSS, 2,5 мМ пробенецид, 20 мМ HEPES, рН 7,4) для снижения фоновой флуоресценции. Последнюю порцию буферного раствора удаляли и заменяли на 100 мкл свежего буферного раствора для промывки. Для анализа антагонистического действия в лунки добавляли по 50 мкл анализируемого соединения (при конечной концентрации от 10 мкМ до 1,4 нМ) и через 7 мин добавляли вещество Р (при конечной концентрации 10-8 М, агонист NK1) или NKA (при конечной концентрации 10-7 М, агонист NK2). Параметры сканирования в системе FLIPR составляют: продолжительность экспозиции 0,4 с, фильтр 1, объем образца 50 мкл, высота автоматической пипетки 125 мкл, скорость диспергирования 40 мкл/с без перемешивания. Максимальные изменения флуоресценции получали с использованием статистической функции программного обеспечения FLIPR, а данные наносили на график с использованием графопостроителя GraphPad Prism 4. Все точки представляли в виде процента ингибирования действия контрольного агониста. Величины IC50 определяли с использованием сигмоидного графика доза/ответ. Эффективность действия антагониста (рА2) рассчитывали по уравнению:
pA2=-log(IC50/(1+[L]/EC50)),
где IC50 анализируемого соединения определяли по графику зависимости концентрация/ответная реакция, [L] означает концентрацию агониста (вещество Р для NK1, NKA для NK2), a EC50 означает эффективность действия агониста на соответствующий клонированный NK рецептор человека (для вещества Р величина EC50=10-9.6 М, для NKA величина EC50=10-8.8 М). Полученные результаты суммированы в таблице 5.
6. Определение эффективности антагонистического действия анализируемых соединений на рецепторы NK-1 и NK-2 in vivo
Антагонистическую активность анализируемых соединений в отношении рецепторов NK-1 и NK-2 исследовали с использованием анестезированных морских свинок в каждом случае при внутривенном и пероральном введении in vivo. Указанная модель испытаний позволяет одновременно детектировать у животного оба антагонистических действия на NK-2 в трех различных органах (дыхательные пути, ободочная кишка и кровоток) и на NK-1 (быстрое падение кровяного давления).
Морских свинок (Pirbright-White, масса тела 500-700 г) анестезировали кетамином/ксилазином (67/13 мг/кг подкожно, первоначальная доза, затем дозы вводили при необходимости). Животным вводили внутривенный катетер для доставки соединения и внутриартериальный катетер для измерения кровяного давления. Животных подвергали искусственной вентиляции легких через трахеальную трубочку и регистрировали респираторное давление с использованием датчика давления. В дистальную ободочную кишку животных вводили баллон для манометрической регистрации подвижности ободочной кишки с использованием датчика давления. У каждого животного непрерывно регистрировали на самописце и на компьютере кровяное давление, частоту сердечных сокращений, респираторное давление и давление в ободочной кишке. Для стимуляции рецепторов NK-1 и NK-2 животным вводили нейрокинин А (NKA, 200 пмоль/животное, внутривенно в виде болюсного вливания). Введение NKA приводит к значительному увеличению респираторного давления (бронхостеноз) и давления в ободочной кишке и к двухфазному снижению кровяного давления. Первая фаза гипотензии (фаза максимальной гипотензии в первую минуту после введения NKA) опосредуется рецепторами NK-1, поскольку они полностью блокируются специфичными антагонистами рецептора NK-1. С другой стороны, вторая фаза замедленной гипотензии (фаза максимальной гипотензии через 2-5 мин) опосредуется рецепторами NK-2, поскольку они блокируются специфичными антагонистами рецептора NK-2. Дозы анализируемых соединений приводятся в виде значений ED50, которые в каждом случае снижают ответную реакцию на стимуляцию NKA на 50% от первоначального значения, что является характеристическими показателями для индивидуального измерения параметров бронхостеноза, давления в ободочной кишке и изменения кровяного давления, опосредованных NK-1 или NK-2.
Антагонистическое действие анализируемых соединений сначала исследовали по кумулятивной схеме, где промежуток между введением стимулирующей дозы NKA и завершением введения соответствующих доз анализируемых соединений составлял 1 мин. Указанные значения ED50, полученные по графикам кумулятивная доза/ответ, приводятся в таблице 6.
Данные, приведенные выше в таблице 6, свидетельствуют о том, что соединения 1, 2 и 6-11 после кумулятивного введения внутривенно (детектирование антагонизма через 1 мин после завершения введения анализирумых соединений) благодаря антагонистическому действию на рецептор NK-1 заметно воздействуют на раннюю гипотензию, а также за счет антагонистического действия на рецептор NK-2 влияют на подвижность ободочной кишки, снижение кровяного давления и сопротивление дыханию.
Для дополнительного исследования антагонистического действия анализируемых соединений в зависимости от времени определяли действие стимула NKA через разные промежутки времени (1, 30, 60, 90, 120, 150 и 180 мин) после перорального введения анализируемых соединений. Затем антагонистическое действие анализируемых соединений через определенное время после перорального введения анализируемых соединений (1-180 мин после введения) определяли в виде "величины площади под фармакокинетической кривой" (AUC) и полученные значения ED50 представляли в таблице 7.
Соединения по изобретению, прежде всего соединения 1 и 2, приведенные в таблице 7, обладают антагонистическим действием на рецепторы NK2 и NK1 при пероральном введении.
Соединения формулы I можно вводить в виде стандартных лекарственных форм. Дозы могут изменяться индивидуально и в зависимости от типа патологического состояния, подлежащего лечению, и используемого соединения. Однако в общем случае, для введения человеку или крупному млекопитающему пригодными являются лекарственные формы, содержащие в одной дозе от 0,2 до 200 мг, прежде всего от 1 до 50 мг, активного соединения. Твердые или жидкие лекарственные формы могут включать соединения по изобретению в смеси со стандартными фармацевтическими вспомогательными веществами и/или носителями. Примерами твердых лекарственных форм, которые можно вводить пероральным способом, являются таблетки, таблетки с покрытием, капсулы, порошки иди гранулы, или в другом варианте суппозитории. Указанные препараты могут содержать стандартные фармацевтические неорганические и/или органические носители, такие как тальк, лактоза или крахмал, а также стандартные фармацевтические вспомогательные вещества, например замасливатели или дезинтегрирующие агенты для таблеток. Жидкие препараты, такие как суспензии или эмульсии активных соединений, могут содержать обычные разбавители, такие как вода, масла и/или суспендирующие агенты, такие как полиэтиленгликоли и т.п. Кроме того, препараты могут включать другие добавки, такие как консерванты, ароматизаторы и т.п.
Активные соединения смешивают и перерабатывают с фармацевтическими добавками и/или носителями обычным способом. Для получения твердых лекарственных форм активные соединения смешивают с добавками и/или носителями обычным способом и проводят влажную или сухую грануляцию. Гранулы или порошки непосредственно помещают в капсулы или прессуют с образованием ядер таблеток, на которые при необходимости наносят покрытие.
Изобретение иллюстрируется следующими примерами, не ограничивающими его объем.
Пример 1
3-Циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1R,2S)-1-(2-фурил)-2,3-дигидроксипропил]пиперазин-1-ил}бутил]-Н-метил-1-нафтамид (способ 1)
А) 58,0 г 3-цианонафталин-1-карбоновой кислоты (формула II) суспендировали в 600 мл дихлорметана, а затем при перемешивании добавляли 2 мл ДМФА. В полученную суспензию медленно добавляли 35 мл оксалилдихлорида в 65 мл дихлорметана и смесь перемешивали при температуре от 30°С до 40°С в течение 4 ч. Полученный раствор упаривали досуха, при этом получали 67 г 3-цианонафталин-1-карбонилхлорида (формула III), который хранили в холодильнике и использовали без дополнительной очистки.
B) 20 г 3S-(3,4-Дихлорфенил)-4-метиламинобутан-1-ола (формула IV) суспендировали при перемешивании в 200 мл ТГФ при комнатной температуре. 12 г КОН растворяли в 100 мл воды, в полученный раствор добавляли суспензию 17,2 г 3-цианонафталин-1-карбонилхлорида (формула III, стадия А) и смесь перемешивали в течение 3 ч. Органический растворитель удаляли, в остаток добавляли этилацетат и метил-трет-бутиловый эфир. Водную фазу отделяли, органическую фазу четырежды порциями по 50 мл промывали водой, сушили над сульфатом натрия и упаривали досуха, при этом получали 31,8 г [2S-(3,4-дихлорфенил)-4-гидроксибутил]метиламида 3-цианонафталин-1-карбоновой кислоты (формула V) в виде твердого вещества желтоватого цвета, который использовали без дополнительной очистки.
C) 5,8 г [2S-(3,4-дихлорфенил)-4-гидроксибутил]метиламид 3-цианонафталин-1-карбоновой кислоты (формула V, стадия В) растворяли в 100 мл дихлорметана, при комнатной температуре добавляли 2,2 мл триэтиламина и 1,16 мл метансульфонилхлорида, реакционную смесь перемешивали в течение 5 ч и выдерживали в течение 2,5 сут. В смесь добавляли воду, органическую фазу сушили над сульфатом натрия и концентрировали досуха, при этом получали 6,65 г [(2S)-2-(3,4-дихлорфенил)-4-метилсульфонилбутил]метиламида 3-цианонафталин-1 -карбоновой кислоты (формула VI) в виде пены, который использовали без дополнительной очистки.
D) 6,65 г [(2S)-2-(3,4-дихлорфенил)-4-метилсульфонилбутил]метиламида 3-цианонафталин-1-карбоновой кислоты (формула VI, стадия С) растворяли в 150 мл ацетонитрила, добавляли 1,84 г иодида калия, 2,44 г N-трет-бутоксикарбонилпиперазина (формула XIX) и 2,2 мл триэтиламина и смесь кипятили с обратным холодильником в течение 3 ч. Затем смесь охлаждали до комнатной температуры и инкубировали в течение ночи. В смесь добавляли воду и этилацетат, органическую фазу промывали водой и насыщенным раствором бикарбоната натрия, сушили над сульфатом натрия и растворитель выпаривали в вакууме, при этом получали 7,8 г {2S-(3,4-дихлорфенил)-4-[4-(2,2-диметилпропионил)пиперазин-1-ил]бутил}метиламида 3-цианонафталин-1-карбоновой кислоты (формула VIa), который использовали на следующей стадии без дополнительной очистки.
Е) 6,6 г {2S-(3,4-дихлорфенил)-4-[4-(2,2-диметилпропионил)пиперазин-1-ил]бутил}метиламида 3-цианонафталин-1-карбоновой кислоты (формула VIa, стадия D) растворяли в 150 мл этанола и добавляли 20 мл 5н. соляной кислоты. Смесь перемешивали в течение 2 сут, а затем нейтрализовали при добавлении карбоната натрия. Этанол выпаривали и продукт экстрагировали этилацетатом и водой. Слой этилацетата сушили над сульфатом натрия и концентрировали досуха, при этом получали 5,2 г [2S-(3,4-дихлорфенил)-4-пиперазин-1-илбутил]амида 3-цианонафталин-1-карбоновой кислоты (формула VII) в виде аморфного вещества.
F) 3,0 г [2S-(3,4-дихлорфенил)-4-пиперазин-1-илбутил]амида 3-цианонафталин-1-карбоновой кислоты (формула VII, стадия Е), 806 мг 2-фуранбороновой кислоты (формула VIII) и 945 мг (D)-глицеральдегида (формула IX, чистота 80%) в этаноле кипятили с обратным холодильником в течение 5 ч. Смесь выдерживали при комнатной температуре в течение ночи, а затем выпаривали органический растворитель. Полученный продукт очищали хроматографией на колонке (элюент: этилацетат, затем этанол), при этом получали 1,3 г чистого 3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1R,2S)-1-(2-фурил)-2,3-дигидроксипропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамида (формула I) в виде кристаллического вещества. [α]D20-27,6° (с 1, метанол), tпл. 140°С-142°С. МС (ES+): m/z 635 (М+).
Пример 2
3-Циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1R,2S)-1-(2-фурил)-2,3-дигидроксипропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид (способ 2)
А) 23,0 г трет-бутоксикарбонилпиперазина (формула X) растворяли в 600 мл этанола в атмосфере азота при 30°С, добавляли 25 г 2-фуранбороновой кислоты (формула VIII) и 22,0 г (D)-глицеральдагида (формула IX, чистота 80%) в 400 мл этанола и смесь кипятили с обратным холодильником в течение 7 ч. Смесь охлаждали до комнатной температуры и концентрировали досуха. Остаток растворяли в 200 мл этилацетата и 50 мл метил-трет-бутилового эфира, промывали раствором 20 г КОН в 200 мл воды, шестью порциями по 150 мл водой, сушили над сульфатом натрия и растворитель выпаривали, при этом получали 54,7 г трет-бутилового эфира 4-((2S)-1-фуран-2-ил-2-гидроксипропил)пиперазин-1-карбоновой кислоты (формула XI). [α]D20+34,6° (с 1, метанол). tпл. 92°С-93°С.
B) 16,3 г трет-Бутилового эфира 4-((2S)-1-фуран-2-ил-2-гидроксипропил)пиперазин-1-карбоновой кислоты (формула XI, стадия А) растворяли при перемешивании в 50 мл метил-трет-бутилового эфира и добавляли 160 мл 5н. соляной кислоты, при этом наблюдалось интенсивное выделение газа, и смесь перемешивали в течение 24 ч. Затем раствор выливали в 200 мл метил-трет-бутилового эфира и перемешивали. Осадок отделяли фильтрованием, промывали 20 мл метил-трет-бутилового эфира и высушивали в вакууме при 60°С, при этом получали 13,5 г дигидрохлорида (2S)-1-фуран-2-ил- 1-пиперазин-1-ил-бутан-2-ола (формула XII). [α]D20+14,0° (с 1, метанол).
C) В суспензию 25 г гидрохлорида 2S-(3,4-дихлорфенил)-4-метиламинобутан-1-ола (формула IV) в 500 мл ТГФ при перемешивании добавляли 28,4 г гидрокарбоната натрия в 150 мл воды. Затем добавляли раствор 21,1 г трет-бутилоксикарбонилангидрида в 200 мл ТГФ и полученную реакционную смесь перемешивали в течение 4 ч. ТГФ выпаривали в вакууме, в остаток добавляли 500 мл этилацетата, 100 мл насыщенного раствора гидрокарбоната натрия и 300 мл воды. Органический слой отделяли, сушили над сульфатом натрия и удаляли органический растворитель, при этом получали маслообразное вещество, которое очищали хроматографией на колонке с силикагелем, при этом получали 29,5 г очищенного трет-бутилового эфира [(2S)-2-(3,4-дихлорфенил)-4-гидроксибутил]метилкарбаминовой кислоты (формула XX) в виде бесцветного масла, которое медленно кристаллизовалось. 20 г трет-бутилового эфира [(2S)-2-(3,4-дихлорфенил)-4-гидроксибутил]метилкарбаминовой кислоты (формула XX) в атмосфере азота растворяли при перемешивании при комнатной температуре в 150 мл дихлорметана, а затем добавляли по каплям 6 мл триэтиламина и 3 мл метансульфонилхлорида. Раствор перемешивали при комнатной температуре в течение 3 сут, а затем концентрировали. В остаток добавляли 200 мл этилацетата и толуол, органический слой промывали 100 мл воды, насыщенным раствором гидрокарбоната натрия до рН 8-9 и h 100 мл воды, сушили над сульфатом натрия и упаривали досуха, при этом получали 13,3 г соответствующего мезилата (формула XXI). Полученный мезилат (13,3 г) растворяли при перемешивании в атмосфере азота при комнатной температуре в 200 мл ацетона и добавляли 22 г иодида натрия. Смесь перемешивали до завершения реакции (в течение 3 сут), ацетон выпаривали, добавляли 200 мл этилацетата и раствор 33 г пентагидрата тиосульфата натрия в 200 мл воды. Водную фазу отделяли, органическую фазу последовательно промывали 100 мл насыщенного раствора гидрокарбоната натрия и трижды порциями по 100 мл водой, сушили над сульфатом натрия и концентрировали досуха, при этом получали 15,1 г трет-бутилового эфира [(2S)-2-(3,4-дихлорфенил)-4-иодбутил]метилкарбаминовой кислоты (формула XIII).
D) В суспензию 450 мг дигидрохлорида (2S)-1-фуран-2-ил-1-пиперазин-1-илбутан-2-ола (формула XII, стадия В) и 1 мл триэтиламина в 50 мл ТГФ при комнатной температуре добавляли при перемешивании раствор 200 мг трет-бутилового эфира [(2S)-2-(3,4-дихлорфенил)-4-иодбутил]метилкарбаминовой кислоты (формула XIII, стадия С) в 10 мл ТГФ. Затем добавляли приблизительно 100 мг Na2CO3 и смесь кипятили с обратным холодильником в течение 15 ч. Смесь охлаждали до комнатной температуры, суспензию концентрировали в вакууме, остаток растворяли в 50 мл этилацетата и в растворе 200 мг КОН в 10 мл воды. Органическую фазу четырежды порциями по 20 мл промывали водой, сушили над сульфатом натрия и упаривали досуха, при этом получали 203 мг вещества желтоватого цвета, которое по данным ЖХ/МС идентифицировали как требуемый амин формулы XIV.
Е) Амин XIV (стадия D, 460 мг) растворяли при 30°С в 2 мл дихлорметана, при комнатной температуре добавляли при перемешивании 3 мл 5н. раствора HCl в изопропаноле. После образования осадка (через 1 ч) в смесь добавляли 50 мл метил-трет-бутилового эфира и перемешивали в течение 15 ч. Твердое вещество белого цвета отделяли фильтрованием, трижды порциями по 10 мл промывали метил-трет-бутиловым эфиром и высушивали в вакууме при 80°С. Для удаления примеси метил-трет-бутиллового эфира твердое вещество растворяли в метаноле и растворители выпаривали, при этом получали 407 мг (выход 85%) продукта в виде пены, который использовали без дополнительной очистки.
F) В раствор 367 мг амина (стадия Е) и 200 мг КОН в 10 мл ТГФ и 10 мл воды добавляли по каплям суспензию 168 мг 3-цианонафталин-1- карбонилхлорида (формулы III, стадия А в способе 1) в 20 мл дихлорметана. Смесь перемешивали при комнатной температуре в течение 15 ч, а затем концентрировали в вакууме. Остаток растворяли в смеси 30 мл этилацетата и 30 мл метил-трет-бутилового эфира. Органическую фазу четырежды порциями по 20 мл промывали водой, сушили над сульфатом натрия и концентрировали досуха в вакууме, при этом получали 420 мг 3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1R,2S)-1-(2-фурил)-2,3-дигидроксипропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамида (формулы I), идентифицированного по данным ЖХ/МС и ЯМР. [a]D20-27,6° (с 1, метанол). МС (ES+): m/z 635 (М+). tпл. 140°С-142°С.
Пример 3
3-Циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1R,2S)-1-(2-фурил)-2,3-дигидроксипропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид (модифицированный способ 2)
A) 12,2 г ДМСО в 100 мл дихлорметана добавляли по каплям в 7,3 г оксалилхлорида в 100 мл дихлорметана при перемешивании в атмосфере азота при -70°С, полученную смесь перемешивали в течение 15 мин, а затем добавляли 20 г трет-бутилового эфира [2S-(3,4-дихлорфенил)-4-гидроксибутил]метилкарбаминовой кислоты в 200 мл дихлорметана. Смесь перемешивали при -70°С в течение 1 ч. Затем добавляли по каплям 40,3 мл триэтиламина в 50 мл дихлорметана и раствор перемешивали при -70°С в течение 15 мин. Смесь нагревали до комнатной температуры, растворитель удаляли и остаток растворяли в 300 мл толуола и 200 мл этилацетата. Полученный раствор шестикратно промывали 200 мл насыщенного раствора NaCl в воде, сушили над сульфатом натрия и концентрировали досуха, при этом получали 19,7 г трет-бутилового эфира [(2S)-2-(3,4-дихлорфенил)-4-оксобутил]метилкарбаминовой кислоты (формула XVI).
B) В суспензию 280 мг трет-бутилового эфира [(2S)-2-(3,4-дихлорфенил)-4-оксобутил]метилкарбаминовой кислоты (формула XVI, стадия А) в 20 мл ТГФ добавляли смесь 300 мг дигидрохлорида (2S)-1-фуран-2-ил-1-пиперазин-1-илбутан-2-ола (формула XII, стадия В в способе 2), 200 мг ацетата натрия в 50 мл ТГФ и 100 мкл уксусной кислоты и полученную смесь перемешивали при комнатной температуре в течение 5 ч. Затем добавляли 240 мг триацетоксиборгидрида натрия и суспензию перемешивали при комнатной температуре в течение 15 ч. Суспензию концентрировали в вакууме, остаток растворяли в 30 мл этилацетата, 30 мл метил-трет-бутилового эфира и раствора 600 мг КОН в воде. Органическую фазу четырежды порциями по 20 мл промывали водой, сушили над сульфатом натрия и растворители выпаривали, при этом получали 463 мг стекловидного соединения, которое использовали без дополнительной очистки в способе 2 на стадиях Е и F.
Пример 4
3-Циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1R,2S)-1-(2-Фурил)-2,3-дигидроксипропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид (способ 3)
A) 3-Цианонафталин-1-карбоновую кислоту (формула II, 58,0 г) суспендировали в 600 мл дихлорметана, а затем при перемешивании добавляли 2 мл ДМФА. В полученную суспензию медленно добавляли 35 мл оксалилдихлорида в 65 мл дихлорметана и смесь перемешивали при 30°С-40°С в течение 4 ч. Полученный раствор концентрировали досуха, при этом получали 67 г 3-цианонафталин-1-карбонилхлорида (формула III), который хранили в холодильнике, а затем использовали без дополнительной очистки.
B) 3S-(3,4-Дихлорфенил)-4-метиламинобутан-1-ол (формула IV, 20 г) суспендировали при перемешивании в 200 мл ТГФ при комнатной температуре. В суспензию добавляли раствор 12 г КОН в 100 мл воды, 17,2 г 3-цианонафталин-1-карбонилхлорида (формула III, стадия А) и смесь перемешивали в течение 3 ч. Органические растворители удаляли и в остаток добавляли этилацетат и метил-трет-бутиловый эфир. Водную фазу отделяли, органическую фазу четырежды порциями по 50 мл промывали водой, сушили над сульфатом натрия и концентрировали досуха, при этом получали 31,8 г [2S-(3,4-дихлорфенил)-4-гидроксибутил]метиламида 3-цианонафталин-1-карбоновой кислоты (формула V) в виде твердого вещества желтоватого цвета, которое использовали без дополнительной очистки.
C) 25 мл ДМСО в 100 мл дихлорметана добавляли по каплям в 9,7 г оксалилхлорида в 100 мл дихлорметана при перемешивании в атмосфере азота при -70°С, смесь перемешивали в течение 15 мин и добавляли 31,7 г [2S-(3,4-дихлорфенил)-4-гидроксибутил]метиламида 3-цианонафталин-1-карбоновой кислоты (формула V, стадия В) в 200 мл дихлорметана и 6 мл ДМСО. Смесь перемешивали при -70°С в течение 1 ч, добавляли по каплям 52 мл триэтиламина в 50 мл дихлорметана, раствор перемешивали при -70°С в течение 15 мин, а затем нагревали до комнатной температуры. Растворитель удаляли, остаток растворяли в 300 мл толуола и 200 мл этилацетата. Полученный раствор шестикратно промывали 200 мл насыщенного раствора NaCl в воде, сушили над сульфатом натрия и концентрировали досуха, при этом получали 31,0 г [(2S)-2-(3,4-дихлорфенил)-4-оксобутил]метиламида 7-цианонафталин-2-карбоновой кислоты (формула XVII).
D) Дигидрохлорид (2S)-1-фуран-2-ил-1-пиперазин-1-илбутан-2-ола (формула XII, стадия В в способе 2, 860 мг), 860 мг [(2S)-2-(3,4-дихлорфенил)-4-оксобутил]метиламида 7-цианонафталин-2-карбоновой кислоты (формула XVII, стадия С), 200 мкл уксусной кислоты и 0,1 мл воды суспендировали в 150 мл ТГФ и перемешивали в течение 4 ч. Затем добавляли 1,49 г триацетоксиборгидрида натрия и реакционную смесь перемешивали при комнатной температуре в течение 15 ч. Раствор концентрировали и добавляли раствор 0,4 г КОН в 1 мл воды, а также 10 мл метил-трет-бутилового эфира и 50 мл этилацетата. Водную фазу отделяли, органическую фазу четырежды порциями по 20 мл промывали водой, сушили над сульфатом натрия и концентрировали досуха, при этом получали 1,32 г продукта в виде пены. Полученную пену растворяли в 9 мл изопропанола и нагревали до 60°С. Продукт кристаллизовали и вторично растворяли в 28 мл изопропанола (добавленного тремя порциями) при 75°С. Раствор охлаждали до комнатной температуры, полученные кристаллы трижды порциями по 20 мл промывали метил-трет-бутиловым эфиром, при этом получали 1,15 г моноизопропилата 3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1R,2S)-1-(2-фурил)-2,3-дигидроксипропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамида (формула I). tпл. 165°С-166°С.
Пример 5
3-Циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1R,2S)-1-(2-фурил)-2-оксо[1,3]диоксолан-4-ил]пиперазин-1-ил}метил]-N-метил-1-нафтамид

650 мг 3-Циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1R,2S)-1-(2-фурил)-2,3-дигидрокси-пропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамида, полученного по любому из вышеуказанных способов, суспендировали при комнатной температуре в 50 мл дихлорметана. Затем в течение 70 мин добавляли 216 мг N,N'-карбонилдиимидазола в 60 мл дихлорметана и смесь перемешивали при комнатной температуре в течение 5 ч. Смесь промывали 50 мл насыщенного раствора гидрокарбоната натрия и водой до рН 6. Растворители удаляли в вакууме, при этом получали 634 мг 3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1R,2S)-1-(2-фурил)-2-оксо[1,3]диоксолан-4-ил]пиперазин-1-ил}метил]-N-метил-1-нафтамида.
Пример 6
Моноацетат 3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1R,2S)-1-(2-фурил)-2-оксо[1,3]диоксолан-4-ил]пиперазин-1-ил}метил]-N-метил-1-нафтамида
350 мг Моноэтанолята 3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1R,2S)-1-(2-фурил)-2-оксо[1,3]диоксолан-4-ил]пиперазин-1-ил}метил]-N-метил-1-нафтамида растворяли при перемешивании в 50 мл этилацетата при комнатной температуре. Затем добавляли 120 мкл ацетилхлорида и 250 мкл триэтиламина и реакционную смесь перемешивали при комнатной температуре в течение 3 ч. Смесь промывали 50 мл насыщенного раствора карбоната натрия и пятикратно порциями по 30 мл водой, сушили над сульфатом натрия и концентрировали досуха, при этом получали 342 мг смеси, содержащей по данным ЖХ/МС и ЯМР в основном моноуксусный эфир первичного спирта. Продукт очищали хроматографией на колонке с силикагелем (10 г, элюент: этилацетат/этанол), при этом получали 136 мг моноацетата, который характеризовали методами ЖХ/МС и ЯМР.
Пример 7
Моноацетат 3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1R,2S)-1-(2-фурил)-2-оксо[1,3]диоксолан-4-ил]пиперазин-1-ил}метил]-N-метил-1-нафтамида
230 мг Моноэтанолята 3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1R,2S)-1-(2-фурил)-2-оксо[1,3]диоксолан-4-ил]пиперазин-1-ил}метил]-N-метил-1-нафтамида растворяли при комнатной температуре в 10 мл пиридина. Затем добавляли по каплям 150 мкл ацетилхлорида в 10 мл дихлорметана и реакционную смесь перемешивали при комнатной температуре в течение 4 ч. В смесь добавляли 10 мл воды и концентрировали в вакууме. Остаток растворяли в 50 мл этилацетата и шестикратно порциями по 20 мл промывали водой. По данным ЖХ/МС и ЯМР в неочищенной смеси содержался диацетат основного соединения. 150 мг Смеси фракционировали хроматографией на колонке с силикагелем (10 г), при этом получали 84 мг требуемого диэфира (по данным ЯМР и МС).
Соединения формулы I, перечисленные ниже в таблице 8, получали способами, описанными выше, или аналогичными способами.
Соединения 15-22, указанные выше в таблице 8, получали также с использованием автоматического синтезатора. Для этого в каждом случае 200 мкл 0,25 н. исходного раствора соответствующего соединения формулы IX помещали в микрореактор и упаривали в вакууме для удаления воды. Остаток растворяли в 200 мкл этанола. В каждом случае в указанный исходный раствор добавляли 200 мкл исходного раствора (0,25 моль/л) в этаноле рацемического или энантиомерно чистого (см. в каждом случае соответствующее соединение, таблица 8) N-[(2S)-2-(3,4-дихлорфенил)-4-(1-пиперазинил)бутил]-N-метилбензамида формулы VII и 200 мкл 0,25 н. исходного раствора в этаноле соответствующей бороновой кислоты (соединение дигидроксиборана) формулы VIII. Реакционную смесь сначала нагревали при 80°С в течение 2 ч, а затем охлаждали до комнатной температуры и добавляли 1 мл этанола. Затем в смесь добавляли 100 мг анионита Amberjet® и реактор встряхивали в течение 2 ч. Ионобменник отделяли фильтрованием, дважды порциями по 500 мкл промывали этанолом и растворитель упаривали досуха в вакууме. В каждом случае полученные в остатке образцы без дополнительной очистки идентифицировали методами ЖХВР и автоматизированной масс-спектрометрии для определения чистоты и подтверждения структуры.
Пример 8
Капсулы, содержащие 3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1R,2S)-1-(2-фурил)-2,3-дигидроксипропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид
Получали капсулы следующего состава:
Активное соединение, кукурузный крахмал и лактозу перерабатывали в гомогенную пастообразную смесь с использованием ЕЕ. Пасту гранулировали, гранулы помещали в пригодный поддон и высушивали при 45°С для удаления растворителя. Сухие гранулы пропускали через дробилку и смешивали в миксере со следующими вспомогательными веществами:
а затем помещали в капсулы емкостью 400 мг (капсула размером 0).
Описываются соединения 3-цианонафталин-1-карбоновой кислоты и пергидроксиалкилметилпиперазина формулы I, где R1 означает C1-С4алкил, R2 и R3 означают галоген, R4 выбран из группы, включающей 2-фуранил, 3-фуранил, 2-тиофен, 3-тиофен, фенил, бензил, 2-бензофуранил и др., R5 выбран из группы, включающей водород и R6, R6 означает подгруппу общей формулы

которые являются антагонистами рецепторов тахикинина. Описываются также фармацевтические композиции, включающие такие соединения, и способы получения таких соединений и промежуточных продуктов для получения соединений согласно указанным способам. 6 н. и 19 з.п. ф-лы, 8 табл.

1. Соединения общей формулы I

где R1 означает С1-С4алкил,
R2 означает галоген,
R3 означает галоген,
R4 выбран из группы, включающей 2-фуранил, 3-фуранил, 2-тиофен, 3-тиофен, фенил, бензил, 2-бензофуранил, 3-бензофуранил, 5-хлор-2-тиофен, 4-метилфенил, 3,4-метилендиоксифенил, 2-метоксифенил, 4-метоксифенил; 2-пиридинил, 3-пиридинил, 1-бензо[с]тиофен, 4-бензо[с]тиофен, 5-бензо[с]тиофен, 2-бензо[b]тиофен, 3-бензо[b]тиофен, 4-бензо[b]тиофен, 5-бензо[b]тиофен, 6-бензо[b]тиофен, 7-бензо[b]тиофен, 1-бензо[1,3]диоксол, 4-бензо[1,3]диоксол и 5-бензо[1,3]диоксол,
R5 выбран из группы, включающей водород и R6,
R6 означает подгруппу общей формулы

где R7 выбран из группы, включающей водород или С1-С4алканоил, или R7 вместе с другим заместителем, выбранным из группы, включающей R8, R9, R10 и R11, образует 5- или 6-членный цикл с карбонильным мостиком или метиленовым мостиком;
R8 означает водород, или R8 вместе с другим заместителем, выбранным из группы, включающей R7, R9, R10 и R11, образует 5- или 6-членный цикл с карбонильным мостиком или метиленовым мостиком,
R9 означает водород, или R9 вместе с другим заместителем, выбранным из группы, включающей R7, R8, R10 и R11, образует 5- или 6-членный цикл с карбонильным мостиком или метиленовым мостиком,
R10 означает водород, или R10 вместе с другим заместителем, выбранным из группы, включающей R7, R8, R9 и R11, образует 5- или 6-членный цикл с карбонильным мостиком или метиленовым мостиком,
R11 выбран из группы, включающей водород или С1-С4алканоил, или R11 вместе с другим заместителем, выбранным из группы, включающей R7, R8, R9 и R10, образует 5- или 6-членный цикл с карбонильным мостиком или метиленовым мостиком,
k равно 0 или 1,
l равно 0 или 1, m равно 0 или 1,
n равно 0 или 1,
или их физиологически совместимые кислотно-аддитивные соли.
2. Соединения по п.1, где R1 означает метил.
3. Соединения по п.1, где R2 и R3 каждый означает хлор.
4. Соединения по п.1, где R4 выбран из группы, включающей 2-фуранил, 3-фуранил, 2-тиофен, 3-тиофен, фенил, бензил, 2-бензофуранил, 5-хлор-2-тиофен, 4-метилфенил, 3,4-метилендиоксифенил, 2-метоксифенил и 4-метоксифенил.
5. Соединения по п.4, где R4 выбран из группы, включающей 2-фуранил, 3-фуранил, 2-тиофен и 3-тиофен.
6. Соединения по п.1, где R5 означает водород.
7. Соединения по п.1, где R7 и R11 каждый означает водород, k равно 1, а l, m, n каждый равен 0.
8. Соединения по п.1, где R7, R8 и R11 каждый означает водород, k и l каждый равен 1, а m и n каждый равен 0.
9. Соединения по п.1, где R7, R8, R9 и R11 каждый означает водород, k, l и m каждый равен 1, а n равен 0.
10. Соединения по п.1, где R7-R11 каждый означает водород, k, l и m каждый равен 1, а n равен 0.
11. Соединения по п.1, где хиральный центр *С находится в S конфигурации.
12. Соединения по п.1, которые выбраны из группы, включающей
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1R,2S)-1-(2-фурил)-2,3-дигидроксипропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
(2S,3R)-2-(ацетилокси)-3-{4-[(3S)-4-[(3-циано-1-нафтоил)(метил)амино]-3-(3,4-дихлорфенил)бутил]пиперазин-1-ил}-3-(2-фурил)пропилацетат,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[1-(2-фурил)-2-гидроксиэтил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1R,2S,3R,4R)-1-(2-фурил)-2,3,4,5-тетрагидроксипентил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1R,2S,3S,4R)-1-(2-фурил)-2,3,4,5-тетрагидроксипентил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1S,2S,3S,4R)-2,3,4,5-тетрагидрокси-1-(3-тиенил)пентил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1S,2S,3R,4R)-2,3,4,5-тетрагидрокси-1-(3-тиенил)пентил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[1-(2-фурил)-2-гидрокси-1-(гидроксиметил)этил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[1-(2-фурил)-2-гидрокси-1-(гидроксиметил)этил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1S,2S)-2,3-дигидрокси-1-(3-тиенил)пропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1R,2S)-2,3-дигидрокси-1-(2-тиенил)пропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(S)-[(4S)-2-оксо-1,3-диоксолан-4-ил](3-тиенил)метил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-(4-{(R)-2-фурил[(4S)-2-оксо-1,3-диоксолан-4-ил]метил}пиперазин-1-ил)бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1S,2S)-1-(3-фурил)-2,3-дигидроксипропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[1-(2-фурил)-2,3-дигидроксипропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1S,2S)-2,3-дигидрокси-1-фенилпропил]пиперазии-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2)-2-(3,4-дихлорфенил)-4-{4-[(1S,2S)-2,3-дигидрокси-1-(4-метоксифенил)пропил]пиперазин-1-ил}бутил]-метил-1-нафтамид,
N-[(2S)-4-{4-[(1R,2S)-1-(1-бензофуран-2-ил)-2,3-дигидроксипропил]пиперазин-1-ил}-2-(3,4-дихлорфенил)бутил]-3-циано-N-метил-1-нафтамид,
N-[(2S)-4-{4-[(1R,2S)-1-(5-хлор-2-тиенил)-2,3-дигидроксипропил]пиперазин-1-ил}-2-(3,4-дихлорфенил)бутил]-3-циано-N-метил-1-нафтамид,
N-[(2S)-4-{4-[(1S,2S)-1-(1,3-бензодиоксол-5-ил)-2,3-дигидроксипропил]пиперазин-1-ил}-2-(3,4-дихлорфенил)бутил]-3-циано-N-метил-1-нафтамид, и
N-[(2S)-4-{4-[(1R,2S)-1-(1-бензотиен-2-ил)-2,3-дигидроксипропил]пиперазин-1-ил}-2-(3,4-дихлорфенил)бутил]-3-циано-]-N-метил-1-нафтамид.
13. Соединения по п.2, которые выбраны из группы, включающей
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1R,2S)-1-(2-фурил)-2,3-дигидроксипропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
(2S,3R)-2-(ацетилокси)-3-{4-[(3S)-4-[(3-циано-1-нафтоил)(метил)амино]-3-(3,4-дихлорфенил)бутил]пиперазин-1-ил}-3-(2-фурил)пропилацетат,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[1-(2-фурил)-2-гидроксиэтил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1R,2S,3R,4R)-1-(2-фурил)-2,3,4,5-тетрагидроксипентил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1R,2S,3S,4R)-1-(2-фурил)-2,3,4,5-тетрагидроксипентил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1S,2S,3S,4R)-2,3,4,5-тетрагидрокси-1-(3-тиенил)пентил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1S,2S,3R,4R)-2,3,4,5-тетрагидрокси-1-(3-тиенил)пентил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[1-(2-фурил)-2-гидрокси-1-(гидроксиметил)этил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[1-(2-фурил)-2-гидрокси-1-(гидроксиметил)этил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1S,2S)-2,3-дигидрокси-1-(3-тиенил)пропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1R,2S)-2,3-дигидрокси-1-(2-тиенил)пропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(S)-[(4S)-2-оксо-1,3-диоксолан-4-ил](3-тиенил)метил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-(4-{(R)-2-фурил[(4S)-2-оксо-1,3-диоксолан-4-ил]метил}пиперазин-1-ил)бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1S,2S)-1-(3-фурил)-2,3-дигидроксипропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[1-(2-фурил)-2,3-дигидроксипропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1S,2S)-2,3-дигидрокси-1-фенилпропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2)-2-(3,4-дихлорфенил)-4-{4-[(1S,2S)-2,3-дигидрокси-1-(4-метоксифенил)пропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
N-[(2S)-4-{4-[(1R,2S)-1-(1-бензофуран-2-ил)-2,3-дигидроксипропил]пиперазин-1-ил}-2-(3,4-дихлорфенил)бутил]-3-циано-N-метил-1-нафтамид,
N-[(2S)-4-{4-[(1R,2S)-1-(5-хлор-2-тиенил)-2,3-дигидроксипропил]пиперазин-1-ил}-2-(3,4-дихлорфенил)бутил]-3-циано-N-метил-1-нафтамид,
N-[(2S)-4-{4-[(1S,2S)-1-(1,3-бензодиоксол-5-ил)-2,3-дигидроксипропил]пиперазин-1-ил}-2-(3,4-дихлорфенил)бутил]-3-циано-N-метил-1-нафтамид, и
N-[(2S)-4-{4-[(1R,2S)-1-(1-бензотиен-2-ил)-2,3-дигидроксипропил]пиперазин-1-ил}-2-(3,4-дихлорфенил)бутил]-3-циано-N-метил-1-нафтамид.
14. Соединения по п.3, которые выбраны из группы, включающей
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1R,2S)-1-(2-фурил)-2,3-дигидроксипропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
(2S,3R)-2-(ацетилокси)-3-{4-[(35)-4-[(3-циано-1-нафтоил)(метил)амино]-3-(3,4-дихлорфенил)бутил]пиперазин-1-ил}-3-(2-фурил)пропилацетат,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[1-(2-фурил)-2-гидроксиэтил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1R,2S,3R,4R)-1-(2-фурил)-2,3,4,5-тетрагидроксипентил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1R,2S,3S,4R)-1-(2-фурил)-2,3,4,5-тетрагидроксипентил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1S,2S,3S,4R)-2,3,4,5-тетрагидрокси-1-(3-тиенил)пентил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1S,2S,3R,4R)-2,3,4,5-тетрагидрокси-1-(3-тиенил)пентил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[1-(2-фурил)-2-гидрокси-1-(гидроксиметил)этил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[1-(2-фурил)-2-гидрокси-1-(гидроксиметил)этил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1S,2S)-2,3-дигидрокси-1-(3-тиенил)пропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1R,2S)-2,3-дигидрокси-1-(2-тиенил)пропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(S)-[(4S)-2-оксо-1,3-диоксолан-4-ил](3-тиенил)метил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-(4-{(R)-2-фурил[(4S)-2-оксо-1,3-диоксолан-4-ил]метил}пиперазин-1-ил)бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1S,2S)-1-(3-фурил)-2,3-дигидроксипропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[1-(2-фурил)-2,3-дигидроксипропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1S,2S)-2,3-дигидрокси-1-фенилпропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2)-2-(3,4-дихлорфенил)-4-{4-[(1S,2S)-2,3-дигидрокси-1-(4-метоксифенил)пропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
N-[(2S)-4-{4-[(1R,2S)-1-(1-бензофуран-2-ил)-2,3-дигидроксипропил]пиперазин-1-ил}-2-(3,4-дихлорфенил)бутил]-3-циано-N-метил-1-нафтамид,
N-[(2S)-4-{4-[(1R,2S)-1-(5-хлор-2-тиенил)-2,3-дигидроксипропил]пиперазин-1-ил}-2-(3,4-дихлорфенил)бутил]-3-циано-N-метил-1-нафтамид,
N-[(2S)-4-{4-[(1S,2S)-1-(1,3-бензодиоксол-5-ил)-2,3-дигидроксипропил]пиперазин-1-ил}-2-(3,4-дихлорфенил)бутил]-3-циано-N-метил-1-нафтамид, и
N-[(2S)-4-{4-[(1R,2S)-1-(1-бензотиен-2-ил)-2,3-дигидроксипропил]пиперазин-1-ил}-2-(3,4-дихлорфенил)бутил]-3-циано-N-метил-1-нафтамид.
15. Соединения по п.4, которые выбраны из группы, включающей
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1R,2S)-1-(2-фурил)-2,3-дигидроксипропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
(2S,3R)-2-(ацетилокси)-3-{4-[(3S)-4-[(3-циано-1-нафтоил)(метил)амино]-3-(3,4-дихлорфенил)бутил]пиперазин-1-ил}-3-(2-фурил)пропилацетат,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[1-(2-фурил)-2-гидроксиэтил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1R,2S,3R,4R)-1-(2-фурил)-2,3,4,5-тетрагидроксипентил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1R,2S,3S,4R)-1-(2-фурил)-2,3,4,5-тетрагидроксипентил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1S,2S,3S,4R)-2,3,4,5-тетрагидрокси-1-(3-тиенил)пентил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1S,2S,3R,4R)-2,3,4,5-тетрагидрокси-1-(3-тиенил)пентил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[1-(2-фурил)-2-гидрокси-1-(гидроксиметил)этил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[1-(2-фурил)-2-гидрокси-1-(гидроксиметил)этил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1S,2S)-2,3-дигидрокси-1-(3-тиенил)пропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1R,2S)-2,3-дигидрокси-1-(2-тиенил)пропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(S)-[(4S)-2-оксо-1,3-диоксолан-4-ил](3-тиенил)метил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-(4-{(R)-2-фурил[(4S)-2-оксо-1,3-диоксолан-4-ил]метил}пиперазин-1-ил)бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1S,2S)-1-(3-фурил)-2,3-дигидроксипропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[1-(2-фурил)-2,3-дигидроксипропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2S)-2-(3,4-дихлорфенил)-4-{4-[(1S,2S)-2,3-дигидрокси-1-фенилпропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
3-циано-N-[(2)-2-(3,4-дихлорфенил)-4-{4-[(1S,2S)-2,3-дигидрокси-1-(4-метоксифенил)пропил]пиперазин-1-ил}бутил]-N-метил-1-нафтамид,
N-[(2S)-4-{4-[(1R,2S)-1-(1-бензофуран-2-ил)-2,3-дигидроксипропил]пиперазин-1-ил}-2-(3,4-дихлорфенил)бутил]-3-циано-N-метил-1-нафтамид,
N-[(2S)-4-{4-[(1R,2S)-1-(5-хлор-2-тиенил)-2,3-дигидроксипропил]пиперазин-1-ил}-2-(3,4-дихлорфенил)бутил]-3-циано-N-метил-1-нафтамид,
N-[(2S)-4-{4-[(1S,2S)-1-(1,3-бензодиоксол-5-ил)-2,3-дигидроксипропил]пиперазин-1-ил}-2-(3,4-дихлорфенил)бутил]-3-циано-N-метил-1-нафтамид, и
N-[(2S)-4-{4-[(1R,2S)-1-(1-бензотиен-2-ил)-2,3-дигидроксипропил]пиперазин-1-ил}-2-(3,4-дихлорфенил)бутил]-3-циано-N-метил-1-нафтамид.
16. Фармацевтическая композиция, обладающая антагонистическим действием в отношений рецепторов тахикинина, включающая соединение по любому из пп.1-15 и стандартные фармацевтические вспомогательные вещества и/или носители.
17. Применение соединений по любому из пп.1-15 для лечения и/или профилактики респираторных заболеваний, особенно астмы, бронхита, кашля и ринита; кожных заболеваний, особенно воспалительных кожных реакций, аллергических кожных реакций и псориаза; артропатических заболеваний, особенно артрита, васкулитов и системной красной волчанки; функциональных или воспалительных нарушений в желудочно-кишечном тракте, особенно синдрома раздраженного кишечника (IBS), воспалительного заболевания кишечника (IBD), псевдомембранозного колита и диареи; буллезных заболеваний; воспаления мочевого пузыря, такого как цистит и интерстициальный цистит; и мигрени.
18. Применение по п.17, где нарушения представляют собой функциональные или воспалительные нарушения в нижних отделах кишечника в организме млекопитающих и человека, которые связаны с повышенной чувствительностью к боли и/или с задержкой стула в отделе ободочной кишки.
19. Применение по п.17, где нарушение представляет собой IBS.
20. Способ получения соединений общей формулы I

где R1 означает С1-С4алкил,
R2 означает галоген,
R3 означает галоген,
R4 выбран из группы, включающей 2-фуранил, 3-фуранил, 2-тиофен, 3-тиофен, фенил, бензил, 2-бензофуранил, 3-бензофуранил, 5-хлор-2-тиофен, 4-метилфенил, 3,4-метилендиоксифенил, 2-метоксифенил, 4-метоксифенил, 2-пиридинил, 3-пиридинил, 1-бензо[с]тиофен, 4-бензо[с]тиофен, 5-бензо[с]тиофен, 2-бензо[b]тиофен, 3-бензо[b]тиофен, 4-бензо[b]тиофен, 5-бензо[b]тиофен, 6-бензо[b]тиофен, 7-бензо[b]тиофен, 1-бензо[1,3]диоксол, 4-бензо[1,3]диоксол и 5-бензо[1,3]диоксол,
R5 выбран из группы, включающей водород и R6,
R6 означает подгруппу общей формулы

где R7 выбран из группы, включающей водород или С1-С4алканоил, или R7 вместе с другим заместителем, выбранным из группы, включающей R8, R9, R10 и R11, образует 5- или 6-членный цикл с карбонильным мостиком или метиленовым мостиком,
R8 означает водород, или R8 вместе с другим заместителем, выбранным из группы, включающей R7, R9, R10 и R11, образует 5- или 6-членный цикл с карбонильным мостиком или метиленовым мостиком,
R9 означает водород, или R9 вместе с другим заместителем, выбранным из группы, включающей R7, R8, R10 и R11, образует 5- или 6-членный цикл с карбонильным мостиком или метиленовым мостиком,
R10 означает водород, или R10 вместе с другим заместителем, выбранным из группы, включающей R7, R8, R9 и R11, образует 5- или 6-членный цикл с карбонильным мостиком или метиленовым мостиком,
R11 выбран из группы, включающей водород или С1-С4алканоил, или R11 вместе с другим заместителем, выбранным из группы, включающей R7, R8, R9 и R10, образует 5- или 6-членный цикл с карбонильным мостиком или метиленовым мостиком,
k равно 0 или 1,
l равно 0 или 1, m равно 0 или 1,
n равно 0 или 1, или их физиологически совместимых кислотно-аддитивных солей,
характеризующийся тем, что
а) соединение общей формулы VII

взаимодействует с соединением общей формулы VIII

и соединением общей формулы IX

с образованием соединения общей формулы I, или
(b) соединение общей формулы XV

взаимодействует с соединением формулы III

с образованием соединения общей формулы I, или
с) соединение общей формулы XVII

взаимодействует с соединением общей формулы XII

с образованием соединения общей формулы I,
которое необязательно превращают в его физиологически совместимую кислотно-аддитивную соль.
21. Соединения общей формулы VII
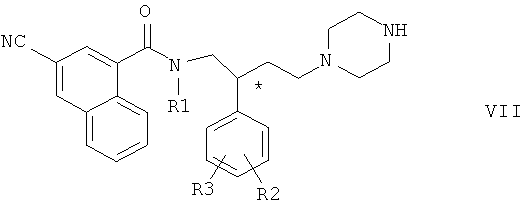
где R1 означает С1-С4алкил,
R2 означает галоген, и
R3 означает галоген.
22. Соединения по п.21, где R1 означает метил, a R2 и R3 каждый означает хлор.
23. Способ подавления тахикинин-опосредованного состояния в организме млекопитающего, заключающийся в том, что указанному млекопитающему вводят эффективное в отношении блокирования рецептора тахикинина количество соединения по любому из пп.1-15.
24. Способ по п.23, где тахикинин означает нейрокинин, а рецептор тахикинина означает рецептор NK1 или NK2.
25. Способ по п.23, где тахиканин-опосредованое состояние выбрано из группы, включающей гипотензию, бронхостеноз и подвижность ободочной кишки.
| Станок для балансировки деталей | 1985 |
|
SU1293506A1 |
| УСТРОЙСТВО ТЕЛЕКОНТРОЛЯ ДЛЯ РАССРЕДОТОЧЕННЫХ ОБЪЕКТОВ | 1972 |
|
SU428434A1 |
| ПРОИЗВОДНЫЕ 3-ФЕНИЛПИРИДИНА И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2000 |
|
RU2236402C2 |
Авторы
Даты
2011-05-27—Публикация
2006-11-30—Подача