Изобретение относится к области экспериментальной биологии и медицины, где необходима подготовка препаратов для светлопольной, флуоресцентной, конфокальной и мультифотонной микроскопии, оптической томографии (оптической проекционной томографии, SPIM, ультрамикроскопии). Оно может быть использовано для предклинических исследований распределения в тканях меченых фармакологических препаратов, оценки клеточных эффектов фармакологических препаратов и физиологических воздействий, работы с материалом биопсий в диагностических и исследовательских целях.
В последние годы возросли требования к методам детекции молекулярных зондов в исследуемых образцах биологической ткани. Для полноты извлекаемых сведений и исключения артефактов требуется представление данных не на плоскостном материале, а в трехмерном объеме. Однако в настоящее время во всем мире исследования проводятся на гистологических срезах, потому что образцы толщиной более 100 мкм обладают сильной рассеивающей способностью из-за разницы коэффициентов преломления клеточных компартментов в биологической ткани.
Известен способ оптического просветления, в котором в качестве образца ткани использовали эмбрионов шпорцевой лягушки до 26 стадии, которых фиксировали описанным в этой работе фиксатором Дента (метанол : диметилсульфоксид в соотношении 4:1) в течение 2-12 ч, затем обесцвечивали в отбеливателе Дента (метанол : диметилсульфоксид: 30% перекись водорода в соотношении 4:1:1) в течение 48 ч. Хранили в метаноле при -20°С. После регидратации в буфере (2 раза по 5 мин) проводили иммуногистохимическую реакцию, по окончании которой дегидратировали эмбрионы в метаноле 2 раза по 5-15 мин и просветляли в смеси бензилбензоат : бензиловый спирт в соотношении 2:1. [Dent J.A., Poison A.G., Klymkowsky M.W. A whole-mount immunocytochemical analysis of the expression of the intermediate filament protein vimentin in Xenopus // Development. - 1989. - V.105. - №1. - P.61-74].
Однако описанный способ в данной работе применялся к образцам малого размера (толщина до 100 мкм) и использовались эмбрионы, а не ткани взрослых животных, исследование которых наиболее актуально в современной экспериментальной медицине и диагностике. Визуализация маркеров в зрелой нервной системе в отличие от эмбриональной ткани сильно затруднена.
Известен способ просветления образцов большего размера - мозжечка взрослой мыши. После глубокой анестезии мышей перфузировали раствором 4% параформальдегида и затем изолированные образцы постфиксировали в 4% растворе парформальдегида в течение 24-48 ч при 4°С. Затем постфиксировали в фиксаторе Дента в течение 12-18 ч, инкубировали в отбеливателе Дента в течение 8 ч и дегидратировали в 100% метаноле 2 раза по 30 мин. Потом проводили циклы замораживания - оттаивания (4-5 циклов заморозки до температуры -80°С и оттаивания до комнатной температуры) и оставляли на 12-18 ч в метаноле при -80°С. Для проведения иммуногистохимической реакции препараты регидратировали и окрашивали, а затем для оптического просветления вновь дегидратировали в 30%, 50%, 80% и 100% метаноле по 30-60 мин в каждом и просветляли в смеси бензилбензоат : бензиловый спирт в соотношении 2:1 [R.V.Sillitoe, R.Hawkes. Whole-mount immunohistochemistry: a high-throughput screen for patterning defects in the mouse cerebellum // J.Histochem. Cytochem. - 2002. - V.50. - 2. - P.235-244].
Недостатками известного способа просветления являются недостаточная равномерность оптического просветления мозжечка из-за миелинизации нервной ткани взрослого животного и возможность просветлять образцы толщиной не более 300 мкм.
Известен также способ оптического просветления поджелудочной железы взрослой мыши, в котором изолированную поджелудочную железу фиксировали в 4% растворе параформальдегида в течение 2-3 ч, ступенчато дегидратировали в метаноле и хранили при -20°С. Перед иммуногистохимической реакцией обесцвечивали модифицированным отбеливателем Дента (метанол: 16,7% диметилсульфоксид: 15% Н2О2) в течение 12-24 ч и проводили 3-5 циклов замораживания в метаноле до -80°С минимум на 1 ч и оттаивания при комнатной температуре, затем ткань регидратировали и окрашивали. Для просветления заливали в агарозу, ступенчато дегидратировали в метаноле и погружали в смесь бензилбензоат : бензиловый спирт 2:1 минимум на 24 ч. Данный способ был опробован и на других органах мыши: печень, желудок, мозг (до 5 недель), однако эти результаты в статье не приводятся [Alanentalo Т., Asayesh, Н.Morrison, С.Е.Lorén, D.Holmberg, J.Sharpe, U.Ahlgren. Tomographic molecular imaging and 3D quantification within adult mouse organs // Nature Methods. - 2007. - V.4. - 1. - P.31-33]. Недостатками данного способа является невысокая степень просветления из-за сильной эндогенной пигментации указанных внутренних органов, неравномерность и недостаточная степень просветления нервной ткани из-за сильной миелинизации головного мозга у взрослых животных.
Известен способ просветления целой улитки уха взрослой мыши (до 6 месяцев) с использованием смеси метилсалицилат : бензилбензоат. Улитку перфузировали 4% раствором параформальдегида и постфиксировали 12-18 часов в 4% растворе параформальдегида при +4°С. Для просветления образцы ткани обезвоживали в 70% растворе этанола от 2 до 18 ч, затем в 90% растворе этанола в течение 30 мин и 2 смены 100% этанола по 2 ч в каждом. Приготовленную просветляющую смесь метилсалицилат : бензилбензоат в соотношении 5:3 разводили с абсолютным этанолом в соотношении 1:1 в течение 4 ч, затем 3 смены со смесью метилсалицилат : бензилбензоат в соотношении 5:3 по 2 часа, 4 ч и 12-18 ч соответственно [MacDonald GH, Rubel EW. Three-dimensional imaging of the intact mouse cochlea by fluorescent laser scanning confocal microscopy. // Hear Res. - 2008. - V.243. - 1-2. - P.1-10]. Недостатком этого способа является недостаточная просветляющая способность данного просветляющего состава при обработке образцов других биологических тканей и ограничение по толщине обрабатываемого образца.
Ближайшим аналогом заявляемого способа является способ, в котором просветляли целый мозг (размером до 1,5 см) мыши в возрасте 3-5 недель [Dodt H.-U., Leischner U., Shierloh A., Jahrling N., Mauch C.P., Deininger K., Deussing J.M., Eder M., Zieglgansberg W., Becker K. Ultramicroscopy: three-dimensional visualization of neuronal networks in the whole mouse brain // Nature Methods. - 2007. - V.4. - 4. - P.331-336.)]. Мышей после глубокой анестезии перфузировали 4% раствором параформальдегида, извлекали мозг и постфиксировали его 1 ч в 4% растворе параформальдегида при +4°С. Промывали 2 раза в буфере и хранили в нем же при +4°С. Затем дегидратировали ткань в последовательной серии растворов этанола (30%, 50%, 70%, 80%, 96% и два раза в 100% этаноле в течение 24 ч в каждом растворе). Затем инкубировали мозг в гексане в течение 1 ч и просветляли в смеси бензилбензоат : бензиловый спирт в соотношении 2:1 минимум 48 ч. Недостатком данного способа является то, что просветление крупного образца ткани происходит неравномерно по всему объему образца, что при анализе под микроскопом не позволяет лазеру проникнуть вглубь ткани и вследствие этого не во всем объеме образца достигается клеточное разрешение.
В настоящем изобретении решается задача оптического просветления образцов биологических тканей взрослых животных на глубину до 1,5 см для достижения клеточного разрешения за счет снижения оптической плотности равномерно по всему объему образца ткани.
Поставленная задача решается тем, что в предлагаемом способе оптического просветления образцов биологической ткани, включающем фиксацию ткани в растворе формальдегида, дегидратацию в водных растворах спиртов, инкубацию образца ткани в гексане, образец ткани дегидратируют в 2-бутоксиэтаноле, последовательно инкубируют в смеси метанол : диметилсульфоксид: 30% перекись водорода, взятых в соотношении 4:1:1, в течение 1-24 ч, затем в смеси хлороформ : метанол, взятых в соотношении 2-1:1, в течение 1 ч, а затем в гексане в течение 1 ч и в 2-бутоксиэтаноле в течение 24 ч, после чего погружают образец в состав ароматических углеводородов с коэффициентом преломления от 1.548 до 1.558 с последующей выдержкой от 1 до 48 ч.
Поставленная задача решается также тем, что ткань фиксируют погружением образца в 1%-5% раствор параформальдегида в течение 24-48 ч.
Поставленная задача решается также тем, что ткань дегидратируют последовательно в несколько этапов в водных растворах 2-бутоксиэтанола с концентрациями, ступенчато повышающимися от 30% до 100% в течение 1-24 ч на каждом этапе.
Поставленная задача решается также тем, что образец ткани хранят в 2-бутоксиэтаноле при комнатной температуре или при +4°С.
Поставленная задача решается также тем, что в качестве составов ароматических углеводородов используют ароматические углеводороды из группы: этилциннамат или смесь этилциннамата с бензиловым спиртом при их соотношении 2:1, или смесь этилциннамата с метилсалицилатом при их соотношении 3:2 или смесь этилциннамата с ксилолом при их соотношении 6:1, или смесь бензилбензоата с бензиловым спиртом при их соотношении 2:1, или смесь метилсалицилата : бензилбензоата при их соотношении 5:3.
Поставленная задача решается также тем, что образец погружают в этилциннамат, нагретый до температуры +37-40°С.
Поставленная задача решается также тем, что инкубацию просветляемых образцов толщиной 100 до 500 мкм проводят в течение 1 часа.
Поставленная задача решается также тем, что инкубацию просветляемых образцов толщиной 0,5-1,5 см проводят в течение 24 ч.
Поставленная задача решается также тем, что между этапами отбеливания в растворе Дента и инкубации в смеси хлороформ : метанол дополнительно проводят регидратацию образцов в серии спиртов с последовательно понижающейся концентрацией и окраску целиковых образцов стандартными гистологическими методами с последующей дегидратацией.
Поставленная задача решается также тем, что ткань дегидратируют последовательно в несколько этапов в водных растворах 2-бутоксиэтанола с концентрациями, ступенчато повышающимся от 30% до 100% в течение 1-24 ч на каждом этапе.
Поставленная задача решается также тем, что после каждого этапа инкубации образец ткани дополнительно отмывают в 2-бутоксиэтаноле в течение 1-24 ч.
Сущность настоящего изобретения поясняется иллюстративным материалом в виде графиков с показателями оптической плотности и микрофотографий просветленных по способу образцов биологической ткани на фиг.1-4, где:
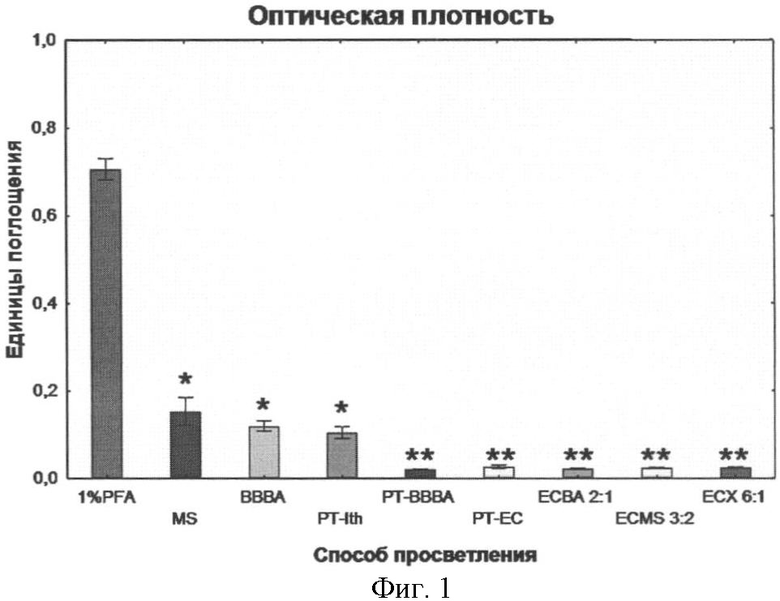
на фиг.1 показана оптическая плотность обонятельных луковиц взрослых мышей после обработки заявленным способом оптического просветления, где указаны параметры оптической плотности при разных способах просветления:
1% PFA - образец, фиксированный 1% раствором параформальдегида;
MS - образец, просветленный известным способом в метилсалицилате (1.536),
ВВВА - образец, просветленный известным способом в смеси бензилбензоат : бензиловый спирт в соотношении 2:1 (1.558);
образцы, просветленные по предлагаемому способу:
предобработка (включающая отбеливание, хлороформ : метанол, гексан, 2-бутоксиэтанол) с последующим просветлением в PT-Ith - 75% водном растворе иоталамата (1.43),
PT-BBBA - предобработка и погружение в бензилбензоат : бензиловый спирт 2:1 (1.558),
РТ-ЕС - предобработка и погружение в этилциннамат (1.558),
ЕСВА 2:1 - предобработка и погружение в этилциннамат : бензиловый спирт 2:1 (1.55),
ECMS 3:2 - предобработка и погружение в этилциннамат : метилсалицилат 3:2 (1.549),
ЕСХ 6:1 - предобработка и погружение в этилциннамат : ксилол 6:1 (1.549);
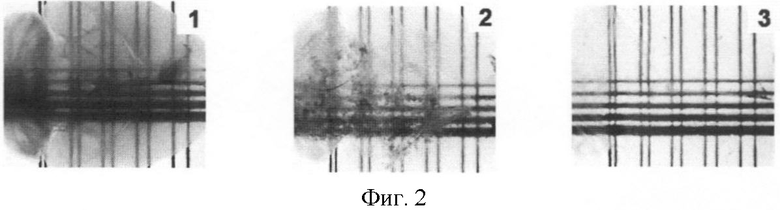
на фиг.2 - представлены микрофотографии оптически просветленных препаратов мозга взрослых мышей с помощью известных способов: 1-е использованием метилсалицилата, 2 - методом Додта и 3 - предлагаемьм способом;
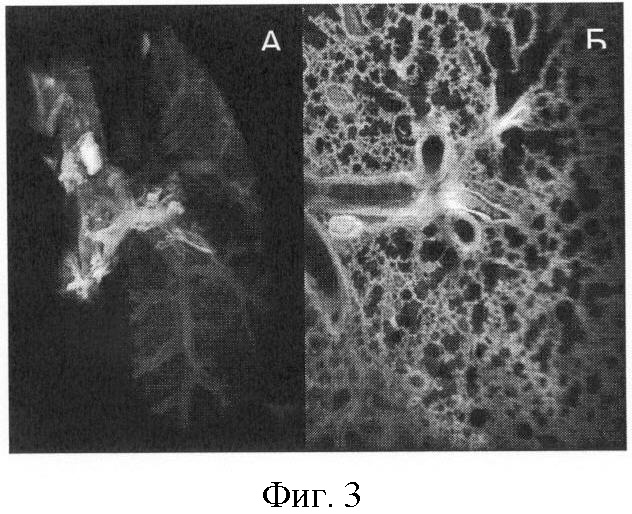
на фиг.3 представлена визуализация морфологии просветленного по разработанному способу легкого мыши, выявленная по его автофлуоресценции на компьютерном оптическом проекционном томографе: А - трехмерная реконструкция доли легкого; Б - оптический срез легкого (зуммирование, позволяющее видеть микроструктуру);
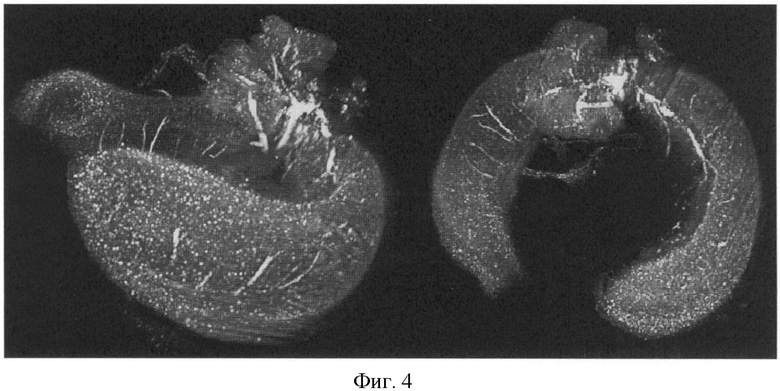
на фиг.4 - представлено проекционное изображение цельного гиппокампа взрослой мыши с экспрессией гена c-fos, выявленной иммуногистохимической окраской с последующим просветлением препарата по предлагаемому способу и визуализацией на компьютерном оптическом проекционном томографе (видна клеточная локализация флуоресцентного маркера по всему объему).
Заявленный способ оптического просветления образцов биологической ткани осуществляют следующим образом.
Образцы биологической ткани (например, обонятельная луковица и гиппокамп взрослой мыши, целый головной мозг взрослой мыши, легкое взрослой мыши) фиксируют в 1% растворе параформальдегида в фосфатно-солевом буфере в случае обонятельных луковиц и гиппокампа или в 4% растворе параформальдегида в фосфатно-солевом буфере в случае целого мозга и легкого в течение 24 ч при +4°С. Всю обработку образцов ткани проводят при постоянном перемешивании и комнатной температуре в полипропиленовых микропробирках объемом 2 мл с плоским дном в объеме растворов 1,5 мл пробирках в случае обонятельной луковицы и гиппокампа и объемом 50 мл в объеме растворов 15 мл в случае целого мозга и легкого. В каждой микропробирке находится один образец ткани. Дегидратируют препараты в 50%, 75%, 95% водных растворах 2-бутоксиэтанола и чистом 2-бутоксиэтаноле в каждом растворе в течение 1 ч в случае обонятельной луковицы и гиппокампа и в течение 24 ч в случае целого мозга и легкого. Затем препараты обесцвечивают в смеси метанол : ДМСО: 30% перекись водорода в соотношении 4:1:1 в течение 1 ч в случае обонятельной луковицы и гиппокампа и в течение 24 ч в случае целого мозга и легкого. В случае препаратов целого мозга проводят отмывку в 2-бутоксиэтаноле в течение 1 ч. Затем препараты инкубируют в гексане в течение 1 ч. В случае препаратов целого мозга проводят отмывку в 2-бутоксиэтаноле в течение 1 ч. Инкубируют в течение 1 ч в смеси хлороформ : метанол в соотношении 1:1 в случае обонятельной луковицы и гиппокампа и в соотношении 2:1 в случае целого мозга и легкого. В случае гиппокампа препарат регидратируют в серии 2-бутоксиэтанола понижающейся концентрации: 70%, 50%, 30% по 60 мин в каждом растворе, окрашивают его по известной методике иммуногистохимии целиковых препаратов и вновь дегидратируют в серии 2-бутоксиэтанола в возрастающей концентрации: 30%, 80%, 96% по 60 мин в каждом растворе. Отмывают препараты в абсолютном 2-бутоксиэтаноле в течение 24 ч, после чего погружают образец в состав ароматических углеводородов с коэффициентом преломления от 1.548 до 1.558: в случае обонятельных луковиц либо в этилциннамат (нагретый до температуры +37-40°С), либо в смесь этилциннамат : бензиловый спирт при их соотношении 2:1, либо в смесь этилциннамат : метилсалицилат при их соотношении 3:2, либо в смесь этилциннамат : ксилол при их соотношении в 6:1, либо в смесь бензилбензоат : бензиловый спирт 2:1, в случае гиппокампа, целого мозга и легкого - в смесь бензилбензоат : бензиловый спирт при их соотношении 2:1 с последующей выдержкой от 1 до 48 ч. Препараты анализировали с помощью методов светлопольной микроскопии и компьютерной оптической проекционной томографии.
Ниже приведены конкретные примеры реализации заявленного способа:
Пример 1.
В качестве образцов ткани взяли изолированные структуры мозга взрослой мыши: обонятельные луковицы. После глубокой анестезии декапитировали взрослых мышей линии С57В 1/6 в возрасте 3-6 месяцев, извлекают головной мозг из черепной коробки, отделяли обонятельные луковицы. Фиксируют луковицы в свежеприготовленном 1% растворе параформальдегида в фосфатно-солевом буфере в течение 24 ч при +4°С. Всю обработку образцов ткани проводят в полипропиленовых микропробирках объемом 2 мл с плоским дном в объеме растворов 1,5 мл при постоянном перемешивании и комнатной температуре. В каждой микропробирке находится один образец ткани. Дегидратируют препарат последовательно в 50%, 75%, 95% водных растворах 2-бутоксиэтанола и чистом 2-бутоксиэтаноле в течение 1 ч в каждом. Часть препаратов для сравнения с известными способами инкубируют в метилсалицилате, в смеси бензилбензоат : бензиловый спирт 2:1 и затем проводят съемку под микроскопом, а остальные инкубируют в свежеприготовленном отбеливателе Дента (метанол : ДМСО: 30% H2O2 4:1:1) 1 ч, в гексане 1 ч, в смеси хлороформ-метанол 1:1 в течение 1 ч, отмывают в 2-бутоксиэтаноле 12 ч и погружают на 1 ч либо в 75% водный раствор производного бензойной кислоты - иоталамата меглумина/натрия либо в смесь бензилбензоат : бензиловый спирт, взятых в соотношении 2:1, либо в этилциннамат либо в этилциннамат : бензиловый спирт с соотношением 2:1, либо в этилциннамат : метилсалицилат 3:2, либо в этилциннамат : ксилол 6:1. Проводят съемку оптически просветленных обонятельных луковиц CCD камерой Nikon DXM 1200 при стандартных условиях в проходящем свете на микроскопе Leica M420 и определяют оптическую плотность образцов в программе Image Pro Plus 3.11 (n=3-4). Анализ оптической плотности является типичной операцией характеристики изображения в программах анализа изображения. Анализ оптической плотности определяет количество материи вещества путем измерения количества света, который он пропускает. Функция стандартной оптической плотности в Image Pro использует следующую формулу расчета стандартной оптической плотности, рассчитанную из оптической интенсивности, описывающую экспоненциальное снижение света внутри материала:
OPTICAL DENSITY(x,y)=-log[(INTENSITY(x,y)-BLACK)/(INCIDENT-BLACK)]
где:
INTENSITY(x,y) - интенсивность пикселя (х,у),
BLACK - интенсивность, когда никакой свет не проходит через материал,
INCIDENT - интенсивность случайного света.
Материал, через который не проходит свет, имеет неопределенную оптическую плотность, а материал, через который свет полностью проходит, имеет оптическую плотность, равную 0. Темные пиксели ведут к высоким значениям оптической плотности, а светлые - к низким. Статическую обработку проводили в программе STATISTICA по непараметрическому тесту Крускал-Уоллиса, различия считали достоверными при p≤0.05.
В результате осуществления данного способа получены данные, представленные на фиг.1. Оптическая плотность фиксированного в растворе параформальдегида образца ткани составляет 0.71±0.05 у.е. поглощения. После обработки образца ткани заявленным способом оптическая плотность снизилась до 0.02±0.01 у.е. Оптическая плотность при обработке ближайшим аналогом приводила к снижению оптической плотности до 0.12±0.01 у.е. Оптическая плотность снизилась у наших образцов на 97% по сравнению с начальным (а у ближайшего аналога - на 83% по сравнению с начальным).
Пример 2.
Для оптического просветления изолированного мозга взрослых мышей линии С57В 1/6 в возрасте 6 месяцев после глубокой анестезии декапитировали, извлекали головной мозг из черепной коробки и фиксировали его в свежеприготовленном 4% растворе параформальдегида в фосфатно-солевом буфере 24 ч при +4°С. Всю обработку образцов ткани проводили в полистироловых пробирках с плоским дном объемом 50 мл в объеме растворов 15 мл при постоянном перемешивании и комнатной температуре, если не указано иначе. В каждой пробирке находился один образец ткани. Часть препаратов целого мозга для сравнения с известными способами дегидратировали по способу Додта в 30%, 50%, 70, 96% и дважды в 100% этаноле в течение 24 ч в каждом и просветляли в смеси бензилбензоат бензиловый спирт при соотношении 2:1. Другую часть препаратов целого мозга дегидратировали по разработанному способу в 50%, 75%, 95% водных растворах 2-бутоксиэтанола и чистом 2-бутоксиэтаноле в течение 24 ч в каждом и инкубировали в свежеприготовленном отбеливателе Дента (метанол : ДМСО: 30% H2O2 4:1:1) 24 ч, отмывали в 2-бутоксиэтаноле в течение 1 ч, инкубировали в гексане в течение 1 ч, отмывали в 2-бутоксиэтаноле в течение 1 ч, инкубировали в смеси хлороформ-метанол 2:1 в течение 1 ч, отмывали в 2-бутоксиэтаноле в течение 24 ч и погружали в смесь бензилбензоат : бензиловый спирт в соотношении 2:1 либо в метилсалицилат на 48 ч. Проводили съемку CCD камерой Nikon DXM 1200 при стандартных условиях в проходящем свете на микроскопе Leica M420 на фоне референтной шкалы, которая располагалась под препаратом.
Полученные микрофотографии представлены на фиг.2. На микрофотографии 1 приведен мозг взрослой мыши после предобработки по предлагаемому способу, но с погружением на последнем этапе в метилсалицилат. На микрофотографии 2 - мозг мыши после просветления по методу Додта. На микрофотографии 3 - мозг мыши, просветленный с использованием разработанного способа. Референтная шкала, находящаяся под образцом, почти не видна на недостаточно просветленных препаратах. Когда оптическая плотность образца снижается, шкала становится видна (3).
Пример 3.
Для оптического просветления изолированного легкого взрослых мышей линии С57В 1/6 в возрасте 3 месяцев после глубокой анестезии декапитировали, извлекали легкие из брюшной полости и фиксировали их в свежеприготовленном 4% растворе параформальдегида в фосфатно-солевом буфере 24 ч при +4°С. Всю обработку образцов ткани проводили в полистироловых пробирках с плоским дном объемом 50 мл в объеме растворов 15 мл при постоянном перемешивании и комнатной температуре, если не указано иначе. В каждой пробирке находился один образец ткани. Дегидратировали препарат в 50%, 75%, 95% водных растворах 2-бутоксиэтанола и чистом 2-бутоксиэтаноле в течение 24 ч в каждом. Инкубировали в свежеприготовленном отбеливателе Дента (метанол : ДМСО: 30% H2O2 4:1:1) 24 ч, в гексане 1 ч, в смеси хлороформ-метанол 2:1 в течение 1 ч и отмывали в 2-бутоксиэтаноле в течение 24 ч. Обработанные препараты оптически просветляли в смеси бензилбензоат : бензиловый спирт в соотношении 2:1 в течение 48 ч. Проводили съемку на компьютерном оптическом проекционном томографе.
Полученные данные представлены на Фиг.3: А - изолированное легкое мыши после фиксации, Б - легкое после просветления по разработанному протоколу. Референтная шкала, находящаяся под образцом, не видна до просветления (А), а когда образец становится оптически прозрачным после просветления, она начинает просвечивать (Б).
Пример 4.
Для оптического просветления изолированного гиппокампа взрослой мыши после иммуногистоимического окрашивания у взрослых самцов мышей линии 129sv в возрасте около 50-60-х постнатальных суток вызывали индукцию экспрессии c-fos в модели условно-рефлекторного замирания на контекст. Для этого мышь помещали в незнакомую экспериментальную камеру и через 2,5 мин наносили болезненный удар током 0,5 А по лапам длительностью 2 с. После этого животное выдерживали в камере еще 30 с, а затем возвращали в домашнюю клетку. Декапитацию производили на пике индуцируемой экспрессии - через 90 мин от начала эксперимента. Затем у животных извлекали мозг и фиксировали его в 1% растворе ПФА при 4°С в течение 24 ч. После этого из мозга извлекали гиппокамп и дегидратировали его в 50%, 75%, 95% водных растворах 2-бутоксиэтанола и чистом 2-бутоксиэтаноле в течение 1 ч в каждом. Для уменьшения собственной пигментации мозга и обесцвечивания кровеносных сосудов образцы 1 ч инкубировали в отбеливателе - метанол : ДМСО: 30% H2O2 в соотношении 4:1:1 при комнатной температуре до полного их обесцвечивания. Для увеличения проницаемости образцов для антител производили пять циклов заморозки в абсолютном метаноле до -70°С и нагревания до комнатной температуры. После этого этапа препараты обрабатывали в течение 1 ч гексаном и 1 ч в смеси хлороформ : метанол 1:1, а затем регидратировали при комнатной температуре в серии 2-бутоксиэтанола понижающейся концентрации: 70%, 50%, 30% по 60 мин в каждом растворе. Окончательную отмывку существляли 0,1 М фосфатным буфером в течение 90 мин. Регидратированные препараты инкубировали либо в растворе кроличьих первичных антител к белку c-Fos (Ab-5, «Oncogene Research Products», Великобритания, в разведении 1:2000), либо к Egrl (sc-189, «Santa Cruz Biotech. Inc.», США, разведение 1:500) в TrisBST (0,05 M Tris-HCl, pH 7,5; 0,15 M NaCl, 0,1 M Triton X-100) с 5% DMSO и 0,01% азидом Na. Для снижения фоновой окраски, вызванной неспецифическим связыванием антител, в инкубационную смесь также добавляли 2% раствор рыбьего желатина («Sigma», США). Инкубацию производили при 4°С в течение 72 ч при постоянном помешивании со скоростью 650 оборотов в минуту. После инкубации с первичными антителами образцы отмывали 4-5 раз по 2-3 ч TrisBST при 4°С, последнюю отмывку осуществляли в течение ночи. Места связывания первичных антител выявляли инкубацией образцов со вторичными противокроличьими флуоресцентными антителами Alexa Fluor 488 (Fab-фрагменты, «Molecular Probes», США, 1:500) в 5% DMSO и 0,1% Triton X-100 в течение 24 ч при 4°С. По завершении инкубации со вторичными антителами образцы отмывали 3-4 раза по 2-3 ч TrisBST при 4°С, последнюю отмывку осуществляли в течение ночи. Оптическое просветление окрашенных целиком препаратов после дегидратации в серии 2-бутоксиэтанола в возрастающей концентрации: 30%, 80%, 96% по 60 мин в каждом растворе и 100% 2-бутоксиэтанол в течение ночи осуществляли в просветляющем составе, состоящем из смеси бензилбензоата и бензилового спирта в соотношении 2:1 в течение 12-18 ч. Съемку препаратов проводили на компьютерном оптическом проекционном томографе.
Образцы гипрокампа становятся оптически прозрачным после просветления, при этом не наблюдается потери флуоресцентного сигнала и достигается клеточное разрешение по всей глубине образца (Фиг.4).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ИММУНОГИСТОХИМИЧЕСКОГО ОКРАШИВАНИЯ ТОТАЛЬНЫХ ПРЕПАРАТОВ ОБРАЗЦОВ БИОЛОГИЧЕСКИХ ТКАНЕЙ (ВАРИАНТЫ) | 2013 |
|
RU2563679C2 |
| СПОСОБ ОКРАШИВАНИЯ ПРЕПАРАТОВ ЦЕЛЬНЫХ БИОЛОГИЧЕСКИХ ТКАНЕЙ И ОРГАНОВ МЕТОДОМ КЛИК-ГИСТОХИМИИ (ВАРИАНТЫ) | 2016 |
|
RU2620559C1 |
| Метод иммуноокрашивания биологического материала для конфокальной микроскопии | 2019 |
|
RU2700410C1 |
| СПОСОБ ВИЗУАЛИЗАЦИИ БИОЛОГИЧЕСКИХ ТКАНЕЙ И/ИЛИ ОРГАНОВ | 2019 |
|
RU2735463C1 |
| СПОСОБ ЛАЗЕРНОЙ БИОМОДУЛЯЦИИ И ПОВЫШЕНИЯ ПРОНИЦАЕМОСТИ ГЕМАТОЭНЦЕФАЛИЧЕСКОГО БАРЬЕРА | 2019 |
|
RU2740123C1 |
| Среда для изготовления постоянных микропрепаратов из биологических объектов | 1989 |
|
SU1725093A1 |
| СПОСОБ СТИМУЛЯЦИИ НЕЙРОГЕНЕЗА В ГИППОКАМПЕ | 2017 |
|
RU2675111C2 |
| ПРИМЕНЕНИЕ ФАКТОРА РОСТА НЕРВОВ В ГЛАЗНЫХ КАПЛЯХ ДЛЯ ЛЕЧЕНИЯ ПАТОЛОГИЙ ЦЕНТРАЛЬНОЙ НЕРВНОЙ СИСТЕМЫ, ТАКИХ КАК БОЛЕЗНЬ АЛЬЦГЕЙМЕРА И ПАРКИНСОНА | 2006 |
|
RU2429007C2 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ГИСТОЛОГИЧЕСКИХ ПРЕПАРАТОВ И КОМПОЗИЦИИ ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ (ВАРИАНТЫ) | 2009 |
|
RU2408887C1 |
| Среда для изготовления постоянных микропрепаратов из биологических объектов | 1989 |
|
SU1725094A1 |
Изобретение относится к способу оптического просветления образцов биологической ткани. Способ включает фиксацию ткани в растворе формальдегида, дегидратацию в водных растворах спиртов и инкубацию образца ткани в гексане. Дегидратацию образца ткани осуществляют в 2-бутоксиэтаноле. Затем образец последовательно инкубируют в смеси метанол : диметилсульфоксид: 30% перекись водорода, взятых в соотношении 4:1:1, в течение 1-24 ч, после - в смеси хлороформ : метанол, взятых в соотношении 2-1:1, в течение 1 ч, а затем в гексане в течение 1 ч и в 2-бутоксиэтаноле в течение 24 ч. После чего образец погружают в состав ароматических углеводородов с коэффициентом преломления от 1,548 до 1,558 с последующей выдержкой от 1 до 48 ч. Достигаемый при этом технический результат заключается в достижении равномерного оптического просветления образцов биологических тканей. 10 з.п. ф-лы, 4 ил.
1. Способ оптического просветления образцов биологической ткани, включающий фиксацию ткани в растворе формальдегида, дегидратацию в водных растворах спиртов, инкубацию образца ткани в гексане, отличающийся тем, что образец ткани дегидратируют в 2-бутоксиэтаноле, затем последовательно инкубируют в смеси метанол : диметилсульфоксид : 30%-ная перекись водорода, взятых в соотношении 4:1:1, в течение 1-24 ч, затем в смеси хлороформ : метанол, взятых в соотношении 2-1:1, в течение 1 ч, а затем в гексане в течение 1 ч и в 2-бутоксиэтаноле в течение 24 ч, после чего погружают образец в состав ароматических углеводородов с коэффициентом преломления от 1,548 до 1,558 с последующей выдержкой от 1 до 48 ч.
2. Способ по п.1, отличающийся тем, что для фиксации образца ткани используют метод погружения в свежеприготовленный раствор 1-5% параформальдегида в фосфатно-солевом буфере в течение 24-48 ч.
3. Способ по п.1, отличающийся тем, что ткань дегидратируют последовательно в несколько этапов в водных растворах 2-бутоксиэтанола с концентрациями, ступенчато повышающимися от 30 до 100% в течение 1-24 ч на каждом этапе.
4. Способ по п.1, отличающийся тем, что образец ткани хранят в 2-бутоксиэтаноле при комнатной температуре или при +4°С.
5. Способ по п.1, отличающийся тем, что в качестве составов ароматических углеводородов используют ароматические углеводороды из группы: этилциннамат, или смесь этилциннамата с бензиловым спиртом при их соотношении 2:1, или смесь этилциннамата с метил салицилатом при их соотношении 3:2, или смесь этилциннамата с ксилолом при их соотношении 6:1, или смесь бензилбензоата с бензиловым спиртом при их соотношении 2:1, или смесь метилсалицилата : бензилбензоата при их соотношении 5:3.
6. Способ по п.5, отличающийся тем, что образец погружают в этилциннамат, нагретый до температуры 37-40°С.
7. Способ по п.1, отличающийся тем, что инкубацию в смеси метанол : диметилсульфоксид : 30%-ная перекись водорода, взятых в соотношении 4:1:1 просветляемых образцов толщиной от 100 до 500 мкм проводят в течение 1 ч.
8. Способ по п.1, отличающийся тем, что инкубацию в смеси метанол : диметилсульфоксид : 30%-ная перекись водорода, взятых в соотношении 4:1:1, просветляемых образцов толщиной от 0,5 до 1,5 см проводят в течение 24 ч.
9. Способ по п.1, отличающийся тем, что между этапами инкубации в смеси метанол : диметилсульфоксид : 30%-ная перекись водорода, взятых в соотношении 4:1:1, в течение 1-24 ч и инкубации в смеси хлороформ : метанол дополнительно проводят регидратацию образцов в серии спиртов с последовательно понижающейся концентрацией и окраску стандартными гистологическими методами целиковых образцов с последующей дегидратацией в 2-бутоксиэтаноле.
10. Способ по п.9, отличающийся тем, что ткань дегидратируют последовательно в несколько этапов в водных растворах 2-бутоксиэтанола с концентрациями, ступенчато повышающимся от 30 до 100% в течение 1-24 ч на каждом этапе.
11. Способ по п.1, отличающийся тем, что после каждого этапа инкубации образец ткани дополнительно отмывают в 2-бутоксиэтаноле в течение 1-24 ч.
| Способ осветления реакционной смеси для фотометрического измерения биологических проб | 1979 |
|
SU1443816A3 |
| RU 2001115008 А, 10.03.2003 | |||
| US 6465208 В1, 15.10.2002 | |||
| СЪЕМНАЯ ЛАПА ДЛЯ БАРАБАНОВ ПОЧВООБРАБАТЫВАЮЩИХ ФРЕЗЕРНЫХ МАШИН | 1929 |
|
SU20846A1 |
| Способ подготовки биологических препаратов к микроскопическим исследованиям | 1984 |
|
SU1254344A1 |
| Способ подготовки к исследованию инвазионного материала | 1985 |
|
SU1409927A1 |
Авторы
Даты
2011-09-20—Публикация
2009-10-14—Подача