Область техники, к которой относится изобретение
Изобретение относится к биотехнологии и генной инженерии, может быть использовано в медицине для ранней диагностики рака желудка и касается способа использования генетически модифицированных бактерий Helicobacter pylori в качестве бактериального сенсора.
Уровень техники
В настоящее время в мире разрабатываются новые высокопроизводительные, неинвазивные и эффективные методы детекции химических и биологических агентов, имеющих значение для медицинской диагностики, мониторинга окружающей среды, контроля безопасности продуктов питания. Одним из таких направлений является разработка биосенсоров, представляющих собой биологическую систему, способную генерировать измеряемый сигнал в ответ на появление (изменение) специфического агента во внешнем окружении [1]. Биосенсорные системы можно разделить на три основных типа, в зависимости от сенсорного компонента: молекулярные, клеточные и тканевые [2-4]. Для создания молекулярных биосенсорных систем используются субклеточные элементы или макромолекулы: антитела, нуклеиновые кислоты, ферменты, ионные каналы и липидный бислой. Основным преимуществом таких систем является высокая специфичность, селективность и быстрота проведения реакции. Однако при использовании таких систем невозможно получить функциональную информацию, в частности, о биосовместимости аналитов. Кроме того, длительность выделения и экстракции макромолекул, с учетом относительно короткого время их жизни, накладывает ограничения на использование этих биосенсорных систем.
Генетически модифицированные клеточные системы стабильны при различных условиях внешней среды, включая изменение температуры или pH. Более того, данные системы могут быть специально адаптированы для идентификации химических токсинов и генотоксинов.
В разработке Rupani и др. [5] была использована бактерия Escherichia coli, трансформированная генно-инженерной конструкцией, состоящей из репортерной системы lux (люцифераза) под контролем промотора белка теплового шока GrpE. Оценивался эффект температуры, стадии роста и индуктора (этанол), концентрация этанола на кинетику и уровень люминесценции.
В другой работе был получен транскрипционный составной белок в Escherichia coli из репортерной системы luxCDABE под контролем промоторов белков UspA и GrpE и проведена оценка интенсивности флуоресцентного ответа при высоких температурах. Было показано, что никель и кобальт в концентрации 0.3 мкМ уже вызывают увеличение экспрессии cnrYXH-luxCDABE [6].
Таким образом, применение клеточных биосенсорных систем является наиболее перспективным инструментом для разработки роботизированных, малозатратных, количественных методов для быстрой и селективной детекции химических и биологических агентов в области медицинской диагностики, мониторинга окружающей среды, безопасности продуктов питания. Уникальность данных технологий заключается в регистрации процессов, происходящих в интактной, живой клеточной системе в режиме реального времени.
Техническим результатом, на который направлено изобретение, является повышение быстродействия и достоверности показаний бактериального сенсора в широком диапазоне изменений pH.
Для этого предложен бактериальный сенсор для детекции изменения pH, где сенсорным элементом является бактериальная клетка Helicobacter pylori, содержащая плазмиду pHP с бактериальным геном gfp под контролем индуцибельного стрессового промотора PflaA.
Бактериальная клетка Helicobacter pylori трансформируется плазмидой pHP, в составе которой находится бактериальный ген gfp под контролем индуцибельного стрессового промотора PflaA. При изменении pH окружающей среды в кислую сторону происходит активация индуцибельного промотора PflaA, повышение уровня экспрессии гена gfp и, соответственно, усиление регистрируемой флуоресценции. При изменении рН окружающей среды в щелочную сторону происходит репрессия индуцибельного промотора PflaA, снижение уровня экспрессии гена gfp и, соответственно, ослабление регистрируемой флуоресценции. Отличительной особенностью сенсора является стабильность бактериальной клетки как в сильно кислых, так и в сильно щелочных, а также мгновенный ответ сенсора на изменение pH, выражающийся в достоверном изменении флуоресценции.
Использование в качестве бактериального сенсора именно H.pylori объясняется тем, что эта бактерия (в отличие от используемых ранее бактерий для создания различных биосенсоров) в силу ограниченных метаболических возможностей в значительной степени зависит от состояния окружающей среды, в том числе и от состояния колонизируемой эпителиальной клетки. Таким образом, перестройка метаболических потоков в бактерии при изменении состояния хозяина и/или окружающей среды является причиной и следствием активации генетического аппарата микроорганизма, что выражается в изменении уровня экспрессии генов.
Helicobacter pylori - грамотрицательная, микроаэрофильная бактерия, колонизирующая слизистую желудка у примерно половины мирового населения. Инфекция H.pylori, являющаяся причиной хронического воспаления, часто не имеет клинических проявлений, но приблизительно у 10% инфицированных она ассоциирована с язвенной болезнью желудка и двенадцатиперстной кишки, атрофическими гастритами, аденокарциномой или экстранодальной В-клеточной MALT-лимфомой [7]. В связи с этим использование в качестве биосенсора этой бактерии позволит проводить раннюю диагностику неопластических процессов в желудке.
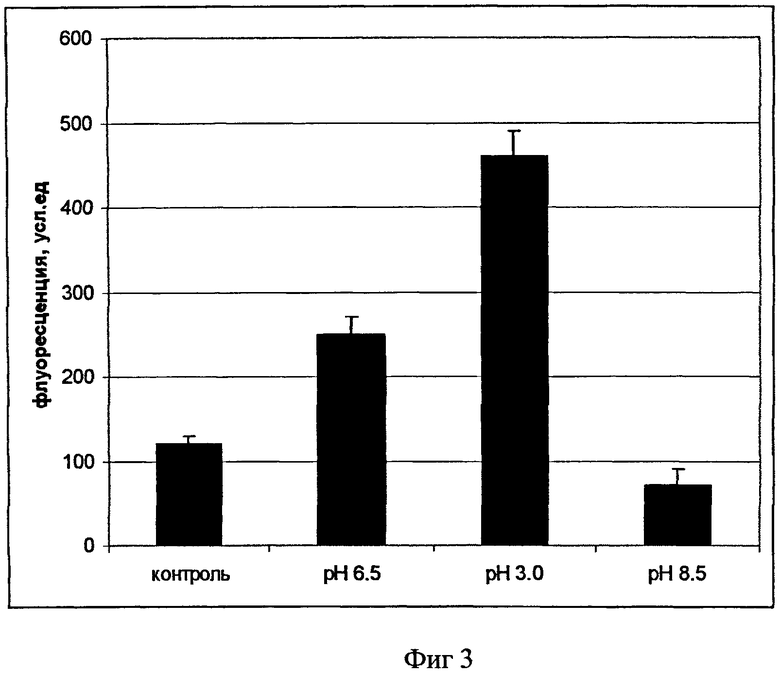
На фигуре 1 дано схематическое изображение плазмиды pHel. Нуклеотидную последовательность, соответствующую индуцибельному стрессовому промотору PflaA, синтезируют на автоматическом синтезаторе нуклеиновых кислот ASM-700 (Биоссет, Россия) и клонируют в плазмидный вектор pHP [8] по сайту рестрикции NcoI, содержащий ген GFP и ген устойчивости к хлорамфениколу. Нуклеотидная последовательность индуцибельного стрессового промотора PflaA приведена на фигуре 2. Полученной плазмидой трансформируют бактерии Helicobacter pylori для получения модифицированных бактерий.
Примеры реализации изобретения
1. Трансформация Helicobacter pylori плазмидным вектором pHP
Культуру клеток H.pylori, выросшую на чашках, в течение 24 часов суспендируют в среде BHI (Biomerieux, France) и добавляют к ним плазмиду pHP, после чего наносят каплями на поверхность агаризованной среды BHI. Чашки с агаром инкубируют в течение суток при 37°С и 5% CO2. По окончании трансформации клетки смывают физиологическим раствором и распределяют по поверхности агара, содержащего антибиотик хлорамфеникол (10 мкг/мл). Трансформанты детектируют на 5-7 день инкубации. Для получения модифицированного штамма Helicobacter pylori отдельные колонии отбирают пипеткой, суспендируют в жидкой питательной среде BHI, содержащей 10% FBS (HyClone, США), 5% дрожжевого экстракта (МедГамал, Россия) и хлорамфеникол в указанной концентрации. Жидкую культуру штамма поддерживают пассированием каждые 48 часов в присутствии антибиотика.
2. Детекция изменения pH среды с использованием бактериального сенсора на основе штамма бактерий Helicobacter pylori
Бактериальный штамм Helicobacter pylori, трансформированный плазмидой pHP, культивируют в течение 24 ч в жидкой питательной среде BHI, содержащей 10% FBS (HyClone, США), 5% дрожжевого экстракта (МедГамал, Россия) и 10 мкг/мл хлорамфеникола. Отбирают четыре порции культуры по 1 мл и центрифугируют при 6000 об/мин 10 мин. Осадок промывают 1 мл физиологического раствора и ресуспендируют в 1 мл жидкой среды BHI (pH 7.0) без добавок. В опытные пробирки добавляют 10 мкл 1н. соляной кислоты (pH 6.5), 50 мкл 1н. соляной кислоты (pH 3.0) и 10 мкл 1н. гидроксида натрия (pH 8.5). На предметное стекло наносят по 1 капле культуры из опытных и контрольной пробирок. Регистрацию флуоресценции проводят с использованием флуоресцентного микроскопа Eclipse C800 (Nikon, Япония). Результаты опыта по изменению флуоресценции клеток штамма Helicobacter pylori, трансформированного плазмидой pHP, при изменении pH приведены на фигуре 3.
Литература
1. Siontorou C.G., Batzias F.А. // Crit Rev Biotechnol. - 2010. - V.30. - P.79-98.
2. Pancrazio J.J., Whelan J.P., Borkholder D.A., Ma W., Stenger D.A. // Ann Biomed Eng. - 1999. - V.27. - P.697-711.
3. Wanekaya A.K., Chen W., Mulchandani A. // J Environ Monit. - 2008. - V.10. - P.703-712.
4. Wilson G.S., Ammam M. // FEBS J. - 2007. - V.274. - P.5452-5461.
5. Rupani S.P., Gu M.B., Konstantinov K.B., Dhurjati P.S., Van Dyk Т.K., LaRossa R.A. // Biotechnol Prog. - 1996. - V.12. - P.387-392.
6. Van Dyk Т.K., Smulski D.R., Reed T.R., Belkin S., Vollmer A.C., LaRossa R.A. // Appl Environ Microbiol. 1995. - V.61. - P.412-417.
7. Polk D.B., Peek R.M. Jr. // Nat Rev Cancer. - 2010. - V.10. - P.403-414.
8. Heuermann D., Haas R. // Mol Gen Genet. - 1998. - V.257. - P.519-528.
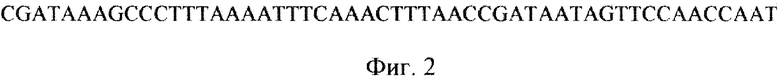
Изобретение относится к биотехнологии и генной инженерии, а именно к бактериальному сенсору для детекции изменения pH. Изобретение может быть использовано в медицине для ранней диагностики рака желудка. Сенсорным элементом является бактериальная клетка Helicobacter pylori, содержащая плазмиду pHP, представленную на фиг.1, с бактериальным геном gfp под контролем индуцибельного стрессового промотора PflaA. Предложенное изобретение позволяет быстро и достоверно измерять pH в широком диапазоне. 3 ил., 2 пр.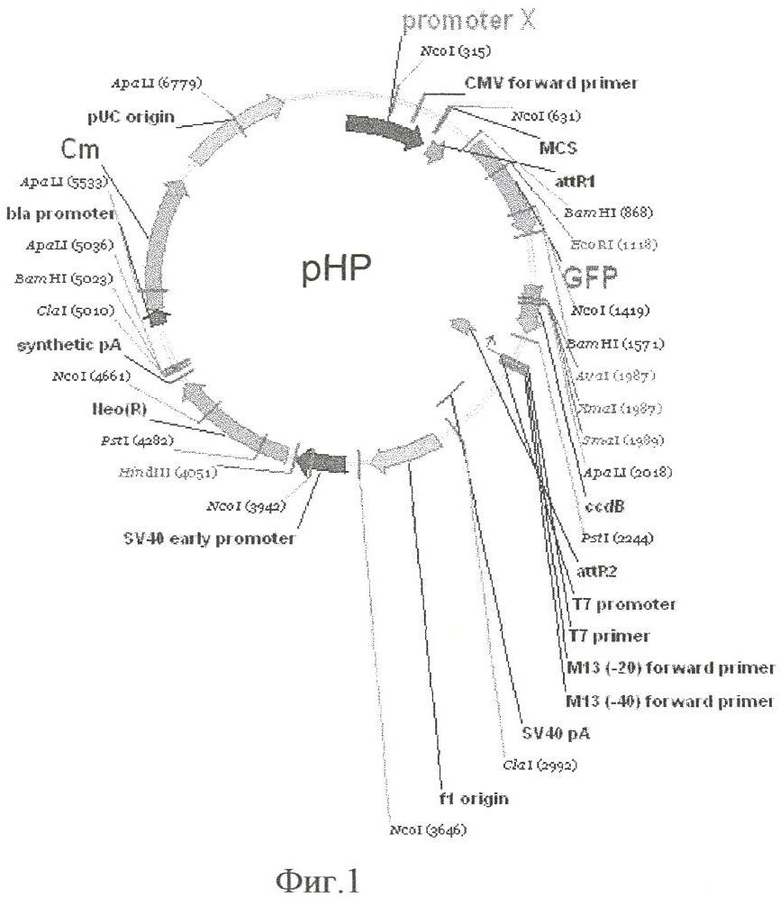
Бактериальный сенсор для детекции изменения pH, отличающийся тем, что сенсорным элементом является бактериальная клетка Helicobacter pylori, содержащая плазмиду pHP, представленную на фиг.1, с бактериальным геном gfp под контролем индуцибельного стрессового промотора PflaA.
| МОМЫНАЛИЕВ К.Т | |||
| и др | |||
| Разработка биологических датчиков, созданных на основе микроорганизмов с ограниченной емкостью генома, для диагностики патологий человека, электронное издание «Наука и технология России», 07.08.2007 | |||
| JOSENHANS С | |||
| ЕТ AL., Green fluorescent protein as a novel marker and reporter system in Helicobacter sp., FEMS Microbiol |
Авторы
Даты
2012-08-10—Публикация
2010-10-04—Подача