Изобретение относится к способу получения чистого халькопирита (CuFeS2) из растворов, содержащих металлы, с использованием ацидотолерантных сульфатредуцирующих бактерий (АСРБ).
Халькопирит - основная руда для получения меди в пирометаллургическом процессе. Медь применяется в электротехнике, в машиностроении, для получения сплавов (бронза, латунь, томпак), для изготовления змеевиков, перегонных кубов, холодильников, труб.
Предложенный способ можно использовать для получения чистого халькопирита из сточных вод, содержащих металлы, и жидких отходов добывающих и перерабатывающих металлургических предприятий, шахтных дренажных вод. Удаление меди из воды в форме сульфидов в настоящее время является одной из наиболее действенных технологий. Использование сульфидогенных бактерий, производящих в результате своей жизнедеятельности сероводород, позволило значительно снизить себестоимость и увеличить эффективность по сравнению с используемым ранее химическим процессом, основанным на внесении NaHS или газообразного H2S. Важным развитием биотехнологического процесса очистки сточных вод явилось его развитие в сторону селективного осаждения металлов, которое позволит вторичное использованием ценных металлов, извлекаемых из отходов.
Биотехнологическое осаждение сульфидов меди из растворов также может быть использовано в качестве составляющей биогидрометаллургической добычи меди, когда маточный раствор с высокой концентрацией металла, полученный при кучном выщелачивании забалансовых руд, направляется затем в цикл осаждения биогенным сероводородом с целью получения концентрата сульфида меди высокого качества. Таким образом, рециклирование меди из сточных вод с получением чистого халькопирита одновременно снижает нагрузку на окружающую среду, оказываемую горнодобывающей и металлургической промышленностью.
Сульфиды металлов могут быть получены химическими методами, например в химической реакции непосредственным соединением металлов с серой. Известен способ получения сульфидов металлов, включая сульфид меди, по технологии самораспространяющегося высокотемпературного синтеза (СВС) (патент РФ №2189944, C01G 1/12, 2000 г.). Данный способ относится к области неорганической химии и включает прессование исходного вещества, воспламенение, сжигание и синтез сульфида металла в режиме горения в атмосфере инертного газа при давлении 0,1-5 МПа. В качестве исходного вещества используют порошкообразную смесь кислородсодержащего соединения металла с серосодержащим органическим веществом при мольном соотношении металла и серы, равном 1:(1-2), соответственно. Недостатками способа является большая энергозатратность производства, необходимость использования специального дорогостоящего оборудования. Кроме того, в качестве исходного вещества используют химически чистые соединения металла, что повышает себестоимость полученных сульфидов металлов. Необходимо отметить и вред, наносимый окружающей среде химическим производством.
Мировым лидером в разработке биотехнологических процессов для осаждения и рециклирования металлов с использованием сульфидогенных микроорганизмов является голландская компания Paques BV [Информационный сайт «Paques» [Электронный ресурс] // Режим доступа: http://www.paques.nl/en/about_paques (свободный)]. Одним из полномасштабных процессов, основанных на осаждении металлов микробным сероводородом, является процесс Sulfateq™, основанный на технологиях Thioteq. Процесс Thioteq состоит из двух стадий: химической и биологической. Раствор, содержащий металлы, подвергается обработке только на химической стадии. Сульфид образуется в отдельном биореакторе и подается в химический реактор с использованием газа-носителя. Содержание сульфида меди в продукт осаждения обычно составляет не менее 90%. Полученные в результате осаждения сульфиды металлов могут поступать в металлургический процесс в качестве концентрата высокого качества. Разобщение процессов производства H2S и осаждения сульфидов связано с токсичностью высоких концентраций меди для бактерий. Разъединение процессов образования сероводорода бактериями и осаждения металлов является одним из основных недостатков технологий. Известно, что микроорганизмы являются важными сайтами нуклеации при осаждении металлов, это ускоряет процессы их осаждения. Разъединение процесса на два реактора - микробиологический и химический, значительно удлиняет процесс образования сульфидов металлов во времени, снижая количество сайтов нуклеации. Необходимость создания двух реакторов также ведет к удорожанию биотехнологии.
В заявленном способе используются ацидотолерантные СРБ, устойчивые к повышенным концентрациям меди и низким значениям pH. Это позволяет осуществлять процесс образования халькопирита в одном реакторе.
Известено образование сульфидов меди видами Desulfovibrio, устойчивыми к меди (Geomicrobiology Journal, 25:219-227, 2008, O.V.Karnachuk; K.Sasaki; A.L.Gerasimchuk; O.Sukhanova; D.A.Ivasenko; A.M.Kaksonen; J.A.Puhakka; O.H.Tuovinen). Образование сульфидов меди (ковеллита, халькоцита, халькопирита) осуществляется сульфатредуцирующими бактериями рода Desulfovibrio. Недостатками с точки зрения налаживания технологического процесса является образование халькопирита (CuFeS2) в смеси в другими сульфидами меди и железа: халькоцитом (Cu2S), ковеллитом (CuS), смититом (Fe9S11).
Наиболее близким по сущности и достигаемому результату к заявленному изобретению является способ получения сульфида меди ковеллита (CuS) путем помещения высокоустойчивых к ионам меди сульфатредуцирующих бактерий в синтетическую среду, содержащую металлы, с добавлением питательных веществ, включающих в себя растворы витаминов, солей, кофакторов, лактата, сульфида натрия, с дальнейшим культивированием при температуре 28°C и высушиванием. При культивировании сульфатредуцирующих бактерий в емкости располагают стеклянные пластины, культивирование при температуре 28°C проводят в течение 8 суток, после высушивания со стеклянных пластин извлекают осадок, содержащий ковеллит (патент РФ №2426783, C12N 1/20, опубл. 20.08.2011).
Недостатками известного способа является то, что в данных условиях образуются исключительно кристаллы ковеллита, получение халькопирита невозможно. В данном способе образование сульфида меди, ковеллита происходит с использованием штаммов сульфатредуцирующих бактерий, растущих на среде с нейтральным pH. Сточные воды горнодобывающих предприятий часто имеют кислую реакцию среды, что затрудняет получение сульфидов металлов с помощью бактерий. Использование АСРБ может решить эту проблему.
Задачей настоящего изобретения является разработка способа получения халькопирита, не содержащего примеси других сульфидов металлов, с использованием ацидотолерантных сульфатредуцирующих бактерий, устойчивых к меди и низким значениям pH.
Поставленная задача решается путем помещения высокоустойчивых к ионам меди АСРБ в синтетическую среду, моделирующую сточные воды, содержащие металлы, с добавлением питательных веществ, включающих в себя растворы витаминов, солей, кофакторов, лактата, сульфида натрия, с дальнейшим культивированием в термостате и высушиванием, но в отличие от прототипа, используются штаммы АСРБ, выращиваемые в кислой среде, в среду добавляется металлическое железо, культивирование проводят при температуре 28°C. Стеклянные пластины при осуществлении данного способа не нужны. После вырастания культуры на дне флакона образуется осадок, содержащий халькопирит.
Культивирование проводят в синтетической среде (таблица 1) с внесением питательных веществ, стимулирующих рост бактерий.
В синтетическую среду перед посевом культуры бактерий вносятся питательные вещества. Состав питательных веществ и последовательность их внесения указаны в таблице 2. Все питательные вещества, кроме витаминов, автоклавируют при 1 атм 30 мин. Витамины стерилизуют фильтрованием с помощью бактериального фильтра (0,20 мкм).
При культивировании АСРБ, необходимых для выполнения предложенного способа, для посева берутся емкости на 120 мл. Культивирование в стеклянных емкостях с добавлением металлического железа проводят в лабораторных условиях. В промышленных масштабах возможно использование биореактора с добавлением металлического железа в виде железной проволоки.
Посев проводят в стерильные емкости, объем инокулята (культуры АСРБ) в количестве 10% от объема емкости. Емкости с инокулятом заливают синтетической средой (со всеми внесенными питательными веществами) до верха. pH среды доводят до 3,5 раствором 1 н. H2SO4. Флаконы закрывают алюминиевыми колпачками, запечатывают и помещают в термостат при температуре 28°C. Образование халькопирита происходит на дне емкости. После культивирования осадок собирают центрифугированием и высушивают на воздухе.
Пример осуществления изобретения в лабораторных условиях приведен ниже.
Пример 1.
Чистую ацидотолерантную культуру СРБ Desulfosporosinus sp.DB культивировали на кислой синтетической среде (начальная pH 3,5), содержащей металлы и металлическое железо, в том числе ионы меди в концентрации 200 мг/л. Штамм Desulfosporosinus sp.DB способен расти при концентрации меди в среде 5000 мг/л. Кристаллы халькопирита получали на дне флакона объемом 120 мл. Флаконы с металлическим железом в виде железной проволоки стерилизовали сухим жаром в стерилизаторе при 160°C 2,2 часа.
Посев проводили в стерильном ламинарном шкафу, который перед этим дезинфицировали ультрафиолетом 30 минут. Перед посевом синтетическую среду доводили до кипения и затем быстро охлаждали под струей холодной воды для удаления растворенного кислорода. В охлажденную до комнатной температуры среду вносили питательные вещества (таблица 2) (в расчете на 1 л) в следующей последовательности: витамины (2 мл), раствор солей (10 мл), раствор кофакторов (1 мл), органический субстрат-лактат (1,6 мл), раствор 1 н. H2SO4 (pH доводили до 3,5), раствор сульфида натрия (2 мл). Стоковый раствор меди добавляли в количестве 4 мл на 1 литр синтетической среды (таким образом достигалась концентрация меди в среде 200 мг/л).
Во флаконы вносили около 50 мл синтетической среды с внесенными в нее добавками и 10 мл инокулята (культуры бактерий), после чего доливали средой до верха. Резиновые пробки притирали к краям флаконов с помощью стерильной иглы, что уменьшало вероятность проникновения кислорода воздуха. В конце посева флаконы закрывали алюминиевыми колпачками, запечатывали флакон закаточной машинкой и помещали термостат при температуре 28°C.
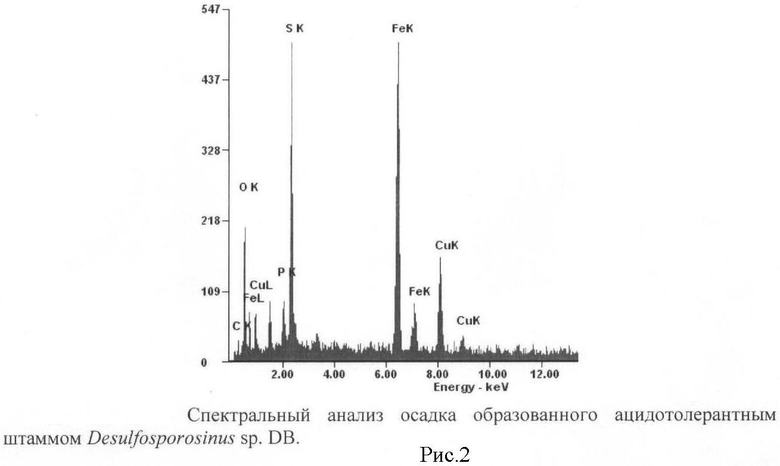
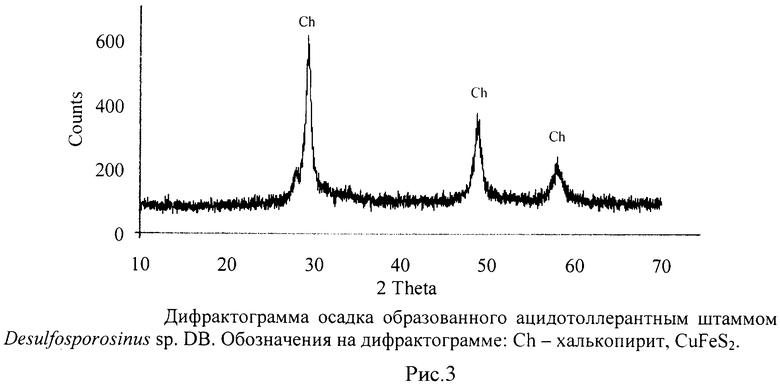
Образованный осадок собирали центрифугированием и высушивали на воздухе. Масса образовавшегося осадка 0,42 г. Размер кристаллов, определенный под сканирующим электронным микроскопом, составлял 100-150 мкм (рисунок 1). Спектральный анализ кристаллов осадка, совмещенный с наблюдением под сканирующим микроскопом (SEM-EDAX), показал наличие пиков Cu, Fe и S (рисунок 2). Измеренное соотношение атомов меди, железа и серы в осадке составляло 1:1,08:2,5, что максимально приближенно к соотношению этих элементов в халькопирите. Небольшие количества Cl и K происходили из синтетической среды, использованной для роста бактерий. Их удаление достигается промывкой дистиллированной водой. Дифракционный анализ, проводимый на дифрактометре Shimadzu XRD600, показал наличие единственной кристаллической фазы - халькопирита (рисунок 3).
Предлагаемый способ включает в себя возможность использования в качестве синтетической среды для получения халькопирита кислых сточных вод и жидких отходов добывающих и перерабатывающих металлургических предприятий.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ КОВЕЛЛИТА С ИСПОЛЬЗОВАНИЕМ СУЛЬФАТРЕДУЦИРУЮЩИХ БАКТЕРИЙ, УСТОЙЧИВЫХ К МЕДИ | 2010 |
|
RU2426783C1 |
| СПОСОБ ПОЛУЧЕНИЯ МИЛЛЕРИТА С ИСПОЛЬЗОВАНИЕМ СУЛЬФАТРЕДУЦИРУЮЩИХ БАКТЕРИЙ | 2012 |
|
RU2528777C2 |
| СПОСОБ ПОЛУЧЕНИЯ СУЛЬФИДА КАДМИЯ С ИСПОЛЬЗОВАНИЕМ СУЛЬФАТРЕДУЦИРУЮЩИХ БАКТЕРИЙ | 2013 |
|
RU2526456C1 |
| СПОСОБ ПОЛУЧЕНИЯ СУЛЬФИДОВ КОБАЛЬТА С ИСПОЛЬЗОВАНИЕМ ШТАММА БАКТЕРИИ DESULFOVIBRIO SP. | 2016 |
|
RU2637389C1 |
| ШТАММ БАКТЕРИЙ DESULFOVIBRIO SP. ДЛЯ ОЧИСТКИ СТОЧНЫХ ВОД ОТ ИОНОВ ТЯЖЕЛЫХ МЕТАЛЛОВ | 2013 |
|
RU2542402C1 |
| АЦИДОФИЛЬНЫЙ ШТАММ DESULFOSPOROSINUS SP. ДЛЯ ОЧИСТКИ ЗАГРЯЗНЕННЫХ ЭКОСИСТЕМ С ЭКСТРЕМАЛЬНО КИСЛЫМИ ЗНАЧЕНИЯМИ ОТ ИОНОВ ТЯЖЕЛЫХ МЕТАЛЛОВ | 2015 |
|
RU2603277C1 |
| ШТАММ БАКТЕРИЙ DESULFOVIBRIO SP. VK-9 ДЛЯ ОЧИСТКИ КИСЛЫХ СТОЧНЫХ ВОД ОТ ИОНОВ ТЯЖЕЛЫХ МЕТАЛЛОВ | 2015 |
|
RU2603249C1 |
| ШТАММ БАКТЕРИЙ DESULFOVIBRIO DESULFURICANS, ИСПОЛЬЗУЕМЫЙ ДЛЯ ОЧИСТКИ ПРОМЫШЛЕННЫХ СТОЧНЫХ ВОД ОТ ИОНОВ ТЯЖЕЛЫХ МЕТАЛЛОВ | 1991 |
|
RU2017814C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЖИДКИХ УГЛЕВОДОРОДОВ | 1991 |
|
RU2027760C1 |
| СПОСОБ ВЫЩЕЛАЧИВАНИЯ ХАЛЬКОПИРИТА | 1997 |
|
RU2180360C2 |

Изобретение относится к способу получения чистого халькопирита (CuFeS2) из растворов, содержащих металлы, с использованием ацидотолерантных сульфатредуцирующих бактерий (АСРБ). Способ получения халькопирита путем помещения ацидотолерантных, высокоустойчивых к ионам меди сульфатредуцирующих бактерий в синтетическую среду, содержащую металлы, с добавлением питательных веществ, включающих в себя растворы витаминов, солей, кофакторов, лактата, сульфида натрия, с дальнейшим культивированием при температуре 28°С. При культивировании сульфатредуцирующих бактерий в емкости добавляют металлическое железо, культивирование проводят в кислой среде при температуре 28°С, собранный со дна флакона осадок, содержащий халькопирит, центрифугируют и высушивают. 3 ил., 2 табл., 1 пр.
Способ получения халькопирита путем помещения ацидотолерантных, высокоустойчивых к ионам меди сульфатредуцирующих бактерий в синтетическую среду, содержащую металлы, с добавлением питательных веществ, включающих в себя растворы витаминов, солей, кофакторов, лактата, сульфида натрия, с дальнейшим культивированием при температуре 28°С, отличающийся тем, что при культивировании сульфатредуцирующих бактерий в емкости добавляют металлическое железо, культивирование проводят в кислой среде при температуре 28°С, собранный со дна флакона осадок, содержащий халькопирит, центрифугируют и высушивают.
| RU 22426783 C1, 20.08.2011 | |||
| СПОСОБ ПОЛУЧЕНИЯ СУЛЬФИДА МЕТАЛЛА | 2000 |
|
RU2189944C2 |
| БУТОРОВА О.П | |||
| и др | |||
| Образование сульфидов металлов чистыми культурами сульфатредуцирующих бактерий, устойчивых к ионам меди // Актуальные аспекты современной микробиологии | |||
| V Молодежная школа-конференция с международным участием | |||
| Тезисы | |||
| - М., 2009. | |||
Авторы
Даты
2013-05-20—Публикация
2012-03-12—Подача