Текст описания приведен в факсимильном виде.








































































































| название | год | авторы | номер документа |
|---|---|---|---|
| КОНЪЮГАТЫ ЛЕКАРСТВЕННЫХ СРЕДСТВ, СОДЕРЖАЩИЕ АНТИТЕЛА ПРОТИВ КЛАУДИНА 18.2 | 2016 |
|
RU2841168C2 |
| ЛЕКАРСТВЕННЫЕ КОНЪЮГАТЫ ИЗ МОНОКЛОНАЛЬНЫХ АГЕНТОВ, СВЯЗЫВАЮЩИХ cMET, И ИХ ПРИМЕНЕНИЕ | 2019 |
|
RU2813828C2 |
| СВЯЗЫВАЮЩИЕ ПРОТЕИНЫ, СПЕЦИФИЧНЫЕ ПО ОТНОШЕНИЮ К ИНСУЛИН-ПОДОБНЫМ ФАКТОРАМ РОСТА, И ИХ ИСПОЛЬЗОВАНИЕ | 2013 |
|
RU2549703C2 |
| НАЦЕЛЕННЫЕ НА uPARAP КОНЪЮГАТЫ АНТИТЕЛО-ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2017 |
|
RU2740311C2 |
| АНТИТЕЛО ПРОТИВ КЛАУДИНА 18.2 И ЕГО КОНЪЮГАТ АНТИТЕЛО-ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2022 |
|
RU2814164C2 |
| АНТИТЕЛА ПРОТИВ CTLA4 И ИХ ПРИМЕНЕНИЯ | 2017 |
|
RU2779312C2 |
| АНТИТЕЛА И МЕТОДЫ АНАЛИЗА ДЛЯ ОБНАРУЖЕНИЯ РЕЦЕПТОРА ФОЛИЕВОЙ КИСЛОТЫ 1 | 2014 |
|
RU2725825C2 |
| АНТИТЕЛА ПРОТИВ CD40 И ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2796413C2 |
| НОВЫЕ АНТИТЕЛА ПРОТИВ PD-L1 | 2016 |
|
RU2736151C2 |
| АНТИТЕЛА ПРОТИВ OX40 И ИХ ПРИМЕНЕНИЯ | 2017 |
|
RU2783314C2 |
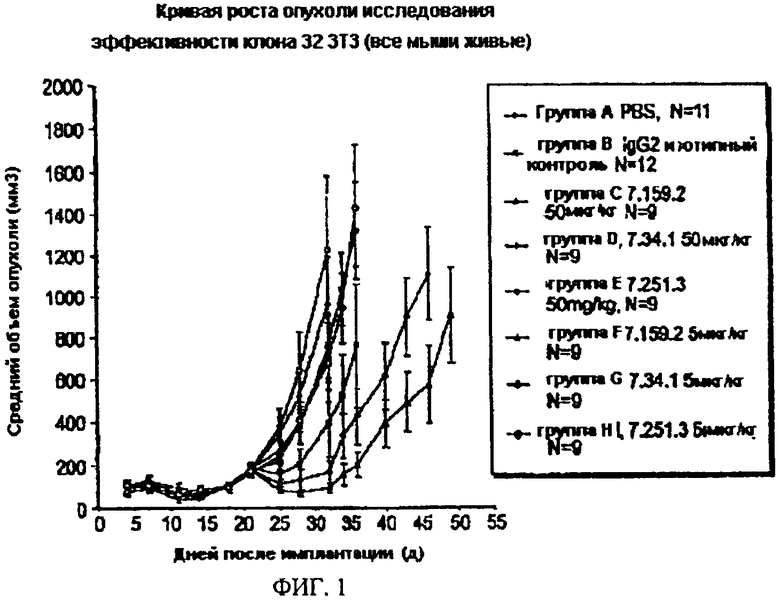
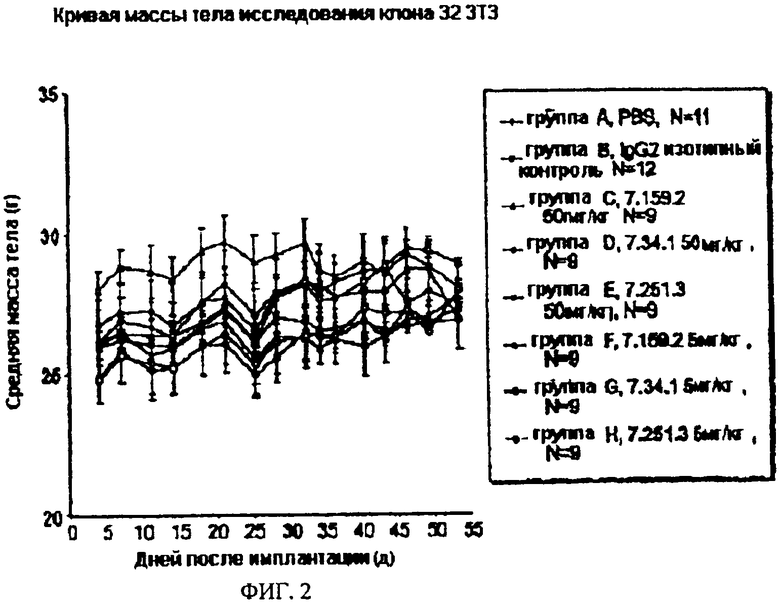
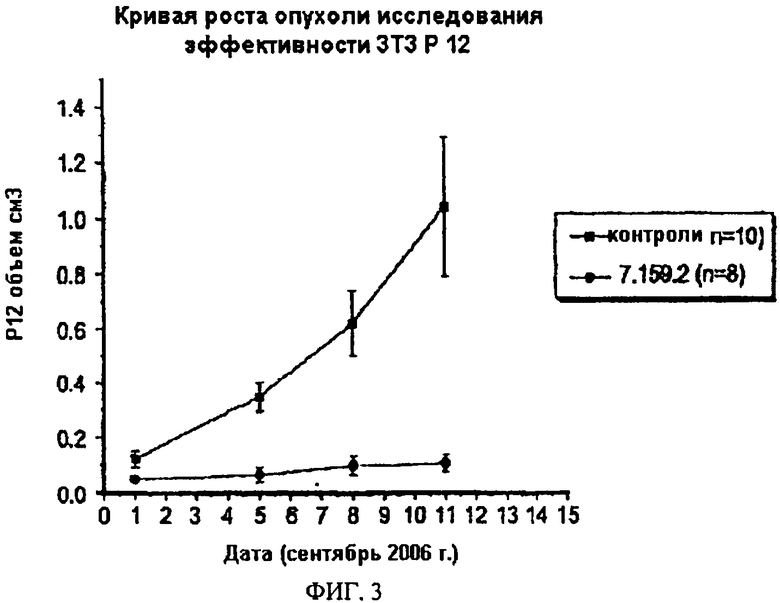
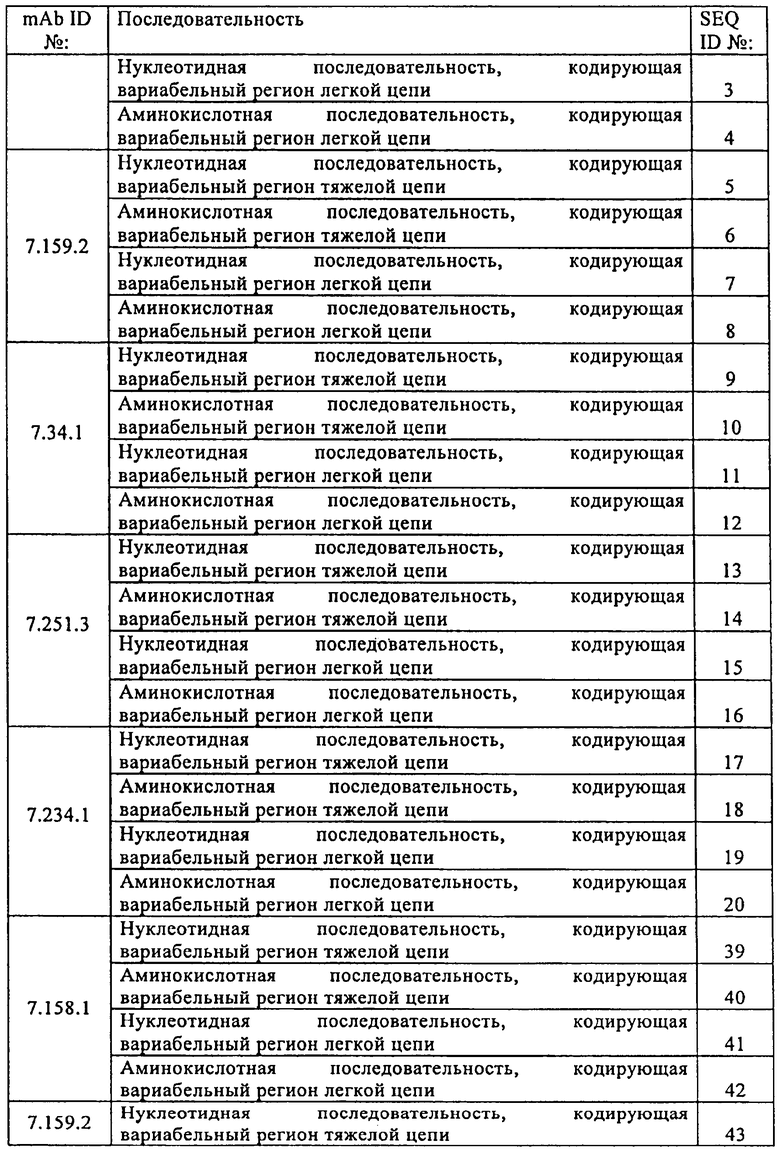
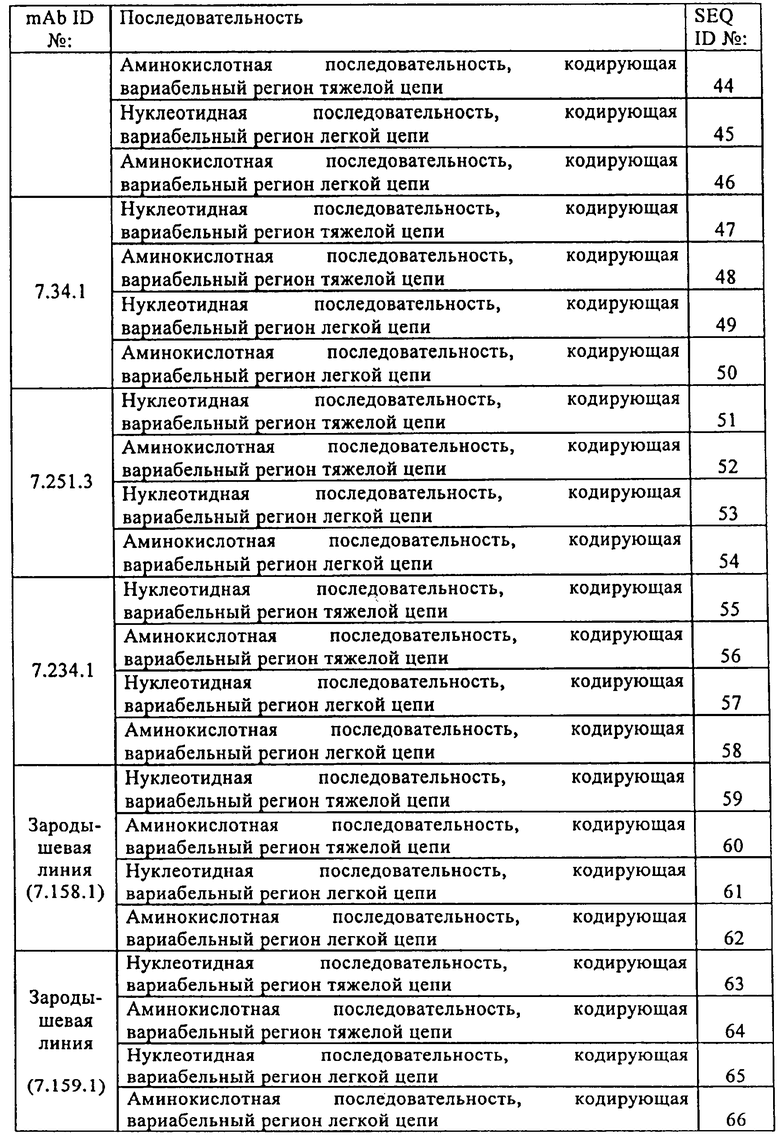
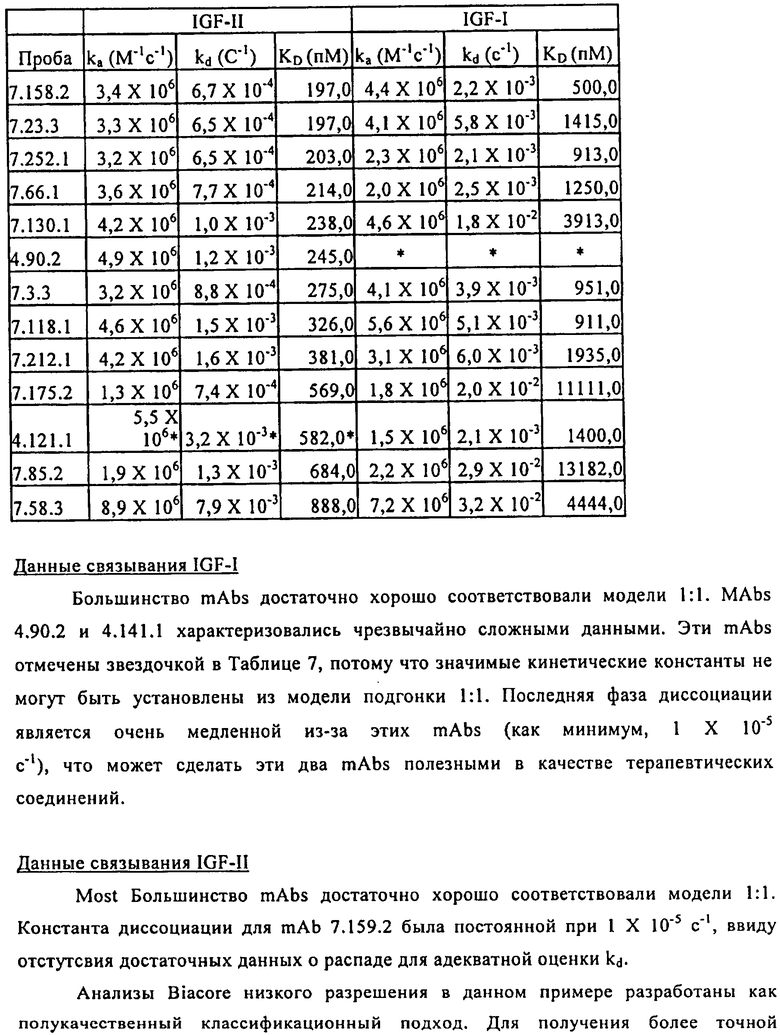
Настоящее изобретение относится к области иммунологии. Предложено полностью человеческое моноклональное антитело, которое связывает инсулиноподобный фактор роста-II (IGF-II) и имеет перекрестную реактивность к IGF-I, а также его антигенсвязывающий фрагмент. Рассмотрены молекула нуклеиновой кислоты, кодирующая антитело по изобретению, вектор и клетка-хозяин для экспрессии антитела по изобретению. Описана фармацевтическая композиция, а также конъюгаты для лечения и диагностики злокачественной опухоли, применение антитела по изобретению в получении лекарственного средства и способ определения уровня IGF-II и IGF-I в пробе пациента. Настоящее изобретение может найти дальнейшее применение в терапии рака. 15 н. и 40 з.п. ф-лы, 27 пр., 18 табл., 3 ил.
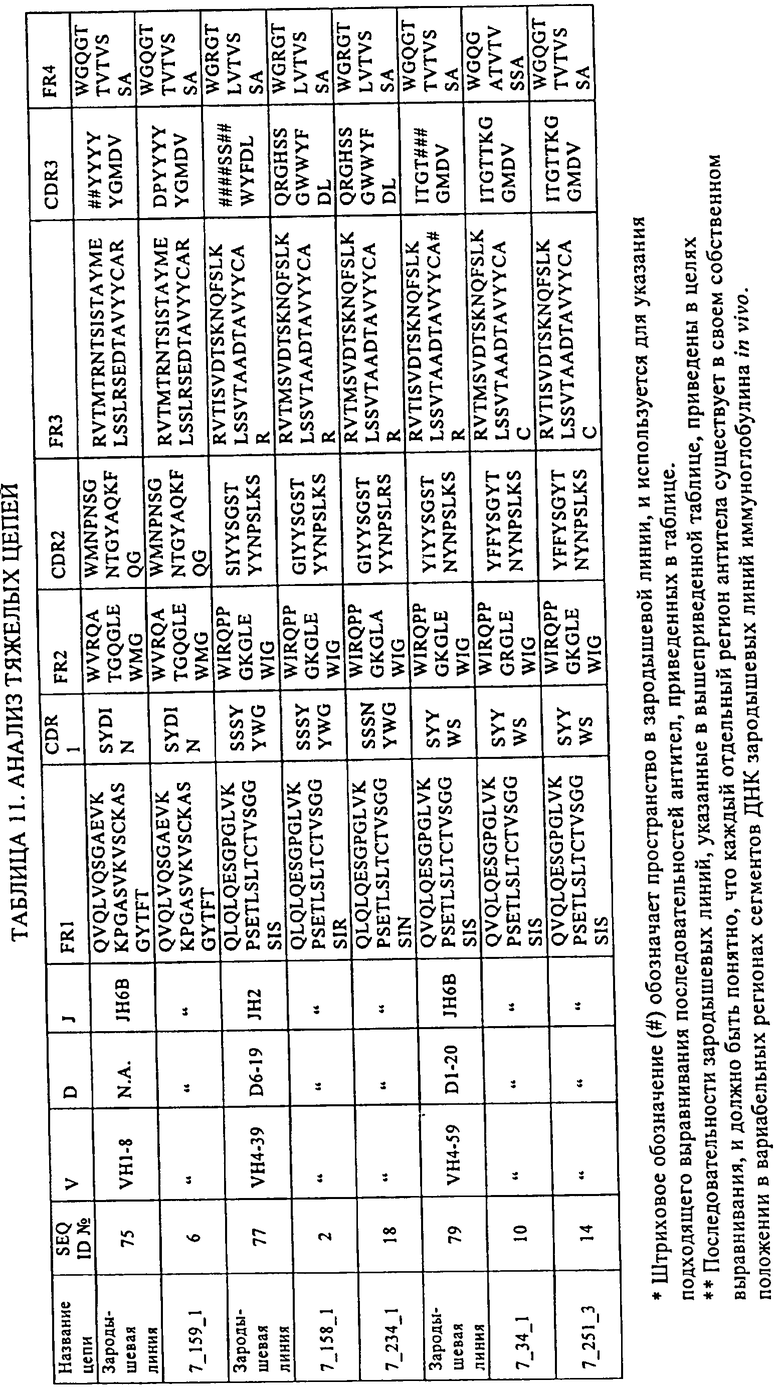
1. Полностью человеческое антитело или его антигенсвязывающий фрагмент, который связывает инсулиноподобный фактор роста-II (IGF-II), имеет перекрестную реактивность к инсулиноподобному фактору роста I (IGF-I) и нейтрализует активность IGF-I и IGF-II, где указанное антитело или его связывающий фрагмент включает
определяющую комплементарность область 1 тяжелой цепи (CDR1), имеющую аминокислотную последовательность «Ser Tyr Asp Ile Asn» (SEQ ID №33);
определяющую комплементарность область 2 тяжелой цепи (CDR2), имеющую аминокислотную последовательность «Туг Met Asn Pro Asn Ser Gly Asn Thr Gly Tyr Ala Gln Lys Phe Gln Gly» (SEQ ID №34);
определяющую комплементарность область 3 тяжелой цепи (CDR3), имеющую аминокислотную последовательность «Asp Pro Tyr Tyr Tyr Tyr Tyr Gly Met Asp Val» (SEQ ID №35);
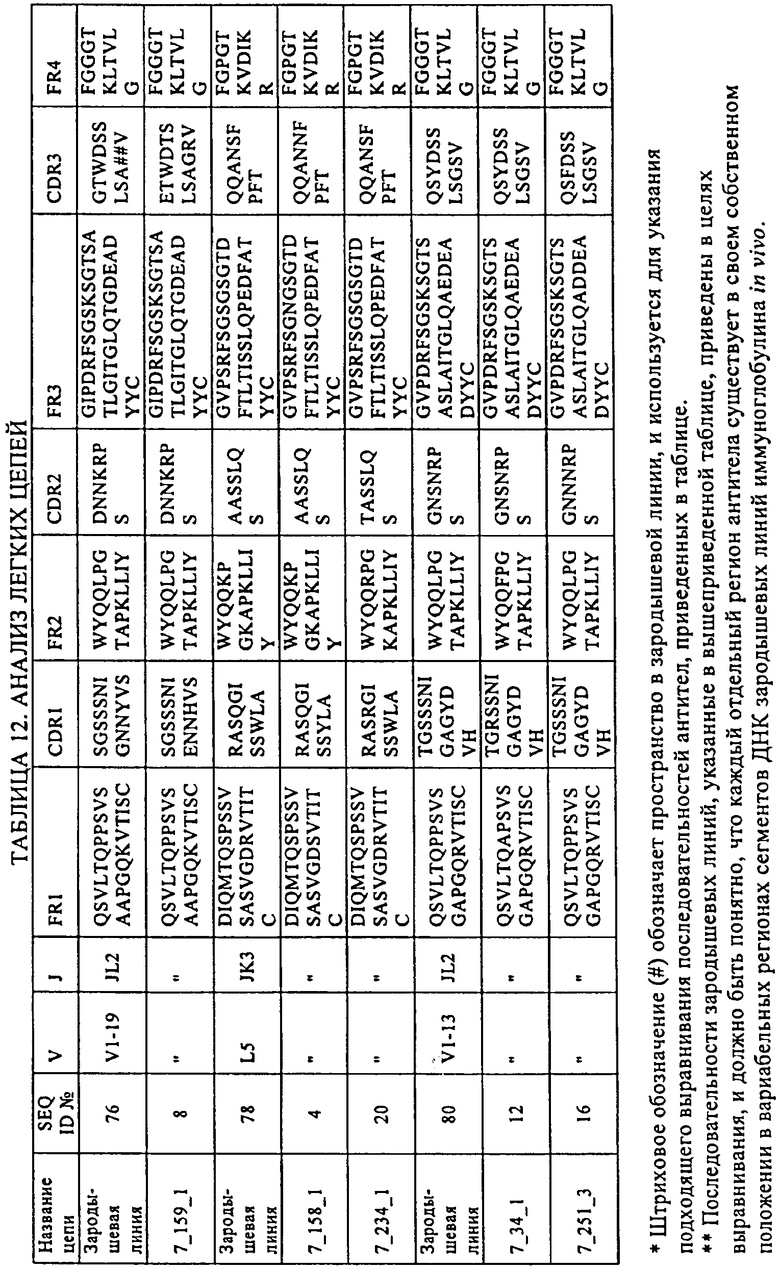
определяющую комплементарность область 1 легкой цепи (CDR1), имеющую аминокислотную последовательность «Ser Gly Ser Ser Ser Asn Ile Glu Asn Asn His Val Ser» (SEQ ID №36);
определяющую комплементарность область 2 легкой цепи (CDR2), имеющую аминокислотную последовательность «Asp Asn Asn Lys Arg Pro Ser» (SEQ ID №37); и
определяющую комплементарность область 3 легкой цепи (CDR3), имеющую аминокислотную последовательность «Glu Thr Trp Asp Thr Ser Leu Ser Ala Gly Arg Val» (SEQ ID №38).
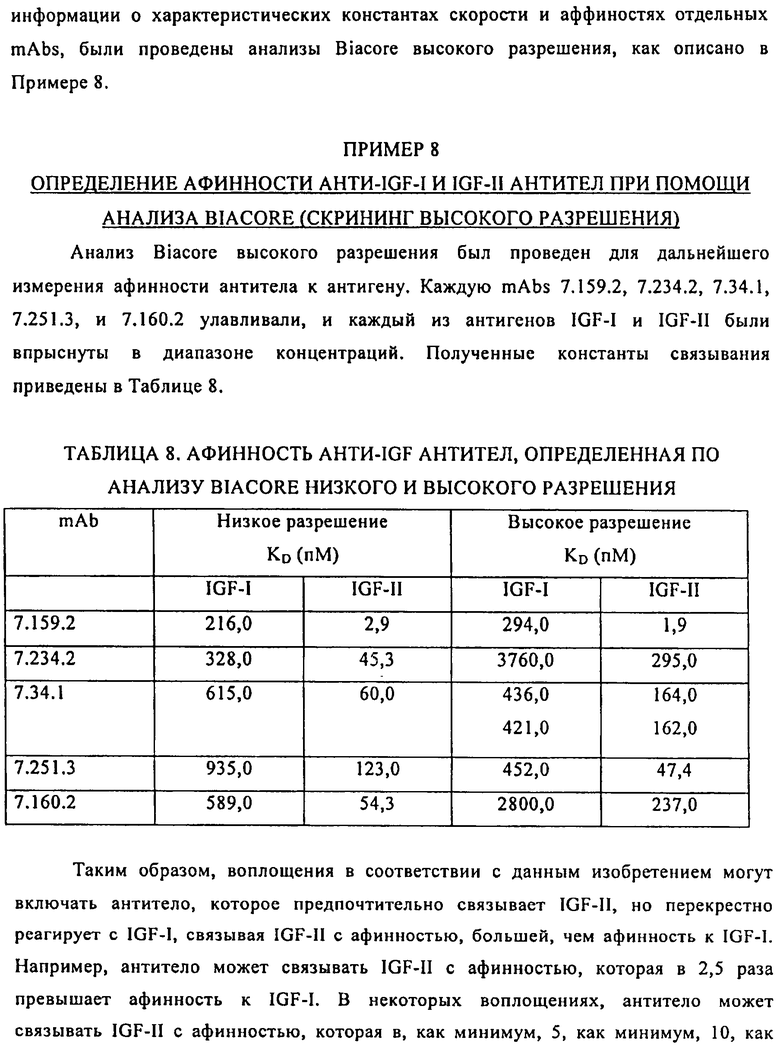
2. Антитело или его антигенсвязывающий фрагмент по п.1, где указанное антитело или его антигенсвязывающий фрагмент связывает IGF-II с аффинностью, которая как минимум в 2,5 раза превышает его аффинность по отношению к IGF-I.
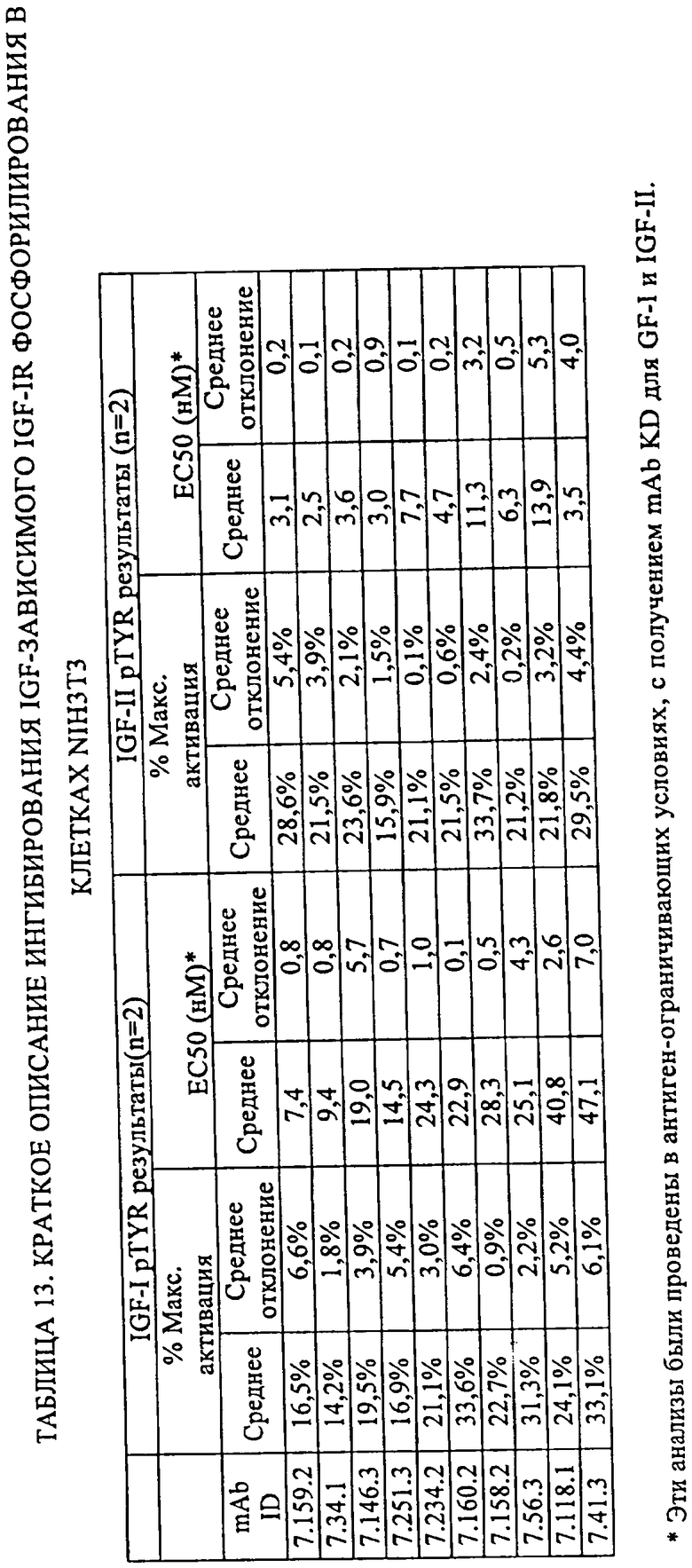
3. Антитело или его антигенсвязывающий фрагмент по п.1, где указанное антитело или его антигенсвязывающий фрагмент имеет EC50 не более 15 нМ для ингибирования IGF-I-зависимого фосфорилирования рецептора IGF-I в клетках NIH3T3, которые эктопически экспрессируют IGF-IR.
4. Антитело или его антигенсвязывающий фрагмент по п.1, где указанное антитело или его антигенсвязывающий фрагмент имеет значение EC50, не превышающее 5 нМ для ингибирования IGF-II-зависимого фосфорилирования рецептора IGF-I в клетках NIH3T3, которые эктопически экспрессируют IGF-IR.
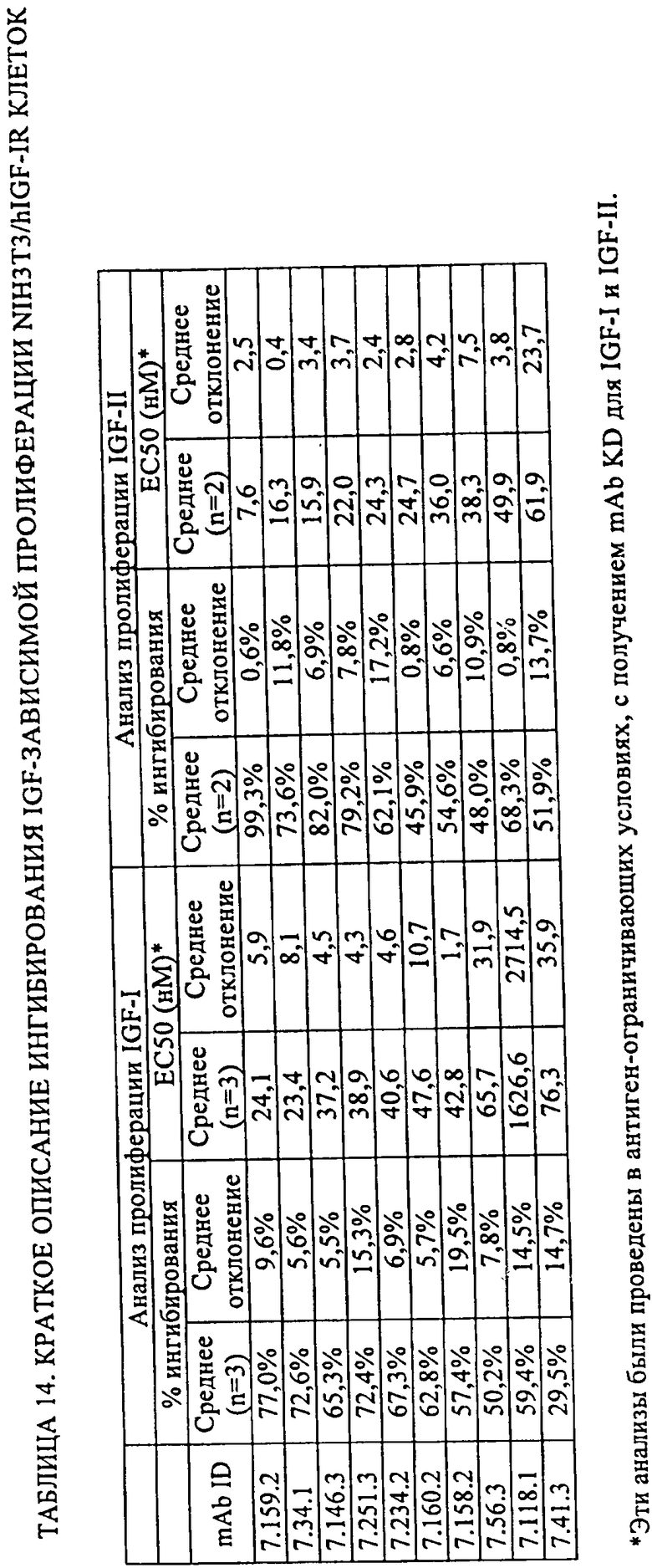
5. Антитело или его антигенсвязывающий фрагмент по п.1, где указанное антитело или его антигенсвязывающий фрагмент ингибирует более чем 70% IGF-II-зависимой пролиферации клеток NIH3T3, которые экспрессируют рекомбинантный hIGF-IR, а значение EC50 не превышает 25 нМ.
6. Антитело или его антигенсвязывающий фрагмент по п.1, где указанное антитело или его антигенсвязывающий фрагмент ингибирует более чем 70% IGF-I-зависимой пролиферации клеток NIH3T3, которые экспрессируют рекомбинантный hIGF-IR, а значение EC50 не превышает 40 нМ.
7. Антитело или его антигенсвязывающий фрагмент по п.1, где указанное антитело или его антигенсвязывающий фрагмент конкурирует за связывание с моноклональным антителом, которое содержит вариабельную область тяжелой цепи, имеющую аминокислотную последовательность SEQ ID №:6.
8. Антитело или его антигенсвязывающий фрагмент по п.7, где указанное моноклональное антитело содержит вариабельную область легкой цепи, имеющую аминокислотную последовательность SEQ ID №:8.
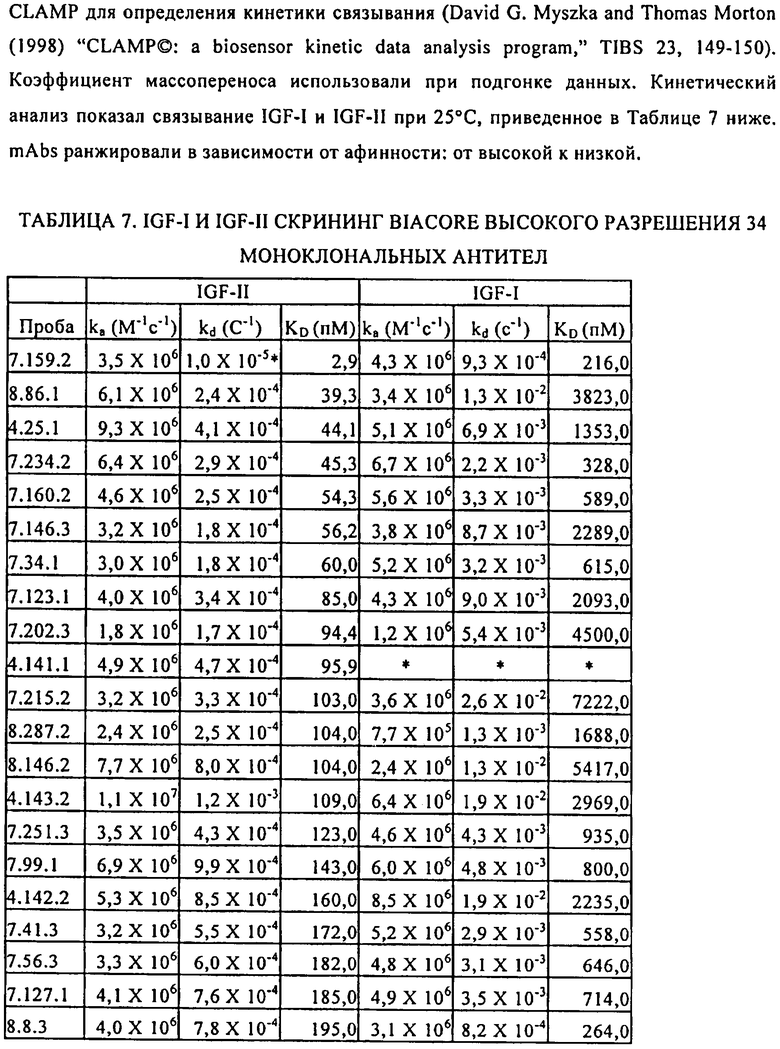
9. Антитело или его антигенсвязывающий фрагмент по любому из пп.1-8, где указанное антитело или его антигенсвязывающий фрагмент связывает IGF-I с KD менее чем 4 нМ.
10. Антитело или его антигенсвязывающий фрагмент по любому из пп.1-8, где указанное антитело или его антигенсвязывающий фрагмент связывает IGF-I с KD менее чем 650 нМ.
11. Антитело или его антигенсвязывающий фрагмент по любому из пп.1-8, где указанное антитело или его антигенсвязывающий фрагмент связывает IGF-II с KD менее чем 300 нМ.
12. Антитело или его антигенсвязывающий фрагмент по любому из пп.1-8, где указанное антитело или его антигенсвязывающий фрагмент представляет собой полностью человеческое моноклональное антитело.
13. Антитело или его антигенсвязывающий фрагмент по любому из пп.1-8, где указанное антитело или его антигенсвязывающий фрагмент является связывающим фрагментом полностью человеческого моноклонального антитела.
14. Антитело или его антигенсвязывающий фрагмент по п.13, где указанное антитело или его антигенсвязывающий фрагмент выбирают из группы, состоящей из Fab, Fab' или Р(ab')2 и Fv.
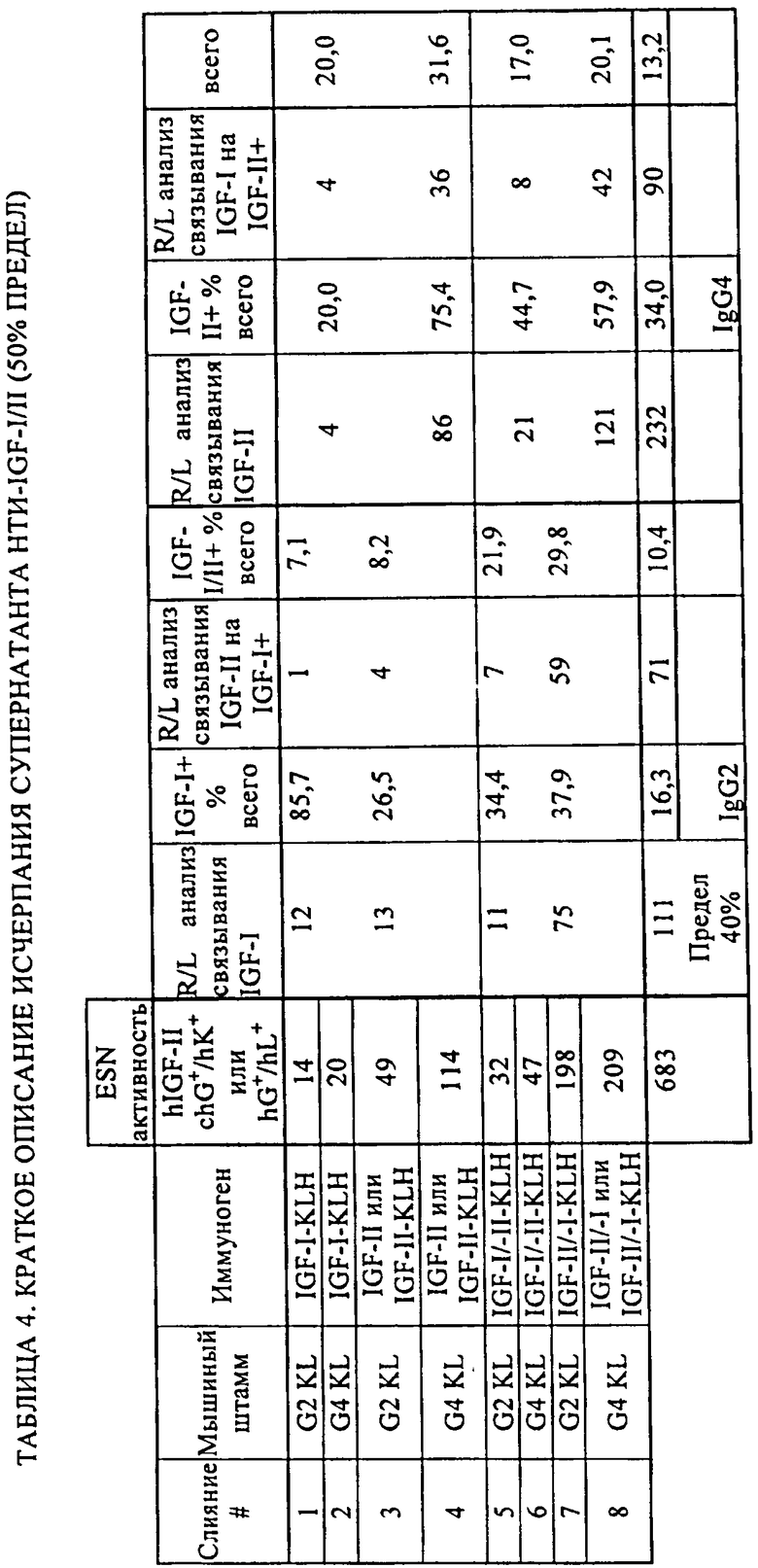
15. Специфическое антитело по любому из пп.1-8, где указанное антитело является моноклональным антителом 7.159.2 (номер доступа ATCC PTA-7424).
16. Антитело или его антигенсвязывающий фрагмент по любому из пп.1-8, где указанное антитело или его антигенсвязывающий фрагмент содержит полипептид тяжелой цепи, имеющий последовательность SEQ ID №:6.
17. Антитело или его антигенсвязывающий фрагмент по любому из пп.1-8, где указанное антитело или его антигенсвязывающий фрагмент содержит полипептид легкой цепи, имеющий последовательность SEQ ID №:8.
18. Фармацевтическая композиция для лечения злокачественной опухоли, включающая эффективное количество антитела или его антигенсвязывающего фрагмента по любому из пп.1-8 в смеси с фармацевтически приемлемым носителем.
19. Молекула нуклеиновой кислоты, кодирующая антитело или его антигенсвязывающий фрагмент по п.1.
20. Вектор для экспрессии антитела или его антигенсвязывающего фрагмента, где вектор содержит молекулу нуклеиновой кислоты по п.19.
21. Клетка-хозяин для экспрессии антитела или антигенсвязывающего фрагмента по п.1, содержащая вектор по п.20.
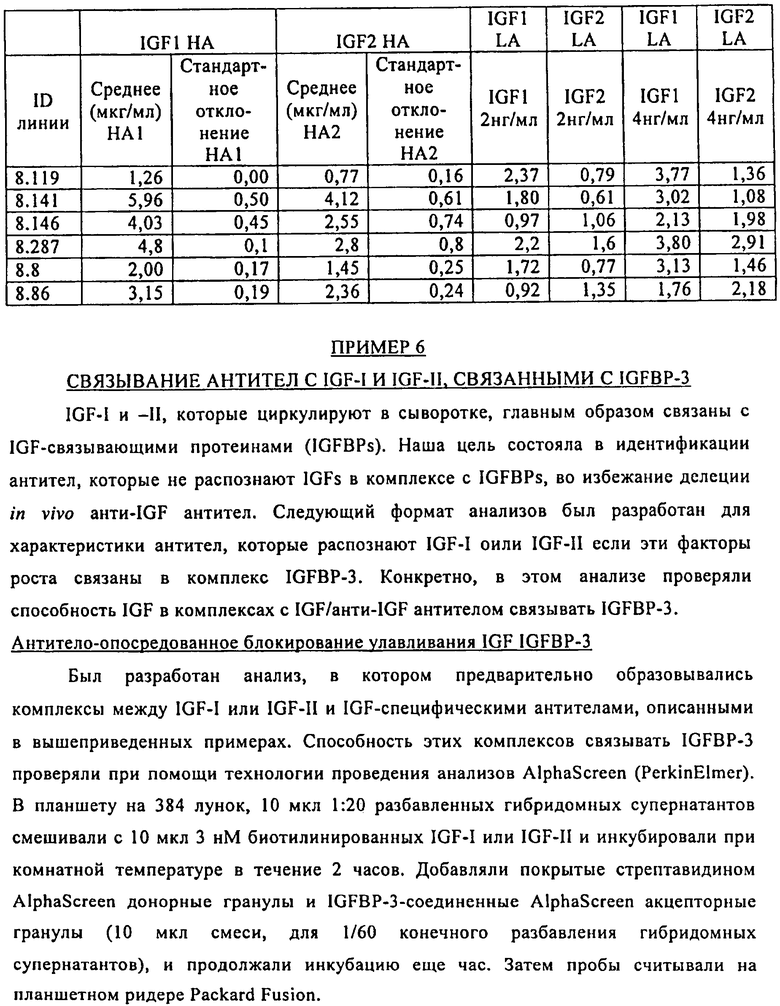
22. Человеческое моноклональное антитело по п.12, где указанное антитело не связывает специфически IGF-II или IGF-I протеины, если указанные протеины связаны с инсулиновыми связывающими рецепторами фактора роста.
23. Способ определения уровня инсулиноподобного фактора роста-II (IGF-II) и инсулиноподобного фактора роста I (IGF-I) в пробе пациента, который включает:
обеспечение пробы пациента;
контактирование указанной пробы с антителом или его антигенсвязывающим фрагментом по п.1; и
определение уровня IGF-I и IGF-II в указанной пробе.
24. Способ по п.23, где пробой пациента является кровь.
25. Применение антитела или его антигенсвязывающего фрагмента по любому из пп.1-8 для получения лекарственного средства для лечения злокачественной опухоли.
26. Применение по п.25, где указанное антитело или его антигенсвязывающий фрагмент представляет собой полностью человеческое моноклональное антитело.
27. Применение по п.25, где указанную злокачественную опухоль выбирают из группы, состоящей из меланомы, немелкоклеточного рака легких, глиомы, печеночно-клеточного рака, опухоли щитовидной железы, рака желудка, рака простаты, рака молочной железы, рака яичников, рака мочевого пузыря, рака легких, глиобластомы, рака эндометрия, рака почек, рака толстой кишки, рака поджелудочной железы, и плоскоклеточного рака.
28. Применение по п.27, где антитело или его антигенсвязывающий фрагмент представляет собой mAb 7.159.2 (номер доступа ATCC PTA-7424).
29. Применение по п.26, где указанное лекарственное средство предназначено для использования в комбинации со вторым анти-неопластическим агентом, выбранным из группы, состоящей из антитела, химиотерапевтического агента и радиоактивного лекарственного средства.
30. Применение по п.26, где указанное лекарственное средство предназначено для использования в сочетании или после проведения традиционной хирургии, трансплантации стволовых клеток костного мозга или трансплантации периферических стволовых клеток.
31. Способ лечения злокачественных опухолей у млекопитающих, включающий:
отбор млекопитающего, нуждающегося в лечении злокачественной опухоли; и
введение указанному млекопитающему терапевтически эффективной дозы антитела или его антигенсвязывающего фрагмента по п.1.
32. Способ по п.31, где указанным животным является человек.
33. Способ по п.31, где указанное антитело или его антигенсвязывающий фрагмент представляет собой полностью человеческое моноклональное антитело.
34. Способ по п.31, где указанную злокачественную опухоль выбирают из группы, состоящей из: меланомы, немелкоклеточного рака легких, глиомы, печеночно-клеточного рака, опухоли щитовидной железы, рака желудка, рака простаты, рака молочной железы, рака яичников, рака мочевого пузыря, рака легких, глиобластомы, рака эндометрия, рака почек, рака толстой кишки, рака поджелудочной железы и плоскоклеточного рака.
35. Способ по п.31, где антитело или его антигенсвязывающий фрагмент выбирают из группы, состоящей из mAb 7.159.2 (номер доступа ATCC PTA-7424).
36. Конъюгат для лечения злокачественной опухоли, причем указанный конъюгат содержит антитело по п.12 или его связывающий фрагмент и терапевтический агент.
37. Конъюгат по п.36, где терапевтический агент представляет собой токсин.
38. Конъюгат по п.36, где терапевтический агент представляет собой радиоактивный изотоп.
39. Конъюгат по п.36, где терапевтический агент является химическим веществом, смесью химических веществ, биологической макромолекулой или экстрактом, полученным из биологического материала.
40. Конъюгат для диагностики злокачественной опухоли, причем указанный конъюгат содержит антитело по п.12 или его связывающий фрагмент и терапевтический агент.
41. Конъюгат по п.40, где терапевтический агент представляет собой токсин.
42. Конъюгат по п.40, где терапевтический агент представляет собой радиоактивный изотоп.
43. Конъюгат по п.40, где терапевтический агент является химическим веществом, смесью химических веществ, биологической макромолекулой или экстрактом, полученным из биологического материала.
44. Антитело или его антигенсвязывающий фрагмент, который связывает инсулиноподобный фактор роста-II (IGF-II), имеет перекрестную реактивность к инсулиноподобному фактору роста I (IGF-I) и нейтрализует активность IGF-I и IGF-II, где указанное антитело или его антигенсвязывающий фрагмент, содержит:
гипервариабельный участок 1 (CDR1) тяжелой цепи, имеющий аминокислотную последовательность, выбранную из группы, включающей "Ser Tyr Tyr Trp Ser" (SEQ ID №:21); "Ser Tyr Tyr Trp Ser" (SEQ ID №:27);
гипервариабельный участок 2 (CDR2) тяжелой цепи, имеющий аминокислотную последовательность "Tyr Phe Phe Tyr Ser Gly Tyr Thr Asn Tyr Asn Pro Ser Leu Lys Ser" (SEQ ID №:22); "Tyr Phe Phe Tyr Ser Gly Tyr Thr Asn Tyr Asn Pro Ser Leu Lys Ser" (SEQ ID №:28);
гипервариабельный участок 3 (CDR3) тяжелой цепи, имеющий аминокислотную последовательность, выбранную из группы включающей " Ile Thr Gly Thr Thr Lys Gly Gly Met Asp Val" (SEQ ID №:23); "Ile Thr Gly Thr Thr Lys Gly Gly Met Asp Val" (SEQ ID №:29);
гипервариабельный участок 1 (CDR1) легкой цепи, имеющий аминокислотную последовательность, выбранную из группы включающей "Thr Gly Ser Ser Ser Asn Ile Gly Ala Gly Tyr Asp Val His» (SEQ ID №:24);
"Thr Gly Arg Ser Ser Asn Ile Gly Ala Gly Tyr Asp Val His" (SEQ ID №:30);
гипервариабельный участок 2 (CDR2) легкой цепи, имеющий аминокислотную последовательность, выбранную из группы, включающей "Gly Asn Asn Asn Arg Pro Ser" (SEQ ID №:25); "Gly Asn Ser Asn Arg Pro Ser"(SEQ ID №:31); и
гипервариабельный участок 3 (CDR3) легкой цепи, имеющий аминокислотную последовательность, выбранную из группы, включающей "Gln Ser Phe Asp Ser Ser Leu Ser Gly Ser Val" (SEQ ID №:26); "Gln Ser Tyr Asp Ser Ser Leu Ser Gly Ser Val" (SEQ ID №:32).
45. Выделенное антитело или его антигенсвязывающий фрагмент, который предпочтительно связывает инсулиноподобный фактор роста-II (IGF-II), имеет перекрестную реактивность к инсулиноподобному фактору роста I (IGF-I), где указанное антитело или его антигенсвязывающий фрагмент включает полипептид тяжелой цепи, содержащий последовательность SEQ ID №6, и полипептид легкой цепи, который включает последовательность SEQ ID №8.
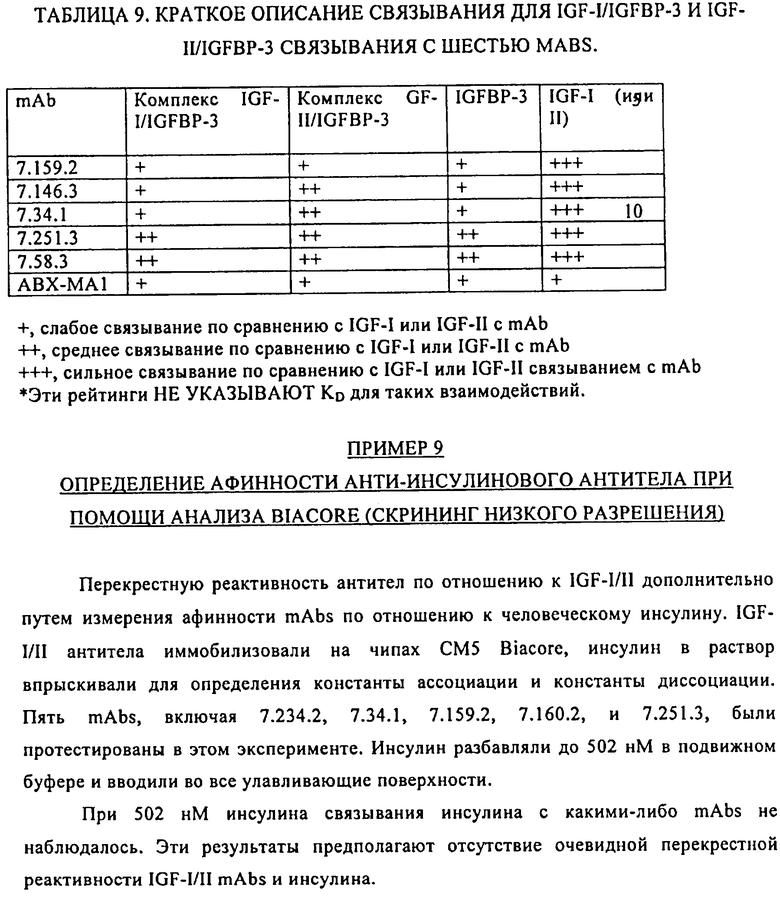
46. Антитело по п.45, где это антитело не связывает специфично протеины IGF-I и IGF-II, когда эти протеины связаны связывающим протеином-3 инсулинового фактора роста.
47. Антитело по п.45, где это антитело является моноклональным антителом.
48. Антитело по п.45, где это антитело является полностью человеческим моноклональным антителом.
49. Фармацевтическая композиция для лечения злокачественной опухоли, включающая эффективное количество антитела или его антигенсвязывающего фрагмента по любому из пп.45-48 и фармацевтически приемлемый носитель.
50. Конъюгат для лечения злокачественной опухоли, причем указанный конъюгат содержит антитело по п.48 или его антигенсвязывающий фрагмент и терапевтический агент.
51. Конъюгат по п.50, где терапевтический агент представляет собой токсин.
52. Конъюгат по п.50, где терапевтический агент представляет собой радиоактивный изотоп.
53. Конъюгат для диагностики злокачественной опухоли, причем указанный конъюгат содержит антитело по п.48 или его антигенсвязывающий фрагмент и терапевтический агент.
54. Конъюгат по п.53, где терапевтический агент представляет собой токсин.
55. Конъюгат по п.53, где терапевтический агент представляет собой радиоактивный изотоп.
| ЕР 1505075 A1, 09.02.2005 | |||
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| ENJOH T | |||
| et al., "Characterization of new monoclonal antibodies to human insulin-like growth factor-II and their application in western immunoblot analysis." J Clin Endocrinol Metab | |||
| Способ изготовления фанеры-переклейки | 1921 |
|
SU1993A1 |
| VAN WYK JJ, BRUTON ET., "Molecular basis for species and | |||
Авторы
Даты
2013-09-10—Публикация
2006-12-08—Подача