Изобретение относится к технологии получения гидридов металлов и направлено на снижение термической стойкости гидрида титана, который используется в водородных технологиях, например, в качестве источника водорода с большим объемным и весовым содержанием водорода.
Известен способ получения гидрида титана, в котором для снижения температуры выделения водорода гидрид титана подвергают размолу в планетарной шаровой мельнице. Эффективный размер частиц гидрида титана в процессе размола снижается с 1200 до 180 нм. Для такого гидрида, согласно имеющимся в литературе данным, степень разложения при нагреве, например, до 450°С, составляет ~6% /В.Д.Добровольский, О.Г.Радченко, Ю.М.Солонин, В.Б.Муратов, И.А.Морозов. Влияние диспергирования и механического легирования бором на термическую устойчивость гидридных фаз сплавов системы Ti-B-H. Порошковая металлургия, 2006, №9/10, с.97-106/.
Недостатком способа снижения термической стойкости порошкообразного гидрида титана путем его измельчения является склонность к пылению получаемого материала как в процессе размола, так и при выделении водорода, возможное загрязнение гидрида титана примесями в процессе размола, повышение реакционной способности взаимодействия с примесями в процессе использования полученного мелкодисперсного вещества, а также сложность способа. Последнее заключается в том, что для осуществления способа необходимо введение дополнительной операции - размола гидрида после его синтеза, что сопровождается, как правило, еще и перезагрузкой гидрида из аппарата синтеза в мельницу.
Наиболее близким к предлагаемому способу (прототипом) получения гидрида титана является способ, согласно которому титан прогревают (активируют) при температуре выше 1000°С, затем его температуру снижают до 400°С, при этой температуре осуществляют подачу водорода к титану и последующую его выдержку в водороде в течение нескольких часов. Затем производят медленное охлаждение титана в среде водорода /К. Маккей. Водородные соединения металлов. -М.: Мир, 1968, с.99/.
Гидрид титана, полученный таким способом, имеет высокую термическую стойкость. По имеющимся у авторов данным степень разложения гидрида при его нагреве до 450°С составляет 3-3,5%. Высокая термическая стойкость гидрида является недостатком при использовании его в источниках водорода.
Задачей, которую решает настоящее изобретение, является снижение термической стойкости гидрида титана.
Технический результат, достигаемый при использовании настоящего изобретения, заключается в следующем:
- степень разложения гидрида титана при нагреве до 450°С повышается с 3-3,5 до 30,3-36%;
- упрощается способ получения порошкообразного гидрида титана, позволяющий снизить термическую стойкость гидрида титана;
- склонность к пылению гидрида титана не увеличивается;
- удельное газосодержание гидрида не изменяется.
Для решения указанной задачи и достижения указанного технического результата в способе получения порошкообразного гидрида титана, заключающемся в активации порошка металла и последующем насыщении его водородом, согласно изобретению активацию порошка металла проводят при температуре 290-350°С ч в течение 3-4 часов, а взаимодействие водорода с титаном проводят при температуре не более 300°С.
Для усиления эффекта снижения термической стойкости гидрида титана порошок титана перед активацией обрабатывают в шаровой мельнице.
Обработку порошка титана в шаровой мельнице проводят в течение 0,5-55 часов с частотой биения шара 5-15 Гц.
В результате снижения температуры активации до 290-350°С и температуры взаимодействия титана с водородом до 300°С и ниже степень разложения гидрида титана при нагреве до 450°С повышается с 3-3,5 (таблица, пп.5-6) до 30,3-36% (таблица, пп.19-21), что свидетельствует о снижении термической стойкости порошка гидрида титана.
Снижение термической стойкости гидрида вместе со снижением температур активации и взаимодействия титана с водородом может происходить, по мнению автора, из-за снижения при более низких температурах отжига имевшихся в титане напряжений и уменьшения релаксации напряжений, возникающих при внедрении водорода в кристаллическую решетку титана.
Проявление этого эффекта в температурной области не более 300°С может быть связано с происходящим при температуре 300°С фазовым переходом. Взаимодействие титана с водородом при температурах не более 300°С происходит с образованием γ-фазы гидрида, в то время как при температурах выше 300°С - с образованием β-фазы гидрида титана.
В случае, если порошок титана перед активацией и насыщением был обработан в шаровой мельнице, степень разложения гидрида титана при его нагреве до 450°С повышается до 78-85% (таблица, пп.25-27). Снижение термической стойкости гидрида титана в этом случае может происходить из-за накопления дефектов и возникновения связанных с ними напряжений в кристаллической решетке на стадии обработки титана в шаровой мельнице.
Данный способ получения порошка гидрида титана поясняется графическими материалами.
На фиг.1 приведена термограмма гидрида титана, полученного путем взаимодействия порошка титана с водородом при температуре 400°С.
На фиг.2 приведена термограмма гидрида титана, полученного путем взаимодействия порошка титана с водородом при температуре 20°С.
На фиг.3 приведена зависимость степени разложения порошка гидрида титана при 450°С от температуры, при которой титан взаимодействовал с водородом.
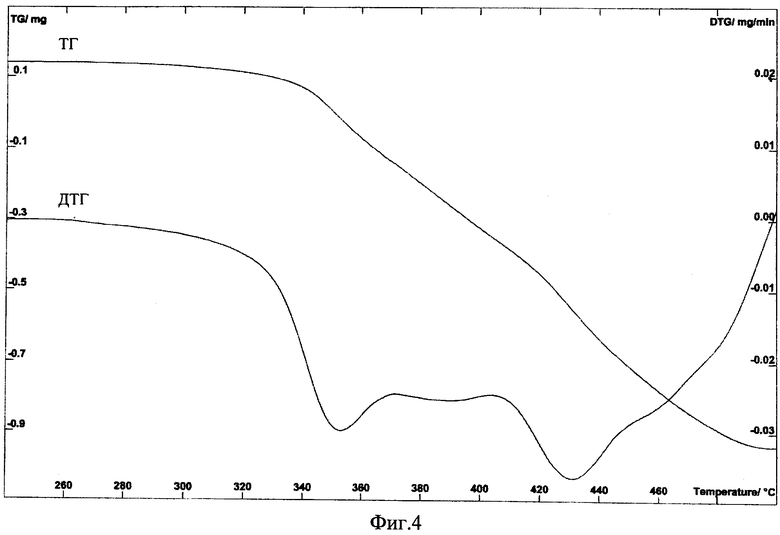
На фиг.4 приведена термограмма порошка гидрида титана, полученного из порошка титана, обработанного в шаровой мельнице.
Для экспериментального подтверждения настоящего изобретения использовался порошок магниетермического губчатого титана марки ТПП-8 с размером частиц ≤160 мкм производства ОАО "Ависма". Использовался исходный порошок титана в состоянии поставки или он же, предварительно обработанный в шаровой мельнице. Для обработки порошка титана использовалась шаровая мельница марки ММ200 фирмы "Resch". Навеска титана массой 2 грамма обрабатывалась в течение заданного времени одним шаром массой 64 г с частотой 5 или 15 Гц. Обработка в шаровой мельнице производились в атмосфере аргона с содержанием O2 и H2O менее 0,1 ppm в боксе фирмы "MBraun".
Синтез порошка гидрида титана производился в установке типа Сивертса после активации образца исходного или обработанного в шаровой мельнице титана путем его прогрева в условиях динамического вакуума (давление остаточных газов в установке ~0,003 мбар). После активации образцу придавалась заданная температура, к нему подавался водород, и в изотермических условиях при заданной температуре производилось взаимодействие порошка титана с водородом. После прекращения поглощения водорода порошок охлаждался, извлекался и проводился его термический анализ.
Контроль термической стойкости порошка гидрида титана осуществлялся методами термического анализа по степени разложения гидрида титана при нагреве до 450°С. Выбор температуры 450°С для контроля стойкости был обусловлен тем, что при этой или близкой к ней температуре начинается разложение гидрида титана, синтез которого производился согласно способу, описанному в прототипе.
Термический анализ гидрида титана проводился на термоанализаторе марки TG-DSC-111 фирмы "Setaram" при нагреве порошка гидрида титана со скоростью 4°С/мин. Погрешность измерения температуры этого прибора составляет ±0,1°С. При анализе в зависимости от температуры порошка гидрида титана регистрировались его масса (кривая ТГ) и скорость изменения массы (кривая ДТГ). Анализ проводился в вакууме (остаточное давление газов в термоанализаторе перед началом проведения анализа ~ 0,05 мбар). Навески составов массой 15÷59 мг в насыпном виде помещались в открытый тигель из плавленого кварца с внутренним диаметром 3 мм.
Все работы по извлечению порошка гидрида титана из реакционной ампулы, их взвешиванию и помещению в тигель термоанализатора производились в атмосфере аргона с содержанием О2 и Н2О менее 0,1 ppm. После этого порошок гидрида титана извлекался из бокса, переносился в термоанализатор, и прибор вакуумировался. Время контакта порошка гидрида титана с воздухом в промежутке между извлечением из бокса и переносом в термоанализатор не превышало 15 с. В специальных опытах после синтеза гидрида непосредственно в термоанализаторе было найдено, что непродолжительный контакт порошка гидрида титана с воздухом не оказывает заметного влияния на их термическую стойкость.
На фиг.1 приведена термограмма нагрева в вакууме при скорости нагрева 4°С/мин исходного гидрида титана, полученного из порошка магниетермического губчатого титана марки ТПП-8 с размером частиц ≤160 мкм, производства ОАО "Ависма". Порошок титана был активирован при температуре 1000°С в течение 2 часов в вакууме, затем охлажден до температуры 400°С, при этой температуре к нему был дан водород при давлении 1 ат, порошок гидрида титана выдержан при температуре 400°С и давлении водорода 1 ат в течение 4 часов и медленно охлажден в среде водорода. Таким образом, была воспроизведена технология синтеза гидрида титана, описанная в прототипе. Из фиг.1 по кривой ДТГ найдено, что разложение исходного гидрида титана начинается при температуре ~425°С. По кривой ТГ найдено, что на момент нагрева гидрида титана до 450°С степень его разложения составила 3,5%. Общая потеря массы образцом составили 3,65%.
На фиг.2 приведена термограмма при скорости нагрева 4°С/мин гидрида титана, полученного из порошка титана марки ТПП-8 с размером частиц ≤160 мкм. Порошок титана был активирован при температуре 300°С в вакууме в течение 4 часов, затем охлажден до температуры 18°С, при этой температуре к нему был дан водород при давлении 1 ат, порошок выдержан при температуре 18°С и давлении водорода 1 ат в течение 12 часов. Из фиг.2 по кривой ДТГ видно, что разложение исходного гидрида титана начинается при температуре ~330°С. По кривой ТГ найдено, что на момент нагрева гидрида титана до 450°С степень его разложения составила 30,3%. Общая потеря массы образцом составили 3,65%.
Из сравнения приведенных на фиг.1 и 2 термограмм видно, что в результате того, что взаимодействие водорода с образцом в последнем случае происходило при температуре 18°С его термическая стойкость, оцененная по степени разложения при нагреве до 450°С, увеличилась с 3,5 до 30,3%, а количество выделяющегося в ходе нагрева газа, с учетом экспериментального разброса, не изменилось.
На фиг.3 приведена зависимость степени разложения гидрида титана от температуры, при которой титан взаимодействовал с водородом. Степень разложения определялась при нагреве гидрида титана до 450°С со скоростью 4°С/мин в вакууме. Из фиг.3 видно, что повышение степени разложения гидрида титана начинается при снижении температуры взаимодействия металла с водородом до ~300°С.
На фиг.4 приведена термограмма при скорости нагрева 4°С/мин гидрида титана, полученного из порошка титана марки ТПП-8 с размером частиц ≤160 мкм. Титан был обработан в шаровой мельнице в течение 55 часов при частоте колебаний шара 10 Гц, затем прогрет при температуре 300°С в вакууме в течение 4, затем охлажден до температуры 40°С, при этой температуре к нему был дан водород при давлении 1 ат, образец выдержан при температуре 40°С и давлении водорода 1 ат в течение 8 часов.
Из фиг.4 по кривой ДТГ найдено, что разложение исходного гидрида титана начинается при температуре ~260°С. По кривой ТГ найдено, что на момент нагрева гидрида титана до 450°С степень его разложения составила 79,4%. Общая потеря массы образцом составили 3,62%.
Из сравнения фиг.2 и 4 видно, что в результате обработки исходного титана в шаровой мельнице степень разложения гидрида титана при нагреве до 450°С выросла с 30,3 до 79,4%.
В таблице представлены некоторые из имеющихся экспериментальных данных, иллюстрирующих применимость заявляемого способа снижения термической стойкости гидрида титана путем его активации при температурах 290-350°С, взаимодействия водорода с титаном при температуре не более 300°С и предварительной обработки исходного титана в шаровой мельнице.
Предлагаемый способ снижения термической стойкости гидрида титана является более простым, чем прототип. Для его осуществления не требуется проведения дополнительных операций. Положительный эффект может быть достигнут только за счет изменения температур активации титана и взаимодействие водорода с металлом.
Как видно из приведенных на фиг.1, 2, 4 и в таблице примеров, экспериментальная проверка применимости предлагаемого способа снижения термической стойкости гидрида титана, заключающегося в активации порошка металла и последующем взаимодействии его с водородом, производилась в температурном диапазоне активации порошка металла от 290 (см. пп.23, 27 таблицы) до 1000°С (пп.5, 6 таблицы) и в температурном диапазоне взаимодействий водорода с порошком металла от 700°С (см. п.1 таблицы) до -15°С (см. п.20 таблицы). Как видно из фиг.3, заметное снижение термической стойкости гидрида титана по сравнению с прототипом (см. пп.5 и 6 таблицы) наблюдается при снижении температуры взаимодействия металла с водородом до 300°С. Активация при этом во всех случаях проводилась в температурном диапазоне 290-350°С.
Из таблицы видно (см. пп.1-20), что снижение температуры, при которой производились активация и взаимодействие металла с водородом, не снижает содержание водорода в гидриде.
Как видно из таблицы (см. пп.21-27) предварительная обработка металла в шаровой мельнице снижает термическую стойкость полученного из него гидрида титана. Обработка проводилась при частотах колебаний шара 5-15 Гц в течение 0,5-55 часов. Однако такая обработка может привести к некоторому снижению содержания водорода в гидриде (см. п.27 таблицы).
Для того чтобы дефекты кристаллической решетки, созданные в процессе обработки металла в шаровой мельнице, не были отожжены в процессе активации, активация такого металла также проводилась при температурах 290-350°С в течение 3-4 часов.
Использование предлагаемого способа снижения термической стойкости гидрида титана обеспечивает по сравнению с существующим способом следующие преимущества:
- степень разложения гидрида титана при нагреве до 450°С повышается с 3-3,5 до 30,3-36%;
- упрощается технология снижения термической стойкости гидрида титана;
- склонность к пылению гидрида титана не увеличивается.
- удельное газосодержание гидрида не снижается.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОБРАБОТКИ ГИДРИДА ТИТАНА | 2011 |
|
RU2466929C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОРОШКА ТИТАНА | 2015 |
|
RU2628228C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПОРОШКОВ ТАНТАЛА | 2014 |
|
RU2582414C1 |
| Способ получения порошков ниобия | 2016 |
|
RU2610652C1 |
| Способ получения порошков тантала | 2017 |
|
RU2647073C1 |
| СПОСОБ ПОЛУЧЕНИЯ МЕЛКОДИСПЕРСНОГО ПОРОШКА ТИТАНА | 2005 |
|
RU2301723C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ГИДРИДА МАГНИЯ ДЛЯ ХИМИЧЕСКОГО ГЕНЕРАТОРА ВОДОРОДА | 2018 |
|
RU2686898C1 |
| СПОСОБ ПОЛУЧЕНИЯ МЕЛКОДИСПЕРСНОГО ПОРОШКА ТИТАНА | 2015 |
|
RU2609762C1 |
| Способ получения гидрированного порошка пластичного металла или сплава | 2021 |
|
RU2759551C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТИТАНСОДЕРЖАЩИХ МЕТАЛЛИЧЕСКИХ ПОРОШКОВ | 2016 |
|
RU2634866C1 |



Изобретение относится к области химии. Порошок титана активируют путем его прогрева в динамическом вакууме при температурах 290-350°С в течение 3-4 часов. После этого осуществляют взаимодействие порошка титана с водородом при температуре не более 300°С. Возможна обработка порошка титана перед активацией в шаровой мельнице в течение 0,5-55 часов с частотой биения шара 5-15 Гц. Изобретение позволяет снизить термическую стойкость порошкообразного гидрида титана. 2 з.п. ф-лы, 4 ил., 1 табл.
1. Способ получения порошкообразного гидрида титана, заключающийся в активации порошка титана и последующем взаимодействии его с водородом, отличающийся тем, что активацию порошка титана проводят путем его прогрева в динамическом вакууме при температуре 290-350°С в течение 3-4 ч, а взаимодействие порошка титана с водородом проводят при температуре не более 300°С.
2. Способ по п.1, отличающийся тем, что порошок титана перед активацией обрабатывают в шаровой мельнице.
3. Способ по п.2, отличающийся тем, что обработку порошка титана в шаровой мельнице проводят в течение 0,5-55 ч с частотой биения шара 5-15 Гц.
| МАККЕЙ К | |||
| Водородные соединения металлов | |||
| - М.: Мир, 1968, c.99 | |||
| Способ получения гидридов переходных металлов | 1975 |
|
SU552293A1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРИДА ТИТАНА | 2002 |
|
RU2208573C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРИДА ТИТАНА И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2008 |
|
RU2385837C2 |
| JP 10195504 A, 28.07.1998 | |||
| WO 2004041717 A1, 21.05.2004. | |||
Авторы
Даты
2014-02-20—Публикация
2012-07-03—Подача