Изобретение относится к биотехнологии, в частности к генетической инженерии, и может быть использовано для получения рекомбинантного полипептида (искусственного антитела), взаимодействующего с фактором некроза опухолей человека (ФНО).
Фактор некроза опухолей (ФНО) - полифункциональный цитокин, один из основных медиаторов воспаления, врожденного иммунитета и функций защиты организма, а также структурной организации лимфоидных органов [Mathew S.J., Haubert D., Kronke M, Leptin M. Looking beyond death: a morphogenetic role for theTNF signalling pathway. J. Cell Sci. 2009. V.122. P.1939-1946]. Многие аутоиммунные и воспалительные заболевания человека сопровождаются сверхпродукцией ФНО, в частности системные или локальные повышенные концентрации этого цитокина характерны для таких патологических состояний, как ревматоидный артрит, псориаз, болезнь Крона, септический шок, рассеянный склероз [Efimov G.A., Kruglov А.А., Tillib S.V., Kuprash D.V. and Nedospasov, S.A. Tumor Necrosis Factor and the consequences of its ablation in vivo. Mol. Immunol. 2009, V.47, P.19-27]. При некоторых заболеваниях нейтрализация активности ФНО дает ярко выраженный клинический эффект, поэтому поиск различных блокаторов ФНО является перспективным направлением белковой инженерии и биотехнологии [Tansey M.G., Szymkowski D.E. The TNF superfamily in 2009: new pathways, new indications, and new drugs. Drug Discov. Today. 2009. V.23-24. P.1082-1088].
Известны способы получения блокаторов ФНО на основе рекомбинантных антител и рекомбинантных полипептидов, в состав которых входят антигенсвязывающие домены антител, специфичных к рецепторам этого цитокина. На их основе получены препараты Инфликсимаб (Infliximab, Remicade), Адалимумаб (Adalimumab, Humira) Этанерсепт (Etanercept), Ленерсепт (Lenercept) [Efimov G.A, Kruglov A.A., Tillib S.V., Kuprash D.V., and Nedospasov, S.A. Tumor Necrosis Factor and the consequences of its ablation in vivo. Mol. Immunol. 2009. V.47. P.19-27]. Эти препараты имеются на российском рынке лекарств, однако их использование достаточно дорого в силу высоких затрат на производство. Существенным недостатком этих препаратов при их длительном применении является возможность возникновения таких побочных эффектов, как угнетение иммунитета и повышенная восприимчивость к инфекциям, в частности к Mycobacterium tuberculosis и Listeria monocytogenes [Quesniaus V.F., Jacobs, M., Allie N., Grivennikov S., Nedospasov, S.A., Garcia I., Olleros M.L., Shebzukov Y., Kuprash D., Vasseui V., Rose S., Court N., Vacher R., Ryffel B. TNF in host resistance to tuberculosis infection. Curr. Dir. Autoimmun. 2010. V.11. P.157-179. Kruglov A.A., Kuchmiy A., Grivennikov S.I., Tumanov A.V., Kuprash D.V., Nedospasov S.A. Physiological functions of tumor necrosis factor and the consequences of its pathologic overexpression or blockade: mouse models. Cytokine & Growth Factor Reviews. 2008. V.19. P.231-244].
Одним из путей радикального удешевления ФНО-блокирующих преператов и минимизации побочных эффектов является использование альтернативных каркасных белков (АКБ), в частности 10-го домена фибронектина человека [Skerra A. Alternative non-antibody scaffolds for molecular recognition. Curr. Opin. Biotechnol. 2007. V.18. P.295-304]. Домен фибронектина (10 домен фибронектина III типа, Fn3) является структурным аналогом VH домена иммуноглобулинов. Этот небольшой белок не содержит остатков цистеина и хорошо экспрессируется в клетках Е.coli в растворимой форме. Варьирование аминокислотных последовательностей в трех петлях Fn3, соответствующих CDR в молекулах антител, позволяют получать белки, обладающие способностью связывать различные антигены, а небольшой размер молекулы способствует хорошему проникновению в ткани [Lipovsek D. Adnectins: engineered target-binding protein therapeutics. Protein Eng Des Sel. 2011. V.1-2. P.3-9].
Известен наиболее близкий к заявленному способ получения ФНО-связывающих белков на основе домена фибронектина [Xu L., Aha P., Gu К., Kuimelis R.G., Kurz М, Lam Т., Lim А.С., Liu Н., Lohse Р.А., Sun L., Weng S., Wagner R.W., Lipovsek D. Directed evolution of high-affinity antibody mimics using mRNA display. Chem Biol. 2002. V.9. P.933-942]. Авторами получена библиотека кодирующих последовательностей домена фибронектина с рандомизированными петлевыми участками BC, DE и FG. Проведена селекция библиотеки с отбором вариантов, связывающих ФНО. Полученные варианты экспрессированы в клетках Е.coli и выявлены эффективные связывающие белки Т09.07 и М12.21. Индукцию проводят в клетках штамма BL21(DE3) путем добавления 0.5 мМ ИПТГ, затем культивирование продолжают в течение 20 ч при 20°C. Выход рекомбинантных белков, обеспечиваемый за счет использования данной конструкции, составляет 1,8 и 3,6 мг/л культуры для Т09.07 и М12.21 соответственно.
К недостаткам способа можно отнести относительно невысокий уровень синтеза белков и высокую концентрацию индуктора.
Технической задачей изобретения является получение полипептида FN3.54, взаимодействующего с фактором некроза опухолей человека, а также увеличение уровня его биосинтеза.
Поставленная задача решается за счет конструирования рекомбинантной плазмидной ДНК рЕТ3.54, кодирующей полипептид, взаимодействующий с ФНО с мол. массой 3,74 Md (5,660 т.п.о.), состоящей из NdeI/XhoI - фрагмента ДНК плазмиды pET32a(+) длиной 5,366 т.п.о., включающего промотор бактериофага T7, терминатор транскрипции бактериофага Т7, ген bla β-лактамазы, определяющий устойчивость трансформированных плазмидой рЕТ3.54 клеток к ампициллину, участок ori инициации репликации; и NdeI/XhoI - фрагмента ДНК размером 0,294 т.п.о., содержащего ген Fn3.54, кодирующий аминокислотную последовательность полипептида FN3.54, взаимодействующего с ФНО-альфа; содержащей уникальные сайты узнавания рестрикционными эндонуклеазами, имеющими следующие координаты: NdeI - 367, XhoI - 635, а также за счет штамма бактерий Escherichia coli BL21(DE3)/pET3.54 - продуцента полипептида FN3.54, взаимодействующего с фактором некроза опухолей человека.
Рекомбинантная плазмидная ДНК рЕТ3.54 кодирует индуцибельный синтез полипептида FN3.54, взаимодействующего с фактором некроза опухолей человека, а штамм Escherichia coli BL21(DE3)/pET3.54 обеспечивает синтез этого полипептида с уровнем экспрессии не ниже 15% суммарного клеточного белка. Индуцибельный высокий уровень синтеза целевого полипептида обеспечивается тем, что плазмида рЕТ3.54 содержит промотор бактериофага Т7 и усилитель трансляции гена 10 бактериофага T7.
Особенностью предложенной плазмидной конструкции является наличие в ее составе кодирующей последовательности полипептида FN3.54, содержащего уникальные аминокислотные остатки в петлевых участках ВС, DE и FG домена 10 фибронектина человека (SEQ ID NO 1), под контролем сильного регулируемого промотора бактериофага Т7, что в совокупности обеспечивает индуцибельный синтез целевого белка (SEQ ID NO 2) с надежной регуляцией и высоким выходом, достигаемым при небольших концентрациях индуктора. Последовательность, кодирующую полипептид FN3.54, получают в результате селекции библиотеки генов фибронектина (10 домен фибронектина III типа, Fn3), рандомизированных в петлевых участках, методом бесклеточного CIS-дисплея с отбором вариантов, связывающих биотинилированный ФНО. На 3'-конце гена FN3.54 расположена последовательность, кодирующая гексагистидиновый таг для последующей очистки при помощи металлоаффинной хроматографии.
Для получения штамма-продуцента полипептида FN3.54, взаимодействующего с ФНО, компетентные клетки Escherichia coli штамма BL21(DE3) трансформируют рекомбинантной плазмидой рЕТ3.54.
Полученный штамм Escherichia coli BL21(DE3)/pET3.54 характеризуется следующими признаками.
Морфологические признаки: клетки мелкие, палочковидной формы,
грамотрицательные, подвижные, размером 1×3-5 мкм, неспороносные.
Культуральные признаки: при росте на агаризованной LB-среде преобладают мелкие колонии диаметром 1-3 мм; круглые, гладкие, полупрозрачные, блестящие, серые, край ровный; консистенция пастообразная. Могут встречаться крупные колонии диаметром 4-5 мм; круглые, гладкие, матовые, край волнистый. Рост в жидких средах (LB, минимальная среда с глюкозой) характеризуется равномерным помутнением среды.
Физиолого-биохимические признаки. Клетки штамма продуцента могут расти в диапазоне температур 20-42°C, оптимальная температура роста составляет 37°C. Наиболее благоприятные для роста значения рН находятся в интервале 6,8-7,2. При росте в аэробных условиях культура может усваивать азот как органических соединений (пептон, триптон, аминокислоты, дрожжевой экстракт), так и аммонийных солей. Углерод усваивается в форме углеводов, многоатомных спиртов (глицерин), аминокислот.
Устойчивость к антибиотикам. Клетки проявляют устойчивость к ампициллину (до 200 мкг/мл), обусловленную наличием в плазмиде гена бета-лактамазы.
Способ, условия и состав среды для хранения штамма. LB-бульон с 15% глицерином, при температуре - 70°C, в криовиалах.
Технический результат заявленного изобретения заключается в том, что полученный штамм Е. coli BL21(DE3)/pET3.54 позволяет получать полипептид FN3.54, взаимодействующий с фактором некроза опухолей человека, в количестве не менее 15% от суммарного клеточного белка при концентрации индуктора 0,2 мМ. В отличие от прототипов в данном штамме достигается в 4,2 и в 8,3 раза более высокий выход целевого белка при использовании в 2,5 раза меньшего количества индуктора (ИПТГ). Совокупность перечисленных свойств штамма Е.coli BL21(DE3)/pET3.54 обусловливает большую технологичность процесса получения полипептида, взаимодействующего с фактором некроза опухолей человека.
Изобретение иллюстрируют графические материалы.
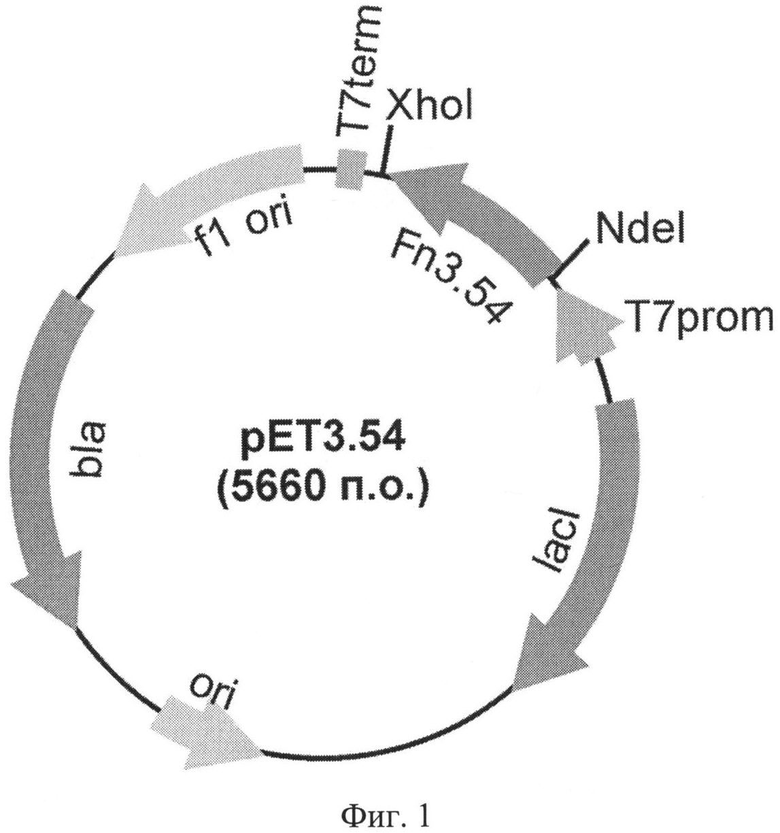
Фиг.1. Физическая карта рекомбинантной плазмиды рЕТ3.54. Указаны уникальные сайты эндонуклеаз рестрикции. T7 promotor - промотор бактериофага T7, lcI - ген 1ас-репрессора, bla - ген устойчивости к ампициллину, ori - участок инициации репликации плазмиды, Fn3.54 - рекомбинантный ген Fn3.54, кодирующий аминокислотную последовательность полипептида FN3.54, взаимодействующего с ФНО.
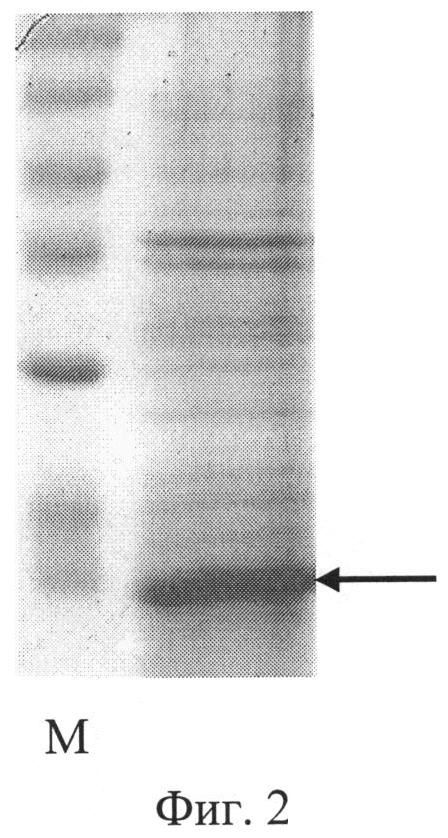
Фиг.2. Электрофореграмма лизатов клеток штамма-продуцента Е. coli BL21(DE3)/ рЕТ3.54 после индукции ИПТГ в 14%-ном полиакриламидном геле (М - белковые маркеры молекулярных масс); стрелкой указан целевой полипептид.
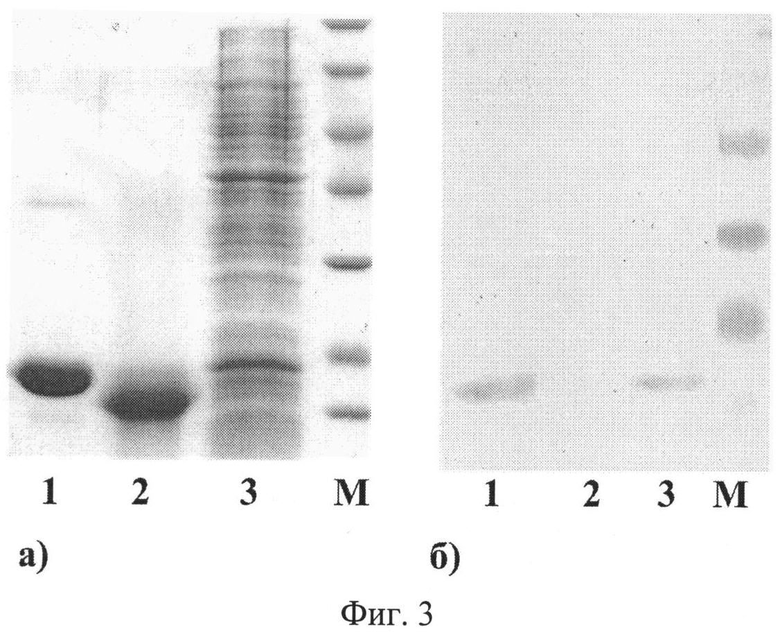
Фиг.3. Электрофореграмма в 14% SDS-ПААГ (а) и Вестерн-блот (б) с использованием белка FN3.54 в качестве антитела. ФНО (1), ГМ-КСФ (2) и биомасса штамма SG20050 с плазмидой pTNF31d, экспрессирующей ФНО (3). M - маркеры молекулярных масс.
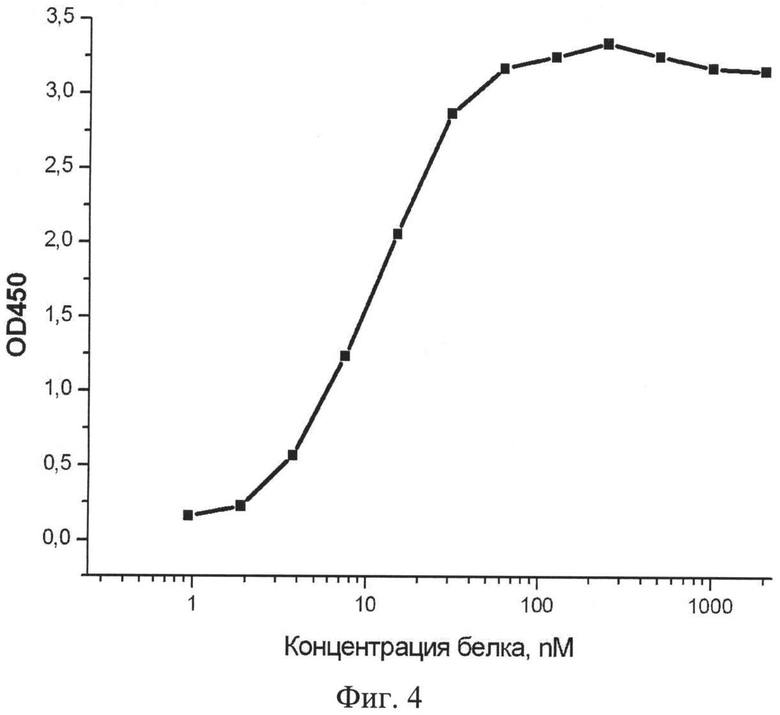
Фиг.4. Иммуноферментный анализ взаимодействия рекомбинантного белка FN3.54 с ФНО.
Изобретение иллюстрируют следующие примеры.
Пример 1.
Конструирование рекомбинантной плазмидной ДНК рЕТ3.54.
а) Конструирование библиотеки
В первой ступени ПЦР получают фрагменты ДНК, содержащие петли ВС, DE и FG с рандомизированной нуклеотидной последовательностью, а также фрагмент, содержащий промотор T7 с прилегающей 5'-концевой областью. В качестве матрицы используют ранее полученную плазмиду pETFN3 [Петровская Л.Е., Шингарова Л.Н., Крюкова Е.А., Болдырева Е.Ф., Якимов С.А., Гурьянова С.В., Новоселецкий В.Н., Долгих Д.А., Кирпичников М.П. Конструирование TNF-связывающих белков на основе домена фибронектина методом пересадки гипервариабельных участков антитела F10. Биохимия. 2012. Т.77. Стр. 79-89]. Все ПЦР-реакции проводят в объеме 50 мкл с использованием 0,5 мкг матрицы, 50 пмоль праймеров, 2 мМ каждого из четырех dNTP, 5 мкл 10х буфера для Pfu ДНК-полимеразы (Fermentas), 2.5 е.а. Pfu ДНК-полимеразы и 0.5 е.а. Taq ДНК-полимеразы (Fermentas). Полимеразные цепные реакции проводят в следующем режиме: денатурация - 1 мин, 94°C; отжиг - 40 с, 52°C; достройка - 40 с, 72°C; количество циклов - 25. Фрагмент с петлей BC амплифицируют в присутствии праймеров SEQ ID NO 3 и SEQ ID NO 7; фрагмент с петлей DE - в присутствии праймеров SEQ ID NO 5 и SEQ ID NO 8; фрагмент с петлей FG - в присутствии праймеров SEQ ID NO 4 и SEQ ID NO 10. 5'-концевой фрагмент с T7-промотором амплифицируют с праймерами SEQ ID NO 6 и SEQ ID NO 9. Продукты ПЦР выделяют из агарозного геля, используя «MinElute Gel Extraction Kit» фирмы «Qiagen».
Во второй ступени ПЦР фрагменты, кодирующие участки ВС, DE и FG, объединяют для получения гена FN3 с рандомизированными петлевыми участками. Амплификацию проводят в присутствии праймеров SEQ ID NO 3 и SEQ ID NO 10 в описанных выше условиях. Выделенный фрагмент соединяют количественно с 5'-концевым фрагментом, содержащим Т7-промотор с помощью ПЦР в присутствии праймеров SEQ ID NO 9 и SEQ ID NO 10.
В завершающей ступени ПЦР ген FN3 с промоторной частью количественно соединяют с геном Rep A [Odegrip R., Coomber D., Eldridge В., Hederer R., Kuhlman P., Ullman C., FitzGerald K., McGregor D. CIS display: In vitro selection of peptides from libraries of protein-DNA complexis. PNAS. 2004. V. 101. P.2806-2810] в присутствии праймеров SEQ ID NO 9 и SEQ ID NO 11. Параметры ПЦР: 3 мин. при 95°C; 30 циклов (денатурация 95°C 40 с, отжиг 56°C 40 с, элонгация 72°С 1,5 мин); достройка 72°С 5 мин. Количество фрагмента FN3-RepA (2636 п.о.) после выделения и очистки оценивают в агарозном геле в присутствии ДНК-стандартов FastRuler Middle Range DNA Ladder (Fermentas). Получают 1,7 мкг (1 пмоль) фрагмента, что соответствует 6×1011 молекулам,
б) Транскрипция-трансляция in vitro и аффинная селекция
Синтез в бесклеточной системе на основе экстракта из Е.coli (EasyXpress Protein Synthesis Kit, Qiagen) проводят при 37°C в термостате с перемешиванием (450 об./мин) в течение 1 ч в соответствии с протоколом производителя (EasyXpress® Protein Synthesis Handbook), используя 1,5-1,7 мкг матрицы. Реакционную смесь после завершения синтеза в бесклеточной системе разбавляют в 10 раз буфером для блокирования (3% BSA, 0,1 мг/мл ДНК-носителя, 2,5 мг/мл гепарина в PBS.), добавляют 25 мкг биотинилированного ФНО [Петровская Л.Е., Шингарова Л.Н., Крюкова Е.А., Болдырева Е.Ф., Якимов С.А., Гурьянова С.В., Новоселецкий В.Н., Долгих Д.А., Кирпичников М.П. Конструирование TNF-связывающих белков на основе домена фибронектина методом пересадки гипервариабельных участков антитела F10. Биохимия. 2012. Т.77. Стр. 79-89] и инкубируют в течение 16 ч при 4°C. К 50 мкл смолы High Capacity Neutravidin Agarose (Pierce), уравновешенной в PBS и выдержанной 2 ч в буфере для блокирования, добавляют полученную смесь и инкубируют 1 ч при комнатной температуре при постоянном перемешивании. После центрифугирования 1 мин при 500g смолу промывают буфером PBST (4 раза по 1 мл) и PBS, связавшиеся с ФНО продукты элюируют 200 µl буфера РВ (Qiagen). Полученный элюат очищают на колонке из набора MinElute Gel Extraction Kit (Qiagen) в соответствии с протоколом производителя, амплифицируют в присутствии праймеров SEQ ID NO 9 и SEQ ID NO 10 и используют в качестве матрицы для последующих раундов селекции [Odegrip R., Coomber D., Eldridge В., Hederer R., Kuhlman P., Ullman C., FitzGerald K., McGregor D. CIS display: In vitro selection of peptides from libraries of protein-DNA complexis. PNAS. 2004. V.101. P.2806-2810].
в) Анализ библиотеки клонов
ПЦР-фрагменты, полученные после 3-го раунда селекции, обрабатывают совместно рестриктазами XhoI и NdeI, выделяют фрагмент (0,294 т.п.о.) из 1,5% агарозного геля. 0,5 мкг полученного фрагмента и 0.2 мкг плазмидного вектора pET32a(+), линеаризированного обработкой рестриктазами NdeI и Xhol, длиной 0,5366 т.п.о. лигируют в течение 3 ч при 13°C в 10 мкл раствора, содержащего 40 мМ трис-HCl (рН 7,8), 10 мМ MgCL-, 10 мМ дитиотреитола, 0,5 мМ аденозинтрифосфата и 3 е.а. Т4 ДНК-лигазы (Fermentas, Литва). 5 мкл лигазной смеси используют для трансформации компетентных клеток Е. coli XL-1 Blue (Stratagene, США). Трансформанты высевают на LB-агар, содержащий 100 мкг/мл ампициллина. Полученные клоны количественно переносят с чашки в 5 мл среды LB и выделяют суммарную плазмидную ДНК. Аликвотой полученной смеси трансформируют компетентные клетки BL21(DE3) и вновь высевают на чашки с ампициллином. Отдельные колонии пересевают в лунки 96-луночного «глубокого» (deep-well) планшета (Greiner), содержащего 1 мл среды для аутоиндукции [Studier, F.W. Protein production by auto-induction in high density shaking cultures. Prot. Expr. Purif. 2005. V.41. P.207-234], и выращивают в течение ночи при 30°C в качалке Innova при 250 об/мин. Планшет центрифугируют 20 минут при 4000 об/мин. Осадки суспендируют в 100 мкл CelLytic (Sigma), выдерживают 10 мин при комнатной температуре с перемешиванием и повторно центрифугируют в тех же условиях. 10 мкл супернатантов используют для анализа связывания с ФНО методом ИФА (пример 6). ДНК клона 3.54, проявившего максимальное связывание, выделяют в препаративных количествах. Структуру клонированного гена подтверждают определением нуклеотидной последовательности. В результате получают целевую плазмидную ДНК pET3.54 (фиг.1).
Пример 2.
Получение штамма-продуцента полипептида FN3.54, взаимодействующего с фактором некроза опухолей человека.
Рекомбинантной плазмидной ДНК рЕТ3.54 трансформируют компетентные клетки Escherichia coli BL21(DE3) (Novagen) и после выращивания рекомбинантных клонов на LB-arape с ампициллином (100 мкг/мл) при 37°C получают штамм-продуцент полипептида FN3.54, взаимодействующего с фактором некроза опухолей человека.
Пример 3.
Определение продуктивности штамма-продуцента полипептида FN3.54, взаимодействующего с ФНО.
Для определения продуктивности штамма E.coli BL21(DE3)/pET3.54 ночную культуру в объеме 100 мкл переносят в 5 мл жидкой среды LB (разбавление до оптической плотности 0.15-0.18 при длине волны 560 нм), содержащей 100 мкг/мл ампициллина, и выращивают до оптической плотности 0,8 (длина волны 560 нм) при 37°C и перемешивании 200 об/мин. Индукцию синтеза полипептида FN3.54 проводят 0,2 мМ ИПТГ, после чего клетки выращивают при 27°С в течение 4 ч. Отбирают пробу культуры в количестве 1 оптическая единица (длина волны 560 нм) и центрифугируют 5 мин при скорости 6000 об/мин. Осажденные клетки суспендируют в 100 мкл буфера, содержащего 125 мМ трис-HCl, pH 6,8, 20% глицерин, 3% додецилсульфат натрия, 3% меркаптоэтанол, 0,005% бромфеноловый синий, инкубируют 10 мин в кипящей водяной бане, образцы объемом 10 мкл анализируют электрофорезом в 13,5% полиакриламидном геле с додецилсульфатом натрия. По окончании электрофореза гель прокрашивают при помощи кумасси R-250. После отмывки красителя гель сканируют и проводят математическую обработку результатов с помощью программы Scion Image (Scion Corp., США). По данным сканирования содержание полипептида FN3.54 составляет 15% от общего клеточного белка. На фиг.2 представлена электрофореграмма лизатов клеток штамма-продуцента Е.coli BL21(DE3)/pET3.54 в 13,5%-ном полиакриламидном геле (M-белковые маркеры молекулярной массы; стрелкой указан полипептид FN3.54, взаимодействующий с фактором некроза опухолей человека).
Пример 4.
Выделение и очистка рекомбинантного полипептида FN3.54.
Проводят индукцию биосинтеза полипептида FN3.54 в клетках штамма-продуцента Е.coli BL21(DE3)/pET3.54 ИПТГ (конечная концентрация 0,2 мМ) при 27°C в течение 4 ч. Клетки центрифугируют. 1 г влажной биомассы индуцированных клеток ресуспендируют в 10 мл буфера (50 мМ Трис-HCl pH 8,0; 200 мМ NaCl), после чего разрушают клетки обработкой в ультразвуковом дезинтеграторе Branson Sonifier 450, не допуская нагрева выше 10°C. Полученную суспензию центрифугируют 15 мин при 17000 об/мин. Осадок растворяют в 10 мл буфера A (20 мМ Трис-HCl, 200 мМ NaCl; pH 8,0), содержащего 6 М мочевину, в течение 1 ч при комнатной температуре и перемешивании. Раствор центрифугируют 15 мин при 17000 об/мин.
Выделение и очистку полипептида FN3.54 из супернатанта проводят с помощью Ni-аффинной хроматографии на колонке Ni-Sepharose FastFlow (GE Healthcare) объемом 2 мл в градиенте концентрации имидазола (0,1-0,5 М) в буфере Б (20 мМ Трис-HCl, 200 мМ NaCl, 4 М мочевина; pH 8,0). Объединенные фракции, содержащие очищенный белок и имеющие по данным белкового электрофореза чистоту более 90%, объединяют, проводят рефолдинг в течение 18 ч при 4°C в буфере С (20 мМ Трис-НС1, 100 мМ NaCl, 2 М мочевина, 0,5 М аргинин, 1 мМ ЭДТА; pH 8,0), диализуют против буфера Д (20 мМ Трис-HCl, 50 мМ NaCl; pH 8,0) и стерилизуют. Средний выход очищенного таким образом полипептида FN3.54 составляет 15 мг из 1 л культуры, что в 4,2 и в 8,3 раза больше, чем у прототипов M12.21 и Т09.07 соответственно.
Пример 5.
Определение специфичности полипептида FN3.54.
Специфичность полученного рекомбинантного белка подтверждают с помощью иммуноблот-анализа. Разделенные гель-электрофорезом по методу Лэммли белки (по 5 мкг ФНО, ГМ-КСФ и лизат клеток штамма-продуцента ФНО) переносят на нитроцеллюлозную мембрану (Bio-Rad, США), которую, после блокирования сайтов неспецифического связывания раствором 3% БСА (Sigma, США), инкубируют с исследуемым белком. Связавшийся полипептид выявляют с использованием конъюгата анти-His-HRP (Invitrogen, США) в соответствии с рекомендациями производителя. Визуализацию иммунного комплекса проводят, добавляя преципитирующий ТМВ (Clinical Science Products). Результаты показывают специфичность связывания рекомбинантного полипептида FN3.54 с ФНО (фиг.3).
Пример 6.
Взаимодействие полученного рекомбинантного полипептида FN3.54 с фактором некроза опухолей человека ИФА.
Способность полученного полипептида FN3.54 взаимодействовать с ФНО тестируют методом ИФА. На твердую фазу сорбируют рекомбинантный ФНО в концентрации 0,25 мкг/лунка и после блокирования мест неспецифического связывания раствором 3% бычьего сывороточного альбумина (БСА, "Sigma", США) инкубируют с очищенным полипептидом, добавленным в последовательных разведениях, начиная с 2 мкг. Иммунный комплекс выявляют добавлением конъюгата анти-His-HRP (Invitrogen, США) в разведении 1:10000. Для визуализации иммунных комплексов в лунки добавляют ТМВ (Clinical Science Products). В качестве отрицательного контроля в параллельных экспериментах тестируют связывание полипептида FN3.54 с БСА. Результаты экспериментов показывают способность полученного рекомбинантного полипептида связывать фактор некроза опухолей и отсутствие взаимодействия между FN3.54 и БСА. Величина константы взаимодействия, рассчитанная методом разведений [Beatty J.D., Beatty B.G., Vlahos W.G., Hill L.R. Method of analysis of non-competitive enzyme immunoassays for antibody quantification. J. Immunol. Methods. 1987. V.100. P.161-72], составляет 1,6×10-8 M.
Таким образом, заявляемое техническое решение позволяет получить рекомбинантный полипептид FN3.54 (искусственное антитело), специфически взаимодействующий с фактором некроза опухолей человека (ФНО-альфа). Биосинтез полипептида индуцибелен, уровень его биосинтеза составляет 15% от суммарного клеточного белка.
Перечень последовательностей, представленных в описании изобретения


Аминокислотная последовательность полипептида FN3.54, кодируемого рекомбинантной плазмидой рЕТ3.54.
SEQ ID NO 3.
CTGCTGATCTCTTGGXXXXXXXCGTTACTACCGTATC
Нуклеотидная последовательность праймера, использованного для конструирования библиотеки генов FN3

Нуклеотидная последовательность праймера, использованного для конструирования библиотеки генов FN3
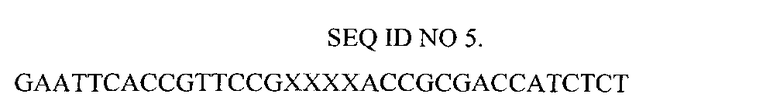
Нуклеотидная последовательность праймера, использованного для конструирования библиотеки генов FN3
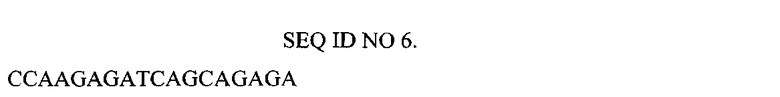
Нуклеотидная последовательность праймера, использованного для конструирования библиотеки генов FN3
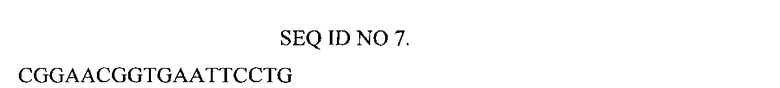
Нуклеотидная последовательность праймера, использованного для конструирования библиотеки генов FN3
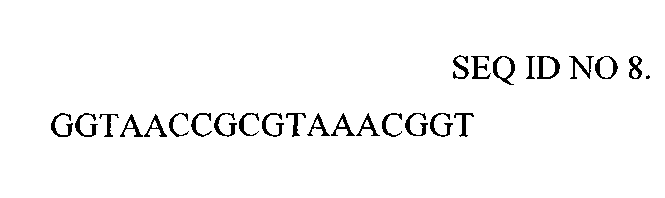
Нуклеотидная последовательность праймера, использованного для конструирования библиотеки генов FN3
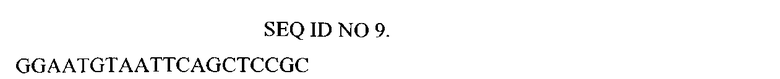
Нуклеотидная последовательность праймера, использованного для конструирования библиотеки генов FN3
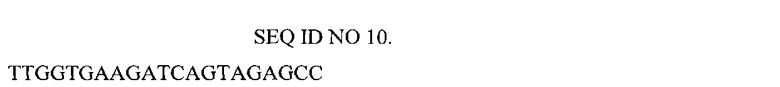
Нуклеотидная последовательность праймера, использованного для конструирования библиотеки генов FN3
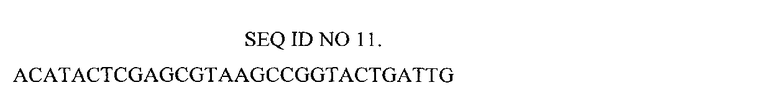
Нуклеотидная последовательность праймера, использованного для конструирования библиотеки генов FN3
Изобретение относится к биотехнологии и представляет собой рекомбинантную плазмидную ДНК pET3.54, кодирующую полипептид FN3.54, взаимодействующий с фактором некроза опухолей человека. Настоящее изобретение раскрывает также рекомбинантный штамм бактерий Escherichia coli BL21(DE3)/pET3.54 - продуцент полипептида FN3.54, взаимодействующего с фактором некроза опухолей человека. Настоящее изобретение позволяет получить целевой белок с высоким выходом при использовании меньшего количества индуктора и уровнем экспрессии более 15% суммарного клеточного белка. 2 н.п. ф-лы, 4 ил., 6 пр.
1. Рекомбинантная плазмидная ДНК pET3.54, кодирующая полипептид FN3.54, имеющий аминокислотную последовательность SEQ ID NO:2, взаимодействующий с фактором некроза опухолей человека с мол. массой 3,74 Md (5,660 т.п.о.), состоящая из NdeI/XhoI - фрагмента ДНК плазмиды pET32a длиной 5,366 т.п.о., включающего промотор бактериофага T7, терминатор транскрипции бактериофага T7, ген bla β-лактамазы, определяющий устойчивость трансформированных плазмидой pET3.54 клеток к ампициллину, участок ori инициации репликации; и NdeI/XhoI - фрагмента ДНК размером 0,294 т.п.о., содержащего ген Fn3.54, кодирующий аминокислотную последовательность полипептида FN3.54, взаимодействующего с фактором некроза опухолей человека.
2. Штамм бактерий Escherichia coli BL21(DE3)/pET3.54 - продуцент полипептида FN3.54, имеющий аминокислотную последовательность SEQ ID NO:2, взаимодействующего с фактором некроза опухолей человека.
| LIHUI XU, et al., Directed Evolution of high-affinity antibody mimics using mRNA display, Chemistry & Biology, Vol.9, August 2002, pp.933-942 | |||
| RU 2005129664 A, 27.03.2007 | |||
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК pFastBac-G2R-IgG, СОДЕРЖАЩАЯ ФРАГМЕНТ ГЕНОМА ВИРУСА НАТУРАЛЬНОЙ ОСПЫ, КОДИРУЮЩИЙ ФАКТОР НЕКРОЗА ОПУХОЛЕЙ СВЯЗЫВАЮЩИЙ БЕЛОК, И ФРАГМЕНТ ГЕНОМА ЧЕЛОВЕКА, КОДИРУЮЩИЙ УЧАСТОК ТЯЖЕЛОЙ ЦЕПИ ИММУНОГЛОБУЛИНА G, И ШТАММ БАКУЛОВИРУСА BvG2RIgG, ПРОДУЦИРУЮЩИЙ РАСТВОРИМЫЙ ХИМЕРНЫЙ БЕЛОК, СОСТОЯЩИЙ ИЗ БЕЛКА ВИРУСА НАТУРАЛЬНОЙ ОСПЫ, СВЯЗЫВАЮЩЕГО ФАКТОР НЕКРОЗА ОПУХОЛЕЙ, И ФРАГМЕНТА ТЯЖЕЛОЙ ЦЕПИ ИММУНОГЛОБУЛИНА G ЧЕЛОВЕКА | 2008 |
|
RU2376375C2 |
| US 7101978 B2, 05.06.2006 | |||
Авторы
Даты
2014-10-20—Публикация
2013-03-04—Подача