Изобретение относится к медицинской химии и касается биологически активных веществ, в частности N-гетарилзамещенных 4-гидрокси-1-метил-2,2-диоксо-1H-2λ6,1-бензотиазин-3-карбоксамидов, проявляющих анальгетическую активность, благодаря чему может быть использовано в химико-фармацевтической промышленности и медицине.
Среди известных лекарств, используемых современной медициной для борьбы с болями и болевыми синдромами различного происхождения, важное место занимают нестероидные противовоспалительные средства оксикамового ряда: N-гетарил-4-гидрокси-2-метил-1,1-диоксо-2H-1λ6,2-бензотиазин-3-карбоксамиды - пироксикам и мелоксикам [1]. К сожалению, при всех своих положительных сторонах эти лекарственные препараты не лишены различного рода недостатков, ставших причиной многочисленных противопоказаний и ограничений в их практическом применении. Основные из них - довольно высокая токсичность [2, 3] и необходимость для достижения анальгетического эффекта принимать значительные дозы препарата [4].
В основу настоящего изобретения поставлена задача получение новых менее токсичных ненаркотических анальгетиков, проявляющих высокий обезболивающий эффект в относительно низких дозах.
Поставленная задача достигается за счет того, что получены N-гетарилзамещенные 4-гидрокси-1-метил-2,2-диоксо-1H-2λ6,1-бензотиазин-3-карбоксамиды общей формулы (1):
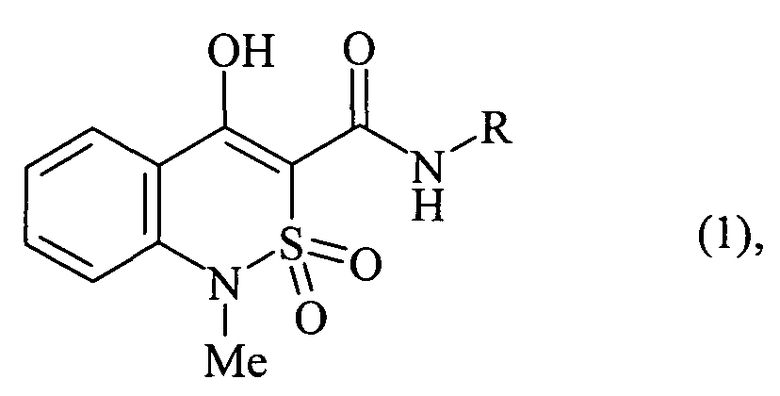
где R=5-метил-1,3-тиазол-2-ил (1a), или 4-этоксикарбонилметил-1,3-тиазол-2-ил (1б), или 6-метилпиридин-2-ил (1в), или 5-хлорпиридин-2-ил (1г), или пиримидин-2-ил (1д), проявляющие анальгетическую активность.
В соответствии с настоящим изобретением заявлено 5 индивидуальных химических соединений, представленных в таблице 1.
Заявленные соединения синтезируют взаимодействием метилового эфира 4-гидрокси-1-метил-2,2-диоксо-1H-2λ6,1-бензотиазин-3-карбоновой кислоты с соответствующими гетариламинами, которые обеспечивают получение заявленных структур 1а-1д, при температуре 150°C в ксилоле и в атмосфере аргона с последующим отделением образовавшегося осадка.
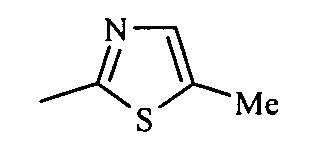
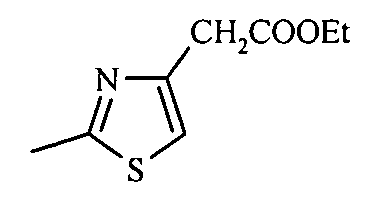
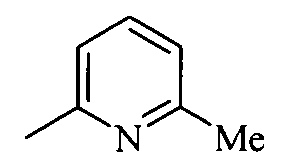
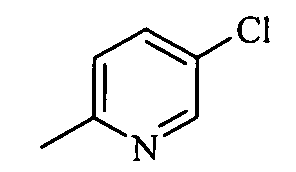
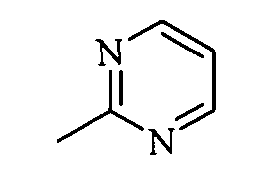
Изобретение иллюстрируется приведенными ниже примерами.
Пример 1. Получение 4-гидрокси-1-метил-N-(5-метил-1,3-тиазол-2-ил)-2,2-диоксо-1H-2λ6,1-бензотиазин-3-карбоксамид (1a). Смесь 2.69 г (0.01 моль) метилового эфира 4-гидрокси-1-метил-2,2-диоксо-1Н-2λ6,1-бензотиазин-3-карбоновой кислоты, 1.14 г (0.01 моль) 2-амино-5-метилтиазола и 5 мл ксилола выдерживают на металлической бане при 150°C в атмосфере аргону в течение 1 часа. Реакционную смесь охлаждают, прибавляют 5 мл этанола и оставляют на несколько часов при комнатной температуре. Образовавшиеся кристаллы амида 1а отфильтровывают, промывают холодным этиловым спиртом, сушат. Выход 3.12 г (89%). Т.пл. 277-279°C разл. (ДМФА-этанол, 1:5). Спектр ЯМР 1H, δ, м.д. (J, Гц): 15.09 (1H, с, 4-OH); 8.82 (1H, с, NH); 8.00 (1H, д, J=7.7, H-5); 7.50 (1H, т, J=7.6, Н-7); 7.18-7.11 (2H, м, H-6+H-8); 6.93 (1Н, с, Н-4′ тиазола); 3.27 (3H, с, NCH3); 2.37 (3H, с, 5′-CH3). Спектр ЯМР 13C, δ, м.д.: 169.9 (4-С-OH), 162.3 (С=O), 159.9 (С-2′ тиазола), 141.1 (С-8a), 133.1 (С-5), 128.9 (С-4′ тиазола), 127.7 (С-5′ тиазола), 125.5 (C-7), 123.5 (С-6), 122.8 (C-8), 117.2 (С-4а), 104.4 (С-3), 30.5 (NCH3), 12.1 (С-5′-CH3). Масс-спектр (ЭУ, 70 эВ), m/z (Iотн, %): 351 [M]+ (8.2), 237 (1.6), 211 (100), 147 (2.9), 140 (76.2), 114 (73.7), 105 (35.2), 91 (53.1), 72 (50.2). Найдено, %: C 47.76; H 3.65; N 12.03; S 18.11. C14H13N3O4S2. Вычислено, %: С 47.85; Н 3.73; N 11.96; S 18.25.
Пример 2. Получение 4-гидрокси-1-метил-N-(4-этоксикарбонилметил-1,3-тиазол-2-ил)-2,2-диоксо-1H-2λ6,1-бензотиазин-3-карбоксамида (1б). Смесь 2.69 г (0.01 моль) метилового эфира 4-гидрокси-1-метил-2,2-диоксо-1H-2λ6,1-бензотиазин-3-карбоновой кислоты, 1.86 г (0.01 моль) 2-амино-4-этокси-карбонилметилтиазола и 5 мл ксилола выдерживают на металлической бане при 150°C в атмосфере аргону в течение 1 часа. Реакционную смесь охлаждают, прибавляют 5 мл этанола и оставляют на несколько часов при комнатной температуре. Образовавшиеся кристаллы амида 1б отфильтровывают, промывают холодным этиловым спиртом, сушат. Выход 3.51 г (83%). Т.пл. 144-146°C (ДМФА-этанол, 1:8). Спектр ЯМР 1Н, δ, м.д. (J, Гц): 16.08 (1Н, с, 4-ОН); 9.67 (1Н, с, NH); 8.01 (1Н, д, J=7.8, Н-5); 7.58 (1Н, т, J=7.8, H-7); 7.25-7.18 (2Н, м, Н-6+Н-8); 7.04 (1Н, с, Н-5′ тиазола); 4.17 (2Н, к, J=7.2, ОСН2); 3.79 (2Н, с, CH2COOEt); 3.32 (3Н, с, NCH3); 1.29 (3H, т, J=7.2, OCH2CH3). Спектр ЯМР 13C, δ, м.д.: 172.6 (COOEt), 169.6 (4-С-OH), 162.8 (С=О), 162.6 (С-2′ тиазола), 141.2 (С-8a), 135.0 (С-4′ тиазола), 133.7 (С-5), 127.6 (С-7), 123.3 (С-6), 123.1 (С-8), 117.5 (С-4а), 111.5 (С-5′ тиазола), 105.0 (С-3), 61.6 (OCH2), 34.3 (CH2COOEt), 30.7 (NCH3), 14.7 (OCH2CH3). Масс-спектр (ЭУ, 70 эВ), m/z (Iотн, %): 423 [M]+ (14.0), 237 (1.9), 212 (47.0), 211 (88.8), 186 (58.0), 147 (5.4), 139 (100), 118 (20.9), 105 (35.1), 91 (53.9), 71 (30.7). Найдено, %: С 48.15; Н 3.96; N 9.98; S 15.02. C17H17N3O6S2. Вычислено, %: С 48.22; Н 4.05; N 9.92; S 15.14.
Пример 3. Получение 4-гидрокси-1-метил-N-(6-метилпиридин-2-ил)-2,2-диоксо-1H-2λ6,1-бензотиазин-3-карбоксамида (1в). Смесь 2.69 г (0.01 моль) метилового эфира 4-гидрокси-1-метил-2,2-диоксо-1H-2λ6,1-бензотиазин-3-карбоновой кислоты, 1.08 г (0.01 моль) 2-амино-6-метилпиридина и 5 мл ксилола выдерживают на металлической бане при 150°C в атмосфере аргону в течение 1 часа. Реакционную смесь охлаждают, прибавляют 5 мл этанола и оставляют на несколько часов при комнатной температуре. Образовавшиеся кристаллы амида 1в отфильтровывают, промывают холодным этиловым спиртом, сушат. Выход 3.17 г (92%). Т. пл. 234-236°C (ДМФА-этанол, 1:3). Спектр ЯМР 1H, δ, м.д. (J, Гц): 15.16 (1Н, уш. с, 4-ОН); 14.55 (1Н, с, CONH); 8.07-8.01 (2Н, м, Н-5+Н-4′); 7.89 (1Н, д, J=7.5, Н-3′); 7.58 (1Н, т, J=7.4, Н-7); 7.27-7.20 (2Н, м, Н-6+Н-8); 7.16 (1Н, д, J=7.1, H-5′); 3.32 (3Н, с, NCH3); 2.62 (3Н, с, 6′-CH3). Спектр ЯМР 13C, δ, м.д.: 174.5 (С=O), 164.1 (4-С-OH), 150.5 (С-6′), 149.7 (С-4′), 146.0 (С-2′), 141.3 (С-8a), 133.3 (С-4а), 127.8 (С-7), 125.0 (С-5′), 122.9 (С-5), 118.9 (С-8), 117.4 (С-3′), 113.8 (С-6), 104.8 (С-3), 30.7 (NCH3), 20.3 (С-6′-CH3). Масс-спектр (ЭУ, 70 эВ), m/z (Iотн, %): 345 [М]+ (8.5), 281 (13.9), 280 (19.8), 237 (52.0), 211 (100), 173 (9.7), 147 (12.1), 146 (23.5), 134 (47.2), 118 (15.2), 108 (75.6), 91 (58.0), 77 (30.9). Найдено, %: С 55.73; Н 4.41; N 12.20; S 9.36. C16H15N3O4S. Вычислено, %: С 55.64; Н 4.38; N 12.17; S 9.28.
Пример 4. Получение 4-гидрокси-1-метил-N-(5-хлорпиридин-2-ил)-2,2-диоксо-1H-2λ6,1-бензотиазин-3-карбоксамида (1г). Смесь 2.69 г (0.01 моль) метилового эфира 4-гидрокси-1-метил-2,2-диоксо-1H-2λ6,1-бензотиазин-3-карбоновой кислоты, 1.29 г (0.01 моль) 2-амино-5-хлорпиридина и 5 мл ксилола выдерживают на металлической бане при 150°C в атмосфере аргону в течение 1 часа. Реакционную смесь охлаждают, прибавляют 5 мл этанола и оставляют на несколько часов при комнатной температуре. Образовавшиеся кристаллы амида 1 г отфильтровывают, промывают холодным этиловым спиртом, сушат. Выход 3.44 г (94%). Т. пл. 230-232°C (ДМФА-этанол, 1:3). Спектр ЯМР 1H, δ, м.д. (J, Гц): 15.09 (1Н, уш. с, 4-ОН); 14.32 (1Н, с, CONH); 8.35 (1Н, д, J=1.4, Н-6′); 8.15 (1Н, д, J=8.1, Н-4′); 8.08 (1Н, д, J=7.9, H-5); 7.91 (1Н, д, J=8.0, H-3′); 7.77 (1Н, т, J=7.6, H-7); 7.48 (1Н, д, J=8.4, H-8); 7.37 (1Н, т, J=7.1, Н-6); 3.49 (3Н, с, NCH3). Спектр ЯМР 13C, δ, м.д.: 171.0 (С=O), 163.9 (4-С-OH), 150.0 (С-6′), 145.6 (С-4′), 144.6 (С-2′), 137.3 (С-8a), 134.5 (С-4а), 127.6 (С-7), 126.1 (С-5′), 124.2 (С-5), 123.9 (С-8), 118.4 (С-3′), 116.2 (С-6), 104.9 (С-3), 31.9 (NCH3). Масс-спектр (ЭУ, 70 эВ), m/z (Iотн, %): 365/367 [M]+ (2.5/3.1), 301/303 (40.4/13.4), 300/302 (30.9/16.4), 237 (6.7), 211 (6.2), 173 (24.6), 154/156 (6.5/3.2), 147 (24.2), 146 (69.5), 128/130 (100/49.4), 118 (9.5), 91 (24.1), 77 (27.2). Найдено, %: С 49.20; H 3.25; N 11.42; S 8.84. C15H12ClN3O4S. Вычислено, %: С 49.25; Н 3.31; N 11.49; S 8.77.
Пример 5. Получение 4-гидрокси-1-метил-N-(пиримидин-2-ил)-2,2-диоксо-1H-2λ6,1-бензотиазин-3-карбоксамида (1д). Смесь 2.69 г (0.01 моль) метилового эфира 4-гидрокси-1-метил-2,2-диоксо-1H-2λ6,1-бензотиазин-3-карбоновой кислоты, 0.95 г (0.01 моль) 2-аминопиримидина и 5 мл ксилола выдерживают на металлической бане при 150°C в атмосфере аргону в течение 1 часа. Реакционную смесь охлаждают, прибавляют 5 мл этанола и оставляют на несколько часов при комнатной температуре. Образовавшиеся кристаллы амида 1д отфильтровывают, промывают холодным этиловым спиртом, сушат. Выход 2.72 г (82%). Т. пл. 213-215°C (ДМФА-этанол, 1:3). Спектр ЯМР 1H, δ, м.д. (J, Гц): 14.38 (2Н, уш. с, 4-ОН+CONH); 8.83 (2Н, д, J=5.4, Н-4′+Н-6′); 8.03 (1H, д, J=8.0, H-5); 7.53 (1H, т, J=7.7, H-7); 7.36 (1H, т, J=5.2, H-5′); 7.22-7.15 (2H, м, Н-6+Н-8); 3.29 (3Н, c, NCH3). Спектр ЯМР 13C, δ, м.д.: 175.2 (С=O), 163.9 (4-С-ОН), 158.3 (С-2′), 154.5 (С-6′), 141.3 (С-4′), 133.4 (С-8a), 128.1 (С-4a), 125.3 (С-7), 123.1 (С-5), 117.6 (С-5′), 116.3 (C-8), 110.6 (С-6), 104.7 (C-3), 30.9 (NCH3). Масс-спектр (ЭУ, 70 эВ), m/z (Iотн, %): 268 (9.1), 237 (7.6), 211 (26.8), 173 (8.1), 147 (6.5), 146 (18.4), 121 (29.0), 118 (15.8), 95 (100), 91 (41.8), 77 (33.2). Найдено, %: С 50.66; Н 3.71; N 16.93; S 9.72. C14H12N4O4S. Вычислено, %: С 50.60; Н 3.64; N 16.86; S 9.65.
Спектры ЯМР 1H и 13C заявленных соединений записаны на приборе Varian Mercury-400 (400 и 100 МГц соответственно) в растворе ДМСО-d6, внутренний стандарт ТМС. Масс-спектры зарегистрированы на приборе Varian 1200L в режиме полного сканирования в диапазоне 35…700 m/z, ионизация электронным ударом 70 эВ при прямом вводе образца. Элементный анализ выполнен на микроанализаторе Euro Vector EA-3000. Температуры плавления определены в капилляре на цифровом анализаторе точки плавления SMP10 Stuart.
Пример 6. Острую токсичность N-гетарил-4-гидрокси-1-метил-2,2-диоксо-1H-2λ6,1-бензотиазин-3-карбоксамидов 1а-д изучали на интактных белых мышах весом 18-22 г по 6 животных в серии с каждой дозой. Исследуемые вещества вводили в виде тонкой водной суспензии, стабилизированной твином-80, перорально (при высоких дозах в 2-3 приема с интервалом 10 минут). Количество выживших животных регистрировали каждые 24 часа в течение 14 суток. Среднесмертельные дозы (LD50) рассчитывали по методу Кербера [5]. Приведенные в таблице 2 данные свидетельствуют о том, что все заявленные вещества по классификации К.К. Сидорова [6], по крайней мере, являются малотоксичными. Пироксикам и мелоксикам значительно уступают им по этому показателю, поскольку по данным литературы [2, 3] их среднесмертельные дозы для мышей перорально составляют всего лишь 250 и 470 мг/кг соответственно.
Пример 7. Анальгетическая активность заявленных N-гетарил-4-гидрокси-1-метил-2,2-диоксо-1H-2λ6,1-бензотиазин-3-карбоксамидов 1а-д изучена на модели термического раздражения кончика хвоста белых крыс (tail-flick) [7]. Кончик хвоста подопытного животного погружают в нагретую до 54°C водяную баню. Определяют исходную продолжительность латентного периода иммерсии (отдергивания) хвоста, выраженную в секундах. Анальгетический эффект (в %) оценивают по изменению длительности латентного периода через 1 ч после введения исследуемых веществ. Для получения статистически достоверных результатов (принят уровень значимости доверительного интервала p≤0.05) в тестировании каждого из заявленных амидов 1а-д, препаратов сравнения и в контроле было задействовано по 7 подопытных животных. Все тестируемые вещества и препараты сравнения (пироксикам и мелоксикам) вводили перорально в виде стабилизированных Твином-80 тонких водных суспензий или растворов в дозе 20 мг/кг. Животные контрольной группы получали эквивалентное количество воды и твина-80.
Представленные в табл.2 полученные экспериментальные данные свидетельствуют о том, что все заявленные соединения способны подавлять вызванную термическим раздражением болевую реакцию гораздо эффективнее, чем известные препараты мелоксикам и пироксикам в одинаковых с ними дозах.
Таким образом, заявленные N-гетарил-4-гидрокси-1-метил-2,2-диоксо-1H-2λ6,1-бензотиазин-3-карбоксамиды по анальгетическим свойствам в несколько раз активнее препаратов сравнения при значительно более низкой токсичности. Все соединения синтезируют из доступных реагентов и по простым методикам, которые могут быть воспроизведены в условиях химико-фармацевтических предприятий или лабораторий с использованием стандартного оборудования.
N-Гетарилзамещенные 4-гидрокси-1-метил-2,2-диоксо-1H-2λ6,1-бензо-тиазин-3-карбоксамиды могут быть использованы как субстанции при создании анальгетических средств в различных лекарственных формах.
Источники информации
1. Машковский М.Д. Лекарственные средства. - М.: РИА «Новая волна»: Издатель Умеренков, 2009. - С.176-178.
2. Kleemann A., Engel J. / Pharmaceutical substances. Synthesis, patents, applications. - Multimedia Viewer, Version 2.00. - Stuttgart: Georg Thime Verlag. 2001.
3. The Merck Index on CD-ROM. - Version 12:3, Merck & Co Inc, Whitehouse station, NJ, USA, 2000. - Published on CD-ROM by Chapman & Hall/CRC.
4. Сигидин Я.А., Шварц Г.Я., Арзамасцев А.П., Либерман С.С./ Лекарственная терапия воспалительного процесса (экспериментальная и клиническая фармакология противовоспалительных препаратов). - М.: Медицина, 1988. - С.62-63.
5. Сернов Л.Н., Гацура В.В. Элементы экспериментальной фармакологии. - М.: ППП "Типография "Наука". - 2000. - С.318.
6. Сидоров К.К. О классификации токсичности ядов при парентеральных способах введения // В кн. Токсикология новых промышленных химических веществ. - М.: Медицина, 1973. - Вып.13. - С.50.
7. Drug Discovery and Evaluation: Pharmacological Assays / H.G. Vogel (Ed.), 3rd ed. - Berlin: Springer. - 2008. - P.1011.
| название | год | авторы | номер документа |
|---|---|---|---|
| 4-ГИДРОКСИ-N-(2-КАРБОКСИФЕНИЛ)1-МЕТИЛ-2,2-ДИОКСО-1H-2λ,1-БЕНЗОТИАЗИН-3-КАРБОКСАМИД, ПРОЯВЛЯЮЩИЙ ДИУРЕТИЧЕСКУЮ АКТИВНОСТЬ | 2013 |
|
RU2535997C1 |
| СПОСОБ ПОЛУЧЕНИЯ 3-АМИНО-8-ГИДРОКСИ-1,6-ДИОКСО-2,7-ДИАЗАСПИРО[4.4]НОН-3-ЕН-4-КАРБОНИТРИЛОВ | 2012 |
|
RU2495040C1 |
| Способ получения аммонийных солей 3-амино-8-гидрокси-1,6-диоксо-4-циано-2,7-диазаспиро[4.4]нон-3-ен-2-идов | 2016 |
|
RU2631856C1 |
| 3'-Ароил-4'-гидрокси-1'-(2-гидроксиметилфенил)-2Н,4Н-спиро[1,4-бензотиазин-2,2'-пиррол]-3,5'(1'Н)-дионы, обладающие анальгетической активностью | 2019 |
|
RU2714511C1 |
| 7α-(1-ГИДРОКСИ-2,2,2-ТРИФТОРЭТИЛ)-17-МЕТИЛ-3,6-ДИМЕТОКСИ-4,5α-ЭПОКСИ-6α,14αЭТЕНОИЗОМОРФИНАН И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2012 |
|
RU2503678C1 |
| Способ получения 3-ароил-N-бензил-2-гидрокси-1-оксобензо[d]пирроло[2,1-b]тиазол-3а(1Н)-карбоксамидов | 2021 |
|
RU2764906C1 |
| 1-АРИЛПИРРОЛО[1,2-A]ПИРАЗИН-3-КАРБОКСАМИДЫ С НЕЙРОПСИХОТРОПНОЙ АКТИВНОСТЬЮ | 2014 |
|
RU2572076C2 |
| Применение 5-бензоил-4-гидрокси-N-(4-йодфенил)-6-(4-хлорфенил)-2-оксогексагидропиримидин-4-карбоксамида в качестве средства, обладающего анальгетической активностью | 2023 |
|
RU2811249C1 |
| НОВЫЕ ПРОИЗВОДНЫЕ БЕНЗОТИАЗИНОНА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ АНТИБАКТЕРИАЛЬНЫХ СРЕДСТВ | 2006 |
|
RU2395508C1 |
| ПРИМЕНЕНИЕ N-[1-АРИЛ-3-ОКСО-2-АЗАСПИРО[3.5]НОНАН-2-ИЛ]БЕНЗАМИДОВ В КАЧЕСТВЕ АНАЛЬГЕТИЧЕСКИХ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2023 |
|
RU2810704C1 |
Изобретение относится к области органической химии, а именно к N-гетарилзамещенным 4-гидрокси-1-метил-2,2-диоксо-1H-2λ6,1-бензотиазин-3-карбоксамидам, общей формулы:
 ,
,
где R=5-метил-1,3-тиазол-2-ил, или 4-этоксикарбонилметил-1,3-тиазол-2-ил, или 6-метилпиридин-2-ил, или 5-хлорпиридин-2-ил, или пиримидин-2-ил. Технический результат: получены новые производные N-гетарилзамещенные 4-гидрокси-1-метил-2,2-диоксо-1H-2λ6,1-бензотиазин-3-карбоксамиды, проявляющие анальгетическую активность. 2 табл., 7 пр.
N-Гетарилзамещенные 4-гидрокси-1-метил-2,2-диоксо-1H-2λ6,1-бензотиазин-3-карбоксамиды общей формулы:
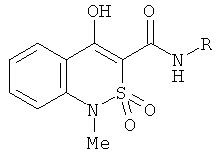
где R=5-метил-1,3-тиазол-2-ил, или 4-этоксикарбонилметил-1,3-тиазол-2-ил, или 6-метилпиридин-2-ил, или 5-хлорпиридин-2-ил, или пиримидин-2-ил, проявляющие анальгетическую активность.
| US 5004742 A1, 02.04.1991 | |||
| Способ получения енольных производных оксикамов | 1984 |
|
SU1503682A3 |
Авторы
Даты
2015-03-20—Публикация
2013-12-18—Подача