Предлагаемое изобретение относится к способам получения новых магнийорганических соединений (МОС), конкретно к совместному способу получения 2,3-диалкилмагнезациклогепт-2-енов общей формулы (1) и 4,5-диалкилмагнезациклогепт-4-енов общей формулы (2):
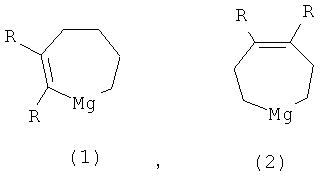
где R-C2H5, н-С3H7, н-С4H9.
Предлагаемые соединения могут найти применение в качестве компоненты каталитических систем в процессах олиго- и полимеризации олефинов, диенов и ацетиленов, а также в тонком органическом и металлоорганическом синтезах.
Известен способ [У.М.Джемилев, Р.М.Султанов, Р.Г.Гаймалдинов, Г.А.Толстиков. Каталитический синтез и превращения магнийциклоалканов. Сообщение 1. Новые каталитические превращения в ряду макгнийциклопентанов. Изв. АН СССР, Сер. хим. №6, 1991, с.1388-1393] совместного получения пятичленного и семичленного циклических МОС, а именно 2-фенилмагнезациклопентана (3) и 2,4-дифенилмагнезациклогептана (III) с выходом 70% и 5% соответственно, взаимодействием магнезациклопентана (5) со стиролом, взятых в мольном соотношении 1:1, в присутствии 2-3 мол.% Cp2ZrCl2 в растворе ТГФ при 25°C (1.5 ч) по схеме:
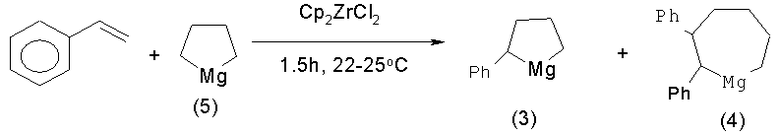
Известный способ не позволяет получать МОС (1) и (2).
Известен способ [K.F.Fujita, Y.Ohnuma, H.Yasuda, H.Tani. Magnesium-butadiene Addition Compounds Isolation, Stmctural Analysis and Chemical Reactivity // J. Organomet. Chem., 201 (1976) 113] получения непредельного магнийорганического соединения, а именно магнезациклонона-3,7-диена общей формулы (6). Реакцией бутадиена с металлическим магнием в присутствии каталитических количеств метилиодида при температуре 40°С в тетра-гидрофуране за 48 часов с выходом 69% по схеме:
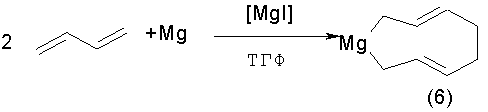
Известным способом не могут быть получены 2,3-диалкилмагнезациклогепт-2-ены (1) и 4,5-диалкилмагнезациклогепт-4-ены (2).
Известен способ получения 2,3,4,5-тетраалкилмагнезациклопента-2,4-диенов (7) [Патент РФ №2290406 (2006)] взаимодействием дизамещенных ацетиленов с н-BuMgCl в присутствии цирконацендихлорида Cp2ZrCl2, взятых в мольном соотношении R-≡-R:н-BuMgCl:Cp2ZrCl2=10:(20-26):(1,0-1,4). Реакцию проводят в атмосфере аргона при комнатной температуре (~20°C) и атмосферном давлении. Время реакции 10-14 часов, выход целевых продуктов 45-60%. Реакция осуществляется в диэтиловом эфире и протекает по схеме:
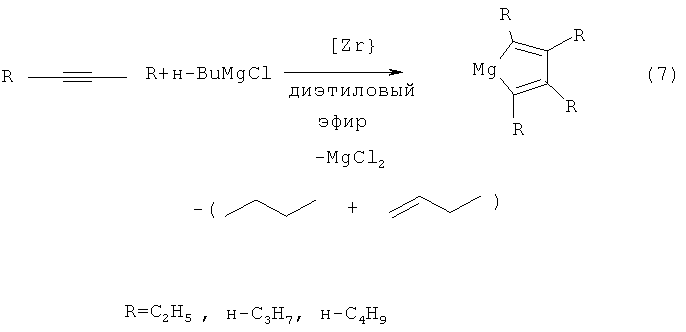
Известный способ не позволяет получать 2,3-диалкилмагнезациклогепт-2-ены (1) и 4,5-диалкилмагнезациклогепт-4-ены (2).
Таким образом, в литературе отсутствуют сведения по синтезу 2,3-диалкилмагнезациклогепт-2-ены общей формулы (1) и 4,5-диалкилмагнезациклогепт-4-ены общей формулы (2).
Предлагается новый способ совместного получения 2,3-диалкилмагнезациклогепт-2-енов (1) и 4,5-диалкилмагнезациклогепт-4-енов (2).
Сущность способа заключается во взаимодействии 2,3-диалкилзамещенных магнезациклопент-2-енов (8) и этилена в присутствии катализатора цирконацендихлорида CpiZrClz. Соотношение (8):Cp2ZrCl2=10:(0,3-0,6). В реакционной зоне избыточное давление этилена поддерживается в пределах 1,0-1,5 МПа. Реакцию проводят при комнатной температуре (~20°C). Время реакции 6-8 часов. В качестве растворителя необходимо использовать смесь диэтилового эфира и тетрагидрофурана в объемном соотношении Et2O:ТГФ=5:1, в других растворителях выход целевых продуктов (1) и (2) незначителен. Выход целевых продуктов (1) и (2) 60-80%.
Реакция протекает по схеме:
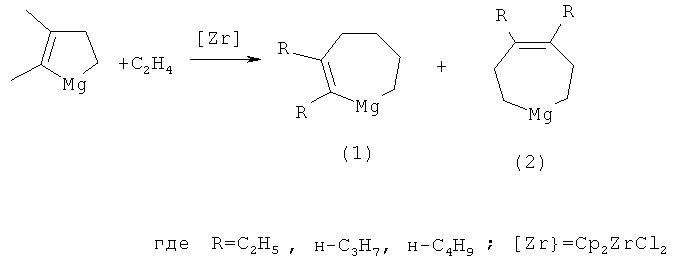
Целевые продукты (1) и (2) образуются лишь с участием в реакции дизамещенных магнезациклопентенов (8), этилена и катализатора Cp2ZrCl2. В присутствии других катализаторов на основе комплексов переходных металлов (например, Ni(acac)2, Fe(acac)3, Cp2TiCl2, Pd(acac)2, CuCl, TiOBu)4) целевые продукты (1) и (2) не образуются.
Проведение реакции в присутствии катализатора Cp2ZrCl2 больше 6 мол.% по отношению к (8) не приводит к существенному увеличению целевых продуктов (1) и (2). Использование в реакции катализатора Cp2ZrCl2 менее 3 мол.% снижает выход МОС (1) и (2). Опыты проводили при комнатной температуре ~20°C.
При более высоких температурах (например, 50°C) уменьшается выход (1) и (2), а при низких температурах (например, 0°C) снижается скорость реакции.
Изменение давления этилена в сторону увеличения приводит к образованию циклических МОС более крупных размеров, а снижение давления ниже 1,0 МПа уменьшает выход целевых продуктов (1) и (2). Существенные отличия предлагаемого способа:
1. В предлагаемом способе в качестве исходных соединений используются 2,3-диалкилзамещенные магнезациклопент-2-ены, этилен, а также катализатор Cp2ZrCl2. В известном способе циклическое непредельное МОС (7) получают с помощью дизамещенных ацетиленов и н-BuMgCl в присутствии катализатора Cp2ZrCl2.
Предлагаемый способ обладает следующими преимуществами:
1. Способ позволяет получать с высоким выходом 2,3-диалкилмагнезациклогепт-2-ены (1) и 4,5-диалкилмагнезациклогепт-4-ены (2), синтез которых в литературе не описан. Способ поясняется следующими примерами:
ПРИМЕР 1. В автоклав из нержавеющей стали объемом 100 мл в атмосфере аргона помещают 50 ммоль предварительно полученного 2,3-дипропилмагнезациклопент-2-ена (8) (1,ОМ раствор в Et2O), 10 мл сухого ТГФ, при температуре 0°C в эту смесь вносят 1,5 ммоль катализатора Cp2ZrCl2, температуру доводят до комнатной и автоклав герметично закрывают. Через специальное устройство в автоклав закачивается этилен. Избыточное давление этилена в реакционной зоне поддерживается на уровне 1,0 МПа до завершения реакции. Реакционная смесь перемешивается при комнатной температуре 6 часов. Получают смесь 2,3-дипропилмагнезациклогепт-2-ена (1) и 4,5-дипропилмагнезациклогепт-4-ена (2) в соотношении (1):(2)=1:1. Выход целевых продуктов определяли по продуктам гидролиза. При гидролизе МОС (1) и (2) образуются 5-пропилнон-4-ен (9) и 4,5-диэтилокт-4-ен (10) с общим выходом 60%, а при дейтеролизе соответственно 1,9-дидейтеро-5-пропилнон-4-ен (11) и 1,6-дидейтеро-3,4-дипропилгекс-3-ен (12).
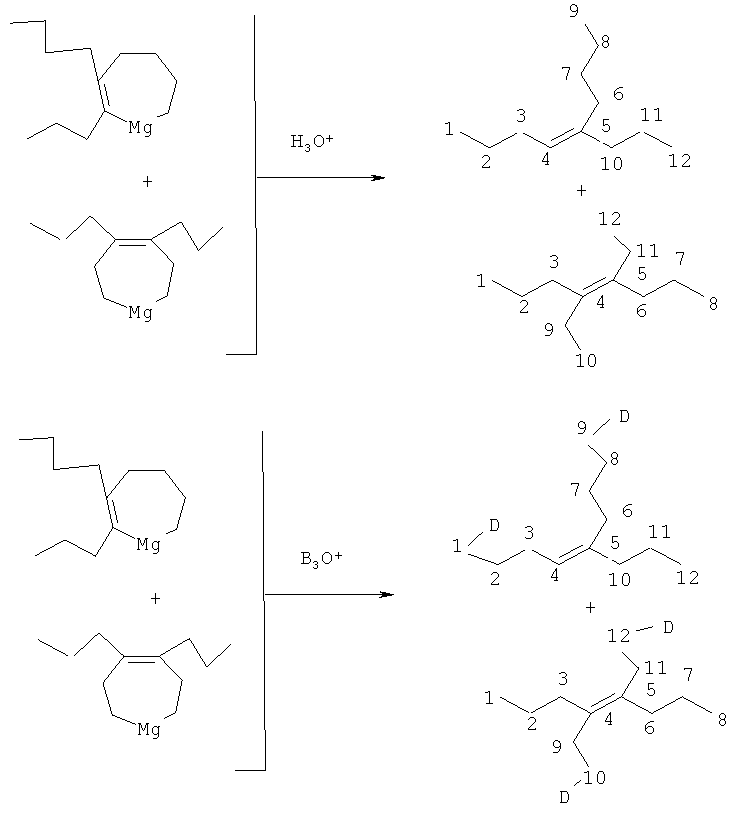
Спектральные характеристики продуктов гидролиза и дейтеролиза:
5-Пропилнон-4-ен (9): Т.кип. 112°C (30 мм рт.ст.). Спектр ЯМР 1H(δ, м.д.): 0.87-0.98 м (9Н, CH3), 1.28-1.52 м (8Н, CH2), 1.68-2,07 м (6Н, CH2), 5.0-5.1 м (1Н,=CH). Спектр ЯМР 13С (δ, м.д.): 14.00 (С1), 23.80 (С2), 31.80 (С3), 125.55 (С4), 31.25 (С5), 31.25 (С6), 30.25 (С7), 22.70 (С8), 13.85 (С9), 34.30 (С10), 21,05 (С11), 13.70 (С12). [M] 168. 4,5-Диэтилокт-4-ен (10): Т.кип. 109°C, (30 мм рт.ст.). Спектр ЯМР 1H(δ, м.д.): 0.87-0.90 м (12Н, CH3), 1.37-1.96 м (8Н, CH2, 1.99-2.15 м (4Н, =СН2). Спектр ЯМР 13С (δ, м.д.): 14.36 (С1, С8), 21.47 (С2, С7), 32.70 (С3, С6), 133.4 (С4, С5), 23.30 (С9, С11), 12.21 (С10, С12). [М]+ 168.
1,9-Дидейтеро-5-пропилнон-4-ен (11): Т.кип. 112°C (30 мм рт.ст.). Спектр ЯМР 1Н (δ, м.д.): 0.88-0.92 м (8Н, CH2, CH2D), 1.29-1.46 м (8Н, СН2), 1.93-1.97 м (6Н, =CH2). Спектр ЯМР 13С (δ, м.д.): 13.70 (С1), 23.80 (С2), 31.80 (С3), 126.55 (С4, JC-D=19 Гц), 143.50 (С5), 38.35 (С6), 29.30 (С7), 23.05 (С8), 13.60 (С9, JC-D=19 Гц), 39.16 (С10), 21,20 (С11), 13.90 (С12). [М]+ 170.
1,6-Дидейтеро-3,4-дипропилгекс-3-ен (12): Т.кип.110°C (30 мм рт.ст.).
Спектр ЯМР 1H(δ, м.д.): 0.91-0.99 м (10Н, CH3, CH2D), 1.43-1.51 м (4Н, CHz), 1.90-2.11 м (8Н, =СН2). Спектр ЯМР 13С (5, м.д.): 11.01 (С1, С6, jc-d=19 Гц), 26.11 (С2, С5), 129.41 (С3, С4), 33.12 (С7, С10), 21.75 (С8, С11), 13.89 (С9, С12). [М]+ 170.
Другие примеры, подтверждающие способ, приведены в таблице 1.
Все опыты проводили при комнатной температуре (~20°C) в смеси растворителей Еt2O:ТГФ (5:1).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 2,3,4,5-ТЕТРААЛКИЛМАГНЕЗАЦИКЛОГЕПТА-2,4-ДИЕНОВ | 2010 |
|
RU2440354C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3-ДИАЛКИЛ-5-АЛКИЛИДЕНМАГНЕЗАЦИКЛОПЕНТ-2-ЕНОВ | 2005 |
|
RU2291870C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3,4,5-ТЕТРААЛКИЛМАГНЕЗАЦИКЛОПЕНТА-2,4-ДИЕНОВ | 2005 |
|
RU2290406C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,4-ДИФЕНИЛМАГНЕЗАЦИКЛОГЕПТАНА | 2009 |
|
RU2423367C2 |
| СПОСОБ ПОЛУЧЕНИЯ 3,4-ДИАЛКИЛМАГНЕЗАЦИКЛОПЕНТАНОВ | 2009 |
|
RU2423364C2 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3,4,5-ТЕТРААЛКИЛМАГНЕЗАЦИКЛОПЕНТА-2,4-ДИЕНОВ | 2008 |
|
RU2397174C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-ХЛОРО-2,3,4,5-ТЕТРААЛКИЛАЛЮМИНАЦИКЛОПЕНТА-2,4-ДИЕНОВ | 2005 |
|
RU2283315C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,3,4-ТРИАЛКИЛМАГНЕЗАЦИКЛОПЕНТ-2-ЕНОВ | 2009 |
|
RU2423365C2 |
| СПОСОБ ПОЛУЧЕНИЯ 3,4-ДИАЛКИЛ-2,5-БИС(ТРИМЕТИЛСИЛИЛ)-МАГНЕЗАЦИКЛОПЕНТА-2,4-ДИЕНОВ | 2005 |
|
RU2290405C1 |
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ 1-(ДИАЛКИЛАМИН)-2,3-ДИАЛКИЛ(ФЕНИЛ)-АЛЮМАЦИКЛОПРОПЕНОВ, 1-(ДИАЛКИЛАМИН)-2,3-ДИАЛКИЛ(ФЕНИЛ)АЛЮМАЦИКЛОПЕНТ-2-ЕНОВ И 1-(ДИАЛКИЛАМИН)-2,3,4,5-ТЕТРААЛКИЛАЛЮМАЦИКЛОПЕНТАДИЕНОВ | 1999 |
|
RU2157374C1 |
Изобретение относится к металлоорганическому синтезу, конкретно к способу совместного получения 2,3-диалкилмагнезациклогепт-2-енов общей формулы (1):
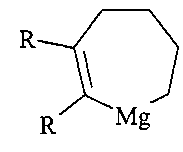 , где R=С2Н5, Н-С3Н7, Н-С4Н9,
, где R=С2Н5, Н-С3Н7, Н-С4Н9,
и 4,5-диалкилмагнезациклогепт-4-енов общей формулы (2):
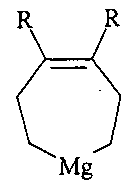 , где R=С2Н5, H-С3Н7, H-С4Н9.
, где R=С2Н5, H-С3Н7, H-С4Н9.
Способ включает взаимодействие 2,3-диалкилмагнезациклопент-2-енов с этиленом в присутствии катализатора - цирконацендихлорида Cp2ZrCl2 под избыточным давлением этилена 1.0-1.5 МПа при мольном соотношении 2,3-диалкилмагнезациклопент-2-ен:Cp2ZrCl2=10:(0,3-0,6). Способ проводят в смеси растворителей диэтиловый эфир-ТГФ, взятых в объемном соотношении 5:1, при температуре ~20°C в течение 6-8 часов. Полученные соединения могут найти применение в качестве сокатализаторов в процессах олигомеризации, полимеризации олефинов, ацетиленов, диенов, а также исходных реагентов для синтеза различных бифункциональных и гетероциклических соединений. 1 табл., 1 пр.
Способ совместного получения 2,3-диалкилмагнезациклогепт-2-енов общей формулы (1):
 , где R=С2Н5, Н-С3Н7, Н-С4Н9,
, где R=С2Н5, Н-С3Н7, Н-С4Н9,
и 4,5-диалкилмагнезациклогепт-4-енов общей формулы (2):

где R=С2Н5, H-С3Н7, H-С4Н9,
характеризующийся тем, что взаимодействие 2,3-диалкилмагнезациклопент-2-енов с этиленом в присутствии катализатора - цирконацендихлорида Cp2ZrCl2 проводят под избыточным давлением этилена 1.0-1.5 МПа, при мольном соотношении 2,3-диалкилмагнезациклопент-2-ен:Cp2ZrCl2=10:(0,3-0,6), в смеси растворителей диэтиловый эфир-ТГФ, взятых в объемном соотношении 5:1, при температуре ~20°C в течение 6-8 часов.
| ДЖЕМИЛЕВ У.М | |||
| и др., Каталитический синтез и превращения магнийциклоалканов | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Новые каталитические превращения в ряду магнийцикопентанов, Изв | |||
| АН СССР, 1991, N 6, с | |||
| Групповой батарейный коммутатор контроллерного типа для телеграфных аккумуляторных батарей | 1924 |
|
SU1388A1 |
| СУЛТАНОВ Р.М | |||
| и др., Селективное циклометаллирование дизамещенных ацетиленов и этилена с помощью Et[2]Mg и EtMgHlg в присутствии комплексов Zr, Журнал | |||
Авторы
Даты
2015-04-10—Публикация
2010-07-20—Подача