Настоящее изобретение относится к новым двухвалентным биспецифическим антителам, их получению и применению.
Предпосылки создания изобретения
В данной области известны сконструированные белки, такие как би- и мультиспецифические антитела, которые могут связываться с двумя или большим количеством антигенов. Указанные мультиспецифические связывающие белки можно создавать на основе методов клеточного слияния, химической конъюгации или рекомбинантной ДНК.
В последние годы создано широкое разнообразие форматов рекомбинантных биспецифических антител, например четырехвалентные биспецифические антитела, полученные путем слияния, например антитела IgG-формата и одноцепочечных доменов (см., например, Coloma M.J. и др., Nature Biotech 15, 1997, cc.159-163; WO 001/077342 и Morrison S.L., Nature Biotech 25, 2007, cc.1233-1234).
Разработано также несколько других новых форматов, в которых уже не сохранялась основная структура антитела (IgA, IgD, IgE, IgG или IgM), таких как диа-, триа- или тетратела, мини-тела, несколько одноцепочечных форматов (scFv, бис-scFv), которые могут связывать два или большее количество антигенов (Holliger Р. и др., Nature Biotech 23, 2005, cc.1126-1136; Fischer N., Leger О., Pathobiology 74, 2007, cc.3-14; Shen J и др., Journal of Immunological Methods 318, 2007, cc.65-74; Wu С. и др., Nature Biotech 25, 2007, cc.1290-1297).
Во всех указанных форматах используют линкеры либо для слияния основной структуры антитела (IgA, IgD, IgE, IgG или IgM) с дополнительным связывающим белком (например, scFv), либо для слияния, например, двух Fab-фрагментов или scFv (Fischer N., Leger О., Pathobiology 74, 2007, cc.3-14). Хотя очевидно, что линкеры имеют преимущество при создании биспецифических антител, с ними могут быть связаны также проблемы терапевтического плана. Фактически эти чужеродные пептиды могут вызывать иммунный ответ против самого линкера или области стыка между белком и линкером. Кроме того, гибкая природа этих пептидов делает их более чувствительными к протеолитическому расщеплению, что может приводить к плохой стабильности, агрегации и повышению иммуногенности антитела. Кроме того, может существовать необходимость в поддержании эффекторных функций, таких как комплементзависимая цитотоксичность (CDC) или антитело-обусловленная клеточнозависимая цитотоксичность (ADCC), которые опосредуются Fc-областью, путем сохранения высокой степени сходства с встречающимися в естественных условиях антителами.
Таким образом, в идеальном варианте необходимо создавать биспецифические антитела, которые обладают очень сходной общей структурой с встречающимися в естественных условиях антителами (типа IgA, IgD, IgE, IgG или IgM), с минимальным отклонением от человеческих последовательностей.
В соответствии с одним из подходов биспецифические антитела с высокой степенью сходства с встречающимися в естественных условиях антителами создавали с помощью технологии квадром (квадрогибридом) (см. Milstein С. и А.С.Cuello, Nature, 305, 1983, cc.537-540) на основе соматического слияния двух различных клеточных линий гибридом, экспрессирующих мышиные моноклональные антитела с требуемыми специфичностями биспецифического антитела. В результате случайного спаривания тяжелых и легких цепей двух различных антител в образующейся линии клеток гибрида гибридомы (или квадромы) получают вплоть до 10 различных видов антител, из которых только одно представляет собой требуемое функциональное биспецифическое антитело. Из-за присутствия ошибочно спаренных побочных продуктов и в значительной степени сниженного выхода продукта, требуются более сложные процедуры очистки (см., например, Morrison S.L., Nature Biotech 25, 2007, cc.1233-1234). В целом, эта же проблема, связанная с ошибочно спаренными побочными продуктами, сохраняется при применении методов рекомбинантной экспрессии.
Подход, с помощью которого можно обойти проблему, связанную с имеющими ошибочные спаривания побочными продуктами, известный под названием «knobs-into-holes» (взаимодействие по типу «выступ-впадина»), направлен на усиление спаривания двух различных тяжелых цепей антитела путем интродукции мутаций в СН3-домены для модификации поверхности раздела в области контакта. На одной цепи имеющие большие размеры аминокислоты заменяли на аминокислоты с короткими боковыми цепями для создания «впадины». И, наоборот, аминокислоты с более крупными боковыми цепями интродуцировали в другой CH3-домен, создавая «выступ». Путем совместной экспрессии этих двух тяжелых цепей (и двух идентичных легких цепей, которые должны соответствовать обеим тяжелым цепям), получали высокий выход гетеродимерной формации («выступ-впадина») относительно гомодимерной формации («впадина-впадина» или «выступ-выступ») (Ridgway J.В., Presta L.G., Carter Р. и WO 1996/027011). Процентное содержание гетеродимера можно дополнительно повышать путем ремоделирования поверхностей раздела двух СН3-доменов с помощью технологии фагового дисплея и интродукции дисульфидного мостика для стабилизации гетеродимеров (Merchant А.М. и др., Nature Biotech 16, 1998, cc.677-681; Atwell S., Ridgway J.B., Wells J.A., Carter P., J Mol Biol 270, 1997, cc.26-35). Новые подходы к технологии «knobs-into-holes» описаны, например, в ЕР 1870459 А1. Хотя указанный формат, вероятно, является очень привлекательным, в настоящее время отсутствуют данные о его развитии в направлении клинического применения. Одним из важных ограничений этой стратегии является то, что легкие цепи двух родительских антител должны быть идентичными для предупреждения ошибочных спариваний и формирования неактивных молекул. Таким образом, эта технология не пригодна для более легкого создания рекомбинантных двухвалентных биспецифических антител к двум антигенам с использованием в качестве исходных двух антител к первому и второму антигену, поскольку должны быть оптимизированы или тяжелые цепи этих антител, и/или идентичные легкие цепи.
В WO 2006/093794 описаны композиции гетеродимерных связывающих белков. В WO 99/37791 описаны многоцелевые производные антител. У Morrison и др., J. Immunolog, 160, 1998, cc.2802-2808 описано влияние замены вариабельных областей на функциональные свойства IgG.
Краткое изложение сущности изобретения
Настоящее изобретение относится к двухвалентному биспецифическому антителу, содержащему:
а) легкую цепь и тяжелую цепь антитела, специфически связывающегося с первым антигеном; и
б) легкую цепь и тяжелую цепь антитела, специфически связывающегося со вторым антигеном, в котором вариабельные домены VL и VH заменены друг на друга
и
в котором CL- и CH1-домены константных областей (константные домены CL и СН1) заменены друг на друга.
Следующим вариантом осуществления изобретения является способ получения двухвалентного биспецифического антитела, предлагаемого в изобретении, заключающийся в том, что
а) трансформируют клетку-хозяина
- векторами, которые содержат молекулы нуклеиновых кислот, кодирующие легкую цепь и тяжелую цепь антитела, которое специфически связывается с первым антигеном,
- векторами, которые содержат молекулы нуклеиновых кислот, кодирующие легкую цепь и тяжелую цепь антитела, которое специфически связывается со вторым антигеном, в котором вариабельные домены VL и VH заменены друг на друга
и
в котором константные домены CL и СН1 заменены друг на друга;
б) культивируют клетку-хозяина в условиях, которые позволяют синтезировать указанную молекулу антитела; и
в) выделяют молекулу антитела из культуры.
Следующим вариантом осуществления изобретения является клетка-хозяин, содержащая
- векторы, которые содержат молекулы нуклеиновых кислот, кодирующие легкую цепь и тяжелую цепь антитела, которое специфически связывается с первым антигеном,
- векторы, которые содержат молекулы нуклеиновых кислот, кодирующие легкую цепь и тяжелую цепь антитела, которое специфически связывается со вторым антигеном, в котором вариабельные домены VL и VH заменены друг на друга
и
в котором константные домены CL и СН1 заменены друг на друга.
Следующим вариантом осуществления изобретения является композиция, предпочтительно фармацевтическая или диагностическая композиция антитела, предлагаемого в изобретении.
Следующим вариантом осуществления изобретения является фармацевтическая композиция, которая содержит антитело, предлагаемое в изобретении, и по меньшей мере один фармацевтически приемлемый эксципиент.
Следующим вариантом осуществления изобретения является способ лечения пациента, который нуждается в терапии, отличающийся тем, что вводят пациенту в терапевтически эффективном количестве антитело, предлагаемое в изобретении.
Подробное описание изобретения
Изобретение относится к двухвалентному биспецифическому антителу, содержащему:
а) легкую цепь и тяжелую цепь антитела, специфически связывающегося с первым антигеном; и
б) легкую цепь и тяжелую цепь антитела, специфически связывающегося со вторым антигеном, в котором вариабельные домены VL и VH заменены друг на друга
и
в котором константные домены CL и СН1 заменены друг на друга.
Таким образом, двухвалентное биспецифическое антитело содержит:
а) первую легкую цепь и первую тяжелую цепь антитела, специфически связывающегося с первым антигеном; и
б) вторую легкую цепь и вторую тяжелую цепь антитела, специфически связывающегося со вторым антигеном,
в котором вариабельные домены VL и VH второй легкой цепи и второй тяжелой цепи заменены друг на друга
и
в котором константные домены CL и СН1 второй легкой цепи и второй тяжелой цепи заменены друг на друга.
Таким образом, для создания антитела, специфически связывающегося со вторым антигеном, применяют следующие процессы:
в легкой цепи
вариабельный домен VL легкой цепи заменяют на вариабельный домен VH тяжелой цепи указанного антитела и константный домен CL легкой цепи заменяют на константный домен СН1 тяжелой цепи указанного антитела;
и в тяжелой цепи
вариабельный домен VH тяжелой цепи заменяют на вариабельный домен VL легкой цепи указанного антитела и константный домен СН1 тяжелой цепи заменяют на константный домен CL легкой цепи указанного антитела.
Понятие «антитело» к контексте настоящего описания относится к полным моноклональным антителам. Такие полные антитела состоят из двух пар, каждая из которых включает «легкую цепь» (LC) и «тяжелую цепь» (НС) (указанные пары легкая цепь (LC)/тяжелая цепь сокращенно обозначают в контексте настоящего описания как LC/HC). Легкие цепи и тяжелые цепи указанных антител представляют собой полипептиды, состоящие из нескольких доменов (областей). В полном антителе каждая тяжелая цепь содержит вариабельную область тяжелой цепи (сокращенно обозначена в контексте настоящего описания как HCVR или VH) и константную область тяжелой цепи. Константная область тяжелой цепи содержит константные СН1-, СН2- и СН3-домены тяжелой цепи (в антителе, которое относится к классам IgA, IgD и IgG) и необязательно константный СН4-домен тяжелой цепи (в антителе, которое относится к классам IgE и IgM). Каждая легкая цепь содержит вариабельный домен легкой цепи VL и константный домен легкой цепи CL. Структура одного из классов встречающихся в естественных условиях антител, а именно антитела класса IgG, показана, например, на фиг.1. Вариабельные домены VH и VL можно дополнительно подразделять на области гипервариабельности, обозначенные как гипервариабельные участки (CDR), перемежающиеся более консервативными областями, которые называют каркасными участками (FR). Каждая VH- и VL-область состоит из трех CDR и четырех FR, которые расположены в направлении от аминоконца к карбоксиконцу в следующем порядке: FR1, CDR1, FR2, CDR2, FR3, CDR3, FR4 (Janeway С.A., Jr. и др., Immunobiology., 5-е изд., изд-во Garland Publishing, 2001; и Woof J., Burton D., Nat Rev Immunol 4, 2004, cc.89-99). Две пары, каждая из которых включает тяжелую цепь и легкую цепь (HC/LC), обладают способностью специфически связываться с одним и тем же антигеном. Таким образом, полное антитело представляет собой двухвалентное моноспецифическое антитело. Указанные «антитела» представляют собой, например, мышиные антитела, человеческие антитела, химерные антитела, гуманизированные антитела и созданные с помощью генной инженерии антитела (варианты антител или мутантные антитела), если они сохраняют свои характерные свойства. Наиболее предпочтительными являются человеческие или гуманизированные антитела, прежде всего в виде рекомбинантных человеческих или гуманизированных антител.
Известно пять типов тяжелых цепей антител млекопитающих, которые обозначают греческими буквами: α, δ, ε, γ и µ (Janeway С.А., Jr. и др., Immunobiology., 5-е изд., изд-во Garland Publishing, 2001). Присутствующий тип тяжелой цепи определяет класс антитела; указанные цепи обнаружены в антителах типа IgA, IgD, IgE, IgG и IgM соответственно (Rhoades R.A., Pflanzer R.G., Human Physiology, 4-е изд., изд-во Thomson Learning, 2002). Различные тяжелые цепи отличаются по размеру и составу; α и γ содержат примерно 450 аминокислот, а µ и ε состоят примерно из 550 аминокислот.
Каждая тяжелая цепь содержит две области, т.е. константную область и вариабельную область. Константная область является идентичной во всех антителах одного и того же изотипа, но отличается в антителах различного изотипа. Тяжелые цепи γ, α и δ содержат константную область, которая состоит из трех константных доменов СН1, СН2 и СН3 (выстроены в ряд), и шарнирную область, которая придает гибкость (Woof J., Burton D., Nat Rev Immunol 4, 2004, cc.89-99); тяжелые цепи µ и ε содержат константную область, которая состоит из четырех константных доменов СН1, СН2, СН3 и СН4 (Janeway С.A., Jr. и др., Immunobiology., 5-е изд., изд-во Garland Publishing, 2001). Вариабельная область тяжелой цепи отличается у антител, которые продуцируются различными В-клетками, но является одинаковой у всех антител, продуцируемых индивидуальной В-клеткой или B-клеточным клоном. Вариабельная область каждой тяжелой цепи антитела содержит примерно 110 аминокислот и состоит из одного домена.
У млекопитающих известно только два типа легких цепей, которые обозначают как лямбда (λ) и каппа (κ). Легкая цепь состоит из двух последовательно расположенных доменов: один константный домен CL и один вариабельный домен VL. Примерная длина легкой цепи составляет 211-217 аминокислот. Предпочтительно легкая цепь представляет собой легкую каппа (κ)-цепь, а константный домен CL предпочтительно представляет собой C-каппа (κ).
Понятия «моноклональное антитело» или «композиция моноклонального антитела» в контексте настоящего описания относятся к препарату молекул антител одинакового аминокислотного состава.
«Антитела» согласно изобретению могут представлять собой антитела любого класса (например, IgA, IgD, IgE, IgG и IgM, предпочтительно IgG или IgE) или подкласса (например, IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2, предпочтительно IgG1), при этом оба антитела, из которых выводят двухвалентное биспецифическое антитело, предлагаемое в изобретение, имеют Fc-область одного и того же подкласса (например, IgG1, IgG4 и т.п., предпочтительно IgG1), предпочтительно одного и того же аллотипа (например, кавказского).
Понятие «Fc-область (фрагмент) антитела» хорошо известно специалистам в данной области и ее определяют на основе расщепления антител папаином. Антитела, предлагаемые в изобретении, содержат в качестве Fc-области предпочтительно Fc-область, полученную из человеческого антитела, и предпочтительно все другие части человеческих константных областей. Fc-область антитела непосредственно участвует в активации комплемента, C1q-связывании, С3-активации и связывании Fc-рецептора. В то время как влияние антитела на систему комплемента зависит от определенных условий, связывание с C1q обусловлено определенными сайтами связывания в Fc-области. Указанные сайты связывания известны в данной области и описаны, например, у Lukas T.J. и др., J. Immunol. 127, 1981, cc.2555-2560; Brunhouse R. и Cebra J.J., Mol. Immunol. 16, 1979, cc.907-917; Burton D.R. и др., Nature 288, 1980, cc.338-344; Thommesen J.E. и др., Mol. Immunol. 37, 2000, cc.995-1004; Idusogie E.E. и др., J. Immunol. 164, 2000, cc.4178-4184; Hezareh М. и др., J. Virol. 75, 2001, cc.12161-12168; Morgan А. и др., Immunology 86, 1995, cc.319-324; и ЕР 0307434. Указанные сайты связывания представляют собой, например, L234, L235, D270, N297, Е318, K320, K322, Р331 и Р329 (нумерация дана согласно нумерации EU Кэбота, см. ниже). Антитела подклассов IgG1, IgG2 и IgG3, как правило, характеризуются способностью к активации комплемента, C1q-связыванию и С3-активации, в то время как IgG4 не активируют систему комплемента, не связываются с C1q и не активируют С3. Предпочтительно Fc-область представляет собой человеческую Fc-область.
Понятие «химерное антитело» относится к антителу, содержащему вариабельную область, т.е. связывающую область, полученную из одного источника или из одних и тех же видов, и по меньшей мере часть константной области, полученную из другого источника или других видов, и его, как правило, получают с использованием методов рекомбинантой ДНК. Предпочтительными являются химерные антитела, которые содержат мышиную вариабельную область и человеческую константную область. Другими предпочтительными формами «химерных антител», подпадающих под объем настоящего изобретения, являются антитела, константная область которых модифицирована или изменена по сравнению с исходным антителом с целью получения свойств, предлагаемых в изобретении, прежде всего касательно связывания C1q и/или связывания Fc-рецептора (FcR). Такие химерные антитела обозначают также как «антитела переключенного класса». Химерные антитела являются продуктом экспрессии генов иммуноглобулинов, содержащих сегменты ДНК, которые кодируют вариабельные области иммуноглобулинов, и сегменты ДНК, которые кодируют константные области иммуноглобулинов. Методы получения химерных антител включают обычные методы рекомбинантной ДНК и генной трансфекции, которые хорошо известны в данной области (см., например, Morrison S.L. и др., Proc. Natl. Acad. Sci. USA 81, 1984, cc.6851-6855; US 5202238 и US 5204244).
Понятие «гуманизированное антитело» относится к антителам, в которых каркасные или «гипервариабельные участки» (CDR) модифицированы так, что они содержат CDR иммуноглобулина другой специфичности по сравнению со специфичностью родительского иммуноглобулина. В предпочтительном варианте осуществления изобретения для получения «гуманизированного антитела» мышиный CDR трансплантируют в каркасный участок человеческого антитела (см., например, Riechmann L. и др., Nature 332, 1988, cc.323-327; и Neuberger M.S. и др., Nature 314, 1985, cc.268-270). Особенно предпочтительные CDR соответствуют CDR, которые представляют собой последовательности, распознающие антигены, указанные выше для химерных антител. Другими формами «гуманизированных антител», подпадающих под объем настоящего изобретения, являются антитела, константная область которых дополнительно модифицирована или изменена по сравнению с исходным антителом с целью получения свойств, предлагаемых в изобретении, прежде всего касательно связывания C1q и/или связывания Fc-рецептора (FcR).
Понятие «человеческое антитело» в контексте настоящего описания относится к антителам, вариабельные и константные области которых выведены из последовательностей иммуноглобулина человеческой зародышевой линии. Человеческие антитела хорошо известны в данной области (van Dijk M.A. и van de Winkel J.G., Curr. Opin. Chem. Biol. 5, 2001, cc.368-374). Человеческие антитела можно получать также в трансгенных животных (например, мышах), которые в результате иммунизации могут продуцировать полный спектр или определенную часть человеческих антител при отсутствии производства эндогенного иммуноглобулина. Перенос набора генов иммуноглобулинов человеческой зародышевой линии в такую мутантную зародышевую линию мышей должен приводить к производству человеческих антител после антигенной стимуляции (см., например, Jakobovits А., и др., Proc. Natl. Acad. Sci. USA 90, 1993, cc.2551-2555; Jakobovits А. и др., Nature 362, 1993, cc.255-258; Bruggemann M. и др., Year Immunol. 7, 1993, cc.33-40). Человеческие антитела можно получать также с помощью фаговых дисплейных библиотек (Hoogenboom H.R. и Winter, G., J. Mol. Biol. 227, 1992, cc.381-388; Marks J.D. и др., J. Mol. Biol. 222, 1991, cc.581-597). Для получения человеческих моноклональных антител можно использовать также методы Cole с соавторами и Boerner с соавторами (Cole и др., Monoclonal Antibodies and Cancer Therapy, под ред. Alan R. Liss, 1985, с.77; и Boerner Р., и др., J. Immunol. 147, 1991, cc.86-95). Как уже было отмечено для химерных и гуманизированных антител, предлагаемых в изобретении, понятие «человеческое антитело» включает также такие антитела, константная область которых модифицирована с целью получения свойств, предлагаемых в изобретении, прежде всего касательно связывания C1q и/или связывания FcR, например, путем «переключения класса», т.е. замены или мутации Fc-областей (например, IgG1 на IgG4 и/или IgG1/IgG4-мутация).
Понятие «рекомбинантное человеческое антитело» в контексте настоящего описания относится ко всем человеческим антителам, которые получают, экспрессируют, создают или выделяют с помощью методов рекомбинации, например к антителам, выделенным из клетки-хозяина, такой как NS0- или СНО-клетка, или из животного (например, мыши), которое является трансгенным из-за присутствия человеческих генов иммуноглобулинов или антител, экспрессируемых с использованием рекомбинантного экспрессионного вектора, которым трансфектирована клетка-хозяин. Такие рекомбинантные человеческие антитела имеют вариабельную и константную области, которые находятся в преобразованной форме. Рекомбинантные человеческие антитела, предлагаемые в изобретении, подвергают соматической гипермутации in vivo. Таким образом, аминокислотные последовательности VH- и VL-областей рекомбинантных антител представляют собой последовательности, которые, хотя и выведены из последовательностей VH и VL человеческой зародышевой линии и родственных им линий, могут не существовать в естественных условиях в спектре зародышевой линии человеческих антител in vivo.
Понятие «вариабельная область (домен)» (вариабельный домен легкой цепи (VL), вариабельная область тяжелой цепи (VH)) в контексте настоящего описания относится к областям каждой из пары легких и тяжелой цепей, которые участвуют непосредственно в связывании антитела с антигеном. Домены вариабельных человеческих легких и тяжелых цепей имеют одинаковую общую структуру, и каждый домен содержит четыре каркасных участка (FR), последовательности которых являются весьма консервативными, связанных тремя «гипервариабельными участками» (или определяющими комплементарность участками, CDR). Каркасные участки адаптированы к β-складчатой конформации, а CDR могут образовывать петли, соединяющие β-складчатую структуру. CDR в каждой цепи сохраняют их трехмерную структуру с помощью каркасных участков и образуют вместе с CDR из других цепей антигенсвязывающий центр. CDR3-участки тяжелой и легкой цепей антитела играют особенно важную роль в специфичности связывания/аффинности антител, предлагаемых в изобретении, и поэтому являются дополнительным объектом изобретения.
Понятия «гипервариабельный участок» или «антигенсвязывающий центр антитела» в контексте настоящего описания относятся к аминокислотным остаткам антитела, которые ответственны за связывания антигена. Гипервариабельный участок содержит аминокислотные остатки из «определяющих комплементарность участков» или «CDR». «Каркасные» или «FR»-участки представляют собой участки вариабельной области, отличные от указанных в настоящем описании остатков гипервариабельного участка. Таким образом, легкие и тяжелые цепи антитела содержат в направлении от N- к С-концу участки FR1, CDR1, FR2, CDR2, FR3, CDR3 и FR4. CDR каждой цепи разделены аминокислотами указанного каркасного участка. В частности, CDR3 тяжелой цепи представляют собой участок, который вносит наибольший вклад в связывание с антигеном. CDR- и FR-участки определяют с помощью стандартной номенклатуры Кэбота (Kabat и др., Sequences of Proteins of Immunological Interest, 5-е изд., изд-во Public Health Service, National Institutes of Health, Bethesda, MD (1991).
«Константные области (домены)» тяжелой цепи и легкой цепи не принимают непосредственного участия в связывании антитела с антигеном, но обладают различными эффекторными функциями. В зависимости от аминокислотной последовательности константной области их тяжелых цепей антитела или иммуноглобулины подразделяют на указанные выше классы.
Понятие «двухвалентное биспецифическое антитело» в контексте настоящего описания относится к антителу, как оно описано выше, в котором каждая из двух пар, включающая тяжелую цепь и легкую цепь (HC/LC), специфически связывается с различным антигеном, т.е. первая тяжелая и первая легкая цепи (полученные из антитела к первому антигену) специфически связываются обе с первым антигеном, а вторая тяжелая и вторая легкая цепи (полученные из антитела ко второму антигену) специфически связываются обе со вторым антигеном (как показано на фиг.2); указанные двухвалентные биспецифические антитела обладают способностью специфически связываться одновременно с двумя различными антигенами и не более чем с двумя антигенами, в отличие, во-первых, от моноспецифического антитела, которое обладает способностью связываться только с одним антигеном, и, во-вторых, от четырехвалентного тетраспецифического антитела, которое обладает способностью связываться одновременно с четырьмя молекулами антигенов.
Согласно изобретению соотношение между требуемым двухвалентным биспецифическим антителом и нежелательными побочными продуктами можно улучшать путем замены некоторых доменов только в одной паре, включающей тяжелую цепь и легкую цепь (HC/LC). Хотя первая из двух HC/LC-пар, полученная из антитела, которое специфически связывается с первым антигеном, остается практически не измененной, вторую из двух HC/LC-пар, полученную из антитела, которое специфически связывается со вторым антигеном, изменяют с помощью следующей замены:
легкая цепь: замена вариабельного домена VL легкой цепи на вариабельный домен VH тяжелой цепи указанного антитела, которое специфически связывается со вторым антигеном, и константного домена CL легкой цепи на константный домен СН1 тяжелой цепи указанного антитела, которое специфически связывается со вторым антигеном,
тяжелая цепь: замена вариабельного домена VH тяжелой цепи на вариабельный домен VL легкой цепи указанного антитела, которое специфически связывается со вторым антигеном, и константного домена СН1 тяжелой цепи на константный домен CL легкой цепи указанного антитела, которое специфически связывается со вторым антигеном.
Таким образом, образовавшиеся двухвалентные биспецифические антитела представляют собой искусственные антитела, которые содержат
а) легкую цепь и тяжелую цепь антитела, специфически связывающегося с первым антигеном; и
б) легкую цепь и тяжелую цепь антитела, специфически связывающегося со вторым антигеном,
где указанная легкая цепь (антитела, специфически связывающегося со вторым антигеном) содержит вариабельный домен VH вместо VL и константный домен СН1 вместо CL,
где указанная тяжелая цепь (антитела, специфически связывающегося со вторым антигеном) содержит вариабельный домен VL вместо VH и константный домен CL вместо СН1.
Согласно еще одному объекту изобретения указанное улучшенное соотношение между требуемым двухвалентным биспецифическим антителом и нежелательными побочными продуктами можно дополнительно улучшать с помощью одного из указанных ниже двух альтернативных подходов.
А) Первый альтернативный подход (см. фиг.3)
СН3-домены указанного двухвалентного биспецифического антитела, предлагаемого в изобретении, можно изменять с помощью технологии «knob-into-holes», которая описана подробно на нескольких примерах, например в WO 96/027011, Ridgway J.B. и др., Protein Eng 9, 1996, cc.617-621; и у Merchant A.M. и др., Nat Biotechnol 16, 1998, cc.677-681. При использовании этого метода взаимодействующие поверхности двух СН3-доменов изменяют с целью повышения гетеродимеризации обеих тяжелых цепей, содержащих эти два СН3-домена. Каждый из двух СН3-доменов (двух тяжелых цепей) может представлять собой «выступ», а другой представлять собой «впадину». Введение дисульфидного мостика стабилизирует гетеродимеры (Merchant A.M, и др., Nature Biotech 16, 1998, cc.677-681; Atwell S., Ridgway J.B., Wells J.A., Carter P., J Mol Biol 270, 1997, cc.26-35) и повышает выход продукта.
Таким образом, согласно предпочтительному варианту осуществления изобретения СН3-домены двухвалентного биспецифического антитела, в котором первый СН3-домен и второй СН3-домен каждый соприкасается друг с другом на поверхности раздела, которая представляет собой исходную поверхность раздела между СН3-доменами антитела, изменяют с помощью технологии «knob-into-holes», включая дополнительную стабилизацию путем интродукции дисульфидного мостика в СН3-домены (как описано в WO 96/027011, Ridgway J.B. и др., Protein Eng 9, 1996, cc.617-621; Merchant A.M и др., Nature Biotech 16, 1998, cc.677-681; и Atwell S., Ridgway J.B., Wells J.A., Carter P., J Mol Biol 270, 1997, cc.26-35) для активации формирования двухвалентного биспецифического антитела.
Таким образом, согласно одному из объектов изобретения двухвалентное биспецифическое антитело отличается тем, что СН3-домен одной тяжелой цепи и СН3-домен другой тяжелой цепи каждый соприкасаются друг с другом на поверхности раздела, которая представляет собой исходную поверхность раздела между СН3-доменами антитела; при этом поверхность раздела изменяют для активации формирования двухвалентного биспецифического антитела, где изменение отличается тем, что:
а) изменяют СН3-домен одной тяжелой цепи так, что на исходной поверхности раздела СН3-домена одной тяжелой цепи, которая соприкасается с исходной поверхностью раздела СН3-домена второй тяжелой цепи в двухвалентном биспецифическом антителе, аминокислотный остаток заменяют на аминокислотный остаток, который имеет большую по объему боковую цепь, создавая тем самым выпуклость на поверхности раздела СН3-домена одной тяжелой цепи, которая может помещаться в полость на поверхности раздела СН3-домена другой тяжелой цепи, и
б) изменяют СН3-домен другой тяжелой цепи так, что на исходной поверхности раздела второго СН3-домена, которая соприкасается с исходной поверхностью раздела первого СН3-домена в двухвалентном биспецифическом антителе, аминокислотный остаток заменяют на аминокислотный остаток, который имеет меньшую по объему боковую цепь, создавая тем самым полость на поверхности раздела второго СН3-домена, в которую может помещаться выпуклость на поверхности раздела первого СН3-домена.
Предпочтительно указанный аминокислотный остаток, который имеет большую по объему боковую цепь, выбирают из группы, включающей аргинин (R), фенилаланин (F), тирозин (Y), триптофан (W).
Предпочтительно указанный аминокислотный остаток, который имеет меньшую по объему боковую цепь, выбирают из группы, включающей аланин (А), серии (S), треонин (Т), валин (V).
Согласно одному из объектов изобретения оба СН3-домена дополнительно изменяют путем интродукции цистеина (С) в качестве аминокислоты в соответствующих положениях каждого СН3-домена так, чтобы мог образоваться дисульфидный мостик между обоими СН3-доменами.
В другом предпочтительном варианте осуществления изобретения оба СН3-домена изменяют, используя остатки R409D; K370E (K409D) в качестве образующих «выступ» остатков и D399K; E357K в качестве образующих «впадину» остатков, как описано, например, в ЕР 1870459А1.
Или
Б) Второй альтернативный подход (см. фиг.4)
Этот подход предусматривает замену СН3-домена константной области одной тяжелой цепи на СН1-домен константной области тяжелой цепи; и замену СН3-домена константной области другой тяжелой цепи на CL-домен константной области легкой цепи.
CH1-домен константной области тяжелой цепи, на который заменяют СН3-домен тяжелой цепи, может представлять собой домен любого Ig-класса (например, IgA, IgD, IgE, IgG и IgM) или подкласса (например, IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2).
CL-домен константной области легкой цепи, на который заменяют СН3-домен тяжелой цепи, может быть лямбда- (λ) или каппа- (κ) типа, предпочтительно каппа- (κ) типа.
Таким образом, одним из предпочтительных вариантов осуществления изобретения является двухвалентное биспецифическое антитело, которое содержит:
а) легкую цепь и тяжелую цепь антитела, специфически связывающегося с первым антигеном; и
б) легкую цепь и тяжелую цепь антитела, специфически связывающегося со вторым антигеном, в котором вариабельные домены VL и VH заменены друг на друга
и
в котором константные домены CL и СН1 заменены друг на друга, и необязательно
в) СН3-домен одной тяжелой цепи и СН3-домен другой тяжелой цепи, каждый из которых соприкасается друг с другом на поверхности раздела, которая представляет собой исходную поверхность раздела между СН3-доменами антитела; при этом поверхность раздела изменяют для активации формирования двухвалентного биспецифического антитела, где изменение отличается тем, что:
ва) изменяют СН3-домен одной тяжелой цепи так, что на исходной поверхности раздела СН3-домена одной тяжелой цепи, которая соприкасается с исходной поверхностью раздела СН3-домена второй тяжелой цепи в двухвалентном биспецифическом антителе, аминокислотный остаток заменяют на аминокислотный остаток, который имеет большую по объему боковую цепь, создавая тем самым выпуклость на поверхности раздела СН3-домена одной тяжелой цепи, которая может помещаться в полость на поверхности раздела СН3-домена другой тяжелой цепи,
и
вб) изменяют СН3-домен другой тяжелой цепи так, что на исходной поверхности раздела второго СН3-домена, которая соприкасается с исходной поверхностью раздела первого СН3-домена в двухвалентном биспецифическом антителе, аминокислотный остаток заменяют на аминокислотный остаток, который имеет меньшую по объему боковую цепь, создавая тем самым полость на поверхности раздела второго СН3-домена, в которую может помещаться выпуклость на поверхности раздела первого СН3-домена;
или
г) СН3-домен константной области одной тяжелой цепи заменяют на СН1-домен константной области тяжелой цепи; и СН3-домен константной области другой тяжелой цепи заменяют на CL-домен константной области легкой цепи.
Понятия «антиген» или «молекула антигена» в контексте настоящего описания применяют взаимозаменяемо, и они относятся ко всем молекулам, которые могут специфически связываться антителом. Двухвалентное биспецифическое антитело специфически связывается с первым антигеном и вторым отличным от первого антигеном. Понятие «антигены» в контексте настоящего описания включают, например, белки, различные эпитопы белков (в качестве различных антигенов согласно изобретению) и полисахариды. Они главным образом включают части (покрытия, капсулы, клеточные оболочки, жгутики, фимбрии и токсины) бактерий, вирусов и других микроорганизмов. Липиды и нуклеиновые кислоты являются антигенами только при их объединении с белками и полисахаридами. Не относящиеся к микробам экзогенные (чужеродные) антигены могут включать пыльцу, белок яиц и белки из трансплантированных тканей или органов или антигены, находящиеся на поверхности трансфузируемых кровяных клеток. Предпочтительно антиген выбирают из группы, включающей цитокины, белки клеточной поверхности, ферменты и рецепторы цитокинов, белков клеточной поверхности, ферментов и другие рецепторы.
Опухолевые антигены представляют собой антигены, которые презентуются молекулами ГКГ I или ГКГ II на поверхности опухолевых клеток. Иногда эти антигены презентуются опухолевыми клетками и никогда здоровыми клетками. В этом случае их называют специфическими для опухоли антигенами (TSA), и они, как правило, являются результатом специфической для опухоли мутации. Более распространенными являются антигены, которые презентуются опухолевыми клетками и здоровыми клетками, и их называют ассоциированными с опухолью антигенами (ТАА). Цитотоксические Т-лимфоциты, которые распознают эти антигены, могут обладать способностью разрушать опухолевые клетки до их пролиферации или метастазирования. Опухолевые антигены могут находиться также на поверхности опухоли в форме измененного в результате мутации рецептора, в этом случае они должны распознаваться В-клетками.
В одном из предпочтительных вариантов осуществления изобретения по меньшей мере один из двух различных антигенов (первый и второй антиген), с которым двухвалентное биспецифическое антитело специфически связывается, представляет собой опухолевый антиген.
В другом предпочтительном варианте осуществления изобретения оба различных антигена (первый и второй антиген), с которыми двухвалентное биспецифическое антитело специфически связывается, представляют собой опухолевые антигены; в этом случае первый и второй антиген могут представлять собой также два различных эпитопа одного и того же специфического для опухоли белка.
В другом предпочтительном варианте осуществления изобретения по меньшей мере один из двух различных антигенов (первый и второй антиген), с которым двухвалентное биспецифическое антитело специфически связывается, представляет собой опухолевый антиген, а другой представляет собой антиген эффекторной клетки, такой, например, как Т-клеточный рецептор, CD3, CD16 и т.п.
В другом предпочтительном варианте осуществления изобретения по меньшей мере один из двух различных антигенов (первый и второй антиген), с которым двухвалентное биспецифическое антитело специфически связывается, представляет собой опухолевый антиген, а другой представляет собой противораковую субстанцию, такую как токсин или ингибитор киназы.
В контексте настоящего описания понятие «специфически связывается» или «связывается специфически с» относится к антителу, специфически связывающемуся с антигеном. Предпочтительно аффинность к связыванию антитела, специфически связывающегося с указанным антигеном, характеризуется значением KD 10-9 молей/л или ниже (например, 10-10 молей/л), предпочтительно значением KD 10-10 молей/л или ниже (например, 10-12 молей/л). Аффинность к связыванию определяют с помощью стандартного анализа связывания, такого как поверхностный плазменный резонанс (Biacore®).
Понятие «эпитоп» включает любую полипептидную детерминанту, обладающую способностью специфически связываться с антителом. В некоторых вариантах осуществления изобретения эпитопная детерминанта включает химически активные поверхностные группы молекул, такие как аминокислоты, боковые цепи сахаров, фосфорил или сульфонил, и в некоторых вариантах осуществления изобретения могут иметь специфические трехмерные структурные характеристики и/или специфические характеристики заряда. Эпитоп представляет собой область антигена, которая связывается антителом. В некоторых вариантах осуществления изобретения считается, что антитело специфически связывается с антигеном, когда оно преимущественно распознает его антиген-мишень в сложной смеси белков и/или макромолекул.
Еще одним вариантом осуществления изобретения является способ получения двухвалентного биспецифического антитела, предлагаемого в изобретении, заключающийся в том, что
а) трансформируют клетку-хозяина
- векторами, которые содержат молекулы нуклеиновых кислот, кодирующие легкую цепь и тяжелую цепь антитела, специфически связывающегося с первым антигеном,
- векторами, которые содержат молекулы нуклеиновых кислот, кодирующие легкую цепь и тяжелую цепь антитела, специфически связывающегося со вторым антигеном, в котором вариабельные домены VL и VH заменены друг на друга
и
в котором константные домены CL и СН1 заменены друг на друга;
б) культивируют клетку-хозяина в условиях, которые позволяют синтезировать указанную молекулу антитела; и
в) выделяют молекулу антитела из культуры.
В целом, применяют два вектора, кодирующих легкую цепь и тяжелую цепь антитела, которое специфически связывается с первым антигеном, и еще два вектора, кодирующих легкую цепь и тяжелую цепь антитела, которое специфически связывается со вторым антигеном. Один из двух векторов кодирует соответствующую легкую цепь, а другой из двух векторов кодирует соответствующую тяжелую цепь. Однако в альтернативном варианте способа получения двухвалентного биспецифического антитела, предлагаемого в изобретении, можно применять для трансформации клетки-хозяина только один первый вектор, кодирующий легкую цепь и тяжелую цепь антитела, специфически связывающегося с первым антигеном, и только один второй вектор, кодирующий легкую цепь и тяжелую цепь антитела, специфически связывающегося со вторым антигеном.
Изобретение относится также к способу получения антител, заключающемуся в том, что культивируют соответствующие клетки-хозяева в условиях, которые позволяют синтезировать молекулы антител, и выделяют антитела из культуры, например, предусматривающему экспрессию
- первой нуклеотидной последовательности, которая кодирует легкую цепь антитела, специфически связывающегося с первым антигеном,
- второй нуклеотидной последовательности, которая кодирует тяжелую цепь антитела, специфически связывающегося с первым антигеном,
- третьей нуклеотидной последовательности, которая кодирует легкую цепь антитела, специфически связывающегося со вторым антигеном, в котором вариабельный домен VL легкой цепи заменен на вариабельный домен VH тяжелой цепи, и в которой константный домен CL легкой цепи заменен на константный домен СН1 тяжелой цепи, и
- четвертой нуклеотидной последовательности, которая кодирует тяжелую цепь антитела, специфически связывающегося со вторым антигеном, в котором вариабельный домен VH тяжелой цепи заменен на вариабельный домен VL легкой цепи и константный домен СН1 тяжелой цепи заменен на константный домен CL легкой цепи.
Еще одним вариантом осуществления изобретения является клетка-хозяин, содержащая
- векторы, которые содержат молекулы нуклеиновых кислот, кодирующие легкую цепь и тяжелую цепь антитела, специфически связывающегося с первым антигеном,
- векторы, которые содержат молекулы нуклеиновых кислот, кодирующие легкую цепь и тяжелую цепь антитела, специфически связывающегося со вторым антигеном, в котором вариабельные домены VL и VH заменены друг на друга
и
в котором константные домены CL и СН1 заменены друг на друга.
Еще одним вариантом осуществления изобретения является клетка-хозяин, которая содержит
а) вектор, содержащий молекулу нуклеиновой кислоты, которая кодирует легкую цепь, и вектор, содержащий молекулу нуклеиновой кислоты, которая кодирует тяжелую цепь антитела, специфически связывающегося с первым антигеном,
б) вектор, содержащий молекулу нуклеиновой кислоты, которая кодирует легкую цепь, и вектор, содержащий молекулу нуклеиновой кислоты, которая кодирует тяжелую цепь, антитела специфически связывающегося со вторым антигеном, в котором вариабельные домены VL и VH заменены друг на друга
и
в котором константные домены CL и СН1 заменены друг на друга.
Еще одним вариантом осуществления изобретения является композиция, предпочтительно фармацевтическая или диагностическая композиция двухвалентного биспецифического антитела, предлагаемого в изобретении.
Еще одним вариантом осуществления изобретения является фармацевтическая композиция, содержащая двухвалентное биспецифическое антитело, предлагаемое в изобретении, и по меньшей мере один фармацевтически приемлемый эксципиент.
Еще одним вариантом осуществления изобретения является способ лечения пациента, который нуждается в терапии, отличающийся тем, что вводят пациенту в терапевтически эффективном количестве двухвалентное биспецифическое антитело, предлагаемое в изобретении.
Понятие «нуклеиновая кислота или молекула нуклеиновой кислоты» в контексте настоящего описания относится к молекулам ДНК и молекулам РНК. Молекула нуклеиновой кислоты может быть одноцепочечной или двухцепочечной, но предпочтительно представляет собой двухцепочечную ДНК.
В контексте настоящего описания понятия «клетка», «клеточная линия» и «клеточная культура» используются взаимозаменяемо, и все такие определения включают потомство. Так, понятия «трансформанты» и «трансформированные клетки» относятся к первичной рассматриваемой клетке и полученным из нее культурам безотносительно к количеству переносов. Следует понимать также, что все потомство может не быть полностью идентичным по составу ДНК из-за преднамеренных или случайных мутаций. Под объем изобретения подпадает вариант потомства, имеющего такую же функцию или биологическую активность, которая обнаружена у исходной трансформированной клетки. Если используются другие определения, то это будет очевидно из контекста.
Понятие «трансформация» в контексте настоящего описания относится к процессу переноса вектора/нуклеиновой кислоты в клетку-хозяина. Если в качестве клеток-хозяев применяют клетки без труднопреодолимых барьеров клеточных оболочек, то трансфекцию осуществляют, например, с помощью метода осаждения фосфатом кальция, который описан у Graham и Van der Eh, Virology 52, 1978, cc.546 и далее. Однако можно применять также другие методы интродукции ДНК в клетки, такие как инъекция ядер или слияние протопластов. Если применяют прокариотические клетки или клетки, которые содержат выраженные конструкции клеточных оболочек, можно применять, например, метод трансфекции, основанной на обработке кальцием, с использованием хлорида кальция, который описан у Cohen F.N. и др., PNAS. 69, 1972, cc.2110-2114.
Рекомбинантное получение антител с помощью трансформации хорошо известно в данной области и описано, например, в обзорных статьях Makrides S.C., Protein Expr. Purif. 17, 1999, cc.183-202; Geisse S. и др., Protein Expr. Purif. 8, 1996, cc.271-282; Kaufman R.J., Mol. Biotechnol. 16, 2000, cc.151-161; Werner R.G. и др., Arzneimittelforschung 48, 1998, cc.870-880, а также в US 6331415 и US 4816567.
В контексте настоящего описания понятие «экспрессия» относится к процессу, при котором нуклеиновая кислота транскрибируется в мРНК, и/или к процессу, при котором транскрибируемая мРНК (которую обозначают также как транскрипт) затем может транслироваться в пептиды, полипептиды или белки. И транскрипты, и кодируемые полипептиды обозначают в целом как генный продукт. Если полинуклеотид выводят из геномной ДНК, то экспрессия в эукариотической клетке может включать сплайсинг мРНК.
«Вектор» представляет собой молекулу нуклеиновой кислоты, в частности самореплицирующуюся, которая переносит встроенную молекулу нуклеиновой кислоты в клетки-хозяева и/или между клетками-хозяевами. Понятие включает векторы, функция которых прежде всего состоит во встраивании ДНК или РНК в клетку (например, хромосомная интеграция), в репликационные векторы, функция которых прежде всего состоит в репликации ДНК или РНК, и в экспрессионные векторы, функция которых прежде всего состоит в транскрипции и/или трансляции ДНК или РНК. Под понятие подпадают также векторы, которые обладают несколькими указанными функциями.
«Экспрессионный вектор» представляет собой полинуклеотид, который при интродукции в соответствующую клетку-хозяина может транскрибироваться и транслироваться в полипептид. Понятие «экспрессионная система», как правило, относится к приемлемой клетке-хозяину, содержащей экспрессионный вектор, функцией которой может быть выход требуемого продукта экспрессии.
Двухвалентные биспецифические антитела, предлагаемые в изобретении, предпочтительно получают методами рекомбинации. Указанные методы хорошо известны в данной области и предусматривают экспрессию белка в прокариотических и эукариотических клетках с последующим выделением полипептида антитела и, как правило, очисткой до фармацевтически приемлемой чистоты. Для экспрессии белка нуклеиновые кислоты, кодирующие легкие и тяжелые цепи или их фрагменты, встраивают в экспрессионные векторы с помощью стандартных методов. Экспрессию осуществляют в приемлемых прокариотических или эукариотических клетках-хозяевах типа СНО-клеток, NS0-клеток, SP2/0-клеток, HEK293-клеток, COS-клеток, PER.C6-клеток, дрожжей или клеток E.coli, и антитело выделяют из клеток (из супернатанта или клеток после лизиса). Двухвалентные биспецифические антитела могут присутствовать в целых клетках, в клеточном лизате или в частично очищенной или практически очищенной форме. Очистку осуществляют для удаления других клеточных компонентов или других загрязнителей, например, других клеточных нуклеиновых кислот или белков, стандартными методами, которые включают обработку щелочью/ДСН, хроматографию на колонках и другие методы, хорошо известные в данной области (см. в Current Protocols in Molecular Biology, под ред. Ausubel F., и др., изд-во Greene Publishing and Wiley Interscience, New York, 1987).
Экспрессия в NS0-клетках описана, например, у Barnes L.M. и др., Cytotechnology 32, 2000, cc.109-123; и Barnes L.M. и др., Biotech. Bioeng. 73, 2001, cc.261-270. Кратковременная экспрессия описана, например, у Durocher Y. и др., Nucl. Acids. Res. 30, 2002, с. Е9. Клонирование вариабельных областей описано у Orlandi R. и др., Proc. Natl. Acad. Sci. USA 86, 1989, cc.3833-3837; Carter P. и др., Proc. Natl. Acad. Sci. USA 89, 1992, cc.4285-4289; и Norderhaug L. и др., J. Immunol. Methods 204, 1997, cc.77-87. Предпочтительная система кратковременной экспрессии (HEK 293) описана у Schlaeger E.-J. и Christensen K., в Cytotechnology 30, 1999, cc.71-83 и у Schlaeger E.-J. в J. Immunol. Methods 194, 1996, cc.191-199.
Контролирующие последовательности, которые можно применять для прокариот, представляют собой, например, промотор, необязательно последовательность оператора и сайт связывания рибосом. Известно, что эукариотические клетки могут использовать промоторы, энхансеры и сигналы полиаденилирования.
Нуклеиновая кислота «функционально связана», когда она помещена под функциональный контроль другой нуклеотидной последовательности. Например, ДНК предпоследовательности или лидера секреции функционально связана с ДНК, кодирующей полипептид, если она экспрессируется в виде предбелка, который участвует в секреции полипептида; промотор или энхансер функционально связан с кодирующей последовательностью, если он оказывает воздействие на транскрипцию последовательности; или сайт связывания рибосом функционально связан с кодирующей последовательностью, если он помещен так, чтобы он облегчал трансляцию. Как правило, «функционально связаны» означает, что последовательности ДНК, будучи связаны, являются смежными, а в случае лидера секреции, смежными в рамке считывания. Однако не требуется, чтобы энхансеры были смежными. Связывание осуществляют путем лигирования в пригодных сайтах рестрикции. Если такие сайты не существуют, то согласно общепринятой практике используют синтетические олигонуклеотидные адаптеры или линкеры.
Двухвалентные биспецифические антитела можно отделять от культуральной среды с помощью общепринятых методов очисти иммуноглобулинов, таких, например, как хроматография на белок А-сефарозе, хроматография на гидроксилапатите, гель-электрофорез, диализ или аффинная хроматография. ДНК или РНК, которые кодируют моноклональные антитела, легко выделять и секвенировать с помощью общепринятых методов. Источником таких ДНК и РНК могут служить клетки гибридом. После выделения ДНК можно встраивать в экспрессионные векторы, которыми затем трансфектируют клетки-хозяева, такие как клетки HEK 293, СНО-клетки или клетки миеломы, которые иначе не могут продуцировать белок иммуноглобулина, для синтеза рекомбинантных моноклональных антител в клетках-хозяевах.
Варианты аминокислотной последовательности (или мутанты) двухвалентного биспецифического антитела получают путем интродукции соответствующих нуклеотидных замен в ДНК антитела или путем синтеза нуклеотидов. Однако такие модификации можно осуществлять только в очень ограниченном диапазоне, например, как описано выше. Например, модификации не должны изменять вышеуказанные характеристики антитела, такие как изотип IgG и связывание с антигеном, но могут повышать выход продукта рекомбинации, стабильность белка или облегчать очистку.
Следующие примеры, перечень последовательностей и чертежи даны с целью лучшего понимания настоящего изобретения, полный объем которого представлен в приведенной ниже формуле изобретения. Очевидно, что могут быть сделаны модификации в изложенных процедурах без отклонения от сути изобретения.
Перечень последовательностей
SEQ ID NO:1 аминокислотная последовательность тяжелой цепи антитела <IGF-1R> дикого типа.
SEQ ID NO:2 аминокислотная последовательность легкой цепи антитела <IGF-1R> дикого типа.
SEQ ID NO:3 аминокислотная последовательность тяжелой цепи * (НС*) антитела <IGF-1R>, несущего замену VL-VH/CL-CH1, в котором VH-домен тяжелой цепи заменен на VL-домен легкой цепи и СН1-домен тяжелой цепи заменен на CL-домен легкой цепи.
SEQ ID NO:4 аминокислотная последовательность легкой цепи * (LC*) антитела <IGF-1R>, несущего замену VL-VH/CL-CH1, в котором VL-домен легкой цепи заменен на VH-домен тяжелой цепи и CL-домен легкой цепи заменен на СН1-домен тяжелой цепи.
SEQ ID NO:5 аминокислотная последовательность эктодомена (ECD) IGF-1R, несущего метку, которая представляет собой His-стрептавидин-связывающий пептид (ECD IGF-1R-His-SBP).
SEO ID NO:6 аминокислотная последовательность тяжелой цепи антитела к ангиопоэтину-2 <ANGPT2> дикого типа.
SEO ID NO:7 аминокислотная последовательность легкой цепи антитела к ангиопоэтину-2 <ANGPT2> дикого типа.
SEQ ID NO:8 аминокислотная последовательность тяжелой цепи * (НС*) антитела <ANGPT2>, несущего замену VL-VH/CL-CH1, в котором VH-домен тяжелой цепи заменен на VL-домен легкой цепи и СН1-домен тяжелой цепи заменен на CL-домен легкой цепи.
SEQ ID NO:9 аминокислотная последовательность легкой цепи * (LC*) антитела <ANGPT2>, несущего замену VL-VH/CL-CH1, в котором VL-домен легкой цепи заменен на VH-домен тяжелой цепи и CL-домен легкой цепи заменен на СН1-домен тяжелой цепи.
SEQ ID NO:10 аминокислотная последовательность СН3-домена («выступы») с заменой T366W для применения в технологии «knobs-into-holes».
SEQ ID NO:11 аминокислотная последовательность СН3-домена («впадина») с заменой T366S, L368A, Y407V для применения в технологии «knobs-into-holes».
SEQ ID NO:12 аминокислотная последовательность тяжелой цепи антитела <VEGF> дикого типа.
SEQ ID NO:13 и 14 аминокислотная последовательность легкой цепи антитела <VEGF> дикого типа с лидерной последовательностью и без нее.
SEQ ID NO:15 аминокислотная последовательность тяжелой цепи * (НС*) антитела <ANGPT2>, несущего замену VL-VH/CL-CH1, в котором VH-домен тяжелой цепи заменен на VL-домен легкой цепи и СН1-домен тяжелой цепи заменен на CL-домен легкой цепи, и СН3-домен несет аминокислотную последовательность с заменой T366S, L368A, Y407V («впадина») для применения в технологии «knobs-into-holes».
SEQ ID NO:16 аминокислотная последовательность тяжелой цепи антитела <VEGF> дикого типа, в котором СН3-домен несет аминокислотную последовательность с заменой T366W («выступы») для применения в технологии «knobs-into-holes».
SEQ ID NO:17 аминокислотная последовательность тяжелой цепи(С)* (НС*) антитела <ANGPT2>, несущего замену VL-VH/CL-CH1, в котором VH- домен тяжелой цепи заменен на VL-домен легкой цепи и СН1-домен тяжелой цепи заменен на CL-домен легкой цепи, с встроенным дополнительно глицином.
SEO ID NO:18 аминокислотная последовательность легкой цепи(G)* (LC*) антитела <ANGPT2>, несущего замену VL-VH/CL-CH1, в котором VL-домен легкой цепи заменен на VH-домен тяжелой цепи и CL-домен легкой цепи заменен на СН1-домен тяжелой цепи, с встроенным дополнительно глицином.
Описание чертежей
На чертежах показано:
на фиг.1 - схематическое изображение встречающегося в естественных условиях полного антитела типа IgG, специфического в отношении одного антигена, с двумя парами тяжелых и легких цепей, каждая из которых содержит расположенные в общепринятом порядке вариабельные и константные домены;
на фиг.2 - схематическое изображение двухвалентного биспецифического антитела, содержащего: а) легкую цепь и тяжелую цепь антитела, которое специфически связывается с первым антигеном; и б) легкую цепь и тяжелую цепь антитела, которое специфически связывается со вторым антигеном, в котором вариабельные домены VL и VH заменены друг на друга и в котором константные домены CL и СН1 заменены друг на друга;
на фиг.3 - схематическое изображение двухвалентного биспецифического антитела, содержащего: а) легкую цепь и тяжелую цепь антитела, которое специфически связывается с первым антигеном; и б) легкую цепь и тяжелую цепь антитела, которое специфически связывается со вторым антигеном, в котором вариабельные домены VL и VH заменены друг на друга и в котором константные домены CL и СН1 заменены друг на друга, и в котором СН3-домены обеих тяжелых цепей изменены с помощью технологии «knobs-into-holes»;
на фиг.4 - схематическое изображение двухвалентного биспецифического антитела, содержащего: а) легкую цепь и тяжелую цепь антитела, которое специфически связывается с первым антигеном; и б) легкую цепь и тяжелую цепь антитела, которое специфически связывается со вторым антигеном, в котором вариабельные домены VL и VH заменены друг на друга и в котором константные домены CL и СН1 заменены друг на друга, и в котором один из СН3-доменов константной области обеих тяжелых цепей заменен на СН1-домен константной области тяжелой цепи; а другой СН3-домен константной области тяжелой цепи заменен на CL-домен константной области легкой цепи;
на фиг.5 - схематическое изображение белковой последовательности тяжелой цепи *<IGF-1R> НС* антитела <IGF-1R>, несущего замену VL-VH/CL-СН1;
на фиг.6 - схематическое изображение белковой последовательности легкой цепи *<IGF-1R> LC* антитела <IGF-1R>, несущего замену VL-VH/CL-СН1;
на фиг.7 - плазмидная карта экспрессионного вектора pUC-HC*-IGF-1R тяжелой цепи *<IGF-1R> НС*;
на фиг.8 - плазмидная карта экспрессионного вектора pUC-LC*-IGF-1R легкой цепи *<IGF-1R> LC*;
на фиг.9 - плазмидная карта экспрессионного вектора 4700-Hyg-OriP;
на фиг.10 - результаты, полученные с помощью ДСН-ПААГ, для очищенного моноспецифического двухвалентного антитела <IGF-1R>, несущего замену VL-VH/CL-CH1 (IgG1*), у которого НС* и LC* выделены с помощью иммунопреципитации с использованием белок А-агарозы из супернатантов клеточных культур после кратковременной трансфекции клеток линии HEK293-F;
на фиг.11 - данные о связывании моноспецифического антитела <IGF-1R>, несущего замену VL-VH/CL-CH1, и антитела дикого типа <IGF-1R> с ECD IGF-1R, полученные на основе оценки связывания с помощью ELISA;
на фиг.12 - плазмидная карта экспрессионного вектора pUC-HC*-ANGPT2> тяжелой цепи* <ANGPT2> НС*;
на фиг.13 - плазмидная карта экспрессионного вектора pUC-LC*-ANGPT2> легкой цепи* <ANGPT2> LC*;
на фиг.14 - данные, полученные с помощью ДСН-ПААГ в восстанавливающих и невосстанавливающих условиях для очищенной смеси, которая содержит А) моноспецифическое антитело <IGF-1R>, несущее замену VL-VH/CL-CH1, Б) биспецифическое антитело <ANGPT2-IGF-1R>, несущее замену VL-VH/CL-CH1, и В) антитела <ANGPT2> дикого типа («смесь, содержащая биспецифическое антитело, несущее замену VL-VH/CL-CH1»), из супернатантов клеточных культур с помощью аффинной хроматографии на белке А с последующей гель-фильтрацией и концентрированием;
на фиг.15 - принцип осуществления клеточного FACS-анализа, позволяющего выявлять образование мостиковой связи типа IGF-1R-ANGPT2, с использованием клеток линии I24, экспрессирующих IGF-1R, с целью выявления присутствия функционального биспецифического антитела <ANGPT2-IGF-1R>, несущего замену VL-VH/CL-CH1;
на фиг.16 - результаты, полученные для образцов А-Ж, с помощью клеточного FACS-анализа, позволяющего выявлять образование мостиковой связи типа IGF-1R-ANGPT2, с использованием клеток линии I24, экспрессирующих IGF-1R, с целью выявления присутствия функционального биспецифического антитела <ANGPT2-IGF-1R>, несущего замену VL-VH/CL-CH1, в супернатантах клеточных культур;
на фиг.17 - результаты, полученные для образцов А-Ж, с помощью клеточного FACS-анализа, позволяющего выявлять образование мостиковой связи типа IGF-1R-ANGPT2 с использованием клеток линии I24, экспрессирующих IGF-1R, с целью выявления присутствия функционального биспецифического антитела <ANGPT2-IGF-1R>, несущего замену VL-VH/CL-СН1;
на фиг.18 - схематическое изображение принципа анализа связывания ECD IGF-1R на основе ELISA;
на фиг.19 - схематическое изображение принципа анализа связывания ANGPT2 на основе ELISA;
на фиг.20 - схематическое изображение принципа анализа, позволяющего выявлять образование мостиковой связи типа VEGF-ANGPT2, на основе ELISA;
на фиг.21 - схематическое изображение принципа анализа, позволяющего выявлять образование мостиковой связи типа ANGPT2-VEGF, на основе Biacore;
на фиг.22 - А) полученные с помощью ДСН-ПААГ данные очистки антитела <IGF-1R>, несущего замену VL-VH/CL-CH1, где очищенное антитело <IGF-1R>, несущее замену VL-VH/CL-CH1, соответствует концентрированному, полученному с помощью гель-фильтрации (SEC) пулу; Б) данные, полученные с помощью гель-фильтрации очищенного антитела <IGF-1R>, несущего замену VL-VH/CL-CH1;
на фиг.23 - А) полученные с помощью ДСН-ПААГ данные очистки антитела <ANGPT2>, несущего замену VL-VH/CL-CH1, где очищенное антитело <ANGPT2>, несущее замену VL-VH/CL-CH1, соответствует концентрированному, полученному с помощью SEC пулу; Б) данные, полученные с помощью гель-фильтрации очищенного антитела<ANGPT2>, несущего замену VL-VH/CL-CH1;
на фиг.24 - данные о связывании с ANGPT2 моноспецифического антитела <ANGPT2>, несущего замену VL-VH/CL-CH1, и антитела <ANGPT2> дикого типа, полученные с помощью анализа связывания на основе ELISA;
на фиг.25 - данные о связывании с ANGPT2 моноспецифического антитела <ANGPT2>, несущего замену VL-VH/CL-CH1, и антитела <ANGPT2> дикого типа, полученные с помощью Biacore-анализа;
на фиг.26 - данные полученные с помощью ДСН-ПААГ в восстанавливающих и невосстанавливающих условиях фракций, элюированных после гель-фильтрации биспецифического антитела <VEGF-ANGPT2>, несущего замену VL-VH/CL-CH1;
на фиг.27 - расшифровка полос, полученных при осуществлении ДСН-ПААГ, с помощью масс-спектрометрии нативных фракций. Показано положение белков, идентифицированных с помощью масс-спектрометрии в образцах, соответствующих ДСН-ПААГ в невосстанавливающих условиях;
на фиг.28 - данные ELISA-анализа элюированных фракций 5 и 9, полученных при осуществлении гель-фильтрации, биспецифического антитела <VEGF-ANGPT2>, несущего замену VL-VH/CL-CH1, который позволяет выявлять образование мостиковой связи типа VEGF-ANGPT2. Биспецифическое и четырехвалентное антитело TvG6-Ang23, распознающее одновременно ANGPT2 и VEGF, включено в качестве положительного контроля;
на фиг.29 - данные, полученные с помощью поверхностного плазменного резонанса, фракций 5 и 9, полученных при осуществлении гель-фильтрации, биспецифического антитела <VEGF-ANGPT2>, несущего замену VL-VH/CL-CH1, на основе Biacore-анализа, позволяющего выявлять образование мостиковой связи типа VEGF-ANGPT2. Биспецифическое и четырехвалентное антитело TvG6-Ang23, распознающее одновременно ANGPT2 и VEGF, включено в качестве положительного контроля;
на фиг.30 - схематическое изображение биспецифического антитела <VEGF-ANGPT2>, несущего замену VL-VH/CL-CH1, для гетеродимеризации которого применяли технологию «knobs-in-holes»;
на фиг.31 - данные, полученные с помощью Biacore-анализа, о связывании с ANGPT2 моноспецифического антитела <ANGPT2>, несущего замену VL-VH(G)/CL-CH1(G), и антитела <ANGPT2> дикого типа.
Примеры
Материалы и общие методы
Общая информация, касающаяся нуклеотидных последовательностей легких и тяжелых цепей человеческого иммуноглобулина, представлена у: Kabat Е.А. и др., Sequences of Proteins of Immunological Interest, 5-е изд., изд-во Public Health Service, National Institutes of Health, Bethesda, MD, 1991. Аминокислоты цепей антител пронумерованы согласно нумерации EU (Edelman G.M. и др., Proc. Natl. Acad. Sci. USA 63, 1969, cc.78-85; Kabat Е.А. и др., Sequences of Proteins of Immunological Interest, 5-е изд., изд-во Public Health Service, National Institutes of Health, Bethesda, MD, 1991).
Методы рекомбинантной ДНК
Для манипуляций с ДНК использовали стандартные методы, описанные у Sambrook J. и др., Molecular cloning: A laboratory manual; Cold Spring Harbor Laboratory Press, Cold Spring Harbor, New York, 1989. Реагенты для молекулярной биологии использовали согласно инструкциям производителей.
Синтез генов
Требуемые сегменты генов получали из олигонуклеотидов, созданных путем химического синтеза. Генные сегменты длиной 600-1800 т.п.н., которые фланкированы уникальными сайтами рестрикции, собирали путем отжига и лигирования олигонуклеотидов, включая ПЦР-амплификацию и последующее клонирование через указанные сайты рестрикции, например, KpnI/SacI или AscI/PacI в клонирующем векторе pGA4, основой которого является плазмида pPCRScript (фирма Stratagene). Последовательности ДНК субклонированных генных фрагментов подтверждали путем секвенирования ДНК. Синтез генных фрагментов осуществляли в порядке, представленном в спецификации фирмы Geneart (Регенсбург, Германия).
Определение последовательностей ДНК
Последовательности ДНК определяли путем секвенирования двух цепей на фирме MediGenomix GmbH (Мартинсрид, Германия) или фирме Sequiserve GmbH (Фатерштеттен, Германия).
Анализ последовательностей ДНК и белков и обработка данных о последовательностях
Применяли пакет программ фирмы GCG (Genetics Computer Group, Мэдисон, шт.Висконсин), версия 10.2 и Infomax's Vector NT1 Advance suite, версия 8.0 для создания, картирования, анализа, аннотирования и иллюстрации последовательностей.
Экспрессионные векторы
Для экспрессии описанных антител применяли варианты экспрессионных плазмид, предназначенных для кратковременной экспрессии (например, в клетках HEK293 EBNA или HEK293-F), либо на основе кДНК-конструкции с использованием промотора CMV-интрона А, либо на основе геномной конструкции с использованием промотора CMV.
Помимо кассеты экспрессии антитела векторы содержали:
- сайт инициации репликации, обеспечивающий репликацию указанной плазмиды в Е.coli, и
- ген β-лактамазы, который придает устойчивость в Е.coli к ампициллину.
Транскрипционная единица гена антитела состояла из следующих элементов:
- уникальный(ые) сайт(ы) рестрикции на 5'-конце,
- немедленно-ранний энхансер и промотор из человеческого цитомегаловируса,
- расположенная за ним последовательность интрона А в случае экспрессии на основе кДНК-конструкции,
- 5'-нетранслируемая область гена человеческого антитела,
- сигнальная последовательность тяжелой цепи иммуноглобулина,
- цепь человеческого антитела (дикого типа или с заменой доменов) либо в виде кДНК-конструкции, либо в виде геномной конструкции с экзон-интронной конструкцией иммуноглобулина,
- 3'-нетранслируемая область с сигнальной последовательностью полиаденилирования и
- уникальный(ые) сайт(ы) рестрикции на 3'-конце.
Слияние генов, содержащих описанные цепи антитела, как указано ниже, осуществляли с помощью ПЦР и/или синтеза и сборки генов с использованием известных методов и процедур рекомбинации путем соединения соответствующих сегментов нуклеиновых кислот, например, с использованием уникальных сайтов рестрикции в соответствующих векторах. Субклонированные нуклеотидные последовательности подтверждали секвенированием ДНК. Для кратковременных трансфекций создавали большие количества плазмид посредством получения плазмид из трансформированных культур Е.coli (набор Nucleobond AX, фирма Macherey-Nagel).
Методики культивирования клеток
Применяли стандартные методики культивирования клеток, описанные в Current Protocols in Cell Biology, под ред. Bonifacino J.S., Dasso M., Harford J.B., Lippincott-Schwartz J. и Yamada K.M., изд-во John Wiley & Sons, Inc., 2000. Биспецифические антитела экспрессировали путем кратковременной котрансфекции соответствующими экспрессионными плазмидами выращенных в виде прикрепленных культур клеток HEK293-EBNA или выращенных в виде суспензионных культур клеток HEK29-F, как будет описано ниже.
Кратковременные трансфекций в системе HEK293-EBNA
Биспецифические антитела экспрессировали путем кратковременной котрансфекции соответствующими экспрессионными плазмидами (например, кодирующими тяжелую цепь и модифицированную тяжелую цепь, а также соответствующую легкую цепь и модифицированную легкую цепь) выращенных в виде прикрепленных культур клеток HEK293-EBNA (линия клеток почки человеческого эмбриона 293, экспрессирующая ядерный антиген вируса Эпштейна-Барра; Американская коллекция типовых культур, депонирована под номером АТСС № CRL-10852, партия 959 218), которые культивировали в среде DMEM (модифицированная по методу Дульбекко среда Игла, фирма Gibco), дополненной 10% PCS (фетальная телячья сыворотка, фирма Gibco) с ультранизким содержанием IgG (Ultra Low IgG PCS), 2 мМ L-глутамином (фирма Gibco) и 250 мкг/мл генетицина (фирма Gibco). Для трансфекций применяли реагент для трансфекций типа FuGENE™ 6 (фирма Roche Molecular Biochemicals), используя соотношение реагента FuGENE™ (мкл) и ДНК (мкг) 4:1 (диапазон от 3:1 до 6:1). Белки экспрессировали, применяя соответствующие плазмиды, с использованием молярного соотношения плазмид, кодирующих (модифицированные и дикого типа) легкую цепь и тяжелую цепь, 1:1 (эквимолярное соотношение), в диапазоне от 1:2 до 2:1 соответственно. Клетки подпитывали в день 3 L-глутамином до концентрации 4 мМ, глюкозой (фирма Sigma) и NAA (амид никотиновой кислоты) (фирма Gibco). Собирали супернатанты клеточных культур, содержащие биспецифическое антитело, в дни с 5 по 11 после трансфекции путем центрифугирования и хранили при -20°С. Общую информацию, касающуюся рекомбинантной экспрессии человеческих иммуноглобулинов, например, в HEK293-клетках, см. у Meissner P. и др., Biotechnol. Bioeng. 75, 2001, cc.197-203.
Кратковременные трансфекции в системе HEK293-F
Биспецифические антитела получали путем кратковременной трансфекции соответствующими плазмидами (например, кодирующими тяжелую цепь и модифицированную тяжелую цепь, а также соответствующую легкую цепь и модифицированную легкую цепь), используя систему HEK293-F (фирма Invitrogen) согласно инструкции производителя. В целом, метод состоял в следующем: HEK293-F-клетки (фирма Invitrogen), выращенные в виде суспензионной культуры либо во встряхиваемой колбе, либо в ферментере с мешалкой в бессывороточной среде для экспрессии типа FreeStyle 293 (фирма Invitrogen), трансфектировали смесью четырех экспрессионных плазмид и 293-фектином или фектином (фирма Invitrogen). В 2-литровую встряхиваемую колбу (фирма Corning) высевали клетки HEK293-F с плотностью 1,0×106 клеток/мл в 600 мл и инкубировали при 120 об/мин, 8% СО2. Через 1 день клетки трансфектировали при плотности клеток примерно 1,5×106 клеток/мл с помощью примерно 42 мл смеси А), содержащей 20 мл Opti-MEM (фирма Invitrogen) с 600 мкг общей плазмидной ДНК (1 мкг/мл), которая кодирует тяжелую цепь или модифицированную тяжелую цепь соответственно и соответствующую легкую цепь, в эквимолярном соотношении, и смеси Б), содержащей 20 мл Opti-MEM + 1,2 мл 293-фектина или фектина (2 мкл/мл). В зависимости от поглощения глюкозы в процессе ферментации добавляли раствор глюкозы. Через 5-10 дней собирали супернатант, содержащий секретированное антитело, и либо из супернатанта непосредственно очищали антитела, либо супернатант замораживали и хранили.
Определение белка
Концентрацию белков очищенных антител и их производных определяли на основе оптической плотности (ОП) при 280 нм, используя коэффициент молярной экстинкции, рассчитанный на основе аминокислотной последовательности согласно методу, который описан у Расе и др., Protein Science, 1995, 4, cc.2411-1423.
Определение концентрации антител в супернатантах
Концентрацию антител и их производных в супернатантах клеточных культур определяли путем иммунопреципитации с белок А-агарозными гранулами (фирма Roche). 60 мкл белок А-агарозных гранул отмывали трижды в TBS-NP40 (50 мМ Трис, рН 7,5, 150 мМ NaCl, 1% Nonidet-P40). Затем 1-15 мл супернатанта клеточной культуры наносили на белок А-агарозные гранулы, предварительно уравновешенные в TBS-NP40. После инкубации в течение 1 ч при комнатной температуре гранулы отмывали на фильтрующей колонке типа Ultrafree-MC (фирма Amicon), используя однократно 0,5 мл TBS-NP40, дважды 0,5 мл двукратного (2×) забуференного фосфатом физиологического раствора (2×ЗФР, фирма Roche) и быстро четыре раза 0,5 мл 100 мМ Na-цитратным буфером, рН 5,0. Связанное антитело элюировали, добавляя 35 мкл буфера для образцов NuPAGE® LDS (фирма Invitrogen). Половину образца объединяли с восстановителем для образцов NuPAGE® или оставляли в невосстановленной форме соответственно и выдерживали в течение 10 мин при 70°С. Затем по 5-30 мкл применяли для осуществления ДСН-ПААГ с использованием 4-12% бис-Трис-гелей NuPAGE® (фирма Invitrogen) (применяя буфер MOPS для осуществлении ДСН-ПААГ в невосстанавливающих условиях и буфер MES в виде подвижного буфера с антиоксидантной добавкой NuPAGE® (фирма Invitrogen) для осуществлении ДСН-ПААГ в восстанавливающих условиях) и окрашивали кумасси бриллиантовым голубым.
Концентрацию антител и их производных в супернатантах клеточных культур оценивали количественно с помощью аффинной ЖХВР-хроматографии. В целом, метод состоял в следующем: супернатанты, содержащие антитела и их производные, которые связывались с белком А, вносили на колонку Applied Biosystems Poros A/20 в 200 мМ KH2PO4, 100 мМ натрий-цитратный буфер, рН 7,4 и элюировали из матрикса с помощью 200 мМ NaCl, 100 мМ лимонной кислоты, рН 2,5 с использованием системы Agilent HPLC 1100. Элюированный белок оценивали количественно с помощью УФ-абсорбции и интегрирования площадей пиков. Очищенное стандартное антитело в виде IgG1 служило в качестве стандарта.
В альтернативном варианте концентрацию антител и их производных в супернатантах клеточных культур оценивали с помощью «сэндвич»-IgG-ELISA. В целом, метод состоял в следующем: 96-луночные титрационные микропланшеты, обладающие высокой способностью связывать стрептавидин А (планшеты типа Strepta Well High Bind Strepatavidin А (фирма Roche)), сенсибилизировали из расчета 100 мкл/лунку биотинилированным античеловеческим IgG F(ab')2<h-Fcγ>BI, применяемым в качестве иммобилизованной молекулы (фирма Dianova), в концентрации 0,1 мкг/мл в течение 1 ч при комнатной температуре или в другом варианте в течение ночи при 4°С и затем отмывали трижды, используя 200 мкл/лунку ЗФР, 0,05% Твин (ЗФРТ, фирма Sigma). Добавляли в лунки по 100 мкл/лунку серийных разведении в ЗФР (фирма Sigma), содержащих соответствующее антитело супернатантов клеточных культур, и инкубировали в течение 1-2 ч на шейкере для титрационных микропланшетов при комнатной температуре. Лунки отмывали трижды, используя 200 мкл/лунку ЗФРТ, и связанное антитело выявляли с помощью 100 мкл F(ab')2<hFcγ>POD (фирма Dianova) в концентрации 0,1 мкг/мл в качестве идентифицирующего антитела в течение 1-2 ч на шейкере для титрационных микропланшетов при комнатной температуре. Несвязанное идентифицирующее антитело отмывали трижды, используя 200 мкл/лунку ЗФРТ, и связанное идентифицирующее антитело выявляли, добавляя 100 мкл ABTS/лунку. Определение абсорбции осуществляли на спектрометре типа Tecan Fluor при длине волны 405 нм (длина референс волны 492 нм).
Очистка белков
Белки очищали из профильтрованных супернатанов клеточных культур согласно стандартным протоколам. В целом, метод состоял в следующем: белки наносили на колонку, заполненную белок А-сефарозой (фирма GE Healthcare), и отмывали ЗФР. Элюцию антител осуществляли при рН 2,8 с последующей немедленной нейтрализацией образца. Агрегированный белок отделяли от мономерных антител гель-фильтрацией (Superdex 200, фирма GE Healthcare) в ЗФР или в 20 мМ гистидине, 150 мМ NaCl, pH 6,0. Фракции мономерных антител объединяли, при необходимости концентрировали, используя, например, центрифужный концентратор типа MILLIPORE Amicon Ultra (30 MWCO (молекулярновесовой предел), замораживали и хранили при -20°С или -80°С. Часть образцов оставляли для последующего аналитического изучения белка и его аналитической характеризации, например, с помощью ДСН-ПААГ, гель-фильтрации или масс-спектрометрии.
ДСН-ПААГ
Применяли систему геля NuPAGE® Pre-Cast (фирма Invitrogen) согласно инструкции производителя. В частности, использовали 10% или 4-12% бис-Трис Pre-Cast-гели NuPAGE® Novex® (pH 6,4) и подвижные буферы, такие как NuPAGE® MES (гели, применяемые в восстанавливающих условиях, подвижный буфер с антиоксидантной добавкой NuPAGE®) или MOPS (гели, применяемые в невосстанавливающих условиях).
Аналитическая гель-фильтрация
В качестве гель-фильтрации, предназначенной для определения агрегированного и олигомерного состояния антител, применяли ЖХВР-хроматографию. В целом, метод состоял в следующем: очищенные на белке А антитела вносили в колонку типа Tosoh TSKgel G3000SW в 300 мМ NaCl, 50 мМ KH2PO4/K2HPO4, pH 7,5 в системе Agilent HPLC 1100, или в колонку Superdex 200 (фирма GE Healthcare) в 2×ЗФР в ЖХВР-системе Dionex. Количество элюированного белка определяли на основе УФ-абсорбции и интегрирования площадей пиков. В качестве стандарта применяли стандарт для гель-фильтрации фирмы BioRad (Gel Filtration Standard 151-1901).
Масс-спектрометрия
Общую дегликозилированную массу антител, полученных в результате кроссинговера, определяли и подтверждали с помощью масс-спектрометрии с ионизацией электроспреем (ESI-MC). В целом, метод состоял в следующем: 100 мкг очищенных антител дегликозилировали с помощью 50 мед. N-гликозидазы F (PNGазаF, фирма ProZyme) в 100 мМ KH2PO4/K2HPO4, pH 7 при 37°С в течение 12-24 ч при концентрации белка вплоть до 2 мг/мл и затем обессоливали с помощью ЖХВР на колонке Sephadex G25 (фирма GE Healthcare). Массу соответствующих тяжелых и легких цепей определяли с помощью ESI-MC после дегликозилирования и восстановления. В целом, метод состоял в следующем: 50 мкг антитела в 115 мкл инкубировали с 60 мкл 1М ТСЕР и 50 мкл 8М гидрохлорида гуанидида после обессоливания. Общую массу и массу восстановленных тяжелых и легких цепей определяли с помощью ESI-MC с использованием МС-системы Q-Star Elite, снабженной источником NanoMate.
ELISA для оценки связывания ECD IGF-1R
Особенности связывания созданных антител с внеклеточным доменом (ECD) IGF-1R анализировали с помощью ELISA. Для этой цели внеклеточный домен IGF-1R (остатки 1-462), содержащий встречающуюся в естественных условиях лидерную последовательность и 12 богатых LI-цистеином доменов эктодомена альфа-цепи человеческого IGF-1R (согласно McKern и др., 1997; Ward и др., 2001), слитый с N-концевой меткой, представляющей собой His-стрептавидин-связывающий пептид (His-SBP), клонировали в производном вектора pcDNA3 и кратковременно экспрессировали в НЕК293Р-клетках. Белковая последовательность ECD IGF-1R-His-SBP представлена в SEQ ID NO:10. 96-луночные титрационные микропланшеты, обладающие высокой способностью связывать стрептавидин А (планшеты типа Strepta Well High Bind Strepatavidin А (фирма Roche)), сенсибилизировали, используя 100 мкл/лунку супернатанта клеточной культуры, содержащего растворимый слитый белок IGF-1R-ECD-SBP, в течение ночи при 4°С и отмывали трижды, используя 200 мкл/лунку ЗФР, 0,05% Твин (ЗФРТ, фирма Sigma). Затем добавляли в лунки из расчета 100 мкл/лунку серийные разведения соответствующего антитела и в качестве референс-антитела антитело дикого типа <IGF-1R> в ЗФР (фирма Sigma), который включал 1% БСА (фракция V, фирма Roche), и инкубировали в течение 1-2 ч на шейкере для титрационных микропланшетов при комнатной температуре. При осуществлении серийных разведений в лунки вносили одинаковое количество очищенного антитела. Лунки отмывали трижды, используя 200 мкл/лунку ЗФРТ, и связанное антитело выявляли, используя 100 мкл/лунку F(ab')2<hFcγ>POD (фирма Dianova) в концентрации 0,1 мкг/мл (1:8000) в качестве идентифицирующего антитела, в течение 1-2 ч на шейкере для титрационных микропланшетов при комнатной температуре. Несвязанное идентифицирующее антитело отмывали трижды, используя 200 мкл/лунку ЗФРТ, и связанное идентифицирующее антитело выявляли, добавляя 100 мкл ABTS/лунку. Определение абсорбции осуществляли на спектрометре Tecan Fluor при длине волны 405 нм (длина референс волны 492 нм).
Biacore-анализ с использованием BCD IGF-1R (IGF-1R-ECD)
Связывание созданных антител с человеческим IGF-1R-ECD исследовали также с помощью поверхностного плазменного резонанса, используя устройство типа BIACORE T100 (фирма GE Healthcare Biosciences AB, Упсала, Швеция). В целом, метод состоял в следующем: для оценки аффинности козьи античеловеческие антитела типа IgG JIR 109-005-098 иммобилизовывали на СМ5-чипе посредством аминового сочетания для презентации антител к человеческому IGF-1R-ECD, несущих Fc. Связывание оценивали в HBS-буфере (HBS-P (10 мМ HEPES, 150 мМ NaCl, 0,005% Твин 20, рН 7,4) при 25°С. IGF-1R-ECD (фирма R&D Systems или полученный при создании изобретения) добавляли в раствор в различных концентрациях. Ассоциацию оценивали путем инъекции IGF-1R-ECD в течение промежутка времени от 80 с до 3 мин; диссоциацию оценивали путем отмывки поверхности чипа HBS-буфером в течение 3-10 мин и значение KD определяли, используя модель связывания Ленгмюра при соотношении 1:1. Из-за низкой плотности загрузки и уровня захвата антител <IGF-1R> получали данные о связывании одновалентного IGF-1R-ECD. Данные, полученные для отрицательного контроля (например, кривые, полученные только для буфера) вычитали из кривых, полученных для образца, для коррекции присущего системе сдвига основного уровня и для снижения шумовых сигналов. Применяли программу Biacore T100 Evaluation, версия 1.1.1 для анализа сенсограмм и для расчета данных, касающихся аффинности (фиг.18).
ELISA для оценки связывания ANGPT2
Особенности связывания созданных антител с полноразмерным белком ANGPT2-His (фирма R&D Systems) оценивали с помощью ELISA. Для этой цели полистироловые прозрачные усовершенствованные титрационные микропланшеты фирмы Falcon сенсибилизировали 100 мкл (1 мкг/мл) рекомбинантного человеческого ANGPT2 (фирма R&D Systems, без носителя) в ЗФР в течение 2 ч при комнатной температуре или в течение ночи при 4°С. Лунки отмывали трижды, используя по 300 мкл ЗФРТ (0,2% Твин 20), и блокировали с помощью 200 мкл 2% БСА, 0,1% Твин 20 в течение 30 мин при комнатной температуре и затем отмывали трижды, используя 300 мкл ЗФРТ. Добавляли в лунки по 100 мкл/лунку серийных разведений очищенного антитела <ANGPT2>, несущего замену VL-VH/CL-CH1, и в качестве референс-антитела антитело <ANGPT2> дикого типа в ЗФР (фирма Sigma) и инкубировали в течение 1 ч на шейкере для титрационных микропланшетов при комнатной температуре. Лунки отмывали трижды, используя 300 мкл/лунку ЗФРТ (0,2% Твин 20), и связанное антитело выявляли, используя 100 мкл/лунку (0,1 мкг/мл) F(ab')<hk>POD (фирма Biozol, каталожный №206005) или 100 мкл/лунку (0,1 мкг/мл) F(ab')<hFcγ>POD (фирма Immuno research) в 2% БСА 0,1% Твин 20 в качестве идентифицирующего антитела, в течение 1 ч на шейкере для титрационных микропланшетов при комнатной температуре. Несвязанное идентифицирующее антитело отмывали трижды, используя 300 мкл/лунку ЗФРТ, и связанное идентифицирующее антитело выявляли, добавляя 100 мкл ABTS/лунку. Определение абсорбции осуществляли на спектрометре Tecan Fluor при длине волны 405 нм (длина референс волны 492 нм).
Biacore-анализ для оценки связывания ANGPT2
Связывание созданных антител с человеческим ANGPT2 исследовали также с помощью поверхностного плазменного резонанса, используя устройство типа BIACORE Т100 (фирма GE Healthcare Biosciences AB, Упсала, Швеция). В целом, метод состоял в следующем: для оценки аффинности козьи поликлональные антитела <hIgG-Fcg> иммобилизовывали на СМ5-чипе или СМ4-чипе посредством аминового сочетания для презентации антител к человеческому ANGPT2. Связывание оценивали в HBS-буфере (HBS-P (10 мМ HEPES, 150 мМ NaCl, 0,005% Твин 20, рН 7,4), дополненном 5 мМ Са2+ или без него, при 25°С. Очищенный ANGPT2-His (фирма R&D Systems или полученный и очищенный при создании изобретения) добавляли в раствор в различных концентрациях. Ассоциацию оценивали путем инъекции ANGPT2 в течение 3 мин; диссоциацию оценивали путем отмывки поверхности чипа HBS-буфером в течение 3-5 мин и значение KD определяли, используя модель связывания Ленгмюра при соотношении 1:1. Из-за гетерогенности препарата ANGPT2 связывание при применении ингредиентов в соотношения 1:1 не было обнаружено; в результате проводили только относительную оценку значений KD. Данные, полученные для отрицательного контроля (например, кривые, полученные только для буфера), вычитали из кривых, полученных для образца, для коррекции присущего системе сдвига основного уровня и для снижения шумовых сигналов. Применяли программу Biacore Т 100 Evaluation, версия 1.1.1 для анализа сенсограмм и для расчета данных, касающихся аффинности (фиг.19).
Ингибирование связывания hANGPT2 с Tie-2-ECD (ELISA)
Для оценки способности антител к ANGPT2 оказывать интерферирующее воздействие на связывание с Tie-2 осуществляли описанный ниже ELISA. Опыт проводили в 384-луночных тирационных микропланшетах (фирма MicroCoat, Германия, каталожный №464718) при комнатной температуре (КТ). После каждой стадии инкубации планшеты отмывали трижды ЗФРТ. В начале эксперимента планшеты сенсибилизировали 0,5 мкг/мл белка Tie-2 (фирма R&D Systems, Великобритания, каталожный №.313-Т1) в течение по меньшей мере 2 часов (ч). Затем лунки блокировали ЗФР, дополненным 0,2% Твин-20 и 2% БСА (фирма Roche Diagnostics GmbH, Германия), в течение 1 ч. Разведения очищенных антител в ЗФР инкубировали вместе с 0,2 мкг/мл huANGPT2 (фирма R&D Systems, Великобритания, каталожный №623-AN) в течение 1 ч при КТ. После отмывки добавляли в течение 1 ч смесь, содержащую 0,5 мкг/мл биотинилированного антитела к ANGPT2, клон ВАМ0981 (фирма R&D Systems, Великобритания) и разведенный в соотношении 1:3000 конъюгат стрептавидин-HRP (фирма Roche Diagnostics GmbH, Германия, каталожный №11089153001). Затем планшеты отмывали 6 раз ЗФРТ. Планшеты проявляли, используя свежеприготовленный ABTS-реагент (фирма Roche Diagnostics GmbH, Германия, буфер каталожный №204530001, таблетки каталожный №11112422001), в течение 30 мин при КТ. Абсорбцию оценивали при 405 нм.
ELISA, позволяющий выявлять образование мостиковой связи типа ANGPT2-VEGF
Особенности связывания созданных биспецифических антител оценивали с помощью ELISA с использованием иммобилизованного полноразмерного белка VEGF165-His (фирма R&D Systems) и белка человеческого ANGPT2, конъюгированного с His (человеческий ANGPT2-His) (фирма R&D Systems), для выявления одновременного связывания биспецифического антитела. Только биспецифическое антитело обладало способностью связываться одновременно с VEGF и ANGPT2 и связывать «мостиком» два антигена, в то время как моноспецифические «стандартные» антитела типа IgG1 не обладали способностью связываться одновременно с VEGF и ANGPT2. Для проведения указанного анализа полистироловые прозрачные усовершенствованные титрационные микропланшеты фирмы Falcon сенсибилизировали 100 мкл (2 мкг/мл) рекомбинантного человеческого VEGF 165 (фирма R&D Systems) в ЗФР в течение 2 ч при комнатной температуре или в течение ночи при 4°С. Лунки отмывали трижды, используя 300 мкл ЗФРТ (0,2% Твин 20), и блокировали 200 мкл 2% БСА, 0,1% Твин 20 в течение 30 мин при комнатной температуре и затем отмывали трижды, используя 300 мкл ЗФРТ. По 100 мкл/лунку серий разведений биспецифического антитела и контрольных антител в ЗФР (фирма Sigma) добавляли в лунки и инкубировали в течение 1 ч на шейкере для титрационных микропланшетов при комнатной температуре. Лунки отмывали трижды, используя 300 мкл ЗФРТ (0,2% Твин 20), и связанное антитело выявляли, добавляя 100 мкл (0,5 мкг/мл) человеческого ANGPT2-His (фирма R&D Systems) в ЗФР. Лунки отмывали трижды, используя 300 мкл ЗФРТ (0,2% Твин 20), и связанный ANGPT2 выявляли, используя 100 мкл (0,5 мкг/мл) антитела <ANGPT2> mIgG1-биотин (BAM0981, фирма R&D Systems), в течение 1 ч при комнатной температуре. Несвязанное идентифицирующее антитело отмывали трижды, используя 300 мкл ЗФРТ (0,2% Твин 20), и связанное антитело выявляли, добавляя 100 мкл разведенного в соотношении 1:2000 конъюгата стрептавидин-POD (фирма Roche Diagnostics GmbH, каталожный №. No. 11089153), который разводили в соотношении 1:4 блокирующим буфером, в течение 1 ч при комнатной температуре. Несвязанный конъюгат стрептавидин-POD отмывали 3-6 раз, используя 300 мкл ЗФРТ (0,2% Твин 20), и связанный конъюгат стрептавидин-POD выявляли, добавляя 100 мкл ABTS/лунку. Определение абсорбции осуществляли на спектрометре Tecan Fluor при длине волны 405 нм (длина референс волны 492 нм) (фиг.20).
Biacore-анализ, предназначенный для выявления одновременного связывания биспецифических антител с VEGF и ANGPT2
Для дополнительного подтверждения данных, полученных с помощью ELISA, позволяющего выявлять образование мостиковой связи, осуществляли другой анализ с использованием технологии поверхностного плазменного резонанса и устройства типа Biacore Т100 для доказательства одновременного связывания с VEGF и ANGPT2 согласно следующему протоколу. Данные анализировали с помощью пакета программ Т 100: ANGPT2 иммобилизовывали с уровнем «захвата» 2000-1700 RU (относительные единицы) через антитело, несущее в качестве метки пять атомов гистидина (пентаHis-антитело) (пентаHis-Ат, не содержащее БСА, фирма Qiagen, №34660), которое иммобилизовывали на СМ5-чипе путем аминосочетания (не содержащий БСА). Буфер HBS-N служил в качестве подвижного буфера, для активации применяли смесь EDC/NHS. Иммобилизованное антитело пентаHis-Ат, не содержащее БСА, разводили в буфере для сочетания, представляющем собой NaAc, pH 4,5, концентрация = 30 мкг/мл, карбоксильные группы, которые еще оставались активированными в конце процесса, блокировали путем инъекции 1М этаноламина, опыт осуществляли при плотности лигандов 5000 и 17000 RU. ANGPT2 в концентрации 500 нМ, разведенный в подвижном буфере + 1 мг/мл БСА, «захватывался» пентаHis-Ат при скорости потока 5 мкл/мин. Затем для демонстрации связывания биспецифического антитела с ANGPT2 и с VEGF осуществляли инкубацию с rhVEGF. Для этого биспецифическое антитело связывали с ANGPT2 при скорости потока 50 мкл/мин и в концентрации 100-500 нМ, разведенным в подвижном буфере + 1 мг/мл БСА, и наличие одновременного связывания выявляли путем инкубации с VEGF (rhVEGF, фирма R&D-Systems, каталожный №293-VE) в ЗФР + подвижный буфер, включающий 0,005 об.% Твин-20, + 1 мг/мл БСА, со скоростью потока 50 мкл/мин и при использовании VEGF в концентрации 100-150 нМ. При проведении анализа время ассоциации составляло 120 с, время диссоциации 1200 с. Регенерацию осуществляли при скорости потока 50 мкл/мин с использованием 2×10 мМ глицинового буфера, pH 2,0 и при времени контакта 60 с. Сенсограммы корректировали, используя общепринятое применение двух контролей (референс-контроль: связывание биспецифического антитела и rhVEGF с иммобилизованной молекулой пентаHis-Ат). В качестве контрольных проб-«пустышек» для каждого Ат служили варианты, в которых концентрация rhVEGF составляла «0». Схематическое изображение Biacore-анализа представлено на фиг.21. Сенсограммы корректировали, используя общепринятое применение двух контролей (референс-контроль: связывание биспецифического антитела и rhVEGF с иммобилизованной молекулой пентаHis-Ат). В качестве контрольных проб-«пустышек» для каждого Ат служили варианты, в которых концентрация rhVEGF составляла «0».
Примеры 1
Получение, экспрессия, очистка и характеризация моноспецифического двухвалентного антитела <IGF-1R>, в котором вариабельные домены VL и VH заменены друг на друга и в котором константные домены CL и СН1 заменены друг на друга (сокращенно обозначено в контексте настоящего описания как антитело <IGF-1R>, несущее замену VL-VH/CL-CH1)
Пример 1А
Создание экспрессионных плазмид для моноспецифического двухвалентного антитела <IGF-1R>, несущего замену VL-VH/CL-CH1
Последовательности вариабельных доменов тяжелой и легкой цепи моноспецифического двухвалентного антитела к рецептору инсулиноподобного фактора-1 <IGF-1R>, несущего замену VL-VH/CL-CH1, включая соответствующие лидерные последовательности, описанные в данном примере, выводили из тяжелой цепи человеческого антитела <IGF-1R> (SEQ ID NO:1, плазмида 4843-pUC-HC-IGF-1R) и его легкой цепи (SEQ ID NO:2, плазмида 4842-pUC-LC-IGF-1R), которые описаны в WO 2005/005635, и константные домены тяжелой и легкой цепи выводили из человеческого антитела (С-каппа и IgG1).
Генные сегменты, кодирующие лидерную последовательность, вариабельный домен легкой цепи (VL) и константный домен человеческой легкой каппа-цепи (CL) антитела <IGF-1R> сцепляли и сливали с 5'-концом Fc-доменов константных областей человеческой тяжелой γ1-цепи (шарнир-СН2-СН3). ДНК, кодирующую соответствующий слитый белок, полученный в результате замены VH- и СН1-доменов на VL- и CL-домены, создавали путем синтеза гена и обозначали далее как <IGF-1R> НС* (тяжелая цепь*) (SEQ ID NO:3).
Генные сегменты, кодирующую лидерную последовательность, вариабельный домен тяжелой цепи (VH) и константные домены (СН1) человеческой тяжелой γ1-цепи антитела <IGF-1R> сцепляли в виде независимой цепи. ДНК, кодирующую соответствующий слитый белок, полученный в результате замены VL- и CL-доменов на VH- и СН1-домены, создавали путем синтеза гена и обозначили далее как <IGF-1R> LC* (легкая цепь*) (SEQ ID NO:4).
На фиг.5 и фиг.6 представлено схематическое изображение белковой последовательности модифицированной тяжелой цепи <IGF-1R> НС* и модифицированной легкой цепи <IGF-1R> LC*.
Ниже кратко описаны соответствующие экспрессионные векторы:
Вектор DW047-pUC-HC*-IGF-1R
Вектор DW047-pUC-HC*-IGF-1R представляет собой экспрессионную плазмиду, например, предназначенную для кратковременной экспрессии тяжелой цепи* <IGF-1R> НС* (кассета экспрессии на основе кДНК-конструкции; с CMV-интроном А), в клетках линии HEK293 (EBNA) или для стабильной экспрессии в СНО-клетках.
Помимо экспрессионной кассеты <IGF-1R> НС* этот вектор содержал
- сайт инициации репликации из pUC18, обеспечивающий репликацию указанной плазмиды в Е.coli, и
- ген β-лактамазы, который придает устойчивость в Е.coli к ампициллину.
Транскрипционная единица гена <IGF-1R> НС* содержала следующие элементы:
- уникальный сайт рестрикции AscI на 5'-конце,
- немедленно-ранний энхансер и промотор из человеческого цитомегаловируса,
- расположенную за ним последовательность интрона А,
- 5'-нетранслируемую область гена человеческого антитела,
- сигнальную последовательность легкой цепи иммуноглобулина,
- ген человеческой зрелой НС*-цепи <IGF-1R>, который кодирует слияние вариабельного домена человеческой легкой цепи (VL) и константного домена человеческой легкой каппа-цепи (CL), слитый с 5'-концом Fc-доменов константных доменов человеческой тяжелой γ1-цепи (шарнир-СН2-СН3),
- 3'-нетранслируемую область с сигнальной последовательностью полиаденилирования и
- уникальный сайт рестрикции SgrAI на 3'-конце.
Плазмидная карта экспрессионного вектора DW047-pUC-HC*-IGF-1R, предназначенного для <IGF-1R> НС*, представлена на фиг.7. Аминокислотная последовательность <IGF-1R> НС* (включая сигнальную последовательность) представлена в SEQ ID NO:3.
Вектор DW048-pUC-LC*-IGF-1R
Вектор DW048-pUC-LC*-IGF-1R представляет собой экспрессионную плазмиду, например, предназначенную для кратковременной экспрессии несущей замену VL-VH/CL-CH1 легкой цепи* <IGF-1R> LC* (кассета экспрессии на основе кДНК-конструкции; с CMV-интроном А), в клетках линии HEK293 (EBNA) или для стабильной экспрессии в СНО-клетках.
Помимо экспрессионной кассеты <IGF-1R> LC* этот вектор содержал:
- сайт инициации репликации из pUC18, обеспечивающий репликацию указанной плазмиды в Е.coli, и
- ген β-лактамазы, который придает устойчивость в Е.coli к ампициллину.
Транскрипционная единица гена <IGF-1R> LC** состояла из следующих элементов:
- уникальный сайт рестрикции Sse8387I на 5'-конце,
- немедленно-ранний энхансер и промотор из человеческого цитомегаловируса,
- расположенная за ним последовательность интрона А,
- 5'-нетранслируемая область гена человеческого антитела,
- сигнальная последовательность тяжелой цепи иммуноглобулина,
- ген человеческой зрелой LC*-цепи <IGF-1R>, который кодирует слияние вариабельного домена человеческой тяжелой цепи (VH) и константных доменов человеческой тяжелой γ1-цепи (СН1),
- 3'-нетранслируемая область с сигнальной последовательностью полиаденилирования и
- уникальные сайты рестрикции SalI и FseI на 3'-конце.
Плазмидная карта экспрессионного вектора DW048-pUC-LC*-IGF-1R, предназначенного для легкой цепи* <IGF-1R> LC*, представлена на фиг.8. Аминокислотная последовательность <IGF-1R> LC* (включая сигнальную последовательность) представлена в SEQ ID NO:4.
Плазмиды DW047-pUC-HC*-IGF-1R и DW048-pUC-LC*-IGF-1R можно применять для кратковременных или стабильных котрансфекций, например, клеток HEK293, HEK293 EBNA или СНО (2-векторная система). С целью сравнения осуществляли кратковременную экспрессию антитела <IGF-1R> дикого типа с использованием плазмид 4842-pUC-LC-IGF-1R (SEQ ID NO:2) и 4843-pUC-HC-IGF-1R (SEQ ID NO:1) аналогично методу, описанному в этом примере.
Для достижения более высоких уровней экспрессии при кратковременных экспрессиях в клетках HEK293 EBNA экспрессионную кассету <IGF-1R> НС* можно субклонировать с использованием сайтов AscI, SgrAI, а экспрессионную кассету <IGF-1R> LC* можно субклонировать с использованием сайтов Sse8387I и Fsel в экспрессионном векторе 4700-pUC-Hyg_OriP, который содержит
- элемент OriP и
- ген, обусловливающий устойчивость к гигромицину, в качестве селектируемого маркера.
Транскрипционные единицы тяжелой и легкой цепи можно либо субклонировать в двух независимых векторах 4700-pUC-Hyg-OriP с целью котрансфекций (2-векторная система), либо их можно клонировать в одном общем векторе 4700-pUC-Hyg-OriP (1-векторная система) для последующих кратковременных или стабильных трансфекций с использованием образовавшихся векторов. На фиг.9 показана плазмидная карта основного вектора 4700-pUC-OriP.
Пример 1Б
Создание экспрессионных плазмид для моноспецифического двухвалентного антитела <IGF-1R>, несущего замену VL-VH/CL-CH1
Слитые гены <IGF-1R> (слитые гены НС* и LC*), содержащие измененные Fab-последовательности относительно антитела <IGF-1R> дикого типа, собирали с помощью известных методов и процессов рекомбинации путем соединения соответствующих сегментов нуклеиновых кислот.
Каждую из нуклеотидных последовательностей, кодирующих НС* и LC* IGF-1R, синтезировали путем химического синтеза и затем клонировали в клонирующем векторе pGA4, основой которого является плазмида pPCRScript (фирма Stratagene), на фирме Geneart (Регенсбург, Германия). Кассету экспрессии, кодирующую IGF-1R НС*, встраивали путем лигирования в пригодную для Е.coli плазмиду, используя сайты рестрикции PvuII и BmgBI, с получением конечного вектора DW047-pUC-HC*-IGF-1R; кассету экспрессии, кодирующую соответствующую IGF-1R LC*, встраивали путем лигирования в пригодную для Е.coli плазмиду, используя сайты рестрикции PvuII и SalI, с получением конечного вектора DW048-pUC-LC*-IGF-1R. Субклонированные нуклеотидные последовательности подтверждали путем секвенирования ДНК. Для кратковременных и стабильных трансфекций использовали большие количества плазмид, которые получали из трансформированных культур Е.coli (набор Nucleobond AX, фирма Macherey-Nagel).
Пример 1В
Кратковременная экспрессия моноспецифического двухвалентного антитела <IGF-1R>, несущего замену VL-VH/CL-CH1, в клетках линии HEK293 EBNA
Рекомбинантное антитело <IGF-1R>, несущее замену VL-VH/CL-CH1, экспрессировали путем кратковременной котрансфекции плазмидами DW047-pUC-HC*-IGF-1R и DW048-pUC-LC*-IGF-1R выращенных в виде прикрепленных культур клеток HEK293-EBNA (линия клеток почки человеческого эмбриона 293, экспрессирующая ядерный антиген вируса Эпштейна-Барра; Американская коллекция типовых культур, депонирована под номером АТСС № CRL-10852, партия 959218), которые культивировали в среде DMEM (модифицированная по методу Дульбекко среда Игла, фирма Gibco), дополненной 10% FCS (фетальная телячья сыворотка, фирма Gibco) с ультранизким содержанием IgG (Ultra Low IgG FCS), 2 мМ L-глутамином (фирма Gibco) и 250 мкг/мл генетицина (фирма Gibco). Для трансфекций применяли реагент для трансфекций типа FuGENE™ 6 (фирма Roche Molecular Biochemicals), используя соотношение реагента FuGENE™ (мкл) и ДНК (мкг) 4:1 (диапазон от 3:1 до 6:1). Плазмиды, кодирующие легкие и тяжелые цепи <IGF-1R> НС* и LC* (плазмиды DW047-pUC-HC*-IGF-1R иd DW048-pUC-LC*-IGF-1R), экспрессировали с использованием двух различных плазмид, применяя молярное соотношение плазмид, кодирующих легкую цепь и тяжелую цепь, 1:1 (эквимолярное соотношение) в диапазоне от 1:2 до 2:1 соответственно. Клетки подпитывали в день 3 L-глутамином до концентрации 4 мМ, глюкозой (фирма Sigma) и NAA (амид никотиновой кислоты) (фирма Gibco). Собирали супернатанты клеточных культур, содержащие антитело <IGF-1R>, несущее замену VL-VH/CL-CH1, в дни с 5 по 11 после трансфекции путем центрифугирования и хранили при -20°С. Общую информацию, касающуюся рекомбинантной экспрессии человеческих иммуноглобулинов, например, в HEK293-клетках, см. у Meissner Р. и др., Biotechnol. Bioeng. 75, 2001, cc.197-203.
Пример 1Г
Иммунопреципитация моноспецифического двухвалентного антитела <IGF-1R>, несущего замену VL-VH/CL-CH1
Моноспецифическое двухвалентное антитело <IGF-1R>, несущее замену VL-VH/CL-CH1, выделяли из супернатантов клеточных культур (пример 1В) путем иммунопреципитации с использованием белок А-агарозных гранул (фирма Roche). 60 мкл белок А-агарозных гранул отмывали трижды в TBS-NP40 (50 мМ Трис, рН 7,5, 150 мМ NaCl, 1% Nonidet-P40). Затем 1-15 мл супернатанта клеточной культуры наносили на белок А-агарозные гранулы, предварительно уравновешенные в TBS-NP40. После инкубации в течение 1 ч при комнатной температуре гранулы отмывали на фильтрующей колонке типа Ultrafree-MC (фирма Amicon), используя однократно 0,5 мл TBS-NP40, дважды 0,5 мл двукратного (2×) забуференного фосфатом физиологического раствора (2×ЗФР, фирма Roche) и быстро четыре раза 0,5 мл 100 мМ Na-цитратным буфером, рН 5,0. Связанное антитело элюировали, добавляя 35 мкл буфера для образцов NuPAGE® LDS (фирма Invitrogen). Половину образца объединяли с восстановителем для образцов NuPAGE® или оставляли в невосстановленной форме соответственно и выдерживали в течение 10 мин при 70°С. Затем по 20 мкл применяли для осуществления ДСН-ПААГ с использованием 4-12% бис-Трис-гелей NuPAGE® (фирма Invitrogen) (применяя буфер MOPS для осуществлении ДСН-ПААГ в невосстанавливающих условиях и буфер MES в виде подвижного буфера с антиоксидантной добавкой NuPAGE® (фирма Invitrogen) для осуществлении ДСН-ПААГ в восстанавливающих условиях) и окрашивали кумасси бриллиантовым голубым. На фиг.10 показаны полученные с помощью ДСН-ПААГ результаты стандартного эксперимента по иммунопреципитации. Моноспецифическое двухвалентное антитело <IGF-1R>, несущее замену VL-VH/CL-CH1, напоминало по своим характеристикам типичное антитело типа IgG1, при этом легкая цепь LC* присутствовала в полосе, которой соответствует молекулярная масса примерно 25 кДа, а тяжелая цепь НС* присутствовала в полосе, которой соответствует молекулярная масса 50 кДа. При использовании невосстанавливающих условий может быть обнаружена полоса, которой соответствует молекулярная масса примерно 150 кДа, характерная для полного антитела.
Пример 1Д
Очистка моноспецифического двухвалентного антитела <IGF-1R>, несущего замену VL-VH/CL-CH1, и подтверждение его идентичности с помощью масс-спектрометрии
Экспрессированное и секретированное моноспецифическое двухвалентное антитело <IGF-1R>, несущее замену VL-VH/CL-CH1, очищали из профильтрованных супернатантов клеточных культур с помощью аффинной хроматографии на белке А согласно известным стандартным методам. В целом, метод состоял в следующем: содержащие антитело <IGF-1R>, несущее замену VL-VH/CL-CH1, супернатанты клеточных культур после кратковременных трансфекций осветляли центрифугированием (10000×g в течение 10 мин) и фильтрацией через фильтр с размером пор 0,45 мкм и вносили на содержащую белок А колонку HiTrap MabSelect Xtra (фирма GE Healthcare), уравновешенную ЗФР-буфером (10 мМ Na2HPO4, 1 мМ KH2PO4, 137 мМ NaCl и 2,7 мМ KCl, рН 7,4). Несвязанные белки отмывали уравновешивающим ЗФР-буфером, а затем 0,1 М натрий-цитратным буфером, рН 5,5 и отмывали ЗФР. Для элюции антитела <IGF-1R>, несущего замену VL-VH/CL-CH1, применяли 100 мМ натрий-цитратый буфер, рН 2,8, после чего образцы немедленно нейтрализовали, добавляя 300 мкл 2М Трис, рН 9,0 на 2-миллилитровую фракцию. Агрегированный белок отделяли от мономерных антител с помощью гель-фильтрации на колонке HiLoad 26/60 Superdex 200 prep grade (фирма GE Healthcare) в 20 мМ гистидине, 150 мМ NaCl, рН 6,0, а фракцию мономерных антител затем концентрировали с помощью центрифужного концентратора MILLIPORE Amicon Ultra-15. Антитело <IGF-1R>, несущее замену VL-VH/CL-CH1, замораживали и хранили при -20°С или -80°С. Целостность антитела <IGF-1R>, несущего замену VL-VH/CL-CH1, анализировали с помощью ДСН-ПААГ в присутствии восстановителя или без него и затем окрашивали кумасси бриллиантовым голубым согласно методу, описанному выше в примере 1Г. Очищенное антитело <IGF-1R>, несущее замену VL-VH/CL-CH1, напоминало по своим характеристикам типичное антитело типа IgG1, при этом легкая цепь LC* присутствовала в полосе, которой соответствует молекулярная масса примерно 25 кДа, а тяжелая цепь НС* присутствовала в полосе, которой соответствует молекулярная масса 50 кДа. При использовании невосстанавливающих условий может быть обнаружена полоса, которой соответствует молекулярная масса примерно 150 кДа, характерная для полного антитела. Агрегацию и олигомерное состояние антитела <IGF-1R>, несущего замену VL-VH/CL-CH1, исследовали с помощью аналитической гель-фильтрации и установлено, что очищенное антитело с Fab, полученными в результате кроссинговера, находилось в мономерном состоянии. Охарактеризованные образцы использовали для дальнейшего аналитического исследования белка и изучения функциональных характеристик. С помощью ESI-масс-спектрометрии была подтверждена теоретическая молекулярная масса (которую рассчитывали без учета C-концевого остатка лизина тяжелой цепи и без учета C-концевого остатка пироглутамата легкой цепи) полностью дегликозилированного антитела <IGF-1R>, несущего замену VL-VH/CL-CH1, обнаруженного в основных пиках (фиг 22).
Пример 1Е
Анализ способности моноспецифического двухвалентного антитела <IGF-1R>, несущего замену VL-VH/CL-CH1, связывать IGF-1R с помощью применяемого для оценки связывания IGF-1R-ECD ELISA и Biacore-анализа
Связывающие способности моноспецифического двухвалентного антитела <IGF-1R>, несущего замену VL-VH/CL-CH1, оценивали с помощью ELISA с использованием внеклеточного домена (ECD) IGF-1R согласно описанному выше методу. На фиг.11 представлены стандартизованные результаты, полученные с помощью «сэндвич»-IgG-ELISA на основе титрации антитела <IGF-1R>, несущего замену VL-VH/CL-CH1, и антитела <IGF-1R> дикого типа, из супернатантов после кратковременной экспрессии HEK293E-клеток. Четко продемонстрировано, что антитело <IGF-1R>, несущее замену VL-VH/CL-CH1, обладало функциональной активностью и для него выявлены характеристики связывания и кинетические характеристики, сопоставимые с характеристиками антитела <IGF-1R> дикого типа, и поэтому оно являлось полностью функциональным. Небольшие выявленные различия находились в пределах ошибки метода и могли, например, являться результатом небольшой вариабельности концентраций белка.
Эти данные подтверждали с помощью Biacore-анализа, для которого использовали соответствующие очищенные антитела, при этом установлено, что моноспецифическое двухвалентное антитело <IGF-1R>, несущее замену VL-VH/CL-CH1, обладало аффинностью и кинетическими характеристиками связывания IGF-1R-ECD, сопоставимыми с исходным антителом дикого типа, в пределах ошибки метода. Кинетические данные представлены ниже в таблице:
Пример 1Ж
Анализ способности моноспецифического двухвалентного антитела <IGF-1R>, несущего замену VL-VH/CL-CH1, связывать 1GF-1R с помощью FACS с использованием сверхэкспрессирующих IGF-1R I24-клеток
Для подтверждения активности связывания антитела <IGF-1R>, несущего замену VL-VH/CL-CH1, с IGF-1R, сверхэкспрессируемым на поверхности I24-клеток (NIH3T3-клетки, экспрессирующие рекомбинантный человеческий IGF-1R, фирма Roche), использовали FACS-анализ. В целом, метод состоял в следующем: 5×105 I24-клеток на каждую трубку, предназначенную для осуществления FACS, инкубировали с разведением очищенного антитела <IGF-1R>, несущего замену VL-VH/CL-CH1, и антитела <IGF-1R> дикого типа в качестве референс-антитела и инкубировали на льду в течение 1 ч. Несвязанные антитела отмывали с помощью 4 мл охлажденного на льду ЗФР (фирма Gibco) 4-2% FCS (фирма Gibco). Затем клетки центрифугировали (5 мин при 400 g) и связанное антитело выявляли с помощью конъюгата F(ab')2<hFcγ>PE (фирма Dianova) на льду в течение 1 ч, защищая от действия света. Несвязанное идентифицирующее антитело отмывали с помощью 4 мл охлажденного на льду ЗФР + 2% FCS. Затем клетки центрифугировали (5 мин при 400 g), ресуспендировали в 300-500 мкл ЗФР и связанное идентифицирующее антитело оценивали количественно с помощью устройства FACSCalibur или FACS Canto (фирма BD (FL2-канал, 10000 клеток на процесс). В эксперимент включали в качестве контролей антитела соответствующего изотипа для исключения любых неспецифических случаев связывания. Связывание антитела <IGF-1R>, несущего замену VL-VH/CL-CH1, и антитела <IGF-1R> дикого типа с IGF-1R на поверхности I24-клеток сравнивали путем сопоставления зависящего от концентрации сдвига средней интенсивности флуоресценции.
Дополнительные эксперименты продемонстрировали, что антитело <IGF-1R>, несущее замену VL-VH/CL-CH1, сохраняло также способность индуцировать интернализацию IGF-1R на MCF7-клетках и обладало лишь незначительной ADCC-активностью на DU145-клетках при инкубации с человеческими РВМС, сопоставимой с активностью антитела <IGF-1R> дикого типа.
В сочетании данные, полученные в экспериментах, которые описаны в примере 1, свидетельствуют о том, что на основе замены доменов можно создавать полностью функциональные антитела, свойства которых сопоставимы со свойствами антител дикого типа. Сохранение всех функциональных свойств подтверждено также с помощью биохимических и клеточных анализов. Эти антитела с заменами доменов являлись основой для создания описанных ниже биспецифических антител.
Примеры 2
Получение, экспрессия, очистка и характеризация моноспецифического двухвалентного антитела <ANGPT2>, в котором вариабельные домены VL и VH заменены друг на друга и в котором константные домены CL и СН1 заменены друг на друга (сокращенно обозначено в контексте настоящего описания как антитело <ANGPT2>, несущее замену VL-VH/CL-CH1)
Пример 2А
Создание экспрессионных плазмид для варианта моноспецифического двухвалентного антитела <ANGPT2>, несущего замену VL-VH/CL-CH1
Последовательности вариабельных областей тяжелой и легкой цепи моноспецифического двухвалентного антитела к ангиопоэтину-2 (<ANGPT2>, несущее замену VL-VH/CL-CH1), включая соответствующие лидерные последовательности, описанные в данном примере, выводили из тяжелой цепи человеческого антитела <ANGPT2> (SEQ ID NO:6) и его легкой цепи (SEQ ID NO:7), которые описаны в WO 2006/045049, а константные домены тяжелой и легкой цепи выводили из человеческого антитела (С-каппа и IgG1).
Генные сегменты, кодирующие лидерную последовательность, вариабельный домен легкой цепи (VL) и константный домен человеческой легкой каппа-цепи (CL) антитела <ANGPT2> сцепляли и сливали с 5'-концом Fc-доменов константных областей человеческой тяжелой γ1-цепи (шарнир-СН2-СН3). ДНК, кодирующую соответствующий слитый белок, полученный в результате замены VH- и СН1-доменов на VL- и CL-домены, создавали путем синтеза гена и обозначали далее как <ANGPT2> HC* (тяжелая цепь*) (SEQ ID NO:8).
Генные сегменты, кодирующую лидерную последовательность, вариабельный домен тяжелой цепи (VH) и константные домены (СН1) человеческой тяжелой γ1-цепи антитела <ANGPT2> сцепляли в виде независимой цепи. ДНК, кодирующую соответствующий слитый белок, полученный в результате замены VL- и CL-доменов на VH- и СН1-домены, создавали путем синтеза гена и обозначили далее как <ANGPT2> LC* (легкая цепь*) (SEQ ID NO:9).
Соответствующие экспрессионные векторы аналогичны описанным в примере 1А. Плазмидная карта экспрессионного вектора pUC-HC*-ANGPT2> тяжелой цепи* <ANGPT2> НС* представлена на фиг.12. Аминокислотная последовательность <ANGPT2> НС* (включая сигнальную последовательность) представлена в SEQ ID NO:8.
Плазмидная карта экспрессионного вектора pUC-LC*-ANGPT2> легкой цепи* <ANGPT2> LC* представлена на фиг.13. Аминокислотная последовательность <ANGPT2> LC* (включая сигнальную последовательность) представлена в SEQ ID NO:9. Плазмиды pUC-HC*-ANGPT2> и pUC-LC*-ANGPT2> можно применять для кратковременных или стабильных котрансфекций, например, клеток HEK293-F, HEK293 EBNA или СНО (2-векторная система).
Для достижения более высоких уровней экспрессии при кратковременных экспрессиях в клетках HEK293 EBNA экспрессионную кассету <ANGPT2> НС* можно субклонировать с использованием сайтов AscI, SgrAI, а экспрессионную кассету <ANGPT2> LC* можно субклонировать с использованием сайтов Sse8387I и FseI в экспрессионном векторе 4700 pUC-Hyg_OriP, который описан в примере 1А. Транскрипционные единицы тяжелой и легкой цепи можно либо субклонировать в двух независимых векторах 4700-pUC-Hyg-OriP с целью котрансфекций (2-векторная система), либо их можно клонировать в одном общем векторе 4700-pUC-Hyg-OriP (1-векторная система) для последующих кратковременных или стабильных трансфекций с использованием образовавшихся векторов через сайты FseI, SgrAI, Sse8387I и AscI.
Антитело <ANGPT2> дикого типа клонировали в плазмидах SB04-pUC-HC-ANGPT2 (SEQ ID NO:6) и SB06-pUC-LC-ANGPT2 (SEQ ID NO:7), которые являются аналогами векторов, описанных в данном примере и выше в примере 1А. Транскрипционные единицы тяжелой и легкой цепи антитела <ANGPT2> дикого типа субклонировали из созданных из базисных векторов плазмид SB04-pUC-HC-ANGPT2 и SB06-pUC-LC-ANGPT2 через сайты FseI, SgrAI, Sse8387I и AscI в плазмидах SB07-pUC-Hyg-OriP-HC-ANGPT2 и SB09-pUC-Hyg-OriP-LC-ANGPT2 для достижения более высоких уровней кратковременной экспрессии в HEK293E-клетках. Для сравнения и при осуществлении экспериментов по совместной экспрессии (см. пример 3) антитело <ANGPT2> дикого типа либо кратковременно (ко)экспрессировали с использованием либо плазмид SB07-pUC-Hyg-OriP-HC-ANGPT2 и SB09-pUC-Hyg-OriP-LC-ANGPT2, либо плазмид SB04-pUC-HC-ANGPT2 и SB06-pUC-LC-ANGPT2.
Пример 2Б
Создание экспрессионных плазмид для моноспецифического двухвалентного антитела <ANGPT2>, несущего замену VL-VH/CL-CH1
Слитые гены антитела <ANGPT2>, несущего замену VL-VH/CL-CH1 (слитые гены НС* и LC*), содержащие измененные Fab-последовательности относительно антитела <ANGPT2> дикого типа, собирали с помощью известных методов и процессов рекомбинации путем соединения соответствующих сегментов нуклеиновых кислот.
Каждую из нуклеотидных последовательностей, кодирующих НС* и LC* антитела <ANGPT2>, несущего замену VL-VH/CL-CH1, синтезировали путем химического синтеза и затем клонировали в клонирующем векторе pGA4, основой которого является плазмида pPCRScript (фирма Stratagene), на фирме Geneart (Регенсбург, Германия). Кассету экспрессии, кодирующую НС* антитела <ANGPT2>, несущего замену VL-VH/CL-CH1, встраивали путем лигирования в пригодную для Е.coli плазмиду, используя сайты рестрикции PstI и EcoNI, с получением конечного вектора pUC-HC*-<ANGPT2>; кассету экспрессии, кодирующую соответствующую <ANGPT2> LC*, встраивали путем лигирования в пригодную для Е.coli плазмиду, используя сайты рестрикции PvuII и FseI, с получением конечного вектора pUC-LC*-<ANGPT2>. Субклонированные нуклеотидные последовательности подтверждали путем секвенирования ДНК. Для кратковременных и стабильных трансфекций использовали большие количества плазмид, которые получали из трансформированных культур Е.coli (набор Nucleobond AX, фирма Macherey-Nagel).
Пример 2В
Кратковременная экспрессия моноспецифического двухвалентного антитела <ANGPT2>, несущего замену VL-VH/CL-CH1, в клетках линии HEK293 EBNA
Рекомбинантное антитело <ANGPT2>, несущее замену VL-VH/CL-CH1, экспрессировали путем кратковременной котрансфекции плазмидами pUC-HC*-ANGPT2> и pUC-LC*-ANGPT2> выращенных в виде прикрепленных культур клеток HEK293-EBNA (линия клеток почки человеческого эмбриона 293, экспрессирующая ядерный антиген вируса Эпштейна-Барра; Американская коллекция типовых культур, депонирована под номером АТСС № CRL-10852, партия 959218), которые культивировали в среде DMEM (модифицированная по методу Дульбекко среда Игла, фирма Gibco), дополненной 10% FCS (фетальная телячья сыворотка, фирма Gibco) с ультранизким содержанием IgG (Ultra Low IgG FCS), 2 мМ L-глутамином (фирма Gibco) и 250 мкг/мл генетицина (фирма Gibco). Для трансфекций применяли реагент для трансфекций типа FuGENE™ 6 (фирма Roche Molecular Biochemicals), используя соотношение реагента FuGENE™ (мкл) и ДНК (мкг) 4:1 (диапазон от 3:1 до 6:1). Плазмиды, кодирующие легкие и тяжелые цепи <ANGPT2> НС* и LC* (плазмиды pUC-HC*-ANGPT2> и pUC-LC*-ANGPT2>), экспрессировали с использованием двух различных плазмид, применяя молярное соотношение плазмид, кодирующих легкую цепь и тяжелую цепь, 1:1 (эквимолярное соотношение) в диапазоне от 1:2 до 2:1 соответственно. Клетки подпитывали в день 3 L-глутамином до концентрации 4 мМ, глюкозой (фирма Sigma) и NAA (фирма Gibco). Собирали супернатанты клеточных культур, содержащие антитело <ANGPT2>, несущее замену VL-VH/CL-CH1, в дни с 5 по 11 после трансфекции путем центрифугирования и хранили при -20°С. Общую информацию, касающуюся рекомбинантной экспрессии человеческих иммуноглобулинов, например, в HEK293-клетках, см. у Meissner Р. и др., Biotechnol. Bioeng. 75, 2001, cc.197-203.
Пример 2Г
Очистка моноспецифического двухвалентного антитела <ANGPT2>, несущего замену VL-VH/CL-CH1, и подтверждение его идентичности с помощью масс-спектрометрии
Экспрессированное и секретированное моноспецифическое двухвалентное антитело <ANGPT2>, несущее замену VL-VH/CL-CH1, очищали из профильтрованных супернатантов клеточных культур с помощью аффинной хроматографии на белке А согласно известным стандартным методам. В целом, метод состоял в следующем: содержащие антитело <ANGPT2>, несущее замену VL-VH/CL-CH1, супернатанты клеточных культур после кратковременных трансфекции осветляли центрифугированием (10000 g в течение 10 мин) и фильтровали через фильтр с размером пор 0,45 мкм и вносили на содержащую белок А колонку HiTrap MabSelect Xtra (фирма GE Healthcare), уравновешенную ЗФР-буфером (10 мМ Na2HPO4, 1 мМ KH2PO4, 137 мМ NaCl и 2,7 мМ KCl, рН 7,4). Несвязанные белки отмывали уравновешивающим ЗФР-буфером, а затем 0,1 М натрий-цитратным буфером, рН 5,5 и отмывали ЗФР. Для элюции антитела <ANGPT2>, несущего замену VL-VH/CL-CH1, применяли 100 мМ натрий-цитратный буфер, рН 2,8, после чего образцы немедленно нейтрализовали, добавляя 300 мкл 2М Трис, рН 9,0 на 2-миллилитровую фракцию. Агрегированный белок отделяли от мономерных антител с помощью гель-фильтрации на колонке HiLoad 26/60 Superdex 200 prep grade (фирма GE Healthcare) в 20 мМ гистидине, 150 мМ NaCl, pH 6,0, а фракцию мономерных антител затем концентрировали с помощью центрифужного концентратора MILLIPORE Amicon Ultra-15. Антитело <ANGPT2>, несущее замену VL-VH/CL-СН1, замораживали и хранили при -20°С или -80°С. Целостность антитела <ANGPT2>, несущего замену VL-VH/CL-CH1, анализировали с помощью ДСН-ПААГ в присутствии восстановителя или без него и затем окрашивали кумасси бриллиантовым голубым (фиг.23А). Агрегацию и олигомерное состояние антитела <ANGPT2>, несущего замену VL-VH/CL-CH1, исследовали с помощью аналитической гель-фильтрации (фиг.23Б). Охарактеризованные образцы использовали для дальнейшего аналитического исследования белка и изучения функциональных характеристик. С помощью ESI-масс-спектрометрии была подтверждена теоретическая молекулярная масса полностью дегликозилированного антитела <ANGPT2>, несущего замену VL-VH/CL-CH1, обнаруженного в основных пиках. Не обнаружено никакого загрязнения напоминающими антитело белками.
Пример 2Е
Анализ способности моноспецифического двухвалентного антитела <ANGPT2>, несущего замену VL-VH/CL-CH1, связывать ANGPT2 с помощью применяемого для оценки связывания ANGPT2 ELISA и Biacore-анализа
Связывающие способности моноспецифического двухвалентного антитела <ANGPT2>, несущего замену VL-VH/CL-CH1, оценивали с помощью ELISA с использованием полноразмерного белка ANGPT2-His (фирма R&D Systems) согласно описанному выше методу. На фиг.24 представлены результаты, полученные с помощью предназначенного для оценки связывания «сэндвич»-ELISA на основе титрации очищенного антитела <ANGPT2>, несущего замену VL-VH/CL-CH1, и антитела <ANGPT2> дикого типа. Четко продемонстрировано, что антитело <ANGPT2>, несущее замену VL-VH/CL-CH1, обладало функциональной активностью и для него выявлены характеристики связывания и кинетические характеристики, сопоставимые с характеристиками антитела <ANGPT2> дикого типа, и поэтому оно являлось полностью функциональным. Небольшие выявленные различия находились в пределах ошибки метода и могли, например, являться результатом небольшой вариабельности концентраций белка.
Эти данные подтверждены с помощью Biacore-анализа, для которого использовали соответствующие очищенные антитела, при этом установлено, что моноспецифическое двухвалентное антитело <ANGPT2>, несущее замену VL-VH/CL-CH1, характеризуется значением KD, равным 13 пМ, и таким образом, имеет сопоставимые в пределах ошибки метода параметры аффинности и кинетические характеристики связывания с ANGPT2 с исходным антителом <ANGPT2> дикого типа, для которого значение KD составляет 12 пМ (фиг.25)
Пример 2Ж
Анализ функциональных свойств моноспецифического двухвалентного антитела <ANGPT2>, несущего замену VL-VH/CL-CH1
Для демонстрации того, что функциональные свойства моноспецифического двухвалентного антитела <ANGPT2>, несущего замену VL-VH/CL-CH1 сопоставимы со свойствами исходного антитела <ANGPT2> дикого типа, сравнивали способность двух антител оказывать интерферирующее воздействие на связывание ANGPT2 с внеклеточным доменом его Tie2-рецептора с помощью предназначенного для оценки связывания ELISA, описанного выше. По данным соответствующего предназначенного для оценки связывания ELISA значение ЕС50, характеризующее интерферирующее воздействие антитела <ANGPT2>, несущего замену VL-VH/CL-CH1, на связывание с человеческим ANGPT2, составляло 135 нг/мл, что сопоставимо со значением ЕС50 145 нм, полученным для исходного антитела <ANGPT2> дикого типа. Эти данные были подтверждены с помощью клеточного конкурентного анализа связывания лиганда, который проводили с использованием HEK293-клеток, сверхэкспрессирующих на поверхности Tie2, в котором установлено, что значение ЕС50, характеризующее интерферирующее воздействие антитела <ANGPT2>, несущего замену VL-VH/CL-CH1, на связывание с человеческим ANGPT2, составляло 225 нг/мл, что сопоставимо со значением ЕС50 205 нМ, полученным для исходного антитела <ANGPT2> дикого типа (данные не представлены).
В сочетании данные, полученные в экспериментах, которые описаны в примере 2, свидетельствуют о том, что на основе замены доменов можно создавать полностью функциональные антитела, свойства которых сопоставимы со свойствами антител дикого типа. Сохранение всех функциональных свойств подтверждено также с помощью биохимических и клеточных анализов. Эти антитела с заменами доменов являлись основой для создания описанных ниже биспецифических антител, что представлено ниже в примерах 3 и 4.
Пример 2З
Метод молекулярного моделирования антител с заменой доменов позволил установить, что стерическое пространство между замененным доменами может ограничивать укладку. По этой причине при создании настоящего изобретения создавали конструкции, в которые интродуцировали дополнительный остаток глицина на С-конец замененных доменов Fab-фрагментов, например, между VL-CL и связывающей шарнирной областью или на конец свободного VH-CH1-домена соответственно. Соответствующее моноспецифическое двухвалентное антитело обозначено далее как антитело <ANGPT2>, несущее замену VL-VH(G)/CL-CH1(G).
Последовательности вариабельных областей тяжелой и легкой цепи моноспецифического двухвалентного антитела к ангиопоэтину-2 (<ANGPT2>, несущее замену VL-VH/CL-CH1), включая соответствующие лидерные последовательности, описанные в данном примере, выводили из тяжелой цепи человеческого антитела <ANGPT2> (SEQ ID NO:6) и его легкой цепи (SEQ ID NO:7), которые описаны в WO 2006/045049, а константные домены тяжелой и легкой цепи выводили из человеческого антитела (С-каппа и IgG1).
Генные сегменты, кодирующие лидерную последовательность, вариабельный домен легкой цепи (VL) и константный домен человеческой легкой каппа-цепи (CL) антитела <ANGPT2> сцепляли и сливали с 5'-концом Fc-доменов константных областей человеческой тяжелой γ1-цепи (шарнир-СН2-СН3) и включали дополнительный остаток глицина. ДНК, кодирующую соответствующий слитый белок, полученный в результате замены VH- и СН1-доменов на VL- и CL-домены, создавали путем синтеза гена и обозначали далее как <ANGPT2> HC(G)* (тяжелая цепь*) (SEQ ID NO:17).
Генные сегменты, кодирующую лидерную последовательность, вариабельный домен тяжелой цепи (VH) и константные домены (СН1) человеческой тяжелой γ1-цепи антитела <ANGPT2> сцепляли в виде независимой цепи, включающей дополнительный остаток глицина. ДНК, кодирующую соответствующий слитый белок, полученный в результате замены VL- и CL-доменов на VH- и CH1-домены, создавали путем синтеза гена и обозначили далее как <ANGPT2> LC(G)* (легкая цепь*) (SEQ ID NO:9). <ANGPT2> HC(G)* (тяжелая цепь*) (SEQ ID NO:18).
Соответствующие экспрессионные векторы аналогичны описанным выше в примере 2. Затем эти экспрессионные векторы применяли для кратковременной совместной экспрессии соответствующего антитела <ANGPT2>, несущего замену доменов VL-VH(G)/CL-CH1(G), в HEK293-F-клетках. Соответствующее антитело <ANGPT2>, несущее замену VL-VH(G)/CL-CH1(G), очищали после кратковременной экспрессии согласно описанному выше методу и анализировали с использованием ДСН-ПААГ, гель-фильтрации и масс-спектрометрии соответствующего антитела. Уровни экспрессии белков были достаточно высокими и сходными с уровнями, полученными для традиционного антитела, несущего замену VL-VH/CL-CH1, описанного выше. Для всех изученных свойств не выявлено никаких неожиданных результатов, и они были сопоставимы со свойствами соответствующего антитела <ANGPT2> дикого типа. На фиг.31 приведены данные, демонстрирующие фактически сопоставимые свойства антитела <ANGPT2> дикого типа и антитела <ANGPT2>, несущего замену VL-VH(G)/CL-CH1(G), которые получены с помощью предназначенного для оценки связывания ANGPT2 Biacore-анализа. В пределах ошибки метода аффинность к связыванию обоих антител с человеческим ANGPT2 оказалась сопоставимой и характеризовалась значениями KD (среднее по двум повторностям), составляющими примерно 38 пМ для антитела <ANGPT2> дикого типа и примерно 45 пМ для антитела <ANGPT2>, несущего замену VL-VH(G)/CL-CH1(G).
Примеры 3
Экспрессия биспецифического двухвалентного антитела <ANGPT2-IGF-1R>, в котором тяжелая и легкая цепи специфически связываются с IGF-1R, вариабельные домены VL и VH заменены друг на друга и константные домены CL и СН1 заменены друг на друга (сокращенно обозначено в контексте настоящего описания как антитело <ANGPT2-IGF-1R>, несущее замену VL-VH/CL-CH1)
Пример 3А
Кратковременная совместная экспрессии антитела <ANGPT2> дикого типа и антитела <IGF-1R>, несущего замену VL-VH/CL-CH1 в клетках линии HEK293 EBNA с получением биспецифического антитела <ANGPT2-IGF-1R>, несущего замену VL-VH/CL-CH1
Для создания функционального биспецифического антитела, распознающего ANGPT2, на основе Fab-фрагмента антитела <ANGPT2> дикого типа, с одной стороны, и распознающего IGF-1R, на основе Fab-фрагмента антитела <IGF-1R>, несущего замену VL-VH/CL-CH1, с другой стороны, две экспрессионные плазмиды, кодирующие антитело <IGF-1R>, несущее замену VL-VH/CL-CH1 (пример 1А), совместно экспрессировали с двумя экспрессионными плазмидами, кодирующими антитело <ANGPT2> дикого типа (пример 2А). С учетом статистической ассоциации тяжелых цепей дикого типа (НС) и тяжелых цепей, полученных в результат кроссинговера Fab (НС*), это приводило к получению биспецифического и двухвалентного антитела <ANGPT2-IGF-1R>, несущего замену VL-VH/CL-CH1. Принимая, что оба антитела одинаково хорошо экспрессировались и при этом не образовывались побочные продукты в количестве, которое может повлиять на результат, этот процесс должен приводить к получению нижеуказанных трех основных продуктов в соотношении 1:2:1: моноспецифическое антитело <IGF-1R>, несущее замену VL-VH/CL-CH1, биспецифическое антитело <ANGPT2-IGF-1R>, несущее замену VL-VH/CL-CH1, и антитело <ANGPT2> дикого типа. Кроме того, можно ожидать получения нескольких побочных продуктов, таких как димеры LC-LC* (Fab2-фрагмент), НС-НС* (одновалентное антитело) и HC*-LC.
В противоположность этому при совместной экспрессии двух экспрессионных плазмид, кодирующих антитело <IGF-1R> дикого типа (пример 1А), двух экспрессионных плазмид, кодирующих антитело <ANGPT2> дикого типа, в качестве референс-антител должно образовываться лишь незначительное количество функционального биспецифического антитела <IGF-1R-ANGPT2> из-за статистической ассоциации тяжелых цепей, но неконтролируемой ассоциации легких цепей с обеими тяжелыми цепями из антител дикого типа <IGF-1R> и <ANGPT2>.
Для создания смеси основных продуктов, таких как А) антитело <IGF-1R>, несущее замену VL-VH/CL-CH1, Б) биспецифическое антитело <ANGPT2-IGF-1R>, несущее замену VL-VH/CL-CH1, и В) антитело <ANGPT2> дикого типа, четырьмя плазмидами DW047-pUC-HC*-IGF-1R и DW048-pUC-LC*-IGF-1R и либо плазмидами SB07-pUC-Hyg-OriP-HC-ANGPT2 и SB09-pUC-Hyg-OriP-LC-ANGPT2 (либо плазмидами SB04-pUC-HC-ANGPT2 и SB06-pUC-LC-ANGPT2) кратковременно котрансфектировали выращенные в виде прикрепленных культур клетки HEK293-EBNA (линия клеток почки человеческого эмбриона 293, экспрессирующая ядерный антиген вируса Эпштейна-Барра; Американская коллекция типовых культур, депонирована под номером АТСС № CRL-10852, партия 959218), которые культивировали в среде DMEM (модифицированная по методу Дульбекко среда Игла, фирма Gibco), дополненной 10% FCS (фетальная телячья сыворотка, фирма Gibco) с ультранизким содержанием IgG (Ultra Low IgG FCS), 2 мМ L-глутамином (фирма Gibco) и 250 мкг/мл генетицина (фирма Gibco). Для трансфекции применяли реагент для трансфекции типа FuGENE™ 6 (фирма Roche Molecular Biochemicals), используя соотношение реагента FuGENE™ (мкл) и ДНК (мкг) 4:1 (диапазон от 3:1 до 6:1). Плазмиды, кодирующие легкую и тяжелую цепь НС* и LC* антитела <IGF-1R> (плазмиды DW047-pUC-HC*-IGF-1R и DW048-pUC-LC*-IGF-1R), и НС и LC антитела <ANGPT2> (плазмиды SB07-pUC-Hyg-OriP-HC-ANGPT2 и SB09-pUC-Hyg-OriP-LC-ANGPT2 или плазмиды SB04-pUC-HC-ANGPT2 и SB06-pUC-LC-ANGPT2 соответственно), экспрессировали, используя четыре различных плазмиды в молярном соотношении плазмид, кодирующих легкие и тяжелые цепи, составляющем 1:1 (эквимолярное соотношение). Клетки подпитывали в день 3 L-глутамином до концентрации 4 мМ, глюкозой (фирма Sigma) и NAA (фирма Gibco). Собранный супернатант, содержащий смесь основных продуктов, таких как А) антитело <IGF-1R>, несущее замену VL-VH/CL-CH1, Б) биспецифическое антитело <ANGPT2-IGF-1R>, несущее замену VL-VH/CL-CH1, и В) антитело <ANGPT2> дикого типа, обозначили как «смесь, содержащая биспецифическое антитело, несущее замену VL-VH/CL-CH1». Супернатанты клеточных культур, которые включали смесь, содержащую биспецифическое антитело, несущее замену VL-VH/CL-CH1, собирали в дни с 5 по 11 после трансфекции путем центрифугирования и хранили при -20°С.
Для сравнения антитело <IGF-1R> дикого типа кратковременно совместно экспрессировали с использованием кодирующих НС и LC плазмид (4842-pUC-LC-IGF-1R и 4843-pUC-HC-IGF-1R, пример 1А) в сочетании с антителом <ANGPT2> дикого типа с использованием кодирующих НС и LC плазмид (SB07-pUC-Hyg-OriP-HC-ANGPT2 и SB09-pUC-Hyg-OriP-LC-ANGPT2 или SB04-pUC-HC-ANGPT2 и SB06-pUC-LC-ANGPT2 соответственно). Клетки подпитывали в день 3 L-глутамином до концентрации 4 мМ, глюкозой (фирма Sigma) и NAA (фирма Gibco). Собранный супернатант, содержащий смесь различных вариантов антител дикого типа <IGF-1R> и <ANGPT2>, которые представляли собой либо моноспецифические, либо биспецифические, либо неспособные к связыванию варианты из-за неконтролируемой ассоциации легких цепей с обеими тяжелыми цепями из антител дикого типа <IGF-1R> и <ANGPT2>, что приводило к неправильной ассоциации легких цепей, обозначили как «смесь дикого типа». Супернатанты клеточных культур, которые включали смесь дикого типа, собирали в дни с 5 по 11 после трансфекции путем центрифугирования и хранили при -20°С.
Поскольку для антитела <ANGPT2> дикого типа обнаружен более высокий выход кратковременной экспрессии по сравнению с антителом <IGF-1R> дикого типа и антителом <IGF-1R>, несущим Fab, полученными в результате кроссинговера, то соотношение плазмид, кодирующих антитело <ANGPT2> дикого типа, и плазмид, кодирующих антитело <IGF-1R>, несущее замену VL-VH/CL-CH1, сдвигалось в сторону экспрессии антитела <ANGPT2> дикого типа. Соотношение плазмид следовало адаптировать в последующих экспериментах так, чтобы получать одинаковый уровень экспрессии обеих специфичностей и более равномерное распределение различных антител.
Пример 3Б
Иммунопреципитация биспецифического антитела <ANGPT2-IGF-1R>, несущего замену VL-VH/CL-CH1
Смесь, содержащую основные продукты, а именно А) моноспецифическое антитело <IGF-1R>, несущее замену VL-VH/CL-CH1, Б) биспецифическое антитело <ANGPT2-IGF-1R>, несущее замену VL-VH/CL-CH1, и В) антитело <ANGPT2> дикого типа («смесь, содержащая биспецифическое антитело, несущее замену VL-VH/CL-CH1»), выделяли из супернатантов клеточных культур (пример 3А) путем иммунопреципитации с использованием белок А-агарозных гранул (фирма Roche). 60 мкл белок А-агарозных гранул отмывали трижды в TBS-NP40 (50 мМ Трис, рН 7,5, 150 мМ NaCl, 1% Nonidet-P40). Затем 1-15 мл супернатанта клеточной культуры наносили на белок А-агарозные гранулы, предварительно уравновешенные в TBS-NP40. После инкубации в течение 1 ч при комнатной температуре гранулы отмывали на фильтрующей колонке типа Ultrafree-MC (фирма Amicon), используя однократно 0,5 мл TBS-NP40, дважды 0,5 мл двукратного (2×) забуференного фосфатом физиологического раствора (2×ЗФР, фирма Roche) и быстро четыре раза 0,5 мл 100 мМ Na-цитратного буфера, рН 5,0. Связанное антитело элюировали, добавляя 35 мкл буфера для образцов NuPAGE® LDS (фирма Invitrogen). Половину образца объединяли с восстановителем для образцов NuPAGE® или оставляли в невосстановленной форме соответственно и выдерживали в течение 10 мин при 70°С. Затем по 20 мкл применяли для осуществления ДСН-ПААГ с использованием 4-12% бис-Трис-гелей NuPAGE® (фирма Invitrogen) (применяя буфер MOPS для осуществлении ДСН-ПААГ в невосстанавливающих условиях и буфер MES в виде подвижного буфера с антиоксидантной добавкой NuPAGE® (фирма Invitrogen) для осуществлении ДСН-ПААГ в восстанавливающих условиях) и окрашивали кумасси бриллиантовым голубым. По данным ДСН-ПААГ для трех изученных видов антител никаких различий не обнаружено. Все антитела напоминали по своим характеристикам типичное антитело в виде IgG1, при этом легкая цепь присутствовала в полосе, которой соответствует молекулярная масса примерно 25 кДа, а тяжелая цепь присутствовала в полосе, которой соответствует молекулярная масса 50 кДа. При использовании невосстанавливающих условий может быть обнаружена полоса, которой соответствует молекулярная масса примерно 150 кДа, характерная для полного антитела. Поэтому для доказательства присутствия функционального биспецифического антитела <ANGPT2-IGF-1R>, несущего замену VL-VH/CL-СН1, полученную в результате кроссинговера, смесь трех видов антител очищали (пример 3В) и подвергали анализу с использованием клеточного FACS, позволяющего выявлять образование мостиковой связи (пример 3Г).
Пример 3В
Очистка биспецифического антитела <ANGPT2-IGF-1R>, несущего замену VL-VH/CL-CH1
Смесь, содержащую основные продукты, а именно А) моноспецифическое антитело <IGF-1R>, несущее замену VL-VH/CL-CH1, Б) биспецифическое антитело <ANGPT2-IGF-1R>, несущее замену VL-VH/CL-CH1, и В) антитело <ANGPT2> дикого типа («смесь, содержащая биспецифическое антитело, несущее замену VL-VH/CL-CH1»), описанную в примере 3А, очищали из профильтрованных супернатантов клеточной культуры с помощью аффинной хроматографии на белке А согласно известным стандартным методам. В целом, метод состоял в следующем: содержащие смесь антител супернатанты клеточных культур, полученные в результате кратковременных трансфекций плазмидами DW047-pUC-HC*-IGF-1R и DW048-pUC-LC*-IGF-1R и SB07-pUC-Hyg-OriP-HC-ANGPT2 и SB09-pUC-Hyg-OriP-LC-ANGPT2, осветляли центрифугированием (10000 g в течение 10 мин) и фильтровали через фильтр с размером пор 0,45 мкм и вносили на содержащую белок А колонку HiTrap MabSelect Xtra (фирма GE Healthcare), уравновешенную ЗФР-буфером (10 мМ Na2HPO4, 1 мМ KH2PO4, 137 мМ NaCl и 2,7 мМ KCl, рН 7,4). Несвязанные белки отмывали уравновешивающим ЗФР-буфером, а затем 0,1 М натрий-цитратным буфером, рН 5,5 и отмывали ЗФР. Для элюции биспецифического антитела <ANGPT2-IGF-1R>, несущего замену VL-VH/CL-CH1, применяли 100 мМ натрий-цитратый буфер, рН 2,8, после чего образцы немедленно нейтрализовали, добавляя 300 мкл 2М Трис, рН 9,0 на 2-миллилитровую фракцию. Агрегированный белок отделяли от мономерных антител с помощью гель-фильтрации на колонке HiLoad 26/60 Superdex 200 prep grade (фирма GE Healthcare) в 20 мМ гистидине, 150 мМ NaCl, рН 6,0, а фракцию мономерных антител затем концентрировали с помощью центрифужного концентратора MILLIPORE Amicon Ultra-15. Смесь, содержащую антитело, несущее замену VL-VH/CL-CH1, замораживали и хранили при -20°С или -80°С. Целостность видов антител анализировали с помощью ДСН-ПААГ (см. фиг.14) в присутствии восстановителя или без него и затем окрашивали кумасси бриллиантовым голубым согласно методу, описанному в примере 1Г. Входящие в смесь антитела напоминали по своим характеристикам типичные антитела в виде IgG1, при этом легкая цепь присутствовала в полосе, которой соответствует молекулярная масса примерно 25 кДа, а тяжелая цепь присутствовала в полосе, которой соответствует молекулярная масса 50 кДа. При использовании невосстанавливающих условий может быть обнаружена полоса, которой соответствует молекулярная масса примерно 150 кДа, характерная для полного антитела. С помощью ДСН-ПААГ после очистки на белке А не было обнаружено никаких заметных побочных продуктов, таких как одновалентные антитела и т.д. Агрегацию и олигомерное состояние биспецифического антитела <ANGPT2-IGF-1R>, несущего замену VL-VH/CL-CH1, исследовали с помощью аналитической гель-фильтрации и установлено, что очищенные виды антител находились в мономерном состоянии. Охарактеризованные образцы использовали для дальнейшего аналитического исследования белка и изучения функциональных характеристик. Для доказательства присутствия функционального биспецифического антитела <ANGPT2-IGF-1R>, несущего замену VL-VH/CL-CH1, смесь трех видов антител подвергали анализу с использованием клеточного FACS, позволяющего выявлять образование мостиковой связи (пример 3Г).
С целью сравнения смесь дикого типа, полученную в результате совместной экспрессии плазмид для НС- и LC-цепей антитела <IGF-1R> дикого типа (4842-pUC-LC-IGF-1R и 4843-pUC-HC-IGF-1R, пример 1А) в сочетании с плазмидами для НС- и LC-цепей антитела <ANGPT2> дикого типа (SB07-pUC-Hyg-OriP-HC-ANGPT2 и SB09-pUC-Hyg-OriP-LC-ANGPT2), очищали из профильтрованных супернатантов клеточной культуры с помощью аффинной хроматографии на белке А с последующей гель-фильтрацией согласно описанному выше методу.
Пример 3Г
Выявление функционального биспецифического антитела <ANGPT2-IGF-1R>, несущего замену VL-VH/CL-CH1, с помощью клеточного FACS-анализа, позволяющего выявлять образование мостиковой связи, с использованием экспрессирующих IGF-1R клеток линии I24
Для подтверждения присутствия функционального биспецифического антитела <ANGPT2-IGF-1R>, несущего замену VL-VH/CL-CH1, в смеси, которая содержала биспецифическое антитело, несущее замену VL-VH/CL-CH1, включающую следующие основные продукты: А) моноспецифическое антитело <IGF-1R>, несущее замену VL-VH/CL-CH1, Б) биспецифическое антитело <ANGPT2-IGF-1R>, несущее замену VL-VH/CL-CH1, и В) антитело <ANGPT2> дикого типа, полученной после кратковременной совместной экспрессии согласно методу, описанному в примере 3А, проводили клеточный FACS-анализ, позволяющий выявлять образование мостиковой связи такой как IGF-1R-ANGPT2, с использованием клеток линии I24 (NIH3T3-клетки, экспрессирующие рекомбинантный человеческий IGF-1R, фирма Roche). Принцип анализа показан на фиг.15. Биспецифическое антитело <ANGPT2-IGF-1R>, несущее замену VL-VH/CL-CH1, которое присутствовало в супернатанте (пример 3А) или в очищенной смеси антител (пример 3В) соответственно, обладало способностью связываться с IGF-1R на поверхности I24-клеток и одновременно с ANGPT2; и таким образом обладало способностью соединять мостиковой связью два его антигена-мишени с двумя противоположными Fab-фрагментами.
В целом, метод состоял в следующем: 5×105 клеток линии I24 на трубку, предназначенную для осуществления FACS, инкубировали либо с 50 мкл неразведенного супернатанта клеточной культуры, либо с 160 мкг/мл разведения общей очищенной смеси антител на льду в течение 1 ч. В первом случае клетки инкубировали с А) супернатантами клеточных культур, полученных после совместной экспрессии возникших в результате кроссинговера плазмид <IGF-1R> (DW047-pUC-HC*-IGF-1R и DW048-pUC-LC*-IGF-1R) и плазмид <ANGPT2> дикого типа (SB04-pUC-HC-ANGPT2> и SB06-pUC-LC-ANGPT2), которые обозначали как «смесь, содержащая биспецифическое антитело, несущее замену VL-VH/CL-CH1», или Б) супернатантами клеточных культур, полученных после совместной экспрессии плазмид <IGF-1R> дикого типа (4842-pUC-LC-IGF-1R и 4843-pUC-HC-IGF-1R) и плазмид <ANGPT2> дикого типа (SB04-pUC-HC-ANGPT2> и SB06-pUC-LC-ANGPT2), которые обозначали как «смесь дикого типа» (фиг.16). Во втором случае соответствующую очищенную смесь антител из смеси, содержащей биспецифическое антитело, несущее замену VL-VH/CL-CH1, или смесь из «смеси дикого типа» наносили на I24-клетки (пример 3В, фиг.17). Несвязанное антитело отмывали 4 мл охлажденного на льду ЗФР (фирма Gibco) + 2% FCS (фирма Gibco), клетки центрифугировали (5 мин при 400 g) и связанное биспецифическое антитело выявляли с помощью 50 мкл (2 мкг/мл) человеческого ангиопоэтина-2 (ANGPT2) (фирма R&D Systems) в течение 1 ч на льду. Затем несвязанный ангиопоэтин-2 (ANGPT2) отмывали однократно (фиг.16) или дважды (фиг.17), используя 4 мл охлажденного на льду ЗФР (фирма Gibco) + 2% FCS (фирма Gibco), клетки центрифугировали (5 мин при 400 g) и связанный ангиопоэтин-2 выявляли с помощью 50 мкл (5 мкг/мл) антитела <Ang-2> mIgG1-биотин (BAM0981, фирма R&D Systems) в течение 45 мин на льду; в альтернативном варианте клетки инкубировали с 50 мкл (5 мкг/мл) конъюгата mIgG1-биотин в качестве контроля изотипа (фирма R&D Systems). Несвязанное идентифицирующее антитело отмывали 4 мл охлажденного на льду ЗФР (фирма Gibco) + 2% FCS (фирма Gibco), клетки центрифугировали (5 мин при 400 g) и связанное идентифицирующее антитело выявляли с помощью 50 мкл конъюгата 1:400 стрептавидин-РЕ (SA-PE) (фирма Invitrogen/Zymed) в течение 45 мин на льду, защищая от действия света. Несвязанный конъюгат стрептавидин-РЕ отмывали 4 мл охлажденного на льду ЗФР + 2% FCS. Затем клетки центрифугировали (5 мин при 400 g), ресуспендировали в 300-500 мкл ЗФР и связанный конъюгат стрептавидин-РЕ оценивали количественно с помощью устройства FACSCalibur (фирма BD (FL2-канал, 10000 клеток на процесс). В эксперимент включали в качестве контролей антитела соответствующего изотипа для исключения любых неспецифических случаев связывания. Кроме того, в качестве контролей включали очищенные моноспецифические двухвалентные антитела в виде IgG1, такие как <IGF-1R> и <ANGPT2>.
На фиг.16 представлены результаты, полученные с помощью клеточного FACS-анализа, позволяющего выявлять образование мостиковой связи, с использованием I24-клеток, для осуществления которого применяли супернатанты клеточных культур; на фиг.17 представлены результаты, полученные с использованием очищенной смеси антител. В обоих случаях, когда применяли технологию VL-VH/CL-CH1-замены, инкубация с супернатантом или очищенным антителом из «смеси, содержащей биспецифическое антитело, несущее замену VL-VH/CL-CH1», которую получали после совместной экспрессии антитела, несущего замену VL-VH/CL-CH1, и антитела дикого типа, приводила к существенному сдвигу флуоресценции, что свидетельствует о присутствии функционального биспецифического антитела <ANGPT2-IGF-1R>, несущего замену VL-VH/CL-CH1, которое обладало способностью связываться одновременно с IGF-1R на поверхности I24-клеток и с ANGPT2; и таким образом обладало способностью соединять мостиковой связью два его антигена-мишени с двумя противоположными Fab-фрагментами. В отличие от этого и как было предсказано, в случае совместной экспрессии двух антител дикого типа, образовывалось лишь очень незначительное относительное количество функциональных биспецифических антител, что приводило лишь к незначительному сдвигу флуоресценции при FACS-анализе, позволяющем выявлять образование мостиковой связи, когда вносили супернатант клеточной культуры или очищенное антитело из «смеси дикого типа» после совместной экспрессии плазмид <IGF-1R> дикого типа и плазмид <ANGPT2> дикого типа, что свидетельствует о присутствии лишь небольшого относительного количества функционального биспецифического антитела <IGF-1R-ANGPT2> дикого типа.
Эти результаты свидетельствуют о том, что путем совместной экспрессии плазмид, несущих замену VL-VH/CL-CH1, которые кодируют антитело <IGF-1R>, и плазмид дикого типа, которые кодируют антитело <ANGPT2>, можно легко создавать функциональное биспецифическое антитело <ANGPT2-IGF-1R>, несущее замену VL-VH/CL-CH1, которое одновременно распознает две различные мишени. В противоположность этому совместная экспрессия двух плазмид дикого типа, кодирующих антитела <IGF-1R> и <ANGPT2>, приводит к высокой вариабельности образовавшихся антител и лишь к очень небольшому содержанию функционального биспецифического антитела <IGF-1R-ANGPT2> дикого типа.
Примеры 4
Создание двухвалентного биспецифического антитела <VEGF-ANGPT2>, несущего замену VL-VH/CL-CH1, с модифицированными СН3-доменами (технология «knobs-into-holes») (фиг.30)
Как видно из приведенного выше примера, совместная экспрессия плазмид, кодирующих антитела дикого типа, и плазмид, кодирующих антитела, несущие замену VL-VH/CL-CH1, приводила к созданию смеси, которая содержала биспецифическое антитело, несущее замену VL-VH/CL-CH1, включающей следующие основные продукты: А) моноспецифическое антитело несущее замену VL-VH/CL-CH1, Б) биспецифическое антитело, несущее замену VL-VH/CL-CH1, и В) антитело дикого типа. Для дополнительного повышения выхода биспецифического антитела <VEGF-ANGPT2>, несущего замену VL-VH/CL-CH1, применяли технологию «knobs-into-holes» для совместной экспрессии антитела <ANGPT2>, несущего замену VL-VH/CL-CH1, и антитела <VEGF> дикого типа с целью повышения гетеродимеризации соответствующих немодифицированных и модифицированных тяжелых цепей (с использованием НС и НС*) и получения более гомогенного и функционального препарата биспецифического антитела. В этом примере описано создание биспецифического антитела, распознающего одновременно VEGF и ANGPT2, на основе антитела <VEGF> дикого типа G6-31 и описанного выше МАт536, представляющего собой несущее замену VL-VH/CL-CH1 антитело <ANGPT2>.
Как описано выше, генные сегменты, кодирующие лидерную последовательность, вариабельный домен легкой цепи (VL) и константный домен легкой каппа-цепи (CL) антитела <ANGPT2>, сцепляли и сливали с 5'-концом Fc-доменов константных областей человеческой тяжелой γ1-цепи (шарнир-СН2-СН3). ДНК, кодирующую соответствующий слитый белок, полученный в результате замены VH- и СН1-доменов на VL- и CL-домены, создавали путем синтеза гена и обозначали далее как <ANGPT2> HC* (тяжелая цепь*) (SEQ ID NO:8).
Генные сегменты, кодирующую лидерную последовательность, вариабельный домен тяжелой цепи (VH) и константные домены (СН1) человеческой тяжелой γ1-цепи антитела <ANGPT2>, сцепляли в виде независимой цепи. ДНК, кодирующую соответствующий слитый белок, полученный в результате замены VL- и CL-доменов на VH- и СН1-домены, создавали путем синтеза генов и обозначили далее как <ANGPT2> LC* (легкая цепь*) (SEQ ID NO:9).
Последовательности вариабельных доменов тяжелой и легкой цепи моноспецифического двухвалентного антитела <VEGF> дикого типа, обозначенного как G6-31, включая соответствующие лидерные последовательности, которые описаны в этом примере, выводили из вариабельных доменов тяжелой цепи (SEQ ID NO:12), и вариабельных доменов легкой цепи (SEQ ID NO:13) человеческого антитела <VEGF>, такого как G6-31, они обе выведены из полученного с помощью фагового дисплея человеческого антитела к VEGF, такого как G6-31, которое подробно описано у Liang и др., J Biol Chem. 13, 281(2), январь 2006 г., cc.951-961 и в US 2007/0141065, а константные домены тяжелой и легкой цепи выводили из человеческого антитела (С-каппа и IgG1).
Для этой цели плазмиду, кодирующую тяжелую цепь антитела <VEGF> дикого типа G6-31, модифицировали путем интродукции генного сегмента СН3, созданного с помощью синтеза генов и кодирующего образующий «выступы» остаток T366W (SEQ ID NO:10), в СН3-домен соответствующей тяжелой цепи антитела <VEGF> дикого типа G6-31, получая последовательность, которая представлена в SEQ ID NO:16; в противоположность этому плазмиду, кодирующую тяжелую цепь* НС* несущего замену VL-VH/CL-CH1 антитела <ANGPT2> МАт536, модифицировали путем интродукции генного сегмента СН3, созданного с помощью синтеза генов и кодирующего образующие «впадину» остатки T366S, L368A, Y407V (SEQ ID NO:11), в СН3-домен соответствующей тяжелой цепи* НС* несущего замену VL-VH/CL-CH1 антитела <ANGPT2> МАт536, получая последовательность, которая представлена в SEQ ID NO:15. В этом случае плазмиды, кодирующие несущее «выступы» антитело <VEGF> дикого типа G6-31, создавали в виде геномных векторов, а плазмиды, кодирующие несущее замену VL-VH/CL-CH1 антитело <ANGPT2> МАт536, создавали в виде несущих интронА-кДНК векторов.
Затем соответствующие четыре плазмиды, которые кодируют тяжелую цепь НС с «выступами» (SEQ ID NO:16) антитела <VEGF> G6-31 и его легкую цепь дикого типа LC (SEQ ID NO:14), и модифицированную тяжелую цепь* НС* с «впадинами» несущего замену VL-VH/CL-CH1 антитела <ANGPT2> (SEQ ID NO:15) и его модифицированную легкую цепь* LC* (SEQ ID NO:8), совместно экспрессировали в эквимолярном соотношении путем кратковременных трансфекций системы HEK293-F согласно методу, описанному выше, в 2,6-литровом масштабе в ферментере типа Quad. Антитела очищали с помощью колонки HiTrap MabSelect (фирма GE), после чего подвергали гель-фильтрации на колонке HiLoad Superdex 200 26/60 (фирма GE) согласно описанному выше методу. Выход после SEC составлял примерно 38 мг очищенных фракций антител после кратковременной экспрессии в 2-литровом масштабе. На фиг.26 представлены данные, полученные с помощью ДСН-ПААГ в восстанавливающих и невосстанавливающих условиях, фракций, полученных после очистки с помощью гель-фильтрации. С помощью ДСН-ПААГ в восстанавливающих условиях можно продемонстрировать, что были синтезированы соответствующие дикого типа и модифицированные тяжелые и легкие цепи, и они очищены до гомогенного состояния. Однако при применении ДСН-ПААГ в невосстанавливающих условиях видно, что присутствует еще несколько видов антител.
Далее фракции, полученные с помощью гель-фильтрации, анализировали масс-спектрометрическим методом (либо дегликозилированные, но не восстановленные, либо дегликозилированные и восстановленные образцы). С помощью масс-спектрометрии во фракциях можно идентифицировать несколько видов антител и выявить соответствующие им полосы при применении соответствующего ДСН-ПААГ (фиг.27). Ниже в таблице представлены виды антител, которые можно идентифицировать:
Таким образом, требуемое биспецифическое антитело <VEGF-ANGPT2>, несущее замену VL-VH/CL-CH1, которое распознает, с одной стороны, VEGF, а с другой стороны, ANGPT2, можно точно идентифицировать с помощью масс-спектрометрии и можно выявлять также с помощью соответствующего ДСН-ПААГ. Схематическое изображение требуемого биспецифического антитела <VEGF-ANGPT2>, несущего замену VL-VH/CL-CH1, представлено на фиг.30. Наиболее высокую концентрацию указанного требуемого антитела можно обнаружить во фракциях 5 и 6, в выходящих позднее фракциях его концентрация снижалась.
Кроме того, присутствие биспецифического антитела <VEGF-ANGPT2>, несущего замену VL-VH/CL-CH1, которое обладало способностью одновременно связываться с ANGPT2 и VEGF, подтверждали с помощью описанного выше ELISA-анализа, который позволяет выявлять образование мостиковой связи (фиг.28) и описанного выше Biacore-анализа, который позволяет выявлять образование мостиковой связи (фиг.29), с помощью которых продемонстрировано, что требуемое биспецифическое антитело обладало способностью связываться одновременно с ANGPT2 и VEGF. В этих анализах четырехвалентное биспецифическое антитело TvG6-Ang23 служило в качестве контроля.
Следует отметить, что из-за относительно высокого уровня сверхэкспрессии антитела <VEGF> дикого типа, такого как G6-31, например, в результате более высокого выхода продуктов экспрессии при использовании геномных векторов, кодирующих производные G6-31, формирование неактивных побочных продуктов увеличивалось, приводя к избытку неактивных димеров G6-31 и состоящих из половинок антитела (полуантитела). Для достижения максимального выхода требуемого биспецифического антитела <VEGF-ANGPT2>, несущего замену VL-VH/CL-CH1, начаты дополнительные исследования, предназначенные для достижения однородной экспрессии всех четырех цепей антитела и снижения образования побочных продуктов. Эти исследования включают I) оптимизацию эквимолярной стехиометрии 4-х плазмид, которые применяют для совместной экспрессии, например, путем объединения транскрипционных единиц в одной или двух плазмидах с интродукцией соответствующих контролирующих элементов; а также II) оптимизацию гетеродимеризации, например, с использованием различных технологий «knobs-in-holes», таких как интродукция дисульфидного мостика в СН3-домен, например, Y349C в несущую «выступ» цепь и D356C в несущую «впадину» цепь и/или их объединение с применением остатков R409D; K370E (K409D) в качестве образующих «выступы» остатков и D399K; E357K в качестве образующих «впадину» остатков, которые описаны в ЕР 1870459А1.
| название | год | авторы | номер документа |
|---|---|---|---|
| ДВУХВАЛЕНТНЫЕ БИСПЕЦИФИЧЕСКИЕ АНТИТЕЛА | 2008 |
|
RU2575066C2 |
| ДВУХВАЛЕНТНЫЕ БИСПЕЦИФИЧЕСКИЕ АНТИТЕЛА | 2008 |
|
RU2587616C2 |
| ТРИ- ИЛИ ТЕТРАСПЕЦИФИЧЕСКИЕ АНТИТЕЛА | 2010 |
|
RU2570633C2 |
| СПОСОБ ПОЛУЧЕНИЯ МУЛЬТИСПЕЦИФИЧЕСКИХ АНТИТЕЛ | 2018 |
|
RU2750721C2 |
| СПОСОБ ПОЛУЧЕНИЯ МУЛЬТИСПЕЦИФИЧЕСКИХ АНТИТЕЛ | 2018 |
|
RU2780629C1 |
| АНТИГЕНСВЯЗЫВАЮЩИЕ БЕЛКИ | 2012 |
|
RU2607038C2 |
| БИСПЕЦИФИЧЕСКИЕ АНТИТЕЛА | 2011 |
|
RU2573588C2 |
| ПРЕДПОЧТИТЕЛЬНОЕ СПАРИВАНИЕ ДОМЕНОВ АНТИТЕЛ | 2018 |
|
RU2792440C2 |
| БИСПЕЦИФИЧЕСКИЕ АНТИГЕНСВЯЗЫВАЮЩИЕ БЕЛКИ | 2010 |
|
RU2573914C2 |
| ПОЛИСПЕЦИФИЧНЫЕ АНТИТЕЛА, ВКЛЮЧАЮЩИЕ АНТИТЕЛА ПОЛНОЙ ДЛИНЫ И ОДНОЦЕПОЧЕЧНЫЕ ФРАГМЕНТЫ FAB | 2010 |
|
RU2598248C2 |



































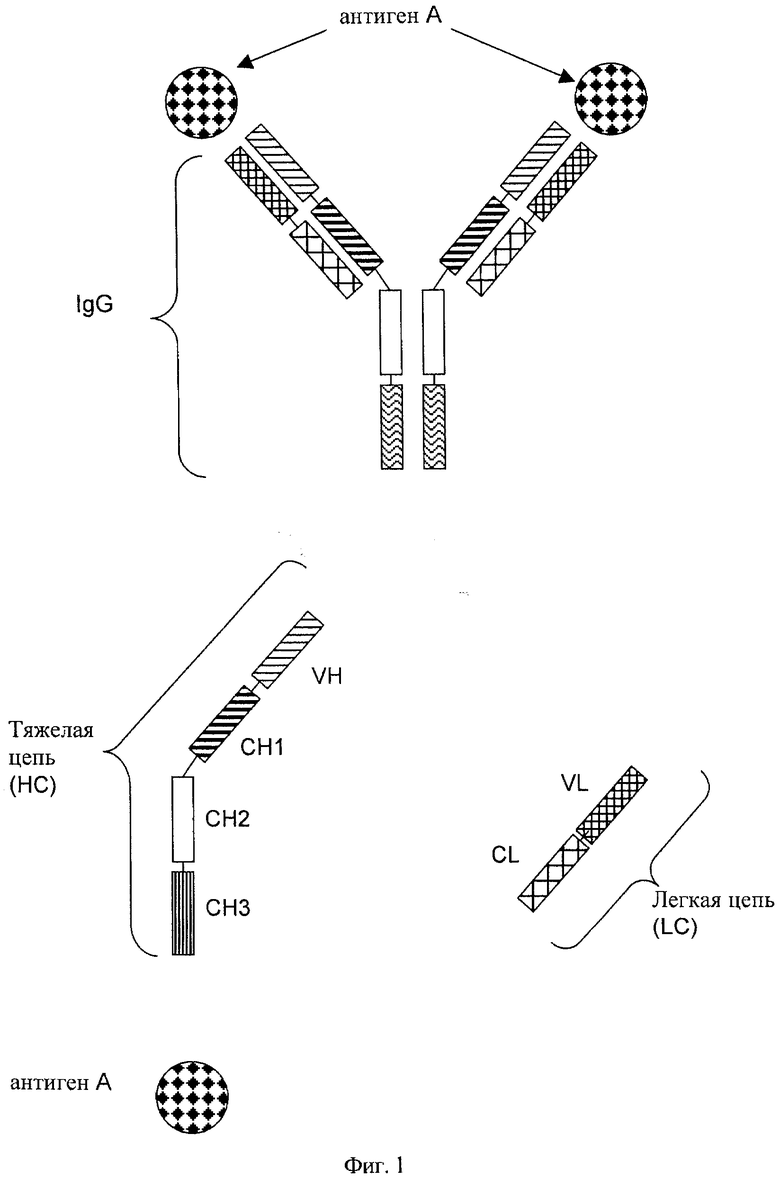
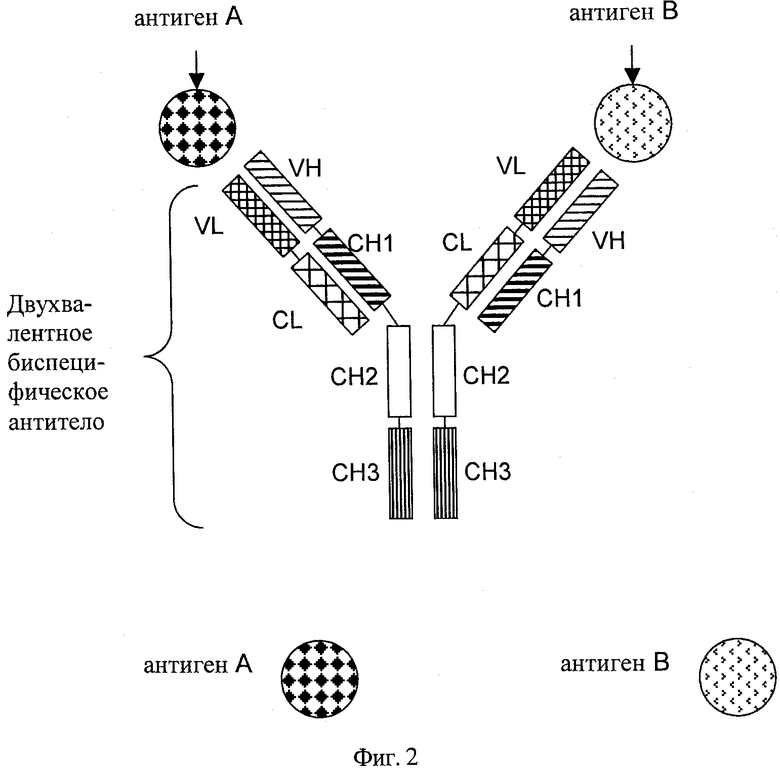
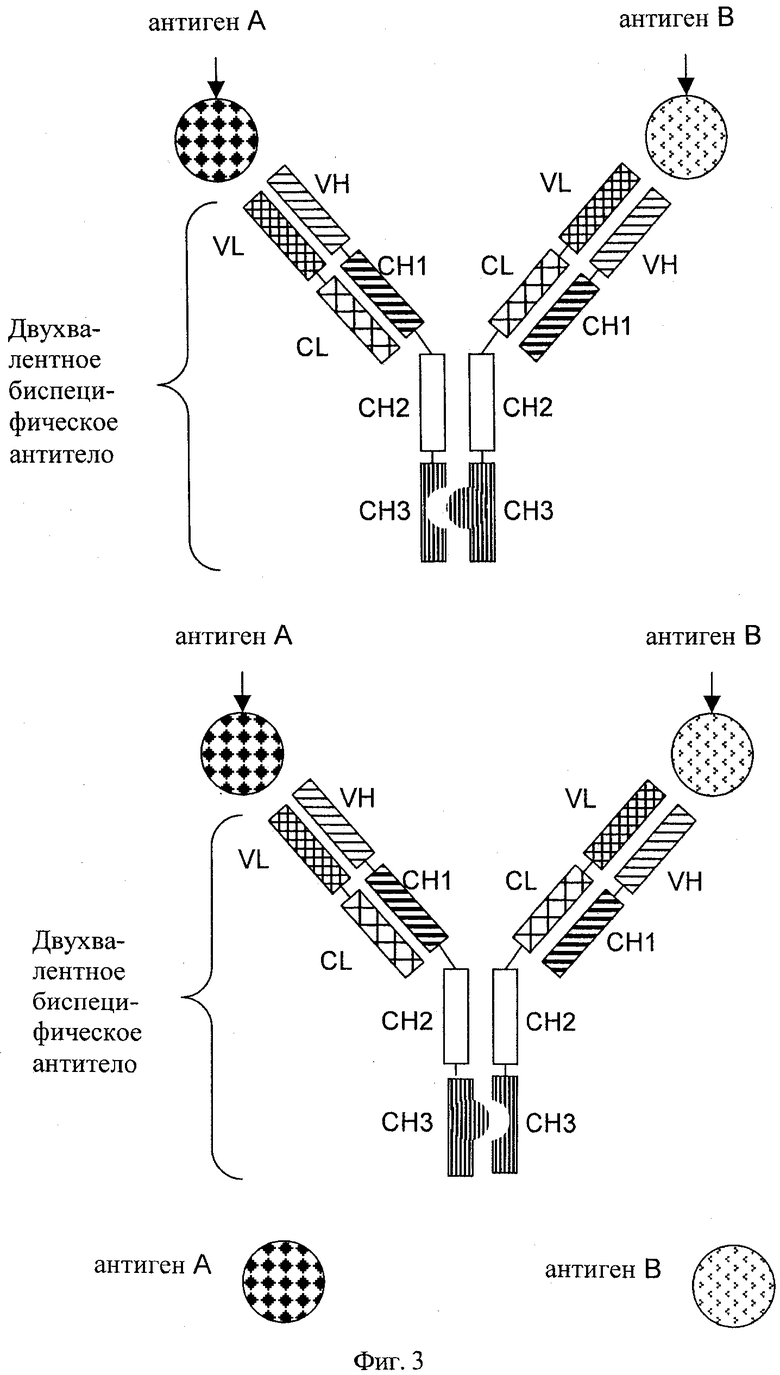
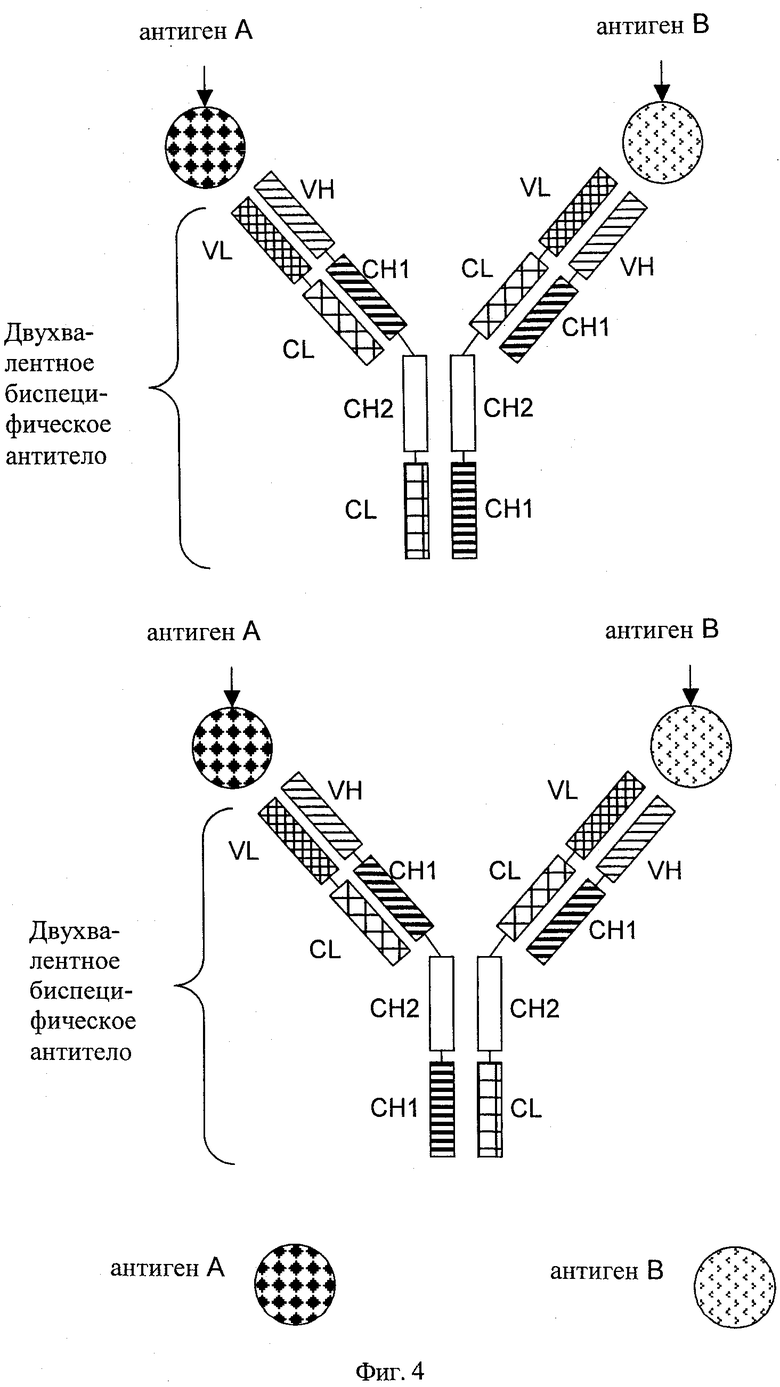
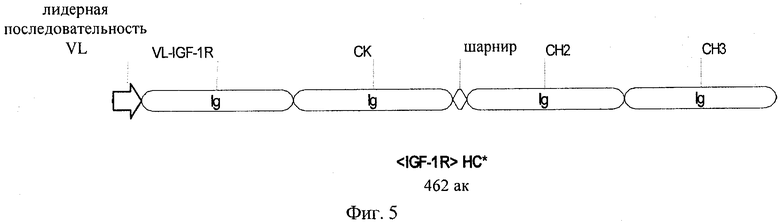
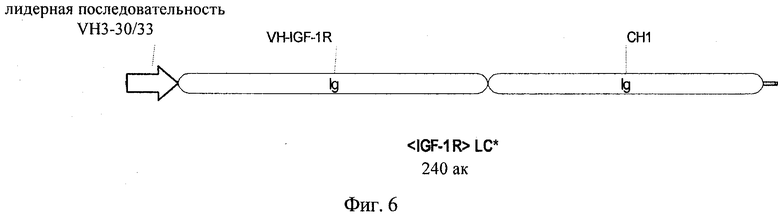
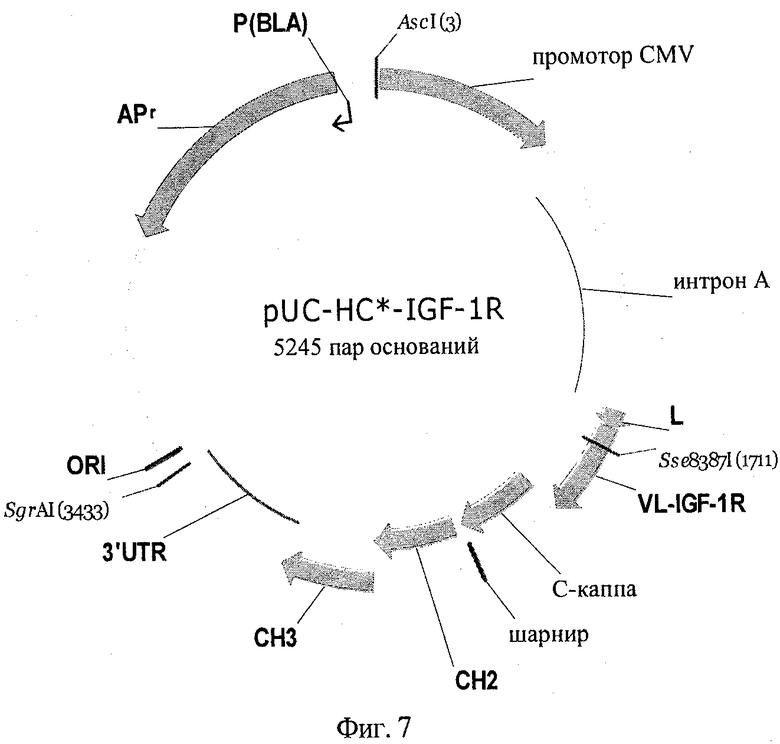
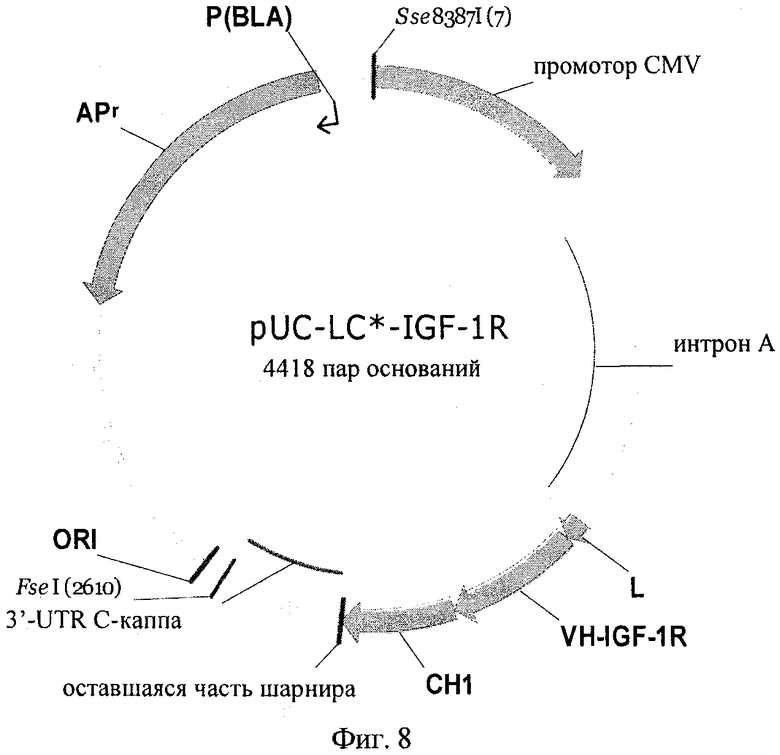
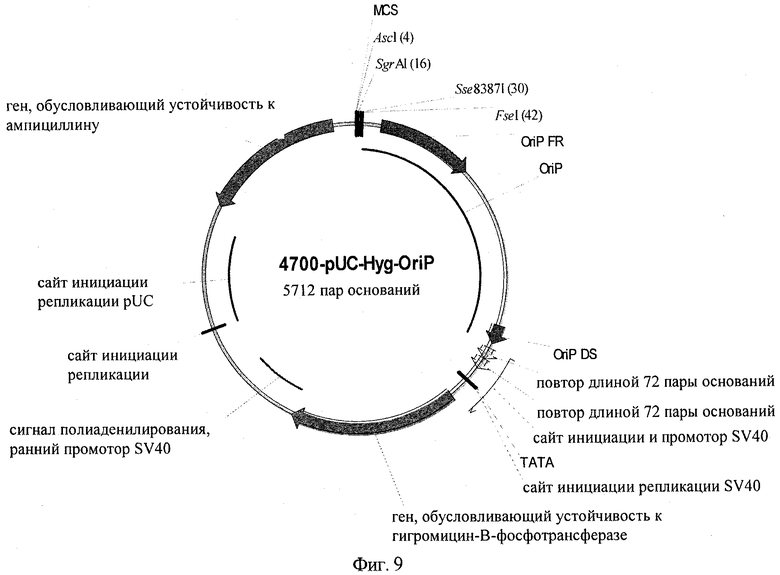
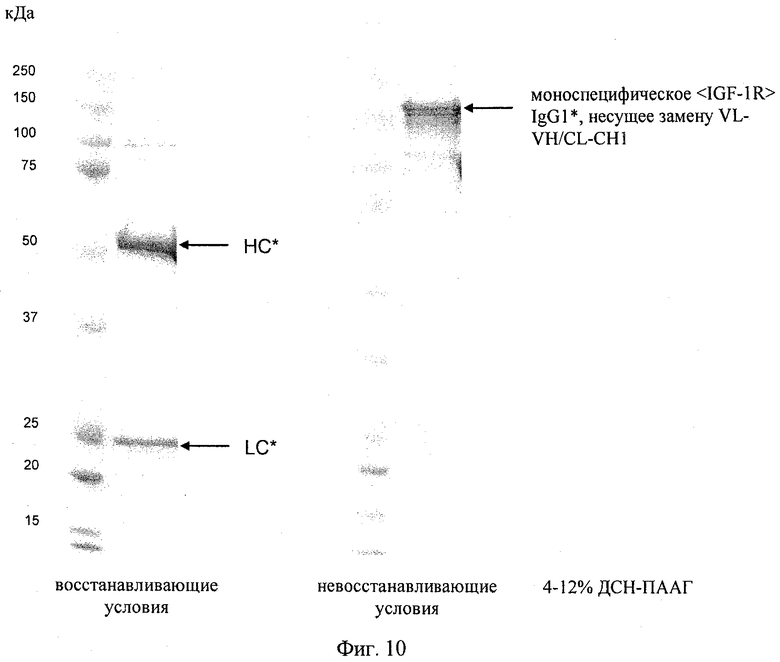
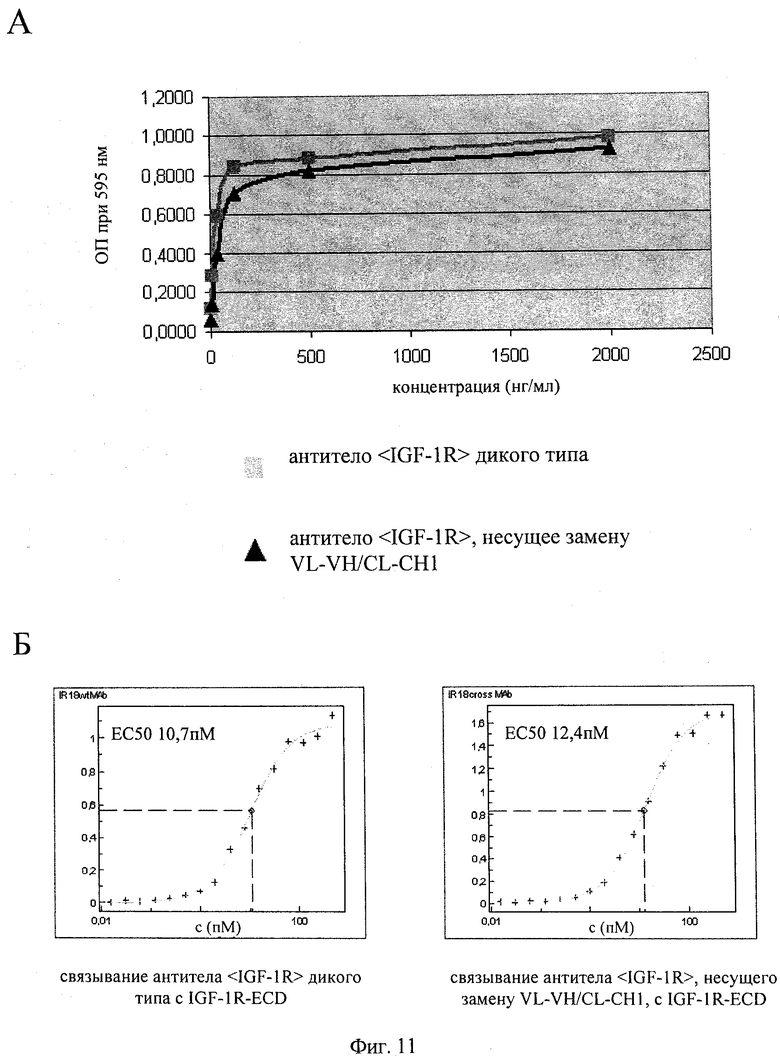
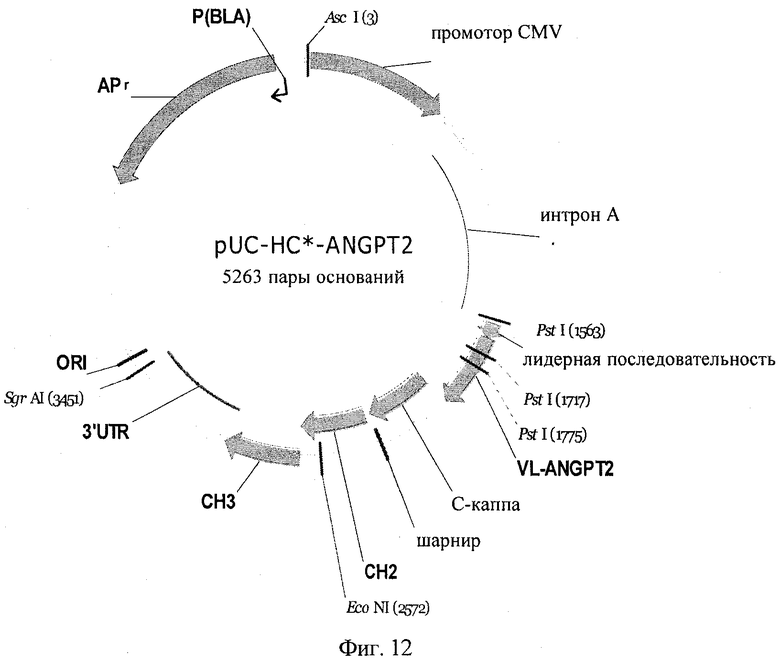
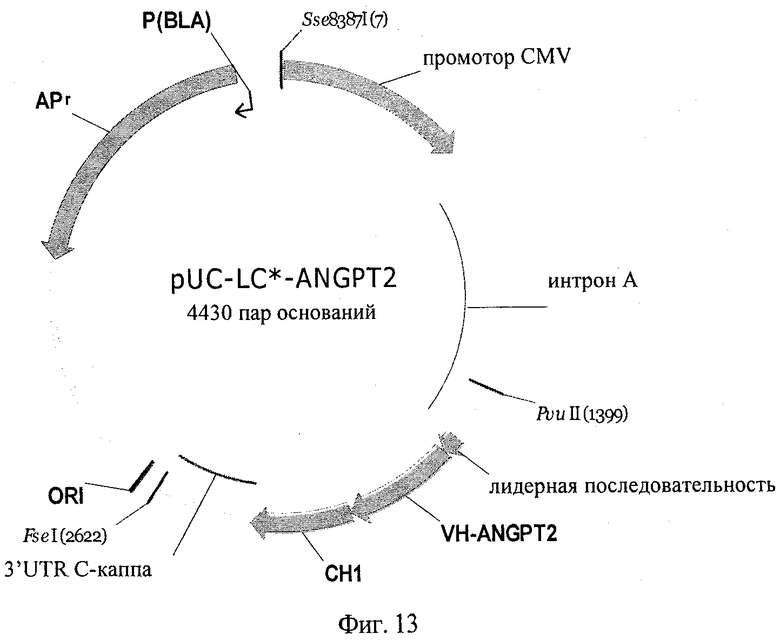
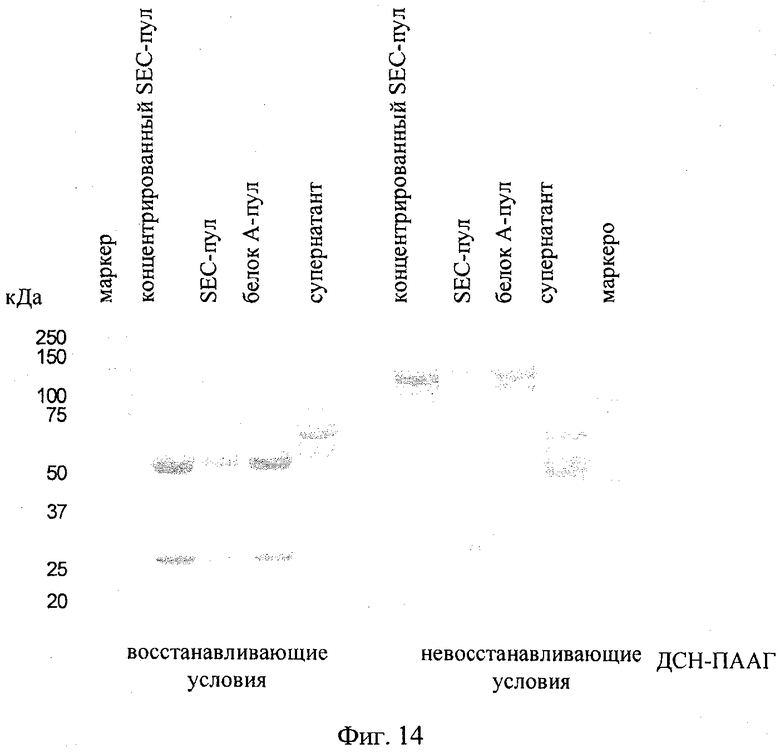
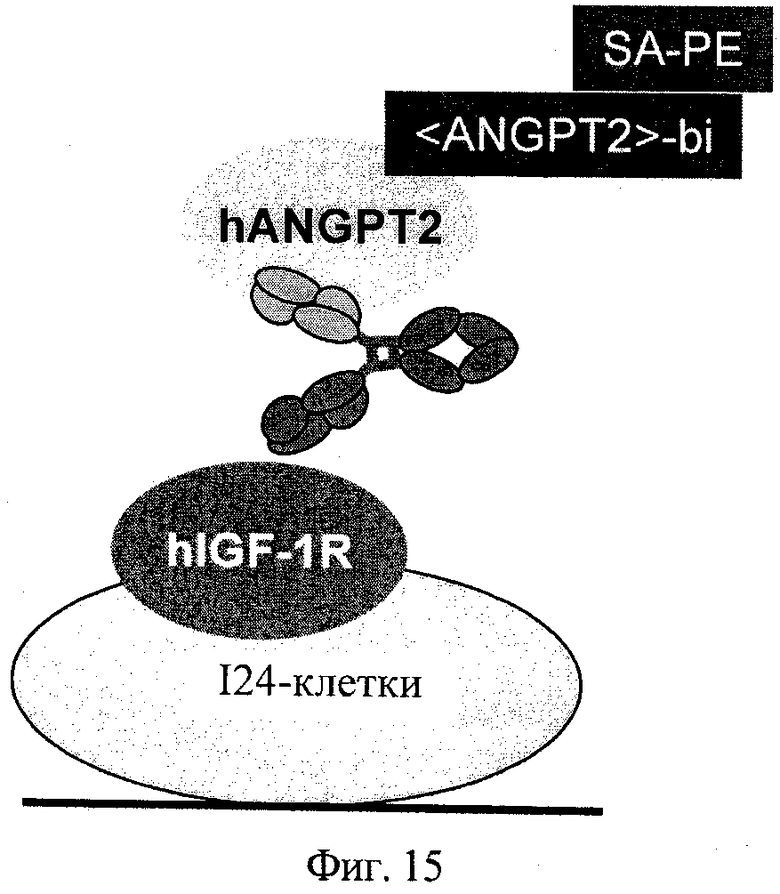
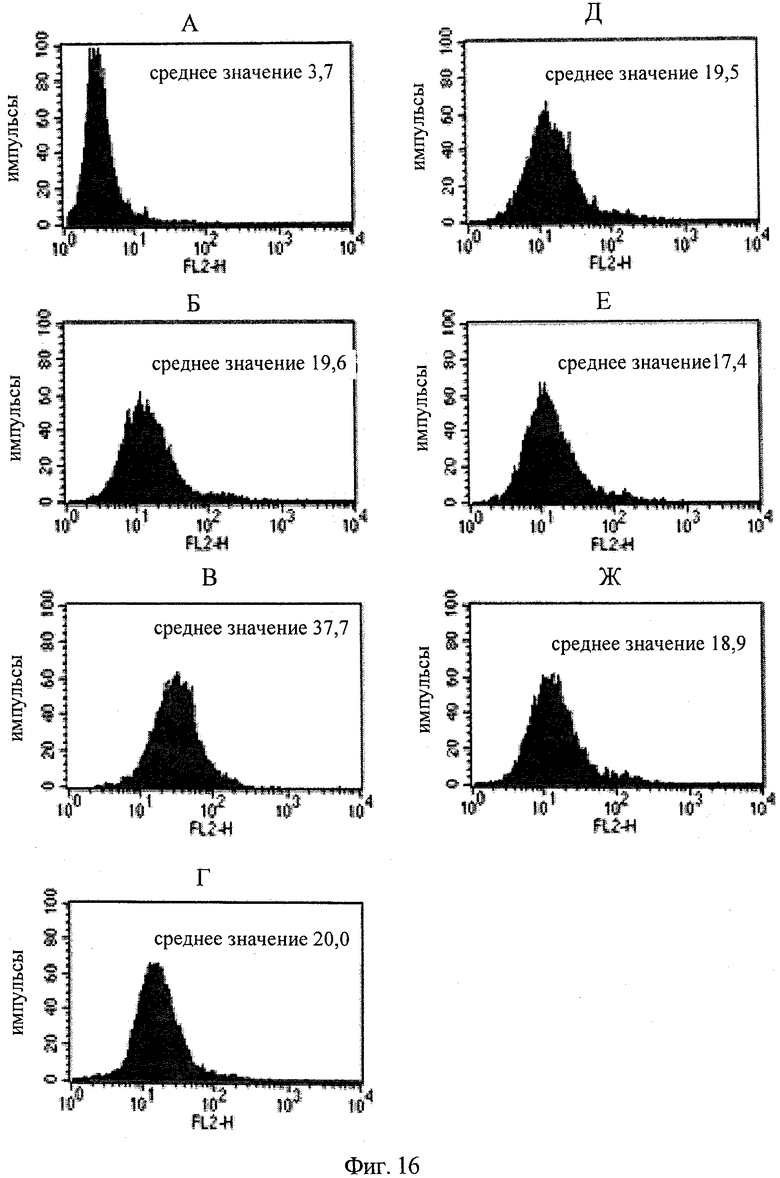
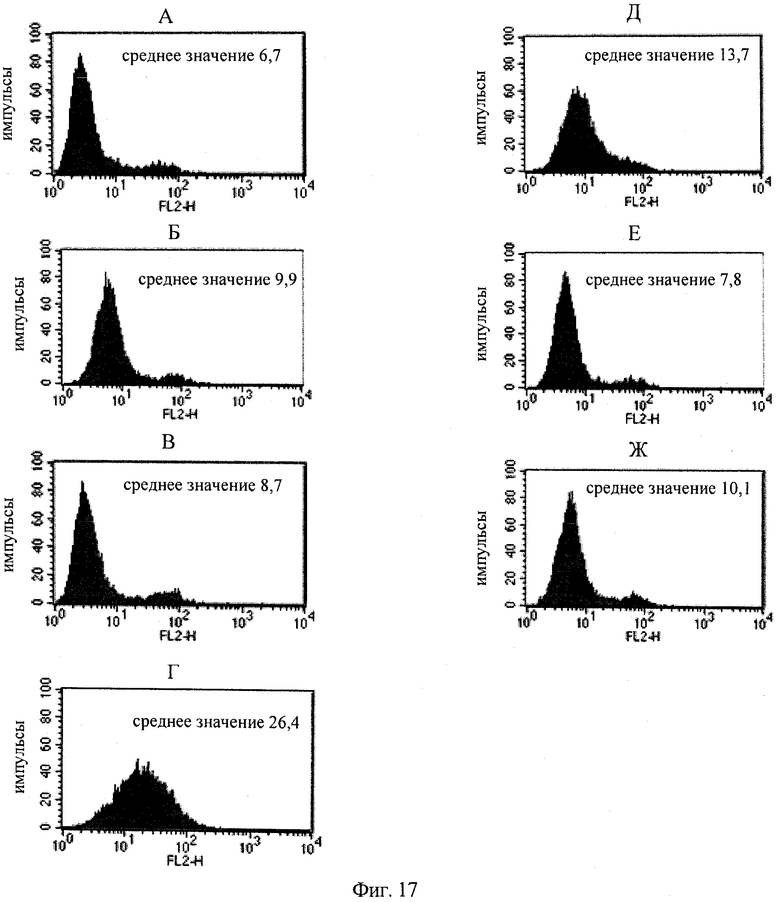
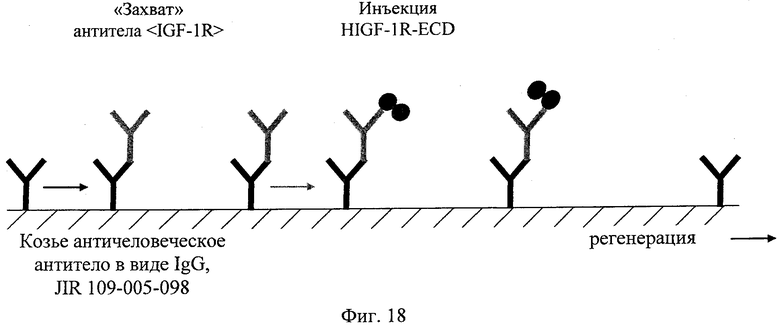
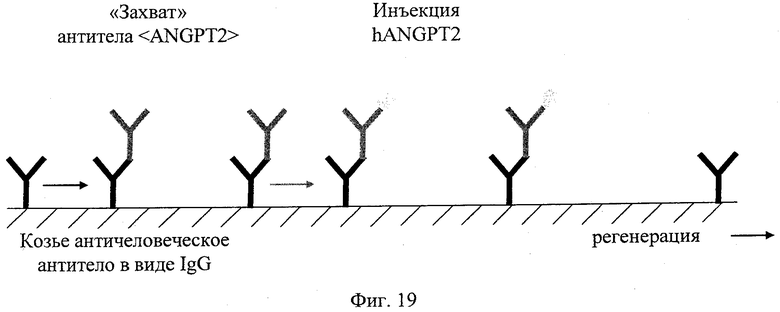
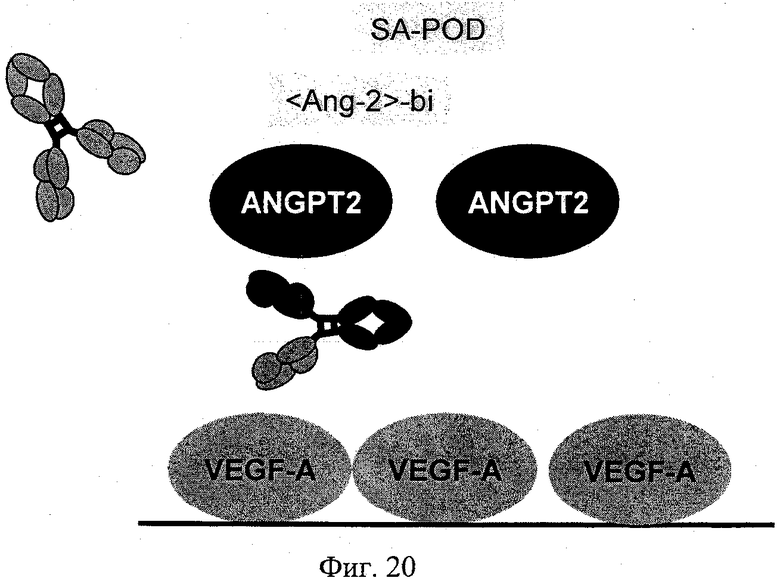
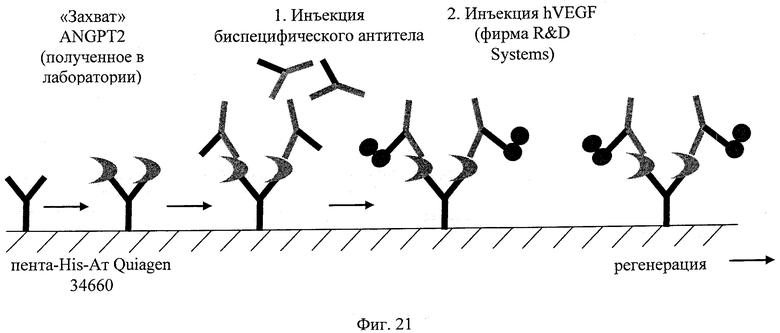
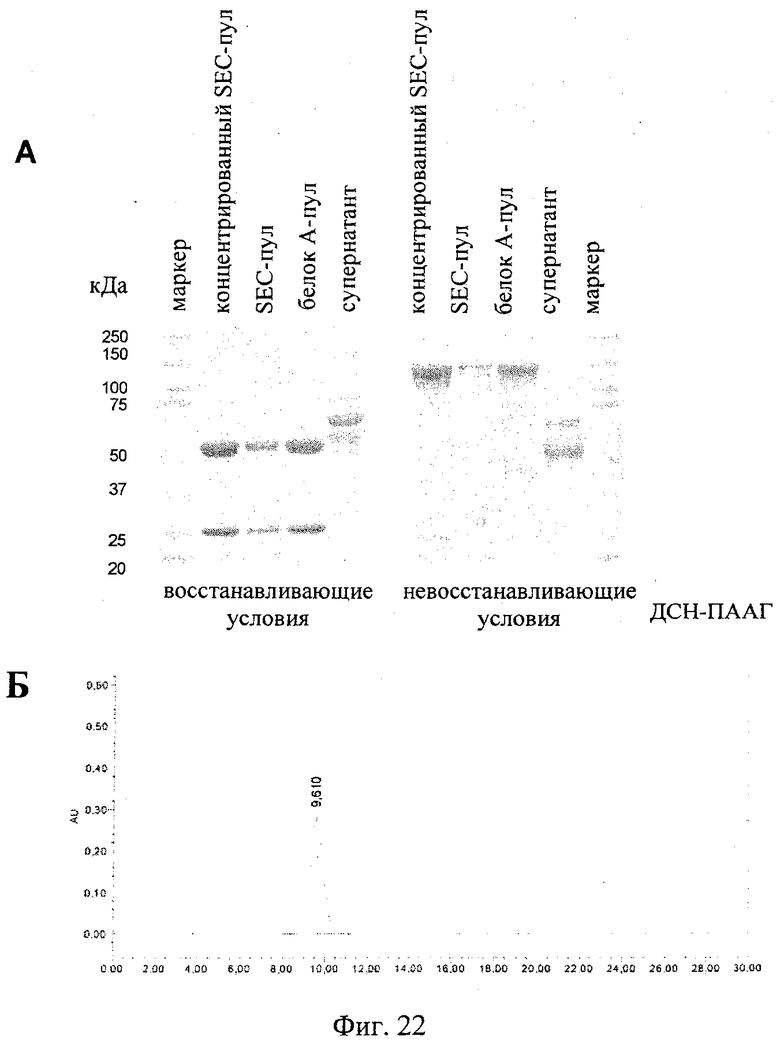
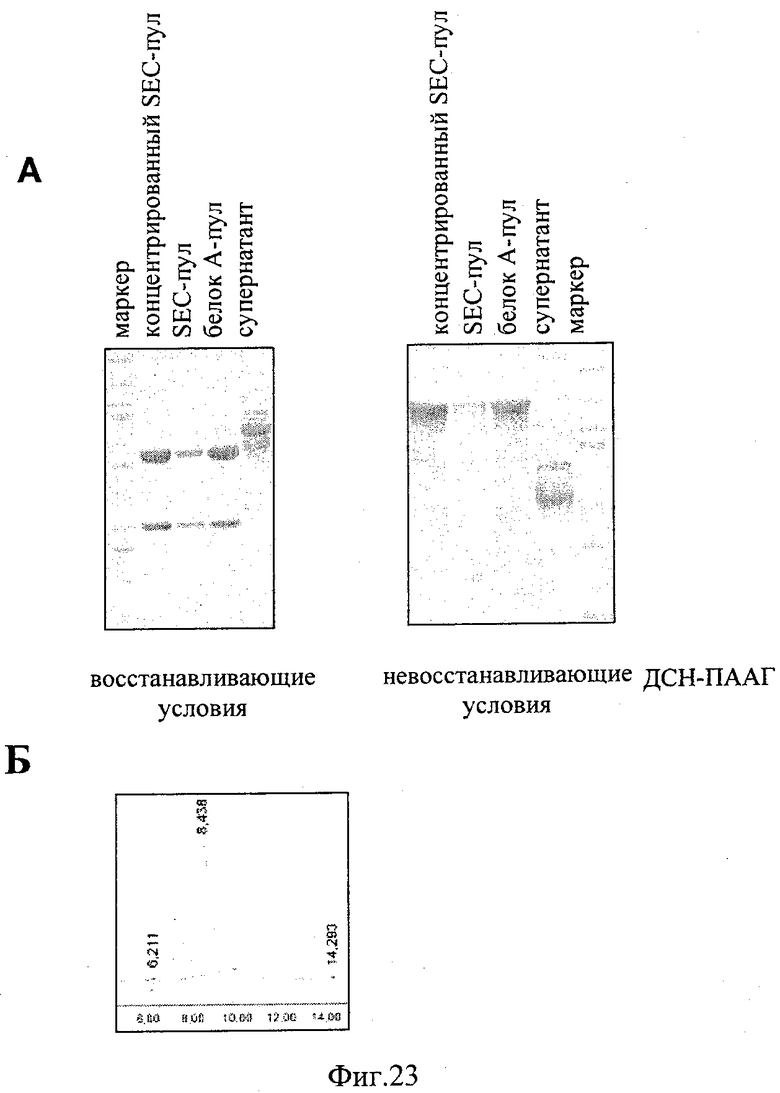
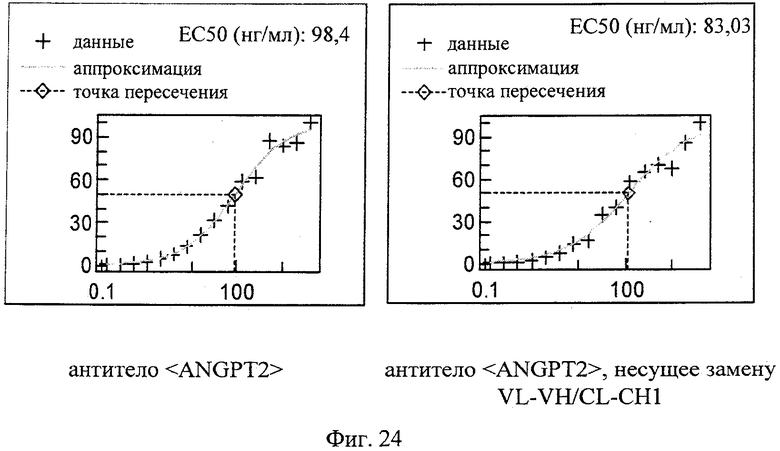
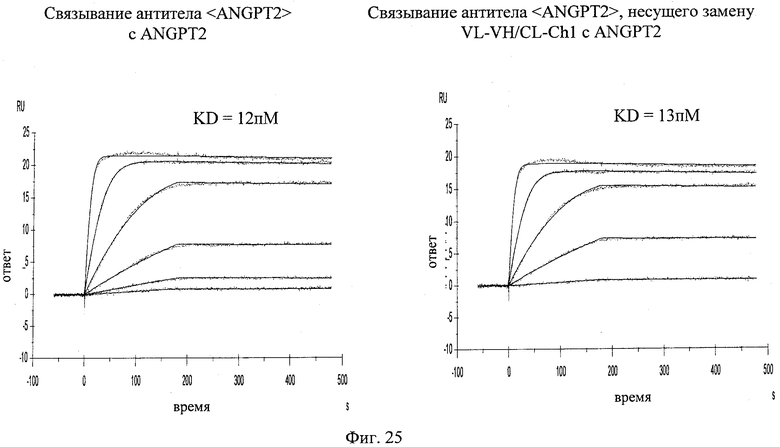
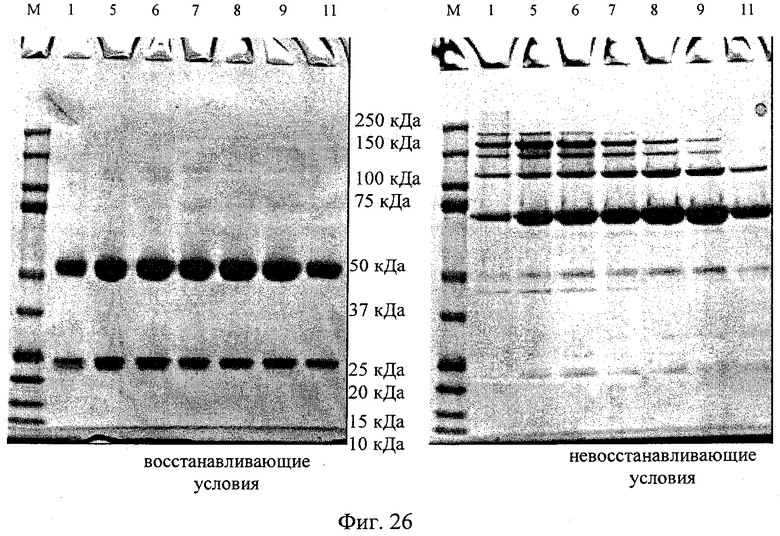
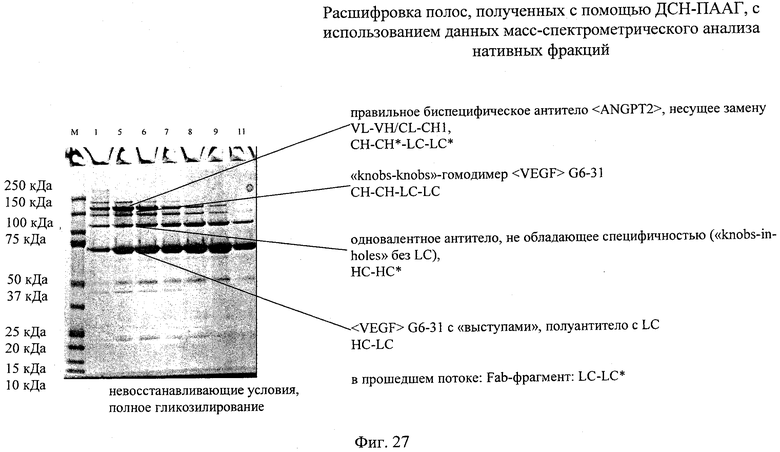
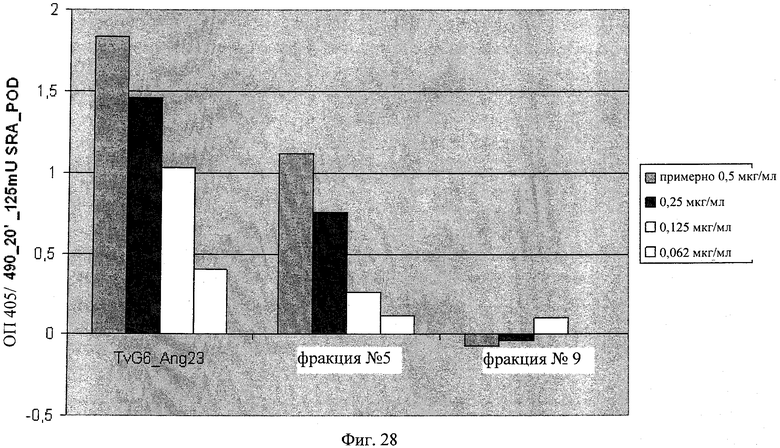
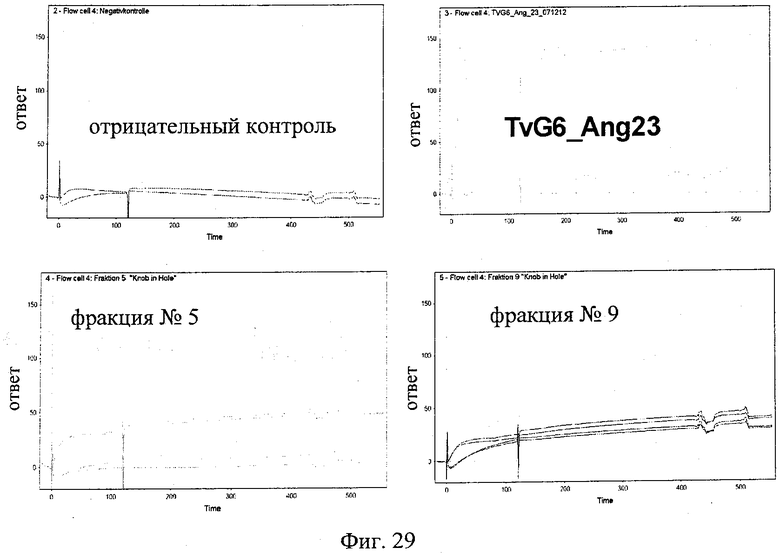
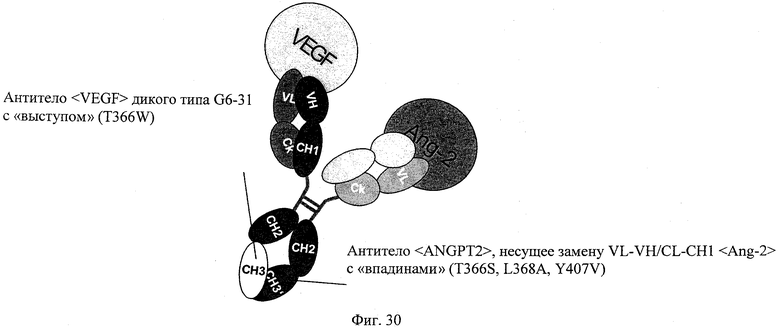
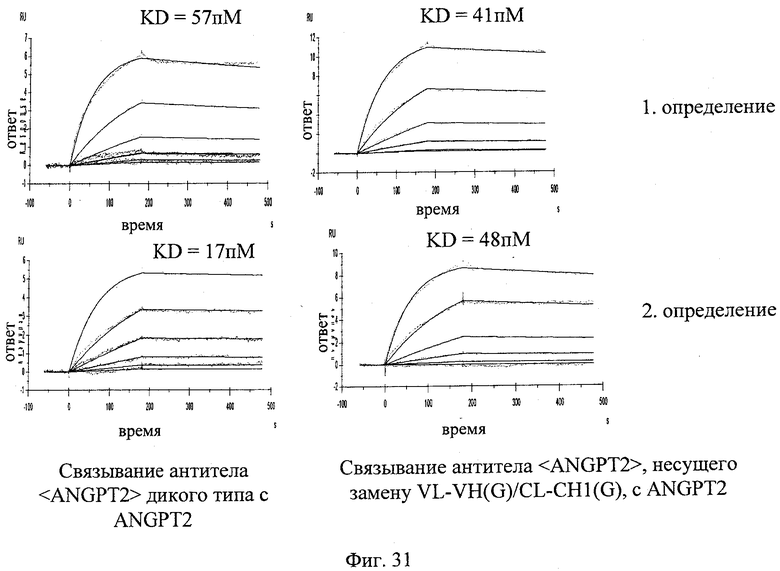
Изобретение относится к области биохимии, в частности к cпособу получения двухвалентного биспецифического антитела, который включает трансформацию клетки-хозяина векторами, содержащими молекулы нуклеиновых кислот, кодирующих первую легкую цепь и первую тяжелую цепь двухвалентного биспецифического антитела, и векторами, содержащими молекулы нуклеиновых кислот, кодирующих вторую легкую цепь и вторую тяжелую цепь двухвалентного биспецифического антитела, культивирование клетки-хозяина в условиях, которые обеспечивают синтез молекулы двухвалентного биспецифического антитела и выделение молекулы двухвалентного биспецифического антитела из указанной культуры. При этом указанное антитело содержит первую легкую цепь и первую тяжелую цепь антитела, специфически связывающегося с первым антигеном, и вторую легкую цепь и вторую тяжелую цепь антитела, специфически связывающегося со вторым антигеном, в котором вариабельные домены VL и VH второй легкой цепи и второй тяжелой цепи заменены друг на друга и константные домены CL и СН1 второй легкой цепи и второй тяжелой цепи заменены друг на друга. Изобретение позволяет повышать выход правильного биспецифического антитела путем увеличения уровня правильной гетеродимеризации тяжелых цепей дикого типа и модификацией полученных в результате кроссинговера тяжелых цепей. 1 з.п. ф-лы, 31 ил., 3 табл., 4 пр.
1. Способ получения двухвалентного биспецифического антитела, где антитело содержит:
а) первую легкую цепь и первую тяжелую цепь антитела, специфически связывающегося с первым антигеном; и
б) вторую легкую цепь и вторую тяжелую цепь антитела, специфически связывающегося со вторым антигеном,
в котором вариабельные домены VL и VH второй легкой цепи и второй тяжелой цепи заменены друг на друга и константные домены CL и СН1 второй легкой цепи и второй тяжелой цепи заменены друг на друга,
где СН3-домен одной тяжелой цепи и СН3-домен другой тяжелой цепи каждый соприкасается друг с другом на поверхности раздела, которая представляет собой исходную поверхность раздела между СН3-доменами антитела; при этом поверхность раздела изменена для активации формирования двухвалентного биспецифического антитела, где изменение отличается тем, что:
а) изменен СН3-домен одной тяжелой цепи
так, что на исходной поверхности раздела СН3-домена одной тяжелой цепи, которая соприкасается с исходной поверхностью раздела СН3-домена второй тяжелой цепи в двухвалентном биспецифическом антителе, аминокислотный остаток заменен на аминокислотный остаток, который имеет большую по объему боковую цепь, что приводит к созданию выпуклости на поверхности раздела СН3-домена одной тяжелой цепи, которая может помещаться в полость на поверхности раздела СН3-домена другой тяжелой цепи, и
б) изменен СН3-домен другой тяжелой цепи
так, что на исходной поверхности раздела второго СН3-домена, которая соприкасается с исходной поверхностью раздела первого СН3-домена в двухвалентном биспецифическом антителе, аминокислотный остаток заменен на аминокислотный остаток, который имеет меньшую по объему боковую цепь, что приводит к созданию полости на поверхности раздела второго СН3-домена, в которую может помещаться выпуклость на поверхности раздела первого СН3-домена, причем указанный аминокислотный остаток, который имеет большую по объему боковую цепь, выбран из группы, включающей аргинин (R), фенилаланин (F), тирозин (Y), триптофан (W), а указанный аминокислотный остаток, который имеет меньшую по объему боковую цепь, выбран из группы, включающей аланин (А), серин (S), треонин (Т), валин (V),
причем способ включает следующие этапы:
а) трансформация клетки-хозяина
- векторами, содержащими молекулы нуклеиновых кислот, кодирующих первую легкую цепь и первую тяжелую цепь двухвалентного биспецифического антитела;
- векторами, содержащими молекулы нуклеиновых кислот, кодирующих вторую легкую цепь и вторую тяжелую цепь двухвалентного биспецифического антитела,
б) культивирование клетки-хозяина в условиях, которые обеспечивают синтез молекулы двухвалентного биспецифического антитела;
в) выделение молекулы двухвалентного биспецифического антитела из указанной культуры.
2. Способ по п.1, отличающий тем, что оба СН3-домена антитела изменены путем интродукции цистеина (С) в качестве аминокислоты в соответствующие положения каждого СН3-домена, так что может быть сформирован дисульфидный мостик между обоими СН3 доменами.
| MERCHANT AM | |||
| et al., An efficient route to human bispecific IgG, Nat Biotechnol, 1998, v.16(7), pp | |||
| Замок с ключом фигурного сечения | 1914 |
|
SU677A1 |
| WO2006093794 A1, 08.09.2006 | |||
| WO9937791 A1, 29.07.1999 | |||
| XIE Z | |||
| et al., A new format of bispecific antibody: highly efficient heterodimerization, expression and tumor cell lysis, J Immunol Methods, 2005, v | |||
| ДЖИНО-ПРЯДИЛЬНАЯ МАШИНА | 1920 |
|
SU296A1 |
| Прибор для очистки паром от сажи дымогарных трубок в паровозных котлах | 1913 |
|
SU95A1 |
| RU94028282 А1, 20.07.1996 | |||
Авторы
Даты
2015-04-10—Публикация
2008-12-16—Подача