Сущность изобретения
Настоящее изобретение относится к новой библиотеке для получения мутеинов и к новым мутеинам, полученным из липокалина 2 человека (Lcn2, hNGAL), и близким белкам, которые связываются с определенной мишенью с обнаруживаемой аффинностью. Изобретение также относится к соответствующим молекулам нуклеиновой кислоты, кодирующим такой мутеин и способу их получения. Изобретение также относится к способу получения такого мутеина. Кроме того, изобретение относится к фармацевтической композиции, содержащей такой мутеин липокалина, а также к различным применениям мутеина.
Мутеины Lcn2 по настоящему изобретению демонстрируют возможность использования в качестве лекарственных и/или диагностических средств для некоторых заболеваний. Например, они могут использоваться для связывания и истощения патологических форм природных биологических молекул, таких как бета-амилоидный пептид при болезни Альцгеймера. В другом примере их можно использовать для специфической направленной доставки различных меток или токсинов к связанным с заболеванием клеточным поверхностным маркерам, таким как экстрадомен В фибронектина, который связан с неоваскуляризацией опухоли. За счет определенных положительных эффектов мутеинов Lcn2, которые можно получить по настоящему изобретению, возможны различные другие применения или примеры.
Уровень техники
Болезнь Альцгеймера (AD) является наиболее частой формой деменции у пожилых людей. Нарушенный процессинг предшественника амилоидного белка связан с AD, приводя к образованию потенциально нейротоксического белка, содержащего остатки 40-42 бета-амилоидного пептида (Aβ). Последующая агрегация Aβ в олигомеры и длинные фибриллы играет ключевую роль в развитии болезни, завершаясь образованием старческих бляшек (Haass and Selkoe, Nat. Rev. Mol. Cell Biol. (2007) 8, 101-112). Несмотря на возрастающее значение AD, по-прежнему имеется нерешенная потребность в эффективных лекарственных средствах для профилактики, лечения или замедления данной деменции.
Существующие в настоящее время подходы, направленные против амилоида, нацелены на: (i) профилактику образования Aβ; (ii) блокирование его агрегации; (iii) снижение уровня растворимого Aβ в мозге и (iv) разрушение имеющихся амилоидных бляшек. До настоящего времени иммунотерапия, включающая активную и пассивную иммунизацию пациентов с AD, была наиболее перспективной в данной области (Dodel et al. (2003) Lancet Neurology, 2, 215-220; Lichtlen and Mohajeri (2007) J. Neurochem., 104, 859-874; Brody and Holtzmann (2008) Annu. Rev. Neurosci., 31, 175-193). Однако недавние клинические испытания активной иммунизации пациентов с AD были приостановлены в результате повышенной частоты возникновения менингоэнцефалита у 6% пациентов. За счет этих возможных побочных эффектов Fc-опосредованных иммунологических функций, не связывающиеся с Ig соединения, такие как антикалины, обеспечивают альтернативу. Обнаружение молекулы аффитела со специфичностью к бета-амилоиду является одним примером потенциальных свойств инженерных белков, не связывающихся с Ig (Gronwall et al. (2007) J. Biotechnol., 128, 162-183; Hoyer et al. (2008) Proc. Natl. Acad. Sci. USA, 105, 5099-5104).
Однако бактериальная природа аффител может быть нежелательна в связи с иммуногенностью у пациента-человека.
Фибронектин (FN) играет важную роль в адгезии, миграции, пролиферации и дифференцировке клеток. FN представляет собой крупный, модульный, димерный гликопротеин, содержащий многочисленные домены типа I, II и III. Альтернативные сплайсированные варианты FN, такие как его экстрадомен В (ED-B), который находится между доменами FNIII7 и FNIII8, экспрессируются со специфичным для ткани и стадии развития характером (Zardi et al. (1987) EMBO J., 6, 2337-2342).
ED-B отсутствует в тканях здоровых взрослых людей, за исключением заживления ран и неопластической васкуляризации. Следовательно, ED-B-содержащий фибронектин экспрессируется на высоком уровне во многих типах опухолей, в которых происходит неоваскуляризация и проходит аномальный ангиогенез. Несмотря на то, что фактическая биологическая роль ED-B в ангиогенезе остается неясной, его присутствие в FN служит превосходным маркером опухолегенеза. В целом, отличие между злокачественными тканями и здоровыми органами является преимущественной терапевтической стратегией избирательной направленной доставки лекарственных препаратов непосредственно в опухолевую ткань, что приводит к повышенной местной концентрации препарата.
Для специфического обнаружения и направленной доставки к ED-B были получены рекомбинантные фрагменты антител с использованием технологии фагового дисплея антител. Одни фрагменты выделенных антител представляют одноцепочечные Fv L19 (Carnemolla et al. (1996) Int. J. Cancer, 68, 397-405; Ebbinghaus et al. (2004) Curr. Pharm. Des., 10, 1537-1549). В настоящее время направление L19 к ED-B в комбинации с эффективным цитотоксическим препаратом является перспективной возможностью для лечения и диагностики рака (Schliemann and Neri (2007) Biochim. Biophys. Acta, 1776, 175-192; Kaspar et al. (2006) Int. J. Cancer, 118, 1331-1339).
Однако фрагмент scFv L19 склонен к олигомеризации.
В результате вышеуказанных существующих проблем для лечения болезни Альцгеймера и диагностики или терапии опухолей целью настоящего изобретения является обеспечение способов и соединений, которые можно использовать для лечения болезни Альцгеймера, а также в диагностике и терапии опухолей.
Подробное описание изобретения
Заявители обнаружили, что специфические мутеины белков, полученные из липокалина 2, являются привлекающими внимание соединениями за счет их более высокой стабильности и меньшего размера. Заявители идентифицировали определенную группу мутеинов липокалина 2 с мутациями в определенных положениях, которые обладают высокой аффинностью и специфичностью, например, к ED-B. Такие мутеины Lcn2 специфически распознают фибронектин, содержащий ED-B, на клетках человека с высокой чувствительностью и, таким образом, являются перспективными для применения в качестве лекарственных средств для диагностики и лечения опухолевых заболеваний.
Заявители также смогли идентифицировать определенные мутеины Lcn2c с высокой аффинностью и специфичностью для Aβ пептида. Такие мутеины Lcn2 могут даже ингибировать агрегацию Aβ и, таким образом, являются перспективными, возможно после дальнейшего усовершенствования и модификации, в качестве лекарственных средств для лечения AD.
Кроме того, настоящее изобретение также относится к новым рандомизированным библиотекам, основанным на скэффолде Lcn2 человека, которые позволят эффективно получать мутеины, такие как мутеины по настоящему изобретению, с высокой аффинностью и специфичностью для определенной мишени в общем. Примеры таких библиотек или их разделов показаны на фигурах 1 и 2.
В одном из аспектов, по меньшей мере в 1, 2, 3, 4, 5, 6, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 нуклеотидных триплетах, кодирующих любое из положений последовательности 36, 40, 41, 49, 52, 68, 70, 72, 73, 77, 79, 81, 96, 100, 103, 106, 125, 127, 132 и 134 линейной полипептидной последовательности hLcn2, проводили случайный мутагенез заменой в данных положениях группой нуклеотидных триплетов. Группа нуклеотидных триплетов может относиться, не ограничиваясь этим, (a) к менее чем 64 возможным триплетам, кодированных нуклеотидами NNN (если N=A, T, G, C, что означает 4×4×4=64 возможных триплетов), (b) к менее чем 32 возможным триплетам, кодированных нуклеотидами NNK или NNS, (с) к менее чем необходимым триплетам для кодирования всех 20 природных протеиногенных аминокислот. В еще одном варианте осуществления нуклеотидные триплеты, кодирующие цистеин, не используются для замены во время мутагенеза. Это означает, что мутагенез не приводит к образованию мутеинов, содержащих новые цистеины, помимо тех цистеинов, которые уже входили в исходную, не мутагенизированную последовательность. Таким образом, в данном аспекте определяется, каким образом нуклеотидные триплеты выглядят, когда не введены в положения, которые подвергаются мутагенезу, как определено в данном разделе (см. пример 1 и фигуру 2).
Таким образом, в первом аспекте настоящее изобретение относится к способу получения мутеина, полученного из липокалина 2 человека (Lcn2; также известного как липокалин, связанный с желатиназой нейтрофилов, hNGAL, или как сидерокалин). Мутеины, полученные с использованием этого способа, могут связываться с неприродной мишенью с обнаруживаемой аффинностью. Способ включает проведение мутагенеза молекулы нуклеиновой кислоты, кодирующей липокалин 2 (Lcn2, hNGAL) человека, в нуклеотидном триплете, кодирующем по меньшей мере одно из положений в последовательности, соответствующих положениям 96, 100 и 106 линейной последовательности полипептида липокалина 2 человека, с получением одной или более молекул нуклеиновой кислоты мутеинов.
Согласно вышеуказанному термин «липокалин 2 человека» или «липокалин, связанный с желатиназой нейтрофилов (hNGAL)» включает структурные гомологи, уже идентифицированные или которые будут выделены, от других видов, которые обладают гомологией аминокислотных последовательностей или идентичностью последовательностей более чем примерно на 60%. Предпочтительно, чтобы данные липокалины человека, описанные выше, содержали 1, 2, 3, 4, 5, 6, 8, 9, 10, 11, 12, 13, 14, 15, 16 или 17 мутированных аминокислотных остатков в любом из положений последовательности, соответствующих положениям последовательности 33, 36, 40, 41, 42, 43, 44, 46, 47, 48, 49, 50, 51, 52, 54, 55, 59, 65, 68, 70, 72, 73, 75, 77, 78, 79, 80, 81, 86, 87, 98, 96, 99, 100, 103, 106, 107, 110, 111, 125, 127, 132, 134, 136 и 138 линейной полипептидной последовательности hNGAL. В том смысле, в котором в настоящем документе используется термин «гомология» в его обычном понимании, то он включает идентичные аминокислоты, а также аминокислоты, которые относятся к консервативным заменам (например, замене остатка глютамина на остаток аспартата) в эквивалентных положениях в линейной аминокислотной последовательности двух белков, которые сравниваются друг с другом. В том смысле, в котором в настоящем изобретении используется термин «идентичность последовательностей» или «идентичность», он означает процент парных идентичных остатков - после выравнивания по гомологии последовательности полипептида по настоящему изобретению с интересующей последовательностью - по числу остатков в более длинной из данных двух последовательностей.
Процент гомологии последовательностей или идентичность последовательностей определяется в настоящем документе с использованием программы BLASTP, версия blastp 2.2.5 (16 ноября, 2002; см. Altschul S.F. et al. (1997) Nucl. Acids Res., 25, 3389-3402). Процент гомологии основан на выравнивании полных полипептидных последовательностей (матрица: BLOSUM 62; цены гэпов: 11,1; значение порога установлено на 10-3), включая пропептидные последовательности с использованием липокалина 2 человека в качестве стандарта при парном сравнении. Ее рассчитывают в виде процента числа «позитивов» (гомологичных аминокислот), указанных результатом программы BLASTP, деленное на общее число аминокислот, выбранных программой при выравнивании. В данной связи следует отметить, что общее число выбранных аминокислот может отличаться от длины липокалина 2 человека.
В случае иного белка, чем липокалин 2 человека, используемого в настоящем изобретении, определение мутированных положений последовательности, данное для липокалина 2 человека, можно отнести к другому липокалину с помощью опубликованных выравниваний последовательностей или способов выравнивания, известных специалистам в данной области. Выравнивание последовательностей можно проводить, например, как описано в международной заявке WO 99/16873 (см. фигуру 3 в настоящем документе) с использованием опубликованного выравнивания, такого как приведено на фигуре 1 у Redl. B. (2000) Biochim. Biophys. Acta, 1482, 241-248. Если имеется трехмерная структура липокалинов, то можно использовать структурное наложение для определения положений последовательности, которые должны подвергнуться мутагенезу в настоящем изобретении. Также для данной цели можно использовать другие способы структурного анализа, такие как мультимерная магнитно-резонансная спектроскопия.
Гомолог липокалина 2 человека может также представлять собой белок-мутеин самого липокалина 2 человека, в котором аминокислотные замены вводят в положения, иные чем положения, выбранные в настоящем изобретении. Например, такой мутеин может представлять белок, в котором мутированы положения в подвергаемых воздействию растворителя β-складках, по сравнению с последовательностью дикого типа липокалина 2 человека для повышения растворимости или стабильности белка.
В общем, термин «липокалин 2 человека» включает все белки, обладающие гомологией последовательностей или идентичностью последовательностей более чем на 60, 70, 80, 85, 90 или 95% по отношению к липокалину 2 человека. Предпочтительно, чтобы данные липокалины человека, описанные выше, содержали 1, 2, 3, 4, 5, 6, 8, 9, 10, 11, 12, 13, 14, 15, 16 или 17 мутированных аминокислотных остатков в любом из положений последовательности, соответствующих положениям последовательности 33, 36, 40, 41, 42, 43, 44, 46, 47, 48, 49, 50, 51, 52, 54, 55, 59, 65, 68, 70, 72, 73, 75, 77, 78, 79, 80, 81, 86, 87, 98, 96, 99, 100, 103, 106, 107, 110, 111, 125, 127, 132, 134, 136 и 138 линейной полипептидной последовательности hNGAL.
Таким образом, в дополнительном аспекте настоящее изобретение относится к мутеину, полученному из липокалина 2 человека (т.е. мутеину липокалина человека или мутированному липокалину человека, предпочтительно, мутированному зрелому hNGAL, где указанный зрелый hNGAL имеет инвентарный номер P80188 в SWISS-PROT Data Bank, более предпочтительно, указанный зрелый hNGAL имеет аминокислотную последовательность SEQ ID NO:44). Этот мутеин включает по меньшей мере один или два мутированных аминокислотных остатка в любом из положений последовательности, соответствующих положениям последовательности 96, 100 и 106 линейной полипептидной последовательности Lcn2 человека, и где мутеин связывается с определенной неприродной мишенью с обнаруживаемой аффинностью.
В том смысле, в котором в настоящем документе используются термины «мутеин», «мутированная» молекула (белка или нуклеиновой кислоты) или «мутант», они относятся к замене, делеции или инсерции соответственно одного или более нуклеотидов или аминокислот по сравнению с встречающимся в природе (дикого типа) нуклеиновокислотным или белковым «стандартным» скэффолдам. Предпочтительно, число соответственно нуклеотидов или аминокислот, которое подвергает замене, делеции или инсерции, составляет 1, 2, 3, 4, 5, 6, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 или более, например, 25, 30, 35, 40, 45 или 50.
В том смысле, в котором в настоящем документе используются термины «липокалин человека, связанный с желатиназой нейтрофилов» или «hNGAL», или «липокалин 2» или «Lcn2», все они относятся к зрелому hNGAL с инвентарным номером P80188 в SWISS-PROT Data Bank (приведенная в настоящем документе в качестве примера последовательность SEQ ID NO:44).
В данном контексте отмечается, что изобретение основано на удивительном открытии того, что мутагенез липокалина 2 человека, крысиного белка, связанного с α2-микроглобулином (A2m), и 24р3/утерокалина мыши (24р3) в одном или более вышеуказанных 3 положений последовательности обеспечивает мутеины, которые обладают достаточным аффинным связыванием с заранее определенной мишенью, которая может включать, не ограничиваясь этим, пептид, белок, фрагмент или домен белка, и небольшую органическую молекулу.
Данная мишень может представлять любую желаемую, неприродную мишень/лиганд. В одном варианте осуществления термин «неприродный лиганд» относится к соединению, которое не связывается с природным зрелым hNGAL в физиологических условиях.
В том смысле, в котором в настоящем документе используются термины «органическая молекула» или «небольшая органическая молекула» для неприродной мишени, они означают органическую молекулу, содержащую по меньшей мере 2 атома углерода, но предпочтительно, не более чем 7 или 12 атомов, вращающихся вокруг углеродных связей, имеющую молекулярную массу в пределах между 100 и 2000 дальтон, предпочтительно, между 100 и 1000 дальтон и, необязательно, молекула включает один или более атомов металла.
В том смысле, в котором в настоящем документе используется термин «пептид» для неприродной мишени, он относится к дипептиду или олигопептиду с 2-45 аминокислотами. В одном из вариантов осуществления пептид содержит 2-40, 2-35, 2-30, 2-25, 2-20, 2-15 или 2-10 аминокислотных остатков. Пептид может представлять собой природный или синтетический пептид, и может содержать - помимо 20 природных L-аминокислот - D-аминокислоты, не встречающиеся в природе аминокислоты и аналоги аминокислот. В одном варианте осуществления пептид представляет собой бета-амилоидный пептид (Абета или Аβ). В еще одном варианте осуществления бета-амилоидный пептид представляет Аβ40 пептид или Аβ42 пептид.
В одном из вариантов осуществления небольшая органическая молекула представляет соединение, проявляющее свойства иммунологического гаптена.
В одном из вариантов осуществления неприродная мишень представляет белок фибронектин или его домен, такой как EB-домен или фрагмент EB-домена.
Мутеин липокалина 2 человека по изобретению может содержать аминокислотную последовательность дикого типа (природную) помимо положений мутированной аминокислотной последовательности. С другой стороны, мутеины липокалина, раскрытые в настоящем документе, также могут содержать аминокислотные мутации помимо положений последовательности, подвергнутых мутагенезу, при условии, что данные мутации не оказывают отрицательного влияния на связывающую активность и укладку мутеина. Такие мутации можно легко провести на уровне ДНК с использованием общепринятых стандартных методов (Sambrook J. et al., Molecular Cloning: A Laboratory Manual, 2nd Ed., Cold Spring Harbor Laboratory Press, Cold Spring Harbor, NY, 1989). Возможные изменения аминокислотной последовательности представляют собой инсерции или делеции, а также аминокислотные замены. Такие замены могут быть консервативными, т.е. аминокислотный остаток замещается аналогичным в химическом отношении аминокислотным остатком. Примерами консервативных замен являются замены среди членов следующих групп: 1) аланин, серин и треонин; 2) аспарагиновая кислота и глутаминовая кислота; 3) аспарагин и глутамин; 4) аргинин и лизин; 5) изолейцин, лейцин, метионин и валин и 6) фенилаланин, тирозин и триптофан. С другой стороны, возможно ввести неконсервативные изменения в аминокислотную последовательность. Кроме того, также вместо замены единичных аминокислотных остатков, также возможно вставить или делецировать одну или более следующих друг за другом аминокислот первичной структуры липокалина 2 человека, при условии, что данные делеции и инсерции проводят к получению стабильно уложенного/функционального мутеина.
Как уже отмечалось, такие модификации аминокислотной последовательности включают направленный мутагенез единичных аминокислотных положений для упрощения субклонирования мутированного гена липокалина или его фрагментов включением сайтов расщепления для некоторых рестриктаз. Кроме того, данные мутации также можно включить для дополнительного повышения аффинности мутеина липокалина для определенной мишени. Кроме того, можно ввести мутации для модуляции некоторых свойств мутеина, например, для повышения стабильности укладки, стабильности в сыворотке, резистентности белка или растворимости в воде, или снижения тенденции к агрегации, если это необходимо. Например, природные остатки цистеина можно мутировать в другие аминокислоты для предупреждения образования дисульфидных мостиков. Однако также возможно преднамеренно мутировать другое положение аминокислотной последовательности в цистеин для введения новых реакционноспособных групп, например, для конъюгации с другими соединениями, такими как полиэтиленгликоль (ПЭГ), гидроксиэтилкрахмал (HES), биотин, пептиды или белки, или для образования не встречающихся в природе дисульфидных связей. Примерные возможности такой мутации для введения остатков цистеина в аминокислотную последовательность мутеина липокалина 2 человека включают введение остатка цистеина (Cys) по меньшей мере в одно из положений последовательности, которое соответствует положениям 14, 21, 60, 84, 88, 116, 141, 145, 143, 146 или 158 последовательности hNGAL дикого типа. Полученные тиоловые группы на стороне любого из аминокислотных положений 14, 21, 60, 84, 88, 116, 141, 145, 143, 146 и/или 158 можно использовать для ПЭГилирования или HESилирования мутеина, например, для повышения периода полураспада соответствующего мутеина липокалина 2 человека.
В одном из вариантов осуществления мутеин по настоящему изобретению содержит мутированные аминокислотные остатки по меньшей мере в любых 2 или всех 3 положениях в последовательности, соответствующих положениям последовательности 96, 100 и 106 линейной полипептидной последовательности липокалина 2 человека.
В дополнительном варианте осуществления мутеин содержит по меньшей мере 1, 2, 3, 4, 5, 6, 8, 9, 10, 11, 12, 13, 14, 15, 16 и 17 мутированных аминокислотных остатков в любом из положений последовательности, соответствующих положениям последовательности 33, 36, 40, 41, 42, 43, 44, 46, 47, 48, 49, 50, 51, 52, 54, 55, 59, 65, 68, 70, 72, 73, 75, 77, 78, 79, 80, 81, 86, 87, 98, 96, 99, 100, 103, 106, 107, 110, 111, 125, 127, 132, 134, 136 и 138 линейной полипептидной последовательности hNGAL. В дополнительном варианте осуществления мутеин содержит по меньшей мере 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17 мутированных аминокислотных остатков в любом из положений последовательности 33, 36, 40, 41, 42, 43, 44, 46, 47, 48, 49, 50, 51, 52, 54, 55, 59, 65, 68, 70, 72, 73, 75, 77, 78, 79, 80, 81, 86, 87, 98, 96, 99, 100, 103, 106, 107, 110, 111, 125, 127, 132, 134, 136 и 138 линейной полипептидной последовательности hNGAL. В еще одном варианте осуществления мутеин содержит 18, 19 или 20 мутированных аминокислотных остатков в любом из положений последовательности 33, 36, 40, 41, 42, 43, 44, 46, 47, 48, 49, 50, 51, 52, 54, 55, 59, 65, 68, 70, 72, 73, 75, 77, 78, 79, 80, 81, 86, 87, 98, 96, 99, 100, 103, 106, 107, 110, 111, 125, 127, 132, 134, 136 и 138 линейной полипептидной последовательности липокалина 2 человека.
В еще одном варианте осуществления настоящего изобретения мутеин содержит мутированные аминокислотные остатки по меньшей мере в любых 10, 14, 15, 20, 22, 24, 26, 28, 29, 30, 31, 32, 33, 35 или всех 45 вышеперечисленных положений последовательности.
Мутеин по изобретению, который связывается с бета-амилоидным пептидом, таким как Aβ40 пептид и Aβ42 пептид, может содержать по сравнению с аминокислотной последовательностью зрелого липокалина 2 человека дикого типа, показанного на фигуре 17 (Lcn2), по меньшей мере 2, 3, 4, 5, 6, 8, 7, 9, 10, 11 или 12 аминокислотных замен, которые включают, не ограничиваясь этим, Leu36→Val или Cys; Ala40→Tyr или Lys, или Val; Ile41→Thr или Ser, или Leu; Gln49→Leu или Trp; Leu70→Gly; Arg72→Gly или Asp; Lys73→Leu или Trp, или Asp; Asp77→Asn или His, или Leu; Trp79→Lys; Asn96→Ile или Arg; Tyr100→Gln или Arg, или Glu; Leu103→Met или Arg, или Gly; Tyr106→Tyr или Ala, или Trp; Lys125→Thr или Val, или Glu; Ser127→Gly или Gln, или Ala; Tyr132→Met или Ser, или Thr и Lys134→Asn. Было установлено, что такие мутеины могут ингибировать агрегацию Aβ в условиях in vitro и in vivo. Предпочтительно, что такой мутеин, описанный в настоящем документе, связывался с и ингибировал агрегацию Aβ, предпочтительно, Aβ40, более предпочтительно, в условиях теста, описанного в примере 11 (предпочтительно, включая соотношение мутеин:Aβ40, равное 1:10). Настоящее изобретение также относится к мутеинам, описанным выше, обладающим сравнимой биологической функцией по сравнению с мутеином US7. Выражение «сравнимая биологическая функция» означает, что такие мутеины способны связываться с и ингибировать агрегацию Aβ, предпочтительно, Aβ40, с отклонением в ингибирующей агрегацию активности по сравнению с US7 не более чем на 40, 30, 20, 15, 10, 5, 2,5, 2 или 1%, например, в условиях, которые тождественны или идентичны описанным в примере 11 (предпочтительно включая соотношение мутеин:Aβ40, равное 1:10). Настоящее изобретение также относится к мутеинам, описанным в настоящем документе, для применения для лечения или профилактики нейродегенеративных заболеваний, таких как болезнь Альцгеймера.
В одном из вариантов осуществления мутеин по изобретению, который связывается с бета-амилоидным пептидом, таким как Aβ40 пептид и Aβ42 пептид, может содержать следующие аминокислотные замены Leu36→Val; Ala40→Tyr; Ile41→Thr; Gln49→Leu; Leu70→Gly; Lys73→Leu; Asp77→Asn; Trp79→Lys; Asn96→Ile; Tyr100→Gln; Leu103→Met; Lys125→Thr; Ser127→Gly; Tyr132→Met и Lys134→Asn. Примером мутеина, содержащего такие аминокислотные замены, является S1-A4, показанный на фигуре 17 (SEQ ID NO:39).
В дополнительном варианте осуществления мутеин по изобретению, который связывается с бета-амилоидным пептидом, таким как Aβ40 пептид и Aβ42 пептид, может содержать следующие аминокислотные замены Leu36→Val; Ala40→Lys; Ile41→Ser; Gln49→Trp; Leu70→Gly; Arg72→Gly; Lys73→Thr; Asp77→His; Trp79→Lys; Asn96→Arg; Tyr100→Arg; Leu103→Arg; Tyr106→Ala; Lys125→Val; Ser127→Gln; Tyr132→Ser и Lys134→Asn. Примером мутеина, содержащего такие аминокислотные замены, является US-7, показанный на фигуре 17 (SEQ ID NO:41).
Изобретение также относится к мутированному зрелому липокалину hNGAL (депозированному под инвентарным номером P80188 в SWISS-PROT Data Bank, предпочтительно, имеющему аминокислотную последовательность, представленную в SEQ ID NO:40), содержащему одну или более мутированных аминокислот, описанных в настоящем документе, в положении, соответствующем положению 36, 40, 41, 49, 70, 72, 73, 77, 79, 96, 100, 103, 106, 125, 127, 132, 134 линейной полипептидной последовательности hNGAL дикого типа.
В еще одном варианте осуществления мутеин по изобретению, который связывается с бета-амилоидным пептидом, таким как Aβ40 пептид и Aβ42 пептид, может содержать следующие аминокислотные замены Leu36→Cys; Ala40→Val; Ile41→Leu; Gln49→Leu; Leu70→Gly; Arg72→Asp; Lys73→Asp; Asp77→Leu; Trp79→Lys; Asn96→Arg; Tyr100→Glu; Leu103→Gly; Tyr106→Trp; Lys125→Glu; Ser127→Ala; Tyr132→Thr и Lys134→Asn. Примером мутеина, содержащего такие аминокислотные замены, является H1-G1, показанный на фигуре 17 (SEQ ID NO:43).
В еще одном варианте осуществления мутеин по изобретению, который связывается с бета-амилоидным пептидом, таким как Aβ40 пептид и Aβ42 пептид, может содержать следующие аминокислотные замены Leu36→Ala; Ala40→Val; Ile41→Leu; Gln49→Leu; Leu70→Gly; Arg72→Asp; Lys73→Asp; Asp77→Leu; Trp79→Lys; Asn96→Arg; Tyr100→Glu; Leu103→Gly; Tyr106→Trp; Lys125→Glu; Ser127→Ala; Tyr132→Thr и Lys134→Asn. Примером мутеина, содержащего такие аминокислотные замены, является H1GA показанный в SEQ ID NO:50.
Предпочтительно, чтобы мутеин, описанный в настоящем документе, связывался с и ингибировал агрегацию Aβ, предпочтительно, Aβ40, более предпочтительно, в условиях теста, описанного в примере 23 (предпочтительно, в соотношении Aβ40:H1GA, равным 10:2). Настоящее изобретение также относится к мутеинам, описанным выше, обладающим сравнимой биологической функцией при сравнении с мутеином H1GA. Выражение «сравнимая биологическая функция» означает, что такие мутеины способны связываться с и ингибировать агрегацию Aβ, предпочтительно, Aβ40, с отклонением в ингибирующей агрегацию активности по сравнению с H1GA не более чем на 40, 30, 20, 15, 10, 5, 2,5, 2 или 1%, например, в условиях, которые тождественны или идентичны описанным в примере 23 (предпочтительно, в соотношении Aβ40:H1GA, равным 10:2). Настоящее изобретение также относится к мутеинам, описанным в настоящем документе, для применения для лечения или профилактики нейродегенеративных заболеваний, таких как болезнь Альцгеймера.
В еще одном варианте осуществления мутеин по изобретению, который связывается с бета-амилоидным пептидом, таким как Aβ40 пептид и Aβ42 пептид, может содержать следующие аминокислотные замены Leu36→Val; Ala40→Val; Ile41→Leu; Gln49→Leu; Leu70→Gly; Arg72→Asp; Lys73→Asp; Asp77→Leu; Trp79→Lys; Asn96→Arg; Tyr100→Glu; Leu103→Gly; Tyr106→Trp; Lys125→Glu; Ser127→Ala; Tyr132→Thr и Lys134→Asn. Примером мутеина, содержащего такие аминокислотные замены, является H1GV, показанный в SEQ ID NO:52.
Предпочтительно, что мутеин, описанный в настоящем документе, связывается с Aβ40 в условиях теста, описанных в примере 21 Настоящее изобретение также относится к мутеинам, описанным выше, обладающим сравнимой биологической функцией по сравнению с мутеином H1GV. Выражение «сравнимая биологическая функция» означает, что такие мутеины способны связываться с Aβ, предпочтительно, с Aβ40, с отклонением в ингибирующей агрегацию активности по сравнению с H1GV не более чем 40, 30, 20, 15, 10, 5, 2,5, 2 или 1%, например, в условиях, которые тождественны или идентичны описанным в примере 21. Настоящее изобретение также относится к мутеинам, описанным в настоящем документе, для применения для лечения или профилактики нейродегенеративных заболеваний, таких как болезнь Альцгеймера.
В еще одном варианте осуществления мутеин по изобретению, который связывается с экстрадоменом В или его фрагментом, содержит следующие аминокислотные замены Leu36→Lys; Ala40→His; Ile41→Asp; Gln49→Arg; Tyr52→Gln; Ser68→Asn; Leu70→Arg; Arg72→Val; Lys73→His; Asp77→Asn; Trp79→Arg; Arg81→Trp; Tyr100→Trp; Tyr106→Trp; Lys125→Arg; Ser127→Tyr; Tyr132→Leu; Lys134→Glu и Ser146→Asn. Примером мутеина, содержащего такие аминокислотные замены, является N7A, показанный на фигуре 17 (SEQ ID NO:20).
В еще одном варианте осуществления мутеин по изобретению, который связывается с экстрадоменом В или его фрагментом, содержит следующие аминокислотные замены Leu36→Arg; Ala40→Met; Ile41→Arg; Gln49→Ala; Tyr52→Val; Ser68→Lys; Leu70→Met; Arg72→Gln; Lys73→Arg; Asp77→Lys; Trp79→Met; Arg81→Asn; Asn96→Ala; Tyr100→Pro; Leu103→Pro, Tyr106→Thr; Lys125→His; Ser127→Phe и Lys134→His. Примером мутеина, содержащего такие аминокислотные замены, является N9B, показанный на фигуре 17 (SEQ ID NO:24).
В еще одном варианте осуществления мутеин по изобретению, который связывается с экстрадоменом В или его фрагментом, содержит следующие аминокислотные замены Leu36→Ala; Ala40→Thr; Ile41→Trp; Gln49→Tyr; Tyr52→Gln; Ser68→Asn; Arg72→Met; Lys73→Ser; Asp77→Arg; Trp79→Met; Arg81→His; Asn96→Ser; Tyr100→Trp; Tyr106→Trp; Lys125→Arg; Ser127→Tyr; Tyr132→Phe и Lys134→Gly. Примером мутеина, содержащего такие аминокислотные замены, является N10D, показанный на фигуре 17 (SEQ ID NO:26).
В еще одном варианте осуществления мутеин по изобретению, который связывается с экстрадоменом В или его фрагментом, содержит следующие аминокислотные замены Leu36→Glu; Ala40→Ser; Ile41→Leu; Gln49→Arg; Leu70→Arg; Lys73→Ser; Asp77→His; Trp79→Leu; Asn96→Leu; Tyr100→Lys; Leu103→His; Tyr106→Phe; Lys125→Thr; Ser127→Ala и Lys134→Phe. Примером мутеина, содержащего такие аминокислотные замены, является N7E, показанный на фигуре 17 (SEQ ID NO:22).
Вышеприведенные мутеины, описанные при обращении к фигуре 17, могут содержать дополнительные аминокислотные замены. Мутеины могут дополнительно содержать аминокислотные замены, которые могут включать, не ограничиваясь этим, Gln28→His или Cys87→Ser. Другие возможные аминокислотные замены включают, не ограничиваясь этим, Tyr52→Gln или Val; Ser68→Lys или Asn или Arg81→Trp или Asn, или His.
Мутеины липокалина по изобретению способны связываться с желаемой неприродной мишенью с обнаруживаемой аффинностью, т.е. константой диссоциации (KD), составляющей по меньшей мере 200 нМ. В еще одном варианте осуществления мутеин связывается с определенной неприродной мишенью с KD по меньшей мере 1 мкМ или ниже, или 100 мкМ или ниже, или 1 мкМ или ниже, или 500 нМ, или 200 нМ или ниже, или 100 нМ или ниже, или 50 нМ или ниже, или 10 нМ или ниже, или 1 нМ или ниже. В еще одном варианте осуществления мутеины липокалина связываются с желаемой мишенью с константой диссоциации для определенной мишени, равной по меньшей мере 100, 20, 1 нМ или даже ниже. Аффинность связывания мутеина с желаемой мишенью можно определить с использованием большого числа методов, таких как титрование с использованием флуоресцентных индикаторов, конкурентный ELISA или поверхностный плазмонный резонанс (Biacore).
Специалистам в данной области, очевидно, понятно, что образование комплекса с мишенью зависит от многих факторов, таких как концентрация партнеров по связыванию, присутствие конкурентов, ионная сила буферной системы и т.д. Отбор и обогащение обычно проводят в условиях, обеспечивающих выделение мутеинов липокалина, обладающих в комплексе с желаемой мишенью, константой диссоциации на уровне, указанном выше. Однако можно провести стадии промывания и элюирования в условиях различной жесткости. Также возможен отбор на основе кинетических характеристик. Например, отбор можно провести в условиях, способствующих образованию комплекса мишени с мутеинами, который показывает медленную диссоциацию от мишени, или другими словами, с низким значением koff. Альтернативно отбор можно осуществить в условиях, способствующих быстрому образованию комплекса между мутеином и мишенью, или другими словами, высоким значением kon.
Мутеин по изобретению, как правило, находится в виде мономерного белка. Однако также возможно, чтобы мутеин липокалина по изобретению был способен к спонтанной димеризации или олигомеризации. Несмотря на то, что применение мутеинов липокалина, которые образуют стабильные мономеры, может быть предпочтительным для некоторых применений, например, за счет более быстрой диффузии и лучшего проникновения в ткани, в других случаях может быть преимущественным применение мутеинов липокалина, которые образуют стабильные гомодимеры или мультимеры, поскольку такие мультимеры могут обеспечить (дополнительное) повышенную аффинность и/или авидность для определенной мишени. Кроме того, олигомерные формы мутеина липокалина могут иметь замедленные скорости диссоциации или более длительный период полураспада.
Также следует отметить, что на образование комплекса между соответствующим мутеином и его лигандом оказывает влияние много различных факторов, таких как концентрации соответствующих партнеров по связыванию, присутствие конкурентов, рН и ионная сила используемой буферной системы, и экспериментальный метод, используемый для определения константы диссоциации KD (например, титрование с использованием флуоресцентных индикаторов, конкурентный ELISA или поверхностный плазмонный резонанс, и это только, назвав некоторые из них) или даже математический алгоритм, который используют для обработки экспериментальных данных.
Следовательно, специалистам в данной области также понятно, что значения KD (константы диссоциации комплекса, образованного между соответствующим мутеином и его мишенью/лигандом) могут варьировать в определенных экспериментальных пределах в зависимости от метода и экспериментальной системы, которые используются для определения аффинности конкретного мутеина липокалина для определенного лиганда. Это означает, что может быть незначительное отклонение в установленных значениях KD или пределах толерантности, в зависимости, например, от того определяли значение KD с использованием поверхностного плазмонного резонанса (Biacore) или конкурентного ELISA.
В одном из вариантов осуществления мутеины, раскрытые в настоящем документе, можно связать через N- или С-конец с аффинной меткой, такой как пентагистидиновая метка, гексагистидиновая метка или Strep-метка®. Таким образом, настоящая заявка также включает все подробно и в общих чертах описанные мутеины, содержащие такие метки.
В том смысле, в котором в настоящем изобретении используется термин «фрагмент» по отношению к мутеину липокалина, он относится к белкам или пептидам, полученным из полноразмерного зрелого Lcn2, которые укорочены по N- и/или С-концу, т.е. с отсутствием по меньшей мере одной из N- и/или С-концевых аминокислот. Такие фрагменты содержат, предпочтительно, по меньшей мере 10, более предпочтительно, 20, наиболее предпочтительно, 30 или более следующих друг за другом аминокислот первичной последовательности зрелого Lcn2, и которые обычно детектируются в иммуноанализе зрелого Lcn2.
Также в объем настоящего изобретения включаются вышеуказанные мутеины, которые изменены в отношении их иммуногенности.
Цитотоксические Т-клетки распознают пептидные антигены на клеточной поверхности антигенпрезентирующих клеток вместе с молекулами главного комплекса гистосовместимости класса I (MHC). Способность пептидов связываться с молекулами MHC является аллель-специфической и коррелирует с их иммуногенностью. Для снижения иммуногенности определенного белка возможность прогнозировать то, какие пептиды в белке обладают потенциальной активностью связываться с определенной молекулой MHC, имеет большое значение. Ранее были описаны подходы, которые использовались для расчетного подхода для идентификации потенциальных эпитопов Т-клеток, для прогноза связывания определенной пептидной последовательности с молекулами MHC класса I (Altuvia et al. (1995) J. Mol. Biol. 249:244-250).
Такой подход также можно использовать для идентификации потенциальных эпитопов для Т-клеток в мутеинах по изобретению и сделать выбор в зависимости от предполагаемого применения конкретного мутеина на основе его предполагаемой иммуногенности. Также возможно подвергнуть области пептидов, которые были прогнозированы, как содержащие эпитопы для Т-клеток, дополнительному мутагенезу для снижения или элиминации таких эпитопов для Т-клеток и, таким образом, свести до минимума иммуногенность. Описано удаление амфипатических эпитопов из генно-инженерных антител (Mateo et al. (2000) Hybridoma, 19(6):463-471), и данный протокол можно адаптировать к мутеинам по настоящему изобретению.
Полученные таким образом мутеины могут обладать минимальной иммуногенностью, которая желательна для их использования в терапевтических и диагностических применениях, таких, как описаны ниже.
Для некоторых применений также пригодно использовать мутеины по изобретению в конъюгированной форме. Следовательно, изобретение также относится к мутеинам липокалина, которые конъюгированы с соединением, которое может включать, не ограничиваясь этим, органические молекулы, ферментную метку, метку в окрашенной форме, цитостатический агент, токсин, метку, которую можно фотоактивировать и которая подходит для применения в фотодинамической терапии, флуоресцентную метку, радиоактивную метку, хромогенную метку, люминесцентную метку, комплексы металлов, металл, такой как коллоидное золото, гаптены, дигоксигенин, биотин или химиотерапевтический металл, которые можно упомянуть в качестве только некоторых, приходящих на память, примеров. Мутеин также можно конъюгировать с молекулой органического лекарственного препарата. Конъюгацию можно провести с использованием обычных способов сочетания, известных в данной области.
В общем, возможно ввести метку в мутеин Lcn2, описанный в настоящем документе, с использованием подходящего химического соединения или фермента, который непосредственно или опосредованно образует детектируемое соединение или сигнал в химической, физической, оптической или ферментативной реакции. Примером физической реакции и одновременно оптической реакции/маркера является эмиссия флуоресценции при облучении. Щелочная фосфатаза, пероксидаза хрена или β-галактозидаза являются примерами ферментных меток (и одновременно оптических меток), которые катализируют образование хромогенных продуктов реакции. В общем, для конъюгации с мутеинами по настоящему изобретению можно использовать все метки, которые обычно применяются для антител (за исключением меток, которые используются исключительно с сахарной группой Fc-фрагмента иммуноглобулинов). Мутеины по изобретению также можно конъюгировать с любым подходящим терапевтически активным агентом, например, для направленной доставки таких агентов к конкретной клетке, ткани или органу или для избирательного воздействия на клетки, например, на опухолевые клетки, не оказывая отрицательного влияния на окружающие нормальные клетки. Примеры таких терапевтически активных агентов включают радионуклиды, токсины, небольшие органические молекулы и лекарственные пептиды (такие как пептиды, функционирующие в качестве агонистов/антагонистов рецепторов клеточной поверхности или пептиды, конкурирующие за сайт связывания белка в данной клеточной мишени). Примеры подходящих токсинов включают, не ограничиваясь этим, коклюшный токсин, дифтерийный токсин, рицин, сапорин, эндотоксин Pseudomonas, калихеамицин или его производное, таксоид, майтанзиноид, тубулизин или аналог доластина. Аналог доластина может быть ауристатином Е, монометилауристином Е, ауристатином PYE и ауристатином PHE. Примеры цитотоксического агента включают, не ограничиваясь этим, цисплатин, карбоплатин, оксалиплатин, 5-фторурацил, таксотер (доцетаксел), паклитаксел, антрациклин (доксорубицин), метотрексат, винбластин, винкристин, виндезин, винорелбин, дакарбазин, циклофосфамид, этопозид, адриамицин, кампотецин, соединения, близкие комбретатастину А-4, сульфонамиды, оксадиазолины, бензо[b]тиофеновые синтетические спирокетальные пираны, производные монотетрагидрофурана, курацин и производные курацина, производные метоксиэстрадиола и лейковорин. Мутеины липокалина по изобретению также можно конъюгировать с терапевтически активными нуклеиновыми кислотами, такими как антисмысловые молекулы нуклеиновой кислоты, малые интерферирующие РНК, микроРНК или рибозимы. Такие конъюгаты можно получить с использованием способов, хорошо известных в данной области.
В одном из вариантов осуществления мутеины по изобретению также можно сочетать с направляющей группой, которая направляет его в определенную область организма, для доставки мутеинов по изобретению в желаемую область или зону организма. Одним примером, в котором может быть желательна такая модификация, является прохождение через гематоэнцефалический барьер. Для прохождения гематоэнцефалического барьера мутеины по изобретению можно сочетать с группами, которые облегчают активный транспорт через данный барьер (см. Gaillard P.J. et al. (2005) International Congress Series, 1277, 185-198 или Gaillard P.J. et al. (2005) Expert Opin. Drug Deliv., 2(2), 299-309). Такие соединения, доступны, например, под торговым названием 2B-TransTM (to-BBB technologies BV, Leiden, NL). Другие молекулы, приведенные в качестве примера направляющих молекул, с которыми можно сочетать мутеины по настоящему изобретению, включают антитела, фрагменты антител или мутеины липокалина с аффинностью к желаемой молекуле-мишени. Молекулой-мишенью для направляющих групп может быть, например, антиген клеточной поверхности. Антиген клеточной поверхности может быть специфическим для типа клеток или тканей, например, раковых клеток. Показательными примерами таких клеточных поверхностных белков являются HER-2 или протеогликаны, такие как NEU-2.
Как уже указывалось выше, в некоторых вариантах осуществления мутеин по изобретению может быть конъюгирован с соединением, которое удлиняет период полураспада мутеина (по этому вопросу см. также PCT публикацию международной заявки WO 2006/56464, в которой описаны такие стратегии конъюгации применительно к мутеинам липокалина человека, связанного с желатиназой нейтрофилов, со связывающей аффинностью для CTLA-4). Соединение, которое удлиняет период полураспада, может представлять молекулу полиалкиленгликоля, такого как полиэтиленгликоль (ПЭГ) или его активированное производное; гидроксиэтилкрахмал, молекулы жирных кислот, таких как пальмитиновая кислота (Vajo&Duckworth (2000) Pharmacol. Rev., 52:1-9), Fc-фрагмент иммуноглобулина, СН3-домен иммуноглобулина, СН4-домен иммуноглобулина, альбумин или его фрагмент, альбумин-связывающий пептид или альбумин-связывающий белок, трансферрин, назвав только некоторые из них. Альбумин-связывающий белок, может представлять собой бактериальный альбумин-связывающий белок, антитело, фрагмент антитела, включая домены антител (см., например, патент США 6696245) или мутеин липокалина со связывающей активностью в отношении альбумина. Следовательно, соединения, подходящие для конъюгации, в целях удлинения периода полураспада мутеина липокалина по изобретению, включают альбумин (Osborn et al. (2002) J. Pharmacol. Exp. Ther., 303:540-548) или альбумин-связывающий белок, например, бактериальный альбумин-связывающий белок, такой как стрептококковый белок G (Konig T. and Skerra A. (1998) J. Immunol. Methods, 218:73-83). Другими примерами альбумин-связывающих пептидов, которые можно использовать в качестве партнера по конъюгации, являются, например, пептиды с консенсусной последовательностью Cys-Xaa1-Xaa2-Xaa3-Xaa4-Cys, в которой Xaa1 представляет Asp, Asn, Ser, Thr или Trp; Xaa2 представляет Asn, Gln, His, Ile, Leu или Lys; Xaa3 представляет Ala, Asp, Phe, Trp или Tyr; и Xaa4 представляет Asp, Gly, Leu, Phe, Ser или Thr, как описано в заявке на патент США 2003/0069395 или Dennis et al. (Dennis et al. (2002) J. Biol. Chem., 277:35035-35043).
В других вариантах осуществления сам альбумин или биологически активный фрагмент альбумина можно использовать в качестве соединения для мутеина липокалина согласно изобретению, которое удлиняет период полураспада мутеина. Термин «альбумин» включает все альбумины млекопитающих, такие как сывороточный альбумин человека или бычий сывороточный альбумин, или альбумин крысы. Альбумин или его фрагмент можно получить рекомбинантным способом, как описано в патенте США № 5728553 или заявках на Европейский патент 0330451 и 0361991. Рекомбинантный альбумин человека (Recombumin® для применения в качестве белкового стабилизатора, например, доступен от Novozymes Delta Ltd. (Nottingham, Великобритания).
Если альбумин-связывающий белок представляет фрагмент антитела, то он может представлять доменное антитело. Доменные антитела (dAb) конструируют для точного контроля биофизических свойств и в условиях in vivo периода полураспада для обеспечения оптимального профиля препарата по безопасности и эффективности. Доменные антитела являются промышленно доступными, например, от Domantis Ltd. (Cambridge, Великобритания и MA, США).
При использовании трансферрина в качестве группы для увеличения периода полураспада мутеинов по изобретению можно получить мутеины, генетически слитые по N- или С-концу, или обоими концами, с негликозилированным трансферрином. Негликозилированный трансферрин имеет период полураспада, составляющий 14-17 суток, и слитый белок с трансферрином будет аналогично иметь увеличенный период полураспада. Носитель-трансферрин также обеспечивает высокую биодоступность, биологическое распределение и стабильность в системе кровообращения. Данная технология является промышленно доступной от BioRexis (BioRexis Pharmaceutical Corporation, PA, США). Рекомбинантный трансферрин человека BioRexis (DeltaFerrinTM) для использования в качестве стабилизатора белка также является промышленно доступным от Novozymes Delta Ltd. (Nottingham, Великобритания).
Если Fc-фрагмент иммуноглобулина используют для пролонгирования периода полураспада мутеинов по изобретению в сыворотке, то можно использовать технологию SynFusionTM, промышленно доступную от Syntonix Pharmaceuticals, Inc. (MA, США). Применение данной технологии Fc-слияния позволяет получить более длительно действующие биологические фармацевтические продукты, и они могут состоять, например, из двух копий мутеина, связанного с Fc-фрагментом антитела для улучшения фармакокинетики, повышения растворимости и эффективности получения.
Еще одной альтернативой для пролонгации периода полураспада мутеина по изобретению является слияние мутеина по N- или С-концу по изобретению с длинными неструктурированными, гибкими богатыми глицином последовательностями (например, полиглицином примерно с 20-80 последовательными остатками глицина). Данный подход раскрыт в международной заявке WO 2007/038619, например, имеющий название «rPEG» (рекомбинантный ПЭГ).
В том случае, если используют полиалкиленгликоль в качестве соединения, которое увеличивает период полураспада мутеина, то полиалкиленгликоль может быть замещенным или незамещенным. Он также может представлять активированное производное полиалкилена. Примерами подходящих соединений являются молекулы полиэтиленгликоля (ПЭГ), описанные в международной заявке WO 99/64016, в патентах США № 6177074 или 6403564 в отношении интерферона, или как описано для других белков, таких как ПЭГ-модифицированнная аспарагиназа, ПЭГ-аденозиндезаминаза (ПЭГ-ADA) или ПЭГ-супероксиддисмутаза (см., например, Fuertges et al. (1990) The Clinical Efficacy of Poly(Ethylene Glycol)-Modified Proteins J. Control. Release, 11:139-148). Молекулярная масса такого полимера, предпочтительно, полиэтиленгликоля, может находиться в пределах от 300 до примерно 70000 Д, включая, например, полиэтиленгликоль с молекулярной массой примерно 10000, примерно 20000, примерно 30000 или примерно 40000 Д. Кроме того, как, например, описано в патентах США № 6500930 или 6620413, углеводные олигомеры и полимеры, такие как крахмал или гидроксиэтилкрахмал (HES), можно конъюгировать с мутеином по изобретению в целях удлинения периода полураспада в сыворотке.
В еще одном варианте осуществления для обеспечения подходящих аминокислотных боковых цепей для конъюгации одного из вышеуказанных соединений с мутеинами по изобретению можно ввести мутагенезом искусственные аминокислоты. В общем, такие искусственные аминокислоты предназначаются для повышения реакционноспособности мутеина и, таким образом, они способствуют его конъюгации с желаемой группой. Одним примером такой искусственной аминокислоты, которую можно ввести через искусственную tРНК, является пара-ацетилфенилаланин.
Для некоторых применений мутеинов, раскрытых в настоящем документе, может быть преимущественным использовать их в форме слитых белков. В некоторых вариантах осуществления мутеин по изобретению сливают по его N- или С-концу с белком, доменом белка или пептидом, таким как сигнальная последовательность и/или аффинная метка.
Для фармацевтических применений мутеин по изобретению может быть слит с партнером по слиянию, который удлиняет период полураспада мутеина в сыворотке (вновь см. PCT публикацию международной заявки WO 2006/56464, в которой описан подходящий партнер по слиянию применительно к мутеинам липокалина человека, связанного с желатиназой нейтрофилов, со связывающей аффинностью для CTLA-4). Аналогично конъюгированным соединениям, описанным выше, партнер по слиянию может представлять Fc-фрагмент иммуноглобулина, СН3-домен иммуноглобулина, СН4-домен иммуноглобулина, альбумин, альбумин-связывающий пептид или альбумин-связывающий белок, назвав только некоторые из них. Вновь, альбумин-связывающий белок может представлять бактериальный альбумин-связывающий белок или мутеин липокалина со связывающей активностью в отношении альбумина. Следовательно, партнеры, подходящие для слияния, в целях удлинения периода полураспада мутеина липокалина по изобретению, включают альбумин (Osborn et al. (2002) см. выше, J. Pharmacol. Exp. Ther., 303:540-548) или альбумин-связывающий белок, например, бактериальный альбумин-связывающий домен, такой как домен стрептококкового белка G (Konig T. and Skerra A. (1998) J. Immunol. Methods, 218:73-83). Альбумин-связывающие пептиды, описанные Dennis et al., (2002) см. выше или в заявке на патент США 2003/0069395, имеющие консенсусную последовательность Cys-Xaa1-Xaa2-Xaa3-Xaa4-Cys, в которой Xaa1 представляет Asp, Asn, Ser, Thr или Trp; Xaa2 представляет Asn, Gln, His, Ile, Leu или Lys; Xaa3 представляет Ala, Asp, Phe, Trp или Tyr; и Xaa4 представляет Asp, Gly, Leu, Phe, Ser или Thr, также можно использовать в качестве партнера по слиянию. Также можно использовать сам альбумин или биологически активный фрагмент альбумина в качестве партнера по слиянию с мутеином липокалина по изобретению. Термин «альбумин» включает все альбумины млекопитающих, такие как сывороточный альбумин человека или бычий сывороточный альбумин, или альбумин крысы. В данной области хорошо известно рекомбинантное получение альбумина и его фрагментов и, например, описанное в патенте США № 5728553 или заявках на Европейский патент 0330451 и 0361991.
Партнер по слиянию может придавать новые свойства мутеину липокалина по изобретению, такие как ферментативная активность или аффинность связывания для других молекул. Примерами подходящих белков для слитых конструкций являются щелочная фосфатаза, пероксидаза хрена, глутатион-S-трансфераза, альбумин-связывающий домен белка G, белок А, фрагменты антитела, домены олигомеризации, мутеины липокалина с такой же или другой специфичностью связывания (что приводит к образованию «дуокалинов», см. Schlehuber S. and Skerra A. (2001) Duocalins, engineered ligand-binding proteins with dual specificity derived from the lipocalin fold, Biol. Chem., 382:1335-1342), или токсины.
В частности, может быть возможным слить мутеин липокалина по изобретению с активным сайтом отдельного фермента, таким образом, что оба «компонента» полученного слитого белка будут одновременно функционировать на определенной терапевтической мишени. Связывающий домен мутеина липокалина присоединяется к вызывающей заболевание мишени, позволяя домену фермента элиминировать биологическую функцию мишени.
Аффинные метки, такие как Strep-метка® или Strep-метка® II (Schmidt T.G.M. et al. (1996) J. Mol. Biol., 255:753-766), myc-метка, FLAG-метка, His6-метка или HA-метка, или белки, такие как глутатион-S-трансфераза, также обеспечивающие простое детектирование и/или выделение рекомбинантных белков, являются еще одними примерами предпочтительных партнеров по слиянию. Наконец, в качестве подходящих партнеров слияния для мутеина липокалина являются белки с хромогенными или флуоресцентными свойствами, такие как зеленый флуоресцентный белок (GFP) или желтый флуоресцентный белок (YFP).
В том смысле, в котором в настоящем документе используется термин «слитый белок», он также включает мутеины липокалина по изобретению, содержащие сигнальную последовательность. Сигнальные последовательности на N-конце полипептида направляют данный полипептид в специфический клеточный компартмент, например, периплазму E. coli или эндоплазматический ретикулюм эукариотических клеток. В данной области известно большое количество сигнальных последовательностей. Предпочтительной сигнальной последовательностью для секреции полипептида в периплазму E. coli является сигнальная последовательность OmpA.
Настоящее изобретение также относится к молекулам нуклеиновой кислоты (ДНК или РНК), содержащим нуклеотидные последовательности, кодирующие мутеины, описанные в настоящем документе. Поскольку вырожденность генетического кода позволяет заменять некоторые кодоны на другие кодоны, определяющие одну и туже аминокислоту, то изобретение не ограничивается конкретной молекулой нуклеиновой кислоты, кодирующей мутеин по изобретению, а включает все молекулы нуклеиновой кислоты, содержащие нуклеотидные последовательности, кодирующие функциональный мутеин.
Следовательно, настоящее изобретение также включает последовательность нуклеиновой кислоты, кодирующую мутеин по изобретению, содержащую мутацию по меньшей мере в одном кодоне любого из аминокислотных положений 96, 100 и 106 линейной полипептидной последовательности Lcn2.
Изобретение, раскрытое в настоящем документе, также включает молекулы нуклеиновой кислоты, кодирующие мутеины Lcn2, которые содержат дополнительные мутации помимо указанных положений в последовательности, предназначенных для экспериментального мутагенеза. Часто такие мутации являются толерабельными или даже могут быть преимущественными, например, если они способствуют повышенной эффективности укладки, стабильности в сыворотке, термической стабильности или аффинности связывания с лигандом мутеина.
Молекула нуклеиновой кислоты, описанная в данной заявке, может быть «функционально связана» с регуляторной последовательностью (или регуляторными последовательностями) для экспрессии данной молекулы нуклеиновой кислоты.
Молекула нуклеиновой кислоты, такая как ДНК, относится к «молекуле нуклеиновой кислоты, способной экспрессироваться» или «обеспечивающей экспрессию нуклеотидной последовательности», если она содержит элементы последовательности, содержащие информацию относительно транскрипционной и/или трансляционной регуляции, и такие последовательности «функционально связаны» с нуклеотидной последовательностью, кодирующей полипептид. Функциональной связью является связь, при которой регуляторные элементы последовательности и последовательность, предназначенная для экспрессии, связаны таким образом, что вместе они способствуют экспрессии гена. Точная природа регуляторных областей, необходимых для экспрессии гена, может варьировать среди видов, но, в общем, такие области содержат промотор, который у прокариот, включает промотор per se, т.е. элементы ДНК, направленные на инициацию транскрипции, а также элементы ДНК, которые при транскрипции в РНК, будут «сигналить» об инициации трансляции. Такие промоторные области обычно включают 5'-некодирующие последовательности, участвующие в инициации транскрипции и трансляции, такие как -35/-10 boxes и последовательность Шайн-Дальгарно у прокариот или последовательности TATA box, CAAT и 5'-кэппированные элементы у эукариот. Также такие области могут включать энхансер или репрессор, а также транслированную сигнальную и лидерные последовательности для направления нативных полипептидов в определенный компартмент клетки-хозяина.
Кроме того, 3'-некодирующие последовательности могут содержать регуляторные элементы, принимающие участие в терминации транскрипции, полиаденилировании или тому подобное. Однако, если такие последовательности терминации не являются удовлетворительными в функциональном отношении в конкретной клетке-хозяине, то их можно заменить сигналами, функциональными для этой клетки.
Следовательно, молекула нуклеиновой кислоты по изобретению может содержать регуляторную последовательность, предпочтительно, промоторную последовательность. В еще одном предпочтительном варианте осуществления молекула нуклеиновой кислоты по изобретению содержит промоторную последовательность и последовательность терминации транскрипции. Подходящими прокариотическими промоторами являются, например, промотор tet, промотор lacUV5 или промотор Т7. Примерами промоторов, подходящих для экспрессии в эукариотических клетках, являются промотор SV40 или промотор CMV.
Молекулы нуклеиновой кислоты по изобретению также могут быть фрагментом вектора или любого другого вида клонирующего носителя, такого как плазмида, фагемид, фаг, бакуловирус, космида или искусственная хромосома.
В одном из вариантов осуществления молекула нуклеиновой кислоты находится в фазмиде. Фазмидный вектор означает вектор, кодирующий межгенную область подходящего фага, такого как M13 или f1, или его функциональный фрагмент, слитый с интересующей кДНК. После суперинфицирования бактериальных клеток-хозяев таким фагемидным вектором и соответствующим фагом-хелпером (например, M13K07, VCS-M13 или R408) продуцируются интактные фаговые частицы, тем самым способствуя физическому сочетанию кодированных гетерологичных кДНК с ее соответствующим полипептидом, экспонированным на поверхности фага (см. обзор, например, Kay B.K. et al. (1996) Phage Display of Peptides and Proteins - A Laboratory Manual, 1st Ed., Academic Press, New York NY; Lowman H.B. (1997) Annu. Rev. Biophys. Biomol. Struct., 26:401-424 или Rodi D.J. and Makowski L. (1999) Curr. Opin. Biotechnol., 10:87-93).
Такие клонирующие векторы включают, помимо регуляторных последовательностей, описанных выше, и нуклеиновой кислоты, кодирующей мутеин липокалина по изобретению, последовательности репликации и контрольные последовательности, происходящие от видов, совместимых с клеткой-хозяином, которую используют для экспрессии, а также селектируемые маркеры, придающие селектируемый фенотип трансформированным и трансфектированным клеткам. В данной области известно большое количество подходящих клонирующих векторов, и они являются промышленно доступными.
ДНК-молекулу, кодирующую мутеины липокалина по изобретению, и, в частности, клонирующий вектор, содержащий кодирующую последовательность такого мутеина липокалина, можно трансформировать в клетку-хозяин, способную к экспрессии гена. Трансформацию можно проводить с использованием стандартных методов (Sambrook J. et al. (1989) см. выше).
Таким образом, изобретение также относится к клетке-хозяину, содержащей молекулу нуклеиновой кислоты, раскрытую в настоящем документе.
Трансформированные клетки-хозяева культивируют в условиях, подходящих для экспрессии нуклеотидной последовательности, кодирующей слитый белок по изобретению. Подходящими клетками-хозяевами могут быть прокариотические клетки, такие как Escherichia coli (E. coli) или Bacillus subtilis, или эукариотические клетки, такие как Saccharomyces cerevisiae, Pichia pastoris, клетки насекомых SF9 или High5, иммортализованные клеточные линии млекопитающих (например, клетки HeLa или CHO) или первичные клетки млекопитающих.
Изобретение также относится к способу получения мутеина по изобретению, в котором мутеин, фрагмент мутеина или слитый белок мутеина и другого полипептида получают, начиная с нуклеиновой кислоты, кодирующей мутеин с помощью генно-инженерных методов. Способ можно осуществить в условиях in vivo, например, мутеин можно получить в бактериальном или эукариотической микроорганизме-хозяине и затем выделить из этого микроорганизма-хозяина или его культуры. Также возможно получить белок в условиях in vitro, например, при использовании трансляционной системы в условиях in vitro.
При получении мутеина в условиях in vivo нуклеиновую кислоту, кодирующую мутеин по изобретению, вводят в подходящий бактериальный или эукариотический микроорганизм-хозяин с использованием технологии рекомбинантной ДНК (уже упомянутой выше). Для данной цели клетку-хозяин вначале трансформируют клонирующим вектором, содержащим молекулу нуклеиновой кислоты, кодирующую мутеин по изобретению, с использованием принятых стандартных методов (Sambrook J. et al., 1989, см. выше). Затем клетку-хозяин культивируют в условиях, обеспечивающих экспрессию гетерологичной ДНК и, таким образом, синтез соответствующего полипептида. Затем полипептид выделяют из клетки или из культуральной среды.
В одном из аспектов настоящее изобретение относится к способу получения мутеина по изобретению, включающему:
(а) мутагенез молекулы нуклеиновой кислоты, кодирующей липокалин 2 человека в нуклеотидном триплете, кодирующем по меньшей мере одно из любых положений в последовательности, соответствующих положениям 96, 100 и 106 линейной полипептидной последовательности Lcn2, с получением одной или более молекул нуклеиновой кислоты мутеина.
Способ может дополнительно включать:
(b) экспрессию одной или более молекул нуклеиновой кислоты мутеина, полученных на стадии (а) в подходящей экспрессионной системе, и
(с) обогащение одним или более мутеинами, обладающими обнаруживаемой аффинностью связывания для определенной мишени с помощью отбора и/или выделения.
В том смысле, в котором в настоящем документе используется термин «мутагенез», он означает, что выбраны такие экспериментальные условия, когда природная аминокислота в данном положении последовательности Lcn2 (hNGAL; инвентарный номер P80188 в SWISS-PROT Data Bank) может быть замещена по меньшей мере одной аминокислотой, которая отсутствует в данном конкретном положении в соответствующей природной полипептидной последовательности. Термин «мутагенез» также включает (дополнительную) модификацию длины сегментов последовательности с помощью делеции или инсерции одной или более аминокислот. Таким образом, в объем изобретения входит вариант, когда, например, одна аминокислота в выбранном положении последовательности заменяется фрагментом из трех случайных мутаций, что приводит к инсерции двух аминокислотных остатков по сравнению с длиной соответствующего сегмента белка дикого типа. Такую инсерцию или делецию можно ввести независимо друг от друга в любом из пептидных сегментов, которые можно подвергнуть мутагенезу по изобретению. В одном приводимом в качестве примера варианте осуществления изобретения инсерцию нескольких мутаций можно ввести в петлю АВ выбранного скэффолда липокалина (см. международную заявку на патент WO 2005/0192256, в полном объеме включенную в данный документ для сведения). Термин «случайный мутагенез» означает, что отсутствует заранее определенная единичная аминокислота (мутация) в определенном положении последовательности, но по меньшей мере две аминокислоты можно включить с определенной вероятностью в заранее определенное положение последовательности во время мутагенеза.
Кодирующую последовательность липокалина 2 человека используют в качестве стартовой точки для мутагенеза пептидных сегментов, выбранных в настоящем изобретении. Для мутагенеза указанных аминокислотных положений в распоряжении специалиста в данной области имеются различные общепринятые стандартные методы для сайт-направленного мутагенеза (Sambrook J. et al., 1989, см. выше). Обычно применяемым методом является введение мутаций с помощью ПЦР (полимеразной цепной реакции) с использованием смеси синтетических олигонуклеотидов, которые содержат композицию вырожденных оснований в желаемых положениях последовательности. Например, использование кодона NNK или NNS (где N = аденин, гуанин или цитозин, или тимин; K = гуанин или тимин; S = аденин или цитозин) позволяет включить все 20 аминокислот плюс amber стоп-кодон во время мутагенеза, в то время как кодон VVS ограничивает число возможных для включения аминокислот до 12, поскольку он исключает аминокислоты Cys, Ile, Leu, Met, Phe, Trp, Tyr, Val, от включения в выбранное положение полипептидной последовательности; использование кодона NMS (где M = аденин или цитозин), например, ограничивает число возможных аминокислот до 11 в выбранном положении, поскольку он исключает аминокислоты Arg, Cys, Gly, Ile, Leu, Met, Phe, Trp, Val от включения в выбранное положение последовательности. В данном отношении можно отметить, что кодоны для других аминокислот (иных, чем обычные 20 природных аминокислот), таких как селеноцистеин или пирролизин, также можно включить в нуклеиновую кислоту мутеина. Также возможно, как описывает Wang L. et al. (2001) Science, 292:498-500 или Wang L. and Schultz P.G. (2002) Chem. Comm., 1:1-11, использовать «искусственные» кодоны, такие как UAG, которые обычно распознаются в качестве стоп-кодонов для инсерции других необычных аминокислот, например, о-метил-L-тирозина или п-аминофенилаланина.
Применение нуклеотидных кирпичиков-блоков с пониженной специфичностью пар оснований, например, инозина, 8-оксо-2'-дезоксигуанозина или 6(2-дезокси-β-D-рибофуранозил)-3,4-дигидро-8Н-пиримино-1,2-оксазин-7-он (Zaccolo et al., J. Mol. Biol., 1996, 255:589-603) является другой возможностью для введения мутаций в выбранный сегмент последовательности.
Дополнительной возможностью является так называемый триплетный мутагенез. В данном способе используются смеси различных нуклеотидных триплетов, где каждый кодирует одну аминокислоту, для включения в кодирующую последовательность (Virnekas B., Ge L., Pluchthun A., Schneider K.C., Wellnhofer G., Moroney S.E., 1994, Trinucleotide phosphoramidites: ideal reagents for synthesis of mixed oligonucleotides for random mutagenesis, Nucleic Acids Res., 22:5600-5607).
Одна возможная стратегия для введения мутаций в выбранные области соответствующих полипептидов основана на использовании четырех олигонуклеотидов, каждый из которых частично происходит из одного из соответствующих сегментов последовательности, предназначенных для мутации. При синтезе данных олигонуклеотидов специалист в данной области может использовать смеси кирпичиков-блоков нуклеиновой кислоты для данных нуклеотидных триплетов, которые соответствуют аминокислотным положениям, предназначенным для мутации таким образом, что кодоны, кодирующие все природные аминокислоты, возникают случайно, что в конечном итоге приводит к получению библиотеки пептидов липокалина. Например, первый олигонуклеотид соответствует по его последовательности - помимо мутированных положений - кодирующей цепи пептидного сегмента, предназначенного для мутирования, в основном в N-концевом положении полипептида липокалина. Следовательно, второй олигонуклеотид соответствует некодирующей цепи второго сегмента последовательности, следующего в полипептидной последовательности. Третий олигонуклеотид, в свою очередь, соответствует кодирующей цепи соответствующего третьего сегмента данной последовательности. Наконец, четвертый олигонуклеотид соответствует некодирующей цепи четвертого сегмента последовательности. Полимеразную цепную реакцию можно провести с соответствующим первым и вторым олигонуклетидом и по отдельности, если необходимо, с соответствующим третьим и четвертым олигонуклеотидом.
Продукты амплификации обеих данных реакций можно объединить различными известными методами в одну нуклеиновую кислоту, содержащую последовательность от первого до четвертого сегментов последовательности, в которые введены мутации в выбранных положениях. После этого оба продукта можно подвергнуть, например, новой полимеразной цепной реакции с использованием фланкирующих олигонуклеотидов, а также одну или более опосредующих молекул нуклеиновой кислоты, которые вносят последовательность между вторым и третьим сегментом последовательности. При выборе числа и расположения в последовательности олигонуклеотидов, используемых для мутагенеза, специалист в данной области имеет в своем распоряжении многочисленные альтернативы.
Молекулы нуклеиновой кислоты, определенные выше, можно соединить лигированием с пропуском 5'- и 3'-последовательностей нуклеиновой кислоты, кодирующей полипептид липокалина и/или вектор, и можно клонировать в известный микроорганизм-хозяин. Для лигирования и клонирования имеется большое число методов (Sambrook J. et al., 1989, см. выше). Например, последовательности узнавания для рестриктаз, также присутствующие в последовательности клонирующего вектора, можно встроить в последовательности синтетических олигонуклеотидов. Таким образом, после амплификации соответствующего продукта ПЦР и ферментативного отщепления полученный фрагмент можно легко клонировать с использованием соответствующих последовательностей распознавания.
Более длинные сегменты последовательности в гене, кодирующем белок, выбранный для мутагенеза, также можно подвергнуть случайному мутагенезу с использованием известных способов, например, применением полимеразной цепной реакции в условиях повышенного показателя ошибки, химическим мутагенезом или с использованием бактериальных штаммов-мутаторов. Такие способы также можно использовать для дополнительной оптимизации аффинности или специфичности мутеина липокалина для мишени. Мутации, возможно, имеющие место вне сегментов экспериментального мутагенеза, часто являются устойчивыми или даже могут быть преимущественными, например, если они вносят свой вклад в повышение эффективности укладки или стабильности укладки мутеина липокалина.
Согласно одному варианту осуществления настоящего изобретения вышеуказанный способ включает мутагенез молекулы нуклеиновой кислоты, кодирующей белок липокалина 2 человека по меньшей мере в 2 или 3 триплетах, кодирующих любое из вышеуказанных положений липокалина 2 человека.
В еще одном варианте осуществления способ дополнительно включает мутагенез молекулы нуклеиновой кислоты по меньшей мере в одном нуклеотидном триплете, кодирующем любое из положений последовательности, соответствующих положениям последовательности 33, 36, 40, 41, 42, 43, 44, 46, 47, 48, 49, 50, 51, 52, 54, 55, 59, 65, 68, 70, 72, 73, 75, 77, 78, 79, 80, 81, 86, 87, 98, 96, 99, 100, 103, 106, 107, 110, 111, 125, 127, 132, 134, 136 и 138 линейной полипептидной последовательности hNGAL.
В еще одном варианте осуществления способ включает мутагенез молекулы нуклеиновой кислоты в нуклеотидных триплетах, кодирующих по меньшей мере любые 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20 положений последовательности, соответствующих положениям последовательности 33, 36, 40, 41, 42, 43, 44, 46, 47, 48, 49, 50, 51, 52, 54, 55, 59, 65, 68, 70, 72, 73, 75, 77, 78, 79, 80, 81, 86, 87, 98, 96, 99, 100, 103, 106, 107, 110, 111, 125, 127, 132, 134, 136 и 138 линейной полипептидной последовательности липокалина 2 человека.
Согласно способу по изобретению мутеин получают, начиная с нуклеиновой кислоты, кодирующей hNGAL. Такую нуклеиновую кислоту подвергают мутагенезу и вводят в подходящий бактериальный или эукариотический микроорганизм-хозяин с использованием технологии рекомбинантной ДНК. Библиотеку нуклеиновых кислот ликалина 2 человека можно получить с использованием любого подходящего метода, который известен в данной области, для получения мутеинов липокалина с антителоподобными свойствами, т.е. мутеинов, которые обладают аффинностью для определенной мишени. Примеры таких комбинаторных методов подробно описаны, например, в международных заявках на патент WO 99/16873, WO 00/75308, WO 03/029471, WO 03/029462, WO 03/029463, WO 2005/019254, WO 2005/019255, WO 2005/019256 или WO 2006/56464. Содержание каждой из данных патентных заявок в полном объеме включено в данный документ для сведения. После экспрессии последовательностей нуклеиновой кислоты, которые были подвергнуты мутагенезу в соответствующем хозяине, из полученной библиотеки можно отобрать клоны, несущие генетическую информацию для множества соответствующих мутеинов липокалина, которые связываются с определенной мишенью. Можно использовать хорошо известные методы для отбора данных клонов, такие как фаговый дисплей (см. обзоры Kay B.K. et al., 1996, выше; Lowman H.B., 1997, выше или Rodi D.J. and Makowski L., 1999, выше), скрининг колоний (см. обзоры Pini A. et al. (2002) Comb. Chem. High Througput Screen., 5:503-510), рибосомный дисплей (см. обзоры Amstutz P. et al. (2001) Curr. Opin. Biotechnol., 12:400-405) или дисплей мРНК у Wilson D.S. et al. (2001) Proc. Natl. Acad. Sci. USA, 98:3750-3755 или способы, конкретно описанные в международных заявках WO 99/16873, WO 00/75309, WO 03/029462, WO 03/029463, WO 2005/019254, WO 2005/019255, WO 2005/019256 или WO 2006/56464.
Согласно данному раскрытию стадия (с) дополнительно включает в другом варианте осуществления вышеуказанного способа:
(i) обеспечение в качестве определенной мишени/лиганда соединения, выбранного из группы, состоящей из химического соединения в свободной или конъюгированной форме, которое обладает свойствами, например, иммунологического гаптена, пептида, белка или другой макромолекулы, такой как полисахарид, молекула нуклеиновой кислоты (например, ДНК или РНК), или целой вирусной частицы или вироида;
(ii) контактирование множества мутеинов с указанной мишенью/лигандом с образованием комплексов указанного лиганда и мутеинов, обладающих аффинностью связывания для указанной мишени/лиганда; и
(iii) удаление мутеинов, не обладающих или обладающих недостаточной аффинностью связывания.
В конкретных вариантах осуществления изобретения мишень/лиганд представляет неприродную мишень, которая включает, не ограничиваясь этим, пептид, белок, фрагмент или домен белка, и небольшую органическую молекулу. В одном варианте осуществления небольшая органическая молекула представляет соединение, проявляющее свойства иммунологического гаптена. В еще одном варианте осуществления пептид представляет бета-амилоидный пептид, такой как Аβ40 пептид или Аβ42 пептид. В еще одном варианте осуществления неприродная мишень представляет белок фибронектин или его домен, такой как EB-домен или фрагмент EB-домена.
В одном варианте осуществления способов по изобретению отбор на стадии (с) проводят в конкурентных условиях. В том смысле, в котором в настоящем документе используется выражение «конкурентные условия», оно означает, что отбор мутеинов включает по меньшей мере одну стадию, в которой мутеины и определенный неприродный лиганд липокалина 2 человека (мишени) приводят в контакт в присутствии дополнительного лиганда, который конкурирует за связывание мутеинов с мишенью. Такой дополнительный лиганд может представлять физиологический лиганд мишени, избыток самой мишени или любой другой нефизиологический лиганд мишени, который связывается по меньшей мере с перекрывающимся эпитопом с эпитопом, распознающимся мутеинами по изобретению, и таким образом, мешает связыванию мутеинов с мишенью. Альтернативно, дополнительный лиганд конкурирует за связывание мутеинов посредством образования комплекса с эпитопом, отличным от сайта связывания мутеинов с мишенью, под действием аллостерических эффектов.
Вариант осуществления метода фагового дисплея (см. обзор Kay B.K. et al. (1996) выше; Lowman H.B. (1997) и Makowski L. (1999) выше) с использованием подходящего фага M13 приведен в качестве примера метода отбора, который можно использовать в настоящем изобретении. Еще одним вариантом осуществления технологии фагового дисплея, который можно использовать для отбора мутеинов по изобретению, является технология гиперфага фага, описанная Broders et al. (Broders et al. (2003) «Hyperphage. Improving antibody presentation in phage display». Methods Mol. Biol., 205:295-302). Также можно использовать другой нитчатый фаг, такой как f1, или литический фаг, такой как Т7. В приведенном в качестве примера методе отбора продуцируются фагемиды М13, обеспечивающие экспрессию мутированной последовательности нуклеиновой кислоты липокалина в виде слитого белка с сигнальной последовательностью на N-конце, предпочтительно, сигнальной последовательностью OmpA, и с капсидным белком pIII фага М13 или его фрагментами, способными включаться в капсиду фага на C-конце. С-концевой фрагмент ∆pIII белка капсидного фага, содержащего аминокислотные 217-406 последовательности дикого типа, предпочтительно, используют для получения слитых белков. В одном варианте осуществления особенно предпочтительным является С-концевой фрагмент pIII, в котором цистеиновый остаток в положении 201 отсутствует или замещен другой аминокислотой.
Следовательно, дополнительный вариант осуществления способов по изобретению включает функциональное слияние нуклеиновой кислоты, кодирующей множество мутеинов липокалина 2 человека и возникающих в результате мутагенеза на 3'-конце, с геном, кодирующим белок оболочки pIII нитчатого бактериофага, относящегося к семейству M13, или фрагмент белка данной оболочки, для отбора по меньшей мере одного мутеина по связыванию с определенным лигандом.
Слитый белок может содержать дополнительные компоненты, такие как аффинная метка, которая обеспечивает иммобилизацию, детектирование и/или выделение слитого белка или его фрагментов. Кроме того, стоп-кодон можно расположить между областями последовательности, кодирующими липокалин или его мутеины, и геном капсиды фага или его фрагментами, где стоп-кодон, предпочтительно, amber стоп-кодон по меньшей мере частично транслируется в аминокислоту во время трансляции в подходящем штамме-супрессоре.
Например, плазмидный вектор pTLPC27, в настоящее время названный pTlc27, который описан в настоящем документе, используется для получения фагемидной библиотеки, кодирующей мутеины липокалина 2 человека. Молекулы нуклеиновой кислоты по изобретению, кодирующие мутеины hNGAL, вставляют в вектор с использованием двух сайтов рестрикции BstXI. После лигирования подходящий штамм-хозяин, такой как E. coli XL1-Blue, трансформируют с получением смеси нуклеиновых кислот с получением большого числа независимых клонов. Если желательно, то можно приготовить соответствующий вектор для получения гиперфагемидной библиотеки.
Затем полученную библиотеку суперинфицируют в жидкой культуре соответствующим фагом-хелпером М13 или гиперфагом для получения функциональных фагемид. Рекомбинантный фагемид экспонирует мутеин липокалина на своей поверхности в виде слитого белка с белком оболочки pIII или его фрагментом, в то время как N-концевая сигнальная последовательность слитого белка обычно отщепляется. С другой стороны, она также несет одну или более копий нативного капсидного белка pIII, поставляемого фагом-хелпером, и таким образом способна инфицировать реципиента, в основном бактериальный штамм, несущий F- или F'-плазмиду. В случае гиперфагового дисплея гиперфагемиды экспонируют мутеины липокалина на своей поверхности в виде слитого белка с инфекционным белком оболочки pIII, но не с нативным капсидным белком. Во время или после инфицирования фагом-хелпером или гиперфагом экспрессию гена слитого белка из мутеина липокалина и капсидного белка pIII можно индуцировать, например, добавлением ангидротетрациклина. Выбирают такие условия индукции, что значительная фракция полученных фагемид экспонирует по меньшей мере один мутеин липокалина на своей поверхности. В случае гиперфагового дисплея условия индукции обеспечивают популяцию гиперфагемид, несущих между третьим и пятым слитыми белками, состоящими из мутеина липокалина и капсидного белка pIII. Известны различные методы выделения фагемид, такие как преципитация полиэтиленгликолем. Как правило, выделение имеет место после инкубационного периода, составляющего 6-8 ч.
Затем выделенные плазмиды можно подвергнуть отбору при инкубации с желаемой мишенью, где мишень представлена в форме, обеспечивающей по меньшей мере временную иммобилизацию таких фагемид, которые несут мутеины с желаемой связывающей активностью, как слитые белки в их оболочке. Среди различных вариантов осуществления, известных специалистам в данной области, мишень можно конъюгировать, например, с белком-носителем, таким как сывороточный альбумин, и можно связать через такой белок-носитель с белком связывающей поверхности, например, полистиролом. Предпочтительно, можно использовать микротитрационные планшеты, подходящие для постановки ELISA, или так называемые «иммуно-стик» для иммобилизации мишени. Альтернативно, можно использовать конъюгаты мишени с другими связывающими группами, такими как биотин. Затем мишень можно иммобилизовать на поверхности, которая селективно связывает данную группу, например, микротитрационные планшеты или парамагнитные частицы, покрытые стрептавидином, нейтравидином или авидином. Если мишень сливают с Fc-фрагментом иммуноглобулина, то иммобилизацию также можно провести с поверхностями, например, микротитрационными планшетами или парамагнитными частицами, которые покрыты белком А или белком G.
Неспецифические фагемид-связывающие сайты, находящиеся на поверхностях, можно насытить блокирующими растворами, известными для способов ELISA. Затем, как правило, фагемиды приводят в контакт с мишенью, иммобилизованной на поверхности в присутствии физиологического буфера. Несвязанные фагемиды удаляют многократным промыванием. Фагемидные частицы, оставшиеся на поверхности, затем элюируют. Для элюирования возможно несколько способов. Например, фагемиды можно элюировать добавлением протеаз или в присутствии кислот, оснований, детергентов или хаотропных солей, или в умеренно денатурирующих условиях. Предпочтительным способом является элюирование с использованием буферов с рН 2,2, в таком случае затем элюат нейтрализуют. Альтернативно, можно добавить раствор свободной мишени для конкуренции с иммобилизованной мишенью для связывания с фагемидами, или мишень-специфические фагемиды можно элюировать конкуренцией с иммуноглобулинами или природными белками-лигандами, которые специфически связываются с интересующей мишенью.
Затем клетки E. coli инфицируют элюированными фагемидами. Альтернативно, нуклеиновые кислоты можно экстрагировать из элюированных фагемид и использовать для анализа последовательности, амплификации или трансформации клеток иным способом. Начиная с клонов E. coli, полученных таким образом, вновь получают свежие фагемиды или гиперфагемиды суперинфицированием фагами-хелперами М13 или гиперфагом с использованием способа, описанного выше, и амплифицированные таким образом фагемиды вновь подвергают отбору на иммобилизованной мишени. Часто требуются многочисленные циклы отбора для получения фагемид с мутеинами по изобретению в достаточно обогащенной форме. Число циклов отбора, предпочтительно, выбирают таким образом, чтобы в последующем функциональном анализе по меньшей мере 0,1% испытуемых клонов продуцировал мутеины с обнаруживаемой аффинностью для определенной мишени. В зависимости от размера, т.е. сложности используемой библиотеки, как правило, для этой цели необходимо 2-8 циклов.
Для функционального анализа отобранных мутеинов штамм E. coli инфицируют фагемидами, полученными из циклов отбора, и выделяют соответствующую двухцепочечную плазмидную ДНК. Начиная с этой плазмидной ДНК или также с одноцепочечной ДНК, экстрагированной из фагемид, последовательности нуклеиновой кислоты отобранных мутеинов по изобретению можно определить с использованием способов, известных в данной области, и на этой основе вывести аминокислотную последовательность. Мутированную область или последовательность полного мутеина hNGAL можно субклонировать в другой вектор экспрессии и экспрессировать в подходящем микроорганизме-хозяине. Например, вектор pTLPC26, в настоящее время названный pTlc26, можно использовать для экспрессии штаммов E. coli, таких как E. coli TG1. Полученные таким образом мутеины липокалина 2 человека можно выделить различными биохимическими способами. Мутеины hNGAL, полученные, например, с pTlc26, несут аффинный пептид Strep-метку II (Schmidt et al., выше) на их С-концах и, следовательно, предпочтительно, их можно выделить аффинной хроматографией со стрептавидином.
Также отбор можно проводить с помощью других методов. Многие соответствующие варианты осуществления известны специалистам в данной области, или они описаны в литературе. Однако можно использовать комбинацию методов. Например, отобранные клоны или по меньшей мере обогащенные с использованием “фагового дисплея”, можно дополнительно подвергнуть «скринингу колоний». Данный метод обладает тем преимуществом, что индивидуальные клоны можно непосредственно выделить по отношению к получению мутеина липокалина 2 человека с обнаруживаемой аффинностью связывания для мишени.
В дополнении к применению E. coli в качестве микроорганизма-хозяина в способе «фаговый дисплей» или способе «скрининг колоний», для этой цели можно использовать другие бактериальные штаммы, дрожжи или также клетки насекомых или клетки млекопитающих. После отбора мутеина липокалина 2 человека из произвольной библиотеки, как описано выше, также можно использовать разрабатывающиеся способы, в том числе, ограниченный мутагенез, для оптимизации мутеина, который уже обладает некоторой связывающей активностью для мишени в отношении аффинности или специфичности мишени.
После отбора мутеина с аффинностью к данной мишени можно дополнительно подвергнуть такой мутеин другому мутагенезу для последующего отбора вариантов с еще более высокой аффинностью или вариантов с улучшенными свойствами, такими как более высокая термостабильность, повышенная стабильность в сыворотке, термодинамическая стабильность, повышенная растворимость, улучшенный мономерный профиль, повышенная резистентность к термической денатурации, химической денатурации, протеолизу или воздействию детергентов и т.д. Такой дополнительный мутагенез, в то случае, если он направлен на обеспечение более высокой аффинности, может рассматриваться в качестве «созревания аффинности» in vitro, его можно достичь сайт-специфической мутацией, основанной на рациональном дизайне или случайной мутации. Другим возможным подходом для получения более высокой аффинности или улучшенных свойств является применение подверженной ошибкам ПЦР, что приводит к точечным мутациям в выбранном ряду положений последовательности мутеина липокалина. Подверженную ошибкам ПЦР можно осуществить, следуя любому известному протоколу, такому как описан Zaccolo et al. (1996) J. Mol. Biol., 255:589-603. Другие способы случайного мутагенеза thatare, подходящие для таких целей, включают случайный инсерционный/делеционный мутагенез (RID), описанный Murakami et al. (2002) Nat. Biotechnol., 20, 76-81, или негомологичную случайную рекомбинацию (NRR), описанную Bittker et al. (2002) Nat. Biotechnol., 20, 1024-1029. Если желательно, то созревание аффинности можно провести согласно процедуре, описанной в международной заявке WO 00/75308 или Schlehuber et al. (2000) J. Mol. Biol., 297, 1105-1120, где получали мутеины билин-связывающего белка, обладающего высокой аффинностью к дигоксигенину. Дополнительным подходом для повышения аффинности является проведение позиционного мутагенеза с насыщением. При таком подходе можно создать «небольшие» библиотеки нуклеиновых кислот, в которые вводят аминокислотные замены/мутации только в отдельных положениях в любом из четырех петлей-сегментов. Затем данные библиотеки непосредственно подвергают стадии отбора (скрининг аффинности) без дополнительных раундов пэннинга. Такой подход позволяет идентифицировать остатки, вносящие вклад в повышенное связывание желаемой мишени, и позволяет идентифицировать «горячие пятна», имеющие значение для связывания.
В одном варианте осуществления вышеуказанный способ модификации мутеина дополнительно включает введение остатка Cys по меньшей мере в одно из любых положений последовательности, которые соответствуют положениям последовательности 14, 21, 60, 84, 88, 116, 141, 145, 143, 146 или 158 последовательности липокалина 2 человека дикого типа и присоединение группы, которая способна модифицировать период полураспада в сыворотке указанного мутеина через тиоловую группу остатка Cys, введенного по меньшей мере в одно из любых положений последовательности, которые соответствуют положениям последовательности 14, 21, 60, 84, 88, 116, 141, 145, 143, 146 или 158 последовательности hNGAL дикого типа. Группу, которая способна модифицировать период полураспада указанного мутеина, можно выбрать из группы, состоящей из молекулы полиалкиленгликоля и гидроксиэтилкрахмала.
В дополнительном аспекте настоящее изобретение относится к мутеину липокалина 2 человека, обладающего обнаруживаемой аффинностью связывания, к определенному неприродному лиганду липокалина 2 человека, который можно получить или получен подробно описанными способами по изобретению.
В некоторых мутеинах липокалина 2 человека по изобретению природная дисульфидная связь между Cys 76 и Cys 175 удаляется. Следовательно, такие мутеины (или любой другой мутеин липокалина 2 человека, который не содержит внутримолекулярной дисульфидной связи) можно получить в клеточном компартменте, имеющем восстановительный потенциал среды, например, в цитоплазме грамотрицательных бактерий.
В том случае, когда мутеин липокалина по изобретению содержит внутримолекулярные дисульфидные связи, то может быть предпочтительным направить синтезирующийся полипептид в клеточный компартмент, имеющий окислительный потенциал среды с использованием соответствующей сигнальной последовательности. Такую окислительную среду можно обеспечить в периплазме грамотрицательных бактерий, таких как E. coli, во внеклеточной среде грамположительных бактерий или в просвете эндоплазматического ретикулюма в эукариотических клетках, и обычно он способствует образованию структурных дисульфидных связей.
Однако также возможно получить мутеин по изобретению в цитозоле клетки-хозяина, предпочтительно, E. coli. В этом случае полипептид можно получить непосредственно в растворимом и уложенном состоянии или выделить в форме телец включения с последующей ренатурацией в условиях in vitro. Дополнительной возможностью является применение специфических штаммов-хозяев, имеющих окислительную внутриклеточную среду, которая может таким образом способствовать образованию дисульфидных связей в цитозоле (Venturi et al. (2002) J. Mol.Biol., 315, 1-8).
Однако мутеин по изобретению необязательно можно получить или продуцировать только с использованием генной инженерии. Предпочтительнее мутеин липокалина также можно получить химическим синтезом, таким как твердофазный синтез полипептидов Меррифилда, или транскрипцией или трансляцией в условиях in vitro. Например, возможно, что многообещающие мутации идентифицируют с использованием молекулярного моделирования и затем синтезируют желаемый (планируемый) полипептид в условиях in vitro и исследуют активность связывания с определенной мишенью. Способы твердофазного и/или синтеза белков в растворе хорошо известны в данной области (см. обзор Lloyd-Williams et al. (1997), Chemical Approaches to the Synthesis of Peptides and Proteins. CRC Press, Boca Raton, Fields, GB and Colowick (1997) Solid-Phase Peptide Synthesis. Academic Press, San Diego or Bruckdorfer et al. (2004) Curr. Pharm. Biotechnol., 5, 29-43).
В еще одном варианте осуществления мутеины по изобретению можно получить трансляцией/транскрипцией в условиях in vitro с использованием общепринятых способов, известных специалистам в данной области.
Изобретение также относится к фармацевтической композиции, содержащей по меньшей мере один мутеин по изобретению, указанный в формуле изобретения, или слитый белок или его конъюгат, и необязательно фармацевтически приемлемый наполнитель.
Мутеины липокалина по изобретению можно вводить любым парентеральным или непарентеральным (энтеральным) путем, который эффективен для белковых препаратов. Парентеральные способы применения включают, например, внутрикожную, подкожную, внутримышечную или внутривенную инъекцию или инфузии, например, в виде инъекционных растворов, инфузионных растворов или настоек, а также инстилляцию или ингаляцию аэрозоля, например, в виде аэрозольных смесей, спреев или порошков. Непарентеральные способы доставки представляют, например, пероральный путь, например, в форме пилюль, таблеток, капсул, растворов или суспензий, или ректальный путь, например, в виде суппозиториев. Мутеины по изобретению можно вводить системно или местно в композициях, содержащих обычные нетоксичные фармацевтически приемлемые наполнители или носители, добавки и растворители, как это желательно.
В одном варианте осуществления настоящего изобретения фармацевтический препарат вводят парентерально млекопитающему и, в частности, людям. Соответствующие способы введения включают, не ограничиваясь этим, например, внутрикожную, подкожную, внутримышечную или внутривенную инъекцию или инфузии, например, в виде инъекционных растворов, инфузионных растворов или настоек, а также инстилляцию или ингаляцию аэрозолей, например, в виде аэрозольных смесей, спреев или порошков. Комбинация внутривенной и подкожной инфузии и/или инъекции может быть наиболее подходящей в случае соединений с относительно коротким периодом полураспада в сыворотке. Фармацевтическая композиция может представлять водный раствор, эмульсию масло-в-воде или эмульсию вода-в-масле.
В этом отношении следует отметить, что трансдермальные способы доставки, например, ионофорез, сонофорез или усиленная доставка с помощью микроиглы, описанная Meidan and Michniak (2004) Am. J. Ther., 11(4), 312-316, также можно использовать для трансдермальной доставки мутеинов, описанных в настоящем документе. Непарентеральные пути введения представляют, например, пероральное введение в форме пилюль, таблеток, капсул, растворов или суспензий, или ректальное введение, например, в виде суппозиториев. Мутеины по изобретению можно вводить системно или местно в композициях, содержащих обычные нетоксичные фармацевтически приемлемые наполнители или носители, добавки и растворители.
Дозировка используемого мутеина может варьировать в широких пределах для достижения желаемого профилактического или терапевтического ответа. Она будет зависеть, например, от аффинности соединения для выбранного лиганда, а также от периода полураспада комплекса мутеина и лиганда в условиях in vivo. Кроме того, оптимальная доза будет зависеть от биологического распределения мутеина или его слитого белка, или его конъюгата, способа введения, тяжести заболевания/расстройства, которое подвергается лечению, а также общего состояния пациента. Например, при использовании в виде мази для местного применения, можно использовать высокую концентрацию мутеина липокалина человека. Однако, если желательно, то мутеин также можно вводить в композиции с замедленным высвобождением, например, липосомальной дисперсии или полимерных микросферах на основе геля, таких как PolyActiveTM или OctoDEXTM (см. Bos et al., Business Briefing:Pharmatech., 2003:1-6).
Следовательно, мутеины по настоящему изобретению можно формулировать в композиции с использованием фармацевтически приемлемых ингредиентов, а также общепринятых методов получения (Gennaro and Gennaro (2000) Remington: The Science and Practice of Pharmacy, 20th Ed., Lippincott Williams&Wilkins, Philadelphia, PA). Для получения фармацевтических композиций можно использовать фармацевтически инертные неорганические и органические наполнители. Например, для приготовления пилюль, порошков, желатиновых капсул или суппозиториев, можно использовать лактозу, тальк, стеариновую кислоту и ее соли, жиры, воски, твердые или жидкие полиолы, природные и отверждаемые масла. Подходящие наполнители для приготовления растворов, суспензий, эмульсий, аэрозольных смесей или порошков для восстановления в растворы или аэрозольные смеси перед использованием включают воду, спирты, глицерин, полиолы и их подходящие смеси, а также растительные масла.
Фармацевтическая композиция также может содержать добавки, например, такие как наполнители, связующие вещества, смачивающее вещество, скользящие вещества, стабилизаторы, консерванты, эмульгаторы, и, кроме того, растворители или солюбилизаторы, или агенты для достижения депо-эффекта. Последнее представляет собой вариант, когда слитые белки могут аккумулироваться с медленным или замедленным высвобождением, или системы направленной доставки, такие как липосомы или микрокапсулы.
Композиции можно стерилизовать многочисленными способами, включая фильтрование через задерживающий бактерии фильтр, или включение стерилизующих агентов в виде стерильных твердых композиций, которые можно растворить в стерильной воде или другой стерильной среде непосредственно перед применением.
Мутеин по настоящему изобретению или слитый белок, или его конъюгат можно использовать во многих применениях. В общем, такой мутеин можно использовать во всех применениях, в которых используются антитела, за исключением таковых со специфичностью, основанной на гликозилировании Fc-фрагмента.
Следовательно, в еще одном аспекте изобретения мутеины по изобретению липокалина 2 человека используют для связывания и/или детектирования определенного неприродного лиганда липокалина человека. Такое применение может включать стадии приведения в контакт мутеина с образцом, в котором предположительно находится определенный лиганд, в подходящих условиях, обеспечивая тем самым образование комплекса мутеина и определенного лиганда, и детектирование мутеина в виде комплекса соответствующим сигналом.
Детектируемый сигнал можно обеспечить с помощью метки, как уже пояснялось выше, или изменением физических свойств за счет связывания, т.е. образования самого комплекса. Одним примером является поверхностный плазмонный резонанс, показатель, который изменяется во время связывания партнеров по связыванию, из которых один иммобилизован на поверхности, такой как золотая фольга.
Мутеины липокалина 2 человека, раскрытые в настоящем документе, также можно использовать для выделения определенного неприродного лиганда липокалина 2 человека. Такое применение может включать стадии приведения в контакт мутеина с образцом, в котором предположительно находится указанный лиганд, в подходящих условиях, с обеспечением тем самым образования комплекса мутеина и определенного лиганда, и выделение комплекса мутеин/лиганд из образца.
В обоих случаях при использовании мутеина для детектирования определенного неприродного лиганда, а также выделения определенного лиганда, мутеин и/или мишень можно иммобилизовать на подходящей твердой фазе.
Мутеины липокалина 2 человека по изобретению также можно использовать для направленной доставки соединения в заранее выбранное место. В одном таком варианте осуществления мутеин липокалина 2 человека используют для направленной доставки фармацевтически активного соединения в заранее выбранное место в организме или ткань, включающей:
(a) конъюгацию мутеина с указанным соединением и
(b) доставку комплекса мутеин/соединение в заранее определенное место.
Для этой цели мутеин приводят в контакт с интересующим соединением для обеспечения образования комплекса. Затем комплекс, содержащий мутеин и интересующее соединение, доставляется в заранее определенное место. Этого можно достичь, например, сочетанием мутеина с направляющей группой, такой как антитело, фрагмент антитела или мутеин липокалина или фрагмент мутеина липокалина с аффинностью связывания для выбранной мишени.
Данное применение, в частности, подходит, но не ограничивается этим, для доставки лекарственного препарата (избирательно) в заранее определенное место в организме, такое как инфицированная область, ткань или орган тела, которые предположительно лечатся лекарственным препаратом. Помимо образования комплекса мутеина и интересующего соединения мутеин также можно подвергнуть взаимодействию с определенным соединением с получением конъюгата мутеина и соединения. Аналогично вышеуказанному комплексу, такой конъюгат может подходить для доставки соединения в заранее выбранное место-мишень. Такой конъюгат мутеина и соединения также может содержать линкер, ковалентно связывающий мутеин и соединение друг с другом. Необязательно такой линкер является стабильным в кровяном русле, но расщепляется в клеточной среде.
Мутеины, раскрытые в настоящем документе, и его производные можно использовать таким образом во многих областях аналогично антителам или их фрагментам. В дополнении к их применению для связывания с подложкой, что позволяет иммобилизовать или выделить мишень данного мутеина или конъюгата, или слитого белка данной мишени, мутеины можно использовать для мечения ферментом, антителом, радиоактивным соединением или любой другой группой, обладающей биохимической активностью или определенной способностью к связыванию. При этом их соответствующие мишени или конъюгаты, или слитые белки можно детектировать или приводить в контакт с ними. Например, мутеины по изобретению могут служить для детектирования химических структур с помощью общепринятых аналитических методов (например, ELISA или вестерн-блоттинг), или микроскопией или иммуносенсорными методами. В данном случае детектирующий сигнал можно получить непосредственно с использованием подходящего конъюгата мутеина или слитого белка, или опосредованно, например, иммунохимическим детектированием связанного мутеина через антитело.
Многочисленные возможные применения мутеинов по изобретению также имеются в медицине. В дополнении к их применению в диагностике и доставке лекарственных препаратов можно получить мутантный полипептид по изобретению, который связывается, например, с тканеспецифическими или опухольспецифическими молекулами клеточной поверхности. Такой мутеин может, например, использоваться в конъюгированной форме или в виде слитого белка для «визуализации опухолей» или непосредственно для терапии рака.
Таким образом, настоящее изобретение относится к применению мутеинов липокалина 2 человека по изобретению для образования комплекса с определенным неприродным лигандом или мишенью.
В дополнительном аспекте настоящее изобретение также относится к применению мутеина по изобретению для производства фармацевтической композиции. Полученная таким образом композиция может быть пригодной для лечения нейродегенеративных расстройств, таких как болезнь Альцгеймера. Фармацевтическую композицию также можно использовать для лечения рака, лечения фиброза или лечения воспаления. Фармацевтическую композицию можно использовать в качестве монотерапии или комбинированной терапии.
В еще одном аспекте настоящее изобретение относится к диагностическому или аналитическому набору, содержащему мутеин по настоящему изобретению.
Еще один аспект настоящего изобретения относится к способу лечения индивида, страдающего нейродегенеративным заболеванием, или раком, или фиброзом, или воспалением, включающему введение соответствующего мутеина по изобретению или фармацевтической композиции, содержащей мутеин по изобретению, индивиду, нуждающемуся в этом.
Индивид, нуждающийся в таком лечении, может быть, если назвать только показательные примеры, человеком, собакой, мышью, крысой, свиньей, обезьяной, такой как cymologous обезьяны.
В еще одном аспекте настоящее изобретение относится к способу визуализации в условиях in vivo у индивида, включающему введение указанному индивиду мутеина по изобретению или фармацевтической композиции, содержащей мутеин по изобретению. Индивид можно определить, как приведено выше.
Изобретение также дополнительно иллюстрируется последующими неограничивающими примерами и прилагаемыми фигурами, где:
На фигуре 1 показана стратегия сборки ПЦР для одновременного случайного мутагенеза в 20 аминокислотных положениях 36, 40, 41, 49, 52, 68, 70, 72, 73, 77, 79, 81, 96, 100, 103, 106, 125, 127, 132 и 134 (подчеркнуты и пронумерованы) в аминокислотной последовательности зрелого Lcn2. Данные 20 положений разделены на четыре подгруппы последовательностей. Для рандомизации аминокислот в каждой подгруппе синтезировали олигодезоксинуклеотид (SEQ ID NO:1, SEQ ID NO:2, SEQ ID NO:3, SEQ ID NO:4), где использовали смеси NNK нуклеотидов в мутированных кодонах. N означает смесь всех четырех оснований A, C, G и Т, в то время как K означает смесь только двух оснований G и Т; следовательно, такой триплет кодирует все 20 природных аминокислот, а также amber стоп-кодон TAG, который транслируется в глутамин в supE-штаммах E. coli XL1-blue (Bullock et al. (1987), BioTechniques, 5, 376-378) или TG1 (Sambrook et al., Molecular Cloning. A Laboratory Manual (1989) Cold Spring Harbor Press), которые использовали для получения фагемида и экспрессии гена. Также в реакции сборки использовали четыре дополнительных олигодезоксинуклеотида (SEQ ID NO:5, SEQ ID NO:6, SEQ ID NO:7, SEQ ID NO:8) с фиксированными нуклеотидными последовательностями, соответствующими некодирующей цепи (показана ниже последовательности двухцепочечной ДНК в 3'-5'-направлении) и заполнение гэпов между вышеуказанными олигодезоксинуклеотидами. Два более коротких фланкирующих олигодезоксинуклеотида (SEQ ID NO:9, SEQ ID NO:10), которые добавляли в избытке и содержали группы биотина, служили в качестве праймеров для амплификации ПЦР собранного, полностью синтетического фрагмента гена. Два фланкирующих праймера, каждый включал сайт рестрикции BstXI (CCANNNNNNTGG), образуя взаимно несовместимые выступы при ферментативном расщеплении. Такое специфическое расположение сайтов рестрикции способствовало особенно эффективному лигированию и клонированию синтетического гена. Замена аминокислоты Gln28 на His по сравнению с исходной последовательностью Lcn2 была необходима для введения первого сайта BstXI, в то время как второй сайт имелся изначально в кДНК Lcn2. Кроме того, неспаренный остаток Cys87 замещали на Ser во время сборки гена. После одного раунда ПЦР полученный фрагмент гена вставляли в вектор, обеспечивая отсутствующие фрагменты структурного гена Lcn2. На данной фигуре также показаны два коротких праймера (SEQ ID NO:45 и SEQ ID NO:46), соответственно, слева и справа кассеты, фланкированной двумя сайтами рестрикции BstXI, которые служили для секвенирования двухцепочечной ДНК.
На фигуре 2 приведена нуклеотидная последовательность библиотеки синтетических генов Lcn2 (только центральная кассета, фланкированная двумя сайтами рестрикции BstXI, как показано на фигуре 1). Данный фрагмент гена готовили в Sloning BioTechnology GmbH. По сравнению с ДНК-библиотекой, представленной на фигуре 1, имеется два различия. Первое, там, где это было возможным, использовали кодоны, оптимизированные для экспрессии в E. coli, для немутированных аминокислотных положений. Второе, использовали смесь 19 различных триплетов (GAC, TTC, CTG, CAC, AAT, AGC, ACC, GCA, ATG, CCT, GTT, TGG, GAG, CAA, ATC, GGA, GGT, GCA, TAC), где каждый кодировал разную аминокислоту, за исключением Cys, в 20 рандомизированных положениях, которые идентичны положениям, представленным на фигуре 1. Нумерация аминокислот соответствует внутренней схеме, использованной Sloning BioTechnology GmbH, где Gly 1 является кодоном первой аминокислоты, непосредственно следующей слева от сайта рестрикции BstXI.
На фигуре 3 показаны профили SEC элюирования рекомбинантных Aβ слитых белков Trx-Aβ28 (А) и MBP-Aβ40 (В) после экспрессии в E. coli. В обоих случаях чистоту синтетического Aβ40 и рекомбинантного слитого Aβ белка оценивали SDS-PAGE (C). Оба слитых белка экспрессировали в цитоплазме E. coli JM83. После разделения клеток с помощью клеточного френч-пресса белки очищали аффинной хроматографией с His6-меткой и затем наносили на колонку Superdex 75 HR 10/30 в случае Trx-Aβ28 и Superdex 200 HR 10/30 в случае MBP-Aβ40. Оба белка элюировались в основном в виде мономера в эксклюзионной хроматографии и в основном были гомогенными после очистки. Aβ40 получали от Keck Foundation, обрабатывали HFIP, выпаривали в SpeedVac и, наконец, растворяли в дистиллированной H2O. Анализ в 15% геле показывает образцы Aβ40 после обработки HFIP и Trx-Aβ28 и MBP-Aβ40 после очистки IMAC и SEC. М представляет маркер молекулярной массы с соответствующим размером полос в кДа, расположенный в левой стороне геля.
На фигуре 4 показано перекрывание профилей элюирования SEC мутеинов Lcn2 H1-G1, S1-A4 и US7 (A) и анализ очищенных белков с использованием 15% SDS-PAGE (В). Три мутеина Lcn2 H1-G1, S1-A4 и US7 экспрессировали в периплазме E. coli JM83 или TG1-F (как показано) и очищали аффинной хроматографией со Strep-меткой II. Все три мутеина элюировались в основном в виде мономерных белков с колонки Superdex 75 HR 10/30 с объемом удерживания 10-11 мл. Максимальные интенсивности различались в зависимости от выхода экспрессии конкретного мутеина. (В) Показаны результаты анализа 15% SDS-PAGE рекомбинантного Lcn2 дикого типа (дорожки 1, 5) и мутеинов US7 (дорожки 2, 6), H1-G1 (дорожки 3, 7) и S1-A4 (дорожки 4, 8) после аффинной хроматографией со Strep-меткой II и SEC. Дорожки 1-4 показывают, что мутеины Lcn2 восстанавливались под действием 2-меркаптоэтанола, дорожки 5-8 показывают белки в нередуцирующих условиях. М представляет маркер молекулярной массы с соответствующим размером полос в кДа, расположенный в левой стороне геля.
На фигуре 5 показана активность связывания мутеинов Lcn2 H1-G1, S1-A4 и US7 в ELISA с иммунным захватом с различными биотинилированными Аβ-мишенями. StrepMAB-Immo в концентрации 10 мкг/мл иммобилизовали на микротитрационных планшетах и использовали для захвата 1 мкМ мутеинов Lcn2 через Strep-метку II. На фигуре А-С показано связывание мутеинов Lcn2 S1-A4 и US7 с (А) биотинилированным Аβ-40, (В) биотинилированным Trx-Aβ28 и (С) биотинилированным MBP-Aβ40. Связывание детектировали при инкубации с ExtrAvidin/AP и последующей хромогенной реакцией с pNPP. Овальбумин (Ova), тиоредоксин (Trx) и мальтоза-связывающий белок (MBP) использовали в качестве отрицательных контролей. Дополнительно тестировали связывание липокалина дикого типа (wt). По данным был построен график на основе модели моновалентного связывания. На фигуре D показана та же постановка ELISA с Lcn2 H1-G1 и биотинилированными Аβ-40 и Trx-Aβ28 в качестве мишеней. Определенные значения KD для Аβ-40 составили 2,7 нМ для S1-A4, 6,8 нМ для US7 и 16,2 нМ для H1-G1, соответствующие значения для Trx-Aβ28 равнялись 1,9 нМ, 2,4 нМ и 24,3 нМ. Связывание с MBP-Aβ40 показало значения KD, равные 4,7 нМ для S1-A4 и 11,4 нМ для US7. Следовательно, значения KD для Аβ16-27 составили 2,6 нМ и 2,1 нМ.
На фигуре 6 показана связывающая активность мутеинов Lcn2 S1-A4 и US7 в прямом ELISA. Аβ-мишени Trx-Aβ28 и MBP-Aβ40, а также контрольный мальтоза-связывающий белок (МВР) иммобилизовали в концентрации 2 мкМ в PBS в течение ночи. Связанные мутеины Lcn2 детектировали с помощью Strep-метки II с использованием стрептавидин/AP с последующей хромогенной реакцией с pNPP. В качестве контроля тестировали связывание липокалина дикого типа (wt). По данным был построен график на основе модели моновалентного связывания. Значения KD для Trx-Aβ28 составили 16,2 нМ для S1-A4 и 9,6 нМ для US7, соответствующие значения для MBP-Aβ40 равнялись 149 нМ и 49,7 нМ.
На фигуре 7 показана связывающая активность мутеинов Lcn2 S1-A4 (А) и US7 (В) в конкурентном ELISA. StrepMAB-Immo в концентрации 10 мкг/мл иммобилизовали на микротитрационных планшетах и использовали для захвата 1 мкМ мутеина Lcn2 через Strep-метку II. В конкурентном анализе биотинилированный Trx-Aβ28 в качестве маркера в постоянной концентрации смешивали с различными концентрациями немеченого Trx-Aβ28. Затем связанный биотинилированный Trx-Aβ28 детектировали при инкубации с ExtrAvidin/AP с последующей хромогенной реакцией с pNPP. По данным был построен график с использованием сигмоидального уравнения. Значения KD составили 21,7 нМ для S1-A4 и 76,9 нМ для US7.
На фигуре 8 показан кинетический анализ в режиме реального времени мутеинов Lcn2 S1-A4 (А) и US7 (В) на аппарате Biacore со скоростью потока 10 мкл/мин. Слитый белок MBP-Aβ40 присоединяли с использованием реакции сочетания аминов к чипу CMD 200I (∆RU=1455) и каждый из очищенных мутеинов Lcn 2 наносили последовательно в различных концентрациях. В каждом случае анализированный сигнал показан в виде серой линии, в то время кривая показана в виде черной линии. Значения kon и koff обоих мутеинов достоверно различались (kon (S1-A4)=0,48·105 М-1сек-1, kon (US7)=2,02·105 М-1сек-1, koff (S1-A4)=8,36·105 сек-1, koff (US7)=25,2·105 сек-1). Однако общие значения KD были очень схожими и составили 1,74 нМ для S1-A4 и 1,25 нМ для US7.
На фигуре 9 показана функциональная активность мутеинов Lcn2 S1-A4 и US7, анализированных в тесте агрегации тиофлавина Т. 100 мкМ Aβ40 инкубировали с 10 мкМ US7, S1-A4, липокалина дикого типа (wt) или с PBS при 37°С без встряхивания. На указанные временные интервалы 20 мкл каждой пробы смешивали с 180 мкл 5 мкМ раствора тиофлавина Т и определяли флуоресценцию при длине волны возбуждения 450 нм и волне эмиссии 482 нм. Мутеин Lcn2 US7 существенно ингибировал агрегацию в соотношении 1:10 (US7:Aβ40). S1-A4 был не способен достоверно ингибировать агрегацию при данном соотношении, но проявлял четкое ингибирование при соотношении 1:2 (S1-A4:Aβ40) (данные не приводятся). Lcn2 дикого типа не оказывал ингибирующего эффекта на агрегацию Aβ.
На фигуре 10 показаны результаты анализа SDS-PAGE, после окрашивания кумасси бриллиантовым синим, рекомбинантного ED-B (дорожка 1), FN7B8 (дорожка 2) и FN789 (дорожка 3) после ионообменной хроматографии. Все образцы восстанавливали 2-меркаптоэтанолом. М: маркер молекулярной массы (Fermentas, St. Leon-Rot, Германия).
На фигуре 11 показаны результаты анализа SDS-PAGE, после окрашивания кумасси бриллиантовым синим, Lcn2 мутеинов N7A (дорожка 1), N7E (дорожка 2), N9B (дорожка 3) и N10D (дорожка 4) после очистки аффинной хроматографией со Strep-меткой II. Все образцы восстанавливали 2-меркаптоэтанолом. М: маркер молекулярной массы (Fermentas, St. Leon-Rot, Германия).
На фигуре 12 представлены результаты оценки связывающей активности в ELISA. Микротитрационный планшет был покрыт серией разведений отобранных Lcn2 мутеинов с последующим детектированием с помощью конъюгата стрептавидин-щелочная фосфатаза и субстратом pNPP. Рекомбинантные Lcn2 мутеины N7A, N9B и N10D демонстрировали низкие сигналы в данном тесте для FN789, в котором отсутствовал ED-B и служили в качестве отрицательного контроля.
На фигуре 13 приведены результаты кинетического анализа в режиме реального времени Lcn2 мутеина N9B, полученные на аппарате Bicore. FN7B8 присоединяли с использованием реакции сочетания аминов к сенсорному чипу CMD 200 m (∆RU=500) и очищенный мутеин Lcn2 наносили в различных концентрациях. В каждом случае определенный сигнал показан в виде серой линии, в то время кривая показана в виде черной линии. Кинетические константы, установленные по данной серии кривых, приведены в таблице 2 (пример 17).
На фигуре 14 приведены результаты кинетического анализа в режиме реального времени Lcn2 мутеина N7E, определенные на аппарате Bicore. FN7B8 присоединяли с использованием реакции сочетания аминов к сенсорному чипу CMD 200 m (∆RU=500) и очищенный мутеин Lcn2 наносили в различных концентрациях. В каждом случае определенный сигнал показан в виде серой линии, в то время кривая показана в виде черной линии. Кинетические константы, установленные по данной серии кривых, приведены в таблице 2 (пример 17).
На фигуре 15 приведены результаты кинетического анализа в режиме реального времени Lcn2 мутеина N7A, определенные на аппарате Bicore. FN7B8 присоединяли с использованием реакции сочетания аминов к сенсорному чипу CMD 200 m (∆RU=500) и очищенный мутеин Lcn2 наносили в различных концентрациях. В каждом случае определенный сигнал показан в виде серой линии, в то время кривая показана в виде черной линии. Кинетические константы, установленные по данной серии кривых, приведены в таблице 2 (пример 17).
На фигуре 16 приведены результаты кинетического анализа в режиме реального времени Lcn2 мутеина N10D, определенные на аппарате Bicore. FN7B8 присоединяли с использованием реакции сочетания аминов к сенсорному чипу CMD 200 m (∆RU = 500) и очищенный мутеин Lcn2 наносили в различных концентрациях. В каждом случае анализированный сигнал показан в виде серой линии, в то время кривая показана в виде черной линии. Кинетические константы, установленные по данной серии кривых, приведены в таблице 2 (пример 17).
На фигуре 17 показано выравнивание последовательностей мутеинов Lcn2 человека, обозначенных S1-A4 (SEQ ID NO:39); US-7 (SEQ ID NO:41); H1-G1 (SEQ ID NO:43); N7A (SEQ ID NO:20); N7E (SEQ ID NO:22); N9B (SEQ ID NO:24) и N10D (SEQ ID NO:26) с Lcn2. Последняя линия ниже последовательностей указывает вторичные структурные признаки липокалина (Schonfeld et al. (2009) Proc. Natl. Acad. Sci. USA, 106, 8198-8203).
На фигуре 18 показано перекрывания профилей SEC элюирования мутеинов Lcn2 H1GA и H1GV (А), и анализ очищенных белков с использованием 15% SDS-PAGE (В). Мутеины Lcn2 H1GA и H1GV экспрессировали в периплазме E. coli JM83 и очищали аффинной хроматографией со Strep-меткой II. Оба мутеина преимущественно элюировались в виде мономерных белков с колонки Superdex 75 HR 10/30 с объемом удерживания 10-11 мл. Максимальные интенсивности различались в зависимости от выхода экспрессии конкретного мутеина. (В) Показаны результаты анализа 15% SDS-PAGE рекомбинантных мутеинов Lcn2 H1-G1, H1GA и H1GV после очистки аффинной хроматографией со Strep-меткой и SEC. Все мутеины Lcn2 показаны в восстанавливающих условиях с использованием 2-меркаптоэтанола. М представляет маркер молекулярной массы.
На фигуре 19 показана связывающая активность мутеинов Lcn2 H1GA, H1GV и H1-G1 в ELISA с иммунным захватом с биотинилированными Аβ-мишенями Аβ40 (А) и Trx-Aβ28 (B). StrepMAB-Immo в концентрации 10 мкг/мл иммобилизовали на микротитрационных планшетах и использовали для захвата 1 мкМ мутеинов Lcn2 через Strep-метку II. Затем детектировали связывание биотинилированных мишеней, нанесенных серией разведений, при инкубации с ExtrAvidin/AP и последующей хромогенной реакцией с pNPP. Биотинилированный овальбумин (Ova) и тиоредоксин (Trx) использовали в качестве отрицательных контролей, и они не показывали связывания с мутеинами Lcn2 (не показано). По данным был построен график на основе модели моновалентного связывания. Определенные значения KD для Аβ40 составили 4,2 нМ для H1GA, 4,9 нМ для H1GV и 21,5 нМ для H1-G1, соответствующие значения для Trx-Aβ28 равнялись 3,8 нМ, 4,2 нМ и 24,4 нМ, соответственно.
На фигуре 20 показан кинетический анализ в режиме реального времени мутеинов Lcn2 H1GA (А) и H1GV (В) на аппарате Biacore со скоростью потока 20 мкл/мин. Слитый белок MBP-Aβ40 присоединяли с использованием реакции сочетания аминов к чипу CMD 200I (∆RU=1316) и каждый из очищенных мутеинов наносили последовательно в различных концентрациях. В каждом случае анализированный сигнал показан в виде серой линии, в то время кривая показана в виде черной линии. Значения kon и koff обоих мутеинов были следующими kon (H1GA)=5,77·104 М-1сек-1, kon (H1GV)=6,84·104 М-1сек-1, koff (H1GA)=2,75·10-5 сек-1, koff (H1GV)=7,26·10-5 сек-1). Общие значения KD составили 0,476 нМ для H1GA и 1,06 нМ для H1GV.
На фигуре 21 показан кинетический анализ в режиме реального времени мутеина Lcn2 H1GA на аппарате Biacore Т100 с иммобилизованным Aβ40 с использованием увеличенного времени диссоциации для кривой, записанной при высокой концентрации. Пептид-мишень Aβ40 присоединяли с использованием реакции сочетания аминов к чипу Biacore CM5 (∆RU=325) и очищенный мутеин Lcn2 H1GA наносили со скоростью потока 30 мкл/мин. Для точного определения значения koff диссоциацию проводили в течение 7200 сек при самой высокой тестированной концентрации. Значения kon определяли с использованием серии разведений мутеина Lcn2 H1GA при одинаковом времени ассоциации и диссоциации, равном 300 сек. Определенные кинетические значения H1GA равнялись: kon=1,25·105 М-1сек-1, koff=1,18·10-5 сек-1 и KD=0,095 нМ.
На фигуре 22 (А) показана функциональная активность мутеина Lcn2 H1GA, тестированного в тесте агрегации тиофлавина Т. 500 мкл мономера Aβ с концентрацией 1 мг/мл инкубировали при отсутствии или в присутствии различных молярных соотношений мутеина Lcn2 H1GA в 0,5×PBS при 37°С при перемешивании. Реакции агрегации проводили в трех параллелях. Для определения флуоресценции 20 мкл образца, отобранные через периодические интервалы времени, в каждом случае смешивали с 180 мкл ThT до конечной концентрации 50 мкМ в 0,5×PBS и анализировали при длине волны возбуждения 450 нм и волне эмиссии 482 нм. Мутеин Lcn2 H1GA существенно ингибировал агрегацию в эквимолярном соотношении. При субэквимолярном соотношении 10:2 (Aβ40:H1GA) агрегация также была достоверно ниже. (В) В противоположность эквимолярные количества BSA и Lcn2, которые использовали в качестве отрицательных контролей, не оказывали ингибирующего действия на агрегацию Aβ40.
На фигуре 23 обобщены результаты определения значений KD, определенные при различной постановке ELISA, а также по данным поверхностного плазмонного резонанса для мутеинов Lcn2 H1GA и H1GV.
На фигуре 24 показано выравнивание последовательностей мутеинов Lcn2 S1-A4 (SEQ ID NO:39); US-7 (SEQ ID NO:41); H1-G1 (SEQ ID NO:43); H1GA (SEQ ID NO:50); H1GV (SEQ ID NO:52); N7A (SEQ ID NO:20); N7E (SEQ ID NO:22); N9B (SEQ ID NO:24) и N10D (SEQ ID NO:26) с Lcn2 (SEQ ID NO:44).
На фигуре 25 показано взаимное выравнивание последовательностей мутеинов H1-G1 (SEQ ID NO:50) и H1GV (SEQ ID NO:52) с их предшественником H1-G1 (SEQ ID NO:43) и Lcn2 дикого типа (SEQ ID NO:44).
На фигуре 26 показана специфическая связывающая активность варианта Lcn2 N7E для FN7B8 в ELISA. Микротитрационные планшеты покрывали FN7B8, FN789, BSA или овальбумином и инкубировали с серийными разведениями N7E с последующим детектированием с использованием конъюгата стрептавидин-щелочная фосфатаза и субстрата pNPP. Вариант Lcn2 N7E проявил незначительные сигналы в данном тесте для FN789, BSA или овальбумина.
На фигуре 27 приведены результаты кинетического анализа в режиме реального времени вариантов Lcn2 N7A (A), N7E (B), N9B (C) и N10D (D), определенные на аппарате Bicore X. Единичный домен фибронектина ED-B присоединяли с использованием реакции сочетания аминов к сенсорному чипу CMD 200 m (∆RU=180) и очищенные варианты Lcn2 наносили в различных концентрациях. Анализированные сигналы показаны в виде кривых вместе с графиками. Кинетические константы, установленные по данным сенсограммам, приведены в таблице 3 (пример 24).
На фигуре 28 показана аналитическая эксклюзионная хроматография вариантов Lcn2 N7A (A), N10D (B), N9B (C) и N7E (D). Очищенный аффинной хроматографией белок наносили на колонку Superdex S75 10/30, уравновешенную TBS. Стрелки указывают эксклюзионный объем колонки (6,7 мл). Аналитическая гель-фильтрация давала большой пик каждого из четырех вариантов Lcn2. Средняя молекулярная масса белков равнялась 21,0 кДа для N7A, 21,3 кДа для N10D, 21,7 кДа для N9B и 21,7 кДа для N7E, указывая на присутствие только мономерных форм.
Пример 1. Конструирование библиотеки мутантных Lcn2 в формате фагового дисплея
Готовили комбинаторную библиотеку вариантов Lcn2 на основе клонированной кДНК (Breustedt et al. (2006) Biochim Biophys. Acta, 1764, 161-173), которая несла аминокислотные замены Cys87Ser для удаления одной непарной тиоловой боковой цепи (Goetz et al. (2000) Biochemistry, 39, 1935-1941), а также Gln28His для введения второго сайта рестрикции BstXI. Мутагенез и сборку полимеразной цепной реакцией (ПЦР) в данной области в основном проводили согласно опубликованной стратегии (Beste et al. (1999) Proc. Natl. Acad. Sci. USA, 1898-1903; Skerra, J. (2001) Biotechnol., 74, 257-275), используя одну реакцию амплификации с олигодезоксинуклеотидами (SEQ ID NO:1-10), как показано на фигуре 1. Олигодезоксинуклеотиды конструировали таким образом, что праймеры с последовательностями SEQ ID NO:1-4 соответствовали кодирующей цепи и несли вырожденные кодоны в аминокислотных положениях 36, 40, 41, 49, 52, или 68, 70, 72, 73, 77, 79, 81, или 96, 100, 103, 106, 125, 127, 132 и 134 соответственно, в то время как праймеры с последовательностями SEQ ID NO:5-8 соответствовали некодирующей цепи и не содержали вырожденных кодонов или антикодонов. Два фланкирующих праймера с последовательностями SEQ ID NO:9 и SEQ ID NO:10 использовали в избытке, и они служили для амплификации собранного рандомизированного фрагмента гена. Все стадии ПЦР проводили с использованием ДНК-полимеразы Go-Taq Hot Start (Promega, Mannheim, Германия), как описано (Schlehuber et al., J. Mol. Biol., (2000), 297, 1105-1120).
Олигодезоксинуклеотиды, которые не несли вырожденных кодонов, получали от Metabion с чистотой для ВЭЖХ (Munich, Германия). NNK-содержащие олигодезоксинуклеотиды получали обессоленными от того же поставщика и затем очищали PAGE с мочевиной. Полученную ДНК-библиотеку расщепляли с использованием BstXI (Promega, Mannheim, Германия) и клонировали в фагемидный вектор phNGAL102 (SEQ ID NO:11), который основан на общем векторе экспрессии pASK111 (Vogt and Skerra, J. Mol. Recognit., 2001, 14(1), 79-86), и кодирует слитый белок, состоящий из сигнального пептида OmpA, модифицированного зрелого Lcn2 с последующим amber-кодоном и С-концевым фрагментом белка оболочки гена III нитчатого бактериофага М13, т.е. аналогичный описанному для билин-связывающего белка (Beste et al., выше; Skerra, выше). После электропорации E. coli XL1-Blue (Bullock et al., Biotechniques, 1987, 5, 376-378) со смесью для лигирования, состоящей из 8,4 мкг расщепленного продукта ПЦР и 94 мкг расщепленной ДНК-плазмиды, получали 1×1010 трансформантов.
Альтернативно, клонированную синтетическую произвольную библиотеку Lcn2, приведенную на фигуре 2, получали от Sloning BioTechnology GmbH (Puchheim, Германия). Центральную генную кассету, фланкированную двумя сайтами рестрикции BstXI, амплифицировали ПЦР в 20 циклах с использованием соответствующих праймеров (SEQ ID NO:9 и SEQ ID NO:10) и субклонировали в phNGAL108 (SEQ ID NO:12) с получением библиотеки со сложностью, соответствующей 1,7×1010 независимых трансформантов. phNGAL108, который основан на общем векторе экспрессии pASK75 (Skerra., Gene, 1994, 151, 131-135), кодирует слитый белок, состоящий из сигнального пептида OmpA, модифицированного зрелого Lcn2, Strep-метки с последующим amber-кодоном и полноразмерным белком оболочки гена III нитчатого бактериофага М13 (Vogt and Skerra (2004) ChemBioChem, 5, 191-199).
Последующие стадии получения библиотеки проводили одинаково для обеих библиотек Lcn2. 100 мкл культуры, содержащей клетки, которые трансформировали фазмидными векторами на основе phNGAL102 или phNGAL108, соответственно, кодирующих библиотеку мутеинов липокалина в виде слитых белков фага pIII, переносили в стерильную колбу Эрленмейра и инкубировали в течение 1 ч при 37°С, 160 об/мин в среде 2Y без селекционного давления антибиотиков. Перед инфицированием фагом-хелпером VCS-M13 культуру разводили средой 2Y до оптической плотности, составляющей OD550 0,1, с добавлением соответствующего антибиотика и затем культивировали в идентичных условиях, пока значение OD550 не достигало 0,6. После инфицирования фагом-хелпером VCS-M13 (Agilent Technologies, La Jolla, США) при множественности инфекции, равной примерно 10, культуру встряхивали еще в течение 30 мин при 37°С, 100 об/мин. Затем температуру термостата снижали до 26°С и скорость шейкера вновь увеличивали до 160 об/мин, через 10 мин добавляли канамицин (70 мкг/мл) с последующей индукцией экспрессии гена добавлением ангидротетрациклина (ACROS Organics, Geel, Бельгия) в концентрации 25 мкг/мл (125 мкл стокового раствора с концентрацией 200 мкг/мл в диметилформамиде, ДМФА на литр культуры). Инкубацию продолжали еще в течение 12-15 ч при 26°, 160 об/мин.
Клетки из полной культуры осаждали центрифугированием (30 мин, 18000 g, 4°С). Супернатант, содержащий фагемидные частицы, стерилизовали фильтрованием (0,45 мкм), смешивали с 1/4 объема 20% масс./об. ПЭГ 8000, 15% масс./об. NaCl и инкубировали на льду по меньшей мере в течение 2 ч. После центрифугирования (30 мин, 18000 g, 4°С) осажденные фагемидные частицы из 1 л культуры растворяли в 30 мл холодного BBS/E (200 мМ Na-бората, 160 мМ NaCl, 1 мМ ЭДТА, рН 8,0), содержащего 50 мМ бензамидина (Sigma) и Pefabloc 1 мкг/мл (Roth, Karlsruhe, Германия). Раствор инкубировали на льду в течение 1 ч. После осаждения нерастворенных компонентов центрифугированием (10 мин, 43000 g, 4°С), каждый супернатант переносили в новый реакционный сосуд.
Добавление 1/4 объема 20% масс./об. ПЭГ 8000, 15% масс./об. NaCl и инкубация в течение 60 мин на льду служили для репликации фагемидных частиц до того, как фагемиды разливали на аликвотные порции и замораживали при -80°С для хранения. Для первого цикла отбора фагемиды оттаивали и центрифугировали (30 мин, 34000 g, 4°С), супернатант удаляли и осажденные фагемидные частицы растворяли и объединяли в общем объеме 400 мкл PBS, содержащем 50 мМ бензамидина. После инкубации в течение 30 мин на льду раствор центрифугировали (5 мин, 18500 g, 4°С) для удаления остаточных агрегатов и супернатант непосредственно использовали для отбора фаговым дисплеем.
Пример 2. Приготовление Aβ мишеней в различных форматах
Aβ40 пептид (SEQ ID NO:29), соответствующий аминокислотам 1-40 зрелой бета-амилоидной последовательности (Dodel et al. (2003) Lancet Neurology, 2, 215-220) получали в виде синтетического, лиофилизованного пептида с С-концевой группой биотина, присоединенной через лизиновый спейсер (Peptide Speciality Laboratory, Heidelberg, Германия), или в форме без метки (W. M. Keck Laboratory, New Haven, США). Гомогенно мономерный Aβ40 получали растворением 5 мг пептида в 0,5 мл 1,1,1,3,3,3-гексафтор-2-пропанола (HFIP; Sigma-Aldrich, Steinheim, Германия) при комнатной температуре по меньшей мере в течение 0,5 ч. Затем HFIP выпаривали в SpeeVac концентраторе и Aβ40 растворяли в соответствующем объеме дистиллированной Н2О с последующей обработкой ультразвуком (Bandelin, Sonorex, RK100, Германия) в холодной воде в течение 15 мин. После фильтрования на фильтре с размером пор 0,22 мкм (Spin-X Centrifuge Tube Filter, Corning, США) определяли концентрацию белка по поглощению при 280 нм с использованием расчетного коэффициента экстинкции, равного 1490 М-1см-1 (Gasteiger et al., (2003) ExPASy: the proteomics server for in depth protein knowledge and analysis. Nucleic Acids Res., 31, 3784-3788, http://www.expasy.ch/tools/proparam.html).
Более короткие варианты бета-амилоидного пептида, такие как N-концевой Aβ1-11 пептид (SEQ ID NO:30) и центральный Aβ16-27 пептид (SEQ ID NO:31) также получали от Peptide Speciality Laboratory. Более короткие варианты непосредственно растворяли в выбранном буфере без предварительной обработки HFIP.
В дополнении к синтетическим пептидам конструировали два вектора, кодирующих различные рекомбинантные Aβ слитые белки, для экспрессии в бактериях. Вначале конструировали слитый белок с мальтоза-связывающим белком (MBP, pMBP-His, SEQ ID NO:32) по методу Hortscansky et al. ((2005) Protein Sci., 14, 1753-1759) с получением pASK75-MBP-Abeta40 (SEQ ID NO:33). Затем конструировали pASK75-TrxAbeta28H6 (SEQ ID NO:34), в который вставляли аминокислоты 1-28 зрелого амилоидного пептида в петлю активного сайта тиоредоксина (Trx, pASK75-TrxH6, SEQ ID NO:35), по методу Moretto et al. ((2007) J. Biol. Chem., 282, 11436-11445).
Последующее клонирование Aβ40 человека, несущего приращенный N-конец в рамке считывания с геном мальтоза-связывающего белка, давало новую плазмиду pASK75-MBP-Aβ40, производное вектора pASK75 (Scerra, Gene, 1994, 151, 131-135). Данный вектор кодирует слитый белок из мальтоза-связывающего белка с последующей His6-меткой для легкой очистки белка, сайта узнавания вируса гравировки табака etch (TEV) для расщепления слитого белка, а также последовательность Aβ40 человека. Вектор находится под тесным контролем тетрациклиновой системы промотор/оператор и позволяет экспрессировать слитые белки с высокими выходами в цитоплазме E. coli.
Последовательность, кодирующую аминокислоты 1-28 зрелого амилоидного пептида (Aβ28), вставляли в петлю тиреодоксина через уникальный сайт CpoI, находящийся в петле активного сайта тиоредоксина (нуклеотидные положения 99-105, соответствующие аминокислотным остаткам 34 и 35) с получением вектора pASK75-Trx-Abeta28H6.
Оба Aβ слитых белка, Trx-Aβ28 и MBP-Aβ40, а также неслитые контрольные белки Trx и MBP экспрессировали в E. coli JM83 (Yanisch-Perron et al., Gene, 1985, 33, 103-119) при 37°С. Экспрессию белка индуцировали при оптической плотности OD550, равной 0,5, добавлением 200 мкг/л ангидротетрациклина (aTc; Acros, Geel, Бельгия), растворенного в несодержащем воды диметилформамиде (ДМФА; Sigma-Aldrich, Steinheim, Германия), и постоянной инкубации со встряхиванием в течение 3 ч. Клетки собирали центрифугированием при 4200g при 4°С в течение 20 мин. Клеточный осадок после центрифугирования из 2 л культуры ресуспендировали в 20 мл лизирующего буфера (100 мМ Трис/HCl буфер, рН 8,0, 50 мМ NaCl, 1 мМ ЭДТА) и полученную суспензию гомогенизировали трехкратным пропусканием через клеточный френч-пресс. Нерастворенное вещество удаляли центрифугированием (34500 g, 4°С, 20 мин), супернатант фильтровали на фильтре с размером пор 0,45 мкм (Filtpour S 0,45; Sarstedt, Nuembrecht, Германия) и использовали для аффинной хроматографии через His6-метку каждого белка. После аффинной хроматографии с иммобилизованным ионом металла (IMAC) слитые белки дополнительно очищали эксклюзионной хроматографией (SEC).
Концентрацию белка определяли по поглощению при 280 нм с использованием расчетных коэффициентов экстинкции 66350 М-1см-1 для MBP (SEQ ID NO:32), 69330 М-1см-1 для MBP-Aβ40 (SEQ ID NO:33), 15470 М-1см-1 для Trx-Aβ28 (SEQ ID NO:34) и 13980 М-1см-1 для Trx (SEQ ID NO:35) (Gasteiger et al., выше).
Для последующих опытов оба Aβ слитых белка, Trx-Aβ28 и MBP-Aβ40, а также овальбумин (Ova; Sigma-Aldrich, Steinheim, Германия), Trx и MBP, которые служили в качестве контрольных белков, метили биотином или дигоксигенином (DIG) при молярном соотношении 2:1 (реагент для введения метки: белок-мишень).
Для этого N-гидроксисукцинимидный эфир D-биотиноил-ε-аминокапроновой кислоты или N-гидроксисукцинимидный эфир дигоксигенин-3-О-метилкарбонил-ε-аминокапроновой кислоты (Roche Diagnostics, Mannheim, Германия), растворенные в несодержащем воды диметилформамиде (ДМФА; Sigma-Aldrich, Steinheim, Германия) или диметилсульфоксиде (ДМСО; Sigma-Aldrich, Steinheim, Германия), добавляли в 2-кратном молярном соотношении к белку в PBS (4 мМ KH2PO4, 16 мМ Na2HPO4, 115 мМ NaCl, рН 7,4). Смесь перемешивали в течение 1 ч при комнатной температуре. Затем добавляли 1 М Трис/HCl буфер, рН 8,0 до конечной концентрации 10 мМ и инкубировали в течение 10 мин для насыщения оставшихся активных NHS-эфирных групп и меченые белки очищали SEC или на колонке Superdex 75 HR 10/30 (Amersham-Pharmacia, Freiburg, Германия). Для применения в качестве мишени при отборе фаговым дисплеем Trx-Aβ28 вначале метили дигоксигенином в течение 1 ч, затем - блокировали неспаренные остатки Cys - добавляли 50-молярный избыток иодоацетамида (Sigma-Aldrich, Steinheim, Германия) с последующей инкубацией в течение 1 ч. Затем модифицированный белок обрабатывали 1 М Трис/HCl буфером, рН 8,0 и очищали, как описано выше.
Пример 3. Отбор мутеинов Lcn2 с аффинностью к Aβ40 пептиду фаговым дисплеем
Для каждого цикла пэннинга примерно 1012 рекомбинантных фагемид в PBS (4 мМ KH2PO4, 16 мМ Na2HPO4, 115 мМ NaCl, рН 7,4) блокировали 2% (масс./об.) BSA в PBS/T (PBS, содержащем 0,1% (об./об.) твина 20 [полиоксиэтиленсорбитан монолаурат; AppliChem, Darmstadt, Германия]) в течение 1 ч. Порции 50 и 25 мкл суспензии покрытых стрептавидином магнитных шариков (Dynabeads M-280 Streptavidin; Dynal Biotech, Invitrogen, Karlsruhe, Германия и Streptavidin Magnetic Particles; Roche Diagnostics, Mannheim, Германия) по отдельности промывали PBS/T и блокировали 2% (масс./об.) BSA в течение 1 ч. 25 мкл блокированных шариков использовали для предварительной адсорбции блокированных фагемид для удаления фагемид, специфичных для шариков, и 50 мкл использовали позднее для отборочного цикла.
Блокированные фагемиды инкубировали в течение 30 мин с 25 мкл отмытыми и блокированными магнитными шариками, покрытыми стрептавидином. Затем шарики опускали с помощью одной магнитной трубчатой подставки (Promega, Mannheim, Германия) в течение 2 мин, и супернатант, содержащий фагемиды, не связанные с шариками, инкубировали в течение 1-2 ч с 100 нМ биотинилированного Aβ40 из примера 2 в общем объеме 400 мкл. Затем смесь фагемид и мишени-пептида инкубировали в течение 0,5 ч с 50 мкл блокированных шариков и затем опускали с помощью одной магнитной трубчатой подставки в течение 2 мин. Супернатант, содержащий несвязанные фагемиды, отбрасывали. Комплексы мишень/фагемиды, связанные с магнитными шариками, промывали 10 раз 400 мкл PBS/T и затем связанные фагемиды элюировали при вращении в течение 10 мин 350 мкл смеси 0,1 М глицин/HCl, рН 2,2 с последующей немедленной нейтрализацией 55 мкл 0,5 М Трис-основания. Альтернативно элюирование проводили в денатурирующих условиях с 400 мкл 4 М мочевины в PBS в течение 30 мин с последующим разведением 1 мл PBS. Элюирование в денатурирующих условиях проводили с использованием кислоты или мочевины для циклов отбора 1 и 2, в то время как элюирование в циклах 3 и 4 проводили в конкурентных условиях при добавлении 400 мкл 10 мкМ небиотинилированного Aβ40 к шарикам со связанными фагемидами и вращением в течение 1 ч. В целом проводили 4 цикла отбора.
Для амплификации элюированных фагемид культуру E. coli XL-1 Blue в фазе экспоненциального роста инфицировали в течение 30 мин при 37°С. Оставшиеся связанные с шариками фагемиды элюировали добавлением E. coli XL-1 Blue в фазе экспоненциального роста непосредственно к шарикам. После центрифугирования при 4°С бактериальный осадок ресуспендировали в подходящем объеме среды 2× YT (16 г/л триптона Bacto, 10 г/л дрожжевого экстракта Bacto, 5 г/л NaCl, рН 7,5), высевали на чашки с LB-Cam (10 г/л триптона Bacto, 5 г/л дрожжевого экстракта Bacto, 5 г/л NaCl, 15 г/л агара Bacto, 35 мг/л хлорамфеникола, рН 7,5) и инкубировали в течение 14-16 ч при 32°С. Затем клетки соскребали с чашек и использовали для высвобождения и повторной амплификации рекомбинантных фагемид.
Скрининг обогащенных пулов фагемид проводили скринингом ELISA (пример 5) после четвертой стадии пэннинга.
Пример 4. Отбор мутеинов Lcn2 с аффинностью к слитому белку Trx-Aβ28 фаговым дисплеем
Для каждого цикла пэннинга примерно 1012 рекомбинантных фагемид в PBS (4 мМ KH2PO4, 16 мМ Na2HPO4, 115 мМ NaCl, рН 7,4) вначале блокировали в течение 1 ч 2% (масс./об.) BSA в PBS/T (PBS, содержащем 0,1% (об./об.) твина 20) для циклов 1 и 2. Начиная с цикла отбора 3, в качестве блокирующего реагента использовали 2% (масс./об.) снятое молоко (Sucofin, TSI, Zeven, Германия). Порции 50 и 25 мкл суспензии покрытых анти-DIG-IgG магнитных шариков (Europa Bioproducts Ltd., Cambridge, Великобритания), промывали PBS/T и по отдельности блокировали 2% (масс./об.) BSA в течение 1 ч или снятым молоком.
Блокированные фагемиды инкубировали в течение 30 мин с 25 мкл отмытыми и блокированными магнитными шариками, покрытыми анти-DIG-IgG. Затем шарики опускали с помощью одной магнитной трубчатой подставки (Promega, Mannheim, Германия) в течение 2 мин и супернатант, содержащий фагемиды, не связанные с шариками, инкубировали в течение 30 мин с 15 мкМ немеченого Trx из примера 2 для удаления фагемид, специфичных для Trx. Затем добавляли дигоксигенированный и карбоксиметилированный Trx-Aβ28 из примера 2 до конечной концентрации 100 нМ и смесь инкубировали в течение 1-2 ч в общем объеме 400 мкл. Затем смесь фагемид, Trx и Trx-Aβ28 инкубировали с высушенными, блокированными шариками из порции в 50 мкл в течение 0,5 ч. Затем шарики опускали с помощью одной магнитной трубчатой подставки в течение 2 мин. Супернатант, содержащий несвязанные фагемиды, отбрасывали. Магнитные шарики со связанными фагемидами промывали 10 раз 500 мкл PBS/T. Затем связанные фагемиды элюировали при вращении в течение 30 мин 400 мкл 4 М мочевины в PBS в течение 30 мин с последующим разведением 1 мл PBS. В целом проводили 6 циклов отбора.
Для амплификации элюированных фагемид культуру E. coli XL-1 Blue в фазе экспоненциального роста инфицировали в течение 30 мин при 37°С. Оставшиеся связанные с шариками фагемиды элюировали добавлением E. coli XL-1 Blue в фазе экспоненциального роста непосредственно к шарикам. После центрифугирования при 4°С бактериальный осадок ресуспендировали в подходящем объеме среды 2× YT (16 г/л триптона Bacto, 10 г/л дрожжевого экстракта Bacto, 5 г/л NaCl, рН 7,5), высевали на чашки с LB-Cam (10 г/л трипотона Bacto, 5 г/л дрожжевого экстракта Bacto, 5 г/л NaCl, 15 г/л агара Bacto, 35 мг/л хлорамфеникола, рН 7,5) и инкубировали в течение 14-16 ч при 32°С. Затем клетки соскребали с чашек и использовали для высвобождения и повторной амплификации рекомбинантных фагемид.
Скрининг обогащенных пулов фагемид проводили скрининговым анализом колоний с фильтром-сэндвичем (пример 6) после шестой стадии пэннинга.
Пример 5. Идентифицикация мутеинов Lcn2, специфичных для Aβ, скрининговым ELISA
После четырех циклов отбора фагемид с Aβ40, как описано в примере 3, обогащенный пул мутеинов Lcn2 субклонировали в phNGAL98 (SEQ ID NO:27), использованный для трансформации штамма TG1-F- E. coli (производное E. coli K12 TG1 (Kim et al. (2009) J. Am. Chem. Soc., 131, 3565-3576) и подвергали скрининговым ELISA.
Для данной цели единичные колонии из обогащенного пула культивировали в 96-луночных планшетах (мультилуночный планшет 96 с круглым дном с крышкой; Sarstedt, Nuembrecht, Германия) в 10 мкл среды TB-Amp (12 г/л триптона Bacto, 24 г/л дрожжевого экстракта Bacto, 55 мМ глицерина, 17 мМ KH2PO4, 72 мМ K2HPO4, 100 мг/л ампициллина) при 37°С в течение ночи. В новый планшет вносили 100 мкл среды TB-Amp с ночными культурами и культивировали до фазы экспоненциального роста при 22°С или 37°С. Экспрессию мутеинов Lcn2 в периплазме индуцировали 20 мкл 0,2 мкг/мл ангидротетрациклина (aTc; Acros, Geel, Бельгия), растворенного в несодержащем воде диметилформамиде (ДМФА; Sigma-Aldrich, Steinheim, Германия) в течение 13-17 ч при 20°С. Периплазматические белки высвобождали 40 мкл BBS (800 мМ Na-бората, 640 мМ NaCl, 8 мМ ЭДТА, рН 8,0), содержащем 1 мг/мл лизоцима при инкубации в течение 1 ч при 4°С и с встряхиванием при 750 об/мин (Thermomixer Comfort, Eppendorf, Hamburg, Германия). После блокирования 40 мкл 10% (масс./об.) BSA в PBS/T (4 мМ KH2PO4, 16 мМ Na2HPO4, 115 мМ NaCl, рН 7,4 с 0,05% (об./об.) твина 20) в течение 1 ч при 4°С и 750 об/мин планшеты центрифугировали в течение 10 мин при 4°С и 3000 g. Супернатант использовали для ELISA.
Для селективного захвата мутеинов Lcn2, содержащих С-концевую Strep-метку II (Schidt and Skerra, Nat. Protocol., 2007, 2, 1528-1535), 96-луночный микротитрационный планшет MaxiSorp из полистирола (Nunc, Langenselbold, Германия) покрывали 10 мкг/мл StrepMAB-Immo (IBA, Gottingen, Германия) в PBS течение ночи при 4°С и блокировали 3% (масс./об.) BSA в PBS/T (PBS с 0,1% (об./об.) твина 20) при комнатной температуре в течение 1 ч. После 3 стадий отмывки PBS/T, 120 мкл клеточного экстракта из вышеуказанной смеси вносили в лунку инкубировали в течение 1,5 ч при 300 об/мин. После отмывки биотинилированный Aβ40 из примера 2 вносили в концентрации 0,5 мкМ и инкубировали в течение 1 ч. В качестве контроля использовали биотинилированный Ova вместо Aβ40. Лунки вновь промывали и биотинилированный пептид или белок детектировали с использованием 50 мкл конъюгата ExtrAvidin/AP (Sigma-Aldrich, Steinheim, Германия) в разведении 1:5000 в PBS/T в течение 1 ч с последующим развитием сигнала в присутствии 100 мкл 0,5 мг/мл п-нитрофенилфосфата (AppliChem, Darmstadt, Германия) в 100 мМ Трис/HCl буфера, рН 8,8, 100 мМ NaCl, 5 мМ MgCl2 в течение 1 ч. Определяли поглощение при длине волны 405 нм на ридере SpectraMax 250 (Molecular Devices, Sunnyvale, США).
Альтернативно 0,5 мкМ небиотинилированного Aβ40 из примера 2 непосредственно иммобилизовали на 96-луночном микротитрационном планшете из полистирола MaxiSorp (Nunc, Langenselbold, Германия) с последующим блокированием. После инкубации с клеточным экстрактом, как описано выше, и отмывки связанные мутеины Lcn2 детектировали по Strep-метке II с использованием разведения 1:1500 конъюгата стрептактин/AP (IBA, Gottingen, Германия). В качестве контроля 0,5 мкМ Ova иммобилизовали на планшете для постановки ELISA.
Пример 6. Идентифицикация мутеинов Lcn2, специфичных для Trx-Aβ28 с использованием скринингового анализа колоний с фильтром-сэндвичем
После шести циклов отбора фагемид с Trx-Aβ28, как описано в примере 4, мутированную кассету гена Lcn2 субклонировали с помощью BstXI (Fermentas, St. Leon-Rot, Германия) в плазмиду phNGAL124 (SEQ ID NO:42), которая кодирует слитый белок из сигнального пептида OmpA, Lcn2-кодирующей области с С-концевой Strep-меткой II (Schmidt and Skerra (2007) Nat. Protoc., 2, 1528-1535), и последующего amber стоп-кодона, а также гена альбумин-связывающей области (ABD) из стрептококкового альбумин-связывающего белка G (Schlehuber et al., J. Mol. Biol., 2000, 297, 1105-1120).
Затем проводили скрининговый анализ колоний с фильтром-сэндвичем, посредством которого из колоний высвобождались слитые белки Lcn2-ABD, высеянные на гидрофильную фильтровальную мембрану (PVDF типа GVWP, 0,22 мкм; Millipore, Schwalbach, Германия) и функционально захватывались низлежащей второй мембраной (Immobilon-P, 0,45 мкм; Millipore, Schwalbach, Германия), покрытой сывороточным альбумином человека (HSA, Sigma-Aldrich, Steinheim, Германия), следуя протоколу, подробно описанному Schlehuber et al., J. Mol. Biol., 2000, 297, 1105-1120). Эту мембрану зондировали 100 нМ DIG-меченного Trx-Aβ28 из примера 2 в PBS/T в течение 1 ч. Конъюгат связанной мишени детектировали с использованием конъюгата анти-DIG Fab/щелочная фосфатаза (AP) (Roche Diagnostics, Mannheim, Германия) с последующим проведением хромогенной реакции с 5-бром-4-хлор-3-индолилфосфатом, солью 4-толуидина (BCIP; AppliChem, Darmshdt, Германия) и нитротетразолием синим (NBT; AppliChem, Darmshdt, Германия). Имея идентифицированные пятна с интенсивными окрашенными сигналами на этой мембране, собирали соответствующие колонии с первого фильтра и размножали рядом в сравнении во вторичном скрининге колоний.
Для данной цели выделенные бактерии, а также бактерии, экспрессирующие контрольные мутеины Lcn2, такие как липокалин дикого типа, наносили на свежую гидрофильную мембрану и культивировали до того, как небольшие колонии становились видимыми. Связывание тестировали для DIG-меченного Aβ28, а также для DIG-меченных контрольных белков Trx и Ova. Мутеины Lcn2, которые давали специфические сигналы для мишени Trx-Aβ28 в данном вторичном скрининге, дополнительно размножали для выделения плазмиды и последующего анализа последовательности.
Пример 7. Продукция в растворимом виде и очистка мутеинов Lcn2, специфичных для Aβ и ED-B
Рекомбинантный Lcn2 и его мутеины получали секрецией в периплазму в E. coli BL21 (Studer and Moffat, J. Mol. Biol., 1986, 189, 113-130), E. coli W31110 (Bachmann, Microbiol. Rev., 1990, 54, 130-197), E. coli JM83 (Yanish-Perron et al., Gene, 1985, 33, 103-119) или штамм TG1-F- E. coli (производное E. coli K12 TG1 [Kim et al., J. Am. Chem. Soc., 2009, 131, 3565-3576], который освобождали от его эписомы с использованием акридинового оранжевого). Для экспрессии белка в растворимом виде использовали плазмиду phNGAL98 (SEQ ID NO:27), кодирующую слитый белок из сигнального пептида OmpA со зрелым белком Lcn2 (SEQ ID NO:28) и С-концевой Strep-меткой II, посредством чего плазмида несла два несовместимых сайта рестрикции BstXI для ненаправленного субклонирования мутированной генной кассеты.
Растворимый белок очищали аффинной хроматографией с использованием Strep-метки II (Schidtand Skerra, Natl. Proc., 2007, 2, 1528-1535) с последующей эксклюзионной хроматографией (SEC) на колонке Superdex 75 HR 10/30 (Amerhsham-Pharmacia, Freiburg, Германия) с использованием PBS буфера. Чистоту белка проверяли с использованием SDS-PAGE (Fling and Gregerson, Anal. Biochem, 1986, 155, 83-88). Концентрацию белка определяли по поглощению при 280 нм с использованием расчетных коэффициентов экстинкции 31400 М-1см-1 для Lcn2 дикого типа (SEQ ID NO:44) и 26930 М-1см-1 для Аβ-специфических мутеинов H1-G1 (SEQ ID NO:43), 24410 М-1см-1 для S1-A4 (SEQ ID NO:38) и 26930 М-1см-1 для US7 (SEQ ID NO:41). Расчетные коэффициенты экстинкции для ED-B-специфических мутеинов Lcn2 составили 37930 М-1см-1 для мутеина N7A (SEQ ID NO:20), 22920 М-1см-1 для N7E (SEQ ID NO:22), 21430 М-1см-1 для N9B (SEQ ID NO:24) и 39420 М-1см-1 для N10D (SEQ ID NO:26) (Gasteiger et al., выше).
Пример 8. Определение связывающей активности для различных Aβ мишеней в опытах с ELISA
Для селективного захвата мутеинов Lcn2, содержащих С-концевую Strep-метку II (Schidt and Skerra (2007) Nat. Protocol., 2, 1528-1535), 96-луночный микротитрационный планшет MaxiSorp из полистирола (Nunc, Langenselbold, Германия) покрывали 10 мкг/мл StrepMAB-Immo (IBA, Gottingen, Германия) в PBS в течение ночи при 4°С и блокировали 3% (масс./об.) BSA в PBS/T при комнатной температуре в течение 1 ч. После 3 стадий отмывки PBS/T, 50 мкл 1 мкМ раствора очищенных мутеинов Lcn2 из примера 7 вносили во все лунки на 1 ч. После отмывки по 50 мкл серии разведений биотинилированных мишеней Aβ40, MBP-Aβ40 или Trx-Aβ28 из примера 2 вносили и инкубировали в течение 1 ч, при этом биотинилированные формы Ova, MBP и Trx из примера 2 служили в качестве отрицательных контрольных белков. Лунки вновь промывали и связанный конъюгат детектировали с 50 мкл конъюгата ExtrAvidin/AP (Sigma-Aldrich, Steinheim, Германия) в разведении 1:5000 в PBS/T в течение 1 ч с последующим развитием сигнала в присутствии 100 мкл 0,5 мг/мл п-нитрофенилфосфата (AppliChem, Darmstadt, Германия) в 100 мМ Трис/HCl буфера, рН 8,8, 100 мМ NaCl, 5 мМ MgCl2. Поглощение во времени ∆A/∆t определяли при длине волны 405 нм на ридере SpectraMax 250 (Molecular Devices, Sunnyvale, США) и строили график с использованием программного обеспечения KaleidaGraph (программное обеспечение Synergy, Reading, PA) по уравнению:
∆A= ∆Amax×[L]tot/(KD+L]tot)
где [L]tot представляет концентрацию использованного конъюгата лиганда, и KD представляет константу диссоциации (Voss and Skerra, Protein Eng., 1997, 10, 975-982).
Альтернативно, для «прямой» ELISA 2 мкМ немеченой мишени Aβ40 из примера 2 адсорбировали на 96-луночном микротитрационном планшете MaxiSorp из полистирола (Nunc, Langenselbold, Германия) и инкубировали с очищенным мутеином Lcn2, который детектировали по Strep-метке II с использованием разведения 1:1500 конъюгата стрептавидин/AP (GE Healthcare UK Ltd., Buckinghamshire, Великобритания). В качестве контроля 2 мкМ MBP из примера 2 адсорбировали на планшет для постановки ELISA. Определяли поглощение при длине волны 405 нм на ридере SpectraMax 250 (Molecular Devices, Sunnyvale, Великобритания).
Альтернативно «конкурентный» ELISA проводили аналогичным путем, как ELISA с «иммунным захватом», который описан выше. Вновь, после иммобилизации StrepMAB-Immo и отмывки 50 мкл 1 мкМ раствора очищенного мутеина Lcn2 из примера 7 вносили во все лунки на 1 ч. После отмывки биотинилированную мишень Trx-Aβ28 из примера 2 вносили в постоянной концентрации, составляющей 5 нМ (для S1-A4) или 40 нМ (для US7), в присутствии различных концентраций свободного немеченой мишени Trx-Aβ28 в качестве конкурента. Начиная с 100-кратного избытка, концентрацию конкурента снижали в 3 раза на каждой стадии. В данном случае график строили с использованием сигмоидального уравнения:
∆A=(∆Amax-∆Amin)/(1+[L]tot свобод/(KD)P)+∆Amin
с наклоном кривой p (коэффициент Хилла) в качестве дополнительного параметра.
В последующей таблице 1 обобщены значения KD, определенные ELISA в различных форматах, а также с использованием поверхностного плазмонного резонанса (см. пример 9).
Пример 9. Определение связывающей активности для Aβ с использованием поверхностного плазмонного резонанса
Анализ мутеинов Lcn2 в режиме реального времени проводили в системе Biacore X (Biacore, Uppsala, Швеция) c использованием PBS/T (PBS, содержащий 0,005% (об./об.) твина 20) в качестве буфера для анализа. Раствор MBP-Aβ40 с концентрацией 50 мкг/мл из примера 2 в 10 мМ Na-ацетате с рН 4,5 иммобилизовали на чипе CMD 200I (Xantec, Dusseldorf, Германия) с использованием обычной реакции сочетания аминов с получением плотности лиганда, равной 1455 резонансных единиц (RU). Очищенные мутеины Lcn2 S1-A4 и US7 из примера 7 наносили в концентрациях в пределах от 2 нМ до 125 нМ со скоростью потока 10 мкл/мин. Сенсограммы корректировали вычитанием соответствующих сигналов, определенных для контрольного канала, который активировали и блокировали этаноламином. Кинетическую оценку данных проводили при построении графика с использованием программного обеспечения BIAevalution V 3.0 (Karlsson et al. (1991) J. Immunol. Methods, 145, 229-240). Во время данной стадии в общем определяли значения kon и koff, в то время как различие в максимальном отклике Rmax получали локально для каждой кривой.
Пример 10. Определение эпитопа для Aβ с использованием эпитопного картирования на мембране SPOT
Мембрану SPOT (Amino-PEG500-UC540 sheet, 100×150 мм, Intavis, Koln, Германия) для картирования эпитопа Aβ в мутеинах Lcn2 S1-A4 и US7 готовили автоматическим методом, как описано Frank, J. Immunol. Methods, 2002, 262, 13-26) с использованием аппарата MultiPep (Intavis, Koln, Германия), и активированные аминокислоты получали от того же поставщика. Аминокислотную последовательность Aβ40 (SEQ ID NO:29) синтезировали на мембране в виде последовательных гексамеров, декамеров и пентадекамеров, каждый с дислокацией 1 аминокислоты, покрывая, таким образом, полную последовательность. С-концы данных пептидов ковалентно связавались с мембраной, в то время как N-концы подвергались ацетилированию. Иммобилизованная Strep-метка II служила в качестве положительного контроля для метода детектирования.
Снятие защиты с боковых цепей проводили 95% трифторуксусной кислотой (Sigma-Aldrich, Stennheim, Германия), 3% триизопропилсиланом (Sigma-Aldrich, Steinheim, Германия) и 2% дистиллированной H2O в течение 2 ч. После четырехкратной отмывки мембраны дихлорметаном (Sigma-Aldrich, Steinheim, Германия), дважды диметилформамидом (Sigma-Aldrich, Stennheim, Германия) и дважды этанолом мембрану высушивали на воздухе.
Перед использованием мембрану один раз промывали этанолом, 3 раза - PBS (4 мМ KH2PO4, 16 мМ Na2HPO4, 115 мМ NaCl, рН 7,4) и блокировали 3% (масс./об.) BSA в PBS/T (PBS, содержащий 0,1% (об./об.) твина 20) в течение 1 ч. После трехкратного промывания PBS/T мембрану инкубировали с мутеином Lcn2 S1-A4 (50 нМ), US7 (100 нМ) или Lcn2 дикого типа (100 нМ) в PBS/T в течение 1 ч и промывали 3 раза PBS/T. Затем мембрану инкубировали с конъюгатом стрептавидин/АР в разведении 1:1500 (GE Healthcare, Buckinghamshire, Великобритания) в PBS/T в течение 1 ч для детектирования белка посредством Strep-метки II. Затем мембрану промывали 3 раза PBS/T и один раз буфером АР (100 мМ Трис/HCl, рН 8,8, 100 мМ NaCl, 5 мМ MgCl2) c последующей постановкой хромогенной реакции с 5-бром-4-хлор-3-индолилфосфатом, солью 4-толуидина (BCIP; AppliChem, Darmstadt, Германия) и нитротетразолием синим (NBT; AppliChem, Darmstadt, Германия) в буфере АР, как описано Schlehuber et al., J. Mol. Biol. (2000) 297, 1105-1120).
Сравнение мембран, инкубированных с S1-A4 и Lcn2 дикого типа, соответственно, давало отчетливые пятна, которые появлялись при инкубации мембраны с S1-A4, но не с Lcn2 дикого типа. Оказалось, что с пентадекамерными фрагментами Aβ40 мотив LVFFAED был важен для связывания S1-A4. С более короткими гексамерными и декамерными пептидными последовательностями наблюдали связывание S1-A4C с минимальными мотивами VFFAED и FFAEDV. Мутеин Lcn2 US7 показал аналогичный эпитопный профиль в данном тесте.
Пример 11. Функциональный анализ мутеинов Lcn2 с аффинностью для Aβ в тесте агрегации ThT
Солюбилизированный и гомогенно мономерный, небиотинилированный Aβ40 из Примера 2 подвергали анализу в тесте агрегации тиофлавина Т в присутствии или отсутствии различных мутеинов Lcn2. Тиофлавин Т (ThT; Sigma-Aldrich, Steinheim, Германия) специфически связывается с богатыми β-складками амилоидными фибриллами и олигомерными предшественниками, но не с мономерным Aβ пептидом, что выражается в повышении флуоресценции ThT (Khurana et al., J. Struc. Biol., 2005, 151, 229-238).
Для этого ThT растворяли в дистиллированной H2O в концентрации 1 мМ. Рабочий раствор готовили разведением 1 мМ стокового раствора до конечной концентрации 5 мкМ с использованием 5 мМ глицина/NaOH, рН 8,5. 500 мкл смеси 1:1 из 200 мкМ Aβ40 в дистиллированной H2O (растворенный, как в примере 2) и 20 мкМ мутеина Lcn2 из примера 7 в PBS инкубировали при 37°С без вращения. Перед каждым определением флуоресценции на различные временные точки пробы быстро обрабатывали на Vortex 10 раз и 20 мкл соответствующей пробы смешивали с 180 мкл рабочего раствора ThT. Интенсивность флуоресценции определяли при длине волны экстинкции 450 нм и волне эмиссии 482 нм в люминесцентном спектрофотометре (LS 50 B, Perkin Elmer, Waltham, США).
Как показано на фигуре 9, мутеин Lcn2 US7 вызывал сильное ингибирование агрегации Aβ40 в соотношении 1:10.
Пример 12. Получение фрагментов рекомбинантного фибронектина, содержащих экстрадомен В (ED-B)
Три различных рекомбинантных фрагмента фибронектина человека использовали в качестве мишеней для отбора: один экстрадомен В (называемый ED-B; Zardi et al. (1987) EMBO Journal, 6, 2337-2342), тот же домен в контексте его смежных доменов 7 и 8 (относится в настоящем документе к FN7B8) и FN7B89, содержащий обычные домены 7, 8 и 9, таким образом, с отсутствием ED-B (Carnemolla et al. (1996) Int. J. Cancer 68, 397-405; Leahy et al. (1994) Proteins, 19, 48-54).
Кодирующие последовательности FN7B8, FN7B89 и ED-B клонировали в вектор pASK75 (Skerra (1994) Gene, 151, 131-135) и его производное pASG-IBA-33 (IBA, Gottingen, Германия) с получением pASK75-FN7B8 (SEQ ID NO:13), pASK75-FN789 (SEQ ID NO:17) и pASG-IBA-33-EDB (SEQ ID NO:15), соответственно. Все конструкции содержали His6-метку на карбоксиконце для очистки аффинной хроматографией с иммобилизованным ионом металлом (IMAC) и получали в виде растворимых белков в цитоплазме E. coli TG1/F [производное E. coli K12 TG1 9 (Gibson (1984) Studies on the Epstein-Barr virus genome, Cambridge University, Англия] или BL21 (Studier and Moffatt (1986) 189, 113-130). Следовательно, культивировали 2 л культуры E. coli, несущей экспрессионную плазмиду, до фазы серединного логарифмического роста при 37°С в среде LB, содержащей 100 мкг/мл ампициллина. После добавления 200 мкг/л ангидротетрациклина (Acros, Geel, Бельгия) культивирование продолжали течение 5-7 ч при 37°С. Клетки концентрировали центрифугированием, ресуспендировали в 35 мл охлажденного на льду буфера для хроматографии (40 мМ Hepes/NaOH, 1 М NaCl, рН 7,5) и лизировали обработкой ультразвуком (S250D, Branson, Danbury CT, США).
Проколол выделения, описанный ниже, был одинаковым для всех трех рекомбинантных фрагментов фибронектина. Очищенный лизат наносили на колонку с Zn2+/IDA-сефарозой (GE Healthcare, Munich, Германия), заряженной 10 мМ ZnSO4 и уравновешивали 40 мМ Hepes/NaOH, 1 М NaCl, рН 7,5). Связанный белок элюировали пологим градиентом от 0 до 300 мМ имидазола (рН доводили HCl) в буфере для хроматографии. Фракции, содержащие рекомбинантный белок, идентифицировали с помощью SDS-PAGE, смешанным с ЭДТА, до конечной концентрации 1 мМ и диализовали против 20 мМ Hepes/NaOH, рН 7,4 в течение ночи. Затем белок наносили на колонку для ионообменной хроматографии (Resource Q, GE Healthcare, Munich, Германия), уравновешенной 20 или 40 мМ Hepes/NaOH, рН 7,4. Для элюирования связанных фрагментов фибронектина использовали градиент от 0 до 300 NaCl.
Наконец, чистоту белков подтверждали анализом SDS-PAGE и эксклюзионной хроматографией. Для определения концентрации белков по поглощению при длине волны 280 нм использовали следующие расчетные коэффициенты экстинкции (Gasteiger et al. (2003) Nuclei Acids Res., 31, 3784-3788): 31400 М-1см-1 для FN7B8, 28420 М-1см-1 для FN789 и 11460 М-1см-1 для ED-B. Как правило, получали примерно 10-20 мг на 2 л культуры в колбе для встряхивания. Очищенные белки хранили при 4°С и использовали для всех опытов.
Очищенные фрагменты фибронектина метили дигоксигенином, с использованием избытка (молярное соотношение 4:1) N-гидроксисукцинимидного эфира дигоксигенин-3-О-метилкарбонил-ε-аминокапроновой кислоты (Roche Diagnostics, Mannheim, Германия) в течение 1 ч при комнатной температуре, следуя указаниям изготовителя. Для удаления свободного дигоксигенина раствор белка наносили на колонку для обессоливания PD-10 (GE Healthcare, Munich, Германия), уравновешенную 40 мМ Трис/HCl буфер, 115 мМ NaCl и 1 мМ ЭДТА, рН 7,5. Эффективность дигоксигенирования и целостность белка определяли SDS-PAGE, ESI масс-спектрометрией или дот-блотом с окрашиванием анти-дигоксигенин-Ар, Fab-фрагмент (Roche Diagnostics, Mannheim, Германия).
Пример 13. Отбор вариантов Lcn2 с аффинностью к ED-B фаговым дисплеем
В целом проводили четыре цикла отбора фагемидным дисплеем с использованием рандомизированной фагемидной библиотеки Lcn2, основанной на коллекции синтетических генов, исходно синтезированной Sloning BioTechnology GmbH, как описано в примере 1. Для первого цикла отбора примерно 5×1012 рекомбинантных фагемид, растворенных в 300 мкл TBS/E (40 мм Hepes/HCl, 115 М NaCl, 1 мМ ЭДТА, рН 7,4) с добавлением 50 мМ бензамидина, блокировали в течение 30 мин 100 мкл 8% (масс./об.) BSA (Sigma-Aldrich, Munich, Германия) в TBS, содержащем 0,4% (об./об.) твина 20 [полиоксиэтиленсорбитана монолаурата; AppliChem, Darmstadt, Германия]. Затем данный раствор инкубировали в течение 1 ч с магнитными шариками с анти-DIG-IgG (Europa Bioproducts, Cambridge, Великобритания), которые блокировали в течение 1 ч 2% (масс./об.) BSA в TBS/T (TBS, содержащем 0,1% (об./об.) твина 20) и заряжали 400 мкл 0,1 мкМ дигоксигенин-меченным рекомбинантным FN7B8 (см. пример 12).
После сбора шариков с помощью магнита и отбрасывания супернатанта проводили 10 стадий отмывки с TBS/Т и оставшиеся связанные фагемиды вначале элюировали 400 мкл 0,1 М триэтиламина (рН не доводили) в течение 6 мин с последующим вторым элюированием 350 мкл 0,1 М глицином/HCl, рН 2,2 в течение 8 мин. Элюаты собирали и сразу же нейтрализовали соответствующим количеством 2 М уксусной кислоты или 50 мкл 0,5% Трис-основания, соответственно, объединяли и использовали для заражения E. coli XL1-Blue, которые находились в фазе экспоненциального роста. Фагемиды титровали и повторно амплифицировали до следующего цикла пэннинга, следуя опубликованным протоколам (Beste et al. (1999) PNAS, 96, 1898-1903; Schlehuber et al. (2000) J. Mol. Biol., 297, 1109-1120).
Для второго раунда отбора использовали примерно 2×1012 амплифицированных фагемид и элюирование связанных фагемид проводили конкуренцией с 400 мкл 231 нмоль/мл свободного рекомбинантного ED-B в течение 75 мин.
В третьем и четвертом циклах отбора примерно 2×1012 амплифицированных фагемид инкубировали примерно в течение 1 ч с 100 нМ меченных дигоксигенином FN7B8. Затем комплексы фагемид-антиген сажали на магнитные шарики с анти-DIG-IgG в течение 20 мин. После отмывки шариков десять раз TBS/Т связанные фагемиды элюировали конкуренцией с 400 мкл свободного рекомбинантного ED-B в концентрации 140-231 нмоль/мл в течение 75 мин при комнатной температуре.
Пример 14. Отбор вариантов Lcn2 с аффинностью к ED-B скринингом ELISA
Обогащение мутеинами Lcn2 в результате отбора, описанного в примере 13, которые специфически связываются с белком-мишенью ED-B, проводили скрининговым ELISA. С использованием объединенного плазмидного препарата с последней стадии пэннинга кассету мутантных генов субклонировали через BstXI в экспрессионную плазмиду phNGAL98, которая кодирует слитый белок из сигнального пептида OmpA для продукции в периплазме E. coli и кодирующей области Lcn2 с С-концевой Strep-меткой II (Schimdt and Skerra (2007) Nat. Protoc., 2, 1528-1535). Экспрессию отдельных мутеинов Lcn2 в растворенном виде в 96-луночных планшетах проводили следующим образом: 100 мкл среды ТВ (Tartof and Hobbs (1987) Bethesda Research Laboratory Focus, 9, 12), содержащей 100 мкг/мл ампициллина, инокулировали одной, произвольно взятой колонией и инкубировали в течение 5 ч при 37°С со встряхиванием (500-800 об/мин; Thermomixer comfort; Eppendorf, Hamburg, Германия). Каждый клон высевали в 100 мкл свежей среды с 10 мкл этой культуры и инкубировали 1-2 ч при 37°С со встряхиванием с последующим снижением температуры до 22°С. После дополнительной инкубации в течение 2-4 ч экспрессию мутеинов Lcn2 индуцировали в клетках, находящихся в фазе экспоненциального роста, в течение 12-14 ч добавлением 0,2 мкг/мл ангидротетрациклина (Acros, Geel, Бельгия). Высвобождение белков в периплазму проводили при добавлении 4 мкл 2×BBS (0,2 М борат/NaOH, 160 мМ NaCl, 1 мМ ЭДТА, рН 8,0), содержащем 1 мг/мл лизоцима (Roche Diagnostics, Mannheim, Бельгия) в течение 1 ч при комнатной температуре со встряхиванием. Лизаты блокировали 40 мл 10% BSA (масс./об.) BSA (Applichem, Darmstadt, Германия) в TBS и 0,5% твине 20 в течение 1 ч и клеточный дебрис удаляли из сырого экстракта центрифугированием в течение 10 мин.
Для адсорбции FN7B8 или FN7B89 на поверхности 96-луночного планшета Nunc Maxisorp (Thermo Fisher Scientific, Langenselbold, Германия) 50 мкл раствора белка с концентрацией 100 мкг/мл в TBS вносили в лунку и инкубировали в течение ночи при 4°С. После трех стадий отмывки с TBS/Т лунки блокировали 2% (масс./об.) BSA в TBS/Т в течение 3 ч при комнатной температуре и последовательно промывали перед экспозицией сырого экстракта из E. coli. Для постановки ELISA 50 мкл осветленного лизата вносили в каждую лунку, инкубировали в течение 1 ч с последующим трехкратным промыванием TBS/Т. Связанные мутеины Lcn2 детектировали с использованием конъюгата стрептавидин/щелочная фосфатаза (1:1500 в TBS/Т; GE Healthcare, Munich, Германия) с использованием субстрата 4-нитрофенилфосфата (pNpp, 0,5 мг/мл; AppliChem GmbH, Darmstadt, Германия) в 0,1 Трис/HCl буфере, 0,1 М NaCl, 5 мМ MgCl2, рН 8,8 (см. пример 16).
В результате проведения скринингового ELISA идентифицировали четыре клона. В последующих экспериментах (см. примеры 16-18) было установлено, что данные четыре мутеина Lcn2 обладают специфической активностью связывания с FN7B8 в ELISA, SPR-анализе и при иммунофлуоресцентной микроскопии положительных на ED-B клеток злокачественной опухоли ободочной кишки человека. Данные мутеины Lcn2 обозначали, как N7A (SEQ ID NO:20), N7E (SEQ ID NO:22), N9B (SEQ ID NO:24) и N10D (SEQ ID NO:26).
Пример 15. Получение растворимого белка и выделение Lcn2 и его вариантов
Подробное описание см. в примере 7.
Пример 16. Определение связывающей активности для ED-B в ELISA
Для адсорбции FN7B8 или FN789 на поверхности 96-луночного планшета Nunc Maxisorp (Thermo Fisher Scientific, Langenselbold, Германия) 50 мкл раствора белка с концентрацией 100 мкг/мл в TBS/Е вносили в каждую лунку и инкубировали при комнатной температуре в течение 2 ч. Кроме того, для включения контрольных белков в пустые лунки вносили 120 мкл 2% (масс./об.) BSA (AppliChem, Darmstadt, Германия) в TBS/Е. После трех стадий отмывки лунки блокировали 120 мкл 2% (масс./об.) BSA (AppliChem, Darmstadt, Германия) в TBS/ЕТ в течение 2 ч при комнатной температуре и последовательно промывали перед внесением 50 мкл серии разведений очищенного мутеина Lcn2 и инкубировали в течение 1 ч. Лунки вновь промывали и связанные мутеины Lcn2 детектировали с использованием 50 мкл конъюгата стрептавидин/щелочная фосфатаза (GE Healthcare, Munich, Германия) в разведении 1:1500 в TBS/Т в течение 1 ч с последующим развитием сигнала в присутствии 50 мкл 0,5 мг/мл п-нитрофенилфосфата в 100 мМ Трис/HCl буфера, 100 мМ NaCl, 5 мМ MgCl2, рН 8,8. Поглощение во времени ∆A/∆t определяли при длине волны 405 нм на ридере SpectraMax 250 (Molecular Devices, Sunnyvale, CA) и строили график с использованием программного обеспечения KaleidaGraph (программное обеспечение Synergy, Reading, PA) по уравнению:
∆A=∆Amax×[L]tot/(KD+[L]tot)
где [L]tot представляет концентрацию использованного конъюгата лиганда, и KD представляет константу диссоциации (Voss and Scera (1997) Protein Eng., 10, 975-982). Было установлено, что варианты Lcn2 N7A, N9B и N10D, соответственно, специфически связываются с FN7B8 со значениями KD, равными 14,8 нМ (N7A), 40,1 нМ (N9B), 30,0 нМ (N7E) и 51,2 нМ (N10D), но не с FN789 или BSA.
Пример 17. Определение связывающей активности для рекомбинантного фибронектина FN7B8 поверхностным плазмонным резонансом (SPR)
Анализ мутеинов Lcn2 в режиме реального времени проводили в системе Biacore X (Biacore, Uppsala, Швеция) c использованием HBS/ET (20 мМ Hepes, рН 7,5, 150 мМ NaCl, 1 мМ ЭДТА, содержащий 0,005% (об./об.) твина 20) в качестве буфера для анализа. 200 мкг/мл раствора рекомбинантного FN7B8 в 10 мМ Na-ацетате, рН 4,0 иммобилизовали на чипе CMD 200 m Sensorchip (Xantec bioanalytics, Dusseldorf, Германия) с использованием обычной реакции сочетания аминов с получением плотности лиганда, равной 500 резонансных единиц (RU). Очищенный мутеин Lcn2 наносили со скоростью потока 25 мкл/мин в концентрациях в пределах от 2,5 нМ до 160 нМ. Сенсограммы корректировали вычитанием соответствующих сигналов, определенных для контрольного канала, который активировали и блокировали этаноламином. Кинетическую оценку данных проводили при построении графика с использованием программного обеспечения BIAevaluation V 4.1 (Karlsson et al. (1991) J. Immunol. Methods, 145, 229-240).
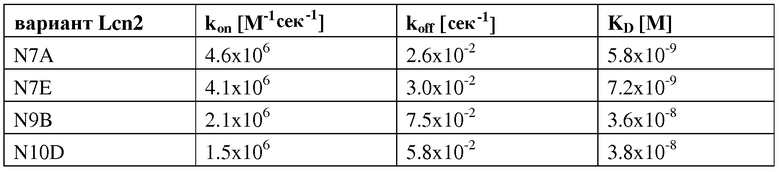
Пример 18. Иммуноокрашивание положительных на ED-B клеток CaCo2
Клетки злокачественной опухоли ободочной кишки человека (клетки CaCo2 были любезно предоставлены H. Daniel, Technische Universitat Munchen, Германия; Pujuguet et al., Am. J. Pathol., 148, 579-592) культивировали в системе Nunc Lab-TekTM II chamber slideTM (4 камеры на предметное стекло; Thermo Fisher Scientific, Langenselbold, Германия) в среде MEM с солями Игла и L-глутамином с добавлением 10% фетальной бычьей сыворотки, 1× MEM заменимых аминокислот и 50 мкг/мл гентамицина (PAA Laboratories, Pasching, Австрия) при 37°С во влажной атмосфере до достижения клеточного слияния на уровне примерно 50-70%. Клеточные слои, прикрепленные к покровному стеклу, промывали PBS (среда Дульбекко без ионов Ca2+ и Mg2+; PAA Laboratories, Pasching, Австрия), затем дистиллированной водой и затем фиксировали и противоокрашивали охлажденным на льду метанолом, содержащим 5 мкг/мл DAPI (4',6-диамидино-2-фенилиндол; Sigma-Aldrich, Munich, Германия) в течение 5 мин.
Все последующие инкубации проводили в темноте. Фиксированные клетки промывали и инкубировали с 500 мкл 1 мкМ Lcn2 дикого типа, мутеина Lcn2, PBS или специфического для ED-B антитела scFv-L19 (Pini et al. (1998) J. Biol. Chem., 273, 21769-21776) в течение 1 ч. Все эти продукты выделяли в виде слитых белков с Strep-меткой II (Schmidt and Skerra, выше). Клетки промывали PBS и инкубировали немеченым антителом StrepMABimmo (5 мкг/мл в PBS; IBA, Gottiingen, Германия) в течение 1 ч с последующими двумя стадиями отмывки. Наконец, специфическое связывание с клетками CaCo2 детектировали с использованием меченного флуоресцентной меткой конъюгата антимышиного IgG (H+L) F(ab')2-фрагмента Dylight-488 (Cell Signaling Technology, Danvers, США), разведенных 1:200 PBS, в качестве вторичного антитела.
Для всех вариантов Lcn2 и также антитела scFv-L19 отмечали специфическое окрашивание клеток, которое наблюдали под микроскопом Axiovert 40 CFL (Carl Zeiss, Gottingen, Германия), в то время как рекомбинантный Lcn2 дикого типа и PBS демонстрировали незначительные сигналы в данном тесте.
Пример 19. Получение Aβ-специфических мутеинов Lcn2 H1GA и H1GV посредством замены остатка свободного цистеина в H1-G1 в положении 36
Cys36 заменяли на Ala или Val сайт-направленным мутагенезом. После этого проводили ПЦР с вырожденным олигодезоксинуклеотидом DH-4 (SEQ ID NO:45) и вторым олигодезоксинуклеотидом J08rev (SEQ ID NO:48), а также плазмидной ДНК, кодирующей Lcn2 мутеин H1-G1 в качестве матрицы (SEQ ID NO:37). Амплифицированные фрагменты субклонировали через BstXI в экспрессионную плазмиду phNGAL98 и секвенировали для идентификации отдельных вариантов замен. В зависимости от введенной аминокислотной замены полученные варианты Lcn2 обозначали H1GA (SEQ ID NO:49, 50) и H1GV (SEQ ID NO:51, 52).
Пример 20. Продукция в растворимом виде и очистка новых Aβ-специфических мутеинов Lcn2 H1GA и H1GV с использованием культур E. coli с высокой оптической плотностью
Рекомбинантный Lcn2 и его мутеины получали секрецией в периплазму E. coli JM83. Для экспрессии растворимого белка использовали плазмиду phNGAL98 с соответствующей вставкой BstXI, кодирующую H1GA (SEQ ID NO:49) или H1GV (SEQ ID NO:51).
Культуры выращивали с вращением при 22°С в 2 л среды LB, содержащей 100 мг/л ампициллина (Amp). Экспрессию гена индуцировали при плотности клеток OD550=2,5 добавлением ангидротетрациклина (aTc) до конечной концентрации 0,2 мг/л. После инкубации в течение 5 ч клетки собирали центрифугированием, ресуспендировали в 40 мл охлажденного на льду периплазматического фракционного буфера (0,5 М сахарозы, 1 мМ ЭДТА, 100 мМ Трис-HCl буфера с рН 8,0), содержащего 0,1 мг/мл лизозима и инкубировали на льду в течение 30 мин. Полученные сферопласты осаждали повторным центрифугированием и получали супернатант, содержащий растворимый рекомбинантный белок.
Растворимый белок очищали аффинной хроматографией с использованием Strep-метки II с последующей эксклюзионной хроматографией (SEC) на колонке Superdex 75 HR 10/30 с использованием PBS буфера (4 мМ KH2PO4, 16 мМ Na2HPO4, 115 мМ NaCl, рН 7,4). Чистоту белка проверяли с использованием SDS-PAGE. Концентрацию белка определяли по поглощению при 280 нм с использованием расчетных коэффициентов экстинкции 27055 М-1см-1 для Аβ-специфических мутеинов H1GA (SEQ ID NO:50) и H1GV (SEQ ID NO:52).
Пример 21. Определение связывающей активности для MBP-Aβ40 с использованием поверхностного плазмонного резонанса на приборе Biacore X
Анализ взаимодействия Lcn2 мутеинов H1GA или H1GV и MBP-Аβ40 (SEQ ID NO:33) в режиме реального времени проводили в системе Biacore X c использованием PBS/T (4 мМ KH2PO4, 16 мМ Na2HPO4, 115 мМ NaCl, рН 7,4, содержащем 0,005% (об./об.) твина 20) в качестве буфера для анализа. Раствор MBP-Aβ40 с концентрацией 15 мкг/мл из примера 2 в 10 мМ Na-ацетате с рН 4,5 иммобилизовали на чипе CMD 200I (Xantec, Dusseldorf, Германия) с использованием обычной реакции сочетания аминов с получением плотности лиганда, равной 1316 резонансных единиц (RU). Очищенные мутеины Lcn2 H1GA или H1GV из примера 20 наносили в концентрациях в пределах от 4 нМ до 128 нМ со скоростью потока 20 мкл/мин. Данные подвергали двойной обработке вычитанием соответствующих сигналов, определенных для контрольного канала, который активировали и блокировали этаноламином, а также вычитанием определенных сигналов для среднего при введении буфера. Кинетическую оценку данных в общем проводили с использованием программного обеспечения BIAevaluation V 3.0 (Karlsson et al. (1991) J. Immunol. Methods, 145, 229-240).
Пример 22. Определение связывающей активности для Aβ40 с использованием поверхностного плазмонного резонанса на приборе Biacore T100
Анализ взаимодействия мутеина Lcn2 H1GA и Аβ40 (SEQ ID NO:29) в режиме реального времени проводили в системе Biacore Т100 (Biacore, Uppsala, Швеция) c использованием PBS/T (4 мМ KH2PO4, 16 мМ Na2HPO4, 115 мМ NaCl, рН 7,4, содержащем 0,005% (об./об.) поверхностно-активного вещества Р20) в качестве буфера для анализа. Раствор Aβ40 с концентрацией 10 мкг/мл из примера 2 в 10 мМ Na-ацетате с рН 4,5 иммобилизовали на чипе CM5 (Biacore, Uppsala, Швеция) с использованием обычной реакции сочетания аминов с получением плотности лиганда, равной 325 резонансных единиц (RU). Очищенный мутеин Lcn2 H1GA из примера 20 наносили в концентрациях в пределах от 1 нМ до 32 нМ со скоростью потока 30 мкл/мин. Серии разведений H1GA наносили со временем ассоциации и диссоциации 300 сек для получения информации по kon. Для точного определения нижнего значения koff анализировали самую высокую концентрацию с использованием времени диссоциации 7200 сек. Данные подвергали двойной обработке, как описано в примере 21. Значения kon и koff для реакции связывания определяли по полной совокупности данных с использованием программного обеспечения Biacore T100 Evaluation V 2.0.3. для обработки данных и построения кинетического графика. Строили общий график с использованием модели связывания 1:1.
Пример 23. Функциональный анализ мутеина Lcn2 H1GA в тесте агрегации ThT
Для постановки теста агрегации тиофлавина Т (ThT) синтетический Aβ пептид (SEQ ID NO:29) растворяли в 1,1,1,3,3,3-гексафтор-2-пропаноле (HFIP; Sigma-Aldrich, Steinheim, Германия) в течение 12 ч. HFIP выпаривали в вакууме и Aβ растворяли в соответствующем объеме дистиллированной H2O, обрабатывали ультразвуком в течение 15 мин при 4°С и фильтровали (центрифужная трубчатая мембрана для фильтрации из целлюлозы ацетата, 0,45 мкм; Costar Spin-X; Corning Inc., Corning, NY). Затем солюбилизированный мономерный Aβ немедленно использовали для постановки тестов по агрегации.
500 мкл раствора Aβ с концентрацией 1 мг/мл инкубировали при отсутствии и в присутствии различных мутеинов Lcn2 в различных молярных соотношениях или BSA в 0,5× PBS при 37°С с перемешиванием. Реакции агрегации проводили в трех параллелях. Для определения флуоресценции периодически отбирали порции объемом 20 мкл и смешивали с 180 мкл ThT при конечной концентрации 50 мкМ в 0,5× PBS и анализировали при волне экстинкции 450 нм и волне эмиссии 482 нм с использованием спектрофлуориметра FluoroMax-3 (HORIBA Jobin Yvon, Grabrunn, Германия).
Пример 24. Определение связывающей активности для одного домена ED-B рекомбинантного фибронектина с использованием поверхностного плазмонного резонанса (SPR)
Анализ взаимодействия Lcn2 мутеинов в режиме реального времени проводили в системе Biacore X c использованием HBS/ET (20 мМ Hepes, рН 7,5, 150 мМ NaCl, 1 мМ ЭДТА, содержащем 0,005% (об./об.) твина 20) в качестве буфера для анализа. Раствор рекомбинантного ED-B с концентрацией 100 мкг/мл в 10 мМ Na-ацетате, рН 4,0 иммобилизовали на чипе CMD 200 m Sensorchip с использованием обычной реакции сочетания аминов с получением плотности лиганда, равной 180 резонансных единиц (RU). Очищенный мутеин Lcn2 наносили со скорость потока 25 мкл/мин в концентрациях в пределах от 2,5 нМ до 160 нМ. Сенсограммы корректировали вычитанием соответствующих сигналов, определенных для контрольного канала, который активировали и блокировали этаноламином. Кинетическую оценку данных проводили построением общего графика с использованием программного обеспечения BIAevaluation V 4.1 (Karlsson et al. (1991) J. Immunol. Methods, 145, 229-240). В случае N10D использовали конкурирующую модель с гетерогенным аналитом для построения графика с получением двух групп кинетических констант.
Кинетические данные по связыванию мутеинов Lcn2 с ED-B, определенные поверхностным плазмонным резонансом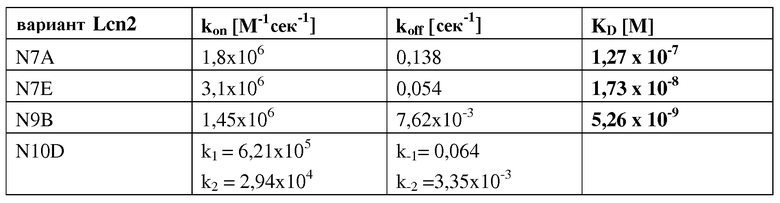
| название | год | авторы | номер документа |
|---|---|---|---|
| МУТЕИНЫ ЛИПОКАЛИНА 2 ЧЕЛОВЕКА (Lcn2, hNGAL) С АФФИННОСТЬЮ ДЛЯ ОПРЕДЕЛЕННОЙ МИШЕНИ | 2019 |
|
RU2804336C2 |
| МУТЕИНЫ ЛИПОКАЛИНА 2 ЧЕЛОВЕКА (Lcn2, hNGAL) С АФФИННОСТЬЮ ДЛЯ ОПРЕДЕЛЕННОЙ МИШЕНИ | 2010 |
|
RU2707126C2 |
| Белки, связывающиеся с гепсидином | 2011 |
|
RU2625011C2 |
| МУТЕИНЫ ЛИПОКАЛИНА 2 ЧЕЛОВЕКА С АФФИННОСТЬЮ В ОТНОШЕНИИ ГЛИПИКАНА-3 (GPC3) | 2016 |
|
RU2756318C2 |
| СЛИТЫЙ ПОЛИПЕПТИД С ПРОТИВОРАКОВОЙ АКТИВНОСТЬЮ | 2016 |
|
RU2727165C2 |
| НОВЫЕ ПОЛИПЕПТИДЫ СО СПЕЦИФИЧЕСКИМ СВЯЗЫВАНИЕМ И ПУТИ ИХ ПРИМЕНЕНИЯ | 2015 |
|
RU2723034C2 |
| МУТЕИНЫ ЛИПОКАЛИНА СЛЕЗНОЙ ЖИДКОСТИ, ОБЛАДАЮЩИЕ АФФИННОСТЬЮ К С-МЕТ РЕЦЕПТОРНОЙ ТИРОЗИНКИНАЗЕ ЧЕЛОВЕКА, И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2009 |
|
RU2515063C9 |
| БЕЛКИ, СПЕЦИФИЧНЫЕ В ОТНОШЕНИИ CD137 | 2016 |
|
RU2736312C2 |
| НОВЫЙ СЛИТЫЙ БЕЛОК, СПЕЦИФИЧНЫЙ ДЛЯ CD137 И PD-L1 | 2019 |
|
RU2818349C2 |
| СЛИТЫЙ ПОЛИПЕПТИД С ПРОТИВОРАКОВОЙ АКТИВНОСТЬЮ | 2016 |
|
RU2754466C2 |








































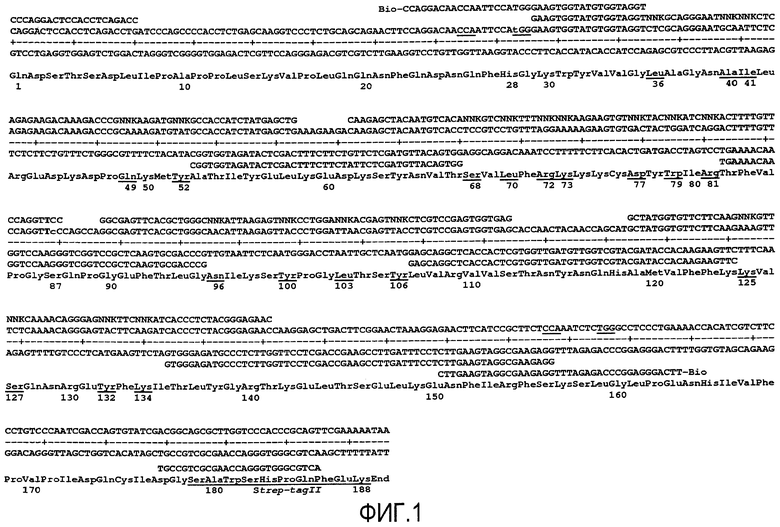
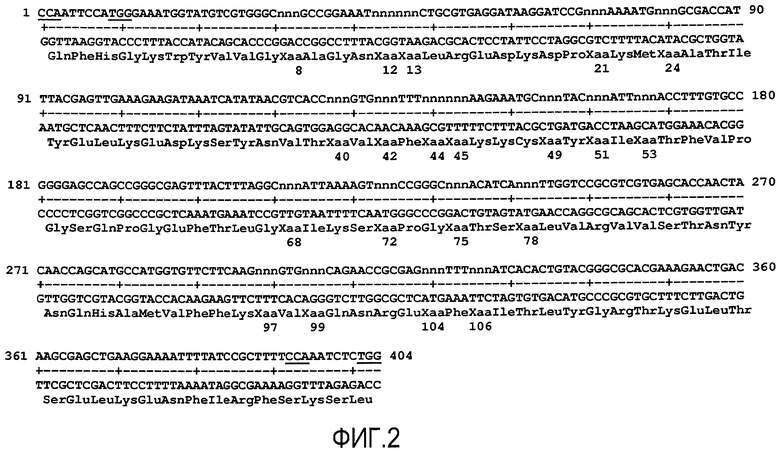
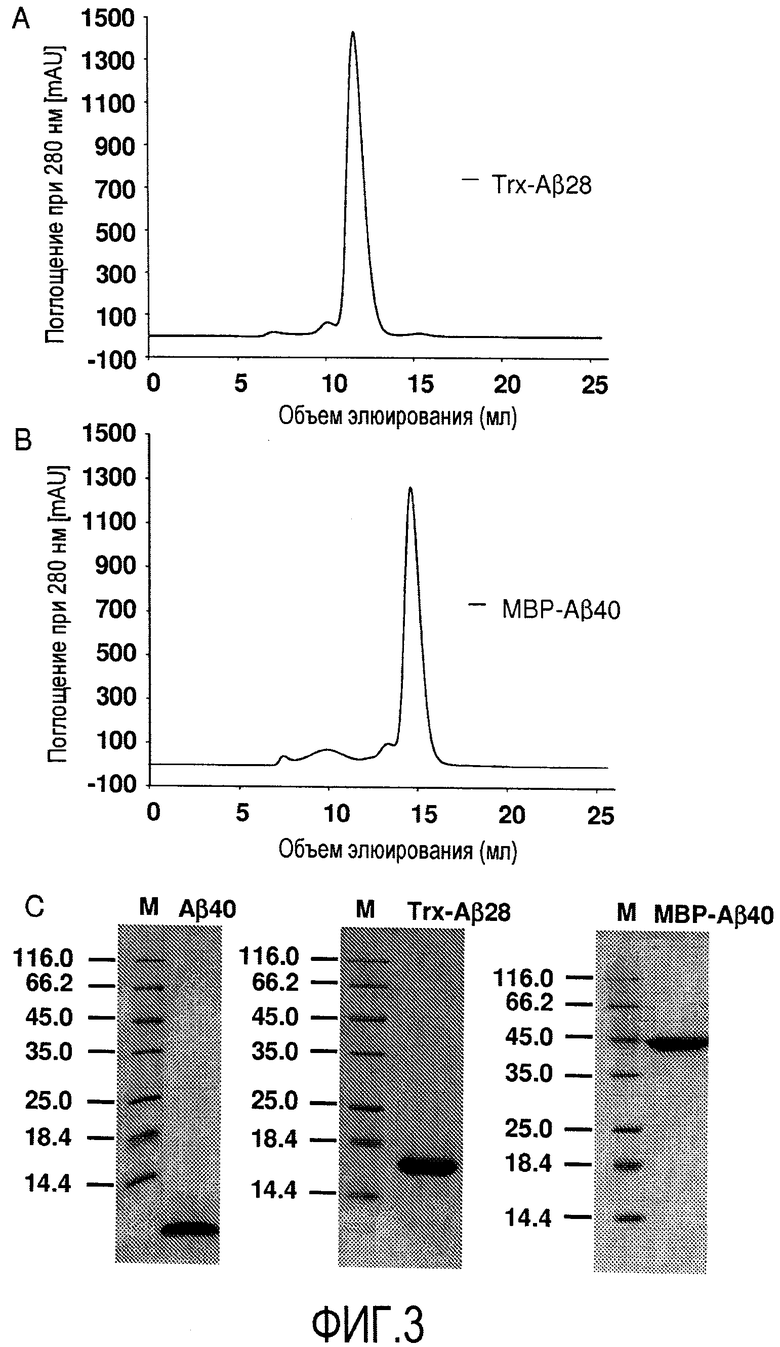
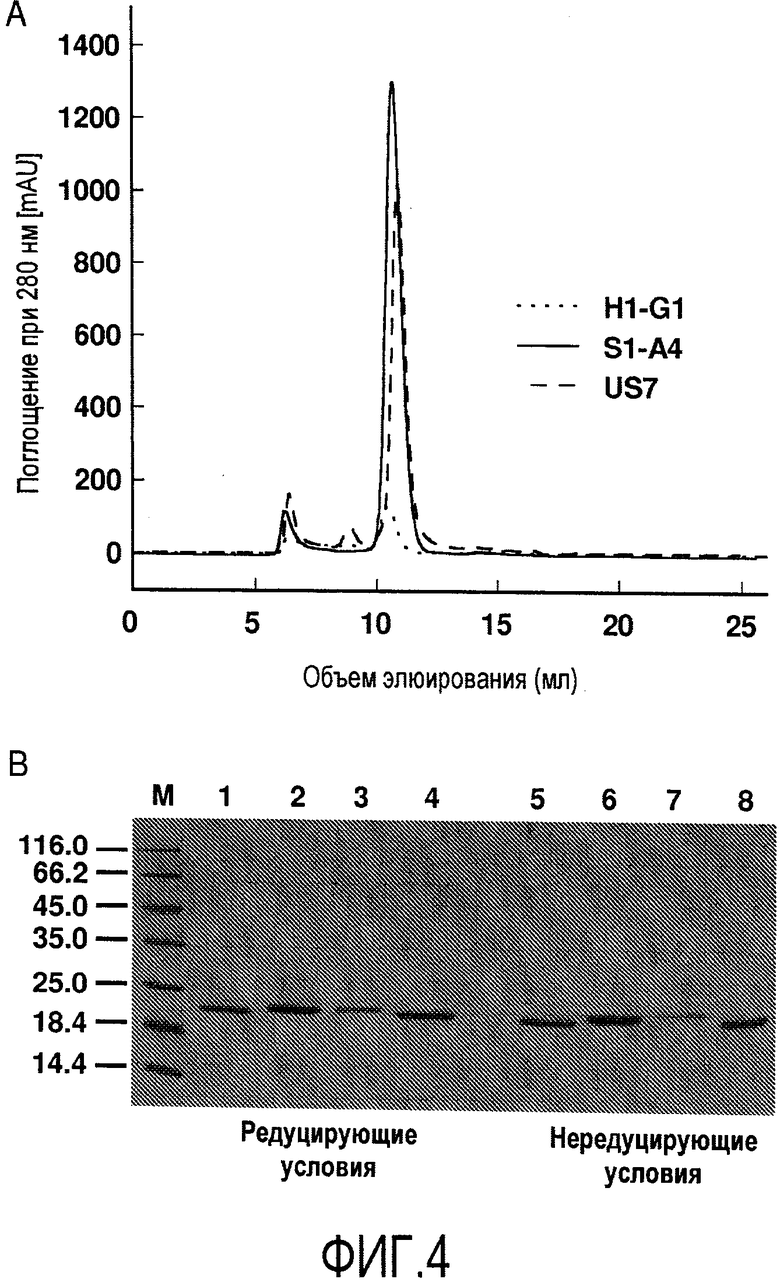
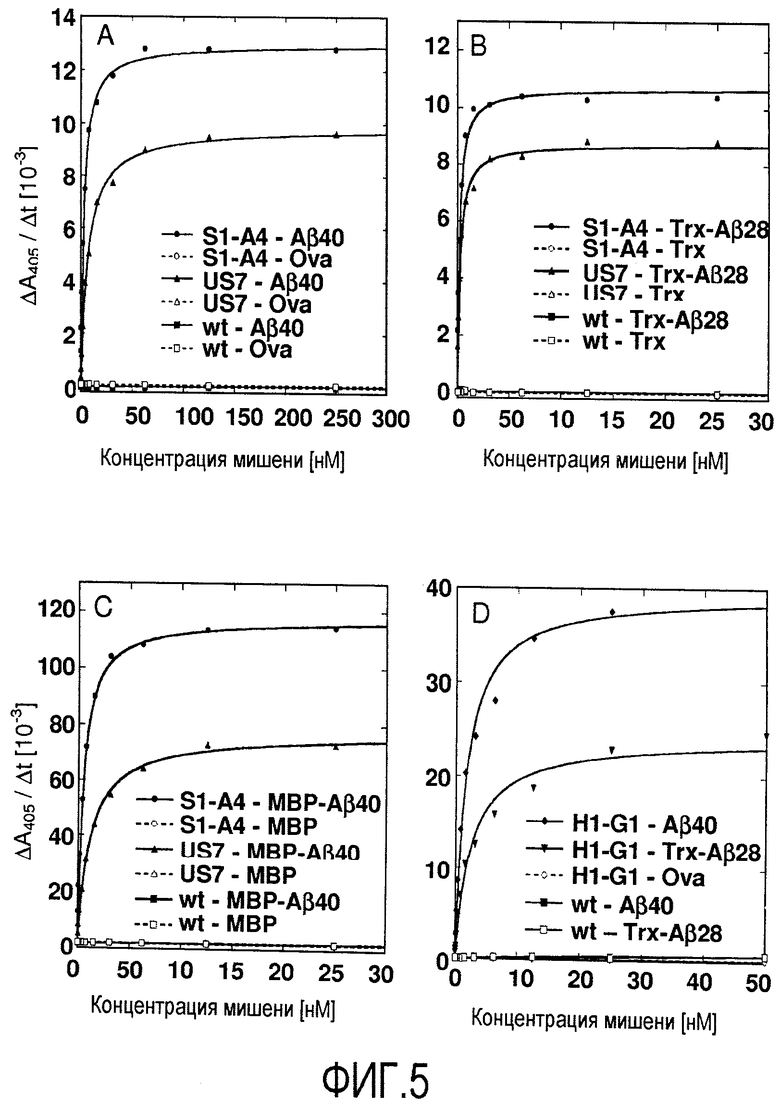
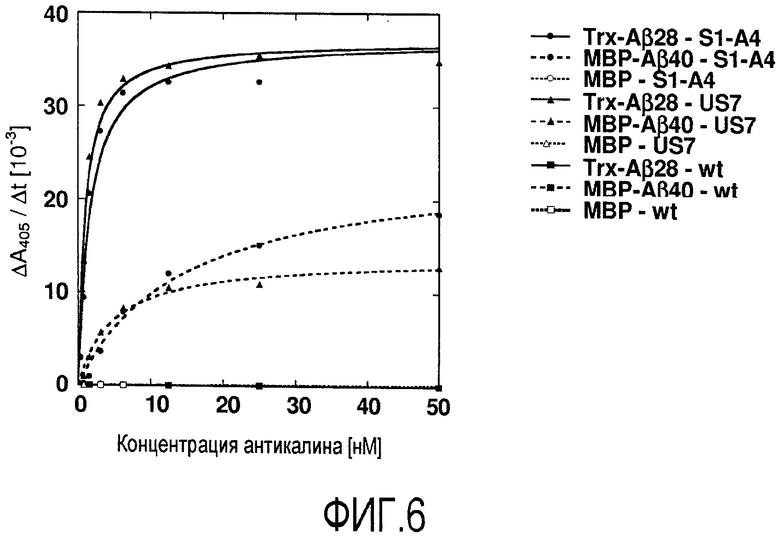
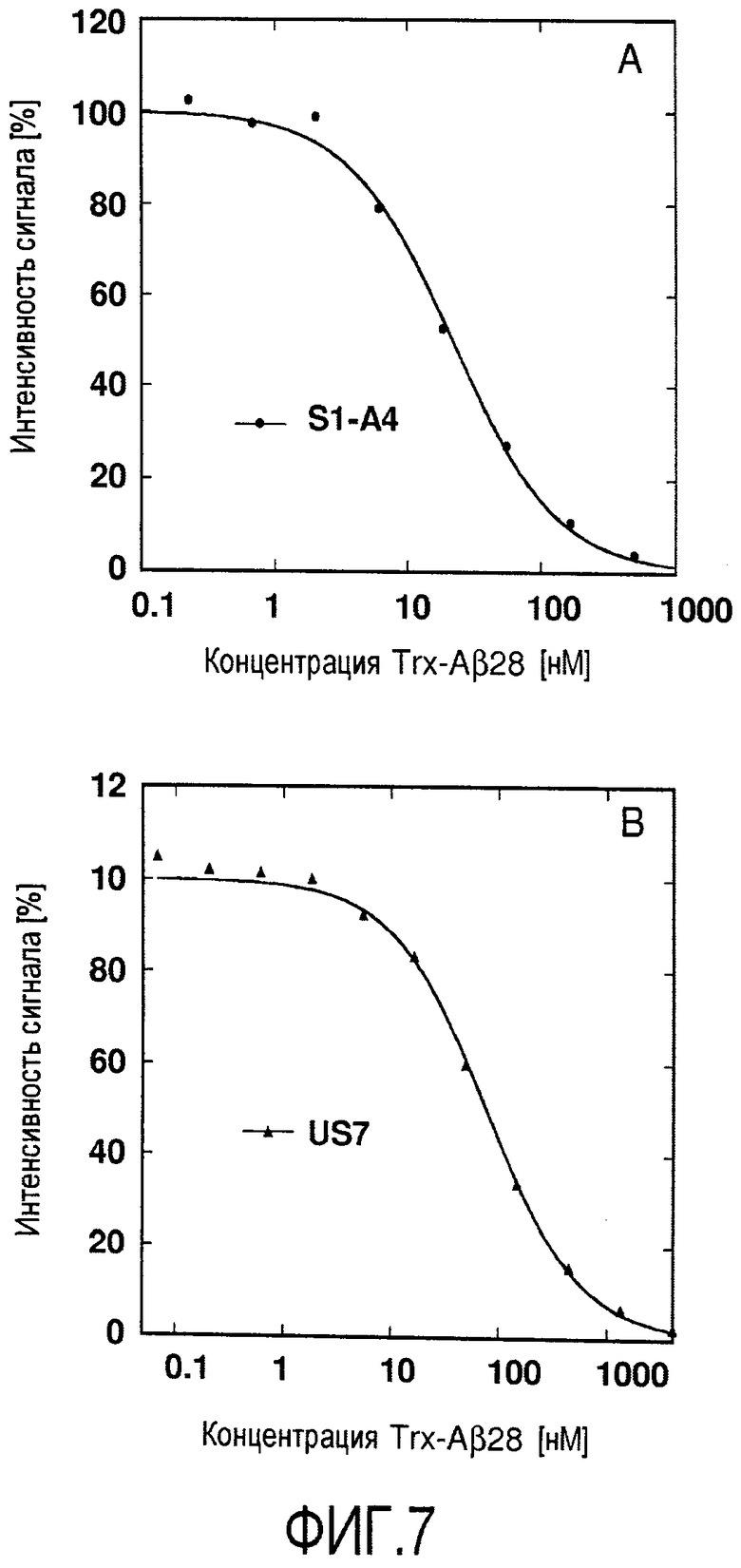
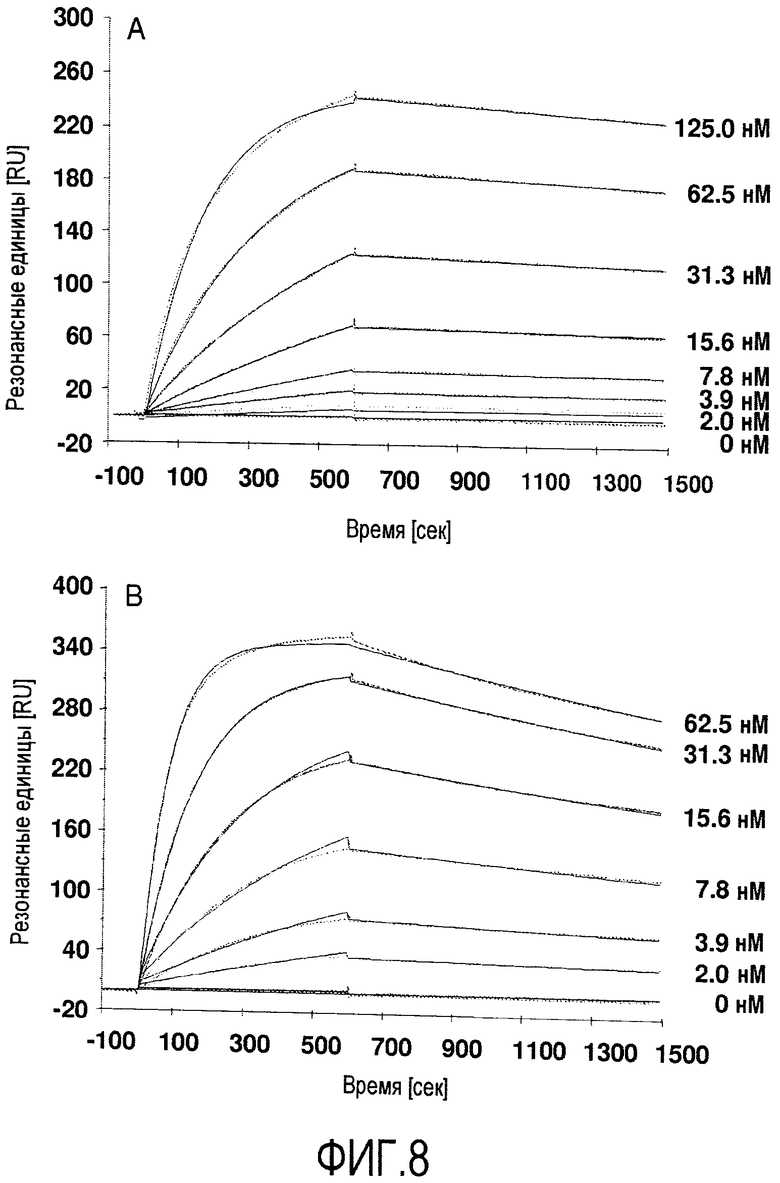
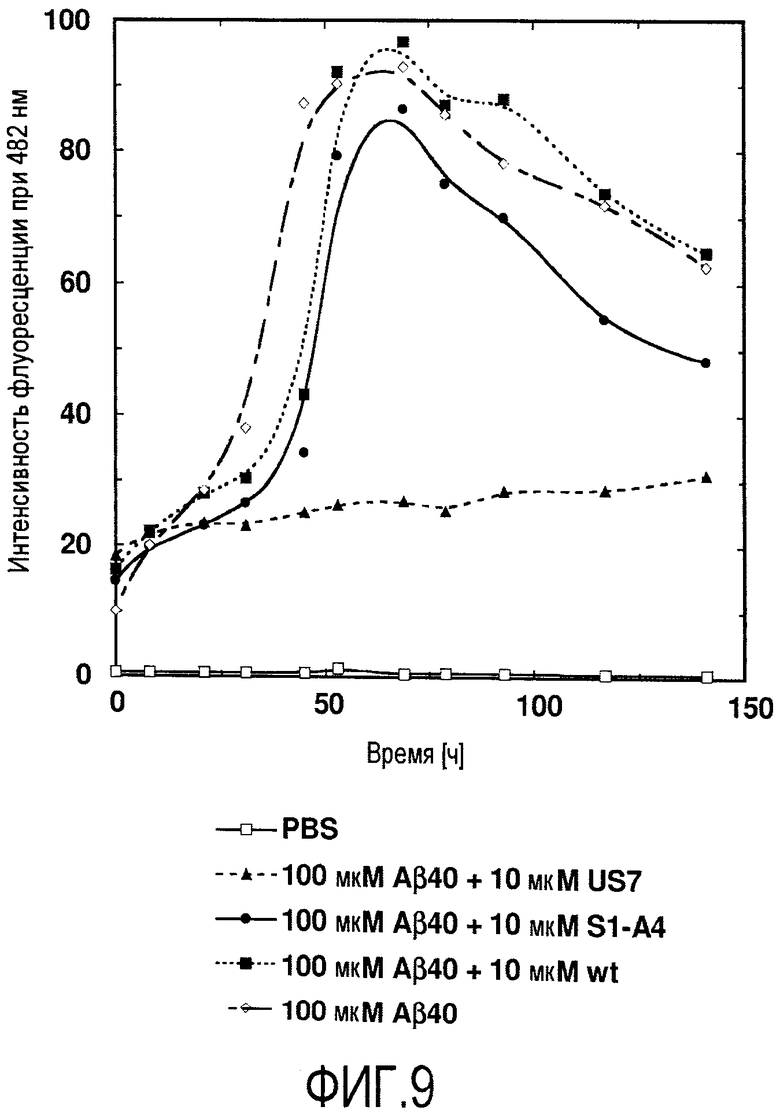
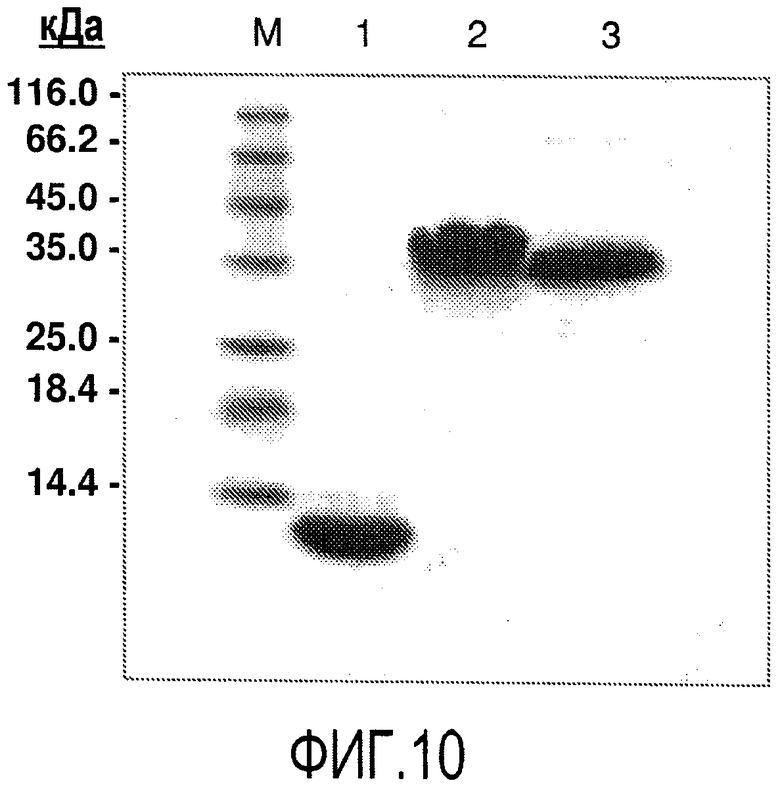
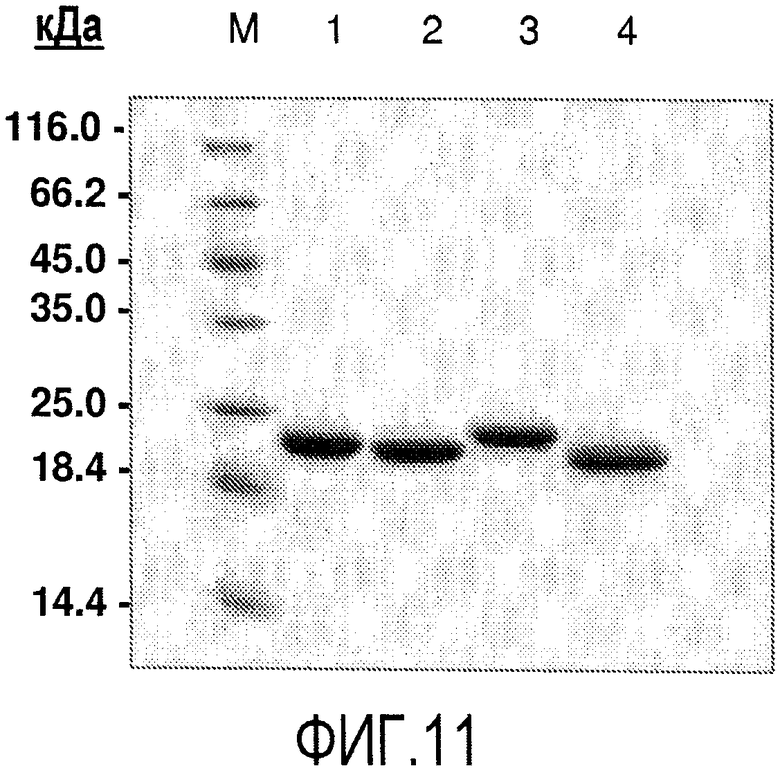
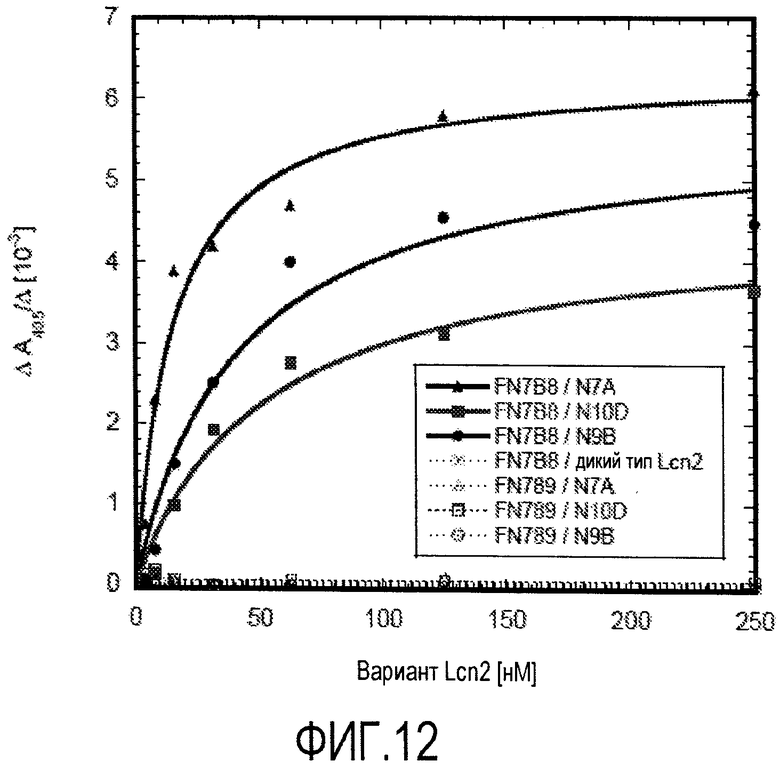
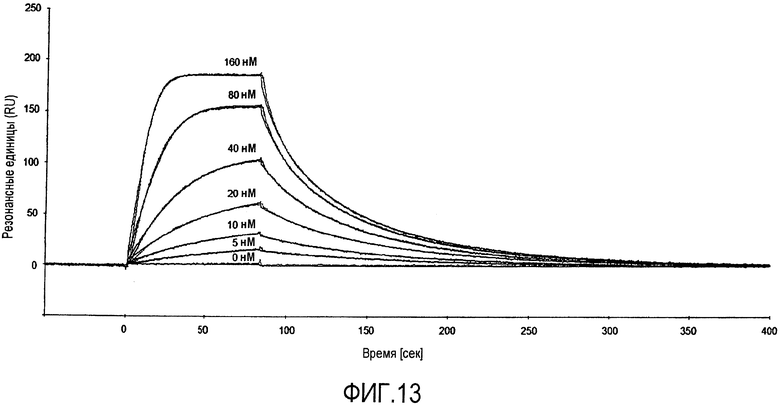
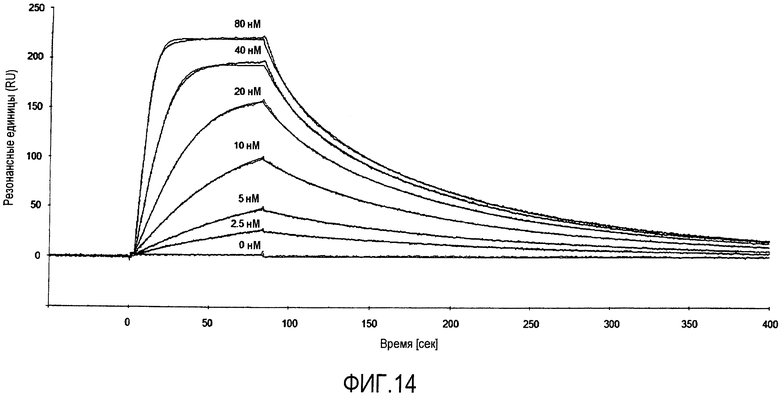
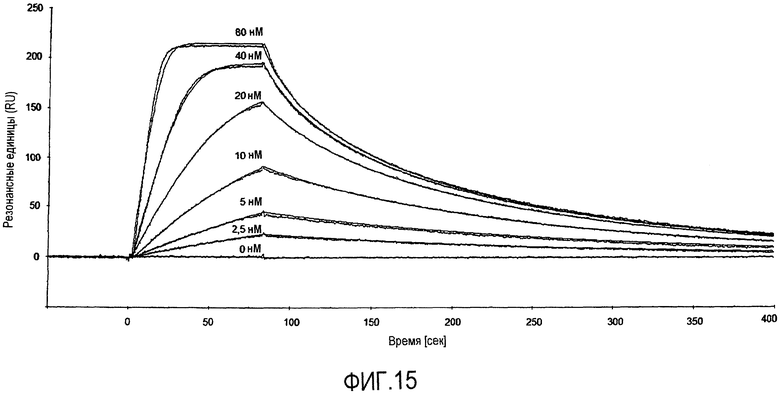
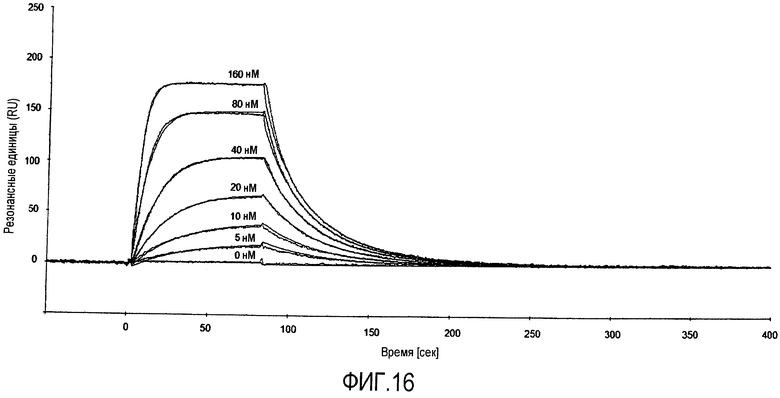
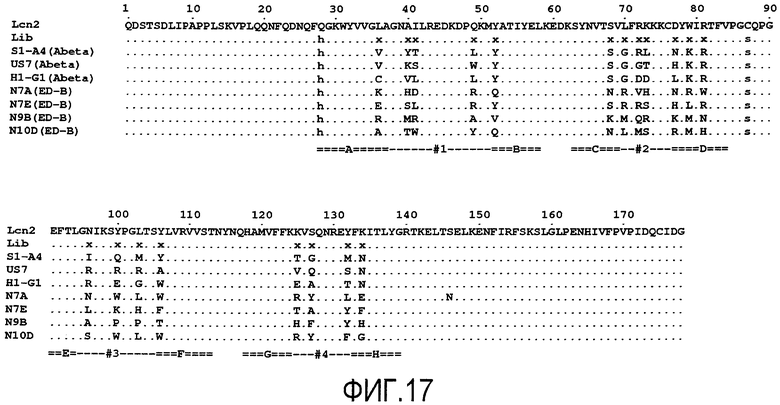
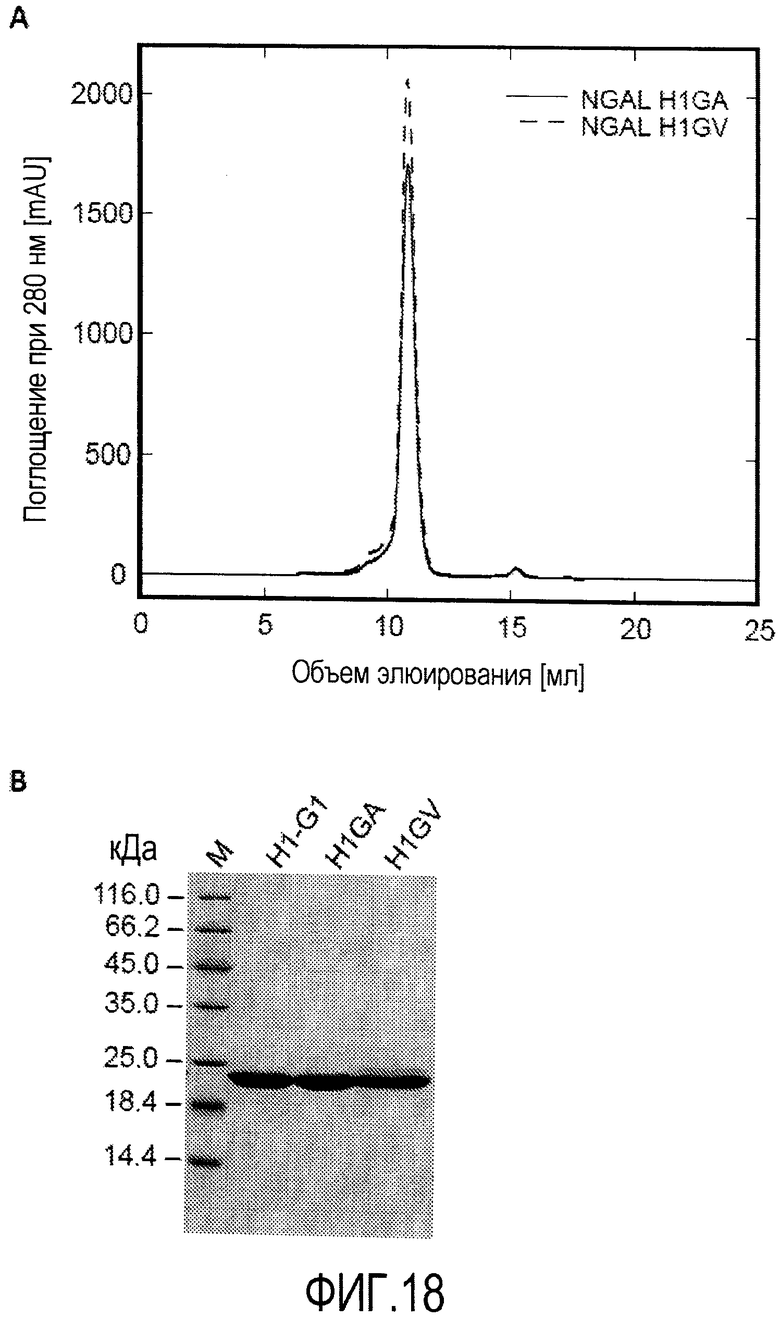
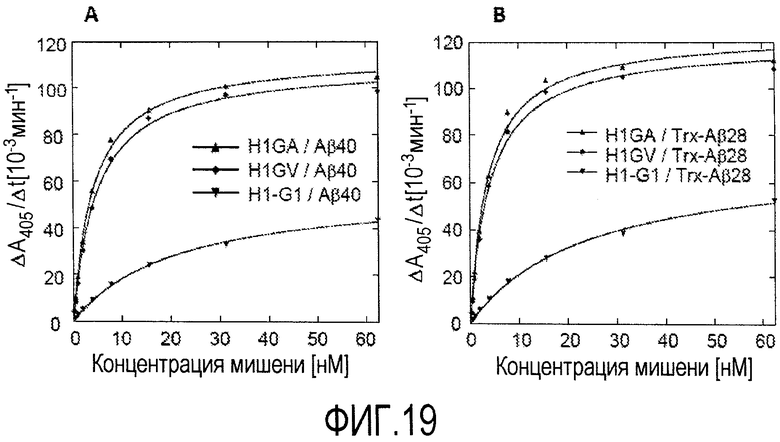
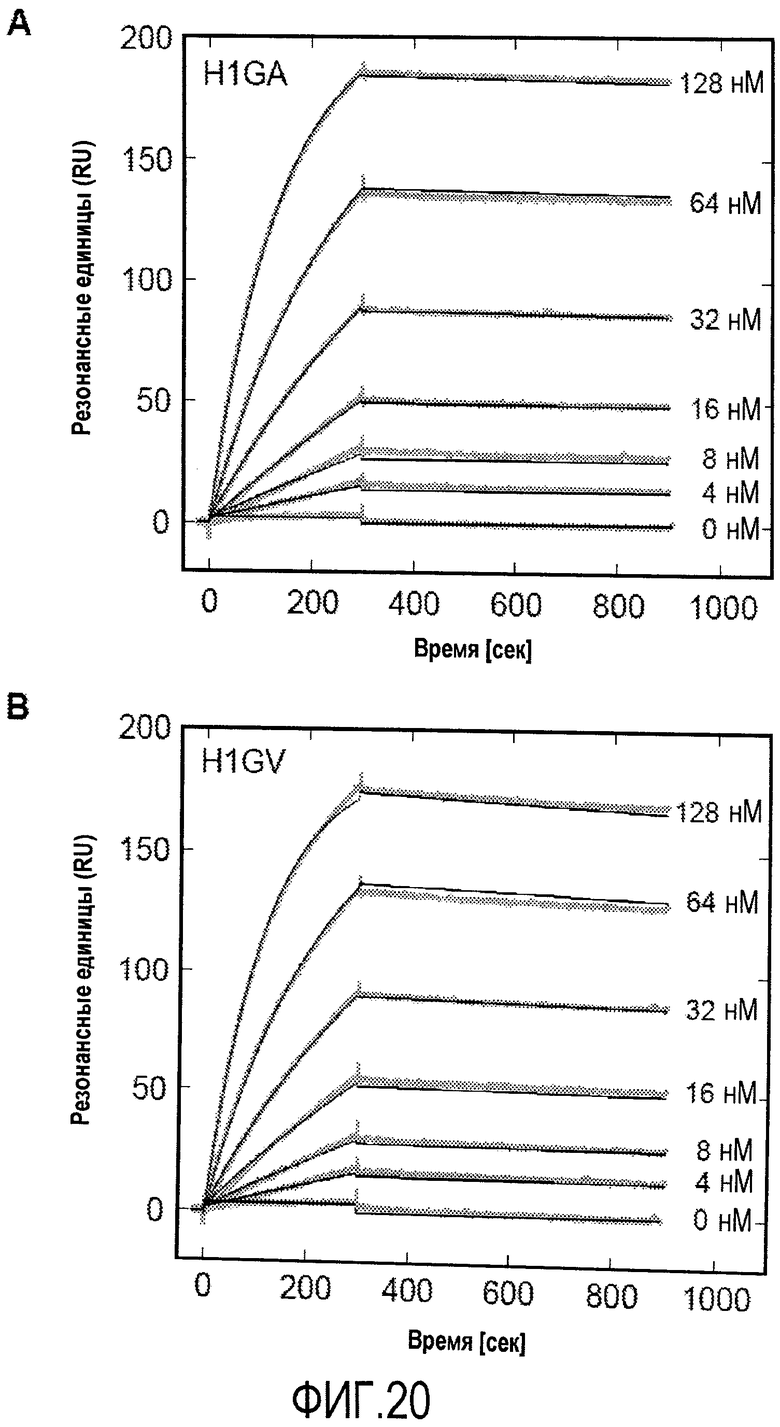
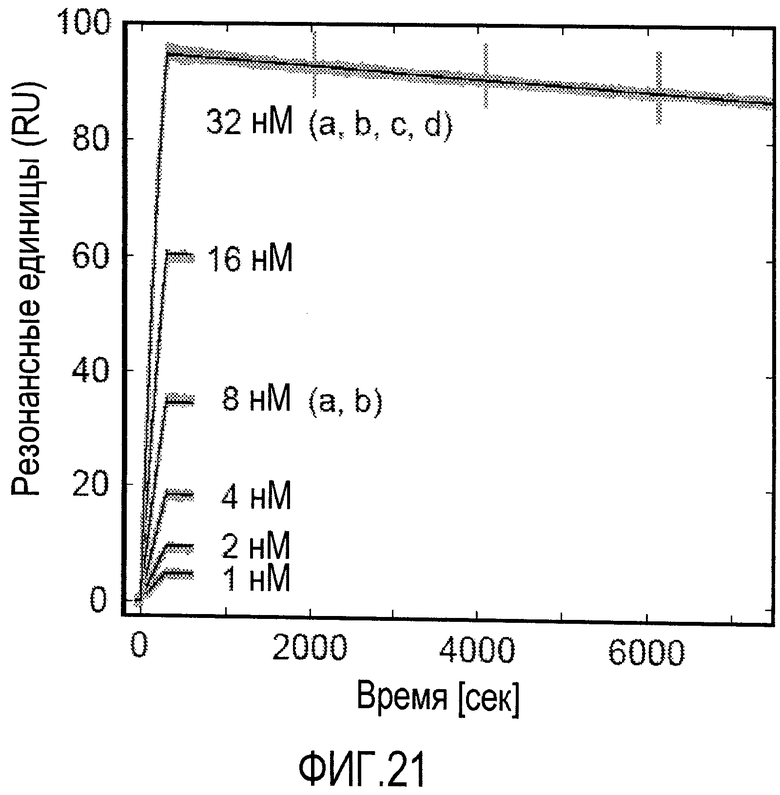
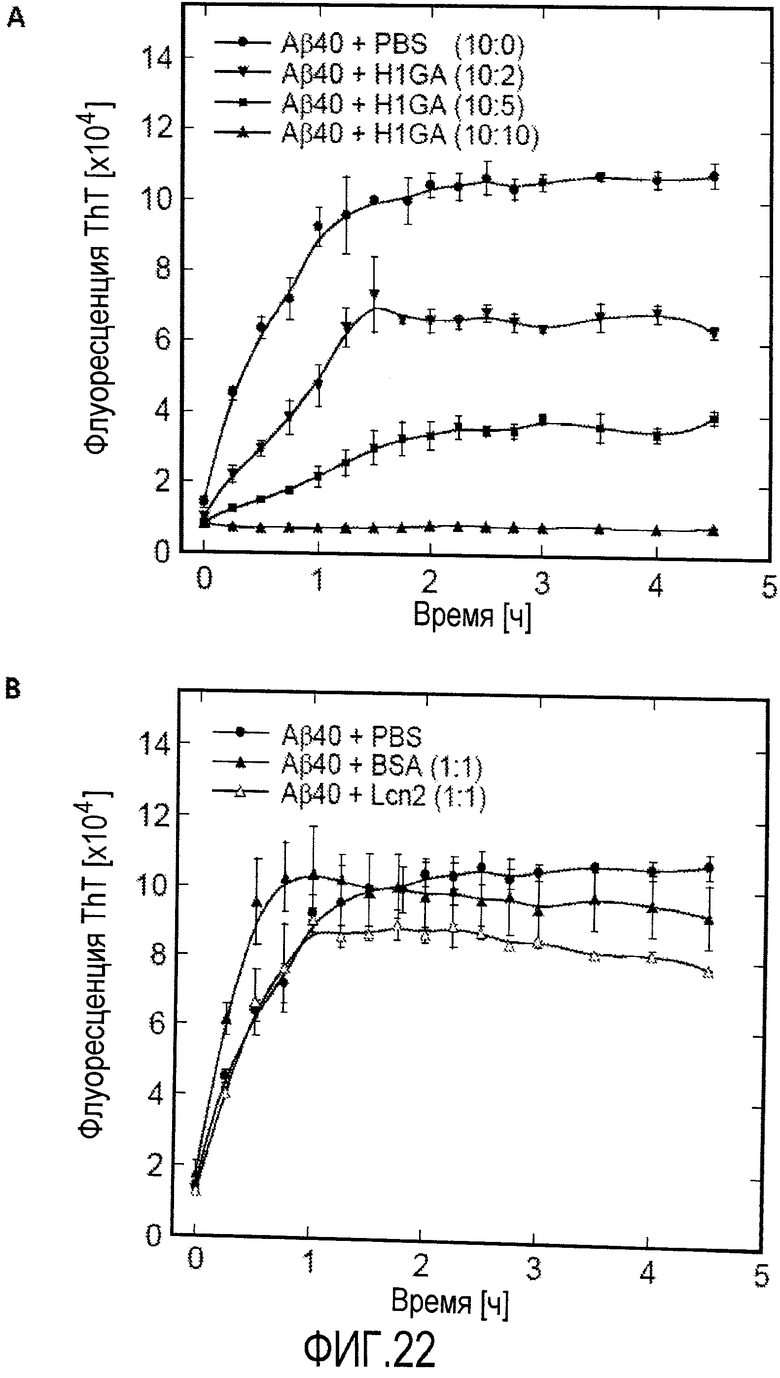
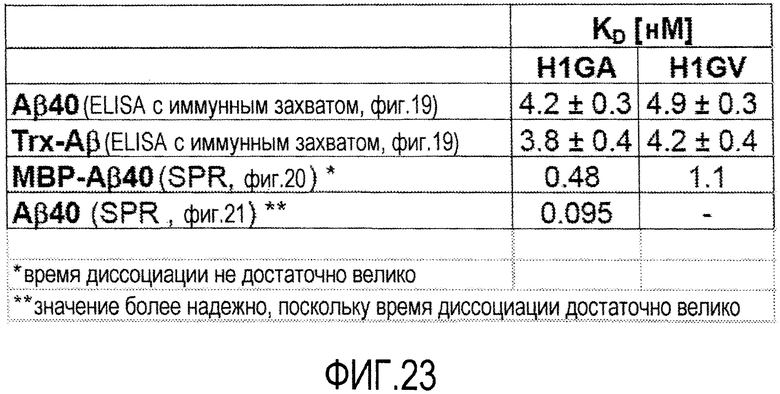
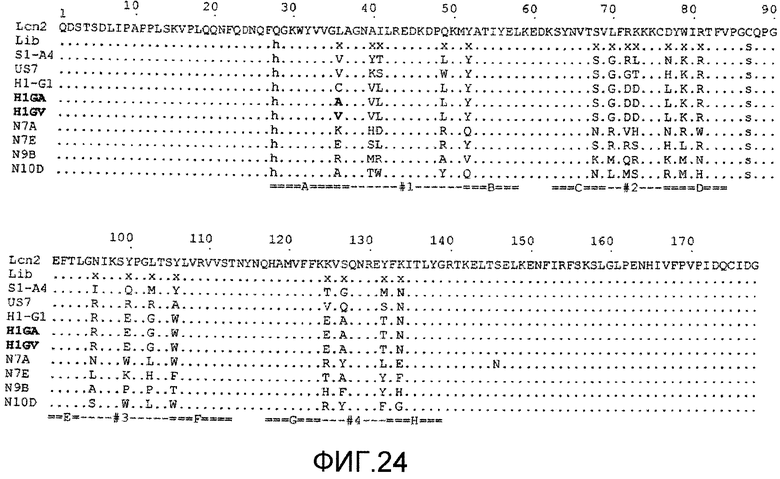

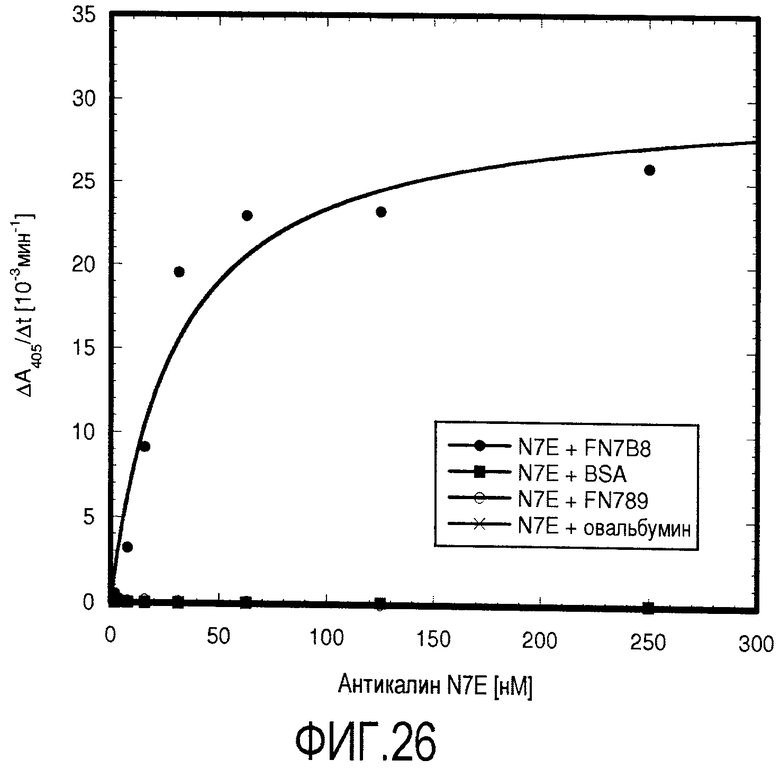
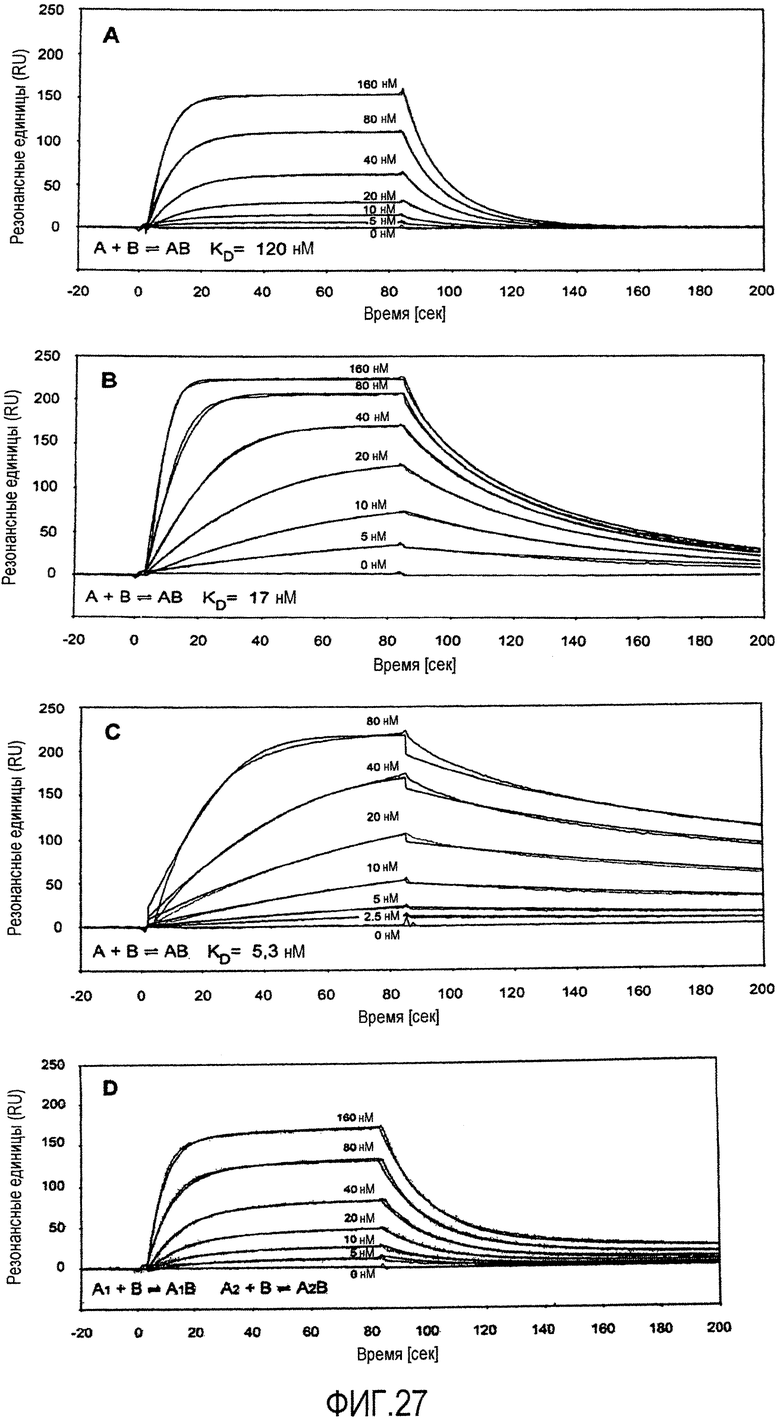
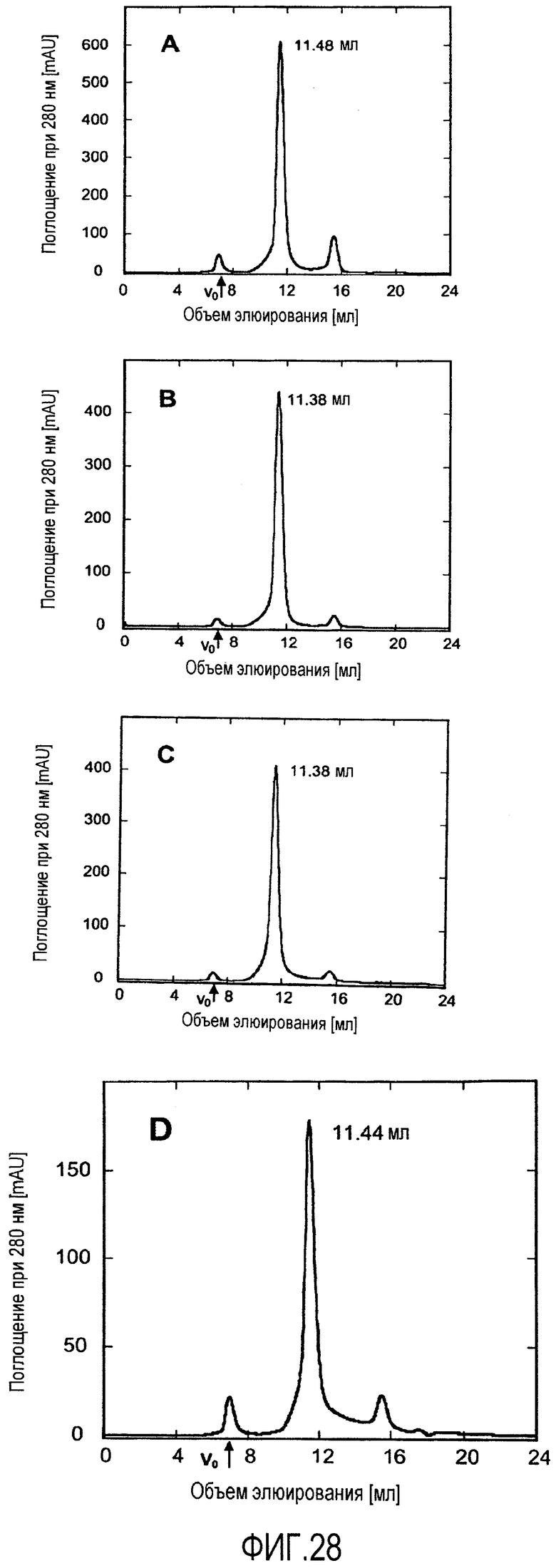
Изобретение относится к области биохимии, в частности к способу получения мутеинов липокалина 2 (Lcn2, hNGAL) человека. Способ основан на мутагенезе молекулы нуклеиновой кислоты, кодирующей белок Lcn2 человека. При этом мутагенезу подвергают по меньшей мере нуклеотидный триплет, кодирующий положение 96 в линейной полипептидной последовательности Lcn2 человека. Также заявлены мутеины, полученные указанным способом, которые связываются с заранее определенной мишенью с обнаруживаемой аффинностью, где указанная мишень не связывается с природным hGAL при физиологических условиях. Изобретение также относится к молекулам нуклеиновой кислоты, кодирующим такие мутеины, клетке-хозяину, а также к диагностическому и аналитическому наборам, включающим мутеины по изобретению. 7 н. и 13 з. п. ф-лы, 28 ил., 3 табл., 24 пр.
1. Способ получения мутеина, полученного из липокалина 2 человека (Lcn2, hNGAL), в котором указанный мутеин связывается с заранее определенной мишенью с обнаруживаемой аффинностью, где указанная мишень не связывается с природным hGAL при физиологических условиях, где способ включает:
(a) стадию, на которой молекулу нуклеиновой кислоты, кодирующую белок Lcn2 человека, подвергают мутагенезу в, по меньшей мере, нуклеотидном триплете, кодирующем положение в последовательности, соответствующее положению 96 в последовательности линейной полипептидной последовательности Lcn2 человека, и в, по меньшей мере, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18 или 19 нуклеотидных триплетах, кодирующих любое положение в последовательности 36, 40, 41, 49, 52, 68, 70, 72, 73, 77, 79, 81, 100, 103, 106, 125, 127, 132 и 134 линейной полипептидной последовательности Lcn2 человека, с получением одной или более молекул нуклеиновой кислоты мутеина,
(b) экспрессию одной или более молекул нуклеиновой кислоты, полученных на стадии (а), в подходящей экспрессионной системе, и
(c) обогащение одним или более мутеинами, обладающими обнаруживаемой аффинностью связывания для определенной мишени с помощью отбора и выделения.
2. Мутеин, полученный из белка Lcn2, который получают способом по п.1, содержащий, по меньшей мере, один мутированный аминокислотный остаток в положении в последовательности, соответствующем положению 96, и, по меньшей мере, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18 или 19 мутированных аминокислотных остатков в любом положении в последовательности, соответствующей положениям в последовательности 36, 40, 41, 49, 52, 68, 70, 72, 73, 77, 79, 81, 100, 103, 106, 125, 127, 132 и 134 линейной полипептидной последовательности Lcn2, и где мутеин связывается с заранее определенной мишенью с обнаруживаемой аффинностью, где указанная мишень не связывается с природным зрелым Lcn2 при физиологических условиях.
3. Мутеин по п.2, содержащий 15, 16 или 17 мутированных аминокислотных остатков в любом из положений 36, 40, 41, 49, 52, 68, 70, 72, 73, 77, 79, 81, 103, 125, 127, 132 или 134 в последовательности линейной полипептидной последовательности hLcn2.
4. Мутеин по п.2, где указанная неприродная мишень выбрана из группы, состоящей из пептида, белка, фрагмента или домена белка, и небольшой органической молекулы.
5. Мутеин по п.4, где пептид является бета-амилоидным пептидом.
6. Мутеин по п.5, где бета-амилоидный пептид является Аβ40 пептидом или Аβ42 пептидом.
7. Мутеин по п.5, где мутеин содержит по сравнению со зрелой аминокислотной последовательностью hLcn2 дикого типа, по меньшей мере, 3, 4, 5, 6, 7, 8, 9, 10, 11 или 12 аминокислотных замен, выбранных из группы, состоящей из Leu36→Val или Cys; Ala40→Tyr или Lys, или Val; Ile41→Thr или Ser, или Leu; Gln49→Leu или Trp; Leu70→Gly; Arg72→Gly или Asp; Lys73→Leu или Trp, или Asp; Asp77→Asn или His, или Leu; Trp79→Lys; Asn96→Ile или Arg; Tyr100→Gln или Arg, или Glu; Leul03→Met или Arg, или Gly; Tyrl06→Ala, или Trp; Lysl25→Thr или Val, или Glu; Ser127→Gly или Gln, или Ala; Tyrl32→Met или Ser, или Thr и Lysl34→Asn.
8. Мутеин по п.7 с последовательностью SEQ ID NO: 39 или SEQ ID NO: 41 или SEQ ID NO: 43.
9. Мутеин по п.4, где белок является фибронектином или его доменом.
10. Мутеин по п.9, где домен фибронектина является экстрадоменом В или его фрагментом.
11. Мутеин по п.9, где мутеин содержит по сравнению со зрелой аминокислотной последовательностью hLcn2 дикого типа, по меньшей мере, 3, 4, 5, 6, 7, 8, 9, 10, 11 или 12 аминокислотных замен, выбранных из группы, состоящей из Leu36→Lys или Glu, или Arg, или Ala; Ala40→His или Met, или Thr, или Ser; Ile41→Asp или Arg, или Trp, или Leu; Gln49→Arg или Ala, или Tyr; Leu70→Arg, или Met; Arg72→Val, или Gin, или Met; Lys73→His или Arg, или Ser; Asp77→Asn или His, или Lys, или Arg; Trp79→Arg или Met, или Leu; Asn96→Lys или Ala, или Ser; Tyr100→Trp или Pro, или Lys; Leul03→His или Pro; Tyrl06→Phe или Trp, или Thr; Lys 125→Arg или His, или Thr; Serl27→Tyr или Phe, или Ala; Tyrl32→Leu или Phe; Lysl34→Glu или His, или Gly, или Phe и Serl46→Asn.
12. Мутеин по п.11 с последовательностью SEQ ID NO: 22 или SEQ ID NO: 24 или SEQ ID NO: 26.
13. Мутеин по любому из пп.2-12, где мутеин дополнительно содержит по сравнению со зрелой аминокислотной последовательностью hLcn2 дикого типа аминокислотные замены, выбранные из группы, состоящей из Gln28→His и Cys87→Ser.
14. Мутеин по любому из пп.2-12, где мутеин конъюгирован с соединением, выбранным из группы, состоящей из органических молекул, ферментных меток, радиоактивных меток, меток в окрашенной форме, флуоресцентных меток, хромогенных меток, люминесцентных меток, гаптенов, дигоксигенина, биотина, цитостатических агентов, токсинов, комплексов металлов, металлов, коллоидного золота, и соединения, которое увеличивает период полураспада мутеина, или где мутеин слит на своем N-конце и/или С-конце с партнером по слиянию, который является белком или доменом белка, или пептидом.
15. Мутеин по любому из пп.2-12, где мутеин связывается с определенной неприродной мишенью с KD, равной по меньшей мере 1 мкМ или ниже, или 100 мкМ или ниже, или 1 мкМ или ниже, или 500 нМ, или 200 нМ или ниже, или 100 нМ или ниже, или 50 нМ или ниже, или 10 нМ или ниже, или 1 нМ или ниже.
16. Молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую мутеин по любому из пп.2-15.
17. Клетка-хозяин для экспрессии мутеина по любому из пп.2-15, содержащая молекулу нуклеиновой кислоты по п.16.
18. Способ получения мутеина по любому из пп.2-15, включающий культивирование клетки-хозяина по п.17 для экспрессии мутеина по любому из пп.2-15 и выделение мутеина из клетки или культуральной среды.
19. Диагностический набор для связывания заранее определенной мишени, содержащий в качестве одного из компонентов набора мутеин по любому из пп.2-15.
20. Аналитический набор для связывания заранее определенной мишени, содержащий в качестве одного из компонентов набора мутеин по любому из пп.2-15.
| KIM H.J | |||
| et al., High-Affinity Recognition of Lanthanide(III) Chelate Complexes by a Reprogrammed Human Lipocalin 2, J | |||
| Am | |||
| Chem | |||
| Soc., 2009, vol.131 (10), pp.3565-3576 | |||
| SKERRA A., Anticalins as alternative binding proteins for therapeutic use, Current Opinion in Molecular Therapeutics, 2007, vol.9, no.4, pp.336-344 | |||
| Способ и приспособление для нагревания хлебопекарных камер | 1923 |
|
SU2003A1 |
| МОДУЛЯТОР АГРЕГАЦИИ ПЕПТИДА β-АМИЛОИДА ДЛЯ ИНГИБИРОВАНИЯ АГРЕГАЦИИ ПЕПТИДОВ ПРИРОДНОГО β -АМИЛОИДА ИЛИ ДЛЯ ЛЕЧЕНИЯ СУБЪЕКТА ОТ НАРУШЕНИЯ, АССОЦИИРОВАННОГО С β -АМИЛОИДОЗОМ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ДЕТЕКЦИИ В БИОЛОГИЧЕСКОМ ОБРАЗЦЕ ПЕПТИДОВ ПРИРОДНОГО β -АМИЛОИДА | 2000 |
|
RU2260599C2 |
Авторы
Даты
2015-09-27—Публикация
2010-12-07—Подача