Область техники, к которой относится изобретение
Настоящее изобретение относится к соединениям, которые могут быть использованы для лечения инфекции Clostridium difficile и заболеваний, вызванных Clostridium difficile, к композициям, содержащим такие соединения, и к способам лечения заболеваний, связанных с Clostridium difficile (CDAD) с помощью таких соединений.
Уровень техники
Антибактериальные средства и Clostridium difficile
Создание лекарств, обладающих антибактериальным действием, представляет собой одно из наиболее важных достижений в медицине 20-го века. С ранее неизлечимыми болезнями стало возможно бороться, и казалось, что с помощью новых невероятных лекарств многие заболевания будут полностью побеждены. Однако несмотря на столь значительные достижения в их лечении, инфекционные заболевания являются третьей из основных причин смертности в США (Clin. Infect. Dis., 2004, 38, 1279-1286) и остаются одной из наиболее значительных проблем здравоохранения во всем мире. Показатели резистентности к лекарствам у всех основных патогенных бактерий быстро растут, и особое беспокойство вызывает возрастание числа нозокомиальных (внутрибольничных) инфекций, а также тяжесть (Infectious Disease Society of America, 2004, Bad Bugs, No Drugs). Появление мультирезистентных патогенов сделало многие современные лекарства первого ряда полностью неэффективными в борьбе с множеством заболеваний.
Предметом особого беспокойства является разновидность бактериальных патогенов, классифицируемых как спорообразующие бактерии. Споры бактерий (эндоспоры) являются латентными нерепродуктивными структурами, образованными бактериями в ответ на стресс из-за неблагоприятных условий окружающей среды. Как только условия окружающей среды становятся благоприятными, споры прорастают и бактерии размножаются. В случае патогенных бактерий прорастание в организме человека-хозяина может в результате вызвать заболевание.
Споры бактерий чрезвычайно устойчивы к действию множества факторов и к условиям окружающей среды, включая радиацию, обезвоживание, температуру, нехватку пищи и химические агенты. Такая природная резистентность к действию химических агентов позволяет спорам сохраняться в течение многих месяцев в таких важнейших местах, как больницы и другие медицинские центры, а также в условиях объектов производства пищевых продуктов, где стандартные очищающие и моющие средства, гермицидные агенты и способы стерилизации не приводят к уничтожению бактерий. В случае производства пищевых продуктов присутствие спор может иметь серьезные последствия, начиная от простой порчи пищевых продуктов и кончая распространением патогенов пищевого происхождения и отравлением продуктами питания. В последнее время внимание привлекли риски, связанные со спорами Bacillus anthracis, возбудителя сибирской язвы. Такие споры могут быть легко получены в виде сухого порошка, который можно распространить множеством способов и использовать в качестве биотеррористического средства. Сибирская язва вызывает наибольшие опасения из всех биотеррористических средств (CDC Emerg. Infect. Dis., 2004, 5 (4), 552-555). Это утверждение можно проиллюстрировать «почтовыми» атаками возбудителя сибирской язвы в Соединенных Штатах в 2001 г. Тогда было подтверждено 22 случая инфицировния, что привело в результате к 5 летальным исходам, причем затраты на очистку и обеззараживание после этих атак составили по оценкам около 1 миллиарда долларов.
Среди спорообразующих бактерии важное место занимают грамположительные эндоспорообразующие бактерии рода Bacillus и Clostridium. Примеры бактерий рода Bacillus, которые связаны с проблемами здоровья человека, включают В. anthracis и В. cereus, но не ограничиваются ими. Bacillus anthracis имеет особенно важное значение как возбудитель сибирской язвы. Инфицирование сибирской язвой может произойти при приеме внутрь, при вдыхании или при кожном контакте со спорами Bacillus anthracis, что в результате приводит к трем различным клиническим формам заболевания. Инфицирование через кожу составляет около 95% всех случаев инфицирования и обычно хорошо контролируется с помощью подходящих антибиотиков. В отсутствие лечения около 20% случаев кожной сибирской язвы приводит к смерти. Кишечная инфекция характеризуется острым воспалением кишечника, которое приводит к тошноте, потере аппетита, рвоте, лихорадке, боли в животе, рвоте с кровью и тяжелой диарее. Кишечная форма сибирской язвы приводит к смерти в 25-60% случаев. Наиболее тяжелой формой заболевания является легочная форма сибирской язвы, которая часто приводит к летальному исходу даже при своевременной и интенсивной антибиотикотерапии. Способность спор возбудителя сибирской язвы легко распространяться по воздуху на обширной территории и индуцировать легочную форму заболевания делает сибирскую язву главным биотеррористическим средством.
Представители рода Clostridium являются грам-положительными, спорообразующими облигатными анаэробами. Примеры видов клостридий, вызывающих заболевания человека, включают С.perfringens, С.tetani, С.botulinium, С.sordellii и С.difficile, но не ограничены только ими. Виды клостридий связаны с разнообразными заболеваниями человека, включающими столбняк, газовую гангрену, ботулизм и псевдомембранозный колит и могут быть причиной пищевых отравлений.
Особенно большое значение имеет заболевание, вызываемое Clostridium difficile. Clostridium difficile вызывает заболевания, связанные с Clostridium difficile (CDAD), и в последние 10 лет отмечается десятикратное увеличение числа случаев CDAD, причем гипервирулентные штаммы и штаммы, резистентные к лекарственным средствам, в настоящее время становятся эндемическими. Данные, недавно полученные НРА, показывают, что в 2006 г. в Англии было зарегистрировано 55681 случаев инфицирования С.difficile у пациентов 65 лет и старше (на 8% больше, чем в 2005 году). Пожалуй, наибольшее беспокойство вызывают появившиеся случаи CDAD, не связанные с применением антибиотиков.
Clostridium difficile представляет собой комменсальную кишечную бактерию, популяция которой контролируются нормальной кишечной флорой. Однако бактерия является возбудителем заболеваний, связанных с С.difficile (CDAD) и была идентифицирована как главная причина наиболее серьезного проявления CDAD-псевдомембранозного колита. CDAD связаны с широким спектром симптомов от легкой диареи до псевдомембранозного колита, токсического мегаколона и летального исхода. Главным фактором риска для развития CDAD является применение антибиотиков, разрушающих нормальную кишечную бактериальную флору, что вызывает чрезмерный рост Clostridium difficile. Хотя клиндамицин является основным антибиотиком, ассоциируемым с CDAD, в настоящее время это заболевание ассоциируется уже почти со всеми антибиотиками, включая антибиотики, относящиеся к классам фторхинолонов, цефалоспоринов, макролидов, р-лактамов и многих других.
Наибольшее беспокойство вызывает CDAD в больничных условиях, и особые опасения связаны с CDAD среди пациентов старшего возраста, для которых уровни смертности особенно высоки. Показатели заболеваемости CDAD резко возросли за последние годы. Более 55000 случаев зарегистрировано в Великобритании в 2006 г.(Отчет отдела инфекционного контроля Агентства защиты здоровья в 2007 г.).
Уровень смертности в США увеличился с 5,7 случаев на миллион населения в 1999 г. до 23,7 случаев на миллион населения в 2004 г. Уровни колонизации С.difficile среди населения достигают 3%, хотя госпитализация приводит к резкому увеличению уровней колонизации, достигающих 25%. Особое беспокойство вызывает появление новых эндемических штаммов. Особенно актуальным примером является гипервирулентный штамм BI/NAP1 (известный также как риботип 027), который демонстрирует повышенное продуцирование токсинов А и В, а также продуцирование дополнительных новых бинарных токсинов.
Решающим фактором, связанным с видами клостридий является высокий уровень бактериальных спор, присутствующих в больничных условиях. Недавно было показано, что многие из стандартных чистящих средств, используемых в больницах, не эффективны для уничтожения клостридиальных спор в окружающей среде, что приводит к неэффективному контролю заболевания (Infect Cont. Hosp.Epidemiol., 2007, 28, 920-5). Чрезмерное спорообразование, характерное для таких штаммов, как BI/NAP1 вносит значительный вклад в рассматриваемую проблему.
Хотя основные факторы риска, связанные с CDAD, обусловлены применением антибиотиков и возрастом (CMAJ, 2008, 179 (8), 767-772; J. Antimicrob. Chem., 2003, 51, 1339-1350), известно и множество других связанных с CDAD факторов, включая, например, применение ингибиторов протонной помпы, применение антагонистов Н2 рецепторов, применение диуретиков, продолжительное пребывание в больнице, использование зондового питания, искусственная вентиляция легких и предрасполагающие сопутствующие заболевания.
Кислотность желудочного сока представляет собой часть механизма естественной защиты против поступивших внутрь (через рот) патогенов, и любое уменьшение кислотности в желудке может в результате привести к колонизации обычно стерильных верхних отделов желудочно-кишечного тракта, что может привести к нарушению нормальной кишечной микрофлоры. В связи с этим, использование средств, подавляющих кислотность желудочного сока, таких как ингибиторы протонной помпы (PPI), антагонисты Н2 гистаминовых рецепторов (H2Ra), связано с повышенным риском образования колоний С.difficile и последующего развития CDAD. Использование PPI и H2Ras ранее ассоциировалось с другими кишечными инфекциями, такими как диарея путешественников, сальмонеллез и холера. Dial с соавторами подтвердили, что риск заболевания CDAD увеличивается при использовании средств, подавляющих кислотность желудочного сока, как вне больницы (JAMA, 2005, 294(23), 2989-2995), так и в больничных условиях (CMAJ, 2004, 171(1). 33-38).
Ингибиторы протонной помпы (PPI) включают (но не ограничиваются только перечисленным) омепразол (лосек, прилосек, зегерид), лансопразол (превацид, зотон, ингибитол), эзомепразол (нексиум), пантопразол (протоникс, сомак, пантолок, пантозол, зуркал, пан) и рабепразол (рабецид, асифекс, париет, рабелок).
Антагонисты H2Ra включают циметидин (тагамет), ранитидин (зинетак, зантак), фамотидин, (пепсидин, пепсид), роксатидин (роксит) и низатидин (тазак, аксид), но не
ограничиваются только ими.
Тройная терапия с использованием PPI или H2Ra вместе с комбинацией двух антибиотиков является общепринятым способом лечения, предназначенным для уничтожения инфекций Helicobacter pylori (Aliment. Pharmacol. Ther., 2001,15(5), 613-624;
Helicobacter., 2005, 10(3'), 157-171). Однако имеется несколько сообщений о том, что указанный курс лечения тройной терапией может приводить в качестве побочного эффекта к CDAD (Am. J. Gastroenterol., 1998, 93(7), 1175-1176; J. Int. Med., 1998, 243(3), 251-253; Aliment. Pharm. Ther., 2001, 15(9), 1445-1452; Med. Sci. Monit, 2001, 1(4), 751-754). Обычные антибактериальные средства, используемые для лечения инфекций Helicobacter pylori, представляют собой комбинацию средств, выбранных из метронидазола, амоксициллина, левофлоксацина и кларитромицина (но не ограниченных только ими), многие из которых напрямую ассоциируются с развитием CDAD.
Применяемые в настоящее время виды терапии крайне ограничены; особенно в свете того факта, что почти все классы антибиотиков могут выступать в качестве причины развития заболевания. Единственным лекарством для лечения CDAD, получившим одобрение FDA, является ванкомицин, хотя метронидазол также широко используется. Широкое применение ванкомицина для лечения CDAD вызывает опасения из-за его бактериостатического действия в отношении клостридий, относительно высокой стоимости и возможного отбора как резистентных штаммов С.difficile, так и других бактерий (особенно Enterococcus spp.). Ключевой проблемой как для метронидазола, так и для ванкомицина является высокая частота рецидивов, причем по меньшей мере 20% пациентов испытывают по меньшей мере один эпизод рецидива. Предполагают, что рецидив происходит из-за неспособности уничтожить споры клостридий в ходе лечения, что в результате приводит к последующему их прорастанию и патогенному состоянию. Такая неспособность контролировать образование спор создает возможность для длительной зараженности больничной среды. По этой причине средства, способные уничтожать вегетативные клетки и контролировать эндоспоры, обладали бы значительным преимуществом.
Основным моментом в выборе терапии для лечения CDAD является прекращение любого антимикробного лечения, за которым следует надлежащее применение или ванкомицина, или метронидазола. Оба средства обычно вводят перорально, хотя метронидазол можно также вводить внутривенно, а в тяжелых случаях ванкомицин можно вводить другими путями, в том числе через толстую кишку, назальный желудочный зонд или в виде ванкомицин-удерживающей клизмы. Дополнительные антибиотики, которые, - как сообщают, используют в лечении CDAD, включают фусидовую кислоту, рифамицин и его аналоги, тейкопланин и бацитрацин, хотя ни один из них не обладает эффективностью, превышающей эффективность ванкомицина или метронидазола. Кроме прекращения послужившего причиной заболевания антибактериального лечения, следует избегать и использования антиперистальтических средств, опиатов или лоперамида, так как они могут замедлить очистку от токсинов, продуцируемых С.Difficile, и усугубить обусловленное токсинами повреждение толстой кишки. Указанные средства могут также вызывать непроходимость кишечника и быть причиной токсической дилатации толстой кишки. (J. Med. Microbiol, 2005, 54, 101-111; JAMA, 1993, 269, 71-5; Postgrad. Med. J, 1990, 66(777), 582).
Альтернативные виды терапии, используемые в виде стандартных одиночных средств или в сочетании с антибактериальными средствами, ставят своей целью или попытку восстановить естественную популяцию микроорганизмов в кишечнике и уменьшить уровни токсинов, продуцируемых С.difficile, или стимулировать иммунную систему (для обзоров см. Antibiotic Treatment for Clostridium difficile-Associated Diarrhea in Adults, Cochrane Database of Systematic Reviews 2007, Issue 3, Art. No.: CD 004610; Clin. Inf. Dis, 2008, 46(S1), S32-S42; Clin. Inf. Dis„ 2007, 45(S2), S122-S128; J. Med. Microbiol., 2005, 54, 101-111 и ссылки, приведенные в них). Таким образом, альтернативные виды лечения CDAD включают введение Saccharomyces boulardii или Lactobacillus acidophilus в сочетании с антибиотиками, трансплантацию фекальных масс и в тяжелых случаях, когда все другие виды терапии не дают результата, хирургию. Хотя частота колэктомии низка (до 3% случаев), она связана с высоким уровнем смертности (до 60%).
В связи с этим, существует насущная потребность в новых и эффективных средствах для лечения заболеваний, связанных со спорообразующими бактериями, особенно с теми, которые вызываются представителями рода Clostridium и Bacillus и, в частности, заболеваниями, связанными с инфицированием бактерией Clostridium difficile. Указанная потребность является особенно острой в свете рефракторной природы бактерии Clostridium difficile, резистентной в отношении многих антибиотиков широкого спектра действия (включая р-лактамные и хинолоновые антибиотики) и частоты, с которой возникает резистентность (Antimicrob. Agents Chemother., 1985, 28(6): 842-844).
Уровень техники
В публикациях международных заявок WO 2007056330, WO 2003105846 и WO 2002060879 описаны различные 2-аминобензимидазолы, выступающие в качестве антибактериальных средств.
WO 2007148093 раскрывает в качестве антибактериальных средств различные 2-аминобензотиазолы.
В WO 2006076009, WO 2004041209 и статье Bowser et al. (Bioorg. Med. Chem. Lett., 2007, 17, 5652-5655) описаны различные производные замещенного бензимидазола, которые могут быть использованы в качестве антибактериальных средств, способных уменьшать резистентность, вирулентность или скорость размножения микробов. Сообщается, что соединения не проявляют собственной антимикробной активности in vitro.
В патенте США US 5,824,698 описаны различные дибензимидазолы в качестве антибиотиков широкого спектра действия, проявляющих активность как в отношении грамотрицательных, так и в отношении грамположительных бактерий, в том числе Staphylococcus spp.и Enterococcus spp.Однако в указанном патенте не сообщается об активности в отношении анаэробных спорообразующих бактерий и, в частности, не имеется данных об активности в отношении любых бактерий Clostridium spp.(в том числе С.difficile).
В заявке на патент США US 2007/0112048 Al описаны различные би- и триарилимидазолидины и би- и триариламидины в качестве антибиотиков широкого спектра действия, проявляющих активность в отношении как грамотрицательных, так и грамположительных бактерий, в том числе Staphylococcus spp., Enterococcus spp. и Clostridium spp. Однако в указанном документе не раскрываются соединения общей формулы (I), описанные в настоящей заявке.
В статье Chaudhuri et al. (J. Org. Chem., 2007, 72, 1912-1923) описаны различные бис-2-(пиридил)-1Н-бензимидазолы (в том числе соединения формулы I, как они описаны в настоящем документе) в качестве средств, связывающихся с ДНК. В этом документе нет данных о потенциальной антибактериальной активности.
Раскрытие изобретения
Таким образом, первым объектом настоящего изобретения является соединение общей формулы (I)
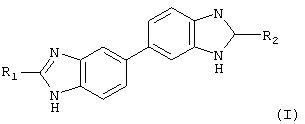
где R1 выбран из необязательно замещенной арильнои, гетероарильной, карбоциклильной и гетероциклильной группы, причем такое необязательное замещение осуществляется одним или несколькими заместителями, выбранными из галогена, CN, NO2, R3, OR3, N(R3)2, COR3, CO3R3, C(=O)SR3, SR3, S(=O)R3, SO2R3, NR4C(=O)R3, NR4CO2R3, ОС(=O)NR3R4, NR4SO2R3, C(=NR4)NR3R4, C(=S)NR3R4, NR4C(=NR4)NR3R4, NR4C(=S)NR3R4, NR4C(=O)NR3R4, CONR3R4 и SO2NR3R4;
R2 представляет собой необязательно замещенную ароматическую 8-14-членную конденсированную бициклическую или трициклическую кольцевую систему, в которой один или несколько атомов углерода могут быть замещены N, О, S, SO или SO2, причем такое необязательное замещение осуществляется одним или несколькими заместителями, выбранными из галогена, CN, NO2, R3, OR3, N(R3)2, COR3, CO2R3, C(=O)SR3, SR, S(=O)R3, SO2R3, NR4C(=O)R3, NR4CO2R3, OC(=O)NR3R4, NR4SO2R3, C(=NR4)NR3R4, C(=S)NR3R4, NR4C(=NR4)NR3R4, NR4C(=S)NR3R4, NR4C(=O)NR3R4, CONR3R4 и SO2NR3R4;
R3 выбран из H, C1-C6 алкила, C2-C6 алкенила, C2-C6 алкинила, С3-С7 карбоциклила, С4-С7 гетероциклила и 5- или 6-членного арила или гетероарила, любой из которых может быть необязательно замещен одним или несколькими заместителями, выбранными из галогена, CN, NO2, R4, OR4, N(R4)2, COR4, CO2R4, C(=O)SR4, SR4, S(=O)R4, SO2R4, NR4C(=O)R4, NR4CO2R4, OC(=O)NR4)2, NR4SO2R4, C(=NR4)N(R4)2, C(=S)N(R4)2, NR4C(=NR4)N(R4)2, NR4C(=S)N(R4)2, NR4C(=O)N(R4)2, CON(R4)2 и SO2N(R4)2;
R4 выбран из водорода, C1-C6 алкила и С3-С7 карбоциклила, необязательно замещенного одним или несколькими атомами галогена;
или его фармацевтически приемлемые N-оксид, соль, гидрат, сольват, комплекс, биоизостера, метаболит или пролекарство для использования в способе лечения заболеваний, связанных с Clostridium difficile (CDAD).
Некоторые из соединений общей формулы (I) являются новыми. Таким образом, согласно изобретению, авторы также изобрели те соединения общей формулы (I), которые являются новыми, вместе со способами для их получения, композициями, их содержащими, и их применением в качестве фармацевтических препаратов.
Следовательно, еще одним объектом изобретения является соединение общей формулы (I)

R1 выбран из необязательно замещенной арильнои, гетероарильной, карбоциклильной и гетероциклильной группы, причем такое необязательное замещение осуществляется одним или несколькими заместителями, выбранными из галогена, CN, NO2, R3, OR3, N(R3)2, СOR3, CO2R3, C(=O)SR3, SR3, S(=O)R3, SO2R3, NR4C(=O)R3, NR4CO2R3, OC(=O)NR3R4, NR4SO2R3, C(=NR4)NR3R4, C(=S)NR3R4, NR4C(=NR4)NR3R4, NR4C(=S)NR3R4, NR4C(=O)NR3R4, CONR3R4 и SO2NR3R4;
R2 представляет собой необязательно замещенную ароматическую 8-14-членную конденсированную бициклическую или трициклическую кольцевую систему, в которой один или несколько атомов углерода могут быть замещены N, О, S, SO или SO2 причем такое необязательное замещение осуществляется одним или несколькими заместителями, выбранными из галогена, CN, NO2, R3, OR3, N(R3)2, COR3, CO2R3, C(=O)SR3, SR3, S(=O)R3, SO2R3, NR4C(=O)R3, NR4CO2R3, ОС(=O)NR3R4, NR4SO2R3, C(=NR4)NR3R4, C(=S)NR3R4, NR4C(=NR4)NR3R4, NR4C(=S)NR3R4, NR4C(=O)NR3R4, CONR3R4 и SO2NR3R4;
R3 выбран из H, C1-C6 алкила, C2-C6 алкенила, C2-C6 алкинила, C3-C7 карбоциклила, C4-C7 гетероциклила и 5- или 6-членного арила или гетероарила, любой из которых может быть необязательно замещен одним или несколькими заместителями, выбранными из галогена, CN, NO2, R4, OR4, N(R4)2, COR4, CO2R4, C(=O)SR4, SR4, S(=O)R4, SO2R4, NR4C(=O)R4, NR4CO2R4, OC(=O)NR4)2, NR4SO2R4, C(=NR4)N(R4)2, C(=S)N(R4)2, NR4C(=NR4)N(R4)2, NR4C(=S)N(R4)2, NR4C(=O)N(R4)2, CON(R4)2 и SO2N(R4)2;
R4 выбран из водорода, C1-C6 алкила и С3-С7 карбоциклила, необязательно замещенного одним или несколькими атомами галогена;
или его фармацевтически приемлемые N-оксид, соль, гидрат, сольват, комплекс, биоизостера, метаболит или пролекарство.
Соединение согласно вышеприведенному определению может быть использовано в терапии или для профилактики, например, для лечения бактериальной инфекции или заболевания (например, для лечения CDAD).
Еще одним объектом изобретения является способ лечения бактериальной инфекции или бактериального заболевания (например, CDAD) у субъекта, включающий введение упомянутому субъекту эффективного количества соединения согласно вышеприведенному определению.
Еще одним объектом изобретения является способ уничтожения бактерии или ингибирования, уменьшения или предотвращения ее роста, включающий контакт указанной бактерии с соединением согласно вышеприведенному определению. В таких вариантах осуществления изобретения бактерия предпочтительно представляет собой Clostridium difficile.
Описываются также комбинации, содержащие соединение по изобретению согласно вышеприведенному определению и различные дополнительные средства, как указано ниже.
В формуле изобретения, изложенной ниже, представлены и другие объекты настоящего изобретения.
Подробное описание изобретения
Все публикации, патенты, патентные заявки и другие ссылки, упомянутые в данном документе, полностью и для всех целей включаются в настоящее описание посредством ссылки, подобно тому, как если бы каждая отдельная публикация, патент или патентная заявка были конкретно и по отдельности включены в описание путем отсылки, а их содержание было приведено здесь в полном объеме.
Определения и общие параметры
Подразумевается, что используемые в настоящей заявке следующие термины, если конкретно не указано иное, имеют указанные ниже значения в дополнение к любым более широким (или более узкими) значениям, используемым в данной области техники.
Если иное не следует из контекста, следует понимать, что использование в настоящем документе единственного числа включает и множественное и наоборот. При этом при использовании единственного числа, а также выражения "один или несколько" и выражения "по меньшей мере" подразумевается, что все эти варианты эквивалентны друг другу.
Используемый в настоящем документе термин "содержать," или его вариации, такие как "содержит" или "содержащий," следует понимать как указание на включение любой указанной сущности (например признака, элемента, характеристики, свойства, стадии метода/способа или ограничения) или группы сущностей (например признаков, элементов, характеристик, свойств, стадий метода/способа или ограничений), но не на отсутствие других сущностей или группы сущностей. Следовательно, используемый в настоящем документе термин "содержащий" является инклюзивным или неограничивающим и не исключает наличия дополнительных неперечисленных сущностей или стадий метода/способа.
Фразу "состоящий по существу из" используют в настоящем документе для указания на необходимость конкретной(ых) сущности(ей) или стадий, в дополнение к тем, которые на практике не влияют на характер или функционирование заявляемого изобретения.
Используемый в настоящем документе термин "состоящий" используют только лишь для обозначения наличия указанной сущности (например, признака, элемента, характеристики, свойства, стадии метода/способа или ограничения) или группы сущностей (например, признаков элементов, характеристик, свойств, стадий метода/способа или ограничений).
Используемый в настоящем документе термин "заболевание" используют для обозначения любого ненормального состояния, которое отрицательно влияет на физиологическую функцию и связано со специфическими симптомами. Термин широко используется для обозначения любых заболеваний, болезней, аномалий, патологий, нарушений, состояний или синдромом, при которых физиологическая функция нарушена, независимо от природы этиологии (или даже независимо от того, установлена ли вообще этиологическая основа заболевания). Таким образом, термин охватывает состояния, возникающие в результате травмы, ранения, хирургического вмешательства, радиологической абляции, отравления или недостаточного питания.
Используемый в настоящем документе термин "бактериальное заболевание" относится к любому заболеванию, которое предполагает участие бактерии (например, которое вызывается, обостряется бактериями, связано с бактериями или характеризуется наличием бактерий), обитающей и/или размножающейся в организме и/или клетках субъекта. Таким образом, термин включает заболевания, которые вызываются или обостряются бактериальными токсинами (которые также можно называть здесь "бактериальной интоксикацией"). Более конкретный термин "заболевание Clostridium difficile" интерпретируется соответствующим образом.
Используемый в настоящем документе термин «заболевание, связанное с Clostridium difficile» (CDAD) используют для обозначения любого заболевания, в котором участвует бактерия Clostridium difficile (например, вызываемого, обостряемого этой бактерией, связанного с присутствием этой бактерии или характеризуемого ее присутствием), обитающая или (размножающаяся) в организме субъекта. Таким образом, этот термин охватывает все заболевания, нарушения, патологии, симптомы, клинические состояния или синдромы, при которых бактерия вида Clostridium difficile выступает в роли этиологического агента, или при котором инфекцию одним или несколькими штаммами Clostridium difficile подозревают, обнаруживают или при котором имеет место такая инфекция. Таким образом, термин включает различные формы колита, псевдомембранозного колита, диареи и антибиотикоассоцированного заболевания.
Используемый в настоящем документе термин "средство, селективное в отношении Clostridium difficile" применяют для указания на соединение, которое проявляет бактериостатическую и/или бактерицидную активность в отношении одного или нескольких штаммов бактерии С.difficile, но которое не проявляет бактериостатической и/или бактерицидной активности в отношении одного или нескольких представителей естественной флоры пищеварительной системы, выбранных из: (a) Escherichia spp.(например Escherichia соlli); (b) Bacteroides spp.(например В. fragilis); (с) Fusobacterium spp.; (d) Eubacterium spp.(e) Ruminococcus spp.; (f) Peptococcus spp.; (g) Peptostreptococcus spp.; (h) Bifidobacterium spp.; (i) Lactobacillus spp.; (j) Enterococcus spp.(например E. faecium); (k) видов клостридий, отличных от С.difficile (например С.perfringens); (1) Enterobacter spp.; (m) Serratia spp.; (n) Klebsiella spp.; (o) Proteus spp.; (p) Pseudomonas spp.и (q) Veillonella spp.
Предпочтительные селективные в отношении Clostridium difficile агенты проявляют бактериостатическую и/или бактерицидную активность в отношении одного или нескольких штаммов бактерии С.difficile, но не проявляют бактериостатической и/или бактерицидной активности в отношении (a) Escherichia coli; или (b) В. fragilis.
Таким образом, некоторые предпочтительные селективные в отношении Clostridium difficile агенты по изобретению проявляют бактериостатическую и/или бактерицидную активность против одного или нескольких штаммов бактерии С.difficile, но не обладают бактериостатической и/или бактерицидной активностью в отношении В. fragilis.
Используемый в настоящем документе термин "бактериальная инфекция" применяют для определения состояния, при котором субъект инфицирован бактерией. Инфекция может быть симптоматической или асимптоматической. В последнем случае субъект может быть идентифицирован как инфицированный на основе различных тестов, включающих, например, биохимические тесты, серологические тесты, тесты на микробиологические культуры и/или микроскопию.
Термины «бактериостатический» и «бактерицидный» представляют собой термины, используемые в уровне техники для определения способности предотвращать рост бактерий (или уменьшать его скорость) и опосредовать (непосредственно или косвенным образом) клеточную деструкцию бактериальных клеток, соответственно. Эти термины не являются взаимоисключающими, и многие средства оказывают как бактериостатическое, так и бактерицидное действие (в некоторых случаях дозоспецифичным или мишенеспецифичным образом). Как правило, терапия бактерицидными средствами приводит к лучшим результатам, и бактерицидные средства являются предпочтительными.
Используемый в настоящем документе термин "антибиотик широкого спектра действия" обозначает средство, которое является бактерицидным и/или бактериостатическим в отношении множества бактерий, включающих как грамположительные, так и грамотрицательные бактерии.
Термин "мультирезистентный" (MDR), применяемый здесь в отношении бактерии, обозначает бактерию, резистентную к двум или нескольким классам антибиотиков, включающим антибиотики, выбранные из пенициллина, метициллина, хинолона, макролида и/или ванкомицина, но не ограниченных ими.
Используемые здесь термины "лечение" или "лечащий" относятся к вмешательству (например, к введению средства субъекту), которое излечивает, улучшает состояние или ослабляет симптомы заболевания или устраняет (или ослабляет воздействие) его причину (ы) (например, патогенную бактерию). В этом случае этот термин используют как синоним термина "терапия". Таким образом, лечение инфекции в соответствии с изобретением можно охарактеризовать непосредственным или опосредованным бактериостатическим и/или бактерицидным действием соединения по изобретению.
Кроме того, используемые здесь термины "лечение" или "лечащий" относятся к вмешательству (например, к введению средства субъекту), которое предотвращает проявление или замедляет развитие болезни или уменьшает (или устраняет) заболеваемость в группе пациентов, получавших лечение. В этом случае термин используют как синоним термина "профилактика".
Термин "субъект" (который следует понимать как включающий понятия "индивидуум", "животное", "пациент" или "млекопитающее" в случаях, где это позволяет контекст) определяет любой субъект, особенно субъект-млекопитающее, для которого показано лечение. Субъекты-млекопитающие включают человека, приматов, домашних животных, сельскохозяйственных животных, домашних животных и грызунов, таких, как мыши, крысы, хомяки и морские свинки. В предпочтительных вариантах осуществления изобретения субъектом является человек.
Термин «грамположительная бактерия» является специальным термином, обозначающим в уровне техники конкретный класс бактерий, которые группируют вместе, исходя из некоторых характеристик окрашивания клеточных стенок.
Термин «грамположительная бактерия с низким содержанием G+C» является специальным термином, обозначающим в уровне техники конкретный подкласс эволюционно родственных грамположительных бактерий, исходя из набора оснований в ДНК. Этот подкласс включает Streptococcus spp., Staphylococcus spp., Listeria spp., Bacillus spp., Clostridium spp., Enter ococcus spp.и Lactobacillus spp.
Термин "минимальная ингибирующая концентрация" или "MIC" обозначает самую низкую концентрацию испытываемого соединения, которая необходима для того, чтобы ингибировать бактериальный изолят in vitro. Общепринятый метод определения MIC антибиотика состоит в приготовлении нескольких пробирок, содержащих последовательные разведения испытываемого соединения, которые затем инокулируют с исследуемым бактериальным изолятом. После инкубирования при соответствующих атмосфере и температуре можно определить MIC антибиотика по пробирке с самой низкой концентрацией, в которой не наблюдают помутнения.
Подразумевается, что используемый в настоящем документе в отношении двух или нескольких соединений и/или средств (также называемых здесь компонентами) термин "комбинация", обозначает вещество, в котором связаны два или несколько соединений/средств. Термины "комбинированный" и "комбинирование" в данном контексте интерпретируются соответствующим образом.
Объединение двух или нескольких соединений/средств в комбинации может происходить физическим и нефизическим путем. Примеры физически объединенных в комбинации соединений/средств включают:
- композиции (например, унитарные препараты), содержащие два или больше соединений/средств в смеси (например, в одной и той же единичной дозе);
- композиции, содержащие вещество, в котором два или несколько соединений/средств связаны химически/физико-химически (например, путем сшивки, агломерации молекул или связывания с остатком общего носителя);
- композиции, содержащие вещество, в котором два или несколько соединений/средств химически/физико-химически «упакованы» вместе (например, размещены на или в липосомах, частицах (например, микро- или наночастицах) или в каплях эмульсии);
- фармацевтические наборы, фармацевтические упаковки, упаковки для пациента, в которых два или несколько соединений/средств упакованы или находятся вместе (например, как часть комплекта единичных доз).
Примеры соединений/средств, объединенных в комбинации нефизическим путем, включают:
- вещество (например, неунитарный препарат), содержащее по меньшей мере одно из двух или большего числа соединений/средств, вместе с инструкциями для экстемпоральной ассоциации по меньшей мере одного соединения/средства для образования физической ассоциации двух или нескольких соединений/средств;
- вещество (например, неунитарный препарат), содержащее по меньшей мере одно из двух или большего числа соединений/средств, вместе с инструкциями для комбинированной терапии двумя или несколькими соединениями/средствами;
- вещество, содержащее по меньшей мере одно из двух или большего числа соединений/средств, вместе с инструкциями для введения группе пациентов, которым другое(ие) из двух или большего числа соединений/средств уже были введены (или вводятся);
- вещество, содержащее по меньшей мере одно из двух или большего числа соединений/средств в количестве или в форме, которые специально адаптированы для применения в комбинации с другим(и) из двух или большего числа соединений/средств.
Используемый в настоящем документе термин "комбинированная терапия" предназначен для обозначения видов терапии, которые включают использование комбинации двух или нескольких соединений/средств (как определено выше). Так, ссылки на "комбинированную терапию", "комбинации" и использование соединений/средств "в комбинации" в настоящем изобретении могут относиться к соединениям/средствам, которые вводятся как часть одной общей схемы лечения. По существу нозология каждого из двух или нескольких соединений/средств может отличаться: все они могут вводиться в одно и то же время или же в разное время. Поэтому понятно, что соединения/средства комбинации можно вводить последовательно (например, до или после) или одновременно, в одном и том же фармацевтическом препарате (т.е. вместе), или в различных фармацевтических препаратах (т.е. по отдельности). Одновременно в одном фармацевтическом препарате означает унитарный препарат, тогда как одновременно в различных фармацевтических препаратах означает неунитарный препарат. Позологии каждого из двух или нескольких соединений/средств в комбинированной терапии могут также отличаться в отношении пути введения.
Используемый в настоящем документе термин "фармацевтический набор" обозначает комплект одной или нескольких единичных доз фармацевтической композиции вместе со средствами дозирования (например, с измерительным устройством) и/или средствами доставки (например, ингалятором или шприцем), все это необязательно содержится в одной общей упаковке. В фармацевтических наборах, содержащих комбинацию двух или нескольких соединений/средств, индивидуальные соединения/средства могут составлять унитарные или неунитарные препараты. Единичные дозы могут находиться в блистерной упаковке. Фармацевтический набор может, кроме того, необязательно содержать инструкции по применению.
Используемый в настоящем документе термин "фармацевтическая упаковка" обозначает комплект одной или нескольких единичных доз фармацевтической композиции, необязательно содержащийся внутри общей внешней упаковки. В фармацевтических упаковках, содержащих два или большее число соединений/средств, индивидуальные соединения/средства могут составлять унитарные или неунитарные препараты. Единичные дозы могут содержаться в блистерной упаковке. Фармацевтическая упаковка может необязательно дополнительно содержать инструкции по применению.
Используемый в настоящем документе термин "упаковка для пациента" означает упаковку лекарств, прописанных пациенту, которая содержит фармацевтические композиции для всего курса лечения. Упаковки для пациента обычно содержат одну или несколько блистерных упаковок. Упаковки для пациента имеют преимущества по сравнению с традиционными препаратами по рецепту, где фармацевт выделяет запас лекарств для пациента из большой партии, так как пациент всегда имеет доступ к вложенной в упаковку инструкции по применению, которая обычно отсутствует в рецепте. Было продемонстрировано, что включение в пакет пациента вкладыша-инструкции по применению улучшает соблюдение пациентами предписаний лечащего врача.
Комбинации по изобретению могут оказывать более эффективное терапевтическое действие, по сравнению с терапевтическим эффектом индивидуальных соединений/средств при их введении по отдельности.
Используемый в настоящем документе термин «эффективное количество» или «терапевтически эффективное количество» соединения обозначает количество, которое может быть введено субъекту без излишней токсичности, раздражения, аллергической реакции или других проблем или осложнений, и соответствующее разумному соотношению полезного эффекта и риска, но достаточное при этом для обеспечения требуемого эффекта, например лечения или профилактики, проявляющихся в постоянном или временном улучшении состояния субъекта. Это количество варьируется от субъекта к субъекту в зависимости от возраста и общего состояния индивидуума, формы введения и других факторов. Таким образом, хотя невозможно наперед указать точное эффективное количество, специалисты в данной области могут определить соответствующее "эффективное" количество в каждом отдельно взятом случае с помощью рутинных исследований и имеющихся у них знаний. Терапевтический результат в данном контексте включает устранение или ослабление симптомов, уменьшение боли или дискомфорта, пролонгированное выживание, улучшение подвижности и другие маркеры клинического улучшения. Терапевтический результат не обязательно должен быть полным излечением.
Используемый в настоящем документе термин "профилактически эффективное количество" относится к количеству, эффективному при дозировке и в течение периодов времени, необходимых для достижения требуемого профилактического результата. Обычно, так как профилактическую дозу вводят субъектам до заболевания или на ранней стадии заболевания, профилактически эффективное количество меньше, чем терапевтически эффективное количество.
Термин "эффективный" включает такие преимущества и эффекты, как аддитивность, синергизм, ослабленное побочное действие, пониженную токсичность или улучшенные показатели или активность. Предпочтительно эффективное действие позволяет снизить дозы каждого или какого-либо из вводимых пациенту компонентов, и тем самым уменьшить токсичность при получении и/или сохранении того же терапевтического эффекта. Синергический эффект в настоящем контексте относится к терапевтическому эффекту, получаемому комбинацией компонентов, который оказывается больше суммы терапевтических эффектов компонентов комбинации, используемых по отдельности. Аддитивный эффект в настоящем контексте относится к терапевтическому эффекту, получаемому комбинацией, который больше терапевтического эффекта любого из компонентов комбинации, используемых по отдельности.
Термин "вспомогательные соединение" (или "вспомогательное средство"), используемый в настоящем документе, предназначен для обозначения любого соединения, которое дает эффективную комбинацию (как определено в настоящем документе) в сочетании с соединением по изобретению. Таким образом, вспомогательное соединение может действовать как дополнение к соединению по изобретению, или может иным образом вносить вклад в эффективность комбинации (например, давая синергический или аддитивный эффект или усиливая активность соединения по изобретению).
Термин "дополнительный", используемый при использовании соединений и комбинаций по изобретению в терапии или профилактике, обозначает виды применения, где вещества вводят вместе с одним или несколькими другими лекарствами, вмешательствами, схемами лечения или видами терапии (такими как хирургия и/или облучение). Таким образом, дополнительные виды терапии могут включать одновременное, раздельное или последовательное введение/нанесение веществ по изобретению и другие виды лечения. Так, в некоторых вариантах осуществления изобретения дополнительное применение веществ по изобретению отражено в составе фармацевтических композиций по изобретению. Например, дополнительное применение может отражаться в конкретной лекарственной форме или в препаратах, в которых соединение по изобретению находится в смеси с другим(и) лекарством(ами), с которыми оно используется дополнительно (или же физически связано с другими лекарственными средствами в единичной дозе). В других вариантах осуществления изобретения дополнительное применение соединений или композиций по изобретению может быть отражено в композициях, включаемых в фармацевтические наборы по изобретению, в которых соединение по изобретению упаковано вместе с другим(и) лекарством(ами) (например, как часть комплекта единичных доз), с которым его дополнительно используют. В других вариантах осуществления изобретения дополнительное применение соединения по изобретению может быть отражено в информации и/или инструкциях, упакованных вместе с соединением, и/или позологии.
Термин "фармацевтически приемлемое производное " применительно к соединению по изобретению обозначает соединения, которые получаются (или могут быть получены) химической дериватизацией исходных соединений по изобретению. Фармацевтически приемлемые производные, таким образом, подходят для введения в ткани млекопитающих или для применения в контакте с тканями млекопитающих без излишней токсичности, раздражения или аллергической реакции (т.е. сообразно разумному соотношению пользы и риска). Предпочтительными производными являются производные, полученные (или те, которые можно получить) алкилированием, этерификацией или ацилированием исходных соединений по изобретению. Производные могут быть активными в чистом виде или могут быть неактивными до тех пор, пока не подвергнутся обработке in vivo. В последнем случае производные по изобретению выступают в роли пролекарств. Особенно предпочтительными пролекарствами являются сложноэфирные производные, которые этерифицированы по одной или нескольким гидроксильным группам и которые активируются гидролизом in vivo. Другими предпочтительными пролекарствами являются ковалентно связанные соединения, которые высвобождают активное исходное лекарство общей формулы (I) после расщепления ковалентной связи или связей in vivo.
Фармацевтически приемлемые производные по изобретению сохраняют часть или всю активность исходного соединения. В некоторых случаях при дериватизации активность увеличивается. Получение производных может также дополнять активность соединения другими видами биологической активности, например биодоступностью.
Термин «фармацевтически приемлемая соль», применительно к соединениям по изобретению, обозначает любую нетоксичную аддитивную соль органической или неорганической кислоты и свободного основания соединения, которая подходит для применения в контакте с тканями млекопитающего, не вызывает избыточной токсичности, раздражения, аллергической реакции, и которая соответствует разумному соотношению пользы и риска. Подходящие фармацевтически приемлемые соли хорошо известны в данной области. Примерами являются соли неорганических кислот (например хлористоводородной, бромистоводородной, серной и фосфорной кислот), органических карбоновых кислот (например уксусной, пропионовой, гликолевой, молочной, пировиноградной, малоновой, янтарной, фумаровой, яблочной, винной, лимонной, аскорбиновой, малеиновой, гидроксималеиновой, дигидроксималеиновой, бензойной, фенилуксусной, 4-аминобензойной, 4-гидроксибензойной, о-аминобензойной, коричной, салициловой, 2-феноксибензойной, 2-ацетоксибензойной и миндальной кислоты) и органических сульфоновых кислот (например, метансульфоновой кислоты и n-толуолсульфоновой кислоты). Соединения по изобретению могут также быть превращены в соли реакцией с галогенидом щелочного металла, например хлоридом натрия, йодидом натрия или йодидом лития. Предпочтительно соединения по изобретению превращаются в соли реакцией со стехиометрическии количеством хлорида натрия в присутствии растворителя, такого как ацетон.
Указанные соли и свободные основания соединений могут существовать или в гидратированной, или в по существу безводной форме. Также предусмотрены кристаллические формы соединений по изобретению, и, как правило, аддитивные соли кислот и соединений по изобретению представляют собой кристаллические вещества, которые растворимы в воде и различных гидрофильных органических растворителях имеют более высокие температуры плавления и повышенную растворимость, по сравнению с теми же соединениями в форме свободных оснований.
Термин «фармацевтически приемлемый сольват», применяемый к соединениям по изобретению, обозначает любую фармацевтически приемлемую сольватную форму указанного соединения, которая сохраняет биологическую эффективность такого соединения. Примеры сольватов включают соединения по изобретению в комбинации с водой (гидраты), изопропанолом, этанолом, метанолом, диметилсульфоксидом, этилацетатом, уксусной кислотой, этаноламином или ацетоном. Кроме того, включены смешиваемые композиции смесей сольватов, такие как соединение по изобретению в сочетании со смесью ацетона и метанола. В предпочтительном варианте осуществления изобретения сольват включает соединение по изобретению в комбинации со смесью, содержащей около 20% этанола и около 80% ацетона. Таким образом, структурные формулы включают как гидратированную, так и негидратированную формы соединения, имеющего указанную структуру.
Термин «фармацевтически приемлемое пролекарство», применительно к соединениям по изобретению, обозначает любое фармацевтически приемлемое соединение, которое в физиологических условиях или в результате сольволиза может превращаться в указанное соединение, в фармацевтически приемлемую соль такого соединения или в соединение, которое обладает по меньшей мере частью антибактериальной активности указанного соединения (например, проявляет активность в отношении Clostridium difficile).
Термин «фармацевтически приемлемый метаболит», применительно к соединениям по изобретению, обозначает фармацевтически активный продукт, получающийся в результате метаболизма конкретного соединения или его соли в организме.
Пролекарства и активные метаболиты соединения по изобретению могут быть идентифицированы с помощью общепринятых методик, известных в данной области техники (см., например, Bertolini et al., J. Med. Chem., 1997, 40, 2011-2016).
Термином «фармацевтически приемлемый комплекс» применительно к соединениям по изобретению обозначают соединения или композиции, в которых соединение по изобретению образует часть компонента. Таким образом, комплексы по изобретению включают производные, в которых соединение по изобретению физически связано (например, ковалентным или нековалентным связыванием) с еще одним остатком или остатками. Таким образом, термин включает многомерные соединения по изобретению. Такие мультимеры могут генерироваться путем связывания или размещения нескольких копий (дубликатов) соединения по изобретению в непосредственной близости друг от друга (например, через мостик или остаток носителя).
Термин «биоизостера» (или просто изостера) представляет собой специальный термин, используемый в уровне техники для обозначения аналогов лекарства, в которых один или несколько атомов (или групп атомов) замещены атомами (или группами атомов), имеющими стерические и/или электронные характеристики, аналогичные характеристикам атомов, которые они замещают. Замещение атома водорода или гидроксильной группы атомом фтора представляет собой часто используемое биоизостерическое замещение. Сила-замещение (C/Si-обмен) представляет собой относительно недавний метод получения изостер. Такой подход включает замену одного или нескольких конкретных атомов углерода в соединении кремнием (для обзора см. Tacke и Zilch (1986) Endeavour, New Series 10:191-197). Сила-замещенные изостеры (изостеры с кремнием) могут проявлять улучшенные фармакологические свойства, например, они могут лучше переноситься пациентом, иметь более длительный период полувыведения или проявлять увеличенную активность (см., например, Englebienne (2005) Med. Chem., 1(3): 215-226). Аналогично замена атома одним из его изотопов, например, замена водорода дейтерием, может также приводить к улучшению фармакологических свойств, например к более длительному периоду полувыведения (см., например, Kushner et al. (1999) Can J Physiol Pharmacol. 77(2):79-88). В наиболее широком аспекте настоящее изобретение включает все биоизостеры (и, более конкретно, все биоизостеры с кремнием) соединений по изобретению.
В наиболее широком аспекте настоящее изобретение включает все оптические изомеры, рацемические формы и диастереоизомеры описанных здесь соединений. Специалисты в данной области техники хорошо понимают, что благодаря наличию асимметрических атомов углерода в соединениях по изобретению, эти соединения могут быть получены в оптически активных и рацемических формах. Если в соединении по настоящему изобретению имеется хиральный центр или другая форма изомерного центра, то подразумевается, что все формы такого изомера или таких изомеров, включая энантиомеры и диастереоизомеры, охватываются настоящим изобретением. Соединения по изобретению, содержащие хиральный центр (или несколько хиральных центров), могут использоваться в виде рацемической смеси, энантиомерно обогащенной смеси, или рацемическая смесь может быть разделена с помощью хорошо известных способов, и индивидуальные изомеры можно использовать по отдельности. Таким образом, ссылки на соединения по настоящему изобретению включают в себя продукты в виде смеси диастереоизомеров, индивидуальных диастереоизомеров, смеси энантиомеров, а также в виде индивидуальных энантиомеров.
Таким образом, настоящее изобретение включает все оптические изомеры и их рацемические формы соединений по изобретению, и, если не указано иное (например, путем использования структурных формул с обозначениями «пунктиром-клинышком), подразумевается, что представленные в настоящем документе соединения охватывают все возможные оптические изомеры соединений, которые подпадают под такое изображение. В случаях, когда стереохимическая форма соединения важна для фармацевтического использования, изобретение предполагает использование выделенного эутомера.
В настоящем описании термин "алкил" обозначает линейную или разветвленную насыщенную углеводородную цепь. Термин "C1-С6 алкил" относится к линейной или разветвленной насыщенной углеводородной цепи, содержащей от одного до шести атомов углерода. Примеры включают метил, этил, н-пропил, изопропил, трет-бутил, н-гексил. Термин "C1-C9 алкил" относится к линейной или разветвленной насыщенной углеводородной цепи, содержащей от одного до девяти атомов углерода. Термин "C1-C15 алкил" относится к линейной или разветвленной насыщенной углеводородной цепи, содержащей от одного до пятнадцати атомов углерода. Алкильные группы по изобретению могут необязательно быть замещены одним или несколькими атомами галогена.
Термин "C1-C4 алкил" имеет аналогичное значение, за исключением того, что содержит от одного до четырех атомов углерода.
Термин "С2-С6 алкенил" относится к линейной или разветвленной углеводородной цепи, содержащей от двух до шести атомов углерода и по меньшей мере одну углерод-углеродную двойную связь. Примеры включают этенил, 2-пропенил и 3-гексенил.
Термин "C1-С6 галогеналкил" относится к C1-С6 алкильной группе, определение которой дано выше, замещенной одним или несколькими атомами галогена.
В настоящем описании термин «алкенил» обозначает линейную или разветвленную углеводородную цепь, содержащую по меньшей мере одну углерод-углеродную двойную связь. Термин «C1-С6 алкенил» относится к линейной или разветвленной ненасыщенной углеводородной цепи, содержащей от одного до шести атомов углерода. Термин «C1-C9 алкенил» относится к линейной или разветвленной ненасыщенной углеводородной цепи, содержащей от одного до девяти атомов углерода. Термин «C1-C15 алкенил» относится к линейной или разветвленной ненасыщенной углеводородной цепи, содержащей от одного до пятнадцати атомов углерода. Предпочтительным является C1-С6 алкенил. Примеры включают этенил, 2-пропенил и 3-гексенил. Алкенильные группы по изобретению могут быть необязательно замещены одним или несколькими атомами галогена.
В настоящем описании термин «алкинил» обозначает линейную или разветвленную углеводородную цепь, содержащую по меньшей мере одну тройную связь углерод-углерод. Термин «C1-С6 алкинил» относится к линейной или разветвленной ненасыщенной углеводородной цепи, содержащей от одного до шести атомов углерода. Термин «C1-C9 алкинил» относится к линейной или разветвленной ненасыщенной углеводородной цепи, содержащей от одного до девяти атомов углерода. Термин «C1-C15 алкинил» относится к линейной или разветвленной ненасыщенной углеводородной цепи, содержащей от одного до пятнадцати атомов углерода. Предпочтительным является C1-С6 алкинил. Примеры включают этинил, 2-пропинил и 3-гексинил. Алкинильные группы по изобретению могут быть необязательно замещены одним или несколькими атомами галогена.
Термин «гетероциклил» обозначает насыщенную или частично насыщенную 3-14-членную кольцевую систему (кроме тех случаев, когда указаны другие количества кольцевых атомов), похожую на циклоалкил, но в которой по меньшей мере один из атомов углерода замещен N, О, S, SO или SO2. Примеры включают пиперидин, пиперазин, морфолин, тетрагидрофуран и пирролидин.
Используемый в настоящем документе термин "карбоциклил" обозначает моно- или полициклический остаток, содержащий 3 или больше (например 3-14, 3-10 или 3-8) атомов углерода. Карбоциклильные остатки по изобретению могут необязательно быть замещены одним или несколькими атомами галогена. Моно- и бициклические карбоциклильные остатки являются предпочтительными. Карбоциклильные остатки могут быть насыщенными или частично ненасыщенными и включают в том числе конденсированные бициклические или трициклические системы. Примеры таких групп включают циклопропил, циклобутил, циклопентил, циклогексил, циклогексенил и мостиковые системы, такие как норборнил и адамантил.
Предпочтительными являются насыщенные карбоциклильные остатки, которые в настоящем документе называются «циклоалкилами», а термин «циклоалкил» используют для обозначения насыщенного 3-14-членного карбоциклического кольца, включая конденсированные бициклические или трициклические системы. Примеры таких групп включают циклопропил, циклобутил, циклопентил, циклогексил и мостиковые системы, такие как норборнил и адамантил. Циклоалкильные остатки по изобретению могут быть необязательно замещены одним или несколькими атомами галогена.
В настоящем описании термин «арил» обозначает 5-14- (например 5-10) членную ароматическую моно-, би- или трициклическую группу, по меньшей мере одно кольцо которой является ароматическим. Так, бициклические арильные группы могут содержать только одно ароматическое кольцо. Примерами ароматических фрагментов являются бензол, нафталин, имидазол и пиридин. Термин также включает бициклические или трициклические системы, в которых одно или несколько колец является ароматическим. Индан представляет собой пример систем такого типа.
Используемый в настоящем документе термин «гетероарил» обозначает арильные фрагменты (согласно приведенному выше определению), которые содержат гетероатомы (например азот, серу и/или кислород). Термин также включает системы, в которых кольцо, имеющее ароматический характер, конденсировано с насыщенным или частично насыщенным кольцом. Примеры включают кольцевые системы пиридина, пиримидина, фурана, тиофена, индола, изоиндола, индолина, бензофурана, бензимидазола, бензимидазолина, хинолина, изохинолина, тетрагидроизохинолина, хиназолина, тиазола, бензтиазола, бензоксазола, индазола и имидазола. Если не указано иное, следует понимать, что термин «арил» включает гетероарильные группы, как они определены выше.
Арильные и гетероарильные группы по изобретению могут необязательно быть замещены одним или несколькими атомами галогена.
В настоящем описании термин «галоген» относится к фтору, хлору, брому или йоду. В общих формулах соединений по настоящему изобретению (и, в частности, в общей формуле (I), как описано ниже), порядок связей указанных колец может варьироваться, когда различные возможные гетероатомы подразумевают конкретные требования к порядку связей, чтобы соответствовать условию ароматичности, предотвращать антиароматичность и стабилизировать таутомерные формы, обусловленные локализацией. В таких случаях предполагается соответствующий порядок связей в кольцевых структурах в структурных формулах по настоящему изобретению.
Термин «симметричный» применительно к соединениям формулы (I) может обозначать соединения, в которых заместители R1 и R2 одинаковые.
Термин «несимметричный» применительно к соединениям формулы (I) может обозначать соединения, в которых заместители R1 и R2 разные.
(2) Соединения по изобретению
(2) Структуры
Особенно предпочтительные соединения общей формулы (I) перечислены в таблице 1 (приведена ниже):
Таблица 1
Название соединения
В каждом случае изобретение включает фармацевтически приемлемые соли, гидраты, сольваты, комплексы, биоизостеры, метаболиты или пролекарства каждого из перечисленных соединений.
Ссылки на конкретные номера соединений относятся к номерам в таблице 1. Некоторые из соединений общей формулы (I) являются новыми. Так, согласно изобретению, изобретение включает те соединения общей формулы (I), которые являются новыми, в качестве соединений как таковых, вместе со способами их получения, композициями, их содержащими, а также их применением в качестве фармацевтических препаратов.
Таким образом, изобретение включает соединение, выбранное из:
2-(2'-(пиридин-4-ил)-1Н,1'Н-5,5'-бибензо[d]имидазол-2-ил)тиено[2,3-b]пиридина,
2-(бензо[b]тиофен-2-ил)-2'-(пиридин-4-ил)-1Н,1'Н-5,5'-бибензо[d]имидазола,
2-(бензофуран-5-ил)-2'-(пиридин-4-ил)-1Н,1'Н-5,5'-бибензо[d]имидазола,
6-(2'-(пиридин-4-ил)-1Н,3'Н-5,5'-бибензо[(1]имидазол-2-ил)бензо[(1]имидазола,
2-(бензо[b]тиофен-5-ил)-2'-(пиридин-4-ил)-1Н,3'Н-5,5'-бибензо[(1]имидазола,
2-(1Н-индол-5-ил)-2'-(пиридин-4-ил)-1Н,3'Н-5,5'-бибензо[(1]имидазола,
2-(2,3-дигидробензофуран-5-ил)-2'-(пиридин-4-ил)-1Н,3'Н-5,5'-бибензо[d]имидазола,
2-(имидазо[1,2-а]пиридин-6-ил)-2'-(пиридин-4-ил)-1Н,1'Н-5,5'-бибензо[d]имидазола,
2-(бензо[d][1,3]диоксол-5-ил)-2'-(пиридин-4-ил)-1Н,1'Н-5,5'-бибензо[d]имидазола,
2-(бензофуран-2-ил)-2'-(пиридин-4-ил)-1Н,1'Н-5,5'-бибензо[d]имидазола,
2-(2'-(пиридин-4-ил)-1Н,1'Н-[5,5'-бибензо[d]имидазол]-2-ил)тиено[2,3-с]пиридина,
2-(имидазо[1,2-а]пиридин-6-ил)-2'-(пиридин-3-ил)-1Н,1'Н-5,5'-бибензо[d]имидазола,
2-(2'-(пиридин-3-ил)-1Н,1'Н-[5,5'-бибензо[а]имидазол]-2-ил)тиено[2,3-b]пиридина, или его фармацевтически приемлемые N-оксид, соль, гидрат, сольват, комплекс, биоизостеру, метаболит или пролекарство, а также композиции (например, фармацевтические композиции), содержащие указанные соединения.
(b) Функция
(i) Действие на штаммы Clostridium difficile и селективность в отношении штаммов Clostridium difficile
Предпочтительными соединениями по изобретению могут быть селективные в отношении Clostridium difficile агенты, как они определены выше в данном документе.
Особенно предпочтительные селективные в отношении Clostridium difficile агенты проявляют бактериостатическую и/или бактерицидную активность в отношении одного или нескольких штаммов С.difficile, но не проявляют бактериостатической и/или бактерицидной активности (MIC>64 мкг/мл) в отношении B.fragilis ATCC25285,
Еще более предпочтительные селективные в отношении Clostridium difficile агенты проявляют бактериостатическую и/или бактерицидную активность в отношении одного или нескольких штаммов С.difficile, но не проявляют бактериостатической и/или бактерицидной активности (MIC>64 мкг/мл) в отношении как Bacteroides fragilis ATCC25285, так и Escherichia coli ATCC25922.
Предпочтительные соединения по изобретению, которые представляют собой селективные в отношении Clostridium difficile агенты могут, таким образом, использоваться для лечения CDAD. При этом существующая кишечная флора не нарушается в сколько-нибудь в значительной с клинической точки зрения степени. Таким образом, такие соединения могут быть использованы в качестве антимикробных средств, которые не вызывают антибиотикоассоциированных заболеваний (как описано в настоящем документе) и/или распространения резистентных в отношении антибиотиков штаммов кишечных патогенов.
Соединения по изобретению, которые действуют как селективные в отношении Clostridium difficile агенты, могут быть идентифицированы посредством определения относительной антибактериальной активности соединения в отношении Clostridium difficile и одного или нескольких индикаторных организмов-представителей нормальной флоры кишечника. Подходящие для этой цели организмы-индикаторы включают: (а) Escherichia spp.(например Escherichia coli); (b) Bacteroides spp.(например В. fragilis); (с) Fusobacterium spp.; (d) Eubacterium spp.(e) Ruminococcus spp.; (f) Peptococcus spp.; (g) Peptostreptococcus spp.; (h) Bifidobacterium spp.; (i) Lactobacillus spp.; (j) Enterococcus spp.(например E. faecium); (k) виды клостридий, отличные от С.difficile (например С.perfringens); (I) Enterobacter spp.; (m) Serratia spp.; (n) Klebsiella spp.; (o) Proteus spp.; (p) Pseudomonas spp. и (q) Veillonella spp.
Альтернативно или дополнительно соединения по изобретению, действующие как селективные в отношении Clostridium difficile агенты, могут быть идентифицированы посредством количественной оценки посевов кала для серии образцов кала, полученных от субъектов, которым вводили дозы испытываемого соединения. In vitro вариант такого подхода основан на определении того, приводит ли испытываемое соединение к значительным изменениям флоры кишечника при инкубировании с разбавленными и отфильтрованными образцами фекалий in vitro. В таком случае изменения флоры можно обнаружить, определяя действие испытываемого соединения на относительное число бактерий - представителей двух или нескольких следующих видов: (a) Escherichia spp.(например Escherichia colt); (b) Bacteroides spp.(например В. fragilis); (с) Fusobacterium spp.; (d) Eubacterium spp.(e) Ruminococcus spp.; (f) Peptococcus spp.; (g) Peptostreptococcus spp.; (h) Bifidobacterium spp.; (i) Lactobacillus spp.; (j) Enterococcus spp.(например E. faecium); (k) видов клостридий, отличных от С.difficile (например, С.perfringens); (1) Enterobacter spp.; (m) Serratia spp.; (n) Klebsiella spp.; (o) Proteus spp.; (p) Pseudomonas spp. и (q) Veillonella spp.
Таким образом, предмет изобретения включает селективный в отношении Clostridium difficile агент, выбранный из:
2-(2'-(пиридин-4-ил)-1Н,1'Н-5,5'-бибензо[d]имидазол-2-ил)тиено[2,3-b]пиридина,
2-(бензо[b]тиофен-2-ил)-2'-(пиридин-4-ил)-1Н,1'Н-5,5'-бибензо[d]имидазола,
2-(бензофуран-5-ил)-2'-(пиридин-4-ил)-1H,1'Н-5,5'-бибензо[d]имидазола,
6-(2'-(пиридин-4-ил)-1Н,3'H-5,5'-бибензо[d]имидазол-2-ил)бензо [d]имидазола,
2-(бензо[b]тиофен-5-ил)-2'-(пиридин-4-ил)-1Н,3'Н-5,5'-бибензо[d]имидазола,
2-(1Н-индол-5-ил)-2'-(пиридин-4-ил)-1Н,3'Н-5,5'-бибензо[d]имидазола,
2-(2,3-дигидробензофуран-5-ил)-2'-(пиридин-4-ил)-1Н,3'Н-5,5'-бибензо[d]имидазола,
2-(имидазо[1,2-а]пиридин-6-ил)-2'-(пиридин-4-ил)-1Н,1'Н-5,5'-бибензо[d]имидазола,
2-(бензо[d][1,3]диоксол-5-ил)-2'-(пиридин-4-ил)-1Н,1'Н-5,5'-бибензо[d]имидазола,
2-(бензофуран-2-ил)-2'-(пиридин-4-ил)-1Н,1'Н-5,5'-бибензо[d]имидазола,
2-(2'-(пиридин-4-ил)-1Н,1'Н-[5,5'-бибензо[d]имидазол]-2-ил)тиено[2,3-с]пиридина,
2-(имидазо[1,2-а]пиридин-6-ил)-2'-(пиридин-3-ил)-1Н,1'Н-5,5'-бибензо[d]имидазола,
2-(24пиридин-3-ил)-1Н,1'Н-[5,5'-бибензо[d]имидазол]-2-ил)тиено[2,3-b]пиридина,
или его фармацевтически приемлемые N-оксид, соль, гидрат, сольват, комплекс, биоизостера, метаболит или пролекарство.
(ii) Действие на прорастание спор
Соединения по изобретению могут ингибировать или предотвращать прорастание спор.
Соединения, ингибирующие прорастание спор, могут быть идентифицированы in vitro путем определения изменений в преломляющей способности, теплостойкости и окрашивании эндоспор: прорастающие эндоспоры становятся темной фазой, чувствительной к теплу и окрашиваемой некоторыми красителями.
(iii) Действие на разрастание спор
Соединения по изобретению могут ингибировать или предотвращать разрастание спор.
Соединения, ингибирующие разрастание спор, могут быть идентифицированы с помощью исследований под микроскопом спор, in vitro подвергаемых воздействию веществ, вызывающих прорастание.
(iv) Бактерицидное и/или бактериостатическое действие
Соединения по изобретению могут быть бактерицидными и/или бактериостатическими средствами.
Предпочтительными являются бактерицидные соединения, как определено выше в данном документе. Такие бактерицидные соединения могут также быть бактериостатическими (например, в зависимости от бактерии-мишени и концентрации).
III. Применение в медицине
(a) Лечение инфекции С.difficile
Соединения по изобретению находят применение в лечении инфекции Clostridium difficile или заболеваний, связанных с Clostridium difficile.
Особенно предпочтительным является лечение заболеваний, связанных с Clostridium difficile (CDAD) Этот термин обозначает набор симптомов и заболеваний, связанных с инфекцией или интоксикацией С.difficile. CDAD включает диарею, вздутие живота, гриппоподобные симптомы, лихорадку, потерю аппетита, боль в животе, тошноту, обезвоживание и воспаление кишечника (колит). Наиболее серьезным проявлением CDAD является псевдомембранозный колит (РМС), который обнаруживается гистологически по колиту со слизистыми бляшками и клинически по тяжелой диарее, коликам в животе и общей токсичности.
Соединения по изобретению находят применение в лечении всех форм CDAD, включая диарею, вздутие живота, гриппоподобные симптомы, лихорадку, потерю аппетита, боль в животе, тошноту, обезвоживание, колит и псевдомембранозный колит.
Изобретение также находит применение в лечении интоксикации клостридиальными экзотоксинами, включающими продуцируемые бактерией Clostridium difficile токсин А (TcdA), токсин В (TcdB) и/или бинарный токсин CDT. Таким образом, соединения по изобретению находят применение в лечении заболеваний, вызванных (или усугубленных) присутствием продуцируемых Clostridium difficile токсина А (TcdA), токсина В (TcdB) и/или бинарного токсина CDT.
(b) Лечение антибиотикоассоциированных заболеваний
Термином «антибиотикоассоциированное заболевание» обозначают состояния, возникающие из-за изменений относительных количеств микроорганизмов, составляющих нормальную флору кишечника, вызванных (частичным) уничтожением флоры в результате введения антибиотиков. Такие заболевания возникают, когда введение антибиотиков (в частности, антибиотиков широкого спектра действия) делает возможным рост патогенных организмов (за счет чрезмерного роста из эндогенных популяций, обычно сдерживаемого нормальной кишечной флорой, или за счет образования колоний условно-патогенных микроорганизмов в местах, лишенных нормальной кишечной флоры действием антибиотиков).
Антибиотикоассоциированные заболевания обычно проявляются как диарея (и связанное с ней обезвоживание), колики в животе, тенезмы и лихорадка. Они также могут приводить к различным формам колита, включая псевдомембранозный колит (РМС). Таким образом, антибиотикоассоциированное заболевание включает антибиотикоассоциированную диарею (AAD) и антибиотикоассоциированный колит (ААС).
Антибиотикоассоциированное заболевание часто вызывается продуцирующими токсины штаммами Clostridium difficile, Staphylococcus aureus (включая метициллин-резистентный штамм S. aureus) и Clostridium perfringens. Бактерия Clostridium difficile является наиболее частой причиной нозокомиальных AAD и вызывает большинство случаев ААС.Бактерия размножается в толстой кишке пациентов, которые получали антибиотики широкого спектра действия или противораковую химиотерапию.
Таким образом, соединения по изобретению находят применение в лечении антибиотикоассоциированных заболеваний, включающих AAD и ААС. Особенно предпочтительными для такого применения являются селективные соединения по изобретению (как описано выше), так как такие соединения по существу не вредят нормальной кишечной флоре.
Соединения по изобретению находят применение в профилактике антибиотикоассоциированного заболевания, включающего AAD и ААС. При таком применении соединения по изобретению можно вводить совместно с другими антибиотиками или видами лечения, которые могут вызывать изменения относительных количеств микроорганизмов, составляющих нормальную флору кишечника.
Таким образом, соединения по изобретению могут быть использованы для лечения субъектов, которых лечили (или лечат) антибиотиками широкого спектра действия.
(с) Лечение колита, псевдомембранозного колита и диареи
Как указано выше, колит, псевдомембранозный колит (РМС) и диарея подразумевают присутствие бактерий, выбранных из Clostridium difficile, Staphylococcus aureus и Clostridium perfringens.
Соответственно, соединения по изобретению находят применение в лечении колита, псевдомембранозного колита(РМС) или диареи.
Особенно предпочтительным является лечение псевдомембранозного колита.
IV. Дополнительные вещества для применения в комбинациях по изобретению
(a) Общая информация
В дополнение к соединениям по изобретению, изобретение также предусматривает применение одного или нескольких следующих ниже дополнительных веществ в качестве дополнительных компонентов по изобретению.
Таким образом, изобретение относится к композициям, содержащим соединения по изобретению в комбинации с одним или несколькими веществами, выбранными из описанных ниже веществ.
(b) Антивирусные дополнительные средства
Комбинации предпочтительно дополнительно содержат один или несколько вспомогательных антивирусных средств. Такие вспомогательные антивирусные средства могут быть выбраны из одного или нескольких: (а) ингибиторов вирусных ферментов (например, выбранных из (i) ингибиторов протеаз, (ii) ингибиторов геликаз и (iii) ингибиторов полимераз); (b) нуклеозидных/нуклеотидных ингибиторов обратной транскриптазы; (с) ненуклеозидных ингибиторов обратной транскриптазы; (d) ингибиторов интегразы (е) ингибиторов созревания; (f) цитокинов или факторов, стимулирующих цитокины; (g) ингибиторов попадания вируса в клетку, например выбранных из: (i) ингибитора присоединения; (ii) ингибитора связывания с корецептором;
и (iii) ингибитора слияния мембран.
(c) Антибактериальные дополнительные средства
Соединения по изобретению можно использовать в комбинации с различивши антибактериальными средствами, включающими (но не ограниченными только перечисленным) один или несколько антибиотиков, выбранных из следующих:
- Аминогликозиды (например амикацин, гентамицин, канамицин, неомицин, нетилмицин, стрептомицин, тобрамицин и паромомицин).
- Ансамицины (например гелданамицин и гербимицин).
- Карбацефемы (например лоракарбеф).
- Карбапенемы (например эртапенем, дорипенем, имипенем/циластатин и меропенем).
- Цефалоспорины (первого поколения), включающие, например, цефадроксил, цефазолин, цефазолин, цефалотин/цефалосин и цефалексин.
- Цефалоспорины (второго поколения), включающие, например, цефаклор, цефамандол, цефокситин, цефпрозил и цефуроксим.
- Цефалоспорины (третьего поколения), включающие, например, цефиксим, цефдинир, цефдиторен, цефоперазон, цефотаксим, цефподоксим, цефтазидим, цефтибутен, цефтизоксим, цефтриаксон и цефдинир.
- Цефалоспорины (четвертого поколения), включающие, например, цефепим.
- Гликопептиды (например ванкомицин и тейкопланин).
- Макролиды (например азитромицин, кларитромицин, диритромицин, эритромицин, рокситромицин, тролеандомицин, телитромицин и спектиномицин).
- Монобактамы (например азтреонам).
- Пенициллины (например амоксициллин, ампициллин, азлоциллин, карбенциллин, клоксациллин, диклоксациллин, флюклоксациллин, мезлоциллин, нафциллин, пенициллин, пиперациллин и тикарциллин).
- Полипептиды (например бацитрацин, полимиксин В и колистин).
- Хинолоны (например ципрофлоксацин, эноксацин, гатифлоксацин, левофлоксацин, ломефлоксацин, моксифлоксацин, норфлоксацин, офлоксацин и тровафлоксацин).
- Сульфонамиды (например мафенид, пронтозил, сульфацетамид, сульфаметизол, сульфанилимид, сульфасалазин, сульфисоксазол, триметоприм, триметоприм-сульфаметоксазол (ко-тримоксазол, TMP-SMX)).
- Тетрациклины (например демеклоциклин, доксициклин, миноциклин, окситетрациклин и тетрациклин).
- Аминокумарины (например новобиоцин, альбамицин, кумермицин и хлоробиоцин).
- Оксазолидиноны (например линезолид и AZD2563).
- Липопептиды (например даптомицин).
- Стрептограмины (например хинупристин/дальфопристин).
- Глицилциклины (например тигециклин).
- Лантибиотики (например лантибиотики типа А (такие как низин, субтилин, эпидермин, мутацин II, мутации I & III) и лантибиотики типа В (такие как мерсацидин, актагардин и цинамицин).
Другие подходящие антибиотики, полезные в качестве дополнительных средств, включают один или несколько антибиотиков, выбранных из следующих: арсфенамина, хлорамфеникола, клиндамицина, линкоамицина, этамбутола, фосфомицина, фусидовой кислоты, фуразолидона, изониазида, линезолида, метронидазола, мупироцина, нитрофурантоина, платенцимицина, пиразинамида, квинупристина/дальфопристина, рифампина/рифампицина и тинизадола.
Таким образом, соединения по изобретению могут быть использованы в комбинации с одним или несколькими антибиотиками, выбранными из: пенициллина, клоксациллина, диклоксациллина, метициллина, нафциллина, оксациллина, ампициллина, амоксициллина, бакампициллина, капреомицина, циклосерина, азлоциллина, карбенициллина, мезлоциллина, пиперациллина, тикарциллина, азитромицина, кларитромицина, клиндамицина, эритромицина, линкомицина, демеклоциклина, доксицилина, этамбутола, этионамида, миноциклина, окситетрациклина, тетрациклина, квинолона, циноксацина, налидиксовой кислоты, фторхинолонов (например левофлоксацина, моксафлоксацина и гатифлоксацина, ципроклоксацина, эноксацина, грепафлоксацина), канамицина, левофлоксацина, ломефлокацина, норфлоксацина, офлоксацина, n-аминосалициловой кислоты, спарфлоксацина, трофлоксацина, бацитрацин, колистина, полимиксина В, сульфонамида, триметоприм-сульфаметоксазола, ко-амоксиклава, цефалотина, цефуроксима, цефтриаксона, ванкомицина, гентамицина, амикацина, метронидазола, хлорамфеникола, стрептомицина, нитрофурантоина, ко-тримоксазола, рифамицина и их производных (например рифампицина, рифабутина и рифапентина), изониазида, пиразинамида, кирромицина, тиострептона, микрококцина, фусидовой кислоты, тиолактомицина и фосмидомицина.
Другие подходящие антибактериальные дополнительные средства могут быть выбраны из средств, перечисленных в таблице, приведенной ниже:
(d) Противогрибковые дополнительные средства
Соединения по изобретению можно использовать в комбинации с различными противогрибковыми средствами (антимикотиками).
(e) Противопротозойные дополнительные средства
Соединения по изобретению можно использовать в комбинации с различными противопротозойными средствами, включающими хлорохин, доксициклин, мефлохин, метронидазол, эплорнитин, фуразолидон, гидроксихлорохин, йодохинол, пентамидин, мебендазол, пиперазин, галофантрин, примахин, пириметамин сульфадоксин, доксициклин, клиндамицин, хинина сульфат, хинидина глюконат, хинина дигидрохлорид, гидроксихлорохина сульфат, прогуанил, хинин, клиндамицин, атоваквон, азитромицин, сурамин, меларсопрол, эфлорнитин, нифуртимокс, амфотерицин В, натрия стибоглюконат, пентамидина изетионат, триметоприм-сульфаметоксазол, пириметамин и сульфадиазин, но не ограничены ими.
(f) Другие дополнительные средства
Соединения по изобретению можно вводить вместе с множеством других средств комбинированной терапии, которые лечат или предотвращают побочные эффекты, возникающие в результате лечения инфекций и/или представляющие собой последствия (осложнения) инфекции. Дополнительные средства такого типа могут иметь или не иметь противоинфекционную активность и включают, например, PPI и H2RA (как описано выше).
Так, соединения по изобретению могут дополнительно использоваться вместе с PPI, включающими омепразол (лосек, прилосек, зегерид), лансопразол (превацид, зотон, ингибитол), эзомепразол (нексиум), пантопразол (протоникс, сомак, пантолок, пантозол, зуркал, пан) и рабепразол (рабецид, асифекс, париет, рабелок), но не ограниченными ими.
Соединения по изобретению можно также дополнительно использовать вместе с антагонистами H2RA, включающими циметидин (тагамет), ранитидин (зинетак, зантак), фамотидин, (пепцидин, пепцид), роксатидин (роксит) и низатидин (тазак, аксид), но не ограниченньши ими.
Соединения по изобретению могут также дополнительно использоваться в тройной терапии ингибиторами протонной помпы (PPI) или антагонистами H2RA вместе с комбинацией двух антибиотиков (включающей антибиотики, выбранные из метронидазола, амоксициллина, левофлоксацина и кларитромицина, но не ограниченной ими).
В качестве дополнительных средств могут быть использованы различные пробиотики, включая, например, клетки Saccharomyces boulardii или Lactobacillus acidophilus. Пробиотики представляют собой монокультуры или смешанные культуры живых микроорганизмов, которые способствуют восстановлению естественной микрофлоры кишечника пациента, нарушенной антимикробным препаратом, индуцировавшим CDAD, или даже средством, используемым для лечения CDAD. Кроме того, такие микроорганизмы могут стимулировать иммунную систему пациента и вызывать продуцирование ферментов, разрушающих токсины, ассоциированные с С.difficile. Конкретными микроорганизмами, которые представляют интерес, являются Saccharomyces spp.("например Saccharomyces boulardii и Saccharomyces cerevisiae) и Lactobacillus spp. например Lactobacillus rhamnosus, Lactobacillus casei, Lactobaccillus acidophilus, Lactobacillus bulgaris и Lactobacillus plantarum), но они не ограничиваются перечисленным. Можно также рассмотреть любую другую традиционную пробиотическую композицию или микроорганизм, который является нормальным элементом желудочно-кишечного тракта человека.
Также в качестве дополнительных веществ могут использоваться пребиотики - средства, направленные на стимулирование роста кишечной флоры. Например, было показано, что применение олигофруктозы увеличивает содержание Bifidobacterium spp. и уменьшает частоту последующих рецидивов у пациентов. По этой причине введение любого антибактериального средства с узким спектром активности в отношении видов Clostridium в сочетании с терапией, направленной на восстановление нормальной популяции кишечных микроорганизмов, может давать значительные преимущества.
Другие подходы, направленные на восстановление нормальной кишечной флоры включают фекальную биотерапию и фекальные клизмы, приготовленные из стула здоровых индивидуумов, которые содержат нормальные микроорганизмы кишечника. Таким образом, с соединениями по изобретению также можно дополнительно использовать фекальную бактериотерапию.
Для того, чтобы блокировать действие токсинов, продуцируемых С.difficile, в качестве дополнительных средств можно применять абсорбенты, которые связывают и изолируют бактериотоксины различных типов. Ионообменные смолы, такие как секвестранты желчных кислот, холестирамин или колестипол, связываются с цитотоксинами С.difficile и таким образом приводят к уменьшению степени заражения кишечника токсинами. Однако ионообменные смолы, как известно, связываются и с лекарствами, такими как ванкомицин, и, следовательно, могут привести к недостаточности уровня антибактериального средства в месте инфекции. Другие абсорбенты, которые можно дополнительно использовать с соединениями по изобретению, включают полимеры, такие как Synsorb 90 и Tolevamer.
Хотя предполагается, что пробиотическая терапия улучшает ответ иммунной системы у пациентов с CDAD, для лечения таких пациентов, особенно в случаях рецидива, когда любое дальнейшее антимикробное лечение будет дополнительно усиливать нарушения кишечной флоры, можно применять также, например, внутривенное введение иммуноглобулина (J. Antimicrob. Chem., 2004, 53, 882-884). Таким образом, соединения по изобретению можно дополнительно использовать вместе с различными иммуноглобулинами.
Хотя в случае пациентов, страдающих CDAD, обычно избегают использования средств, направленных на ослабление диареи, в некоторых случаях можно предположить, что применение таких средств в сочетании с антибактериальными средствами может оказаться полезным, например, при попытках увеличить уровни антимикробного средства в месте инфекции и/или увеличить продолжительность контакта антибактериального средства с кишечным патогеном. Подобные средства могут включать в себя лоперамид (лопекс, имодиум, димор, пепто), дифеноксилат (ломотил, ко-фенотроп), дифеноксин (мотофен) и рацекадотрил, но не ограничиваются только ими. Таким образом, соединения по изобретению можно дополнительно применять вместе с различными антидиарейными средствами, включающими любые препараты из перечисленных выше.
Агенты комбинированной терапии, которые лечат или предотвращают любые из следующих побочных эффектов, можно применять как часть того же курса лечения, что и соединения по изобретению: (а) липодистрофия и вастинг-болезнь; (b) липоатрофия лица;
(с) гиперлипидемия; (d) утомление; (е) анемия; (f) периферическая невропатия; (g) тошнота; (h) диарея; (i) гепатотоксичность; (j) остеопения; (к) обезвоживание и (1) остеопороз.
Указанные лечение или профилактика могут включать введение такого соединения, как определенные выше, в качестве дополнительного средства к одному или нескольким следующим видам лечения или вмешательства:
(a) терапия рака;
(b) терапия СПИДа;
(c) вмешательство, подавляющее иммунитет;
(d) ведение пациента после графт/имплант-трансплантации;
(e) хирургия грибкового поражения ногтя или очищение раны;
(f) местная противогрибковая терапия (например, антимикотиком, выбранным из азолов, аллиламинов (например, тербинафина) или морфолина (например, аморолфина);
(g) системная противогрибковая терапия;
(h) антибактериальная терапия;
(i) противовирусная терапия;
(j) противовоспалительная терапия (например, стероидами);
(k) введение анальгетиков;
(l) введение противозудных средств;
(m) введение пробиотиков;
(n) фекальная бактериотерапия; или
(о) трансплантация кожи.
Таким образом, изобретение может включать лечение или профилактику группы пациентов, с которыми проводят (или провели) один или несколько видов лечения или вмешательства из списка (а) - (о).
(g) Дополнительные виды лечения
Лечение или профилактика могут включать введение такого соединения, как определено выше, в качестве дополнительного средства к одному или нескольким следующим видам лечения или вмешательства:
1. Терапия рака;
2. Виды вмешательства, подавляющие иммунитет;
3. Виды вмешательства, стимулирующие иммунитет;
4. Ведение пациента после графт/имплант-трансплантации;
5. Хирургия грибкового поражения ногтя или очищение раны;
6. Противовоспалительная терапия (например, стероидами);
7. Введение анальгетиков;
8. Введение противозудных средств;
9. Хирургия;
10. Абляция клеток или тканей;
11. Радиотерапия;
12. Криотерапия;
13. Терапия фекальной трансплантацией (фекальная бактериотерапия);
14. Терапия пробиотиками; или
15. Трансплантация кожи.
Таким образом, изобретение может включать лечение или профилактику группы пациентов, с которыми проводят (или провели) один или несколько видов лечения или вмешательства от (1) до (15).
(V) Позология
Соединения по настоящему изобретению можно вводить перорально или парентеральным путем, включая внутривенное, внутримышечное, внутрибрюшинное, подкожное, трансдермальное, аэрозольное (через дыхательные пути), ректальное, вагинальное и местное (включая буккальное и сублингвальное) введение.
Количество вводимого соединения может варьироваться в широких пределах в соответствии с конкретными используемыми единичными дозировками, продолжительностью лечения, возрастом и полом пациента, нуждающегося в лечении, природой и стадией заболевания и конкретным выбранным соединением.
Как правило, эффективное количество вводимого соединения находится в пределах от около 0,01 мг/кг до 10000 мг/кг в день. Стандартная единичная доза может содержать от 0,05 до 500 мг соединения, и ее можно принимать один или несколько раз в день. Соединение можно вводить с фармацевтическим носителем с использованием обычных стандартных лекарственных форм перорально, парентерально или местно, в соответствии с изложенным ниже.
Предпочтительным путем введения является пероральный. Обычно подходящая дозировка составляет от 0,01 до 500 мг на килограмм массы тела реципиента в день, предпочтительно от 0,1 до 1000 мг на килограмм массы тела в день, и наиболее предпочтительно от 1 до 5 мг на килограмм массы тела в день.
Желаемая доза предпочтительно имеет вид однократной дозы для ежедневного введения. Однако можно также использовать две, три, четыре, пять или шесть, или большее число частей дозы, вводимых через соответствующие интервалы времени в течение дня. Указанные части дозы могут вводиться в виде стандартных единичных дозировок, содержащих 0,001-100 мг, предпочтительно 0,01-10 мг, и наиболее предпочтительно 0,5-1,0 мг активного ингредиента на стандартную единичную дозировку.
При определении эффективного количества или дозы лечащий врач рассматривает ряд факторов, включающих (но не ограниченных только этим) активность и продолжительность действия используемых соединений, природу и тяжесть заболевания, подлежащего лечению, а также пол, возраст, массу тела, общее состояние здоровья и индивидуальную ответную реакцию пациента, нуждающегося в лечении, и другие относящиеся к данному случаю обстоятельства. Специалисты в данной области техники понимают, что дозировки можно также определять, используя руководство Goodman & Goldman, The Pharmacological Basis of Therapeutics, Ninth Edition (1996), Appendix II, pp.1707-1711.
Количество соединения, которое может быть скомбинировано с веществами-носителями для получения монолитной лекарственной формы, варьируется в зависимости от субъекта, нуждающегося в лечении, и конкретного способа введения. Например, препарат, предназначенный для перорального введения человеку может содержать от около 0,5 мг до около 7 г активного вещества, необязательно с соответствующим подходящим количеством вещества-носителя, которое может варьироваться от около 5 до около 95 процентов общей композиции. Стандартные единичные дозы соединения по изобретению обычно содержат от около 1 мг до около 500 мг активного ингредиента, например 5 мг, 10 мг, 20 мг, 25 мг, 50 мг, 100 мг, 200 мг, 300 мг, 400 мг, 500 мг, 600 мг, 800 мг или 1000 мг.
Эффективность конкретной дозировки соединения по изобретению можно определить путем мониторинга действия данной дозировки на прогрессирование заболевания или его профилактику.
(VI) Препараты
Соединение по изобретению может принимать любые формы. Оно может быть синтетическим, очищенным или выделенным из природных источников с помощью способов, описанных в данной области техники.
Типичные фармацевтически приемлемые соли получают из муравьиной, уксусной, пропионовой, янтарной, гликолевой, глюконовой, молочной, яблочной, винной, лимонной, аскорбиновой, глюкуроновой, малеиновой, фумаровой, пировиноградной, аспарагиновой, глутаминовой, бензойной, аминобензойной, метилсульфоновой, стеариновой, салициловой, и-гидроксибензойной, фенилуксусной, миндальной, эмбоновой (памоевой), метансульфоновой, этансульфоновой, бензолсульфоновой, пантотеновой, толуолсульфоновой, 2-гидроксиэтансульфоновой, сульфаниловой, циклогексиламиносульфоновой, альгиновой, (3-гидроксимасляной, галактаровой и галактуроновой кислот.
Подходящие фармацевтически приемлемые аддитивные соли включают соли ионов металлов и соли органических ионов. Соли ионов металлов включают (но не ограничены только перечисленным) соответствующие соли щелочных металлов (группа Iа), соли щелочноземельных металлов (группа IIа) и других физиологически приемлемых ионов металлов. Такие соли могут быть получены из ионов алюминия, кальция, лития, магния, калия, натрия и цинка. Органические соли могут быть получены из третичных аминов и четвертичных аммониевых солей, включающих в частности триметиламин, диэтиламин, N,N'-дибензилэтилендиамин, хлорпрокаин, холин, диэтаноламин, этилендиамин, меглюмин (N-метилглюкамин) и прокаин. Все вышеуказанные соли могут быть получены специалистами в данной области техники общепринятыми способами из соответствующих соединений.
Фармацевтические композиции могут включать стабилизаторы, антиоксиданты, красители и разбавители. Фармацевтически приемлемые носители и добавки выбирают таким образом, чтобы свести к минимуму побочные эффекты фармацевтического соединения и не изменить характеристики соединения в такой степени, чтобы лечение стало неэффективным.
Фармацевтические композиции можно вводить энтерально и/или парентерально. Пероральный (внутрижелудочный) путь представляет собой типичный путь введения. Фармацевтически приемлемые носители могут находиться в твердых лекарственных формах, включающих таблетки, капсулы, пилюли и гранулы, которые можно получать с нанесенными покрытиями и в оболочками, такими как энтеросолюбильные покрытия и другие, известные в данной области техники. Жидкие лекарственные формы для перорального введения включают фармацевтически приемлемые эмульсии, растворы, суспензии, сиропы и эликсиры.
Парентеральное введение включает подкожное, внутримышечное, интрадермальное, внутривенное и другие пути введения, известные в данной области техники. Формы для энтерального введения включают растворы, таблетки, капсулы с замедленным высвобождением, капсулы с энтеросолюбильным покрытием и сиропы.
При введении фармацевтическая композиция может иметь температуру тела или близкую к ней.
Композиции, предназначенные для перорального применения, могут быть получены по любому из способов, известных в данной области техники для изготовления фармацевтических композиций, и такие композиции могут содержать одно или несколько веществ, выбранных из группы, состоящей из подсластителей, веществ, придающих вкус и аромат, красящих веществ и консервантов, с целью получения приятных на вид и вкус фармацевтических препаратов. Таблетки содержат активный ингредиент в смеси с нетоксичными фармацевтически приемлемыми эксципиентами, которые подходят для изготовления таблеток. Указанные эксципиенты могут, например, представлять собой инертные разбавители, такие как карбонат кальция, карбонат натрия, лактоза, фосфат кальция или фосфат натрия, гранулирующие и разрыхляющие агенты, например кукурузный крахмал или альгиновая кислота, связующие агенты, например крахмал, желатин или камедь, и вещества, способствующие скольжению, например, стеарат магния, стеариновая кислота или тальк. Таблетки могут быть без оболочки или на них может быть известными способами нанесена оболочка, например, для того, чтобы замедлить их разрушение желудочно-кишечном тракте и тем самым обеспечить пролонгированное действие в течение длительного периода времени. Например, можно использовать вещества, обеспечивающие замедленное действие, такие как глицерилмоностеарат или глицерилдистеарат.
Препараты для перорального применения могут представлять собой твердые желатиновые капсулы, в которых активные ингредиенты смешаны с инертным твердым разбавителем, например карбонатом кальция, фосфатом кальция или каолином; или мягкие желатиновые капсулы, в которых активные ингредиенты находятся в чистом виде или в смеси с водой или масляной средой, например с арахисовым маслом, жидким парафином или оливковым маслом.
Можно получать водные суспензии, которые содержат активные вещества в смеси с эксципиентами, пригодными для получения водных суспензий. Такими эксципиентами являются суспендирующие агенты, например натрийкарбоксиметилцеллюлоза, метилцеллюлоза, гидроксипропилметилцеллюлоза, альгинат натрия, поливинилпирролидон, трагакантовая камедь и аравийская камедь; диспергирующие вещества или вещества, повышающие смачивание, могут представлять собой природные фосфатиды, например лецитин, или продукты конденсации алкиленоксида с жирными кислотами, например полиоксиэтиленстеарат или продукты конденсации этиленоксида с алифатическими спиртами с длинной цепью, например гептадекаэтиленоксицетанол, или продукты конденсации этиленоксида с неполными сложными эфирами - производными жирных кислот и гекситола, такие как, например, полиоксиэтиленсорбитанмоноолеат, или продукты конденсации этиленоксида с неполными сложными эфирами - производными жирных кислот и гекситолангидридов, например, полиоксиэтиленсорбитанмоноолеат.
Водные суспензии могут также содержать один или несколько консервантов, например, этил- или н-пропил-n-гидроксибензоат, одно или несколько красящих веществ, одно или несколько веществ, улучшающих вкус и аромат, и один или несколько подсластителей, таких как сахароза или сахарин.
Масляные суспензии могут быть изготовлены путем суспендирования активного ингредиента в омега-3 жирной кислоте, растительном масле, например, арахисовом масле, оливковом масле, кунжутном масле или кокосовом масле, или в минеральном масле, таком как парафиновое масло. Масляные суспензии могут содержать загуститель, например пчелиный воск, твердый парафин или цетиловый спирт.
Подсластители, такие как представленные выше, и вещества, улучшающие вкус и аромат, могут быть добавлены для получения приятного на вкус перорального препарата. Такие композиции можно хранить, добавляя антиоксидант, например аскорбиновую кислоту.
В диспергируемых порошках и гранулах, подходящих для изготовления водной суспензии путем добавления воды, активный ингредиент находится в смеси с диспергирующим веществом или веществом, повышающим смачивание, суспендирующим агентом и одним или несколькими консервантами. Примером подходящих диспергирующих или повышающих смачивание веществ и суспендирующих агентов могут служить вещества, уже указанные выше. Могут также использоваться дополнительные эксципиенты, например подсластители, вещества, улучшающие вкус и аромат, и красящие вещества.
Сиропы и эликсиры, содержащие соединение по изобретению, могут быть изготовлены с использованием подсластителей, например глицерина, сорбита или сахарозы. Такие препараты могут также содержать средства, уменьшающие раздражение, консерванты, вещества, улучшающие вкус и аромат, и красящие вещества.
Соединение по изобретению можно вводить парентерально, например подкожно, внутривенно или внутримышечно, или инфузионными способами в виде стерильных инъекционных водных или масляных суспензий. Такие суспензии могут быть изготовлены способами, известными специалистам в данной области, с использованием подходящих диспергирующих или улучшающих смачивание веществ и суспендирующих агентов, которые были упомянуты выше, в также других подходящих агентов. Стерильный инъекционный препарат может представлять собой стерильный инъекционный раствор или суспензию в нетоксичном, приемлемом для парентерального введения разбавителе или растворителе, например раствор в 1,3-бутандиоле. Среди приемлемых носителей и растворителей, которые могут быть использованы, можно перечислить воду, раствор Рингера и изотонический раствор хлорида натрия. Кроме того, в качестве растворителя или суспендирующей среды обычно используют стерильные нелетучие масла. Для этой цели можно использовать любое легкое нелетучее масло, в том числе синтетические моно- или диглицериды. Кроме того, для изготовления препаратов для инъекций применяют омега-3 полиненасыщенные жирные кислоты.
Введение лекарственных препаратов можно также осуществлять с помощью ингаляций, используя препараты в виде аэрозолей или растворов для небулайзеров, или ректально, используя препараты в виде суппозиториев, полученных смешиванием лекарственного средства с подходящим не вызывающим раздражения эксципиентом, который представляет собой твердое вещество при обычной температуре, но становится жидким при ректальной температуре и поэтому плавится в прямой кишке, высвобождая лекарство. Такими веществами являются масло какао и полиэтиленгликоли.
Настоящее изобретение также охватывает буккальное и сублингвальное введение, которые включают введение препаратов в виде леденцов, пастилок или жевательной резинки, содержащих описанные здесь соединения по изобретению. Соединения можно наносить на имеющую особый вкус основу, обычно сахарозу и акациевую камедь или трагакант.
Другие способы введения соединений по изобретению включают применение кожных пластырей, высвобождающих лекарственные препараты непосредственно на кожу и/или через кожу субъекта.
Системы для местного применения также охватываются настоящим изобретением и включают мази, порошки, спреи, кремы, желе, примочки, растворы или суспензии.
Композиции по настоящему изобретению можно дополнять вспомогательными веществами, такими как загустители, консерванты, сурфактанты и вещества, способствующие всасыванию. Загустители включают, например, поливиниловый спирт, поливинилпирролидон, метилцеллюлозу, гидроксипропилметилцеллюлозу, гидроксиэтилцеллюлозу, карбоксиметилцеллюлозу, гидроксипропилцеллюлозу или другие вещества, известные специалистам в данной области техники. Такие вещества обычно используют в количествах, составляющих от около 0,01% до около 2% (масс) массы фармацевтической композиции.
Консерванты необязательно используют для предотвращения роста микробов до или во время применения композиций. Подходящие консерванты включают поликватерниум-1, хлорид бензалкония, тимеросал, хлорбутанол, метилпарабен, пропилпарабен, фенилэтиловый спирт, динатриевую соль ЭДТУ, сорбиновую кислоту и другие вещества, известные специалистам в данной области техники. Обычно такие консерванты используют в количествах, составляющих от около 0,001% до около 1,0% (масс) массы фармацевтической композиции.
Растворимость компонентов композиций по настоящему изобретению может быть увеличена с помощью поверхностно-акитвных веществ (сурфактантов) или подходящим сорастворителем в композиции. Такие сорастворители включают полисорбаты 20, 60 и 80, сурфактанты на основе полиоксиэтилена/полиоксипропилена (например, Pluromc F-68, F-84 и Р-103), циклодекстрин или другие вещества, известные специалистам в данной области. Обычно такие сорастворители используют в количестве от около 0,01% до около 2% (масс) фармацевтической композиции.
Фармацевтически приемлемые эксципиенты и носители включают в себя все вышеупомянутые и им подобные. Приведенные выше соображения, касающиеся эффективных препаратов и методик введения, хорошо известны в данной области техники и описаны в обычных руководствах. См., например, Remington: The Science and Practice of Pharmacy, 20th Edition (Lippincott, Williams и Wilkins), 2000; Lieberman et al., ed., Pharmaceutical Dosage Forms, Marcel Decker, New York, N. Y. (1980) and Kihbe et al., ed.. Handbook of Pharmaceutical Excipients (3rd Edition), American Pharmaceutical Association, Washington (1999).
Таким образом, в тех вариантах осуществления изобретения, где из соединения по изобретению составляют композицию с фармацевтически приемлемым эксципиентом, может быть использован любой подходящий эксципиент, в том числе, например, инертные разбавители, разрыхлители, связующие агенты, вещества, способствующие скольжению, подсластители, вещества, придающие вкус и аромат, красящие вещества и консерванты. Подходящие инертные разбавители включают карбонаты натрия и кальция, фосфаты натрия и кальция и лактозу, а кукурузный крахмал и альгиновая кислота являются подходящими разрыхлителями. Связующие агенты могут включать крахмал и желатин, тогда как вещества, способствующие скольжению, если они присутствуют, обычно представляют собой стеарат магния, стеариновую кислоту или тальк. Фармацевтические композиции могут принимать любые подходящие формы, включая, например, такие, как таблетки, эликсиры, капсулы, растворы, суспензии, порошки, гранулы, лаки для ногтей, лаки и виниры, кожные пластыри и аэрозоли.
Фармацевтическая композиция может находиться в виде набора из нескольких составных частей, набор может содержать композицию по изобретению вместе с инструкциями по использованию и/или несколько различных компонентов в стандартной единичной дозе.
Для перорального введения соединение по изобретению может быть включено в состав твердых или жидких препаратов, таких как капсулы, пилюли, таблетки, лепешки, леденцы, расплавы, порошки, гранулы, растворы, суспензии, дисперсии и эмульсии (причем эти растворы, суспензии, дисперсии и эмульсии могут быть как водными, так и неводными). Твердые стандартные единичные дозы могут быть изготовлены в виде капсулы, которая обычно представляет собой капсулу с твердой или мягкой оболочкой желатинового типа, содержащую, например, поверхностно-активные вещества, вещества, способствующие скольжению, и инертные наполнители, такие как лактоза, сахароза, фосфат кальция и кукурузный крахмал. Таблетки для перорального применения могут включать соединение по изобретению, в чистом виде или с фармацевтически приемлемыми эксципиентами, такими как инертные разбавители, разрыхлители, связывающие вещества, вещества, способствующие скольжению, подсластители, вещества, придающие вкус и аромат, и консерванты. Подходящие инертные разбавители включают карбонаты натрия и кальция, фосфаты натрия и кальция и лактозу, при этом кукурузный крахмал и альгиновая кислота являются подходящими разрыхлителями. Связывающие вещества могут включать крахмал и желатин, тогда как вещества, способствующие скольжению, если они имеются, обычно представляют собой стеарат магния, стеариновую кислоту или тальк. Если требуется, на таблетки может быть нанесена оболочка из вещества, например, такого как глицерилмоностеарат или глицерилдистеарат, позволяющая замедлить абсорбцию в желудочно-кишечном тракте. Капсулы для перорального применения включают твердые желатиновые капсулы, в которых соединение по изобретению смешано с твердым разбавителем, и мягкие желатиновые капсулы, в которых активный ингредиент смешан с водой или маслом, таким как арахисовое масло, парафиновое масло или оливковое масло.
Препараты для ректального введения могут представлять собой суппозитории с подходящей основой, например кокосовым маслом или салицилатом. Препараты, подходящие для вагинального введения могут быть изготовлены в виде пессариев, тампонов, кремов, гелей, паст, пен или спреев, содержащих кроме активного ингредиента еще и подходящие носители, известные в данной области техники.
Для внутримышечного, внутрибрюшинного, подкожного и внутривенного применения соединения по изобретению, как правило, предоставляются в стерильных водных растворах или суспензиях, забуференных до соответствующего рН и изотоничности.
Подходящие водные носители включают раствор Рингера, изотонический раствор хлорида натрия. Водные суспензии по изобретению могут включать суспендирующие агенты, такие как производные целлюлозы, альгинат натрия, поливинилпирролидон и трагакантовую камедь и повышающее смачивание вещество, такое как лецитин. Подходящие консерванты для водных суспензий включают этил и н-пропил-n- гидроксибензоат.
Соединения по изобретению могут также быть представлены в виде композиций с липосомами.
В еще одном варианте осуществления изобретения соединения по изобретению формуют в таблетки, используя обычные основы для таблеток, такие как лактоза, сахароза и кукурузный крахмал, в комбинации со связующими веществами, такими как акациевая камедь, кукурузный крахмал или желатин; разрыхлителями, которые предназначены для того, чтобы способствовать разрушению и растворению таблетки после введения, такими как картофельный крахмал, альгиновая кислота, кукурузный крахмал и гуаровая камедь; веществами, способствующими скольжению, для улучшения текучести грану лята при таблетировании и для предотвращения прилипания таблетируемого вещества к поверхностям пресс-форм и пуансона, такими, например, как тальк, стеариновая кислота или стеараты магния, кальция или цинка; красителями, красящими веществами и веществами, придающими вкус и аромат, для улучшения эстетических качеств таблеток и для того, чтобы сделать таблетки более приятными для пациента.
Подходящие эксципиенты для применения в жидких лекарственных формах для перорального введения включают разбавители, такие как вода и спирты, например, этанол, бензиловый спирт и полиэтиленовые спирты, с добавлением фармацевтически приемлемого поверхностно-активного вещества, суспендирующего или эмульгирующего агента, или без него.
Соединения по изобретению можно также вводить парентерально, то есть подкожно, внутривенно, внутримышечно или внутрибрюшинно. В таких вариантах осуществления изобретения соединение используется в виде доз для инъекций в физиологически приемлемом разбавителе с фармацевтически приемлемым носителем (который может представлять собой стерильные жидкость или смесь жидкостей). Подходящие жидкости включают воду, физиологический раствор, водный раствор глюкозы и растворы родственных соединений, спирт (такой как этанол, изопропанол или гексадециловый спирт), гликоли (такие как пропиленгликоль или полиэтиленгликоль), кетали глицерина (такие как 2,2-диметил-1,3-диоксолан-4-метанол), простые эфиры (такие как поли(этиленгликоль)400), масло, жирную кислоту, сложный эфир или глицерид жирной кислоты или глицерид ацетилированной жирной кислоты с добавлением фармацевтически приемлемого поверхностно-активного вещества (такого как мыло или детергент), суспендирующего агента (такого как пектин, карбомеры, метилцеллюлоза, гидроксипропилметилцеллюлоза или карбоксиметилцеллюлоза) или эмульгирующего агента и других фармацевтически приемлемых вспомогательных веществ или без него.
Подходящие масла, которые можно использовать в композициях для парентерального введения по настоящему изобретению, представляют собой масла нефтяного, животного, растительного или синтетического происхождения, например арахисовое масло, соевое масло, кунжутное масло, хлопковое масло, кукурузное масло, оливковое масло, парафиновое масло и минеральное масло.
Подходящие жирные кислоты включают олеиновую кислоту, стеариновую кислоту и изостеариновую кислоту. Подходящими сложными эфирами жирных кислот являются, например, этилолеат и изопропилмиристат. Подходящие мыла включают соли щелочных металлов, аммония и триэтаноламина и жирных кислот, а подходящие детергенты включают катионогенные детергенты, например галогениды диметилдиалкиламмония, галогениды алкилпиридиния и ацетаты алкиламинов; анионогенные детергенты, например алкил-, арил- и олефин сульфонаты; алкил-, олефин, эфир и моноглицерид сульфаты и сульфосукцинаты; неионогенные детергенты, например оксиды жирных аминов, алканоламиды жирных кислот и сополимеры полиоксиэтиленполипропилена; и амфотерные детергенты, например, алкил-β-аминопропионаты и четвертичные аммониевые соли 2-алкилимидазолина, а также их смеси.
Композиции по настоящему изобретению для парентерального введения обычно содержат от около 0,5 до около 25% (масс) соединения по изобретению в растворе. Также могут использоваться консерванты и буферы. Для того, чтобы свести к минимуму или устранить раздражение в месте инъекции, такие композиции могут содержать неионогенный сурфактант, имеющий гидрофильно-липофильный баланс (HLB) от около 12 до около 17. Количество сурфактанта в таких композициях изменяется от около 5 до около 15% (масс). Сурфактант может представлять собой один компонент, имеющий вышеуказанный HLB, или может быть смесью двух или нескольких компонентов, имеющей нужный HLB. Типичными сурфактантами, используемыми в препаратах для парентерального введения являются представители класса сложных эфиров жирных кислот и полиэтиленсорбита, например монолаурат сорбита, и высокомолекулярные аддукты этиленоксида с гидрофобным основанием, образованные конденсацией пропиленоксида с пропиленгликолем.
Соединения по изобретению можно также вводить местно, и при таком введении носитель может соответственно содержать раствор, мазь или гелевую основу. Основа, например, может содержать одно или несколько из следующих веществ: вазелин ланолин, полиэтиленгликоли, пчелиный воск, минеральное масло, разбавители, такие как вода и спирт, и эмульгаторы и стабилизаторы. Препараты для местного введения могут содержать соединение по изобретению в концентрации от около 0,1 до около 10% масс/об, (масса на единицу объема).
При использовании в качестве дополнительного компонента, соединения по изобретению могут приготовлены для применения с одним или несколькими другими лекарственными средствами. В частности, соединения по изобретению можно применять в сочетании с анальгетиками, противовоспалительными средствами (например, стероидами), иммуномодуляторами и спазмолитиками.
Таким образом, дополнительное применение может быть отражено в конкретной лекарственной форме, разработанной для совместимости (или для получения синергического эффекта) с другим(и) лекарственным(и) средством(ами), или в препаратах, в которых соединение смешивают с одним или несколькими противовоспалительными средствами, цитокинами или иммуносупрессорами (или в которых оно физически связано с другим(и) лекарственным(и) средством(ами) в стандартной единичной дозе). Дополнительные виды применения могут также быть отражены в составе фармацевтических наборов по изобретению, в которых соединение по изобретению упаковано вместе (например, как часть комплекта единичных доз) с антимикробными и/или противовоспалительными средствами. Дополнительное применение может также быть описано в информации и/или инструкциях, относящихся к совместному введению соединения с антимикробными и/или противовоспалительными средствами.
(VII) Примеры
Ниже изобретение будет описано со ссылкой на конкретные примеры. Они играют исключительно иллюстративную роль: подразумевается, что примеры никаким образом не ограничивают объем запрошенных исключительных прав или объем описанного изобретения. Упомянутые примеры представляют собой наилучший известный в настоящее время вариант осуществления изобретения на практике.
ВЭЖХ-УФ-МС проводят на приборе «Gilson 321» с детектированием, осуществляемым с помощью детектора «Gilson 170 DAD», и на масс-спектрометре «Finnigan AQA» с электроспрей ионизацией. Используют ВЭЖХ колонку «Phenomenex Gemini С18» (150×4,6 мм) или «Phenomenex Gemini С18» 50 x 4,6 мм 3µ. Препаративную ВЭЖХ осуществляют на приборе «Gilson 321» с детектированием «Gilson 170 DAD». Фракции выделяют, используя коллектор фракций «Gilson 215». Используют Препаративную ВЭЖХ колонку «Phenomenex Gemini С18» (150×10 мм) и подвижную фазу ацетонитрил/вода.
1Н ЯМР спектры регистрируют на приборе фирмы «Bruker» с рабочей частотой 300 МГц. ЯМР спектры получают для растворов в CDCl3, CD3OD или ДМСО-d6 (указаны в ррм), используя в качестве стандартного эталона хлороформ (7,26 м.д.), метанол (3,35 м.д.) или ДМСО-d6 (2,50 м.д.). При описании мультиплетности пиков используют следующие сокращения: с (синглет), д (дублет), т (триплет), м (мультиплет), уш. (уширенный), дд (дублет дублетов), дт (дублет триплетов), тд (триплет дублетов), obsc. («размытый»), арр. (кажущийся). Константы взаимодействия приводятся в герцах (Гц).
Колоночную хроматографию осуществляют или флэш-хроматографией (силикагель, 40-65 мкм), или с помощью автоматизированной системы очистки (системы очистки SP1™ от Biotage® или системы CombiFlash Companion от ISCO). Реакции с использованием микроволнового излучения проводят в реакторе «Initiator 8™» (Biotage) или в системе «Explorer 48» (СЕМ).
Используются следующие сокращения: ДМСО (диметилсульфоксид), ДМФ (диметилформамид), IMS (промышленные денатурированные спирты), IPA (изопропиловый спирт), ТСХ (тонкослойная хроматография), Воc (трвт-бутилоксикарбонил), RT (время удерживания), DCM (дихлорметан), ТФУ (трифторуксусная кислота), ЖХ-МС (жидкостная хромато-масс-спектрометрия), ЯМР (ядерный магнитный резонанс), DME (1,2-диметоксиэтан).
MIC определяют методом микроразведения в жидкой питательной среде в соответствии с протоколами CLSI, описанными в Methods for Antimicrobial Susceptibility Testing of Anaerobic Bacteria; Approved Standard-Seventh Edition [Ml 1-A7, Vol.27, No2, Jan 2007] и Methods for Dilution Antimicrobial Susceptibility Tests for Bacteria That Grow Aerobically; Approved Standard- Seventh Edition [M7-A7, Vol.26, No2, Jan 2006].
Пример 1. Получение соединений общей формулы (I) Способ 1
4-(2-(Пиридин-4-ил)-1Н-бензо[(1]имидазол-5-ил)бензол-1,2-диамин (Промежуточное соединение А)
К перемешиваемому раствору 3,3'-диаминобензидина (3,857 г, 18 ммоль) и 4-пиридинкарбоксальдегида (1,41 мл, 15 ммоль) в IPA (22,5 мл) и H2O (7,5 мл) прибавляют метабисульфит натрия (2,852 г, 15 ммоль). Суспензию нагревают и кипятят в течение 16 часов. Полученную суспензию желтого цвета выливают в воду (200 мл) и осадок отфильтровывают. Желтое твердое вещество растирают в горячем метаноле и отфильтровывают, получая промежуточное соединение А в виде нерастворимого осадка (1,672 г, 5,5 ммоль, 37%).
ЖХ-МС: RT=1,05 мин, MH+ 302,1; 1Н ЯМР (d6-ДМСО): 13,17 (1Н, уш.с), 8,76 (2Н, д, J-6,0), 8,09 (2Н, д, J=6,0), 7,64 (2Н, уш.с), 7,42 (1Н, д, J=8,4), 6,91 (1Н, д, J=1,9), 6,77 (1Н, дд, 7=8,0 и 1,9), 6,60 (1Н, д, J=8,0) и 4,58 (4Н, уш.с).
4-(2-(пиридин-3-ил)-1Н-бензо[(1]имидазол-5-ил)бензол-1,2-диамин (Промежуточное соединение В)
К перемешиваемому раствору 3,3'-диаминобензидина (5,00 г, 23,36 ммоль) и 3-пиридинкарбоксальдегида (1,98 мл, 21,02 ммоль) в IPA (16 мл) и Н2О (16 мл) прибавляют метабисульфит натрия (4,44 г, 23,36 ммоль). Суспензию нагревают до 160°С в системе микроволнового излучения (СЕМ), затем охлаждают до комнатной температуры. Полученную суспензию желтого цвета выливают в воду (150 мл), осадок отфильтровывают и сушат. Твердое вещество очищают колоночной хроматографией на силикагеле, элюируя чистым EtOAc до 9:1 (EtOAc-MeOH), и получают промежуточное соединение В в виде желтого твердого вещества (3,92 г, 13,03 ммоль, 62%).
ЖХ-МС: RT=1,44 мин, МН+ 302,3; 1Н ЯМР (d6-ДМСО): 13,05 (1Н, уш.с), 9,37 (1Н, д, J=2,0), 8,69 (1Н, дд, J=4,7 и 1,5), 8,51 (1Н, дт, J=8,1 и 1,9), 7,70-7,58 (3Н, м), 7,41 (1Н, дд, J=8,5 и 1,5), 6,93 (1Н, д, У- 2,0), 6,79 (1Н, дд, J=8,0 и 2,0), 6,62 (1Н, д, J=8,0) и 4,58 (4Н, уш.с).
2-(2'-(пиридин-4-ил)-1Н,1'Н-5,5'-бибензо[(1]имидазол-2-ил)тиено[2,3-b]пиридин (Соединение 1)
Смесь 4-(2-(пиридин-4-ил)-1Н-бензо[d]имидазол-5-ил)бензол-1,2-диамина (промежуточного соединения А) (50 мг, 0,17 ммоль), тиено[2,3-b]пиридин-2-карбальдегида (33 мг, 0,20 ммоль) и Na2S2O5 (38 мг, 0,20 ммоль) в IPA-H2O (3:1, 8 мл) нагревают при микроволновом излучении при 170°С в течение 10 мин. Смесь абсорбируют на силикагеле, очищают колоночной хроматографией, элюируют (от 95:5 EtOAc-MeOH до 85:15 EtOAc-MeOH) и получают соединение, указанное в заголовке в виде желтого твердого вещества (30 мг, 0,07 ммоль, 40%).
ЖХ-МС: RT=1,38 мин, MH+ 445,1; 1H ЯМР (MeOD): 8,74 (2Н, дд, J=4,7 и 1,6), 8,58 (1Н, дд, J=4,7 и 1,6), 8,31 (1Н, дд, J=8,1 и 1,6), 8,10 (2Н, дд, J=4,7 и 1,6), 7,78 (1Н, с), 7,90-7,62 (6Н, м) и 7,48 (1Н, дд, J=8,1 и 4,7).
Следующие ниже соединения получают аналогично, используя соответствующие промежуточные соединения, и очищают кристаллизацией или колоночной хроматографией в случаях, когда это необходимо:
2-(Бензо[b]тиофен-2-ил)-2'-(пиридин-4-ил)-1Н,1'Н-5,5'-бибензо[а]имидазол (Соединение 2)
ЖХ-МС: RT=1,51 мин, MH+ 444,2; 1Н ЯМР (MeOD): 8,64 (2Н, м), 8,01 (2Н, м), 7,93 (1Н, м), 7,79-7,89 (3Н, м), 7,51-7,78 (5Н, м), 7,34 (2Н, м).
2-(Бензофуран-5-ил)-2'-(пиридин-4-ил)-1Н,1'Н-5,5'-бибензо[(1]имидазол (Соединение 3)
ЖХ-МС: RT=1,23 мин, MH+ 428,1; 1H ЯМР (MeOD): 8,76 (2H, дд, J=4,7 и 1,6), 8,40 (1Н, д, J=1,6), 8,15-8,08 (3Н, м), 8,00-7,60 (8Н, м) и 7,02 (1Н, дд, J=2,2 и 0,9).
6-(2'-(пиридин-4-ил)-1Н,3'Н-5,5'-бибензо[(1]имидазол-2-ил)бензо[(1]имидазол
(Соединение 4)
ЖХ-МС: RT=1,09 мин, MH+ 428,5; 1H ЯМР (MeOD): 8,75 (2H, дд, J=4,6 и 1,7), 8,42 (1Н, уш.с), 8,32 (1Н, с), 8,12 (2H, дд, 7=4,6 и 1,7), 8,07-7,71 (7Н, м) и 7,62 (1Н, дд, J=8,4 и 1,7).
2-(бензо[b]тиофен-5-ил)-2'-(пиридин-4-ил)-1Н,3'Н-5,5'-бибензо[(1]имидазол
(Соединение 5)
ЖХ-МС: RT=1.26 мин, MH+ 444,2; 1H ЯМР (MeOD): 8,65 (2H, дд, J=4,6 и 1,7), 8,49 (1Н, т, J=1,1), 8,01-7,99 (4H, м), 7,78-7,51 (7Н, м) и 7,43 (1Н, д, J=5,5).
2-(1Н-индол-5-ил)-2'-(пиридин-4-ил)-1Н,3'Н-5,5'-бибензо[(1]имидазол (Соединение 6)
ЖХ-МС: RT=1,16 мин, МН+ 427,3; 1H ЯМР (MeOD): 8,64 (2H, дд, J=4,6 и 1,7), 8,25 (1Н, д, J=1,1), 8,01 (2H, дд, J=4,6 и 1,7), 7,83-7,43 (6Н, м), 7,50-7,43 (2 Н, м) 7,25 (1Н, д, J=3,2) и 6,51 (1Н, дд, J=3,2 и 0,8).
2-(2,3-Дигидробензофуран-5-ил)-2'-(пиридин-4-ил)-1Н,3'Н-5,5'-бибензо[d]имидазол (Соединение 7)
ЖХ-МС: RT=1,21 мин, МН+ 430,1; 1H ЯМР (d6-ДМСО): 8,76 (2H, дд, J=4,6 и 1,6), 8,09 (2H, дд, J=4,6 и 1,6), 8,03 (1Н, с), 7,92 (2H, дд, J=8,2 и 1,8), 7,84-7,52 (5Н, м), 6,93 (1Н, д, J=8,3), 4,62 (2H, т, J=8,7) и 3,28 (2H, m, J=8,8).
2-(Имидазо[1,2-а]пиридин-6-ил)-2'-(пиридин-4-ил)-1Н,1'Н-5,5'-бибензо[(1]имидазол (Соединение 8)
ЖХ-МС: RT=1,11 мин, МН+ 428,1; 1H ЯМР (MeOD): 9,18 (1Н, с), 8,76 (2H, дд,7=4,6 и 1,6), 8,12 (2H, дд, J=4,6 и 1,6), 8,04 (1Н, с), 8,00 (1Н, дд, J=9,4 и 1,7) и 7,95-7,64 (8Н, м).
2-(Бензо[(1][1,3]диок:сол-5-ил)-2'-(пиридин-4-ил)-1Н,1'Н-5,5'-бибензо[(1]имидазол (Соединение 9)
ЖХ-МС: RT=1,23 мин, MH+ 431,8; 1H ЯМР (MeOD): 8,76 (2H, дд, J=4,7 и 1,6), 8,13 (2H, дд, J=4,6 и 1,6), 7,93-7,61 (8Н, м), 7,02 (1Н, д, J=8,1) и 6,09 (2H, с).
2-(Бензофуран-2-ил)-2'-(пиридин-4-ил)-1Н,1'Н-5,5'-бибензо[(1]имидазол (Соединение 10)
ЖХ-МС: RT=1,48 мин, MH+ 428,5; 1H ЯМР (MeOD): 8,64 (2H, дд, J=4,6 и 1,7), 8,00 (2H, дд, 7=4,6 и 1,7) и 7,79 (2H, м), 7,65-7,52 (6Н, м), 7,49 (1Н, д, J=0,9) 7,33 (1Н, дт, J=7,3 и 1,3), 7,23 (1Н, дт, J=7,5 и 1,0).
2-(2'-(Пиридин-4-ил)-1Н,1'Н-[5,5'-бибензо[(1]имидазол]-2-ил)тиено[2,3-с]пиридин
(Соединение 11)
ЖХ-МС: RT=1,36 мин, MH+ 445,2; 1H ЯМР (MeOD): 9,14 (1Н, с), 8,70 (2Н, д, J=5,4), 8,41 (1Н, д, J=5,5), 8,05 (2Н, д, J=5,5), 7,98 (1Н, с) и 7,91-7,55 (7 Н, м) 2-(Имидазо[1,2-а]пиридин-6-ил)-2'-(пиридин-3-ил)-1Н,1'Н-5,5'-бибензо[(1]имидазол
(Соединение 12)
ЖХ-МС: RT=1,80 мин, MH+ 428,7; 1H ЯМР (d6-ДМСО): 13,26 (2Н, уш.с), 9,52 (1Н, с), 9,45 (1Н, д, J=2,0), 8,76 (1Н, дд, J=4,8 и 1,5), 8,60 (1 Н, дт, J=8,0 и 1,8), 8,20 (1Н, с), 8,07 (1 Н, дд, J=9,4 и 1,7), 7,95 (2Н, д, J=7,0), 7,85-7,73 (4H, м) и 7,70-7,63 (3Н, м). 2-(2'-(Пиридин-3-ил)-1Н,1'Н-[5,5'-бибензо[(1]имидазол]-2-ил)тиено[2,3-b]пиридин
(Соединение 13)
ЖХ-МС: RT=2,33 мин, МН+ 446,1; 1H ЯМР (d6-ДМСО); 13,33 (2Н, уш.с), 9,39 (1Н, д, J=2,2), 8,70 (1Н, дд, J=4,8 и 1,6), 8,63 (1Н, дд, J=4,6 и 3,0), 8,54 (1Н, дт, J=8,0 и 2,0), 8,41 (1Н, дд, J=8,0 и 1,6), 8,17 (1Н, с), 8,07-7,69 (4H, м), 7,69-7,58 (3Н, м) и 7,52 (1Н, дд, J=8,0 и 4,6).
Пример 2. Активность соединений по изобретению
Список предпочтительных соединений общей формулы (I) вместе с их минимальной ингибирующей концентрацией (MIC) в отношении Clostridium difficile АТСС700057 и панелью индикаторных бактерий флоры кишечника суммированы в таблице 2 (ниже).
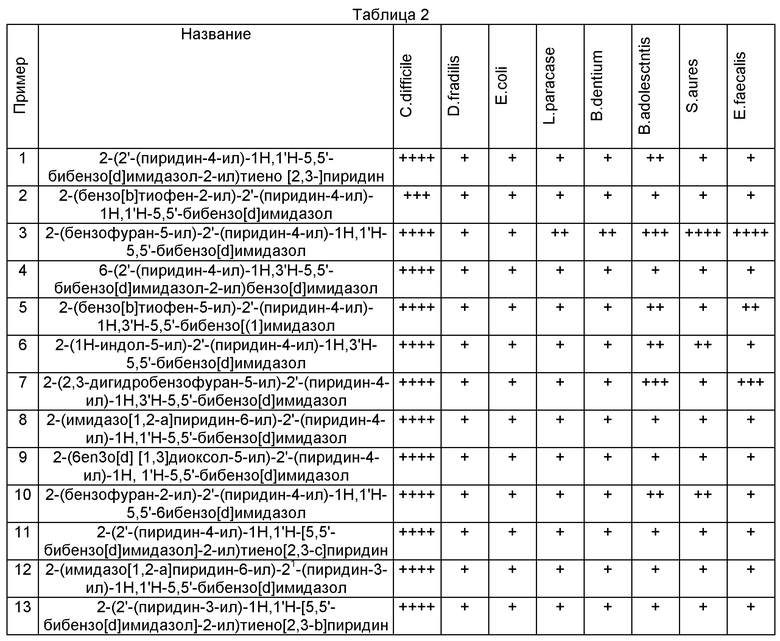
В представленной выше таблице для указания значений MIC используются следующие обозначения:
MIC≤1 мкг/мл=++++
МIС≤4 мкг/мл=+++
MIC≤32 мкг/мл=++
MIC≥64 мкг/мл=+
Использовали следующие штаммы бактерий:
Bacteroides fragilis ATCC 25285
Escherichia coli ATCC25922
Lactobacillus paracasei Zl 83
Bifidobacterium dentium NCTC 11816
В. adolescentis MWR144
Staphylococcus aureus ATCC29213
Enterococcus faecalis ATCC29212.
Индикаторными штаммами являются представители нормальной флоры кишечника, и, следовательно, они являются моделью микробной флоры кишечника. Таким образом, полученные данные показывают, что соединения по изобретению являются селективными средствами в отношении Clostridium difficile (как определено выше), т.е. проявляют бактериостатическую и/или бактерицидную активность в отношении С.difficile, но не вредят нормальной флоре кишечника. Следовательно, соединения по изобретению полезны в лечении CDAD, не вызывая при этом патологического нарушения нормальной флоры кишечника.
(VIII) Эквиваленты
В вышеприведенном описании подробно изложены предпочтительные в настоящее время варианты осуществления настоящего изобретения. При рассмотрении этого описания специалисты в данной области могут представить себе множество всевозможных вариантов и изменений, возможных при его осуществлении. Подразумевается, что такие изменения и варианты охватываются прилагаемой формулой изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИБАКТЕРИАЛЬНЫЕ СОЕДИНЕНИЯ | 2009 |
|
RU2525915C2 |
| ПРОИЗВОДНЫЕ 5-ГИДРОКСИМЕТИЛОКСАЗОЛИДИН-2-ОНА ДЛЯ ЛЕЧЕНИЯ БАКТЕРИАЛЬНЫХ КИШЕЧНЫХ ЗАБОЛЕВАНИЙ | 2009 |
|
RU2527769C2 |
| АНИОННЫЕ ПОЛИМЕРЫ В КАЧЕСТВЕ ВЕЩЕСТВ ДЛЯ СВЯЗЫВАНИЯ ТОКСИНОВ И АНТИБАКТЕРИАЛЬНЫХ СРЕДСТВ | 2000 |
|
RU2246938C2 |
| АНТИТЕЛА ДЛЯ ЛЕЧЕНИЯ АССОЦИИРОВАННЫХ С CLOSTRIDIUM DIFFICILE ИНФЕКЦИИ И ЗАБОЛЕВАНИЙ | 2011 |
|
RU2630663C9 |
| НОВЫЕ ПРОТИВОБАКТЕРИАЛЬНЫЕ СРЕДСТВА ДЛЯ ЛЕЧЕНИЯ ГРАМПОЛОЖИТЕЛЬНЫХ ИНФЕКЦИЙ | 2009 |
|
RU2512396C2 |
| МАКРОЦИКЛИЧЕСКИЕ ПОЛИМОРФЫ, КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ТАКИЕ ПОЛИМОРФЫ, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ И ПОЛУЧЕНИЯ | 2008 |
|
RU2478643C2 |
| ИММУНОГЕННАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ИЛИ ПРОФИЛАКТИКИ CLOSTRIDIUM DIFFICILE, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И СПОСОБ ИНДУКЦИИ ИММУННОГО ОТВЕТА К C. DIFFICILE | 2008 |
|
RU2550271C2 |
| ЭКСТРАКТЫ KIBDELOS PORANGIUM В КАЧЕСТВЕ АНТИБАКТЕРИАЛЬНЫХ СРЕДСТВ | 2010 |
|
RU2572621C2 |
| Способ лечения инфекционных заболеваний с использованием композиции, включающей полученный из плазмы иммуноглобулин М (IgM) | 2016 |
|
RU2731108C2 |
| ЛЕЧЕНИЕ БАКТЕРИАЛЬНЫХ ИНФЕКЦИЙ | 2005 |
|
RU2377251C2 |
Изобретение относится к области органической химии, а именно к производному бибензоимидазола общей формулы (I), где R1 является пиридилом; R2 представляет собой ароматическую 9-членную бициклическую кольцевую систему, в которой один или два атома углерода могут быть замещены N, О, или S; или к его фармацевтически приемлемой соли, гидрату или сольвату. Также изобретение относится к комбинации на основе соединения формулы (I) и дополнительного указанного средства, фармацевтической композиции на основе соединения формулы (I), способу лечения инфекции Clostridium difficile и способу уничтожения бактерии Clostridium difficile. Технический результат: получены новые производные бибензоимидазола, обладающие полезными биологическими свойствами. 5 н. и 9 з.п. ф-лы, 2 табл., 2 пр.
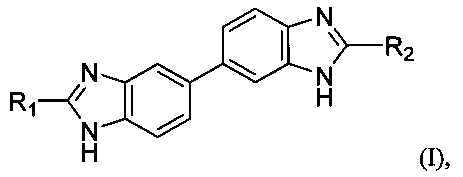
1. Соединение формулы (I)

в которой R1 является пиридилом;
R2 представляет собой ароматическую 9-членную бициклическую кольцевую систему, в которой один или два атома углерода могут быть замещены N, О, или S;
или его фармацевтически приемлемые соль, гидрат или сольват.
2. Соединение по п.1, в котором R2 представляет собой ароматическую конденсированную 5- и 6-членную бициклическую кольцевую систему.
3. Соединение по п.2, в котором R2 представляет собой (а) тиенопиридинильную группу или (b) бензотиофенильную группу, или (с) бензофуранильную группу, или (d) пиридилимидазолильную группу, или (е) бензодиоксолильную группу, или (f) индолильную группу.
4. Соединение по п.1, которое выбрано из следующих соединений:
2-(2′-(пиридин-4-ил)-1Н,1′Н-5,5′-бибензо[d]имидазол-2-ил)тиено[2,3-b]пиридин,
2-(бензо[b]тиофен-2-ил)-2′-(пиридин-4-ил)-1Н,1′Н-5,5′-бибензо[d]имидазол,
2-(бензофуран-5-ил)-2′-(пиридин-4-ил)-1Н,1′Н-5,5′-бибензо[d]имидазол,
6-(2′-(пиридин-4-ил)-1Н,3′Н-5,5′-бибензо[d]имидазол-2-ил)бензо[d]имидазол,
2-(бензо[b]тиофен-5-ил)-2′-(пиридин-4-ил)-1Н,3′Н-5,5′-бибензо[d]имидазол,
2-(1H-индол-5-ил)-2′-(пиридин-4-ил)-1Н,3′Н-5,5-бибензо[d]имидазол,
2-(2,3-дигидробензофуран-5-ил)-2′-(пиридин-4-ил)-1Н,3′Н-5,5′-бибензо[d]имидазол,
2-(имидазо[1,2-а]пиридин-6-ил)-2′-(пиридин-4-ил)-1Н,1′Н-5,5′-бибензо[d]имидазол,
2-(бензо[d][1,3]диоксол-5-ил)-2′-(пиридин-4-ил)-1Н,1′Н-5,5′-бибензо[d]имидазол,
2-(бензофуран-2-ил)-2′-(пиридин-4-ил)-1Н,1′Н-5,5′-бибензо[d]имидазол,
2-(2′-(пиридин-4-ил)-1Н,1′Н-[5,5′-бибензо[d]имидазол]-2-ил)тиено[2,3-с]пиридин,
2-(имидазо[1,2-а]пиридин-6-ил)-2′-(пиридин-3-ил)-1Н,1′Н-5,5′-бибензо[d]имидазол, и
2-(2′-(пиридин-3-ил)-1Н,1′Н-[5,5′-бибензо[d]имидазол]-2-ил)тиено[2,3-b]пиридин
или их фармацевтически приемлемых солей, гидратов или сольватов.
5. Комбинация, предназначенная для лечения заболеваний, связанных с Clostridium difficile (CDAD), включающая эффективное количество соединения по любому из предшествующих пунктов и дополнительное средство, выбранное из (а) ванкомицина, (b) метронидазола, (с) пробиотика, (d) пребиотика, (е) секвестранта бактериотоксина (например ионообменной смолы), (f) внутривенного иммуноглобулина и (g) антидиарейного средства.
6. Комбинация по п.5, содержащая соединение по любому из пп. 1-4 и пробиотик, выбранный из Saccharomyces spp. и/или Lactobacillus spp.
7. Комбинация по любому из пп.5-6, в которой соединение и дополнительное средство физически или нефизически ассоциированы друг с другом.
8. Фармацевтическая композиция, предназначенная для лечения заболеваний, связанных с Clostridium difficile (CDAD), содержащая эффективное количество соединения по любому из пп.1-4 или комбинацию по любому из пп.5-7.
9. Соединение по любому пп.1-4 для применения в способе лечения заболеваний, связанных с Clostridium difficile (CDAD).
10. Способ лечения инфекции Clostridium difficile или заболевания, связанного с Clostridium difficile, у субъекта, включающий введение упомянутому субъекту эффективного количества соединения по любому из пп.1-4, комбинации по любому из пп.5-7 или фармацевтической композиции по п. 8.
11. Соединение по п.9 или способ по п.10 для применения в способе лечения CDAD с сохранением нормальной флоры кишечника.
12. Соединение или способ по пп.9-11, где CDAD выбрано из (а) колита, (b) псевдомембранозного колита, (с) диареи и (d) антибиотикоассоциированного заболевания.
13. Соединение по п.12, где антибиотикоассоциированное заболевание выбрано из (а) антибиотикоассоциированной диареи и (b) антибиотикоассоциированного колита, для применения в лечении подгруппы пациентов, выбранных из (а) субъектов, которых лечили или лечат ингибиторами протонной помпы, (b) субъектов, которых лечили или лечат антагонистами Н2 рецепторов, (с) субъектов, которых лечили или лечат диуретиками, (d) госпитализированных субъектов, (е) субъектов с постоянным зондовым питанием, (f) субъектов, подвергаемых искусственной вентиляции легких, (g) субъектов, которых лечили или лечат пробиотиками и (g) субъектов, которых лечили или лечат ванкомицином и/или метронидазолом.
14. Способ уничтожения бактерии Clostridium difficile или ингибирования, уменьшения или предотвращения ее роста, включающий введение указанной бактерии в контакт с соединением по любому из пп.1-4.
| Jun Yin et al: "Efficient Synthesis and Characterization of Novel Bibenzimidazole Oligomers and Polymers as Potential Conjugated Chelating Ligands", J | |||
| Org | |||
| Chem., 2005, 70 (23), pp | |||
| Приспособление для снятия и насадки сцепных скоб нормальных винтовых стяжек | 1927 |
|
SU9436A1 |
| Распылительная головка к электро-МЕТАллизАТОРу | 1979 |
|
SU793654A1 |
| ПРОИЗВОДНЫЕ БЕНЗИМИДАЗОЛА, ИХ ТАУТОМЕРЫ ИЛИ ИХ СОЛИ И ЛЕКАРСТВЕННОЕ СРЕДСТВО С АНТАГОНИСТИЧЕСКИМ В ОТНОШЕНИИ АНГИОТЕНЗИНА II ДЕЙСТВИЕМ | 1993 |
|
RU2126401C1 |
Авторы
Даты
2016-02-20—Публикация
2011-06-01—Подача