Изобретение относится к области синтеза наноразмерного диоксида титана, а именно к способу приготовления η-модификации TiO2.
Наноразмерные модификации TiO2 применяют в качестве фотокатализаторов (очистка сточных вод от цианистых соединений на предприятиях золотодобывающей промышленности [Bateman Р. / The gold mining industry committed to safe cyanide use / Mining Environmental Management / 2001, P. 4], органических загрязнений и патогенных бактерий на предприятиях органического синтеза и животноводческих комплексах [Technical report «Treatment of cyanide heap Leaches and tailings», September 1994. U.S. Environmental Protection Agency Office of Solid Waste Special Waste Branch 401 M Street, SW Washington, DC 20460]), преобразователя солнечной энергии в электрическую [Fujishima, A. / TiO2 Photocatalysis: fundamentals and applications / Tokyo: BKC / 1999, P. 242], в медицине (создание лекарственных средств нового поколения на основе искусственных нанобиоконструкций, содержащих наночастицы TiO2, доставка препарата в клетки [Hoffman Allan S. / The origins and evolution of «controlled» drug delivery systems / J. Contr. Release / 2008, V. 132, P. 153-163], фотоэлектрохимическая стерилизация микробных клеток, применение в онкологии). Недавно получена новая наноразмерная модификация TiO2 (η-TiO2) [US 20060171877 A1, 03.08.2006], которую предложено использовать в качестве адсорбента [US 20060171877 A1, 03.08.2006] и фотокатализатора [Савинкина Е.В., Оболенская Л.Н., Кузьмичева Г.М., Дорохов А.В., Фотокатализатор на основе наноразмерной η-модификации диоксида титана, Патент РФ №RU 2469788 C1 (2011)].
Описан способ получения образцов с наноразмерной модификацией диоксида титана гидролизом сульфата титанила [Коленько Ю.В. и др. / Фазовый состав нанокристаллического диоксида титана, синтезированного в гидротермальных условиях из различных соединений титанила / Неорганические материалы / 2004, Т. 40, №9, с. 942-949; R. Liao, B. Liao / Synthesis and stabilization of nano-sized titanium dioxide / International Journal of Chemical Reactor Engineering / 2007, 5. P.A24.; C.S. Fang, Y.W. Chen / Preparation and Characterization of TiO2-Coated Optical-Fiber in a Photo Reactor /Materials Chemistry and Physics / 2003, 78. Р. 739]. Суть метода заключалась в гидролизе водного раствора сульфата титанила с разной концентрацией в присутствии серной кислоты в гидротермальных условиях при температурах 100-250°C в течение 0,5-24 часа и последующем высушивании полученной суспензии пористого диоксида титана.
Известен способ получения наноразмерного диоксида титана со структурой анатаза с использованием в качестве стабилизаторов анатаза неорганических кислот, в частности серной и азотной [Иванов В.К. / Функциональные материалы на основе диоксидов церия и элементов подгруппы титана: синтез, исследование структуры и размерных эффектов / Диссертация на соискание ученой степени доктора наук / Москва, 2011]. Суть метода заключалась в гидролизе водных растворов сульфата титанила TiOSO4 с концентрацией 0.15-0.5 моль/л в присутствии H2SO4 (концентрация кислоты 0.1-1 моль/л) и HNO3 (концентрация кислоты 0.25-1 моль/л) в гидротермальных и гидротермально-микроволновых условиях при температурах 100-240°C.
Однако этими способами получить η-модификацию диоксида титана не удается.
Способ получения η-TiO2 (сульфатный метод), который был описан в патенте [US 20060171877 A1, 03.08.2006], основан на гидролизе сольвата сульфата титанила TiOSO4·xH2SO4·yH2O (концентрация 100-260 г/л) в присутствии H2SO4 в соотношении TiO2:H2SO4 = 0.7:3.0 при температуре до 120°C с использованием в качестве коагулянта HCl. Выход нано-η-TiO2 составлял до 30%.
Наиболее близким техническим решением является получение η-модификации диоксида титана гидролизом сольвата сульфата титанила TiOSO4·xH2SO4·yH2O (концентрация 0.4-0.7 моль/л) при температурах 75-97°C [RU 2469954 С2, 20.12.2012], в качестве коагулянта применялся KCl. Выход нано-η-TiO2 составил 80%.
Недостаток предыдущих методов получения нано-η-TiO2 заключается в использовании коагулянтов, которые могут загрязнять конечный продукт (наноразмерный η-TiO2) и ухудшать его свойства. Кроме того, прекурсор TiOSO4·xH2SO4·yH2O имеет непостоянный состав, то есть содержание H2SO4 и H2O в нем может быть разным, что может плохо сказываться на воспроизводимости результатов.
Технический результат изобретения заключается в способе получения наноразмерной модификации η-TiO2 гидролизом сульфата титанила, взятого в виде дигидрата, без использования коагулянта.
Технический результат достигается тем, что процесс гидролиза сульфата титанила состава TiOSO4·2H2O проводят в присутствии азотной кислоты HNO3 в мольном соотношении HNO3: TiIV = (1-6):1 или в присутствии хлорной кислоты HClO4 в мольном соотношении HClO4: TiIV = (2-6):1 при температуре 90-98°C в течение 40-70 мин, что позволяет получить наноразмерную модификацию η-TiO2 без использования коагулянта с выходом до 90%.
Продукт с наноразмерной модификацией η-TiO2 был получен гидролизом TiOSO4·2H2O в присутствии азотной кислоты HNO3 или хлорной кислоты HClO4 при температуре 90-98°C в течение 40-70 мин при постоянном перемешивании. Указанные кислоты вносили в реакционную смесь до начала гидролиза TiOSO4·2H2O в мольном соотношении кислота: TiIV = (1-6):1 (для HNO3) и (2-6):1 (для HClO4). Полученный порошок отделяли вакуумным фильтрованием, промывали дважды водой и ацетоном, а затем сушили на воздухе в сушильном шкафу (2 часа при 50°C).
Фазовый состав полученных образцов контролировали традиционным рентгенографическим методом. Рентгеновская съемка образцов с вращением проведена на дифрактометре HZG-4 (графитовый плоский монохроматор): излучение CuKα на дифрагированном пучке в пошаговом режиме (время набора импульсов 10 сек, величина шага 0.02°, интервал углов 2Θ=2-50°). Обработка массива экспериментальных данных осуществлена по программе PROFILE FITTING V 4.0 Щуров В.В., Иванов С.А. // Кристаллография. 1997. Т. 42. №2. С. 239]. Размеры областей когерентного рассеяния (ОКР) рассчитаны по формуле Шеррера (т.е. без учета возможных - микронапряжений) D=Kλ/βcosΘ: λ=1.54051 Å - длина волны, 2Θ ~ 25° (d ~ 3.5 Å), β - интегральная ширина пика, коэффициент К (фактор формы кристаллитов) принимали равным 0.9. Стандартное отклонение ±5%.
Исследование микроструктуры полученных образцов проведено методом сканирующей электронной микроскопии (СЭМ) с использованием электронного микроскопа высокого разрешения JSM 7500F.
Пример 1
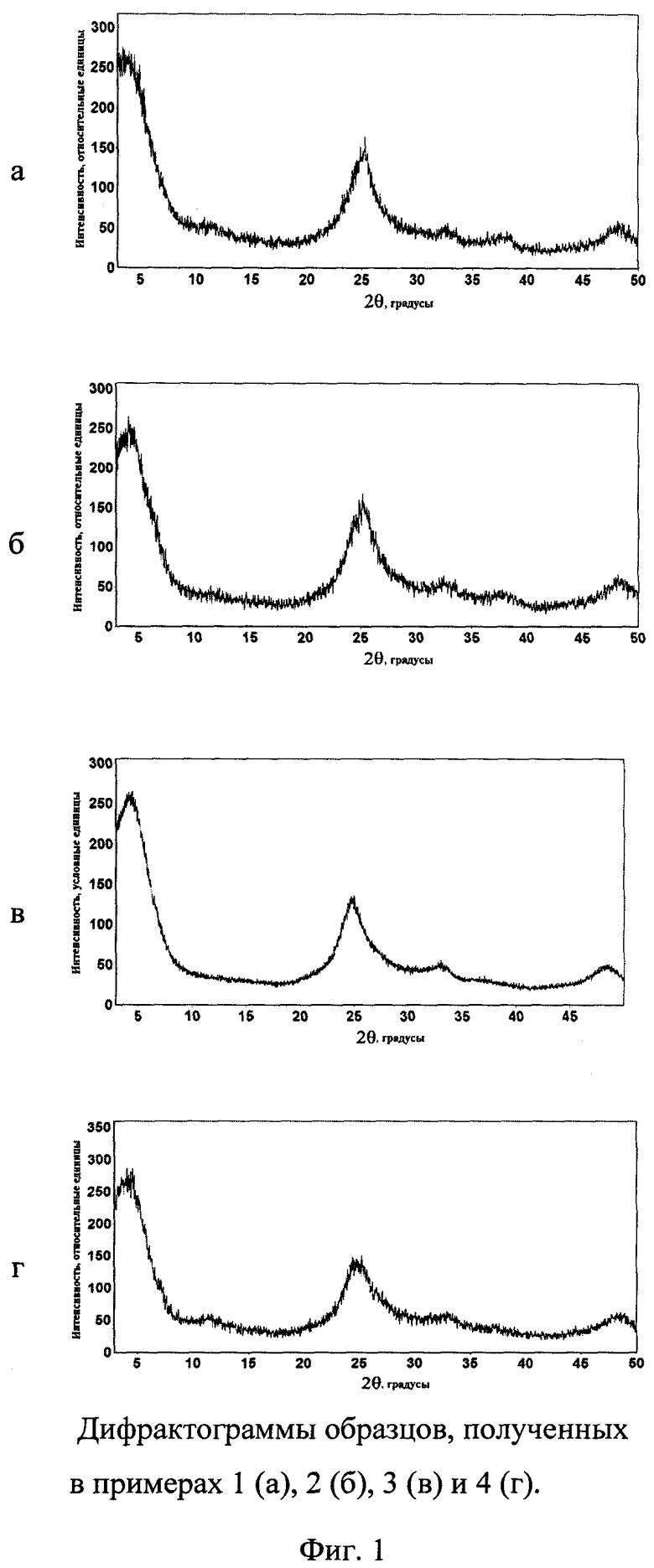
Водный раствор 0.45 моль/л сульфата титанила исходного состава TiOSO4·2H2O смешивают с HNO3 в массовом соотношении 1:3.3, нагревают от комнатной температуры до температуры 95(±2)°C в течение 50 минут при постоянном перемешивании. Полученные образцы отделяют вакуумным фильтрованием, промывают водой и ацетоном, а затем сушат в сушильном шкафу при 50°C 2 часа. Выход TiO2 - 80%. Методом РФА (фиг. 1а) показано, что полученный продукт представляет собой η-TiO2.
Пример 2
Водный раствор 0.45 моль/л сульфата титанила исходного состава TiOSO4·2H2O смешивают с HNO3 в массовом соотношении 1:1, нагревают от комнатной температуры до температуры 95(±2)°C в течение 50 минут при постоянном перемешивании. Полученные образцы отделяют вакуумным фильтрованием, промывают водой и ацетоном, а затем сушат в сушильном шкафу при 50°C 2 часа. Выход TiO2 - 85%. Методом РФА (фиг. 1б) показано, что полученный продукт представляет собой η-TiO2.
Пример 3
Водный раствор 0.45 моль/л сульфата титанила исходного состава TiOSO4·2H2O смешивают с HNO3 в массовом соотношении 1:2, нагревают от комнатной температуры до температуры 95(±2)°C в течение 50 минут при постоянном перемешивании. Полученные образцы отделяют вакуумным фильтрованием, промывают водой и ацетоном, а затем сушат в сушильном шкафу при 50°C 2 часа. Выход TiO2 - 90%. Методом РФА (фиг. 1в) показано, что полученный продукт представляет собой η-TiO2. Согласно данным сканирующей электронной микроскопии полученный образец с η-TiO2 является наноразмерным (фиг. 2): размеры наночастиц ~10÷~15 нм и агрегатов ~30÷~50 нм
Пример 4
Водный раствор 0.45 моль/л сульфата титанила исходного состава TiOSO4·2H2O смешивают с HNO3 в массовом соотношении 1:6, нагревают от комнатной температуры до температуры 95(±2)°C в течение 50 минут при постоянном перемешивании. Полученные образцы отделяют вакуумным фильтрованием, промывают водой и ацетоном, а затем сушат в сушильном шкафу при 50°C 2 часа. Выход TiO2 - 45%. Методом РФА (фиг. 1г) показано, что полученный продукт представляет собой η-TiO2.
Пример 5
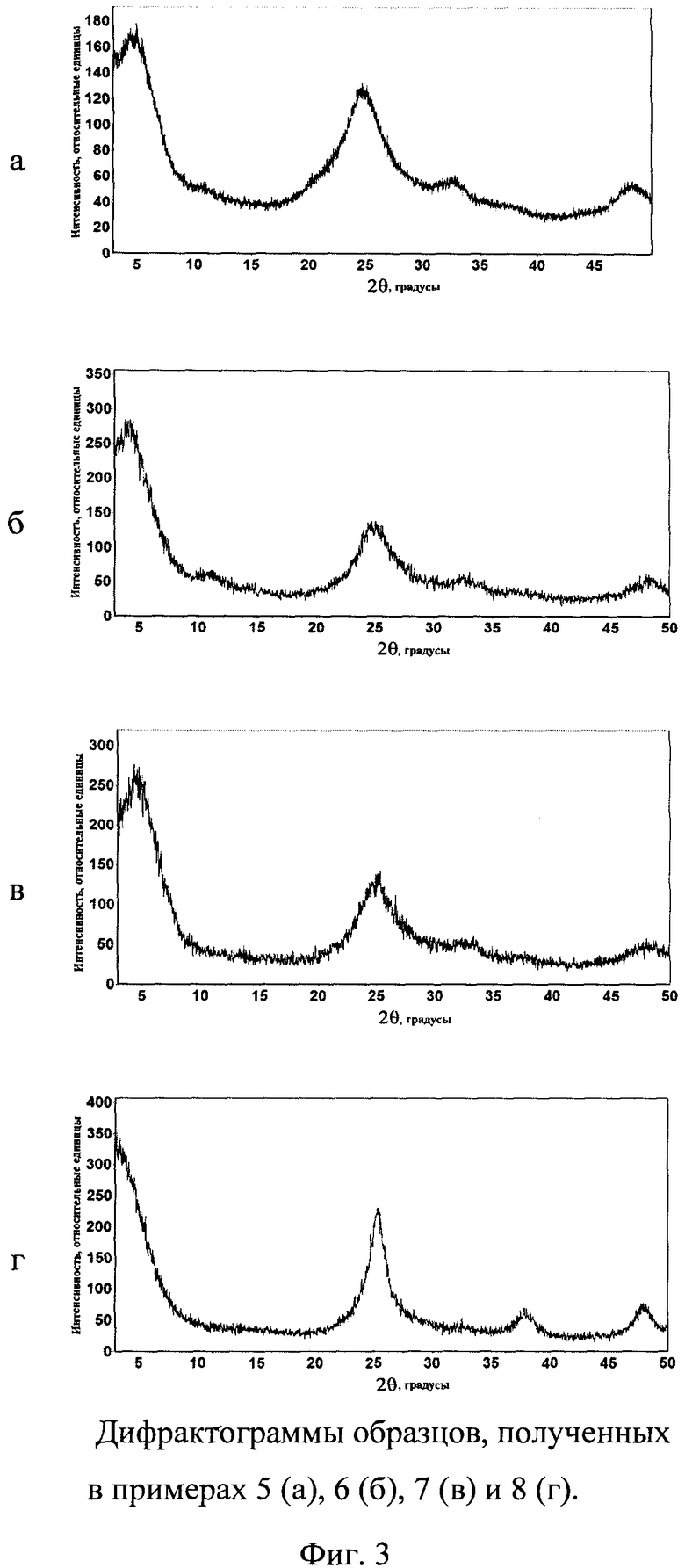
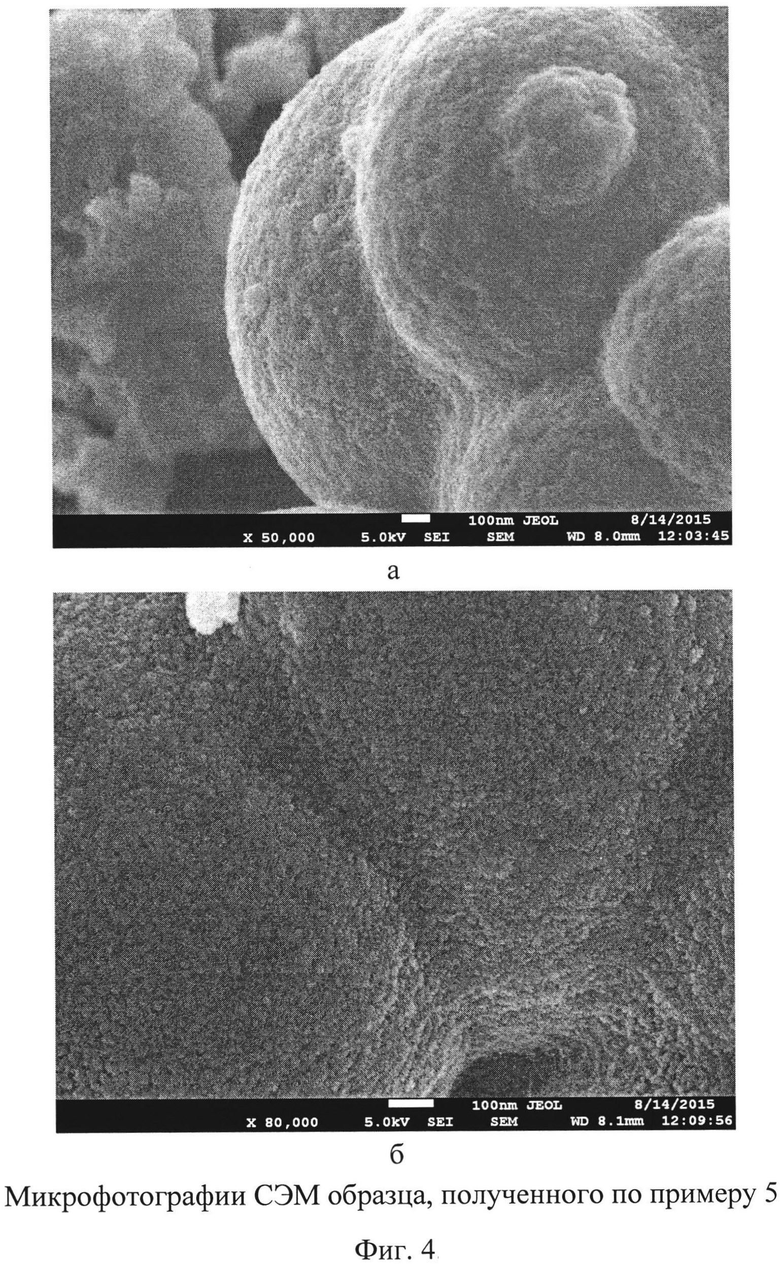
Водный раствор 0.45 моль/л сульфата титанила исходного состава TiOSO4·2H2O смешивают с HClO4 в массовом соотношении 1:3.3, нагревают от комнатной температуры до температуры 95(±2)°C в течение 50 минут при постоянном перемешивании. Полученные образцы отделяют вакуумным фильтрованием, промывают водой и ацетоном, а затем сушат в сушильном шкафу при 50°C 2 часа. Выход TiO2 - 63%. Методом РФА (фиг. 3а) показано, что полученный продукт представляет собой η-TiO2. Согласно данным сканирующей электронной микроскопии полученный образец с η-TiO2 является наноразмерным (фиг. 4): размеры наночастиц ~10÷~20 нм и агрегатов ~1÷~2 мкм.
Пример 6
Водный раствор 0.45 моль/л сульфата титанила исходного состава TiOSO4·2H2O смешивают с HClO4 в массовом соотношении 1:2, нагревают от комнатной температуры до температуры 95(±2)°C в течение 50 минут при постоянном перемешивании. Полученные образцы отделяют вакуумным фильтрованием, промывают водой и ацетоном, а затем сушат в сушильном шкафу при 50°C 2 часа. Выход TiO2 - 70%. Методом РФА (фиг. 3б) показано, что полученный продукт представляет собой η-TiO2.
Пример 7
Водный раствор 0.45 моль/л сульфата титанила исходного состава TiOSO4·2H2O смешивают с HClO4 в массовом соотношении 1:6, нагревают от комнатной температуры до температуры 95(±2)°C в течение 50 минут при постоянном перемешивании. Полученные образцы отделяют вакуумным фильтрованием, промывают водой и ацетоном, а затем сушат в сушильном шкафу при 50°C 2 часа. Выход TiO2 - 45%. Методом РФА (фиг. 3в) показано, что полученный продукт представляет собой η-TiO2.
Пример 8
Водный раствор 0.45 моль/л сульфата титанила исходного состава TiOSO4·2H2O смешивают с HClO4 в массовом соотношении 1:1, нагревают от комнатной температуры до температуры 95(±2)°C в течение 50 минут при постоянном перемешивании. Полученные образцы отделяют вакуумным фильтрованием, промывают водой и ацетоном, а затем сушат в сушильном шкафу при 50°C 2 часа. Выход TiO2 - 60%. Методом РФА (фиг. 3г) показано, что полученный продукт представляет собой анатаз.
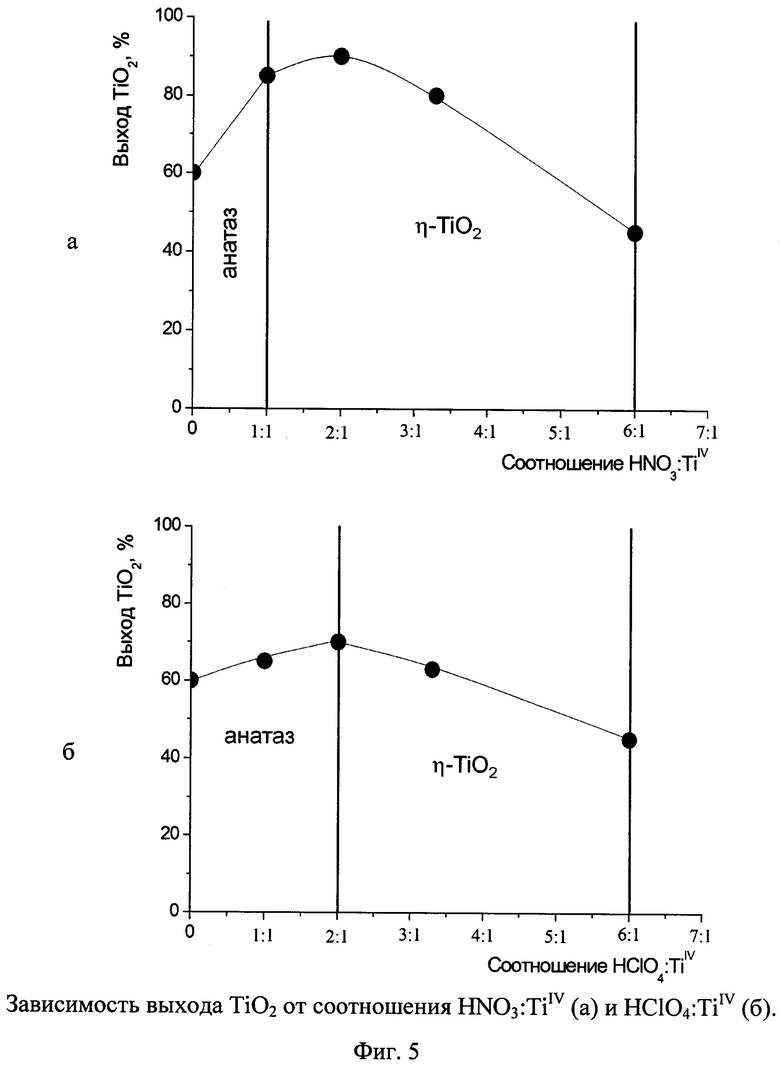
На фиг. 5 приведена зависимость выхода TiO2 от соотношения HNO3: TiIV (фиг. 5а) и HClO4: TiIV (фиг. 5б). Максимальный выход η-TiO2 достигается при мольном соотношении кислота: TiIV = 2:1 (90% - при использовании HNO3 и 70% - при использовании HClO4). По мере увеличения соотношения кислота: TiIV выход η-TiO2 уменьшается.
Пример 9
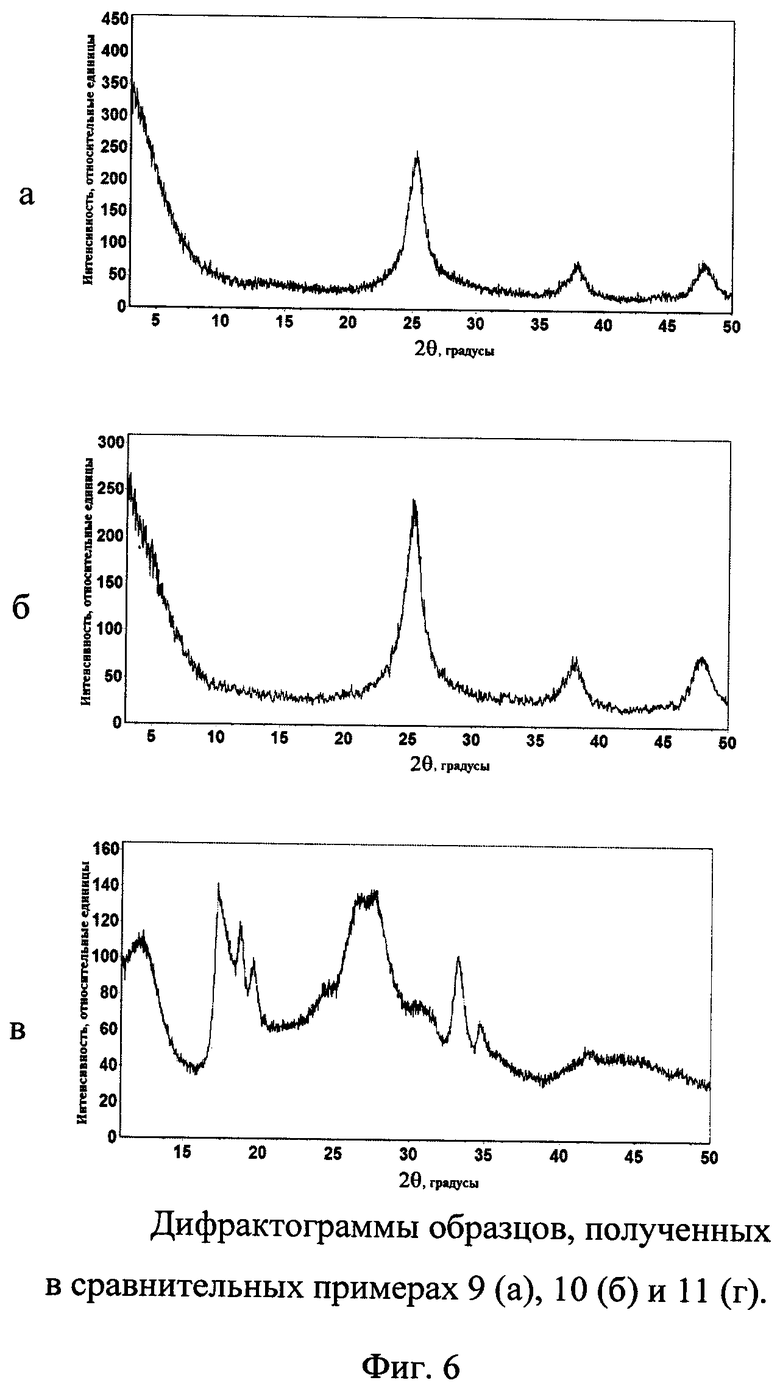
Водный раствор 0.45 моль/л сульфата титанила исходного состава TiOSO4·2H2O нагревают от комнатной температуры до температуры 95(±2)°C в течение 50 минут при постоянном перемешивании. Полученные образцы отделяют вакуумным фильтрованием, промывают водой и ацетоном, а затем сушат в сушильном шкафу при 50°C 2 часа. Выход TiO2 - 60%. Методом РФА (фиг. 6а) показано, что полученный продукт представляет собой анатаз.
Пример 10
Водный раствор 0.45 моль/л сульфата титанила исходного состава TiOSO4·2H2O смешивают с СН3СООН в массовом соотношении 1:3.3, нагревают от комнатной температуры до температуры 95(±2)°C в течение 50 минут при постоянном перемешивании. Полученные образцы отделяют вакуумным фильтрованием, промывают водой и ацетоном, а затем сушат в сушильном шкафу при 50°C 2 часа. Выход TiO2 - 30%. Методом РФА (фиг. 6б) показано, что полученный продукт представляет собой анатаз.
Пример 11
Водный раствор 0.45 моль/л сульфата титанила исходного состава TiOSO4·2H2O смешивают с H3PO4 в массовом соотношении 1:3.3, нагревают от комнатной температуры до температуры 95(±2)°C в течение 50 минут при постоянном перемешивании. Полученные образцы отделяют вакуумным фильтрованием, промывают водой и ацетоном, а затем сушат в сушильном шкафу при 50°C 2 часа. Методом РФА (фиг. 6в) показано, что полученный продукт представляет собой смесь фосфатов титана и других соединений.
Пример 12
Водный раствор 0.45 моль/л сульфата титанила исходного состава TiOSO4·2H2O смешивают с Н3РО4 в массовом соотношении 1:30, нагревают от комнатной температуры до температуры 95(±2)°C в течение 50 минут при постоянном перемешивании. Смесь желеобразная, порошок фильтрованием не отделяется.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ НАНОРАЗМЕРНОЙ η-МОДИФИКАЦИИ ДИОКСИДА ТИТАНА | 2011 |
|
RU2469954C2 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ТИТАНОКСИДНОГО ФОТОКАТАЛИЗАТОРА, АКТИВНОГО В ВИДИМОЙ ОБЛАСТИ СПЕКТРА | 2012 |
|
RU2520100C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ ФОТОКАТАЛИЗАТОРА НА ОСНОВЕ η-МОДИФИКАЦИИ ДИОКСИДА ТИТАНА, ДОПИРОВАННОГО ВАНАДИЕМ, АКТИВНОГО В ВИДИМОЙ ОБЛАСТИ СПЕКТРА | 2013 |
|
RU2540336C1 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОРАЗМЕРНОГО ДИОКСИДА ТИТАНА | 2014 |
|
RU2565193C1 |
| Способ получения интеркалированной поли-N-винилкапролактамом наноразмерной η-модификации оксида титана(IV) | 2017 |
|
RU2666441C1 |
| СПОСОБ МОДИФИЦИРОВАНИЯ МАРГАНЦЕМ НАНОРАЗМЕРНОГО ДИОКСИДА ТИТАНА | 2014 |
|
RU2565689C1 |
| СПОСОБ ПОЛУЧЕНИЯ АДСОРБЕНТА НА ОСНОВЕ НАНОРАЗМЕРНОГО ДИОКСИДА ТИТАНА СО СТРУКТУРОЙ АНАТАЗА | 2011 |
|
RU2463252C1 |
| Способ получения активных в видимой области спектра фотокатализаторов с наноразмерными диоксидами титана со структурой анатаза и смеси анатаза и рутила, допированных переходными металлами (Ni, V, Ag, Cu, Mn) | 2021 |
|
RU2776582C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОРОШКА ДИБОРИДА ТИТАНА | 2015 |
|
RU2603407C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФОТОКАТАЛИЗАТОРА НА ОСНОВЕ ДИОКСИДА ТИТАНА | 2009 |
|
RU2408427C1 |

Изобретение может быть использовано в неорганической химии. Для получения наноразмерной модификации η-TiO2 проводят гидролиз сульфата титанила в присутствии азотной кислоты HNO3 или хлорной кислоты HClO4 в течение 40-70 мин при температуре 90-98°C без использования коагулянта. Азотную кислоту берут в мольном соотношении HNO3 : TiIV = (1-6):1, хлорную кислоту - в мольном соотношении HClO4 : TiIV = (2-6):1. Изобретение позволяет получить нанаразмерный диоксид титана η-TiO2 без использования коагулянта. 3 з.п. ф-лы, 6 ил., 11 пр.
1. Способ приготовления наноразмерной модификации η-TiO2, отличающийся тем, что гидролиз сульфата титанила проводят в присутствии азотной кислоты HNO3 в мольном соотношении HNO3 : TiIV = (1-6):1 или в присутствии хлорной кислоты HClO4 в мольном соотношении HClO4 : TiIV = (2-6):1 при температуре 90-98°C в течение 40-70 мин без использования коагулянта.
2. Способ по п. 1, отличающийся тем, что в качестве исходного реагента использовали сульфат титанила состава TiOSO4·2H2O.
3. Способ по п. 1, отличающийся тем, что гидролиз сульфата титанила проводили в присутствии HNO3 в соотношении HNO3 : TiIV = (1-6):1.
4. Способ по п. 1, отличающийся тем, что гидролиз сульфата титанила проводили в присутствии HClO4 в соотношении HClO4 : TiIV = (2-6):1.
| US 20060171877 A1, 03.08.2006 | |||
| СПОСОБ ПОЛУЧЕНИЯ НАНОРАЗМЕРНОЙ η-МОДИФИКАЦИИ ДИОКСИДА ТИТАНА | 2011 |
|
RU2469954C2 |
| US 6551536 B1, 22.04.2003 | |||
| US 20050265918 A1, 01.12.2005 | |||
| WO 2012066547 A1, 24.05.2012 | |||
| CN 101696031 A, 21.04.2010 | |||
| LO CHIEN-FONG, WU JEFFREY C.S., Preparation and Characterization of TiO2-Coated Optical-Fiber in a Photo Reactor, J | |||
| Chin | |||
| Inst | |||
| Chem | |||
| Engrs., 2005, vol | |||
| Коридорная многокамерная вагонеточная углевыжигательная печь | 1921 |
|
SU36A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
2016-02-27—Публикация
2014-09-19—Подача