Изобретение относится к методам количественного определения действующих биологических веществ в растительном сырье и в препаратах, получаемых из него. Может использоваться в химико-фармацевтической, парфюмерно-косметической и пищевой отраслях.
Целью изобретения является упрощение способа определения количественного содержания панаксозидов в объектах, полученных из женьшеня Panax ginseng.
Из уровня техники известны следующие способы количественного определения панаксозидов:
1) Хроматографическое определение панаксозидов в режиме ВЭЖХ путем градиентного элюирования на окдодецилсилановой колонке в течение 60 мин [1].
Недостатком данного способа является длительность анализа. Проведение элюции в градиентном режиме требует наличия дорогостоящего оборудования и высокого расхода высокочистых органических растворителей.
2) Наиболее близким к заявляемому (прототипом) является способ определения панаксозидов в экстракте женьшеня 1480568 (заявка №4164901, дата приоритета 10.11.1986, дата публикации 30.11.1994, МПК G01N 33/68). Сущность данного изобретения заключается в смешении извлечений из сырья лекарственных форм женьшеня с реактивом, состоящим из ванилина и серной кислоты, дальнейшем нагревании смеси до появления пурпурно-красного окрашивания, определении на спектрофотометре оптической плотности при длине волны, равной 544 нм, и установлении количественного содержания панаксозидов. При осуществлении спектрофотометрического анализа в качестве стандартного образца применяют спиртовой раствор эргокальциферола (витамина D2).
Недостатком данного способа является то, что применяемый ароматический альдегид (ванилин) в качестве реагента способен образовывать окрашенные комплексы как с терпеноидами, так и с фенилпропаноидами [2]. Образованное окрашенное производное нестабильно. Применение серной кислоты и нагревания обуславливают обугливание органического составляющего. Кроме этого образование окрашенного производного зависит от температурного фактора нагревания исследуемых образцов и стандарта, что может способствовать расхождению результатов. Недостатком прототипа является использование в качестве стандарта жирорастворимого масляного раствора витамина D2 (эргокальциферола). Эргокальциферол - вещество, чувствительное к свету при любых условиях, полностью окисляется на воздухе за несколько суток. Отсутствие отечественных производителей данного вещества или указанной лекарственной формы делает затруднительным широкое применение данного способа в лабораторной практике.
Предлагаемый способ направлен на решение указанных задач, а именно оптимизацию количественного определения панаксозидов женьшеня.
Техническим результатом предлагаемого способа является экспериментальное обоснование количественного определения панаксозидов женьшеня:
- повышение специфичности реактива - рациональное соотношение используемых компонентов;
- повышение стабильности реактива;
- уменьшение времени анализа;
- стабильность градуировочных характеристик стандарта;
- применение данного способа при анализе образцов в различных агрегатных состояниях, содержащих панаксозиды;
- уменьшение объема анализируемой пробы;
- доступность реактивов и стандартов.
Предлагается способ количественного определения панаксозидов путем смешивания анализируемого образца с растворами фосфорномолибденовой и серной кислот с последующим определением оптической плотности при длине волны 700 нм и расчетом содержания панаксозидов по предварительно построенному калибровочному графику с использованием стандартного образца.
Отличием является то, что используют 0,002М раствор фосфорномолибденовой кислоты в изопропиловом спирте и 0,8М серную кислоту, взятые в объемном соотношении 1:1:0,5 соответственно, а в качестве стандартного образца применяют урсодеоксихолевою кислоту.
По современной классификации панаксозиды относятся к тритерпеноидам стероидного происхождения [3]. При взаимодействии предлагаемого реактива с тритерпеновыми тетрациклическими сапонинами - панаксозидами женьшеня - в процессе реакции образуется «молибденовая синь». Метод линеен и позволяет определять количество панаксозидов в образце в диапазоне от 2,5 до 30 мг/см3, что подтверждает специфичность реактива и рациональность соотношения используемых компонентов. Признаки формулы находятся в причинно-следственной связи с заявленным техническим результатом.
Гетерополикислоты и их анионы нестабильны при щелочных значениях рН, процесс разрушения возникает под действием воды [4]. Поэтому для стабилизации образующейся «молибденовой сини» необходимо использовать жидкие фазы с органическими растворителями, в максимальной степени исключающие присутствие молекул воды [5]. В наших исследованиях экспериментально установлено использование абсолютизированного изопропилового спирта при растворении кристаллов фосфорномолибденовой кислоты, что позволяет избежать даже незначительного помутнения с образованием аквакомплексов (МоО3).
Наиболее оптимальные физико-химические свойства, применимые к заявляемому способу, обнаруживаются у изопропилового спирта. В линейке алифатических спиртов изопропиловый спирт обладает наименьшей дипольностью (поляризуемостью) [6]. При этом сохраняется неограниченная растворимость воды в данном растворителе [7]. Перечисленные параметры выгодно отличают изопропиловый спирт от других алифатических спиртов.
Новым в достижении технического результата является то, что в качестве реактива используют 0,002М раствор фосфорномолибденовой кислоты в изопропиловом спирте. Соотношение компонентов реакционной смеси позволяет получать оптические плотности в диапазоне 0,05-2,0 в зависимости от концентрации анализируемого компонента или известного стандарта (урсодезоксихолевой кислоты), что подтверждает рациональность соотношения используемых компонентов. Сущность изобретения заключается в следующем. К одному объему исследуемого образца последовательно добавляют: один объем фосфорномолибденового реактива и 0,5 объема кислоты серной концентрированной. Через 5 мин смесь детектируют, учитывая оптическую плотность при длине волны 700 нм. Новым является также и то, что в качестве стандарта используют растворы урсодезоксихолевой кислоты(3α,7β-дигидрокси-5β-холин-24-овая кислота) в изопропиловом спирте.
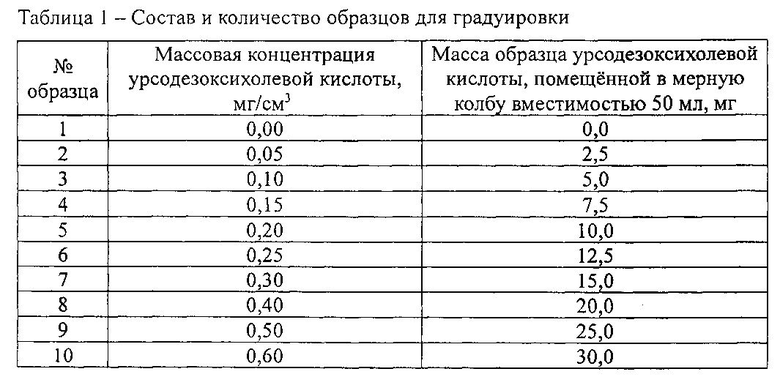
По литературным данным дезоксихолевая кислота и ее аналоги рассматриваются как стабильные слабо подверженные окислительным процессам, в том числе фотоокислению (при нормальных условиях) соединениям. При этом кристаллическое агрегатное состояние урсодезоксихолевой кислоты, достаточная стабильность молекулы, а при необходимости легкость очистки методом перекристаллизации делает ее привлекательной для использования в качестве стандарта [8, 9], что подтверждает доступность реактивов и стандартов. Признаки формулы находятся в причинно-следственной связи с заявленным техническим результатом. Градуировочные характеристики с применением урсодезоксихолевой кислоты необходимо оценивать не реже одного раза в квартал, а также при смене партий реактивов после поверки или ремонта спектрофотометра. В предлагаемом способе средствами контроля являются приготовленные образцы для градуировки (не менее 3 образцов из приведенных в табл. 1).
Международная фармакопея при разработке стандартных образцов, предназначенных для спектрофотометрического определения лекарственных форм, допускает использовать вещества (в качестве стандартного образца), отвечающие требованиям фармакопеи [10]. Описаны лекарственные препараты, содержащие урсодезоксихолевую кислоту в качестве действующего вещества (Урсосан, Урсофальк, Урдокса и др.) [11].
Структурное сходство тритерпеновых тетрациклических сапонинов со стероидным остовом [12] обуславливают возможность применения урсодезоксихолевой кислоты в качестве стандарта при количественном определении панаксозидов. Подтверждается стабильность градуировочных характеристик стандарта.
В заявляемом способе содержание суммы панаксозидов С1 в образце, мг/дм3, рассчитывают по известной формуле:

где D1 - оптическая плотность исследуемого раствора;
D2 - оптическая плотность раствора стандартного образца;
С2 - концентрация раствора стандартного образца, мг/дм3.
Пример 1. В мерную колбу вместимостью 50 мл3 вносят 1 мл настойки из корня женьшеня, доводят объем раствора 96%-ным этиловым спиртом до метки. 1 мл полученного раствора переносят в бюкс. К содержимому бюкса добавляют 1 мл 0,002М раствора фосфорномолибденовой кислоты в изопропиловом спирте и 0,5 мл 0,8М раствора серной кислоты. Содержимое бюкса, тщательно перемешивают.
Приготовление раствора стандартного образца. В мерную колбу вместимостью 50 мл3 вносят навеску урсодеоксихолевой кислоты 10 мг, доводят объем раствора изопропиловым спиртом до метки, 1 мл полученного раствора переносят в бюкс. К содержимому бюкса добавляют 1 мл 0,002М раствора фосфорномолибденовой кислоты в изопропиловом спирте и 0,5 мл 0,8М раствора серной кислоты. Содержимое тщательно перемешивают.
Оптическую плотность приготовленных окрашенных анализируемого и стандартного растворов измеряют на спектрофотометре СФ-2000 в кюветах с толщиной слоя 10 мм при длине волны 700 нм.
Оптическая плотность анализируемого раствора D1 0,2875; оптическая плотность раствора стандартного образца D2 0,528.
Содержание суммы панаксозидов С1, мг/дм3, в анализируемом препарате рассчитывают по известной формуле (1):
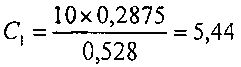
В настойке из корня женьшеня содержится 5,44 мг/дм3 суммы панаксозидов. Ошибка определения суммы панаксозидов не превышает 2%, что подтверждает точность расчетов.
Пример 2. Содержание суммы панаксозидов в капсулах, содержащих сухой концентрат женьшеня. Пробоподготовку осуществляют следующим образом. Содержимое капсулы тщательно перемешивают в ступке, отбирают точную навеску массой 20 мг. Навеску помещают в мерную колбу на 50 мл3 и доводят объем до метки 70%-ным этиловым спиртом.
Приготовление растворов стандартного образца. В мерные колбы на 50 мл3 помещают точные навески: 2,5; 5; 10; 15; 20; 25; 30 мг урсодезоксихолевой кислоты и растворяют в изопропиловом спирте. Для стандартных растворов после реакции с фосфономолибденовой кислотой измеряют оптическую плотность, придерживаясь методологии изложенной в примере 1. По полученным оптическим плотностям стандартных образцов строят калибровочный график.
При измерении на спектрофотометре СФ-2000 оптическая плотность анализируемого раствора D1 1,2875; оптическая плотность раствора стандартного образца D2 1,2089; что приближено к концентрации раствора стандартного образца С2 15 мг/дм3.
Содержание суммы панаксозидов в настойке из листьев женьшеня составит исходя из расчетов по известной формуле (1):
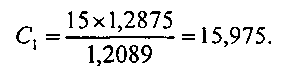
В анализируемом образце массой 20 мг содержится 15,975 мг/дм3 панаксозидов.
Ошибка определения суммы панаксозидов не превышает 3%.
Таким образом, по сравнению с прототипом преимуществом заявляемого способа является применение спиртового раствора урсодезоксихолевой кислоты для количественного определения панаксозидов в сырье и лекарственных формах женьшеня спектрофотометрическим методом. Это позволяет исключить из анализа химически чистые панаксозиды и панаксогенины.
Предлагаемый способ позволяет исключить термическую обработку реакционной смеси, что снижает время проведения анализа. При этом достигается заявленный технический результат. Таким образом, признаки формулы находятся в причинно-следственной связи с заявленным техническим результатом.
Способ предполагает использование реактива с чувствительностью выше, чем в описанном выше прототипе, это позволяет уменьшить объем анализируемой пробы, следовательно, достигается заявленный технический результат.
Предлагаемый способ можно использовать для быстрого, точного, с меньшими затратами средств и труда количественного определения содержания панаксозидов в надземной части женьшеня и его корнях, в биомассе культуры ткани женьшеня, в настойках из корня, листьев, биомассы женьшеня, в капсулах из корня и биомассы женьшеня. Таким образом, способ может быть использован при разных агрегатных состояниях образца, т.е. достигается заявленный технический результат.
Источники информации
1. Determination of ginsenosides in Panax ginseng roots by liquid chromatography with evaporative light-scattering detection / N. Fuzzati; B. Gabetta, K. Jayakar et all. // J. Assoc. Off. Anal. Chem. Int., 2000. V. 83. N. 4. - P. 820-829.
2. Wagner, H. Plant drug analisis - a thin layer chromatography atlas / H. Wagner, S. Blad-Springer // Berlin. 2009. - 384 p.
3. Куркин, В.А. Современные аспекты химической классификации биологически активных соединений лекарственных растений [Текст] / В.А. Куркин // Фармация, 2002. Т. 50. №2. - С. 8-16.
4. Гринберг, А.А. Введение в химию комплексных соединений / А.А. Гринберг // [Текст]: изд. 4-е, исправленное. - Л.: Химия, 1971. - 632 с.
5. Степин, Б.Д. Неорганическая химия [Текст] / Б.Д. Степин, А.А. Цветков //- М.: Высш. шк., 1994. - 608 с.
6. Садек, П. Растворители для ВЭЖХ [Текст] / П. Садек // пер. с английского А.А. Горбатенко и Е.И. Ревиной. - М.: БИНОМ, Лаборатория знаний, 2009, - 704 с.
7. Вайсбергер, А. Органические растворители. Физические свойства и методы очистки / А. Вайсбергер, Э. Проскауэр, Дж. Риддик, Э. Тупс // [Текст]: перевод с английского к.х.н. Н.Н. Тихомировой под ред. д.х.н. Я.М. Варшавского. - М.: Изд-во иностранной литературы. - 1958. - 520 с.
8. Полюдек-Фабини, Р. Органический анализ [Текст]: пер. с немецкого / Р. Полюдек-Фабини, Т. Бейрих. - Л.: Химия, 1981. - 624 с., ил. - Лейпциг, Академ. изд-во Гест и Портиг, 1975.
9. Справочник биохимика [Текст]: пер. с англ. / Р. Досон, Д. Элиот, У. Элиот, К. Джонс. - М.: Мир, 1991. - 544 с.
10. Арзамасцев, А.П. Стандартные образцы лекарственных веществ [Текст] / П.П. Арзамасцев, П.Л. Сенов // - М.: Медицина, 1978. - 248 с.
11. Плотникова, Е.Ю. Урсодезоксихолевая кислота вчера и сегодня [Текст] / Е.Ю. Плотникова, А.С. Сухих // Терапевт. - 2012. - С. 23-32.
12. Saponins, classification and occurrence in the plant kingdom / J.-P. Vincken, L. Heng, Aede de Groot, Harry Gruppen // Phytochemistry. - 2007. - V. 68. - P. 275-297.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ САПОНИНОВ В ЭКСТРАКТЕ ЖЕНЬШЕНЯ | 1986 |
|
RU1480568C |
| Способ количественного определения хлорхолинхлорида | 1978 |
|
SU767639A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПИРАЗИДОЛА | 1990 |
|
RU2006024C1 |
| СПОСОБ КАЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ЦИКЛОДОЛА | 1992 |
|
RU2053499C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ АНТИОКСИДАНТНОЙ АКТИВНОСТИ МИКРООРГАНИЗМОВ | 2011 |
|
RU2465593C1 |
| АДСОРБЕНТ ПОЛИМЕТИЛСИЛОКСАНА ПОЛИГИДРАТ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2020 |
|
RU2761627C1 |
| АДАПТОГЕННЫЙ, ТОНИЗИРУЮЩИЙ, ИММУНОМОДУЛИРУЮЩИЙ, ГИПОГЛИКЕМИЧЕСКИЙ, АНТИГИПОКСИЧЕСКИЙ, ПРОТИВОВОСПАЛИТЕЛЬНЫЙ, НООТРОПНЫЙ, РАДИОПРОТЕКТОРНЫЙ, ФЕРВОПРОТЕКТОРНЫЙ, АКТОПРОТЕКТОРНЫЙ ПРЕПАРАТ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2001 |
|
RU2195950C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИФИДОГЕННОГО ФАКТОРА | 2013 |
|
RU2553513C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АНАФРАНИЛА | 1992 |
|
RU2092815C1 |
| Способ пробоподготовки образцов для аминокислотного анализа в условиях обращенно-фазовой высокоэффективной жидкостной хроматографии | 2024 |
|
RU2829449C1 |
Изобретение относится к области аналитической химии и касается способа определения количественного содержания панаксозидов в объектах, полученных из женьшеня Panax ginseng. Сущность способа заключается в том, что смешивают анализируемый образец с растворами фосфорномолибденовой и серной кислот с последующим определением оптической плотности при длине волны 700 нм и расчетом содержания панаксозидов по предварительно построенному калибровочному графику с использованием стандартного образца. При этом используют 0,002М раствор фосфорномолибденовой кислоты в изопропиловом спирте и 0,8М серную кислоту, взятые в объемном соотношении 1:1:0,5 соответственно, а в качестве стандартного образца применяют урсодеоксихолевую кислоту. Использование способа позволяет с высокой точностью определить содержание панаксозидов. 3 пр.
Способ количественного определения панаксозидов путем смешивания анализируемого образца с растворами фосфорномолибденовой и серной кислот с последующим определением оптической плотности при длине волны 700 нм и расчетом содержания панаксозидов по предварительно построенному калибровочному графику с использованием стандартного образца, отличающийся тем, что используют 0,002М раствор фосфорномолибденовой кислоты в изопропиловом спирте и 0,8М серную кислоту, взятые в объемном соотношении 1:1:0,5 соответственно, а в качестве стандартного образца применяют урсодезоксихолевую кислоту.
| СПОСОБ ОПРЕДЕЛЕНИЯ САПОНИНОВ В ЭКСТРАКТЕ ЖЕНЬШЕНЯ | 1986 |
|
RU1480568C |
| КУРКИН В.А и АКУШСКАЯ А.С | |||
| Разработка методов контроля качества женьшеня настойки // Химия растительного сырья, 2013, 2, С.177-182 | |||
| СПОСОБ ОПРЕДЕЛЕНИЯ ТРИТЕРПЕНОВЫХ САПОНИНОВ В РАСТИТЕЛЬНОМ СЫРЬЕ И ЛЕКАРСТВЕННЫХ ПРЕПАРАТАХ | 2009 |
|
RU2413951C1 |
Авторы
Даты
2016-03-27—Публикация
2015-04-07—Подача