Изобретение относится к области аналитической химии, в частности к определению серебра вольтамперометрическим методом.
Известен вольтамперометрический способ определения серебра в водных средах - патент РФ №2330274 от 27.07.2008, бюл. №21 // Соколов М.А., Алексеева Н.А., Шишкина Е.А. //, заключающийся в электрохимическом осаждении продуктов восстановления серебра на предварительно подготовленном твердом рабочем электроде из инертного материала (например, углеситалла) из раствора, который представляет собой анализируемое вещество, растворенное в фоновом электролите, и последующем электрохимическом растворении ранее осажденных продуктов восстановления серебра с регистрацией вольтамперной кривой. Концентрацию серебра определяют по величине анодного пика электрохимического растворения продуктов восстановления серебра. В качестве фонового электролита, в котором предварительно растворяют анализируемое вещество, используется серная кислота концентрации не менее 0,01 моль/дм3 с добавкой ионов меди таким образом, чтобы в анализируемом растворе суммарная концентрация ионов меди была не менее 3·10-6 моль/дм3. Электрохимическое осаждение продуктов восстановления серебра проводят при отрицательном потенциале твердого рабочего электрода, установленном в диапазоне от -250 до -300 мВ (относительно хлоридсеребряного электрода сравнения). Осажденные продукты восстановления серебра растворяют при скорости изменения потенциала на рабочем электроде не более 500 мВ/с электрохимическим способом и регистрируют вольтамперную кривую. Аналитическим сигналом серебра является высота анодного пика электрохимического растворения серебра на вольтамперной кривой в области потенциалов от +300 до +500 мВ. Изобретение позволяет измерять микроконцентрации серебра до 5·10-8 моль/дм3 в различных объектах с высокой точностью.
Недостатком вольтамперометрического способа измерения концентрации серебра является двухстадийность процесса, а именно предварительное осаждение продуктов восстановления серебра на рабочем электроде и последующее электрохимическое растворение ранее осажденных продуктов восстановления серебра, что увеличивает длительность процесса.
Из известных технических решений наиболее близким по назначению и технической сущности к заявляемому объекту - прототипом - является статья «Определение серебра вольтамперометрическим методом» (авторы Е.А. Лейтес, М.Ю. Быкова // Известия АГУ, №3/1 (41), (75). С. 177-179. 2012). Исследования проводят в постоянно токовом режиме регистрации вольтамперограмм с линейной разверткой потенциала. В качестве фонового электролита для определения серебра применяют KNO3. В двухэлектродной электрохимической ячейке в качестве рабочего используют стеклоуглеродный электрод. Электрод сравнения - насыщенный хлоридсеребряный, соединенный с ячейкой электролитическим ключом, заполненный раствором KNO3. Катодную вольтамперограмму регистрируют от потенциала 0,5 В при скорости развертки V=100 мВ/c. Пик серебра (I) регистрируют при потенциале 0,05 В. Интервал определяемых концентраций составляет от 2·10-6 М до 8·10-5 М. Правильность методики определения серебра (I) на стеклоуглеродном электроде проверена на модельных растворах методом «введено-найдено».
Недостаток прототипа:
недостаточная чувствительность для определения следовых количеств серебра в водных растворах.
Общими для прототипа и заявляемого изобретения является извлечение серебра из фонового раствора, содержащего в качестве одного из компонентов KNO3, на стеклоуглеродный электрод.
Данное изобретение отличается от прототипа тем, что в фоновый раствор, содержащий 4,5 мл 1 М KNO3, добавляют 0,5 мл 0,1 М этилендиаминтетраацетата натрия (ЭДТА) и определяют концентрацию серебра на стеклоуглеродном электроде из образующегося комплексного соединения.
Сущность изобретения
Способ определения серебра катодной вольтамперометрией, заключающийся в том что, определение концентрации серебра проводят в фоновом растворе, содержащем 4,5 мл 1 М KNO3 и 0,5 мл 0,1 М этилендиаминтетраацетат натрия (ЭДТА), выдерживая потенциал электролиза +0,5 В от 10 с до 20 с. Серебро восстанавливается на поверхности стеклоуглеродного электрода в виде комплексного малорастворимого соединения с ЭДТА (рК=7,20). Затем регистрируют вольтамперограмму при линейной развертке потенциала 100 мВ/с. Пик при потенциале +0,05 В соответствует восстановлению серебра и линейно зависит от концентрации серебра в водных растворах. Аналитический сигнал серебра регистрируют и оценивают методом добавок аттестованных растворов относительно насыщенного хлоридсеребряного электрода.
Осуществление изобретения
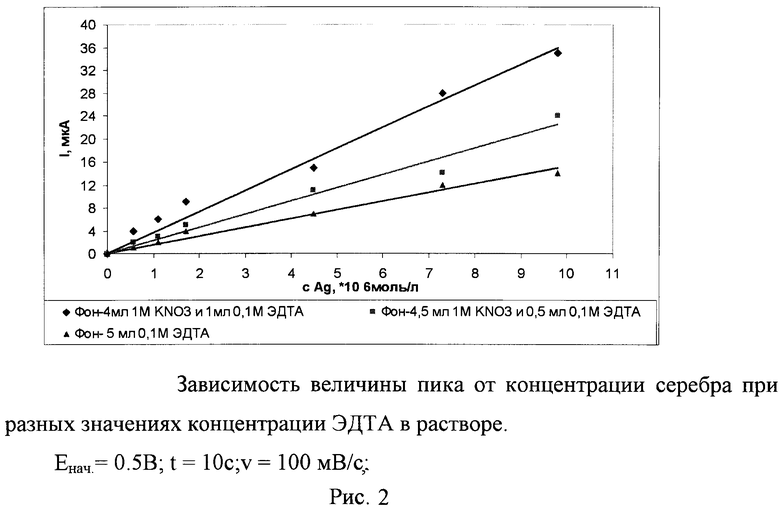
В двухэлектродную электрохимическую ячейку со стеклоуглеродным электродом и хлоридсеребряным электродом сравнения [в насыщенном хлориде калия (KCl), соединенным с ячейкой электролитическим ключом, заполненным нитратом калия (KNO3)], емкостью 10 мл, помещают 5 мл фонового раствора - содержащего 0,5 мл 0,1 М этилендиаминтетраацетата натрия (ЭДТА) и 4,5 мл 1 М нитрата калия (KNO3). Содержание в фоновом растворе ЭДТА выбирается в соответствии с максимальным сигналом серебра и простотой измерений (табл. 1, рис. 1). Оптимальным фоновым раствором для определения серебра является фон 0,5 мл 0,1 М ЭДТА и 4,5 мл 1 М KNO3, в котором значение тока пика не достигает максимума, как в фоновом растворе 1,0 мл 0,1 М ЭДТА и 4,0 мл 1 М KNO3 (табл. 2, рис. 2), но полуширина пика меньше, что упрощает измерения.
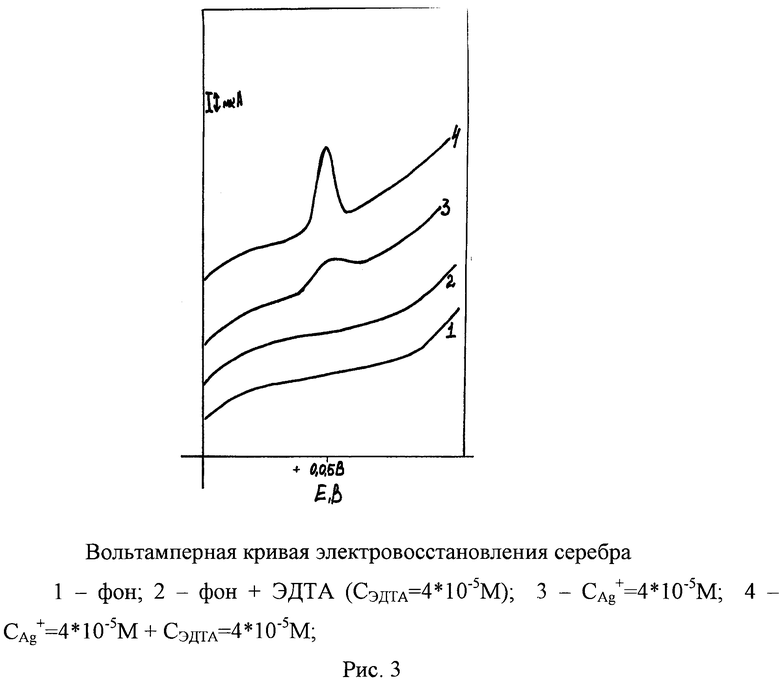
Отсутствие аналитических сигналов свидетельствует о чистоте фонового электролита. Затем в фон вводят пробу, содержащую серебро или модельный раствор (0.02 мл стандартного раствора серебра от 1·10-5 М до 1·10-2 М, при этом концентрация серебра в ячейке составляет от 4·10-8 М до 4·10-5 М, и перемешивают в течение 10-30 с. На индикаторный электрод подают потенциал предварительного электролиза (+0,5 В), так как при этом потенциале регистрируется максимальное значение тока пика, в течение времени накопления от 10 с до 20 с проводят электроконцентрирование определяемого вещества на электроде при потенциале от +0,04 В до +0,07 В и скорости развертки потенциала 100 мВ/с, регистрируют ток пика (Рис. 3), линейно зависящим от концентрации серебра в водных растворах (табл. 3, Рис. 4). Содержание серебра оценивают методом стандартных добавок. Нижняя граница определяемых концентраций серебра в присутствии ЭДТА 2,8·10-8 М (Sr=0,20).
Способ определения серебра позволяет на 2-3 порядка снизить нижнюю границу определяемых содержаний до 2,8·10-8 М (Sr=0,20). Измерение аналитического сигнала проходит в одну стадию, что ускоряет процесс определения концентрации серебра.

Зависимость тока восстановления серебра при различной концентрации комплексона III в растворе (рис. 1.)

Зависимость величины тока восстановления серебра при разных значениях концентрации комплексона III в растворе (рис. 2.)
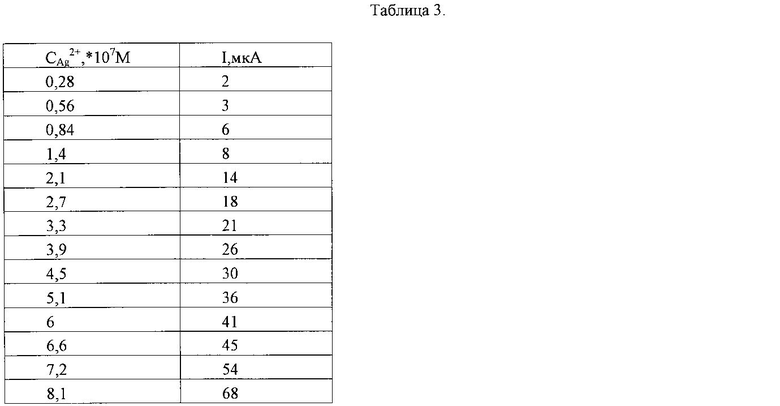
Величина тока восстановления серебра при различной концентрации серебра (I) (рис. 4.)
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ МОЛИБДЕНА КАТОДНОЙ ВОЛЬТАМПЕРОМЕТРИЕЙ | 2013 |
|
RU2533333C1 |
| Способ определения иодид-ионов катодной вольтамперометрией | 2016 |
|
RU2645003C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ РТУТИ КАТОДНО-АНОДНОЙ ВОЛЬТАМПЕРОМЕТРИЕЙ | 2013 |
|
RU2533337C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ Т-2 ТОКСИНА МЕТОДОМ ДИФФЕРЕНЦИАЛЬНОЙ ВОЛЬТАМПЕРОМЕТРИИ | 2015 |
|
RU2580412C1 |
| ВОЛЬТАМПЕРОМЕТРИЧЕСКИЙ СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ КАРБОСУЛЬФАНА В МОДЕЛЬНЫХ РАСТВОРАХ | 2023 |
|
RU2803061C1 |
| Способ определения тиолов | 2015 |
|
RU2613053C1 |
| СПОСОБ ИНВЕРСИОННО-ВОЛЬТАМПЕРОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ ПЛАТИНЫ В НИТРИТНОЙ СРЕДЕ | 2011 |
|
RU2484455C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ЙОДА | 2002 |
|
RU2206086C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ПОТЕНЦИАЛЬНОГО ПРОТИВООПУХОЛЕВОГО СРЕДСТВА -ЭТИЛ 6-НИТРО-7-(4"-НИТРОФЕНИЛ)-5-ЭТИЛ-4,7-ДИГИДРОПИРАЗОЛО[1,5-А]ПИРИМИДИН-3-КАРБОКСИЛАТА- МЕТОДОМ ВОЛЬТАМПЕРОМЕТРИИ | 2022 |
|
RU2802831C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ЦИСТЕИНА В ВОДНЫХ РАСТВОРАХ МЕТОДОМ ЦИКЛИЧЕСКОЙ ВОЛЬТАМПЕРОМЕТРИИ НА ГРАФИТОВОМ ЭЛЕКТРОДЕ, МОДИФИЦИРОВАННОМ КОЛЛОИДНЫМИ ЧАСТИЦАМИ ЗОЛОТА | 2011 |
|
RU2463587C1 |


Изобретение относится к области аналитической химии. Согласно изобретению предложен способ определения серебра катодной вольтамперометрией из фонового раствора, содержащего 4,5 мл 1 М KNO3 и 0,5 мл 0,1 М этилендиаминтетраацетата натрия (ЭДТА), из образующегося комплексного соединения на стеклоуглеродном электроде. При этом на индикаторный электрод подают потенциал предварительного электролиза (+0,5 В), при котором регистрируется максимальное значение тока пика, и в течение времени накопления от 10 с до 20 с проводят электроконцентрирование определяемого вещества на электроде, регистрируют ток пика при потенциале от +0,04 В до +0,07 В и скорости развертки потенциала 100 мВ/с. Изобретение позволяет на 2-3 порядка снизить нижнюю границу определяемых содержаний до 2,8·10-8 М (Sr=0,20), а также поскольку измерение аналитического сигнала проходит в одну стадию, то это ускоряет процесс определения концентрации серебра. 4 ил, 3 табл.
Способ определения серебра катодной вольтамперометрией, включающий в себя определение серебра из фонового раствора, содержащего в качестве одного из компонентов KNO3, на стеклоуглеродном электроде, отличающийся тем, что в фоновый раствор, содержащий 4,5 мл 1М KNO3, добавляют 0,5 мл 0,1М этилендиаминтетраацетата натрия (ЭДТА), выдерживают потенциал электролиза +0,5 В от 10 с до 20 с и определяют концентрацию серебра из образующегося комплексного соединения.
| ВОЛЬТАМПЕРОМЕТРИЧЕСКИЙ СПОСОБ ОПРЕДЕЛЕНИЯ СЕРЕБРА В ВОДНЫХ СРЕДАХ | 2007 |
|
RU2330274C1 |
| Способ потенциометрического определения серебра в тиосульфатных растворах | 1989 |
|
SU1711065A1 |
| Способ определения серебра в кинофотоматериалах | 1986 |
|
SU1460657A1 |
| Способ потенциометрического определения микрограммовых концентраций ионов серебра в воде | 1981 |
|
SU1081517A1 |
| JP2009025217A, 05.02.2009. | |||
Авторы
Даты
2016-04-10—Публикация
2014-12-15—Подача