ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к выгодному промышленному способу получения 1,3-диметиладамантана приведенной ниже формулы (2) из пергидроаценафтена приведенной ниже формулы (1) с применением HF·BF3 в качестве катализатора.
[уравнение реакции 1]

ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Ожидается, что 1,3-диметиладамантан окажется полезным в качестве исходного соединения для получения продуктов тонкого органического синтеза различных типов, в т.ч. фармацевтических препаратов, кроме того, ожидается, что полученные из него дикарбоновая кислота и диол найдут применение при получении полимерных материалов с полезными функциональными свойствами.
В литературе известного уровня техники, в патентном документе 1 описано гидрирование аценафтена приведенной ниже формулы (3) с получением пергидроаценафтена (который ниже по тексту может именоваться просто «PHA») приведенной ниже формулы (1), включающего четыре типа пространственных изомеров.
[уравнение реакции 2]
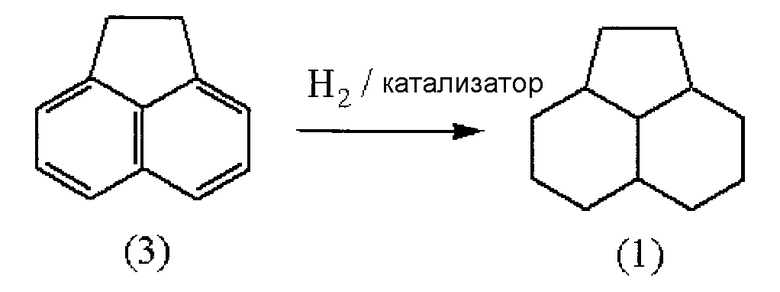
В патентном документе 2 раскрыт способ получения 1,3-диметиладамантана из PHA с применением цеолитного катализатора, в котором осуществлен ионный обмен Ca и La и содержатся Pt и Re, в присутствии H2 и HCl. Однако недостаток данного способа получения 1,3-диметиладамантана из PHA заключается в низком выходе, составляющем всего 38,7%, и в высокой стоимости входящих в состав катализатора Pt и Re.
Известна методика получения незамещенного адамантана, в которой в качестве исходного вещества применяется тетрагидродициклопентадиен, а катализатором является HF·BF3 (смотрите, например, патентные документы 3 и 4). Однако до сих пор не был известен способ селективного получения 1,3-диметиладамантана с высоким выходом с применением HF·BF3 в качестве катализатора.
Что касается получения 1,3-диметиладамантана с помощью кислотного катализатора, известен способ, в котором применяется хлорид алюминия. Однако для получения 1,3-диметиладамантана с высоким выходом в качестве компонента катализатора необходимо применять 1,2-дихлорэтан, который является дорогостоящим. Кроме того, хлорид алюминия невозможно использовать повторно, поэтому появляются значительные количества отходов, образовавшихся из хлорида алюминия. По этим причинам способ с применением хлорида алюминия является невыгодным с промышленной точки зрения (патентный документ 5).
СПИСОК ИСПОЛЬЗОВАННОЙ ЛИТЕРАТУРЫ
ПАТЕНТНАЯ ЛИТЕРАТУРА
Патентный документ 1: Патентная публикация Японии, выложенная в открытый доступ № Sho-62-265238.
Патентный документ 2: Патентная публикация Японии, выложенная для опротестования № Sho-52-2909.
Патентный документ 3: Патентная публикация Японии, выложенная для опротестования № Sho-52-38935.
Патентный документ 4: Патентная публикация Японии, выложенная в открытый доступ № 2001-151705.
Патентный документ 5: Патентная публикация Японии, выложенная для опротестования № Hei-4-37052.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Техническая проблема
Проблема, которую предполагалось решить в настоящем изобретении, заключалась в разработке способа получения 1,3-диметиладамантана с высоким выходом без применения дорогостоящего катализатора и с возможностью регенерации применяемого катализатора, что позволило бы преодолеть описанные выше недостатки известного уровня техники.
Решение проблемы
В результате накопления данных интенсивных исследований реакции изомеризации, в которой 1,3-диметиладамантан получали из исходного пергидроаценафтена, авторы настоящего изобретения обнаружили выгодный способ промышленного получения 1,3-диметиладамантана с высоким выходом, в котором реакцию проводят в не жестких условиях, без необходимости присутствия растворителя, причем HF·BF3 является эффективным катализатором, пригодным для неоднократного использования, что позволило добиться цели изобретения.
Конкретно, настоящее изобретение направлено на следующее.
1. Способ получения 1,3-диметиладамантна приведенной ниже формулы (2) путем осуществления реакции скелетной изомеризации пергидроаценафтена приведенной ниже формулы (1) с применением в качестве катализатора от 0,5 до 1,5 масс. частей HF и от 0,05 до 0,5 масс. частей BF3 на 1 масс. часть пергидроаценафтена при температуре от 60 до 110°C.
[уравнение реакции 3]

2. Способ получения 1,3-диметиладамантана по п.1, где HF и BF3, выделенные из раствора продукта реакции, повторно применяются для проведения реакции.
3. Способ получения 1,3-диметиладамантана по п.1 или 2, где слой катализатора, отделенный от раствора продукта реакции в результате разделения двух жидких фаз, подают в дистилляционную колонну, в которой циркулирует как минимум один углеводород, выбранный из группы, состоящей из бензола, толуола, гексана и гептана, что позволяет регенерировать BF3 и HF и повторно применить BF3 и HF для проведения реакции.
4. Способ получения 1,3-диметиладамантана по любому из пп.1-3, где температура проведения реакции составляет от 60 до 90°C.
5. Способ получения 1,3-диметиладамантана по любому из пп.1-3, где температура проведения реакции составляет от 80 до 105°C.
ПОЛЕЗНЫЕ ЭФФЕКТЫ ОТ ИЗОБРЕТЕНИЯ
В способе по настоящему изобретению не применяется растворитель. Поэтому нет необходимости в проведении стадии удаления растворителя и выделения из него полученного вещества. Кроме того, не требуется применения дорогостоящего катализатора, а применяемый катализатор можно регенерировать. Таким образом, 1,3-диметиладамантан можно получать с высоким выходом и экономической выгодой при уменьшении воздействия на окружающую среду.
ОПИСАНИЕ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Далее по тексту заявки будет приведено подробное описание изобретения. Способ по настоящему изобретению представляет собой способ получения 1,3-диметиладамантана из пергидроаценафтена в качестве исходного вещества с применением HF·BF3 в качестве катализатора без применения растворителя. В настоящем описании формула “HF·BF3” указывает на состояние, когда HF и BF3 совместно присутствуют в реакционной системе, причем это состояние может быть представлено обозначениями HF-BF3, HF/BF3 или HF:BF3. Ведущим исследователем в области сильных кислот является George A. Olah, и в книге George A. Olah et al., “SUPERACIDS” на стр. 51 указано, что HF·BF3 в реакционной системе находится в состоянии показанного ниже равновесия.
[Уравнение реакции 4]

Имеется четыре типа пространственных изомеров PHA. Эти изомеры применяются в качестве исходного вещества в способе по настоящему изобретению независимо или в виде смесей. PHA можно получать известным способом, описанным в технике.
HF, который является одним из компонентов катализатора, применяют в количестве от 0,5 до 1,5 частей по массе, предпочтительно в количестве от 0,5 до 0,7 частей по массе на 1 часть по массе исходного PHA. Если применять HF в количестве менее 0,5 частей по массе, выход 1,3-диметиладамантана снизится. Если применять HF в количестве более 1,5 частей по массе, то выход 1,3-диметиладамантана будет высоким, но при слишком большом количестве HF будет сложнее осуществлять выделение и регенерацию HF, что нецелесообразно в промышленных условиях.
BF3 применяют в количестве от 0,05 до 0,5 частей по массе, предпочтительно в количестве от 0,1 до 0,2 частей по массе, на одну часть по массе исходного PHA. Если применять BF3 в количестве менее 0,05 масс. частей, реакция изомеризации не проходит достаточно эффективно, в результате чего снижаются селективность и выход 1,3-диметиладамантана. Если применять BF3 в количестве более 0,5 частей по массе, выход адамантана повышается, но образуется значительное количество соединения с высокой температурой кипения. С точки зрения легкости проведения стадии разделения и очистки применение такого количества BF3 нецелесообразно в промышленных условиях. Кроме того, давление в реакционной смеси становится слишком высоким, что представляет собой проблему при промышленном производстве.
Фактический выход 1,3-диметиладамантана можно повысить путем регенерации и повторного использования 1-этиладамантана, который является интермедиатом реакции.
Для проведения реакции скелетной изомеризации по настоящему изобретению нет необходимости в применении растворителя.
Предпочтительная температура проведения реакции составляет 60°C или выше, 70°C или выше или 80°C или выше. Предпочтительная температура проведения реакции составляет 110°C или ниже, 105°C или ниже или 90°C или ниже. Например, предпочтительной является температура в диапазоне от 60°C до 110°C, в диапазоне от 60°C до 90°C, в диапазоне от 80°C до 105°C и т.п. Предпочтительный диапазон температуры проведения реакции не ограничен комбинацией этих температурных диапазонов. Если температура проведения реакции менее 60°C, реакция протекает слишком медленно. Если температура проведения реакции превышает 110°C, скорость реакции становится высокой, но при этом трудно управлять ходом реакции и повышается количество продуктов с высокой температурой кипения. В результате этого понижаются выход и селективность реакции, что является нежелательным.
Время проведения реакции, которое меняется в соответствии с количеством PHA или температурой реакции, составляет от 2 до 10 часов.
Предпочтительно, чтобы существовали средства для повторной подачи в реакционную емкость не вступившего в реакцию 1-этиладамантана, выделенного на стадии разделения и очистки. Если продукт реакции оставить стоять по окончании реакции, то реакционная смесь разделится на два слоя, а именно органический слой, содержащий адамантан, и слой катализатора, содержащий соединение с высокой температурой кипения, которое образуется в качестве побочного продукта. Таким образом, предпочтительно, чтобы имелись средства для отделения двух слоев жидкости друг от друга. В качестве альтернативы стадию регенерации катализатора можно также использовать для осуществления разделения двух слоев жидкости. В настоящей заявке «стадия регенерации катализатора» означает стадию извлечения HF и BF3 из реакционного раствора, полученного в результате реакции изомеризации. Стадию регенерации катализатора проводят следующим образом. Весь реакционный раствор или слой катализатора подают в дистилляционную колонну, в которой циркулирует углеводород. В результате HF, имеющий температуру кипения 20°C, отводят в жидкой форме из холодильника, расположенного в верхней части колонны, и BF3, который кипит при -100°C и не превращается в жидкость в холодильнике, находящемся в верхней части колонны, выводят в виде газа. Углеводородный раствор, содержащий 1,3-диметиладамантан, выводят из донной части колонны.
Раствор продукта реакции получают в виде жидкости, содержащей 1,3-диметиладамантан, 1-этиладамантан, т.е. интермедиат реакции, побочный продукт и HF·BF3. Если полученный раствор продукта реакции оставить стоять, он разделится на два слоя, а именно органический слой, содержащий 1,3-диметиладамантан, и слой катализатора, содержащий высококипящее соединение, образующееся в качестве побочного продукта. Таким образом, органический слой можно получить в результате разделения двух слоев жидкости. Отделенный слой катализатора подают в дистилляционную колонну, в которой осуществляется циркуляция углеводородов одного или нескольких типов, выбранных из группы, состоящей, например, из бензола, толуола, гексана, гептана и т.п. В результате BF3 можно выводить из верхней части колонны и HF можно выводить из холодильника, находящегося в верхней части колонны, причем BF3 и HF можно повторно применять в качестве катализаторов. Полученный органический слой нейтрализуют и промывают водой, затем его очищают перегонкой по обычной методике или другим подходящим способом. В результате можно получить 1,3-диметиладамантан.
В качестве альтернативы можно не оставлять стоять продукт реакции и, таким образом, не делить его на две фазы, а именно на органический слой, содержащий 1,3-диметиладамантан, и слой катализатора, содержащий высококипящее соединение, образовавшееся в качестве побочного продукта. Весь раствор продукта реакции можно подавать в описанную выше дистилляционную колонну, в которой осуществляется циркуляция углеводорода. В этом случае BF3 также можно выводить из верхней части колонны и HF можно выводить из холодильника, находящегося в верхней части колонны, причем BF3 и HF можно повторно применять в качестве катализаторов. Углеводородный раствор, содержащий 1,3-диметиладамантан, можно выводить из донной части колонны. Количество углеводорода, применяемого в данном способе, составляет от 1,5 до 3 частей по массе на 1 часть по массе образовавшегося 1,3-диметиладамантана.
Полученный углеводородный раствор, содержащий 1,3-диметиладамантан, нейтрализуют и промывают водой, затем подвергают перегонке по обычной методике или очищают другим способом. Таким образом можно получить 1,3-диметиладамантан.
ПРИМЕРЫ
Далее по тексту настоящее изобретение будет конкретно описано с привлечением примеров. Настоящее изобретение не ограничено приведенными ниже примерами. Продукты реакции анализировали с помощью газового хроматографа (прибора ГХ) в следующих условиях.
Прибор: GC-17A (производства Shimadzu Corporation).
Колонка: HR-1 (производства Shinwa Chemical Industries, Ltd.).
Условия анализа: Температура впрыска 310°C; Температура детектора 310°C.
Температура колонки: 100°C в течение 0 минут, затем повышали температуру до 300°C со скоростью 5°C/мин, затем выдерживали при 300°C в течение 5 минут.
Детектор: пламенно-ионизационный детектор (FID).
Методика: Раствор продукта реакции экстрагировали в полипропиленовой емкости, содержавший дистиллированную воду. Количество дистиллированной воды должно быть достаточным для поглощения HF, образовавшегося в реакции. Раствор продукта реакции оставляли стоять, чтобы получить органический слой в результате разделения жидких фаз. Органический слой один раз промывали 2% водным раствором гидроксида натрия (гидроксид натрия: производства Wako Pure Chemical Industries, Ltd.; вода: дистиллированная вода) и один раз дистиллированной водой. К 0,2 г полученного органического слоя добавляли 0,1 г дибензила, который применяли в качестве внутреннего стандарта (производства Wako Pure Chemical Industries, Ltd.). Полученную смесь разбавляли гептаном и затем помещали в устройство для газовой хроматографии.
Пример 1
Изомеризацию PHA проводили в автоклаве Hastelloy, который имел емкость 0,5 л и был снабжен электромагнитной мешалкой, нагревателем, входом для подачи газа и жидкости и выходом для отведения продукта реакции. В реактор помещали 50 г (2,5 моль) HF производства Morita Chemical Industries Co., LTD и 100 г (0,6 моль) PHA и подавали 16 г (0,24 моль) BF3 производства Stella Chemifa Corporation. После этого смесь веществ без растворителя нагревали до температуры 100°C с помощью нагревателя и перемешивали в течение 4 часов, поддерживая температуру на уровне 100°C. Отбирали образец продукта реакции. Выход 1,3-диметиладамантана составлял 77% по отношению к исходному PHA. Выход интермедиата, т.е. 1-этиладамантана, составлял 15% относительно PHA, и высококипящее соединение в реакционной смеси обнаружено не было. Затем реакционную смесь оставляли стоять, и она разделялась на два слоя, а именно органический слой, содержащий 1,3-диметиладамантан, и слой катализатора. Слой катализатора отделяли, осуществляя разделение двух жидких слоев. Выделенный слой катализатора подавали на дистилляционную колонну, в которой циркулировал гептан. В результате почти все введенное в реакцию количество BF3 выводили из верхней части колонны и почти все введенное в реакцию количество HF выводили из холодильника, расположенного в верхней части колонны.
Пример 2
Реакцию проводили практически в тех же условиях, что и в примере 1, за исключением того, что использовали HF и BF3, регенерированные в примере 1. Выход 1,3-диметиладамантана составил 75%, и дезактивации катализатора не наблюдалось. Как и в примере 1, высококипящее соединение в реакционной смеси обнаружено не было.
Пример 3
Реакцию изомеризации PHA проводили в автоклаве Hastelloy, который имел емкость 0,5 л и был снабжен электромагнитной мешалкой, нагревателем, входом для подачи газа и жидкости и выходом для отведения продукта реакции. В реактор помещали 50 г (2,5 моль) HF производства Morita Chemical Industries Co., LTD и 100 г (0,6 моль) PHA и подавали 16 г (0,24 моль) BF3 производства Stella Chemifa Corporation. После этого смесь веществ без растворителя нагревали до температуры 80°C с помощью нагревателя и перемешивали в течение 4 часов, поддерживая температуру на уровне 80°C. Отбирали образец продукта реакции. Выход 1,3-диметиладамантана составлял 51% по отношению к исходному PHA. Выход интермедиата, т.е. 1-этиладамантана, составлял 42% относительно PHA, и высококипящее соединение в реакционной смеси обнаружено не было. Затем реакционную смесь оставляли стоять, в результате чего она разделялась на два слоя, а именно органический слой, содержащий 1,3-диметиладамантан, и слой катализатора. Слой катализатора отделяли, осуществляя разделение двух жидких слоев. Выделенный слой катализатора подавали на дистилляционную колонну, в которой циркулировал гептан. В результате почти все введенное в реакцию количество BF3 выводили из верхней части колонны и почти все введенное в реакцию количество HF выводили из холодильника, расположенного в верхней части колонны.
Пример 4
Реакцию проводили практически в тех же условиях, что и в примере 3, за исключением того, что использовали HF и BF3, регенерированные в примере 3. Выход 1,3-диметиладамантана составил 51%, и дезактивации катализатора не наблюдалось. Как и в примере 3, высококипящее соединение в реакционной смеси обнаружено не было.
Сравнительный пример 1
Реакцию проводили практически в тех же условиях, что и в примере 1, за исключением того, что температура проведения реакции составляла 50°C. Выход 1,3-диметиладамантана составил лишь 32%.
Сравнительный пример 2
Реакцию проводили практически в тех же условиях, что и в примере 1, за исключением того, что температура проведения реакции составляла 130°C. Выход 1,3-диметиладамантана составил 63%, но образовалось 15% соединения с высокой температурой кипения, что было нежелательно.
ПРОМЫШЛЕННАЯ ПРИМЕНИМОСТЬ
В способе по настоящему изобретению не применяется растворитель. Поэтому нет необходимости в проведении стадии удаления растворителя и выделения из него полученного вещества. Кроме того, для проведения реакции не требуется применения дорогостоящего катализатора, а применяемый катализатор можно регенерировать и применить повторно. 1,3-диметиладамантан можно получать с высоким выходом и экономической выгодой при уменьшении воздействия на окружающую среду.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ГОМОЛОГОВ АДАМАНТАНА | 1969 |
|
SU239302A1 |
| СПОСОБ ПОЛУЧЕНИЯ АДАМАНТАНА | 2009 |
|
RU2494084C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1,3-ДИМЕТИЛАДАМАНТАНА | 2012 |
|
RU2504533C1 |
| 4-(4-АЛКИЛЦИКЛОГЕКСИЛ)БЕНЗАЛЬДЕГИД | 2007 |
|
RU2446141C2 |
| Способ получения алкиладамантанов | 1973 |
|
SU476246A1 |
| 1,3,5,7-ТЕТРААЛКИЛАДАМАНТАНЫ В КАЧЕСТВЕ НОВЫХ ПРОИЗВОДНЫХ АДАМАНТАНА, СПОСОБ ПОЛУЧЕНИЯ 1,3,5,7-ТЕТРААЛКИЛАДАМАНТАНОВ И МОДИФИКАЦИИ СМЕСЕЙ ПОЛИАЛКИЛАДАМАНТАНОВ | 2008 |
|
RU2409545C2 |
| СПОСОБ ПОЛУЧЕНИЯ 2,6-ДИМЕТИЛ-1-НАФТАЛЬДЕГИДА | 2007 |
|
RU2440967C2 |
| СПОСОБ ПОЛУЧЕНИЯ БИСФЕНОЛА А ВЫСОКОЙ ЧИСТОТЫ И ПРОИЗВОДСТВЕННАЯ УСТАНОВКА | 2007 |
|
RU2422429C2 |
| СПОСОБ ПОЛУЧЕНИЯ 4,4'-ДИФОРМИЛДИФЕНИЛАЛКАНА | 2012 |
|
RU2575126C2 |
| СПОСОБ ПРЕВРАЩЕНИЯ ЭТИЛБЕНЗОЛА И СПОСОБ ПОЛУЧЕНИЯ ПАРА-КСИЛОЛА | 2007 |
|
RU2448937C2 |
Изобретение относится к способу получения 1,3-диметиладамантана приведенной ниже формулы (2) путем осуществления реакции скелетной изомеризации пергидроаценафтена приведенной ниже формулы (1) с применением в качестве катализаторов от 0,5 до 1,5 масс. частей HF и от 0,1 до 0,5 масс. частей BF3 на 1 масс. часть пергидроаценафтена при температуре от 60 до 110°С. Использование предлагаемого способа позволяет получать 1,3-диметиладамантан с высоким выходом. 4 з.п. ф-лы, 4 пр.
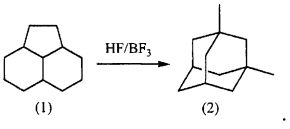
1. Способ получения 1,3-диметиладамантана приведенной ниже формулы (2) путем осуществления реакции скелетной изомеризации пергидроаценафтена приведенной ниже формулы (1) с применением в качестве катализаторов от 0,5 до 1,5 масс. частей HF и от 0,1 до 0,5 масс. частей BF3 на 1 масс. часть пергидроаценафтена при температуре от 60 до 110°С:

2. Способ получения 1,3-диметиладамантана по п. 1, где HF и BF3, выделенные из раствора продукта реакции, повторно применяются для проведения реакции.
3. Способ получения 1,3-диметиладамантана по п. 2, где слой катализатора, отделенный от раствора продукта реакции путем разделения двух жидких фаз, подают в дистилляционную колонну, в которой циркулирует как минимум один углеводород, выбранный из группы, состоящей из бензола, толуола, гексана и гептана, за счет чего осуществляется регенерация BF3 и HF и повторное применение BF3 и HF для проведения реакции.
4. Способ получения 1,3-диметиладамантана по любому из пп. 1-3, где температура проведения реакции находится в диапазоне от 60 до 90°С.
5. Способ получения 1,3-диметиладамантана по любому из пп. 1-3, где температура проведения реакции находится в пределах от 80 до 105°С.
| US 3275700 A, 27.09.1966 | |||
| JP 63159330 A, 02.07.1988 | |||
| СПОСОБ ПОЛУЧЕНИЯ ГОМОЛОГОВ АДАМАНТАНА | 0 |
|
SU239302A1 |
Авторы
Даты
2016-04-10—Публикация
2011-11-08—Подача