РОДСТВЕННАЯ ЗАЯВКА
В настоящей заявке заявляется приоритет по предварительной заявке на патент США 61/496351, озаглавленной «Антитела против G-CSFR и их применение», поданной 13 июня 2011 года, полное содержание которой включено в настоящий документ посредством ссылки.
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
Настоящая заявка подана вместе с перечнем последовательностей в электронном формате. Полное содержание перечня последовательностей включено в настоящий документ посредством ссылки.
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее описание относится к антителам, которые связываются с рецептором гранулоцитарного колониестимулирующего фактора (G-CSFR), и их применению, например, в терапии.
УРОВЕНЬ ТЕХНИКИ
Гранулоцитарный колониестимулирующий фактор (G-CSF) представляет собой основной регулятор продуцирования гранулоцитов. G-CSF продуцируется стволовыми клетками костного мозга, эндотелиальными клетками, макрофагами и фибробластами, а продуцирование инициируется воспалительными стимулами. G-CSF действует через рецептор G-CSF (G-CSFR), который экспрессируется на ранних миелоидных предшественниках, зрелых нейтрофилах, моноцитах/макрофагах, Т - и В-лимфоцитах и эндотелиальных клетках. Мыши с недостатком G-CSF или G-CSFR демонстрируют заметную нейтропению, показывая важность G-CSF в устойчивом гранулопоэзе. Однако G-CSF является несущественным для экстренного гранулопоэза, например, в ответ на инфекцию. G-CSF повышает продуцирование и высвобождение нейтрофилов, мобилизует гематоэтические стволовые клетки и клетки-предшественники, а также модулирует дифференцировку, продолжительность жизни и эффекторные функции зрелых нейтрофилов. G-CSF также может оказывать влияние на макрофаги, включая увеличение количество моноцитов/макрофагов, усиление фагоцитарной функции и регуляцию продуцирования воспалительных цитокинов и хемокинов. Было также показано, что G-CSF мобилизует эндотелиальные клетки-предшественники и вызывает или ускоряет ангиогенез.
Хотя G-CSF используют терапевтически, например, для лечения нейтропении и/или для мобилизации гематопоэтических стволовых клеток, он также обладает негативным действием при некоторых состояниях, например, воспалительных состояниях и/или раке. Например, введение G-CSF обостряет ревматоидный артрит (RA), мышиный коллаген-индуцированный артрит (CIA) и модель пассивного переноса CIA на крысах. G-CSF также был обнаружен в сыворотке и синовиальной жидкости пациентов с RA. Более того, интерлейкин (IL)-l и фактор некроза опухоли a (TNFa), которые обнаружены в повышенных концентрациях у пациентов, страдающих от RA, вызывают продуцирование G-CSF человеческими синовиальными фибробластами и хондроцитами. Мыши с недостатком G-CSF резистентны к индуцированию острого и хронического воспалительного артрита.
Было также показано, что G-CSF играет роль в рассеянном склерозе (MS). Например, G-CSF усиливает адгезию в модели MS с аутореактивной линией Т-клеток к внеклеточному матриксу так же эффективно, как интерферон у и TNFa, которые, как известно, обостряют симптомы MS. Более того, мыши с недостатком G-CSF являются резистентными к развитию экспериментального аутоиммунного энцефаломиелита (ЕАЕ).
G-CSF и G-CSFR также связаны с раком, и исследования показывают, что этот сигнальный путь способствует резистентности к химиотерапии, росту, выживанию, инвазивности и метастазу различных видов рака. Более того, было показано, что G-CSF вызывает ангиогенез, важный процесс при развитии солидных опухолей.
Специалистам в данной области из вышеизложенного понятно, что в данной области существует необходимость в реагентах, которые снижают передачу сигналов G-CSF через G-CSFR. Иллюстративные агенты пригодны для применения в качестве терапевтических средств, например, для лечения или предупреждения G-CSF-опосредованного состояния.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Авторы настоящего изобретения получили класс белков, содержащих связывающие сайты антитела (например. Fab и антитела), которые связываются с человеческим G-CSFR (hG-CSFR) и потенциально нейтрализуют передачу сигналов G-CSF, например, предотвращают образование гранулоцитов из клеток костного мозга CD34+ и/или предотвращают клеточную пролиферацию в ответ на G-CSF, и/или предотвращают нейтрофилию, вызванную введением G-CSF. Класс белков, установленный авторами настоящего изобретения, также перекрестно взаимодействует с G-CSFR яванского макака (cynoG-CSFR), что облегчает доклинические исследования этих белков. Класс белков, определенный авторами настоящего изобретения, связывается с hG-CSFR с высокой аффинностью. Класс белков, определенный авторами настоящего изобретения, представляет собой человеческие антитела, которые пригодны для лечения различных состояний.
В настоящем описании представлен белок, содержащий антигенсвязывающий сайт антитела, причем указанный антигенсвязывающий сайт связывается с hG-CSFR и нейтрализует передачу сигналов G-CSF, и при этом указанный белок ингибирует рост колониеобразующих единиц -гранулоцитов (CFU-G) из клеток костного мозга CD34+, выращенных в присутствии G-CSF, со значением IC50, по меньшей мере, около 0,2 нМ. Например, IC50 составляет 0,1 нМ или менее, например, 0,09 нМ или менее, или 0,08 нМ или менее, или 0,07 нМ или менее, или 0,06 нМ или менее, или 0,05 нМ или менее. В одном примере, IC50 составляет 0,04 нМ или менее. В другом примере, IC50 составляет 0,02 нМ или менее. Способы оценки IC50 белка в таком анализе описаны в настоящем документе. Например, IC50 определяют в присутствии 10 нг/мл hG-CSF.
В одном примере, IC50 определяют выращиванием клеток костного мозга CD34+ в присутствии 10 нг/мл фактора стволовых клеток и 10 нг/мл hG-CSF. Например, клетки выращивают в полутвердой клеточной культуральной среде. В одном примере, CFU-G подсчитывают через 14 дней выращивания.
В настоящем описании дополнительно или альтернативно представлен белок, содержащий антигенсвязывающий сайт антитела, причем указанный антигенсвязывающий сайт связывается с G-CSFR человека и яванского макака с одинаковой аффинностью и нейтрализует передачу сигналов G-CSF. Такие белки являются преимущественными, поскольку они облегчают доклинические исследования на млекопитающих, не являющихся человеком.
В одном примере, аффинность белка определяют с использованием биосенсора, например, резонансом поверхностного плазмона. Например, фиксируют лиганд-связывающую область или растворимый hG-CSFR, или растворимый cynoG-CSFR, или hG-CSFR-Fc, или cyno-G-CSFR-Fc, и определяют аффинность белка настоящего изобретения.
В настоящем изобретении дополнительно представлен белок, содержащий антигенсвязывающий сайт антитела, причем указанный антигенсвязывающий сайт специфически связывается с таким же эпитопом в hG-CSFR, который связывается С1.2 (содержащим вариабельную область тяжелой цепи (VH), содержащую последовательность, представленную в SEQ ID NO:2, и вариабельную область легкой цепи (VL), содержащую последовательность, представленную в SEQ ID NO:3) или C1.2G (содержащим VH, содержащую последовательность, представленную в SEQ ID NO:4) и VL, содержащую последовательность, представленную в SEQ ID NO:5).
В настоящем описании дополнительно или альтернативно представлен белок, содержащий антигенсвязывающий сайт антитела, причем (i) указанный белок конкурентно ингибирует связывание С1.2 (содержащего VH, содержащую последовательность, представленную в SEQ ID NO:2) и VL, содержащую последовательность, представленную в SEQ ID NO:3) или C1.2G (содержащего VH, содержащую последовательность, представленную в SEQ ID NO:4) и VL, содержащую последовательность, представленную в SEQ ID NO:5) с hG-CSFR;
(ii) указанный белок нейтрализует передачу сигналов G-CSF; и (iii) степень связывания указанного белка с полипептидом SEQ ID NO:1, в котором аланин замещен любым из:
(a) аргинина в положении 287 SEQ ID NO:1;
(b) гистидина в положении 237 SEQ ID NO:1;
(c) метионина в положении 198 SEQ ID NO:1;
(d) тирозина в положении 172 SEQ ID NO:1;
(e) лейцина в положении 171 SEQ ID NO:1; или
(f) лейцина в положении 111 SEQ ID NO:1
ниже, чем степень связывания указанного белка с полипептидом SEQ ID NO:1.
В настоящем описании дополнительно или альтернативно представлен белок, содержащий антигенсвязывающий сайт антитела, причем (i) указанный белок конкурентно ингибирует связывание С1.2 (содержащего VH, содержащую последовательность, представленную в SEQ ID NO:2) и VL, содержащую последовательность, представленную в SEQ ID NO:3) или C1.2G (содержащего VH, содержащую последовательность, представленную в SEQ ID NO:4) и VL, содержащую последовательность, представленную в SEQ ID NO:5) с hG-CSFR; (ii) указанный белок нейтрализует передачу сигналов G-CSF; и (iii) предпочтительно связывается с полипептидом SEQ ID NO:1 относительно его способности связываться с полипептидом SEQ ID NO:1, в котором аланин замещен любым из:
(a) аргинина в положении 287 SEQ ID NO:1;
(b) гистидина в положении 237 SEQ ID NO:1;
(c) метионина в положении 198 SEQ ID NO:1;
(d) тирозина в положении 172 SEQ ID NO:1;
(e) лейцина в положении 171 SEQ ID NO:1; или
(f) лейцина в положении 111 SEQ ID NO:1.
В настоящем описании дополнительно или альтернативно представлен белок, содержащий антигенсвязывающий сайт антитела, причем (i), указанный белок связывается с hG-CSFR; (Неуказанный белок нейтрализует передачу сигналов G-CSF; и (iii) степень связывания указанного белка с полипептидом SEQ ID NO:1, в котором аланин замещен любым из:
(a) аргинина в положении 287 SEQ ID NO:1;
(b) гистидина в положении 237 SEQ ID NO:1;
(c) метионина в положении 198 SEQ ID NO:1;
(d) тирозина в положении 172 SEQ ID NO:1;
(e) лейцина в положении 171 SEQ ID NO:1; или
(f) лейцина в положении 111 SEQ ID NO:1
ниже, чем степень связывания указанного белка с полипептидом SEQ ID NO:1.
В настоящем описании дополнительно или альтернативно представлен белок, содержащий антигенсвязывающий сайт антитела, причем (i), указанный белок связывается с hG-CSFR; (ii) указанный белок нейтрализует передачу сигналов G-CSF; и (iii) предпочтительно связывается с полипептидом SEQ ID NO:1 относительно его способности связываться с полипептидом SEQ ID NO:1, в котором аланин замещен любым из:
(a) аргинина в положении 287 SEQ ID NO:1;
(b) гистидина в положении 237 SEQ ID NO:1;
(c) метионина в положении 198 SEQ ID NO:1;
(d) тирозина в положении 172 SEQ ID NO:1;
(e) лейцина в положении 171 SEQ ID NO:1; или
(f) лейцина в положении 111 SEQ ID NO:1.
В одном примере, степень связывания белка с полипептидом, содержащим замещение аланина, снижена, по меньшей мере, приблизительно в 10 раз или 20 раз, или 50 раз, или 100 раз, или 150 раз, или 200 раз, по сравнению со связыванием указанного белка с полипептидом SEQ ID NO:1. Предпочтительно, степень связывания белка с полипептидом, содержащим замещение аланина, снижена, по меньшей мере, в 50 раз. Предпочтительно, степень связывания белка с полипептидом, содержащим замещение аланина, снижена, по меньшей мере, в 60 раз.
В одном примере, антигенсвязывающий сайт белка не связывается обнаруживаемым образом с полипептидом SEQ ID NO:1, в котором аланин замещен аргинином в положении 287 SEQ ID NO:1.
В одном примере, степень связывания оценивают с использованием биосенсора, например, резонансом поверхностного плазмона. Например, белок фиксируют и измеряют степень связывания с полипептидом SEQ ID NO:1 или с формой полипептида, содержащей замещение аланина.
Дополнительные формы полипептида, содержащего аминокислоты SEQ ID NO:1 с другими замещениями или без них, которые связываются или существенно не связываются, или не связываются обнаруживаемым образом, с белком настоящего описания, описаны в настоящем документе, и их следует использовать mutatis mutandis в примерах настоящего описания.
В одном примере, антиген-связывающий сайт перекрестие реагирует с:
(i) полипептидом SEQ ID NO:1, в котором аланин замещен лизином в положении 167 SEQ ID NO:1; и/или
(ii) полипептидом SEQ ID NO:1, в котором аланин замещен гистидином в положении 168 SEQ ID NO:1.
В одном примере, антигенсвязывающий сайт дополнительно перекрестие реагирует с полипептидом SEQ ID NO:1, в котором аланин замещен лейцином в положении 169 SEQ ID NO:1
В одном примере, белок конкурентно ингибирует связывание С1.2 (содержащего VH, содержащую последовательность, представленную в SEQ ID NO:2) и VL, содержащую последовательность, представленную в SEQ ID NO:3) или C1.2G (содержащего VH, содержащую последовательность, представленную в SEQ ID NO:4) и VL, содержащую последовательность, представленную в SEQ ID NO:5) с одним или более из:
(i) полипептида SEQ ID NO:1, в котором аланин замещен лизином в положении 167 SEQ ID NO:1; и/или
(ii) полипептида SEQ ID NO:1, в котором аланин замещен гистидином в положении 168 SEQ ID NO:1.
В одном примере, белок, описанный в настоящем документе по любому примеру, связывается с эпитопом, содержащим остатки в пределах одной или двух, или трех, или четырех областей, выбранных из 111-115, 170-176, 218-234 и/или 286-300 SEQ ID NO:1.
В одном примере, при связывании белка, описанного в настоящем документе по любому примеру, с полипептидом SEQ ID NO:1 и расщеплении при помощи протеолитических ферментов, остается связь с одним или двумя, или тремя, или четырьмя пептидами, содержащими или состоящими из аминокислот 111-115 SEQ ID NO:1 или аминокислот 170-176 SEQ ID NO:1, или аминокислот 218-234 SEQ ID NO:1, или аминокислот 286-300 SEQ ID NO:1.
В одном примере, белок связывается с конформационным эпитопом.
В настоящем описании дополнительно или альтернативно представлен белок, который связывается с hG-CSFR и нейтрализует передачу сигналов G-CSF, указанный белок содержит, по меньшей мере, одно из:
(i) VH, содержащей определяющую комплементарность область (CDR) 1, содержащую последовательность, представленную в SEQ ID NO:6, и CDR2, содержащую последовательность, представленную в SEQ ID NO:7 и CDR3, содержащую последовательность, по меньшей мере, приблизительно на 55% идентичную последовательности, представленной в SEQ ID NO:8;
(ii) VH, содержащей последовательность, по меньшей мере, приблизительно на 80%, такую как на 85%, или 90%, или 91%, или 92%, или 93%, или 94%, или 95%, или 96%, или 97%, или 98%, или 99% идентичную последовательности, представленной в SEQ ID NO:2 и/или 4;
(iii) VL, содержащей CDR1, содержащую последовательность, представленную в SEQ ID NO:9, и CDR2, содержащую последовательность, представленную в SEQ ID NO:10 и CDR3, содержащую последовательность, по меньшей мере, приблизительно на 33% идентичную последовательности, представленной в SEQ ID NO:11; и
(iv) VL, содержащей последовательность, по меньшей мере, приблизительно на 80%, такую как на 85%, или 90%, или 91%, или 92%, или 93%, или 94%, или 95%, или 96%, или 97%, или 98%, или 99% идентичную последовательности, представленной в SEQ ID NO:3 и/или 5.
Такой белок может содержать любую одну или более функциональных активностей, описанных в настоящем документе, например, предпочтительное связывание с полипептидом SEQ ID NO:1 относительно степени его связывания с полипептидом SEQ ID NO:1, в котором аланин замещен любым из:
(a) аргинина в положении 287 SEQ ID NO:1;
(b) гистидина в положении 237 SEQ ID NO:1;
(c) метионина в положении 198 SEQ ID NO:1;
(d) тирозина в положении 172 SEQ ID NO:1;
(e) лейцина в положении 171 SEQ ID NO:1; или
(f) лейцина в положении 111 SEQ ID NO:1.
В одном примере, процентная идентичность у (ii) составляет, по меньшей мере, около 95%.
В одном примере, процентная идентичность у (iv) составляет, по меньшей мере, около 94%.
В одном примере, различия между упомянутой последовательностью и белком заключаются в замещениях.
Специалисты в данной области могут определить сайты мутаций белка настоящего описания, например, в пределах каркасной области белка, содержащей вариабельную область. Более того, авторы настоящего изобретения идентифицировали многочисленные сайты в VH CDR3 и VL CDR3, которые могут быть мутированы, а также многочисленные мутации, которые сохраняют активность белка настоящего описания. Примером мутации является, например, замещение в пределах одного или более (например, 2 или 3, или 4) из четырех С-концевых остатков HCDR3 и/или одного или более (например, 2 или 3, или 4, или 5, или 6) из N-концевых или С-концевых остатков LCDR3. В одном примере, пять N-концевых аминокислот VH CDR3 представляют собой LGELG. В одном примере, три N-концевые аминокислоты CDR3 представляют собой QQS и/или три С-концевые аминокислоты VL CDR3 представляют собой PLT.
В одном примере, VH содержит CDR3, содержащий последовательность LGELGX1X2X3X4, причем:
X1 выбран из группы, состоящей из триптофана, глутамина, метионина, серина, фенилаланина, глутаминовой кислоты и гистидина, и/или представляет собой нейтральную аминокислоту, такую как триптофан, глутамин или метионин, например аминокислота, представляет собой триптофан;
X2 представляет собой аминокислоту, выбранную из группы, состоящей из фенилаланина, тирозина, метионина, серина, глицина и изолейцина, например, представляет собой фенилаланин, тирозин, метионин или серин, например, аминокислота представляет собой фенилаланин;
Х3 представляет собой аминокислоту, выбранную из группы, состоящей из аспарагиновой кислоты, метионина, глутамина, серина, лейцина, валина, аргинина и гистидина, например, представляет собой пролин, глутаминовую кислоту, аланин, лейцин, фенилаланин или тирозин, например аминокислота, представляет собой аспарагиновую кислоту; и
X4 представляет собой любую аминокислоту или аминокислоту, выбранную из группы, состоящей из пролина, глутаминовой кислоты, аланина, лейцина, фенилаланина, тирозина, треонина, аспарагина, аспарагиновой кислоты, серина, глицина, аргинина и лизина, например, аминокислота представляет собой пролин.
В одном примере, VL содержит CDR3, содержащий последовательность X1X2X3X4X5X6X7X8X9, причем:
X1 представляет собой аминокислоту, выбранную из группы, состоящей из глутамина, глутаминовой кислоты, гистидина, аланина и серина и/или представляет собой гидрофильную аминокислоту, такую как глутамин или глутаминовая кислота, например аминокислота, представляет собой глутамин;
Х2 представляет собой аминокислоту, выбранную из группы, состоящей из глутамина, валина, фенилаланина, аспарагина и глутаминовой кислоты, например аминокислота, представляет собой глутамин;
Х3 представляет собой аминокислоту, выбранную из группы, состоящей из серина и глицина, например, аминокислота представляет собой серин;
Х4 представляет собой аминокислоту, выбранную из группы, состоящей из триптофана, метионина, фенилаланина, тирозина, изолейцина и лейцина, например, аминокислота представляет собой триптофан или тирозин;
Х5 представляет собой любую аминокислоту или аминокислоту, выбранную из группы, состоящей из глутаминовой кислоты, метионина, глутамина, триптофана, серина, валина, аспарагина, глицина, аланина, аргинина, гистидина, тирозина, лизина и треонина, например, аминокислота представляет собой серии;
Х6 представляет собой аминокислоту, выбранную из группы, состоящей из тирозина, метионина, изолейцина и треонина, например, аминокислота представляет собой метионин, тирозин или треонин;
Х7 представляет собой аминокислоту, выбранную из группы, состоящей из пролина, аланина, гистидина, глицина и лизина, например, аминокислота представляет собой пролин;
X8 представляет собой аминокислоту, выбранную из группы, состоящей из лейцина, глутамина, метионина, аланина, фенилаланина, изолейцина, лизина, гистидина и глицина, например, аминокислота представляет собой лейцин;
Х9 представляет собой любую аминокислоту или аминокислоту, выбранную из группы, состоящей из треонина, фенилаланина, тирозина, метионина, лизина, серина, гистидина, пролина, триптофана, изолейцина, глутамина, глицина и валина, например, аминокислота представляет собой треонин.
В настоящем описании дополнительно или альтернативно представлен белок (например, антитело), который связывается с hG-CSFR и нейтрализует передачу сигналов G-CSF, указанный белок содержит, по меньшей мере, одну вариабельную область антитела, выбранную из группы, состоящей из:
(i) VH, содержащей аминокислотную последовательность, представленную в SEQ ID NO:2;
(ii) VL, содержащей аминокислотную последовательность, представленную в SEQ ID NO:3;
(iii) VH, содержащей аминокислотную последовательность, представленную в SEQ ID NO:4;
(iv) VL, содержащей аминокислотную последовательность, представленную в SEQ ID NO:5;
(v) VL, содержащей аминокислотную последовательность, представленную в SEQ ID NO:14;
(vi) VH, содержащей аминокислотную последовательность, представленную в SEQ ID NO:15;
(vii) VL, содержащей аминокислотную последовательность, представленную в SEQ ID NO:16;
(viii) VL, содержащей аминокислотную последовательность, представленную в SEQ ID NO:17;
(ix) VL, содержащей аминокислотную последовательность, представленную в SEQ ID NO:18;
(х) VL, содержащей аминокислотную последовательность, представленную в SEQ ID NO:19;
(xi) VH, содержащей аминокислотную последовательность, представленную в SEQ ID NO:20;
(xii) VL, содержащей аминокислотную последовательность, представленную в SEQ ID NO:21;
(xiii) VL, содержащей аминокислотную последовательность, представленную в SEQ ID NO:22;
(xiv) VL, содержащей аминокислотную последовательность, представленную в SEQ ID NO:23;
(xv) VH, содержащей аминокислотную последовательность, представленную в SEQ ID NO:24;
(xvi) VL, содержащей аминокислотную последовательность, представленную в SEQ ID NO:25;
(xvii) VL, содержащей аминокислотную последовательность, представленную в SEQ ID NO:26;
(xviii) VL, содержащей аминокислотную последовательность, представленную в SEQ ID NO:27;
(xix) VH, содержащей аминокислотную последовательность, представленную в SEQ ID NO:28;
(хх) VL, содержащей аминокислотную последовательность, представленную в SEQ ID NO:29;
(xxi) VL, содержащей аминокислотную последовательность, представленную в SEQ ID NO:30;
(xxii) VH, содержащей аминокислотную последовательность, представленную в SEQ ID NO:31;
(xxiii) VL, содержащей аминокислотную последовательность, представленную в SEQ ID NO:32;
(xxiv) VH, содержащей аминокислотную последовательность, представленную в SEQ ID NO:33;
(xxv) VL, содержащей аминокислотную последовательность, представленную в SEQ ID NO:34;
(xxvi) VL, содержащей аминокислотную последовательность, представленную в SEQ ID NO:35;
(xxvii) VH, содержащей аминокислотную последовательность, представленную в SEQ ID NO:36;
(xxviii) VL, содержащей аминокислотную последовательность, представленную в SEQ ID NO:37;
(xxix) VH, содержащей аминокислотную последовательность, представленную в SEQ ID NO:38;
(ххх) VL, содержащей аминокислотную последовательность, представленную в SEQ ID NO:39;
(xxxi) VH, содержащей аминокислотную последовательность, представленную в SEQ ID NO:40;
(xxxii) VL, содержащей аминокислотную последовательность, представленную в SEQ ID NO:41;
(xxxiii) VH, содержащей аминокислотную последовательность, представленную в SEQ ID NO:42;
(xxxiv) VL, содержащей аминокислотную последовательность, представленную в SEQ ID NO:43;
(xxxv) VL, содержащей аминокислотную последовательность, представленную в SEQ ID NO:44;
(xxxvi) VH, содержащей аминокислотную последовательность, представленную в SEQ ID NO:45;
(xxxvii) VL, содержащей аминокислотную последовательность, представленную в SEQ ID NO:46;
(xxxviii) VL, содержащей аминокислотную последовательность, представленную в SEQ ID NO:47;
(xxix) VL, содержащей аминокислотную последовательность, представленную в SEQ ID NO:48;
(xl) VH, содержащей аминокислотную последовательность, представленную в SEQ ID NO:49;
(xli) VL, содержащей аминокислотную последовательность, представленную в SEQ ID NO:50;
(xlii) VH, содержащей аминокислотную последовательность, представленную в SEQ ID NO:51;
(xliii) VL, содержащей аминокислотную последовательность, представленную в SEQ ID NO:52;
(xliv) VH, содержащей аминокислотную последовательность, представленную в SEQ ID NO:53;
(xlv) VL, содержащей аминокислотную последовательность, представленную в SEQ ID NO:54;
(xlvi) VH, содержащей аминокислотную последовательность, представленную в SEQ ID NO:55;
(xlvii) VL, содержащей аминокислотную последовательность, представленную в SEQ ID NO:56;
(xlviii)VH, содержащей аминокислотную последовательность, представленную в SEQ ID NO:57;
(xlix) VL, содержащей аминокислотную последовательность, представленную в SEQ ID NO:58;
(1) VH, содержащей аминокислотную последовательность, представленную в SEQ ID NO:59;
(li) VL, содержащей аминокислотную последовательность, представленную в SEQ ID NO:60;
(lii) VH, содержащей аминокислотную последовательность, представленную в SEQ ID NO:61;
(liii) VL, содержащей аминокислотную последовательность, представленную в SEQ ID NO:62; и
(liv) VL, содержащей аминокислотную последовательность, представленную в SEQ ID NO:63.
В одном примере, белок, описанный в настоящем документе, содержит, по меньшей мере, VH и VL, причем указанные VH и VL связываются с образованием Fv, содержащей антигенсвязывающий домен. Специалистам в данной области понятно, что указанный антигенсвязывающий домен содержит связывающий сайт антитела.
В одном примере, VH и VL находятся в одной полипептидной смеси. Например, белок представляет собой:
(i) одноцепочечный фрагмент Fv (scFv);
(ii) димерный scFv (ди-scFv); или
(iii) по меньшей мере, один из (i) и/или (ii), связанный с константной областью антитела, Fc, или константным доменом тяжелой цепи (СН)2 и/или CH3.
В одном примере, VH и VL находятся в разных полипептидных цепях.
Например, белок представляет собой:
(i) диатело;
(ii) триотело;
(iii) тетратело;
(iv) Fab;
(v) F(ab′)2;
(vi) Fv; или
(vii) один из (i)-(vi), связанный с константной областью антитела, Fc, или константным доменом тяжелой цепи (CH)2 и/или CH3.
Вышеупомянутые белки (описанные в двух предыдущих списках) также могут быть упомянуты как антигенсвязывающие домены или антитела.
В одном примере, белок представляет собой антитело. В одном примере, антитело представляет собой ненагруженное антитело.
В одном примере, белок является химерным, деиммунизированным, гуманизированым, человеческим или приматизированным.
В одном примере, белок или антитело является человеческим.
В настоящем описании дополнительно или альтернативно представлено антитело, которое связывается с hG-CSFR и нейтрализует передачу сигналов G-CSF, указанное антитело содержит:
(i) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO:2 и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO:3;
(ii) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO:4 и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO:5;
(iii) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO:15 и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO:14;
(iv) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO:4 и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO:16;
(v) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO:4 и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO:17;
(vi) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO:4 и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO:18;
(vii) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO:20 и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO:19;
(viii) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO:4 и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO:21;
(ix) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO:4 и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO:22;
(х) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO:24 и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO:23;
(ix) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO:4 и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO:25;
(х) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO:4 и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO:26;
(xi) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO:28 и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO:27;
(xii) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO:4 и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO:29;
(xiii) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO:31 и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO:30;
(xiv) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO:33 и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO:32;
(xv) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO:4 и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO:34;
(xvi) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO:36 и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO:35;
(xvii) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO:38 и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO:37;
(xviii) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO:40 и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO:39;
(xix) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO:42 и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO:41;
(хх) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO:4 и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO:43;
(xxi) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO:45 и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO:44;
(xxii) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO:4 и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO:46;
(xxiii) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO:4 и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO:47;
(xxiv) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO:49 и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO:48;
(xxv) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO:51 и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO:50;
(xxvi) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO:53 и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO:52;
(xxvii) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO:4 и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO:54;
(xxviii) VH, содержащей аминокислотную последовательность, представленную в SEQ ID NO:55 и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO:5;
(xxix) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO:57 и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO:56;
(ххх) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO:59 и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO:58;
(xxxi) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO:61 и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO:60;
(xxxii) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO:4 и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO:62;
(xxxiii) VH, содержащей аминокислотную последовательность, представленную в SEQ ID NO:4 и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO:63; и
(xxxix) VH, содержащую три CDR из набора VH, представленного выше в любом одном или более из (i)-(xxxiii), и VL, содержащую три CDR из набора VL, представленного выше в любом одном или более из (i)-(xxxiii).
Последовательности иллюстративных VH и VL описаны в Таблице 3, причем указанная последовательность CDR3 VH или VL замещена соответствующей последовательностью в VH или VL С1.2 или C1.2G, как описано в настоящем документе.
В одном примере, в настоящем описании представлено антитело, которое связывается с hG-CSFR и нейтрализует передачу сигналов G-CSF, указанное антитело содержит:
(i) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO:2 и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO:3; или
(ii) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO:4 и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO:5.
В настоящем описании дополнительно или альтернативно представлено антитело, содержащее тяжелую цепь, содержащую аминокислотную последовательность, представленную в SEQ ID NO:64 и легкую цепь, содержащую аминокислотную последовательность, представленную в SEQ ID NO:65. В одном примере, указанное антитело связывается с hG-CSFR и нейтрализует передачу сигналов G-CSF.
В настоящем описании дополнительно или альтернативно представлено антитело, содержащее тяжелую цепь, содержащую аминокислотную последовательность, представленную в SEQ ID NO:68 и легкую цепь, содержащую аминокислотную последовательность, представленную в SEQ ID NO:65. В одном примере, указанное антитело связывается с hG-CSFR и нейтрализует передачу сигналов G-CSF.
В настоящем описании дополнительно или альтернативно представлено антитело, содержащее одну тяжелую цепь, содержащую аминокислотную последовательность, представленную в SEQ ID NO:64 и одну тяжелую цепь, содержащую аминокислотную последовательность, представленную в SEQ ID NO:68, и две легкие цепи, содержащие аминокислотную последовательность, представленную в SEQ ID NO:65. В одном примере, указанное антитело связывается с hG-CSFR и нейтрализует передачу сигналов G-CSF.
Упоминание в настоящем документе белка или антитела, которое «связывается с» hG-CSFR обеспечивает буквальное подкрепление белка или антитела, которое «специфически связывается с» hG-CSFR.
В одном примере, белок или антитело, описанное в настоящем документе, существенно не связывается с мышиным G-CSFR и/или не связывается обнаруживаемым образом с мышиным G-CSFR.
В одном примере, белок или антитело, описанное в настоящем документе по любому примеру, конкурентно ингибирует связывание С1.2 и/или C1.2G с hG-CSFR или клеткой, экспрессирующей их, или SEQ ID NO:1, или растворимым hG-CSFR (например, содержащим аминокислоты 1-311 SEQ ID NO:1, гибридизованные с Fc областью антитела).
В одном примере, белок или антитело, описанное в настоящем документе, связывается с лиганд-связывающей областью hG-CSFR и лиганд-связывающей областью cynoG-CSFR с одинаковой аффинностью. В одном примере, белок связывается с растворимым hG-CSFR и растворимым cynoG-CSFR с одинаковой аффинностью. В одном примере, белок связывается с полипептидом, содержащим SEQ ID NO:1 и с полипептидом, содержащим SEQ ID NO:67 с одинаковой аффинностью. В одном примере, белок связывается с hG-CSFR-Fc и cynoG-CSFR-Fc, описанными в настоящем документе, с одинаковой аффинностью. В одном примере, аффинность составляет, по меньшей мере, около 2 нМ, например, по меньшей мере, около 1,5 нМ, такое значение как, по меньшей мере, около 1,2 нМ, 1,1 нМ или 1 нМ. В одном примере, 0,5 нМ, такое значение, как, по меньшей мере, около 0,46 нМ или 0,45 нМ, или 0,40 нМ, или 0,39 нМ. В другом примере, аффинность составляет, по меньшей мере, около 0,1 нМ, такое значение как, по меньшей мере, около 0,09 нМ, например, по меньшей мере, около 0,08 нМ. В одном примере, степень связывания оценивают с использованием биосенсора, например, резонансом поверхностного плазмона. Например, фиксируют лиганд-связывающую область или растворимый hG-CSFR, или растворимый cynoG-CSFR, или hG-CSFR-Fc, или cyno-G-CSFR-Fc, и определяют степень связывания с белком настоящего изобретения.
В другом примере, белок настоящего изобретения фиксируют, например, на биосенсоре, и определяют степень связывания лиганд-связывающей области или растворимого hG-CSFR, или растворимого cynoG-CSFR, или hG-CSFR-Fc, или cyno-G-CSFR-Fc. Например, определяют степень связывания с внеклеточным доменом hG-CSFR или cynoG-CSFR. В соответствии с этим примером, аффинность белка к внеклеточному домену cynoG-CSFR составляет, по меньшей мере, около 1 нМ, такое значение как, по меньшей мере, около 0,9 нМ, например, по меньшей мере, около 0,75 нМ. Например, аффинность составляет, по меньшей мере, около 0,7 нМ, такое значение как, по меньшей мере, около 0,6 нМ, например, по меньшей мере, около 0,5 нМ. В одном примере, аффинность составляет около 0,5 нМ. Альтернативно или дополнительно, аффинность белка к внеклеточному домену hG-CSFR составляет, по меньшей мере, около 7 нМ или 6 нМ, или 5 нМ, такое значение как, по меньшей мере, 4 нМ, например, по меньшей мере, около 3 нМ, например, по меньшей мере, около 2,5 нМ. Например, аффинность составляет, по меньшей мере, около 2,4 или 2,5 нМ.
В настоящем описании представлены также антигенсвязывающие домены или антигенсвязывающие фрагменты вышеупомянутых антител.
В одном примере, белок или антитело, описанное в настоящем документе, содержит константную область IgG4 антитела или стабилизированную константную область IgG4 антитела. В одном примере, белок или антитело содержит IgG4 константную область с пролином в положении 241 (согласно системы нумерации Kabat (Kabat et al., Sequences of Proteins of Immunological Interest Washington DC United States Department of Health and Human Services, 1987 и/или 1991)).
С-концевой лизин константной области тяжелой цепи целого антитела настоящего описания может быть удален, например, при получении или очистке указанного антитела, или рекомбинантным инжинирингом нуклеиновой кислоты, кодирующей тяжелую цепь антитела. Соответственно, целые антитела могут содержать группы антител со всеми удаленными С-концевыми остатками лизина, группы антител без удаленных С-концевых остатков лизина и группы антител, имеющие смесь антител с С-концевыми остатками лизина и без них. В некоторых примерах, группы антител могут дополнительно содержать антитела, в которых С-концевой остаток лизина удален в одной из константных областей тяжелой цепи. Точно так же, композиция целых антител может содержать такую же или похожую смесь групп антител с С-концевыми остатками лизина или без них.
В одном примере, стабилизированная константная область содержит последовательность с положения 119 до положения 445 SEQ ID NO:64. В одном примере, стабилизированная константная область содержит последовательность с положения 119 до положения 444 SEQ ID NO:68. В одном примере, белок или антитело, описанное в настоящем документе, или композиция белка или антитела, описанная в настоящем документе, содержит константую область тяжелой цепи, включая стабилизированную константную область тяжелой цепи, содержащую смесь последовательностей, полностью или частично с С-концевыми остатками лизина или без них.
В одном примере, антитело настоящего описания содержит VH, описанную в настоящем документе, связанную или гибридизованную с константной областью IgG4 или стабилизированной константной областью IgG4 (например, как рассмотрено выше), и VL связана или гибридизована с константной областью легкой каппа-цепи.
В настоящем описании представлен также белок или антитело, которое ингибирует G-CSF-индуцированную пролиферацию клеток BaF3, экспрессирующих hG-CSFR с IC50, по меньшей мере, около 6 нМ. Например, IC50 составляет 5,9 нМ или менее. В другом примере, IC50 составляет 2 нМ или менее, или 1 нМ или менее, или 0,7 нМ или менее, или 0,6 нМ или менее, или 0,5 нМ или менее. В одном примере, IC50 определяют выращиванием клеток BaF3 (например, около 2×104 клеток) в присутствии около 0,5 нг/мл hG-CSF, например, в течение около 48 часов. В одном примере, пролиферацию клеток BaF3 определяют измерением восстановления 3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолия бромида (МТТ).
В настоящем описании представлен также белок или антитело, которое ингибирует G-CSF-индуцированную пролиферацию клеток BaF3, экспрессирующих hG-CSFR с IC50, по меньшей мере, около 10 мкг/мл. Например, IC50 составляет 5 мкг/мл или менее. В другом примере, IC50 составляет 3 мкг/мл или менее, или 2 мкг/мл или менее, или 1 мкг/мл или менее. В одном примере, IC50 составляет около 0,8 мкг/мл. В одном примере, IC50 определяют выращиванием клеток BaF3 (например, около 1×104 клеток) в присутствии около 10 нг/мл hG-CSF, например, в течение около 48 часов. В одном примере, пролиферацию клеток BaF3 определяют измерением внедрением 3H-тимидина.
В одном примере, белок или антитело настоящего описания связывается с растворимым hG-CSFR, содержащим аминокислоты 1-311 SEQ ID NO:1, выраженным как слияние с Fc областью антитела (hG-CSFR-Fc) с аффинностью, по меньшей мере, около 1,5 нМ. Например, аффинность составляет, по меньшей мере, около 0,5 нМ или около 0,4 нМ, или 0,35 нМ, или 0,33 нМ. В одном пример, аффинность белка определяют с использованием биосенсора, например, резонансом поверхностного плазмона. Например, фиксируют hG-CSFR-Fc и определяют аффинность белка настоящего изобретения.
В одном примере, белок или антитело настоящего описания связывается с hG-CSFR, экспрессируемым на поверхности клетки с аффинностью, составляющей, по меньшей мере, около 1 нМ, например, по меньшей мере, 0,5 нМ, такой как, по меньшей мере, 0,4 нМ, например, по меньшей мере, 0,3 нМ, такой как, по меньшей мере, 0,2 нМ.
В одном примере, белок, описанный в настоящем документе по любому примеру, способен уменьшать количество нейтрофилов в кровотоке при введении яванскому макаку. Например, указанный белок уменьшает количество нейтрофилов в кровотоке при введении яванскому макаку в дозе в диапазоне 0,05 мг/кг-30 мг/кг, предпочтительно в диапазоне 0,1 мг/кг-10 мг/кг, например, при введении в дозе 0,1 мг/кг или 1 мг/кг, или 2 мг/кг, или 5 мг/кг, или 10 мг/кг. Например, указанный белок снижает количество нейтрофилов в кровотоке при введении после введения G-CSF или филграстима или его ПЭГилированной формы, например, при введении указанного белка приблизительно через 12 часов после введения G-CSF или филграстима, или его ПЭГилированной формы. В одном примере, уменьшение представляет собой 2-кратное или 3-кратное уменьшение. В одном примере, количество нейтрофилов уменьшается приблизительно через 10-24 часа, например, приблизительно через 12 часов после введения.
В одном примере, белок или антитело, описанное в настоящем документе, является изолированным и/или рекомбинантным.
В одном примере, белок или антитело настоящего описания гибридизовано с другим соединением, например, обнаруживаемой меткой или соединением, которое увеличивает период полувыведения белка или антитела, таким как полиэтиленгликоль или альбумин-связывающий белок.
В настоящем описании представлена также нуклеиновая кислота, кодирующая белок или антитело настоящего описания.
В одном примере, такая нуклеиновая кислота включена в экспрессирующую конструкцию, в которой указанная нуклеиновая кислота функционально связана с промотором. Такая экспрессирующая конструкция может быть в векторе, например, в плазмидном.
В примерах настоящего описания, относящихся к единичным белкам полипептидной цепи, экспрессирующая конструкция может содержать промотор, связанный с нуклеиновой кислотой, кодирующей указанную полипептидную цепь.
В примерах, относящихся к множественным полипептидным цепям, которые образуют белок, экспрессирущая конструкция содержит нуклеиновую кислоту, кодирующую полипептид, содержащий, например, VH, функционально связанную с промотором, и нуклеиновую кислоту, кодирующую полипептид, содержащий, например, VL, функционально связанную с промотором.
В другом примере, экспрессирующая конструкция представляет собой бицистронную экспрессирующую конструкцию, например, содержащую следующие функционально связанные компоненты в порядке от 5′ до 3′:
(i) промотор (ii) нуклеиновую кислоту, кодирующую первый полипептид;
(iii) внутренний сайт связывания рибосомы; и
(iv) нуклеиновую кислоту, кодирующую второй полипептид,
причем первый полипептид содержит VH, а второй полипептид содержит VL, или наоборот.
Настоящее описание охватывает также отдельные экспрессирующие конструкции, одна из которых кодирует первый полипептид, содержащий VH, a другой из которых кодирует второй полипептид, содержащий VL. Например, в настоящем описании представлена также композиция, содержащая:
(i) первую экспрессирующую конструкцию, содержащую нуклеиновую кислоту, кодирующую полипептид, содержащий VH, функционально связанную с промотором; и
(ii) вторую экспрессирующую конструкцию, содержащую нуклеиновую кислоту, кодирующую полипептид, содержащий VL, функционально связанную с промотором.
В настоящем описании представлена также изолированная или рекомбинантная клетка, экспрессирующая белок настоящего описания.
В одном примере, указанная клетка содержит экспрессирующую конструкцию настоящего описания или:
(i) первую экспрессирующую конструкцию, содержащую нуклеиновую кислоту, кодирующую полипептид, содержащий VH, функционально связанную с промотором; и
(ii) вторую экспрессирующую конструкцию, содержащую нуклеиновую кислоту, кодирующую полипептид, содержащий VL, функционально связанную с промотором.
Примеры клеток настоящего описания включают бактериальные клетки, дрожжевые клетки, клетки насекомых или клетки млекопитающих.
В настоящем описании дополнительно представлены способы продуцирования белка или антитела настоящего описания. Например, такой способ включает поддержание экспрессирующей конструкции(ий) настоящего описания в условиях, достаточных для продуцирования белка.
В одном примере, способ продуцирования белка или антитела настоящего описания включает выращивание клетки настоящего описания в условиях, достаточных для продуцирования и, необязательно, секреции белка или антитела.
В одном примере, способ продуцирования белка настоящего описания дополнительно включает выделение белка или антитела и, необязательно, составление указанного белка или антитела в фармацевтическую композицию.
В настоящем описании дополнительно представлена композиция, содержащая белок или антитело настоящего описания и фармацевтически приемлемый носитель.
В настоящем описании дополнительно представлена композиция, содержащая:
(i) антитело, содержащее тяжелую цепь, содержащую аминокислотную последовательность, представленную в SEQ ID NO:64 и легкую цепь, содержащую аминокислотную последовательность, представленную в SEQ ID NO:65; и
(ii) (а) антитело, содержащее тяжелую цепь, содержащую аминокислотную последовательность, представленную в SEQ ID NO:64 и легкую цепь, содержащую аминокислотную последовательность, представленную в SEQ ID NO:65; и/или
(b) антитело, содержащее одну тяжелую цепь, содержащую аминокислотную последовательность, представленную в SEQ ID NO:64 и одну тяжелую цепь, содержащую аминокислотную последовательность, представленную в SEQ ID NO:68, и две легкие цепи, содержащие аминокислотную последовательность, представленную в SEQ ID NO:65, и, необязательно, фармацевтически приемлемый носитель.
В настоящем описании представлен также способ лечения или предупреждения G-CSF-опосредованного состояния у субъекта, указанный способ включает введение белка, антитела или композиции настоящего описания. В этом отношении, белок, антитело или композиция могут быть использованы для предупреждения рецидива состояния, и это считается предупреждением указанного состояния.
В одном примере, G-CSF-опосредованное состояние представляет собой аутоиммунное заболевание, воспалительное заболевание или рак. Например, аутоиммунное заболевание или воспалительное заболевание представляет собой артрит, рассеянный склероз, воспаление легких или хроническую обструктивную болезнь легких.
В одном примере, указанный способ включает введение количества белка или антитела, достаточного для уменьшения количества нейтрофилов у субъекта без инициации нейтропении.
В настоящем описании альтернативно или дополнительно представлен способ уменьшения количества нейтрофилов у субъекта без инициации нейтропении, указанный способ включает введение белка, содержащего антигенсвязывающий сайт, или антитела, которое связывается (или специфически связывается) с hG-CSFR субъекта. Иллюстративный белок представляет собой антитело или содержит его антигенсвязывающий домен (например, VH и/или VL), или представляет собой его антигенсвязывающий фрагмент. Иллюстративные белки и антитела описаны в настоящем документе.
В одном примере, способ, описанный в настоящем документе, включает введение количества белка или антитела, достаточного для уменьшения количества нейтрофилов у субъекта без инициации умеренной нейтропении.
В одном примере, способ, описанный в настоящем документе, включает введение количества белка или антитела, достаточного для уменьшения количества нейтрофилов у субъекта без инициации тяжелой нейтропении.
В одном примере, способ, описанный в настоящем документе, включает введение указанного белка или антитела в диапазоне приблизительно от 0,05 мг/кг до 30 мг/кг. Например, указанный способ включает введение белка или антитела в диапазоне от 0,1 мг/кг до 10 мг/кг или от 0,2 мг/кг до 5 мг/кг. В одном примере, указанный способ включает введение около 0,5-2,0 мг/кг белка или антитела.
В настоящем описании представлено также применение белка или антитела, описанного в настоящем документе в любом примере, в медицине.
В настоящем описании представлено также применение белка или антитела, описанного в настоящем документе по любому примеру, в производстве лекарственного средства для лечения G-CSF-опосредованного состояния.
В настоящем описании представлен также способ локализации и/или обнаружения, и/или диагностирования, и/или прогнозирования G-CSF-опосредованного состояния, связанного с клетками, экспрессирующими G-CSFR, указанный способ включает in vivo обнаружение белка или антитела, описанного в настоящем документе, связанного с G-CSFR экспрессирующей клеткой, при его наличии, причем указанный белок или антитело является гибридизованным с обнаруживаемой меткой.
В одном примере, указанный способ дополнительно включает введение белка субъекту.
В настоящем описании представлен также способ обнаружения G-CSFR или клетки, экспрессирующей его, в образце, указанный способ включает взаимодействие образца с белком или антителом, описанным в настоящем документе по любому примеру, так что образуется комплекс, и обнаружение указанного комплекса, причем обнаружение комплекса является показателем G-CSFR или клетки, экспрессирующей его, в образце.
В настоящем описании представлен также способ диагностирования или прогнозирования G-CSF-опосредованного состояния, указанный способ включает выполнение способа, описанного в настоящем документе по любому примеру, для обнаружения G-CSFR или клетки, экспрессирующей его, причем обнаружение G-CSFR или клетки, экспрессирующей его, является диагностическим или прогностическим для указанного состояния.
В настоящем описании представлен также набор, содержащий белок или антитело, описанное в настоящем документе по любому примеру, упакованный с инструкциями по применению по способу, описанному в настоящем документе.
КЛЮЧ ДЛЯ ПЕРЕЧНЯ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
SEQ ID NO:1 - аминокислоты 25-335 Homo sapiens G-CSFR (hG-CSFR) с C-концевой полигистидиновой меткой
SEQ ID NO:2 - VHC1.2
SEQ ID NO:3 - VLC1.2
SEQ ID NO:4 - VHC1.2G
SEQ ID NO:5 - VLC1.2G
SEQ ID NO:6 - HCDR1 C1.2
SEQ ID NO:7 - HCDR2 C1.2
SEQ ID NO:8 - HCDR3 C1.2
SEQ ID NO:9 - LCDR1C1.2
SEQ ID NO:10 - LCDR2 C1.2
SEQ ID NO:11 - LCDR3 C1.2
SEQ ID NO:12 - консенсусная последовательность HCDR3 C1.2
SEQ ID NO:13 - консенсусная последовательность LCDR3 C1.2
SEQ ID NO:14 - VL антитела 987
SEQ ID NO:15 - VH антитела 987
SEQ ID NO:16 - VL антитела 95
SEQ ID NO:17 - VL антитела 79
SEQ ID NO:18 - VL антитела 83
SEQ ID NO:19 - VL антитела 1003
SEQ ID NO:20 - VH антитела 1003
SEQ ID NO:21 - VL антитела 44
SEQ ID NO:22 - VL антитела 97
SEQ ID NO:23 - VL антитела 986
SEQ ID NO:24 - VH антитела 986
SEQ ID NO:25 - VL антитела 56
SEQ ID NO:26 - VL антитела 77
SEQ ID NO:27 - VL антитела 54
SEQ ID NO:28 - VH антитела 54
SEQ ID NO:29 - VL антитела 802
SEQ ID NO:30 - VL антитела 967
SEQ ID NO:31 - VH антитела 967
SEQ ID NO:32 - VL антитела 989
SEQ ID NO:33 - VH антитела 989
SEQ ID NO:34 - VL антитела 63
SEQ ID NO:35 - VL антитела 1002
SEQ ID NO:36 - VH антитела 1002
SEQ ID NO:37 - VL антитела 994
SEQ ID NO:38 - VH антитела 994
SEQ ID NO:39 - VL антитела 969
SEQ ID NO:40 - VH антитела 969
SEQ ID NO:41 - VL антитела 1000
SEQ ID NO:42 - VH антитела 1000
SEQ ID NO:43 - VL антитела 94
SEQ ID NO:44 - VL антитела 975
SEQ ID NO:45 - VH антитела 975
SEQ ID NO:46 - VL антитела 75
SEQ ID NO:47 - VL антитела 814
SEQ ID NO:48 - VL антитела 973
SEQ ID NO:49 - VH антитела 973
SEQ ID NO:50 - VL антитела 977
SEQ ID NO:51 - VH антитела 977
SEQ ID NO:52 - VL антитела 984
SEQ ID NO:53 - VH антитела 984
SEQ ID NO:54 - VL антитела 61
SEQ ID NO:55 - VH антитела 852
SEQ ID NO:56 - VL антитела 996
SEQ ID NO:57 - VH антитела 996
SEQ ID NO:58 - VL антитела 43
SEQ ID NO:59 - VH антитела 43
SEQ ID NO:60 - VL антитела 999
SEQ ID NO:61 - VH антитела 999
SEQ ID NO:62 - VL антитела 870
SEQ ID NO:63 - VL антитела 877
SEQ ID NO:64 - тяжелая цепь C1.2G со стабилизированной константной областью IgG4
SEQ ID NO:65 - легкая цепь C1.2G с каппа-константной областью
SEQ ID NO:66 - последовательность иллюстративного h-GCSFR
SEQ ID NO:67 - полипептид, содержащий домены Ig и CRH Macaca fascicularis G-CSFR (cynoG-CSFR) с С-концевой полигистидиновой меткой
SEQ ID NO:68 - тяжелая цепь C1.2G со стабилизированной константной областью IgG4 и без С-концевого лизина.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Фигура 1 представляет собой графическое изображение, иллюстрирующее ингибирование G-CSF-опосредованную пролиферацию клеток BaF3 за счет увеличения концентраций различных анти-G-CSFR антител. Относительные значения 1С5о для каждого антитела составили; 10,1 мкг/мл для mAb711, 37,4 мкг/мл для mAb774, 0,8 мкг/мл для C1.2G и не было обнаруживаемым для mAb 744.
Фигура 2А представляет собой графическое изображение, иллюстрирующее относительное связывание C1.2G и mAb744 с сериями аланиновых точечных мутантов SEQ ID NO:1 по сравнению с их связыванием с SEQ ID NO:1 (положения мутаций указаны со ссылкой на SEQ ID NO:1). Изображена кратность снижения KD антитела для мутантного рецептора по сравнению с SEQ ID NO:1.
Фигура 2В представляет собой графическое изображение, иллюстрирующее относительное связывание C1.2G, mAb744 и mAb774 с сериями аланиновых точечных мутантов SEQ ID NO:1 по сравнению с их связыванием с SEQ ID NO:1 (положения мутаций указаны со ссылкой на SEQ ID NO:1). Изображена кратность снижения KD антитела для мутантного рецептора по сравнению с SEQ ID NO:1.
Фигура 3 иллюстрирует результаты анализа, в котором пэгилированный G-CSF вводили яванским макакам, а на следующий день вводили С1.2. Оценили количество нейтрофилов на мкл крови.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Общая информация
В настоящем описании, если специально не указано иное или контекстом не требуется обратное, то ссылка на одну стадию, композицию вещества, группу стадий или группу композиций вещества, включает одну и множество (то есть одну или более) таких стадий, композиций вещества, групп стадий или групп композиций вещества.
Специалистам в данной области понятно, что настоящее описание восприимчиво к изменениям и модификациям, отличным от конкретно описанных. Следует понимать, что настоящее описание включает все такие изменения и модификации. Настоящее описание включает также все стадии, характеристики, композиции и соединения, упомянутые или указанные в настоящем описании, отдельно или вместе, и любые и все комбинации любых двух или более из указанных стадий или характеристик.
Настоящее описание не ограничивается рамками конкретных примеров, описанных в настоящем документе, которые предназначены лишь для целей иллюстрации. Функционально эквивалентные продукты, композиции и способы в явной форме входят в рамки настоящего описания.
Любой пример настоящего описания, описанный в настоящем документе, следует использовать mutatis mutandis в отношении другого примера настоящего описания, если специально не указано иное.
Если специально не указано иное, то все технические и научные термины, используемые в настоящем документе, имеют такое же значение, которое обычно понимается специалистами в данной области (например, в области клеточных культур, молекулярной генетики, иммунологии, иммуногистохимии, химии белков и биохимии).
Если не указано иное, то рекомбинантный белок, клеточная культура и иммунологические приемы, используемые в настоящем описании, представляют собой стандартные методики, хорошо известные специалистам в данной области. Такие приемы описаны и разъяснены в литературных источниках, таких как J. Perbal, A Practical Guide to Molecular Cloning, John Wiley and Sons (1984), J. Sambrook et al. Molecular Cloning: A Laboratory Manual, Cold Spring Harbour Laboratory Press (1989), T.A. Brown (редактор), Essential Molecular Biology: A Practical Approach, томм 1 и 2, IRL Press (1991), D.M. Glover and B.D. Hames (редакторы), DNA Cloning: A Practical Approach, тома 1-4, IRL Press (1995 и 1996), и F.M. Ausubel et al. (редакторы). Current Protocols in Molecular Biology, Greene Pub. Associates and Wiley-Interscience (1988, включая все обновления до сегодняшнего дня), Ed Harlow and David Lane (редакторы) Antibodies: A Laboratory Manual, Cold Spring Harbour Laboratory, (1988), и J.E. Coligan et al. (редакторы) Current Protocols in Immunology, John Wiley & Sons (включая все обновления до сегодняшнего дня).
Описание и определение вариабельных областей и их частей, иммуноглобулинов, антител и их фрагментов в настоящем документе можно дополнительно прояснить в публикации Kabat Sequences of Proteins of Immunological Interest, National Institutes of Health, Bethesda, Md., 1987 и 1991, Bork et al., J Mol. Biol. 242, 309-320, 1994, Chothia and Lesk J. Mol Biol. 196:901-917, 1987, Chothia et al. Nature 342, 877-883, 1989 и/или Al-Lazikani et al., J Mol Biol 273,927-948, 1997.
Термин «и/или», например, «X и/или Y» следует понимать как «X и Y» или «X или Y», и следует применять для обеспечения точного подкрепления обоих значения или для каждого значения.
В настоящем описании слово «включает» или варианты, такие как «содержит» или «содержащий» следует понимать как обозначение включения указанного элемента, целого или стадии, или группы элементов, целых или стадий, а не как исключение любого другого элемента, целого или стадии, или группы элементов, целых или стадий.
При использовании в настоящем документе, термин «получен из» следует понимать как обозначение того, что определенное целое может быть получено из конкретного источника, хотя не обязательно непосредственно из указанного источника.
Некоторые определения
Лишь в целях номенклатуры, но не ограничения, иллюстративная последовательность человеческого G-CSFR представлена в контрольной последовательности NCBI: NP_000751.1 (и представлена в SEQ ID NO:66). Эта последовательность G-CSFR яванского макака может быть определена с использованием последовательностей, представленных в настоящем документе, и/или в опубликованных базах данных, и/или может быть определена с использованием стандартных методик (например, как описано в публикации Ausubel et al., (редакторы). Current Protocols in Molecular Biology, Greene Pub. Associates and Wiley-Interscience (1988, включая все обновления до сегодняшнего дня) или Sambrook et al., Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Laboratory Press (1989)). Упоминание человеческого G-CSFR может быть сокращено до hG-CSFR, а упоминание G-CSFR яванского макака может быть сокращено до cynoG-CSFR. Упоминание растворимого G-CSFR относится к полипептидам, содержащим лиганд-связывающую область G-CSFR. Домены Ig и CRH G-CSFR участвуют в связывании с лигандом и рецепторной димеризации (Layton et al., J. Biol Chem., 272: 29735-29741, 1997 и Fukunaga et al, EMBO J. 10: 2855-2865, 1991). Растворимые формы G-CSFR, содержащие эти части рецептора, были использованы в различных исследованиях указанного рецептора и мутации свободных цистеинов в положениях 78, 16, и 228 указанного рецептора, способствующей экспрессии и выделению растворимого рецепторного полипептида (Mine et al., Biochem., 43: 2458-2464 2004) без ухудшения связывания с лигандом. В текущих исследованиях были использованы растворимые формы рецептора, содержащего аминокислоты 25-335 hG-CSFR с мутациями С78А, C163S и C228S (например, SEQ ID NO:1), и был использован соответствующий сегмент cynoG-CSFR с цистеиновьми мутациями (например, SEQ ID NO 67) для исследования на рецепторе яванского макака. Были также использованы различные точечные мутации растворимого рецептора SEQ ID NO:1 и SEQ ID NO:67. Упоминание hG-CSFR-Fc обозначает полипептид SEQ ID NO:1, в котором С-концевая полигистидиновая метка была замещена последовательностью Fc (например, полипептид, содержащий аминокислоты 1-311 SEQ ID NO:1, гибридизованный с Fc). cynoG-CSFR-Fc обозначает соответствующих сегмент cynoG-CSFR с последовательностью Fc, присоединенной к его С-окончанию (например, полипептид, содержащий аминокислоты 1-311 of SEQ ID NO:67, гибридизованный с Fc). Авторы настоящего изобретения показали, что антитела и белки, содержащие их антигенсвязывающие сайты (например, Fab), связываются с полипептидами hG-CSF дикого типа и с этими мутантными белками с очень похожей аффинностью. Соответственно, исследования с использованием мутантных белков представляют собой модель исследований с использованием hG-CSFR и/или cynoG-CSFR.
Упоминание в настоящем документе G-CSF включает нативные формы G-CSF, его мутантные формы, например, филграстим и пэгилированные формы G-CSF или филграстима. Этот термин охватывает также мутантные формы G-CSF, сохраняющие активность для связывания с G-CSFR (например, hG-CSFR) и инициации передачи сигналов.
Термин «изолированный белок» или «изолированный полипептид» представляет собой белок или полипептид, который в силу своего происхождения или источника получения не связан с природными компонентами, сопровождающими его в нативном состоянии; он практически не содержит других белков из того же источника. Белок может быть представлен практически без естественных связанных компонентов или практически очищенным при выделении, с использованием методик очистки белков, известных в данной области. Под «практически очищенным» подразумевается, что белок практически не содержит загрязняющих агентов, например, по меньшей мере, на 70% или 75%, или 80%, или 85%, или 90%, или 95%, или 96%, или 97%, или 98%, или 99% свободен от загрязняющих агентов.
Термин «рекомбинантный» следует понимать как обозначающий продукт искусственной генетической рекомбинации. Соответственно, в контексте рекомбинантного белка, содержащего антигенсвязывающий домен антитела, этот термин не включает антитело, естественным образом, встречающееся в организме субъекта, то есть продукт природной рекомбинации, который возникает при созревании В-клетки. Однако если такое антитело изолировано, его следует считать изолированным белком, содержащим антигенсвязывающий домен антитела. Точно так же, если нуклеиновая кислота, кодирующая белок, выделена и экспрессирована при помощи рекомбинантных способов, то полученный белок представляет собой рекомбинантный белок, содержащий антиген-связывающий домен антитела. Рекомбинантный белок охватывает также белок, экспрессированный искусственными рекомбинантными способами, если он находится внутри клетки, ткани или организма субъекта, например, в котором он экспрессируется.
Термин «белок» включает одну полипептидную цепь, то есть серию непрерывных аминокислот, связанных пептидными связями, или серию полипептидных цепей, ковалентно или нековалентно связанных друг с другом (то есть полипептидный комплекс). Например, серия полипептидных цепей может быть ковалентно связана при помощи соответствующей химической или дисульфидной связи. Примеры нековалентных связей включают водородные связи, ионные связи, силы Ван дер Ваальса и гидрофобные взаимодействия.
Термин «полипептид» или «полипептидная цепь», как следует понимать из вышеизложенного параграфа, обозначает серию непрерывных аминокислот, связанных пептидными связями.
При использовании в настоящем документе, термин «антигенсвязывающий сайт) обозначает структуру, образованную белком, которая способна связываться или специфически связываться с антигеном. Антигенсвязывающий сайт не обязательно представляет собой серию непрерывных аминокислот или даже аминокислот в одной полипептидной цепи. Например, в Fv, продуцированной из двух различных полипептидных цепей, антигенсвязывающий сайт образуется из серии аминокислот VL и VH, которые взаимодействуют с указанным антигеном, и которые, как правило, но не всегда, находятся в одном или более CDR в каждой вариабельной области. В некоторых примерах, антиген-связывающий сайт представляет собой VH или VL, или Fv.
Специалистам в данной области понятно, что «антитело», как правило, считается белком, который содержит вариабельную область, полученную из множества полипептидных цепей, например, полипептида, содержащего VL, и полипептида, содержащего VH. Антитело, как правило, содержит также константные домены, некоторые из которых могут быть расположены в константной области, которая содержит константный фрагмент или кристаллизующийся фрагмент (Fc), в случае тяжелой цепи. VH и VL взаимодействуют с образованием Fv, содержащей антиген-связывающую область, которая способна специфически связываться с одним или несколькими близкородственными антигенами. Как правило, легкая цепь млекопитающих представляет собой легкую κ-цепь или легкую λ-цепь, а тяжелая цепь млекопитающих представляет собой α, δ, ε, γ или µ. Антитела могут быть любого типа (например, IgG, IgE, IgM, IgD, IgA и IgY), класса (например, IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2) или подкласса. Термин «антитело» охватывает также гуманизированные антитела, приматизированные антитела, человеческие антитела и химерные антитела.
Термины «антитело полной длины», «интактное антитело» или «целое антитело» используются взаимозаменяемо для обозначения антитела в его практически интактной форме, в отличие от антиген-связывающего фрагмента антитела. В частности, целые антитела включают антитела с тяжелыми и легкими цепями, включая область Fc. Константые домены могут быть константными доменами последовательности дикого типа (например, человеческими константными доменами последовательности дикого типа) или вариантами их аминокислотных последовательностей.
При использовании в настоящем документе, «вариабельная область» относится к части легкой и/или тяжелой цепей антитела, как описано в настоящем документе, которая способна специфически связываться с антигеном, и включает аминокислотные последовательности определяющих комплементарность областей (CDR); то есть CDR1, CDR2 и CDR3 и каркасные области (FR). Иллюстративные вариабельные области содержат три или четыре FR (например, FR1, FR2, FR3 и необязательно FR4) вместе с тремя CDR. В случае белка, полученного из IgNAR, указанный белок может не содержать CDR2. VH относится к вариабельной области тяжелой цепи. VL относится к вариабельной области легкой цепи.
При использовании в настоящем документе, термин «определяющие комплементарность области» (синоним CDR; то есть CDR1, CDR2 и CDR3) относится к аминокислотным остаткам вариабельной области антитела, присутствие которых необходимо для связывания антигена. Каждая вариабельная область обычно имеет три области CDR, идентифицируемые как CDR1, CDR2 и CDR3. Аминокислотные положения, заданные для CDR и FR, могут быть определены в соответствии с публикацией Kabat Sequences of Proteins of Immunological Interest, National Institutes of Health, Bethesda, Md., 1987 и 1991, или с другими системами нумерации, при осуществлении настоящего описания, например, в соответствии с канонической системой нумерации Chothia and Lesk J. Mol Biol. 196: 901-917, 1987; Chothia et al. Nature 342, 877-883, 1989; и/или А1-Lazikani et al., J Mol Biol 273: 927-948, 1997; системой нумерации IMGT, описанной в Lefranc et al., Devel. And Compar. Immunol., 27: 55-77, 2003; или системой нумерации АНО, описанной в Honnegher and Plukthun J. Mol. Biol., 309: 657-670, 2001. Например, в соответствии с системой нумерации Kabat, каркасные области (FR) VH и CDR и s расположены следующим образом: остатки 1-30 (FR1), 31-35 (CDR1), 36-49 (FR2), 50-65 (CDR2), 66-94 (FR3), 95-102 (CDR3) и 103-113 (FR4). В соответствии с системой нумерации Kabat, FR и CDR VL расположены следующим образом: остатки 1-23 (FR1), 24-34 (CDR1), 35-49 (FR2), 50-56 (CDR2), 57-88 (FR3), 89-97 (CDR3) и 98-107 (FR4). Настоящее описание не ограничивается FR и CDR, описанными по системе нумерации Kabat, а включает все системы нумерации, в том числе те, которые рассмотрены выше. В одном примере, упоминание в настоящем документе CDR (или FR) представлено в отношении этих областей в соответствии с системой нумерации Kabat.
«Каркасные области» (FR) представляют собой остатки вариабельной области, отличные от остатков CDR.
При использовании в настоящем документе, термин «Fv» обозначает любой белок, состоящий из множества полипептидов или одного полипептида, в котором VL и VH связываются и образуют комплекс, имеющий антиген-связывающий сайт, то есть способный специфически связываться с антигеном. VH и VL, которые образуют антиген-связывающий сайт, могут быть в одной полипептидной цепи или в различных полипептидных цепях. Более того, Fv натоящего описания (а также любой белок настоящего описания) может иметь множество антиген-связывающих сайтов, которые могут связываться или не связываться с одним и тем же антигеном. Следует понимать, что этот термин охватывает фрагменты, напрямую полученные из антитела, а также белки, соответствующие такому фрагменту, полученные при помощи рекомбинантных способов. В некоторых примерах VH не связана с константным доменом тяжелой цепи (СН), и/или VL не связана с константным доменом легкой цепи (CL). Иллюстративные полипептиды или белки, содержащие Fv, включают фрагмент Fab′ фрагмент F(ab′), scFv, диатело, триотело, тетратело или комплекс более высокого порядка, или любое из вышеизложенного, связанное с его константной областью или доменом, например, доменом СН2 или СН3, например, миниантитело. «Фрагмент Fab» состоит из одновалентного антиген-связывающего фрагмента иммуноглобулина, и может быть получен поглощением целого антитела ферментом папаином, с образованием фрагмента, состоящего из интактной легкой цепи и части тяжелой цепи, или может быть получен при помощи рекомбинантных способов. «Фрагмент Fab′» антитела может быть получен обработкой целого антитела пепсином, с последующим восстановлением, с образованием молекулы, состоящей из интактной легкой цепи и части тяжелой цепи, содержащей VH и один константный домен. Таким образом, получают два фрагмента Fab′ из одного обработанного антитела. Фрагмент Fab′ может быть получен также рекомбинантными способами. «Фрагмент F(ab′)2» антитела состоит из димера из двух фрагментов Fab′, удерживаемых вместе двумя дисульфидными связями, и его получают обработкой молекулы целого антитела ферментом пепсином, без последующего восстановления. Фрагмент «Fab2» представляет собой рекомбинантный фрагмент, содержащий два фрагмента Fab, связанных при помощи, например, лейциновой застежки или домена СН3. «Одноцепочечный Fv» или «scFv» представляет собой рекомбинантную молекулу, содержащую фрагмент вариабельной области (Fv) антитела, в которой вариабельная область легкой цепи и вариабельная область тяжелой цепи ковалентно связаны соответствующим гибким полипептидным линкером.
При использовании в настоящем документе, термин «связывает», в отношении взаимодействия белка или его антиген-связывающего сайта с антигеном, обозначает, что это взаимодействие зависит от присутствия конкретной структуры (например, антигенной детерминанты или эпитопа) на антигене. Например, антитело распознает и связывается с определенной белковой структурой, а не с белками в целом. Если антитело связывается с эпитопом «А», то присутствие молекулы, содержащей эпитоп «А» (или свободный «А» без метки) в реакции, содержащей меченый «А» и белок, снижает количество меченого «А», связанного с указанным антителом.
При использовании в настоящем документе, термин «специфически связывается» или «связывается специфически» обозначает, что белок настоящего описания взаимодействует или связывается более часто, более быстро, на более продолжительный период и/или с большей аффинностью с определенным антигеном или клеткой, экспрессирующей его, чем он связывается с альтернативными антигенами или клетками. Например, белок связывается с G-CSFR (например, hG-CSFR) с существенно более высокой аффинностью (например, в 20 раз или 40 раз, или 60 раз, или от 80 раз до 100 раз, или 150 раз, или 200 раз), чем он связывается с другими цитокиновьми рецепторами или с антигенами, которые обычно распознаются полиреактивными природными антителами (то есть природными антителами, которые, как известно, связываются с различными естественными антигенами, встречающимися в организме людей). В одном примере настоящего описания, белок, который «специфически связывается» с одной формой hG-CSFR или полипептидом, содержащим его область (например, лиганд-связывающим доменом hG-CSFR), или полипептидом, содержащим аминокислоты 1-311 SEQ ID NO:1 с аффинностью, по меньшей мере, в 20 раз или 40 раз, или 60 раз, или 80 раз, или 100 раз, или 150 раз, или 200 раз выше, чем он связывается с мутантной формой hG-CSFR или полипептидом, содержащим его регион (например, мутантной формой лиганд-связывающего домена hG-CSFR) или мутантной формой SEQ ID NO:1, содержащей аланин, замещенный нативным аргинином в положении 287. Дополнительные иллюстративные изменения SEQ ID NO:1 и их влияние на связывание описаны в настоящем документе. Как правило, но не обязательно, упоминание связывания обозначает специфическое связывание, и каждый термин следует понимать как обеспечение точного подкрепления другого термина.
При использовании в настоящем документе, термин «не связывается обнаруживаемым образом» следует понимать как обозначающий, что белок, например антитело, связывается с потенциальным антигеном на уровне, составляющем менее 10% или 8%, или 6%, или 5% выше фона. Фон может быть уровнем связывающего сигнала, обнаруживаемым в отсутствие белка и/или в присутствии отрицательного контрольного белка (например, изотипного контрольного антитела), и/или уровнем связывания, обнаруживаемым в присутствии отрицательного контрольного антигена. Степень связывания обнаруживают при помощи биосенсорного анализа (например, Biacore), в котором белок фиксируют и приводят в контакт с антигеном.
При использовании в настоящем документе, термин «существенно не связывается» следует понимать как обзначающий, что уровень связывания белка настоящего описания с полипептидом статистически не выше, чем фон, например, уровня связывающего сигнала, обнаруживаемого в отсутствие белка и/или в присутствии отрицательного контрольного белка (например, изотипного контрольного антитела), и/или уровня связывания, обнаруживаемого в присутствии отрицательного контрольного полипептида. Степень связывания обнаруживают при помощи биосенсорного анализа (например, Biacore), в котором белок фиксируют и приводят в контакт с антигеном.
При использовании в настоящем документе, выражения, относящиеся к «пониженному связыванию» или «связыванию на более низком уровне» в отношении антигена, следует понимать как обозначающие, что антитело связывается с антигеном (например, аланиновым точечным мутантом SEQ ID NO:1 в любом из положений 287, 237, 198, 172, 171 или 111) с аффиностью, которая, по меньшей мере, в 20 раз или 40 раз, или 60 раз ниже, чем с контрольным эпитопом или антигеном (например, SEQ ID NO:1). Например, белок настоящего описания может связываться с полипептидом SEQ ID NO:1, в которой аланин замещен гистидином в положении 237, на уровне в 20 раз или 40 раз, или 60 раз ниже, чем он связывается с полипептидом SEQ ID NO:1. Предпочтительно, указанный белок связывается на уровне в 20 раз ниже, более предпочтительно в 40 раз ниже, еще более предпочтительно в 60 раз ниже.
Белок или антитело может считаться «предпочтительно связывающимся» с полипептидом, если он связывается с этим полипептидом с константной диссоциации (KD), которая меньше, чем KD указанного белка или антитела для другого полипептида. В одном примере, белок или антитело считается предпочтительно связывающимся с полипептидом, если он связывается с этим полипептидом с аффинностью (то есть KD), которая, по меньшей мере, приблизительно 20 раз или 40 раз, или 60 раз, или 80 раз, или 100 раз, или 120 раз, или 140 раз, или 160 раз больше, чем Ко указанного белка или антитела для другого полипептида.
При использовании в настоящем документе, термин «одинаковая аффинность» следует понимать как обозначающий, что белок настоящего описания связывается с двумя антигенами (например, лиганд-связывающим доменом G-CSFR человека и яванского макака) с аффинностями, которые находятся в пределах около 5 раз или менее друг относительно друга, например, в пределах около 4, 3, 2 или 1 раза друг относительно друга, такое значение как в пределах около 0,5 раз друг относительно друга, или степени связывания практически идентичны, например, если аффинность оценивают фиксацией двух антигенов (например, лиганд-связывающего домена G-CSFR или внеклеточных доменов человека и яванского макака) и приведением в контакт фиксированных белков с белком настоящего описания.
Для ясности и как понятно специалистам в данной области на основании представленного в настоящем документе примера рассматриваемого предмента, упоминание «аффинности» в настоящем описании представляет собой ссылку на k.d белка или антитела.
Для ясности и как понятно специалистам в данной области на основании представленного в настоящем документе описания, упоминание «аффинности, составляющей, по меньшей мере, около» следует понимать как обозначение того, что аффинность (или Ко) равна упомянутому значению или выше него (то есть значение, упомянутое как аффинность, ниже), то есть аффинность 2 нМ больше, чем аффинность 3 нМ. Иначе говоря, этот термин может быть «аффинностью Х или менее», причем Х представляет собой значение, упомянутое в настоящем документе.
«IC50, по меньшей мере, около» следует понимать как обозначение, что IC50 равно упомянутому значению или выше него (то есть значение, упомянутое как IC50, ниже), то есть IC50 2 нМ больше, чем IC50 3 нМ. Иначе говоря, этот термин может быть «IC50 Х или менее», причем Х представляет собой значение, упомянутое в настоящем документе.
При использовании в настоящем документе, термин «эпитоп» (синоним «антигенная детерминанта») следует понимать как обозначение области hG-CSFR, с которой связывается белок, содержащий антиген-связывающий сайт антитела. Этот термин не обязательно ограничен определенными остатками или структурой, с которой контактирует белок. Например, этот термин включает область, охватывающую аминокислоты, контактирующие с белком, и/или 5-10 или 2-5, или 1-3 аминокислоты за пределами этой области. В некоторых примерах, эпитоп содержит серию прерывающихся аминокислот, которые расположены вблизи друг друга при складывании hG-CSFR, то есть «конформационный эпитоп». Например, конформационный эпитоп содержит аминокислоты в одной или более, или двух или более, или во всех областях, соответствующих 111-115, 170-176, 218-234 и/или 286-300 SEQ ID NO:1. Специалистам в данной области понятно также, что термин «эпитоп» не ограничивается пептидами или полипептидами. Например, термин «эпитоп» включает химически активные поверхностные группы молекул, такие как сахарные боковые цепи, фосфорильные боковые цепи или сульфонильные боковые цепи, и, в некоторых примерах, может иметь специфические трехмерные структурные характеристики и/или спецические характеристики заряда.
Термин «конкурентно ингибирует» следует понимать как обозначение того, что белок настоящего описания (или его антиген-связывающий сайт) снижает или предотвращает связывание упомянутого антитела или белка с G-CSFR, например, hG-CSFR. Это может быть обусловлено связыванием белка (или антиген-связывающим сайтом) и антитела с одним и тем же или перекрывающимся эпитопом. Из вышеизложенного понятно, что белок не обязательно полностью ингибирует связывание антитело, скорее он должен только уменьшить связывание на статистически значимое значение, например, по меньшей мере, около 10% или 20%, или 30%, или 40%, или 50%, или 60%, или 70%, или 80%, или 90%, или 95%. Предпочтительно, белок уменьшает связывание антитела, по меньшей мере, приблизительно на 30%, более предпочтительно, по меньшей мере приблизительно на 50%, более предпочтительно, по меньшей мере, приблизительно на 70%, еще, по меньшей мере, приблизительно на 75%, по меньшей мере, приблизительно на 80% или 85%, и еще, по меньшей мере, приблизительно на 90%. Способы определения конкурентного ингибирования связывания известны в данной области и/или описаны в настоящем документе. Например, антитело подвергают воздействию G-CSFR в присутствии или в отсутствие белка. Если в присутствии белка связывается меньшее количества антитела, чем в отсутствие белка, то белок считают конкурентно ингибирующим связывание указанного антитела. В одном примере, конкурентное ингибирование обусловлено стерическим затруднением.
«Перекрывание» в контексте двух эпитопов следует понимать как обозначение того, что два эпитопа имеют достаточное количество общих аминокислотных остатков, чтобы обеспечить возможность белку (или его антиген-связывающему сайту), который связывается с одним эпитопом, конкуретно ингибировать связывание белка (или антиген-связывающего сайта), который связывается с другим эпитопом. Например, «перекрывающиеся» эпитопы имеют, по меньшей мере, 1 или 2, или 3, или 4, или 5, или 6, или 7, или 8, или 9, или 20 общих аминокислот.
При использовании в настоящем документе, термин «нейтрализует» следует понимать как обозначение того, что белок способен блокировать, снижать или предотвращать G-CSF-опосредованную передачу сигналов в клетке через G-CSFR. Способы определения нейтрализации известны в данной области и/или описаны в настоящем документе.
При использовании в настоящем документе, термин «состояние» относится к нарушению или препятствию нормальному функционированию, и он не ограничивается каким-либо конкретным состоянием, и включает заболевания и расстройства.
При использовании в настоящем документе, «G-CSF-связанное состояние» относится к любому состоянию, которое обусловлено или связано с нейтрофилами, избытком G-CSF или клеток, экспрессирующих G-CSFR, или с введением G-CSF. Специалисты в данной области могут легко определить такие состояния. В этом отношении, в некоторых примерах состояние представляет собой воспалительное состояние, аутоиммунное состояние или рак (включая метастазы).
При использовании в настоящем документе, термины «предупреждающий», «предупреждать» или «предупреждение» включают введение белка настоящего описания для остановки или затруднения, посредством этого, развития, по меньшей мере, одного симптома состояния. Этот термин охватывает также лечение субъекта в стадии ремиссии для предотвращения или препятствия рецидиву. Например, субъект, страдающий от возвратно-ремиттирующего рассеянного склероза, проходит лечение во время ремиссии для предупреждения, посредством этого, рецидива.
При использовании в настоящем документе, термины «лечащий», «лечить» или «лечение» включают введение белка, описанного в настоящем документе для снижения или исключения, посредством этого, по меньшей мере, одного симптома определенного заболевания или состояния.
При использовании в настоящем документе, термин «нейтропения» следует понимать как охватывающий легкую нейтропению (1000<=ANC<1500), умеренную нейтропению (500<=ANC<1000) и тяжелую нейтропению (ANC<500) (абсолютное количество нейтрофилов (ANC), измеренное в клетках на микролитр крови).
При использовании в настоящем документе, термин «субъект» следует понимать как обозначающий любое животное, включая людей, например, млекопитающее. Иллюстративные субъекты включают, но, не ограничиваясь этим, людей и приматов, не являющихся человеком. Например, субъект представляет собой человека.
Антитела
В одном примере, белок, описанный в настоящем документе по любому примеру, представляет собой антитело.
Способы создания антител известны в данной области и/или описаны в книге Harlow and Lane (редакторы) Antibodies: A Laboratory Manual, Cold Spring Harbor Laboratory, (1988). Как правило, в таких способах G-CSFR (например, hG-CSFR) или его область (например, внеклеточный домен) или иммуногенный фрагмент, или его эпитоп, или клетку, экспрессирующую и демонстрирующую их (например, иммуноген), необязательно составленные в композицию с любым соответствующим или заданным носителем, адъювантом или фармацевтически приемлемым формообразующим средством, вводят животному, не являющемуся человеком, например, мыши, курице, крысе, кролику, морской свинке, собаке, лошади, корове, козе или свинье. Иммуноген может быть введен интраназально, внутримышечно, подкожно, внутривенно, внутрикожно, внутрибрюшинно или другим известным путем.
Продуцирование поликлональных антител можно контролировать отбором образцов крови иммунизированного животного в различных точках после иммунизации. Может быть введена одна или более последующих иммунизации, если необходимо достичь заданного титра антитела. Процесс ревакцинации и титрования повторяют до достижения соответствующего титра. При получении заданного уровня иммуногенности, иммунизированное животное обескровливают, и выделяют и хранят сыворотку, и/или используют животное для получения моноклональных антител (mab).
Моноклональные антитела представляют собой одну иллюстративную форму антитела, охваченную настоящим описанием. Термин «моноклональное антитело» или «mAb» относится к гомогенной популяции антител, способной связываться одним антигеном(ами), например, одним эпитопом в пределах антигена. Этот термин не предназначен для ограничения в отношении источника антитела или способа его получения.
Для получения mAb может быть использован любой из множества известных приемов, такой как, например, способ, иллюстрированный в US4196265 или Harlow and Lane (1988), supra.
Например, соответствующее животное иммунизируют иммуногеном в условиях, достаточных для стимуляции клеток, вырабатывающих антитело. Подопытными животными являются грызуны, такие как кролики, мыши и крысы. Для создания антитела настоящего описания могут быть использованы также мыши, генетически созданные для экспрессии человеческих антител и, например, не экспрессирующие мышиные антитела (например, как описано в WO 2002/066630).
После иммунизации, соматические клетки с возможностью продуцирования антител, в частности, В-лимфоцитов (В-клеток) отбирают для использования в протоколе получения mAb. Эти клетки могут быть получены биопсией селезенки, миндалин или лимфатических узлов, или из образца периферической крови. В-клетки иммунизированного животного затем гибридизуют с бессмертными клетками миеломы, обычно полученными из тех же видов, что и животные, иммунизированные иммуногеном.
Гибриды амплифицируют выращиванием в селективной среде, содержащей агент, который блокирует de novo синтез нуклеотидов в тканевой культуральной среде. Иллюстративные агенты представляют собой аминоптерин, метотрексат и азасерин.
Амплифицированные гибридомы подвергают функциональному отбору по специфичности к антителу и/или титру, такому как, например, проточная цитометрия и/или иммуногистохимия, и/или иммуноанализ (например, радиоиммуноанализ, ферментный иммуноанализ, анализ цитотоксичности, анализ бляшкообразования, дот-иммуноанализ и тому подобные).
Альтернативно, используют технологию ABL-MYC (NeoClone, Madison WI 53713, США) для получения клеточных линий, секретирующих МАЬ (например, как описано в публикации Largaespada et al, J. Immunol. Methods. 197: 85-95, 1996).
Антитела могут быть также получены или выделены скринингом библиотеки дисплея, например, фаговой библиотеки дисплея, например, как описано в US6300064 и/или US5885793. Например, авторы настоящего изобретения полностью выделили человеческие антитела из фаговой библиотеки дисплея.
Как описано в настоящем документе, некоторые белки настоящего изобретения, которые связываются с hG-CSFR, перекрестие взаимодействуют с cynoG-CSFR и/или связываются с некоторыми мутантными формами hG-CSFR или полипептидами, содержащими области hG-CSFR, которые мутировали и/или не другими, и/или связываются со специфическим эпитопом в пределах hG-CSFR. Эти характеристики могут быть использованы при получении антитела или белка, содержащего его связывающий сайт.
Например, скринируют фаговую библиотеку дисплея с полипептидом, содержащим лиганд-связывающий домен hG-CSFR, для определения белков, которые связываются с ним. Мутантные формы лиганд-связывающего домена hG-CSFR (например, аланиновый точечный мутант SEQ ID NO:1 в положении 287), с которыми белок не связывается обнаруживаемым образом, затем используют для удаления перекрестие реактивных белков и мутантных форм лиганд-связывающего домена hG-CSFR или их областей (например, аланиновый точечный мутант SEQ ID NO:1 в положении 168), с которыми связывается белок, используют для выделения белков, которые перекрестно взаимодействуют правильным образом. На основе вышеизложенного также может быть разработан процесс скринирования для иммунизации животных, не являющихся человеком.
В другом примере, скринируют фаговую библиотеку дисплея или иммунизируют животное полипетидом, содержащим лиганд-связывающий домен cynoG-CSFR, и идентифицированные белки и/или антитела скринируют для определения тех из них, которые являются перекрестно реактивными с hG-CSFR и/или его лиганд-связывающим доменом.
В следующем примере, G-CSFR или его лиганд-связывающий домен (необязательно мутантная форма, с которой связан С1.2 или C1.2G) контактирует с С1.2 или C1.2G. Затем библиотеку фагового дисплея приводят в контакт с G-CSFR или лиганд-связывающим доменом, и выбирают фаг-экспрессирующие белки, которые могут конкурировать с С1.2 или C1.2G за связывание.
В следующем примере, химерный белок содержит, например, мышиный G-CSFR, в котором заданный эпитоп из hG-CSFR замещен соответствующей мышиной последовательностью. Этот химерный белок затем используют для иммунизации мышей (у которых менее вероятно начнется иммунная реакция против мышиного белка) и/или для скрининга фаговой библиотеки дисплея. Полученные антитела/белки затем скринируют для определения тех из них, которые связываются с hG-CSFR (в частности, у заданного эпитопа) и не связываются с мышиным G-CSFR.
Антитело настоящего описания может быть синтетическим антителом. Например, антитело представляет собой химерное антитело, гумаризированное антитело, человеческое антитело или деиммунизированное антитело.
Химерные антитела
В одном примере, антитело, описанное в настоящем документе, представляет собой химерное антитело. Термин «химерное антитело» относится к антителам, в которых часть тяжелой и/или легкой цепи идентична или гомологична соответствующим последовательностям в антителах, полученных из конкретных видов (например, мышиных, таких как мышь), или принадлежащих определенному классу или подклассу антител, тогда как остальная цепь(и) идентична или гомологична соответствующим последовательностям в антителах, полученных из других видов (например, приматов, таких как человек), или принадлежащих другому классу или подклассу антител. Как правило, в химерных антителах используют вариабельные области грызунов или кроликов и константные области человека, для получения антитела с преимущественно человеческими доменами. Способы получения химерных антител описаны, например, в US 4816567; и US 5807715.
Гуманизированные и человеческие антитела
Антитело настоящего описания может быть гуманизированными или человеческими.
Термин «гуманизированное антитело следует понимать как относящийся к подклассу химерных антител, имеющих антиген-связывающий сайт или вариабельную область, полученную из антитела из видов, не являющихся человеком, а остальная структура антитела основана на структуре и/или последовательности человеческого антитела. В гуманизированном антителе, антиген-связывающий сайт обычно содержит определяющие комплементарность области (CDR) из нечеловеческих антител, привитых на соответствующие FR в вариабельных областях человеческого антитела, и остальные области из человеческого антитела. Антиген-связывающие сайты могут быть дикого типа (то есть идентичными сайтами нечеловеческого антитела) или модифицированными одним или более аминокислотными замещениями. В некоторых случаях остатки FR человеческого антитела заменены соответствующими нечеловеческими остатками.
В данной области известны способы гуманизации нечеловеческих антители или их частей (например, вариабельных областей). Гуманизация может быть выполнена по способу US 5225539 или US 5585089. Не исключены другие способы гуманизации антител.
Термин «человеческое антитело», используемый в настоящем документе, относится к антителам, имеющим вариабельные области (например, VH, VL) и необязательно константные области, полученные из или соответствующие последовательностям, обнаруживаемьм у людей, например, в зародышевой линии или соматических клетках человека. «Человеческие» антитела могут содержать аминокислотные остатки, не кодируемые человеческими последовательностями, например, мутации, включенные случайными или направленными мутациями in vitro (в частности, мутации, которые затрагивают консервативные замещения, или мутации в небольшом количестве остатков антитела, например, в 1, 2, 3, 4, 5 или 6 из остатков антитела, например, в 1, 2, 3, 4, 5 или 6 из остатков, составляющих один или более из CDR указанного антитела). Эти «человеческие антитела» фактически необязательно вырабатываются в организме человека, скорее, их получают с использованием рекомбинантных способов и/или выделяют из трансгенных животных (например, мышей), содержащих нуклеиновые кислоты, кодирующие константные и/или вариабельные области человеческого антитела (например, как описано выше). Человеческие антитела могут быть получены различными способами, известными в данной области, включая фазговые библиотеки дисплей (например, как описано в US 5885793).
Человеческие антитела, распознающие выбранный эпитоп, могут быть получены также с использованием методики, упоминаемой как «направленная селекция». В этом подходе выбранное нечеловеческое моноклональное антитело, например мышиное антитело, используют для направления селекции полностью человеческого антитела, распознающего тот же эпитоп (например, как описано в US 5565332).
Иллюстративные человеческие антитела описаны в настоящем документе и включают С1.2 и C1.2G и/или их вариабельные области. Эти человеческие антитела обеспечивают преимущество пониженной иммуногенности у человека, по сравнению с нечеловеческими антителами.
Белки, содержащие связывающий домен антитела
Антитела с одним доменом
В некоторых примерах, белок настоящего описания представляет собой или содержит антитело с одним доменом (которое используется взаимозаменяемо с термином «доменное антитело» или «dAb»). Антитело с одним доменом представляет собой одну полипептидную цепь, содержащую всю или часть вариабельной области тяжелой цепи антитела. В некоторых примерах, антитело с одним доменом представляет собой человеческое антитело с одним доменом (Domantis, Inc., Уолтем, штат Массачусетс; смотри, например, US 6248516).
Диатела, триотела, тетратела
В некоторых примерах, белок настоящего описания представляет собой или содержит диатело, триотело, тетратело или белковый комплекс более высокого порядка, такие как описаны в WO 98/044001 и/или WO 94/007921.
Например, диатело представляет собой белок, содержащий две связанные полипептидные цепи, каждая полипетидная цепь содержит структуру VL-x-VH или VH-x-VL, причем VL представляет собой вариабельную область легкой цепи антитела, VH представляет собой вариабельную область тяжелой цепи антитела, Х представляет собой линкер, содержащий недостаточное количество остатков, чтобы обеспечивать возможность связывания VH и VL в одной полипептидной цепи (или образовывать Fv), или отсутствует, и при этом VH одной полипептидной цепи связывается с VL Другой полипептидной смеси с образованием антиген-связывающего сайта, то есть с образованием молекулы Fv, способной специфически связываться с одним или более антигенами. VH и VL могут быть одинаковыми в каждой полипептидной цепи, или VH и VL могут быть различными в каждой цепи, так что они образуют биспецифическое диатело (то есть содержащее две Fv, имеющие различные специфичности).
Одноцепочечная Fv (scFv)
Специалистам в данной области понятно, что scFv содержат области VH и VL в одной полипептидной цепи и полипептидный линкер между VH и VL, который обеспечивает возможность scFv образовывать заданную структуру для связывания антигена (то есть для VH и VL одной полипептидной цепи связываться друг с другом с образованием Fv). Например, линкер содержит в избытке 12 аминокислотных остатков, при этом (Gly4Ser)3 представляет собой один из более благоприятных линкеров scFv.
Настоящее описание подразумевает также дисульфидную стабилизированную Fv (или diFv, или dsFv), в которой один цистеиновый остаток внедрен в FRVH и один - в FR VL, и эти цистеиновые остатки связаны дисульфидной связью с образованием устойчивой Fv.
Альтернативно или дополнительно, настоящее изобретение охватывает димерную scFv, то есть белок, содержащий две молекулы scFv, связанные нековалентной или ковалентной связью, например, доменом лейциновой застежки (например, полученной из Fos или Jun). Альтернативно, две scFv связаны пептидным линкером достаточной длины для обеспечения возможности образования и связывания обеих scFv с антигеном, например, как описано в US 20060263367.
Антитела тяжелой цепи
Антитела тяжелой цепи структурно отличаются от многих других форм антител, поскольку они содержат тяжелую цепь, но не содержат легкую цепь. Соответственно, эти антитела упоминаются также как «антитела только тяжелой цепи». Антитела тяжелой цепи встречаются, например, у верблюдовых и хрящевых рыб (также называемые IgNAR).
Вариабельные области, присутствующие в природных антителах тяжелой цепи, как правило, упоминаются как «VHH домены» в антителах верблюдовых, и V-NAR в IgNAR, чтобы отличать их от вариабельных областей тяжелой цепи, которые находятся в обычных 4-цепочечных антителах (которые упоминаются также как «VH домены», и от вариабельных областей легкой цепи, которые находятся в обычных 4-цепочечных антителах (которые упоминаются также как «VL домены»).
Общее описание антител тяжелой цепи из верблюдовых и их вариабельные области, а также способы их получения и/или выделения, и/или применения, содержатся inter alia в следующих ссылках WO 94/04678, WO 97/49805 и WO 97/49805.
Общее описание антител тяжелой цепи из хрящевых рыб и их вариабельные области, а также способы их получения и/или выделения, и/или применения содержатся inter alia в WO 2005/118629.
Другие антитела и фрагменты антител
Настоящее описание предполагает также другие антитела и фрагменты антител, такие как:
(i) биспецифичные белки «ключ и скважина», описанные в US 5731168;
(ii) гетероконъюгатные белки, например, описанные в US 4676980;
(iii) гетероконъюгатные белки, полученные при помощи химического поперечного сшивателя, например, описанные в US 4676980; и
(iv) Fab3 (например, описанные в ЕР 19930302894).
Деиммунизированные антитела и белки
В настоящем описании рассмотрены также деиммунизированые антитела или белки. Деиммунизированные антитела и белки имеют один или более эпитопов, например, эпитопы В-клеток или эпитопы Т-клеток, удаленные (то есть мутированные) для уменьшения, посредством этого, вероятности того, что у млекопитающего возникнет иммунная реакция против указанного антитела или белка. Способы получения деиммунизированных антител и белков известны в данной области и описаны, например, в WO 00/34317, WO 2004/108158 и WO 004/064724.
Способы внедрения соответствующих мутаций и экспрессии и анализа полученного белка понятны специалистам в данной области на основании описания, представленного в настоящем документе.
Мутации белков
В настоящем описании рассмотрены также мутантные формы белка настоящего описания. В этом отношении данные, представленные в настоящем документе, указывают сайты в пределах CDR или белка настоящего описания, которые могут быть изменены помимо иллюстративных изменений, которые могут быть сделаны. Специалистам в данной области понятно, что изменения могут быть дополнительно или альтернативно сделаны в пределах FR белка, содержащей вариабельную область, без ингибирования или существенного снижения его функции в контексте настоящего описания.
Например, такой мутантный белок содержит одно или более консервативных аминокислотных замещений по сравнению с последовательностью, представленной в настоящем документе. В некоторых примерах, белок содержит 30 или менее, или 20 или менее, или 10 или менее, например, 9 или 8, или 7, или 6, или 5, или 4, или 3, или 2 консервативных аминокислотных замещений. «Консервативное аминокислотное замещение» представляет собой замещение, в котором аминокислотный остаток замещен аминокислотным остатком, имеющим такую же боковую цепь и/или гидрофобность, и/или гидрофильность.
В одном примере, мутантный белок имеет одно или не более чем одно, или два, или три, или четыре, или пять, или шесть консервативных аминокислотных изменений по сравнению с природным белком. Подробности консервативных аминокислотных изменений представлены ниже. Специалистам в данной области понятно, например, из представленного в настоящем документе описания, что такие незначительные изменения могут быть разумно предсказаны и не изменяют активность белка.
В данной области известны семейства аминокислотных остатков, имеющих одинаковые боковые цепи, включая основные боковые цепи (например, лизин, аргинин, гистидин), кислотные боковые цепи (например, аспарагиновая кислота, глутаминовая кислота), незаряженные полярные боковые цепи (например, глицин, аспарагин, глутамин, серии, треонин, тирозин, цистеин), неполярные боковые цепи (например, аланин, валин, лейцин, изолейцин, пролин, фенилаланин, метионин, триптофан), β-разветвленные боковые цепи (например, треонин, валин, изолейцин) и ароматические боковые цепи (например, тирозин, фелиналанин, триптофан, гистидин).
В настоящем описании рассмотрены также неконсервативные аминокислотные изменения (например, замещения) в белке настоящего описания, например, в CDR, такой как CDR3. Например, авторы настоящего изобретения определили несколько неконсервативных аминокислотных замещений, которые могут быть сделаны при сохранении активности белка настоящего описания. В одном примере, указанный белок содержит менее чем 6 или 5, или 4, или 3, или 2, или 1 неконсервативное аминокислотное замещение, например, в CDR3, такой как CDR3.
В настоящем описании рассмотрена также одна или более вставок или делеций по сравнению с последовательностью, представленной в настоящем документе. В некоторых примерах, белок содержит 10 или менее, например, 9 или 8, или 7, или 6, или 5, или 4, или 3, или 2 вставки и/или делеций.
Константные области
В настоящем описании рассмотрены белки и/или антитела, описанные в настоящем документе, содержащие константную область антитела. Сюда входят антиген-связывающие фрагменты антитела, гибридизованного с Fc.
Последовательности константных областей, применимые для получения белков настоящего описания, могут быть получены из ряда различных источников. В некоторых примерах, константная область белка или ее часть получена из человеческого антитела. Константная область или ее часть может быть получена из любого класса антител, включая IgM, IgG, IgD, IgA и IgE, и любого изотипа антител, включая IgG1, IgG2, IgG3 и IgG4. В одном примере, константная область представляет собой константную область IgG4 или стабилизированного IgG4 человеческого изотипа.
В одном примере, область Fc константной области обладает пониженной способностью вызывать эффекторную функцию, например, по сравнению с нативной или дикого типа областью Fc человеческого IgG1 или IgG3. В одном примере, эффекторная функция представляет собой антителозависимую клеточно-обусловленную цитотоксичность (ADCC) и/или антителозависимый клеточно-обусловленный фагоцитоз (ADCP) и/или комплементзависимую цитотоксичность (CDC). Способы оценки уровня эффекторной функции белка, содержащего Fc область, известны в данной области и/или описаны в настоящем документе.
В одном примере, облает Fc представляет собой область Fc IgG4 (то есть из константной области IgG4), например, Fc область человеческого IgG4. Последовательности соответствующих Fc областей IgG4 понятны специалистам в данной области и/или доступны в опубликованных базах данных (например, доступных в Национальном центре биотехнологической информации).
В одном примере, константная область представляет собой константную область стабилизированного IgG4. Термин «константная область стабилизированного IgG4» следует понимать как обозначающую константную область IgG4, которая модифицирована для уменьшения элонгации плеча Fab или склонности к элонгации плеча Fab, или формирования полу-антитела, или склонности к формированию полу-антитела. «Элонгация плеча Fab» относится к типу белковой модификации человеческого IgG4, в которой тяжелая цепь IgG4 и присоединенная легкая цепь (полумолекула) заменяется на пару тяжелой-легкой цепи из другой молекулы IgG4. Так, молекулы IgG4 могут захватывать два отдельных плеча Fab, распознавая два отдельных антигена (что приводит к биспецифическим молекулам). Элонгация плеча Fab происходит естественным образом in vivo и может быть инициирована in vitro очищенными кровяными клетками или восстановительными агентами, такими как восстановленный глутатион. «Полу-антитело» образуется при диссоциации антитела IgG4 с образованием двух молекул, каждая из которых содержит одну тяжелую цепь и одну легкую цепь.
В одном примере, константная область стабилизированного IgG4 содержит пролин в положении 241 шарнирной области в соответствии с системой Rabat (Kabat et al., Sequences of Proteins of Immunological Interest Washington DC United States Department of Health and Human Services, 1987 и/или 1991). Это положение соответствует положению 228 шарнирной области по системе нумерации ЕС (Kabat et al., Sequences of Proteins of Immunological Interest Washington DC United States Department of Health and Human Services, 2001 и Edelman et al., Proc. Natl. Acad. USA, 63, 78-85, 1969). В человеческом IgG4 этот остаток представляет собой, в основном, серин. После замещения серина на пролин, шарнирная область IgG4 содержит последовательность СРРС. В этом отношении, специалистам в данной области понятно, что «шарнирная область» представляет собой богатую пролином часть константной области тяжелой цепи антитела, которая связывается с областями Fc и Fab, обеспечивая подвижность двух плечей Fab антитела. Шарнирная область содержит цистеиновые остатки, которые участвуют в дисульфидных связях между тяжелыми цепями. Она обычно определяется как элонгация Glu226 до Рго243 человеческого IgG1, согласно системе нумерации Kabat. Шарнирные области других изотипов IgG могут быть выровнены с последовательностью IgG1 путем помещения первого и последнего цистеинового остатков, образующих дисульфидные связи (S-S) между тяжелыми цепями в одинаковые положения (смотри, например, WO 2010/080538).
Дополнительные примеры стабилизированных антител IgG4 представляют собой антитела, в которых аргинин в положении 409 константной области тяжелой цепи человеческого IgG4 (согласно системе нумерации ЕС) замещен лизином, треонином, метионином или лейцином (например, как описано в WO 2006/033386). Fc область константной области может дополнительно или альтернативно содержать остаток, выбранный из группы, состоящей из: аланина, валина, глицина, изолейцина и лейцина в положении, соответствующем 405 (по системе нумерации ЕС). Необязательно, шарнирная область содержит пролин в положении 241 (то есть последовательность СРРС) (как описано выше).
В другом примере, Fc область представляет собой область, модифицированную так, чтобы она обладала пониженной эффекторной функцией, то есть «не-иммуностимулирующая Fc область». Например, Fc область представляет собой Fc область IgG1, содержащую замещение в одном или более положениях, выбранных из группы, состоящей из 268, 309, 330 и 331. В другом примере, Fc область представляет собой Fc область IgG1, содержащую одно или более из следующих изменений Е233Р, L234V, L235A и делецию G236 и/или одно или более из следующих изменений A327G, A330S и P331S (Armour et al., Eur J Immunol. 29:2613-2624, 1999; Shields et al., J Biol Chem. 276(9):6591-604, 2001). Дополнительные примеры не-иммуностимулирующих областей Fc описаны, например, в публикации Dall′Acqua et al., J Immunol. 177: 1129-1138 2006; и/или HezarehJ Virol; 75:12161-12168, 2001).
В другом примере, Fc область представляет собой химерную Fc область, например, содержащую, по меньшей мере, один домен СН2 из антитела IgG4 и, по меньшей мере, один домен СН3 из антитела IgG1, причем указанная Fc область содержит замещение в одном или более аминокислотных положениях, выбранных из группы, состоящей из 240, 262, 264, 266, 297, 299, 307, 309, 323, 399, 409 и 427 (нумерация ЕС) (например, как описано в WO 2010/085682). Иллюстративные замещения включают 240F, 262L, 264Т, 266F, 297Q, 299А, 299K, 307Р, 309K, 309М, 309Р, 323F, 399S и 427F.
Дополнительные модификации
В настоящем описании рассмотрены также дополнительные модификации антитела.
Например, антитело содержит одно или более аминокислотных замещений, которые увеличивают период полувыведения белка. Например, антитело содержит Fc область, содержащую одно или более аминокислотных замещений, которые увеличивают аффинность Fc области к неонатальной Fc области (FcRn). Например, Fc область имеет повышенную аффинность к FcRn при более низком рН, например, около рН 6,0, для облегчения связывания Fc/FcRn в эндосоме. В одном примере, Fc область имеет повышенную аффиность к FcRn приблизительно при рН 6 по сравнению с ее аффинностью приблизительно при рН 7,4, что облегчает повторное высвобождение Fc в кровь после клеточного рециклинга. Эти аминокислотные замещения полезны для увеличения периода полувыведения белка, путем снижения клиренса из крови.
Иллюстративные аминокислотные замещения включают T250Q и/или M428L или Т252А, T254S и T266F или M252Y, S254T и Т256Е или H433K и N434F, по системе нумерации ЕС. Дополнительные или альтернативные аминокислотные замещения описаны, например, в US 20070135620 или US 7083784.
Продуцирование белков
В одном примере, белок, описанный в настоящем документе по любому примеру, продуцируется выращиванием гибридомы в условиях, достаточных для продуцирования белка, например, как описано в настоящем документе и/или известно в данной области.
Рекомбинантная экспрессия
В другом примере, белок, описанный в настоящем документе по любому примеру, является рекомбинантным.
В случае рекомбинантного белка, кодирующая его нуклеиновая кислота может быть клонирована в экспрессирующие конструкции или векторы, которые затем трансфицируют в клетки хозяина, такие как клетки Е. coli, клетки дрожжей, клетки насекомых или клетки млекопитающих, такие как клетки COS обезьян, клетки яичников китайских хомяков (СНО), эмбриональные почечные клетки человека (BEK) или клетки миеломы, которые иначе не продуцируют указанный белок. Иллюстративные клетки, используемые для экспрессии белка, представляют собой клетки СНО, клетки миеломы или клетки НЕК. Молекулярные клонирующие методики для достижения этих целей известны в данной области и описаны, например, в публикации Ausubel et al., (редакторы), Current Protocols in Molecular Biology, Greene Pub. Associates and Wiley-Interscience (1988, включая все обновления до сегодняшнего дня) или Sambrook et al., Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Laboratory Press (1989). Для конструирования рекомбинантных нуклеиновых кислот применимо широкое разнообразие способов клонирования и in vitro амплификации. В данной области известны также способы продуцирования рекомбинантных тел, смотри, например, US 4816567 или US 5530101.
После выделения, функционально связанную с промотором нуклеиновую кислоту встраивают в экспрессирующую конструкцию или экспрессирующий вектор для дальнейшего клонирования (амплификации ДНК) или для экспрессии в бесклеточной системе или в клетках.
При использовании в настоящем документе, термин «промотор» следует понимать в самом широком контексте, и он включает транскрипционные регуляторные последовательности геномного гена, включая ТАТА-бокс или сигнальную последовательность, которые необходимы для точной инициации транскрипции, с дополнительными регуляторными элементами (например, восходящими активирующими последовательностями, сайтами, связывающими фактор транскрипции, энхансерами или сайленсерами) или без них, которые изменяют экспрессию нуклеиновой кислоты, например, в ответ на связанные с развитием и/или внешние стимулы, или тканеспецифическим образом. В контексте настоящего описания, термин «промотор» используется также для описания рекомбинантной, синтетической или гибридной нуклеиновой кислоты, или ее производного, который обеспечивает, активирует или усиливает экспрессию нуклеиновой кислоты, с которой он функционально связан. Иллюстративные промоторы могут содержать дополнительные копии одного или более специфических регуляторных элементов для дальнейшего усиления экспрессии и/или изменения пространственной экспрессии и/или временной экспрессии указанной нуклеиновой кислоты.
При использовании в настоящем документе, термин «функционально связанный с» обозначает такое положение промотора относительно нуклеиновой кислоты, что экспрессия нуклеиновой кислоты контролируется этим промотором.
Имеется много векторов для экспрессии в клетках. Эти векторные компоненты обычно включают, но, не ограничиваясь этим, одно или более из следующих: сигнальной последовательности, последовательности, кодирующей белок (например, полученной из информации, представленной в настоящем документе), элемента энхансера, промотора и последовательности, терминирующей транскрипцию. Специалистам в данной области известны соответствующие последовательности для экспрессии белка. Иллюстративные сигнальные последовательности включают прокариотические сигналы секреции (например, pelB, щелочная фосфатаза, пенициллиназа, Ipp или теплостойкий энтеротоксин II), дрожжевые сигналы секреции (например, лидерная инвертаза, лидерный α-фактор или лидерная кислотная фосфатаза) или сигналы секреции млекопитающих (например, gD сигнал простого герпеса).
Иллюстративный промоторы, активные в клетках млекопитающих, включают предранний промотор цитомегаловируса (CMV-IE), промотор человеческого фактора элонгации 1-α (EF1), промоторы низкомолекулярной ядерной РНК (U1a и U1b), промотор тяжелой цепи α-миозина, промотор вакуолизирующего обезьяньего вируса 40 (SV40), промотор вируса саркомы Рауса (RSV), основной поздний промотор аденовируса, промотор  - актина; гибридный регуляторый элемент, содержащий энхансер CMV/промотор
- актина; гибридный регуляторый элемент, содержащий энхансер CMV/промотор  -актина или промотор иммуноглобулина, или его активный фрагмент. Примеры применимых линий клеток-хозяев млекопитающих представляют собой линию почек обезьяны CV1, трансформированную SV40 (COS-7, ATCC CRL 1651); линию эмбриональных почечных клеток человека (клетки 293 или 293, субклонированные для роста в суспензионной культуре; детские клетки почек хомяков (ВНК, АТСС CCL 10); или клетки яичников китайского хомяка (СНО).
-актина или промотор иммуноглобулина, или его активный фрагмент. Примеры применимых линий клеток-хозяев млекопитающих представляют собой линию почек обезьяны CV1, трансформированную SV40 (COS-7, ATCC CRL 1651); линию эмбриональных почечных клеток человека (клетки 293 или 293, субклонированные для роста в суспензионной культуре; детские клетки почек хомяков (ВНК, АТСС CCL 10); или клетки яичников китайского хомяка (СНО).
Типичные промоторы, пригодные для экспрессии в дрожжевых клетках, таких как, например, дрожжевые клетки, выбранные из группы, включающей Pichia pastoris, Saccharomyces cerevisiae и S. pombe, включают, но, не ограничиваясь этим, промотор ADH1, промотор GAL1, промотор GAL4, промотор CUP1, промотор РН05, промотор nmt, промотор RPR1 или промотор TEF1.
Специалистам в данной области известны способы введения изолированной нуклеиновой кислоты или содержащей ее экспрессирующей конструкции в клетку для экспрессии. Методика, используемая для данных клеток, зависит от известных успешных методик. Способы введения рекомбинантной ДНК в клетки включают микроинъекцию, трансфекцию, опосредованную DEAE-декстраном, трансфекцию, опосредованную липосомами, такую как с использованием липофектамина (Gibco, штат Мэриленд, США) и/или целфектина (Gibco, штат Мэриленд, США), ПЭГ-опосредованное поглощение ДНК, электропорацию и бомбардировку микрочастицами, как при использовании покрытых ДНК вольфрамовых или золотых частиц (Agracetus Inc., штат Висконсин, США), среди прочих.
Клетки-хозяева, используемые для продуцирования белка, могут быть выращены в различных средах, в зависимости от используемого типа клеток. Подходящими для выращивания клеток млекопитающих являются среды, имеющиеся в продаже, такие как Ham′s F10 (Sigma), минимальная питательная среда ((MEM), (Sigma), RPMI-1640 (Sigma) и среда Игла, модифицированная по способу Дульбекко ((DMEM), Sigma), Среды для выращивания других клеточных типов, рассмотренных в настоящем документе, известны в данной области.
Выделение белков
Способы выделения белков известны в данной области и/или описаны в настоящем документе.
Если белок секретируется в клеточную среду, то надосадочные жидкости из таких экспрессирующих систем могут быть сначала концентрированы с использованием имеющегося в продаже фильтра для концентрации белка, например, ультрафильтровальной установки Amicon или Millipore Pellicon. Ингибитор протеазы, такой как PMSF, может быть включен в любую из предыдущих стадий для ингибирования протеолиза, а антибиотики могут быть включены для предотвращения роста побочных загрязнителей. Альтернативно или дополнительно, надосадочные жидкости могут быть отфильтрованы и/или отделены от клеток, экспрессирующих белок, например, с использованием непрерывного центрифугирования.
Белок, полученный из клеток, может быть очищен, например, с использованием ионного обмена, гидроксиапатитовой хроматографии, хроматографии гидрофобного взаимодействия, гель-электрофореза, диализа, аффинной хроматографии (например, аффинной хроматографии белка А или хроматографии белка G), или любой комбинацией предыдущих способов. Эти способы известны в данной области и описаны, например, в WO 99/57134 или Ed Harlow and David Lane (редакторы) Antibodies: A Laboratory Manual, Cold Spring Harbor Laboratory, (1988).
Специалистам в данной области известно также, что белок может быть модифицирован так, чтобы он содержал метку для облегчения очистки или обнаружения, например, полигистидиновую метку, например, гексагистидиновую метку, или метку гемагглутинина вируса гриппа (НА), или метку вакуолизирующего обезьяньего вируса 5 (V5), или метку FLAG, или метку глутатион-3-трансферазы (GST). Полученный белок затем очищают с использованием известных в данной области способов, таких как аффинная очистка. Например, белок, содержащий гекса-his метку, очищают взаимодействием образца, содержащего белок, с никель-нитрилотриуксусной кислотой (Ni-NTA), которая специфически связывается с гекса-his меткой, фиксированной на твердой или полутвердой подложке, промыванием образца для элонгации несвязанного белка и последующим элюированием связанного белка. Альтернативно или дополнительно, лиганд или антитело, которое связывается с меткой, используют в способе аффинной очистки.
Оценка активности белка
Связывание с G-CSFR и его мутантами
Специалистам в данной области из настоящего описания понятно, что некоторые белки настоящего описания связываются с лиганд-связывающим доменом hG-CSFR и со специфическими мутантными формами лиганд-связывающего домена hG-CSFR (например, SEQ ID NO:1, без мутаций или с мутациями в определенной точке), и/или связываются с G-CSFR человека и яванского макака. Способы оценки связывания с белком известны в данной области, например, как описано в публикации Scopes (B: Protein purification: principles and practice. Third Edition, Springer Verlag, 1994). Такой способ обычно включает мечение белка и его взаимодействие с фиксированным антигеном. После промывания для удаления неспецифически связанного белка, определяют количество метки и, следовательно, связанного белка. Конечно, фиксированным может быть белок, а метка может быть в антигене. Могут быть также использованы пэннинг-анализы. Альтернативно или дополнительно, могут быть использованы анализы поверхностного плазменного резонанса.
Анализы, описанные выше, могут быть также использованы для обнаружения степени связывания белка с hG-CSFR или его лиганд-связывающим доменом (например, SEQ ID NO:1) или его мутантной формой.
В одном примере, белок настоящего описания связывается с полипептидом SEQ ID NO:1, в котором аланин замещен лизином в положении 167 SEQ ID NO:1, и/или в котором аланин замещен гистидином в положении 168 SEQ ID NO:1, практически в той же степени (например, в пределах 10% или 5%, или 1%), с которой он связывается с SEQ ID NO:1.
В одном примере, белок настоящего описания связывается с полипептидом SEQ ID NO:1, в котором аланин замещен аргинином в положении 287 SEQ ID NO:1, в степени, которая по меньшей мере приблизительно в 100 раз или 150 раз, или 160 раз, или 200 раз ниже, чем он связывается с полипептидом SEQ ID NO:1. В одном примере, белок настоящего описания связывается с полипептидом SEQ ID NO:1, в котором аланин замещен аргинином в положении 287 SEQ ID NO:1, в степени, которая, по меньшей мере, приблизительно в 160 раз ниже, чем он связывается с полипептидом SEQ ID NO:1.
В одном примере, белок настоящего описания связывается с полипептидом SEQ ID NO:1, в котором аланин замещен гистидином в положении 237 SEQ ID NO:1, в степени, которая, по меньшей мере, приблизительно в 20 раз или 40 раз, или 50 раз, или 60 раз ниже, чем он связывается с полипептидом SEQ ID NO:1. В одном примере, белок настоящего описания связывается с полипептидом SEQ ID NO:1, в котором аланин замещен гистидином в положении 237 SEQ ID NO:1, в степени, которая, по меньшей мере, приблизительно в 50 раз ниже, чем он связывается с полипептидом SEQ ID NO:1.
В одном примере, белок настоящего описания связывается с полипептидом SEQ ID NO:1, в котором аланин замещен метионином в положении 198 SEQ ID NO:1, в степени, которая, по меньшей мере, приблизительно в 20 раз или 40 раз, или 60 раз, или 70 раз ниже, чем он связывается с полипептидом SEQ ID NO:1. В одном примере, белок настоящего описания связывается с полипептидом SEQ ID NO:1, в котором аланин замещен метионином в положении 198 SEQ ID NO:1, в степени, которая, по меньшей мере, приблизительно в 40 раз ниже, чем он связывается с полипептидом SEQ ID NO:1.
В одном примере, белок настоящего описания связывается с полипептидом SEQ ID NO:1, в котором аланин замещен тирозином в положении 172 SEQ ID NO:1, в степени, которая, по меньшей мере, приблизительно в 20 раз или 30 раз, или 40 раз ниже, чем он связывается с полипептидом SEQ ID NO:1. В одном примере, белок настоящего описания связывается с полипептидом SEQ ID NO:1, в котором аланин замещен тирозином в положении 172 SEQ ID NO:1, в степени, которая, по меньшей мере, приблизительно в 40 раз ниже, чем он связывается с полипептидом SEQ ID NO:1.
В одном примере, белок настоящего описания связывается с полипептидом SEQ ID NO:1, в котором аланин замещен лейцином в положении 171 SEQ ID NO:1, в степени, которая, по меньшей мере, приблизительно в 100 раз или 120 раз, или 130 раз, или 140 раз ниже, чем он связывается с полипептидом SEQ ID NO:1. В одном примере, белок настоящего описания связывается с полипептидом SEQ ID NO:1, в котором аланин замещен лейцином в положении 171 SEQ ID NO:1, в степени, которая, по меньшей мере, приблизительно в 140 раз ниже, чем он связывается с полипептидом SEQ ID NO:1.
В одном примере, белок настоящего описания связывается с полипептидом SEQ ID NO:1, в котором аланин замещен лейцином в положении 111 SEQ ID NO:1, в степени, которая, по меньшей мере, приблизительно в 20 раз или 40 раз, или 60 раз, или 70 раз ниже, чем он связывается с полипептидом SEQ ID NO:1. В одном примере, белок настоящего описания связывается с полипептидом SEQ ID NO:1, в котором аланин замещен лейцином в положении 111 SEQ ID NO:1, в степени, которая, по меньшей мере, приблизительно в 60 раз ниже, чем он связывается с полипептидом SEQ ID NO:1.
В одном примере, белок настоящего описания связывается с полипептидом SEQ ID NO:1, в котором аланин замещен гистидином в положении 168 SEQ ID NO:1, в степени, которая не более чем в 5 раз или 4 раза, или 3 раза, или 2 раза или 1 раз ниже, чем он связывается с полипептидом SEQ ID NO:1.
В одном примере, белок настоящего описания связывается с полипептидом SEQ ID NO:1, в котором аланин замещен лизином в положении 167 SEQ ID NO:1, в степени, которая не более чем в 5 раз или 4 раза, или 3 раза, или 2 раза или 1 раз ниже, чем он связывается с полипептидом SEQ ID NO:1.
Степень связывания легко определяется при помощи биосенсора.
В настоящем описании рассмотрены также любые комбинации вышеизложенных характеристик. В одном примере, белок, описанный в настоящем документе, имеет все связывающие характеристики, представленные в предыдущих семи параграфах.
Картирование эпитопов
В другом примере, картируют эпитоп, связанный с белком, описанным в настоящем документе. Способы картирования эпитопов понятны специалистам в данной области. Например, продуцируют серии перекрывающихся пептидов, захватывающих последовательность hG-CSFR или его область, содержащую заданный эпитоп, например, пептиды, содержащие 10-15 амнокислот. Затем белок приводят в контакт с каждым пептидом и определяют пептид(ы), с которым он связывается. Это позволяет определять пептид(ы), содержащий эпитоп, с которым связывается белок. Если с белком связывается множество несмежных пептидов, то этот белок может связываться с конформационным эпитопом.
Альтернативно или дополнительно, аминокислотные остатки в пределах hG-CSFR являются мутированными, например, аланин-сканирующим мутагенезом, и определяют мутации, которые снижают или предотвращают связывание белка. Любая мутация, которая снижает или предотвращает связывание белка, вероятно, находится в пределах эпитопа, связанного с белком.
Далее представлен следующий пример, и он включает связывание hG-CSFR или его области с фиксированным белком настоящего описания и расщепление полученного комплекса протеазами. Пептид, который остался связанным с фиксированным белком, затем выделяют и анализируют, например, при помощи масс-спектрометрии, для определения его последовательности.
Следующий способ включает превращение водородов в hG-CSFR или его области в дейтроны и связывание полученного белка с фиксированным белком настоящего изобретения. Затем дейтроны превращают обратно в водород, выделяют hG-CSFR или его область, поглощают ферментами и анализируют, например, при помощи масс-спектрометрии, для определения тех областей, содержащих дейтроны, которые были защищены от превращения в водород за счет связывания с белком, описанным в настоящем документе.
Необязательно определяют константу диссоциации (Kd) белка для hG-CSFR или его эпитопа. «Kd» или «значение Kd» для белка, связывающего hG-CSFR, представляет собой один пример, измеряемый анализом связывания hG-CSFR с радиоактивной меткой или флуоресцентной меткой. В этом анализе уравновешивают белок с минимальной концентрацией меченого hG-CSFR в присутствии титрующих серий hG-CSFR без метки. После промывания для удаления несвязанного hG-CSFR, определяют количество метки, которое является показателем Kd белка.
В соответствии с другим примером, Kd или значение Kd измеряют при помощи анализа поверхностного плазменного резонанса, например, используя поверхностный плазменный резонанс BIAcore (BIAcore, Inc., Пискатауай, штат Нью-Джерси) с фиксированным hG-CSFR или его областью.
В некоторых примерах, выбирают белки, имеющие такую же Kd или более высокую Kd, чем С1.2 или C1.2G, поскольку они, вероятно, конкурируют за связывание с hG-CSFR.
Определение конкурентного связывания
Специалистам в данной области понятны анализы для определения белка, который конкурентно ингибирует связывание моноклонального антитела С1.2 или C1.2G. Например, С1.2 или C1.2G конъюгируют с обнаруживаемой меткой, например, с флуоресцентной меткой или радиоактивной меткой. Меченое антитело и исследуемый белок затем смешивают и приводят в контакт с hG-CSFR или его областью (например, полипептидом, содержащим SEQ ID NO:1), или клеткой, экспрессирующей его. Затем определяют уровень меченого С1.2 или C1.2G и сравнивают с уровнем, обнаруженным при взаимодействии меченого антитела с hG-CSFR, областью или клетками в отсутствие белка. Если уровень меченого С1.2 или C1.2G понижается в присутствии исследуемого белка по сравнению с отсутствием белка, то этот белок считают конкурентно ингибирующим связывание С1.2 или C1.2G с hG-CSFR.
Необязательно, исследуемый белок конъюгируют с различными метками с С1.2 или C1.2G. Такое альтернативное мечение обеспечивает возможность обнаружения уровня связывания исследуемого белка с hG-CSFR или его областью, или с клеткой.
В одном примере, белку обеспечивают возможность связываться с hG-CSFR или его областью (например, полипептидом, содержащим SEQ ID NO:1), или клеткой, экспрессирующей его до контакта с hG-CSFR, областью или клеткой с С1.2 или C1.2G. Снижение количества связанного С1.2 или C1.2G в присутствии белка по сравнению с отсутствием белка указывает, что этот белок конкурентно ингибирует связывание С1.2 или C1.2G с hG-CSFR. Также можно выполнить реципрокный анализ с использованием меченого белка, сначала оставив С1.2 или C1.2G связываться с G-CSFR. В этом случае уменьшенное количество меченого белка, связанного с hG-CSFR в присутствии С1.2 или C1.2G по сравнению с отсутствием С1.2 или C1.2G показывает, что белок конкурентно ингибирует связывание С1.2 или C1.2G с hG-CSFR.
Любой из вышеизложенных анализов может быть выполнен с мутантной формой hG-CSFR и/или последовательности SEQ ID NO:1, и/или лиганд-связывающей областью hG-CSFR, с которой связывается С1.2 или C1.2G, например, как описано в настоящем документе.
Определение нейтрализации
В некоторых примерах настоящего описания, белок способен нейтрализовывать передачу сигналов hG-CSFR.
В данной области известны различные анализы для оценки способности белка нейтрализовывать передачу сигналов лиганда через рецептор.
В одном примере, белок снижает или предотвращает связывание G-CSF с hG-CSFR. Эти анализы могут быть выполнены как анализы конкурентного связывания, как описано в настоящем документе, с использованием меченого G-CSF и/или меченого белка.
В другом примере, белок снижает образование CFU-G, если клетки костного мозга CD34+ выращены в присутствии G-CSF. В таких анализах клетки костного мозга CD34+ выращивают в полутвердой клеточной культуральной среде в присутствии G-CSF (например, около 10 нг/мл клеточной культуральной среди) и необязательно фактора стволовых клеток (например, около 10 нг/мл клеточной культуральной среды), в присутствии или в отсутствие исследуемого белка. Через достаточное время для образования клонов гранулоцитов (CFU-G) определяют количество клонов или колоний. Уменьшение количества колоний в присутствии белка по сравнению с количеством в отсутствие белка указывает, что белок нейтрализует передачу сигналов G-CSF. Исследуя множество концентраций белка, определяют IC50, то есть концентрацию, при которой происходит 50% от максимального ингибирования образования CFU-G. В одном примере, IC50 составляет 0,2 нМ или менее, такое значение как 0,1 нМ или менее, например, 0,09 нМ или менее, или 0,08 нМ или менее, или 0,07 нМ или менее, или 0,06 нМ или менее, или 0,05 нМ или менее. В одном примере, IC50 составляет 0,04 нМ или менее. В другом примере, IC50 составляет 0,02 нМ или менее. Представленные выше значения IC50 относятся к любому анализу CFU-G, описанному в настоящем документе.
В следующем примере белок снижает пролиферацию клеток (например, клеток BaF3), экспрессирующих hG-CSFR, которые выращены в присутствии G-CSF. Клетки выращивают в присутствии G-CSF (например, 0,5 нг/мл) и в присутствии или в отсутствие исследуемого белка. В данной области известны способы оценки клеточной пролиферации, и они включают, например, восстановление МТТ и внедрение тимидина. Белок, который снижает уровень пролиферации по сравнению с уровнем, наблюдаемым в отсутствие этого белка, считают нейтрализующим передачу сигналов G-CSF. Исследуя множество концентраций белка, определяют IC50, то есть концентрацию, при которой происходит 50% от максимального ингибирования клеточной пролиферации. В одном примере, IC50 составляет 6 нМ или менее, такое значение как 5,9 нМ или менее. В другом примере, IC50 составляет 2 нМ или менее, или 1 нМ или менее, или 0,7 нМ или менее, или 0,6 нМ или менее, или 0,5 нМ или менее. Представленные выше значения IC50 относятся к любому анализу клеточной пролиферации, описанному в настоящем документе.
В следующем примере, белок снижает мобилизацию гематопоэтических стволовых клеток и/или эндотелиальных клеток-предшественников in vivo после введения G-CSF и/или уменьшает количество нейтрофилов in vivo, например, после введения G-CSF (однако это не обязательно). Например, белок вводят субъекту, необязательно до, во время или после введения G-CSF или его модифицированной формы (например, ПЭГилированного G-CSF или филграстима). Оценивают количество гематопоэтических стволовых клеток (например, экспрессирующих CD34 и/или Thyl) и/или эндотелиальных клеток-предшественников (например, экспрессирующих CD34 и VEGFR2), и/или нейтрофилов (определяемых морфологически и/или экспрессирующих, например, CD10, CD14, CD31 и/или CD88). Белок, который снижает уровень клетки(ок) по сравнению с уровнем, наблюдаемым в отсутствие этого белка, считают нейтрализующим передачу сигналов G-CSF. В одном примере, белок снижает количество нейтрофилов, не вызывая нейтропению.
В настоящем описании предполагаются другие способы оценки нейтрализации передачи сигналов G-CSF.
Определение эффекторной функции
Как рассмотрено в настоящем документе, некоторые белки настоящего описания имеют пониженную эффекторную функцию. Способы оценки ADCC известны в данной области.
В одном примере, уровень активности ADCC оценивают с использованием анализа высвобождения 51Cr, анализа высвобождения европия или анализа высвобождения 35S. В каждом из этих анализов клетки, экспрессирующие G-CSFR, выращивают с одним или более из упомянутых соединений в течение времени и при условиях, достаточных для поглощения соединения клеткой. В случае анализа высвобождения 35S, клетки, экспрессирующие hG-CSFR, могут быть выращены в 35S-меченым метионином и/или серином в течение времени, достаточного для мечения аминокислот, подлежащих внедрению в только что синтезированные белки. Затем клетки выращивают в присутствии или в отсутствие белка и в присутствии иммунных эффекторных клеток, например, мононуклеарных клетках периферической крови (РВМС) и/или клетках NK. Затем определяют количество 51Cr, европия и/или 35S в клеточной культуральной среде, и небольшое изменение или его отсутствие в присутствии белка по сравнению с отсутствием белка (или пониженный уровень соединения по сравнению с уровнем, наблюдаемым в присутствии анти-hG-CSFR антитела, содержащего Fc человеческого IgG1) указывает, что белок имеет пониженную эффекторную функцию. Примеры публикаций, описывающих анализы для оценки уровня ADCC, индуцированного белком, включают Hellstrom, et ей. Proc. Natl Acad. Sci. USA 83:7059-7063,1986 и Bruggemann, et al., J. Exp. Med. 166:1351-1361, 1987.
Другие анализы для оценки уровня ADCC, индуцированного белком, включают нерадиоактивный анализ цитотоксичности ACTI™ для проточной цитометрии (CellTechnology, Inc., штат Калифорния, США) или нерадиоактивный анализ цитотоксичности CytoTox 96® (Promega, штат Висконсин, США).
Также могут быть выполнены анализы связывания C1q для подтверждения того, что белок способен связывать C1q и может вызывать CDC. Для оценки активации комплемента может быть выполнен анализ CDC (смотри, например, Gazzano-Santoro et al, J. Immunol. Methods 202:163,1996.
Определение периода полувыведения
Некоторые белки, охваченные настоящем описанием, могут иметь улучшенный период полувыведения, например они, модифицированы для увеличения их периода полувыведения по сравнению с белками, которые являются не модифицированными. Способы определения белка с улучшенным периодом полувыведения понятны специалистам в данной области. Например, оценивают способность белка связываться с неонатальным рецептором Fc (FcRn). В этом отношении, увеличенная связывающая аффинность к FcRn повышает период полувыведения молекулы из сыворотки (смотри, например, Kim et al., Eur J Immunol., 24:2429, 1994).
Период полувыведения белка настоящего описания также может быть измерен фармакокинетическими испытаниями, например, по способу, описанному Kim et al, Eur J of Immunol 24:542, 1994. В соответствии с этим способом, белок с радиоактивной меткой вводят внутривенной инъекцией мышам, и периодически измеряют его концентрацию в плазме как функцию от времени, например, от 3 минут до 72 часов после инъекции. Кривая клиренса, полученная таким образом, должна быть двухфазной, то есть содержать альфа-фазу и бета-фазу. Для определения in vivo периода полувыведения белка, рассчитывают скорость клиренса в бета-фазе и сравнивают со скоростью клиренса белка дикого типа или не модифицированного белка.
Оценка терапевтической эффективности
Анализы для оценки терапевтической эффективности описаны выше в настоящем документе в отношении определения нейтрализации под действием белка.
В другом примере, эффективность белка для лечения состояния оценивают с использованием in vivo анализа.
Например, белок испытывают в модели артрита на животных. Иллюстративные модели включают линию SKG мышей (Sakaguchi et al., Nature, 426: 454-460), модель коллагенового артрита II типа на крысах, модель коллагенового артрита II типа на мышах или модели антиген-индуцированного артрита у нескольких видов (Bendele J Musculoskel Neuron Interact; 1(4):377-385, 2001). В этих анализах индуцируют артрит и оценивают способность белка снижать один или более симптомов артрита, например, воспаление суставов и/или маркеры воспаления в синовиальной жидкости. Белок, который снижает симптом артрита, считается применимым для лечения этого состояния или G-CSF-опосредованного состояния (например, G-CSF-опосредованного воспалительного состояния).
Белок может быть также или альтернативно испытан в модели COPD, например, в которой на млекопитающее, не являющееся человеком (например, грызунов, таких как мыши), воздействуют сигаретным дымом. После воздействия животным вводят белок и определяют уровень воспаления легких и/или количество нейтрофилов в легких, или оценивают с использованием стандартных методик. Белок, который снижает воспаление легких и/или количество нейтрофилов, считают применимым для лечения воспаления легких или COPD, или G-CSF-опосредованного состояния (например, G-CSF-опосредованного воспалительного состояния, такого как G-CSF-опосредованное воспалительное состояние легких).
Белки, описанные в настоящем документе, могут быть также испытаны в in vivo моделях воспалительного неврологического заболевания. Иллюстративные модели включают модели ЕАЕ, в которых мышь или крысу иммунизируют белком миелиновой оболочки или белком, полученным из нее (например, MOG, МВР или PLP), и создается иммунная реакция против белка, создавая, посредством этого, модель MS. Альтернативно, Т-клетки, которые являются иммунореактивными с белком миелиновой оболочки, вводят мышам или крысам для инициации ЕАЕ. Иллюстративные модели ЕАЕ рассмотрены, например, в публикации Tsunoda and Fujinami, J Neuropathol Exp Neurol. 55:673-686, 1996.
Другие модели MS включают трансгенных животных, экспрессирующих Т-клеточные рецепторы, специфические для миелинового белка, например, MOG, МВР или PLP. Иллюстративные модели описаны, например, в публикации Bettelli et al., JEM 797:1073-1081, 2003; Illes et al., Proc. Natl. Acad. Sci. USA, 101: 11749-11754, 2004; или Rossi et al., J. Biomolecular Screening, 12: 481-489, 2007; или имеются в продаже, например, у компании Jackson Laboratories USA (например, мыши 2D2, имеющие трансгенные Т-клеточные рецепторы, реактивные с MOG).
В следующем примере, белок, описанный в настоящем документе по любому примеру, испытывают в модели увеита. Модели увеита включают модели, индуцированные иммунизацией млекопитающего, не являющегося человеком, белком, таким как аррестин сетчатки, рековерин или родопсин, или введением в глаза бактериального эндотоксина. Иллюстративные модели увеита описаны, например, в публикации Caspi, Drug Discovery Today, 3:3-9, 2006.
Белок настоящего описания может быть также испытан в моделях ангиогенеза, например, моделях глазного ангиогенеза компании Iris Pharma Inc., или модели альгинат-инкапсулированной опухолевой клетки, и/или оценкой способности раковых клеток метастазировать в организме субъекта.
Состояния, подлежащие лечению
В настоящем описании рассмотрено лечение или предупреждение любого состояния, которое обусловлено или обострено действием G-CSF в организме субъекта. В одном примере, состояние представляет собой аутоиммунное или воспалительное состояние.
В одном примере, воспалительное или аутоиммунное состояние представляет собой воспалительное состояние суставов, такое как воспалительный артрит, ревматоидный артрит или идиопатический артрит, например, подростковый идиопатический артрит. В одном примере, состояние представляет собой ревматоидный артрит.
В одном примере, воспалительное или аутоиммунное состояние представляет собой воспалительное состояние глаз. Например, состояние представляет собой увеит.
В одном примере, воспалительное или аутоиммунное состояние представляет собой воспалительное состояние легких, такое как заболевание легких, связанное с нейтрофильной инфильтрацией, например, COPD. В одном примере, состояние представляет собой COPD.
В одном примере, воспалительное или аутоиммунное состояние представляет собой воспалительное неврологическое состояние, такое как болезнь Девика, вирусная инфекция головного мозга или рассеянный склероз. В одном примере, состояние представляет собой рассеянный склероз, который включает хронический прогрессирующий рассеянный склероз или возвратно-ремиттирующий рассеянный склероз.
В другом примере, состояние представляет собой рак (включая его ангиогенез) или его метастаз.
В одном примере, субъект является резистентным, не реагирующим должным образом или непригодным для лечения другим соединением, используемым для лечения указанного состояния. Например, субъект, страдающий от аутоиммунного или воспалительного состояния, является резистентным, не реагирующим должным образом или непригодным для лечения кортикостероидом и/или иммуносупрессантом, и/или циклофосфамидом, и/или метотрексатом, и/или анти-TNF антителом, или растворимым TNF рецептором, и/или анти-CD20 антителом, и/или анти-1L6 антителом, и/или анти-CD22 антителом.
Композиции
В некоторых примерах белок, описанный в настоящем документе, может быть введен перорально, парентерально, ингаляцией спрея, адсорбцией, абсорбцией, локально, ректально, назально, буккально, вагинально, интравентрикулярно, через имплантированный резервуар в дозированных лекарственных формах, содержащих стандартные нетоксические фармацевтически приемлемые носители, и в любой другой стандартной форме лекарственной форме. Термин «парентеральный», используемый в настоящем документе, включает подкожный, внутривенный, внутримышечный, внутрибрюшинный, внутриоболочечный, внутрижелудочковый, интрастернальный и внутричерепной способ введения инъекций.
Способы получения белка в растворимой форме для введения субъекту (например, фармацевтической композиции) известны в данной области и включают, например, способы, описанные в книге Remington Pharmaceutical Sciences (18e издание. Mack Publishing Co., Истон, штат Пенсильвания, 1990) и Фармакопее США: National Formulary (Mack Publishing Company, Истон, штат Пенсильвания,1984).
Фармацевтические композиции настоящего описания особенно применимы для парентерального введения, такого как внутривенное введение или введение в полость тела или просвет органа или сустава. Композиции для введения обычно содержат раствор белка, растворенного в фармацевтически приемлемом носителе, например, в водном носителе. Могут быть использованы различные водные носители, например, буферный солевой раствор и тому подобные. Композиции могут содержать фармацевтически приемлемые вспомогательные вещества, что необходимо для приближения к физиологическим условиям, такие как рН регулирующие и буферные агенты, агенты для регуляции токсичности и тому подобные, например, ацетат натрия, хлорид натрия, хлорид калия, хлорид кальция, лактат натрия и тому подобные. Концентрация белков настоящего описания в этих композициях может варьироваться в широком диапазоне, и выбирается, в основном, на основании объемов, вязкостей жидкостей, веса тела и тому подобного, в соответствии с конкретным выбранным способом введения и потребностями пациента. Примеры носителей включают воду, солевой раствор, раствор Рингера, раствор декстрозы и 5% альбумин сыворотки человека. Также могут быть использованы неводные носители, такие как смешанные масла и этилолеат. В качестве носителей могут быть использованы также липосомы. Носители могут содержать небольшие количества добавок, которые улучшают изотоничность и химическую стабильность, например, буферы и консерванты.
При составлении композиции, белки настоящего описания вводят, таким образом, который совместим с дозированной лекарственной формой, и в таком количестве, которое является терапевтически/профилактически эффективным. Композиции легко вводят в различных лекарственных формах, таких как типы инъецируемых растворов, описанные выше, но предполагаются также другие фармацевтически приемлемые формы, например, таблетки, пилюли, капсулы или другие твердые вещества для перорального введения, суппозитории, пессарии, назальные растворы или спреи, аэрозоли, средства для ингаляции, липосомальные формы и тому подобные. Также могут быть использованы фармацевтические капсулы или композиции «с медленным высвобождением». Композиции с медленным высвобождением обычно разрабатывают для получения постоянного содержания лекарства в течение продолжительного периода, и они могут быть использованы для доставки соединений настоящего описания.
В публикации WO 2002/080967 описаны композиции и способы введения аэрозольных композиций, содержащих антитела, для лечения, например, астмы, которые также применимы для введения белка настоящего описания.
Комплексные терапии
В одном примере, белок настоящего описания вводят в комбинации с другим соединением, применимым для лечения заболевания или состояния, описанного в настоящем документе, в виде комбинированных или дополнительных стадий лечения, или в качестве дополнительных компонентов терапевтической композиции.
Например, другое соединение представляет собой противовоспалительное соединение. Альтернативно или дополнительно, другое соединение представляет собой иммуноподавляющее средство. Альтернативно или дополнительно, другое соединение представляет собой кортикостероид, такой как преднизон и/или преднизолон. Альтернативно или дополнительно, другое соединение представляет собой метотрексат. Альтернативно или дополнительно, другое соединение представляет собой циклофосфамид. Альтернативно или дополнительно, другое соединение представляет собой мофетила микофенолат. Альтернативно или дополнительно, другое соединение представляет собой анти-CD20 антитело (например, ритуксимаб или офатумумаб). Альтернативно или дополнительно, другое соединение представляет собой анти-С020 антитело (например, эпратузумаб). Альтернативно или дополнительно, другое соединение представляет собой анти-TNF антитело (например, инфликсимаб или адалимумаб, или голимумаб) или растворимый рецептор TNF (например, этанерцепт). Альтернативно или дополнительно, другое соединение представляет собой антагонист CTLA-4 (например, абатацепт, CTLA4-Ig). Альтернативно или дополнительно, другое соединение представляет собой анти-IL-6 антитело. Альтернативно или дополнительно, другое соединение представляет собой антагонист BLys, такой как анти-BLys антитело (например, белимумаб).
В другом примере, другое соединение представляет собой химиотерапевтическое лекарство или другое лекарство, применяемое для лечения рака.
В другом примере, белок, описанный в настоящем документе, вводят до или после лучевой терапии для лечения рака.
Дозы и время введения
Соответствующие дозы белков настоящего описания варьируются в зависимости от конкретного белка, состояния, подлежащего лечению, и/или субъекта, подлежащего лечению. Специалисты в данной области могут определить соответствующую дозу, например, начиная с субоптимальной дозы с постепенным изменением дозы для определения оптимальной или пригодной дозы. Альтернативно, для определения соответствующей дозы для лечения/профилактики, используют данные из анализов в клеточной культуре или исследований на животных, причем соответствующая доза находится в диапазоне циркулирующих концентраций, который содержит ED50 активного соединения с небольшой токсичностью или без нее. Доза может варьироваться в этом диапазоне в зависимости от используемой лекарственной формы и способа введения. Терапевтически/профилактически эффективную дозу можно первоначально оценить по анализам в клеточных культурах. Доза может быть введена в модели на животных для достижения диапазона циркулирующей концентрации в плазме, который содержит IC50 (то есть концентрацию соединения, которая достигает полумаксимального ингибирования симптомов), по результатам определения в клеточной культуре. Такая информация может быть использована для более точного определения пригодных доз для людей. Уровни в плазме могут быть измерены, например, высокоэффективной жидкостной хроматографией.
В некоторых примерах способ настоящего описания включает введение профилактически или терапевтически эффективного количества белка, описанного в настоящем документе.
Термин «терапевтически эффективное количество» представляет собой количество, которое при введении субъекту, нуждающемуся в лечении, улучшает прогноз и/или состояние субъекта, и/или которое снижает или ингибирует один или более симптомов клинического состояния, описанного в настоящем документе, до уровня, который ниже, чем наблюдается и принимается как клинически диагностическая или клинически характеристическая для этого состояния. Количество, подлежащее введению субъекту, зависит от конкретных характеристик состояния, подлежащего лечению, типа и стадии состояния, подлежащего лечению, способа введения и характеристик субъекта, таких как общее состояние здоровья, другие заболевания, возраст, пол, генотип и вес тела. Специалисты в данной области могут определить соответствующие дозы в зависимости от этих и других факторов. Соответственно, этот термин не следует толковать как ограничение настоящего описания до конкретного количества, например, веса или количества белка(ов), скорее настоящее описание охватывает любые количества белка(ов), достаточные для достижения определенного результата у субъекта. В одном примере, терапевтически эффективное количество белка не вызывает нейтропению.
При использовании в настоящем документе, термин «профилактически эффективное количество» следует понимать как достаточное количество белка для предупреждения или ингибирования, или отсрочки возникновения одного или более обнаруживаемых симптомов клинического состояния. Специалистам в данной области известно, что такое количество может варьироваться в зависимости, например, от конкретного введенного белка(ов) и/или конкретного субъекта, и/или типа или тяжести, или степени состояния и/или предрасположенности (генетической или иной) к этому состоянию. Соответственно, этот термин не следует толковать как ограничение настоящего описания до конкретного количества, например, веса или количества белка(ов), скорее настоящее описание охватывает любые количества белка(ов), достаточные для достижения определенного результата у субъекта. В одном примере, профилактически эффективное количество белка не вызывает нейтропению.
Для in vivo введения белков, описанных в настоящем документе, нормальные количества доз могут варьироваться от около 10 нг/кг до около 100 мг/кг веса тела индивидуума, или более, в день. Примеры доз и их диапазоны описаны в настоящем документе. Для повторных введений в течение нескольких дней или более, в зависимости от тяжести заболевания или расстройства, подлежащего лечению, лечение может быть непрерывным до достижения заданного подавления симптомов.
В некоторых примерах, белок вводят в первоначальной (или нагрузочной) доза от около 1 мг/кг до около 30 мг/кг, в таком количестве как от около 1 мг/кг до около 10 мг/кг, или около 1 мг/кг, или около 2 мг/кг, или около 5 мг/кг. Затем белок может вводиться в более низкой поддерживающей дозе от около 0,01 мг/кг до около 2 мг/кг, как от около 0,5 мг/кг до около 1 мг/кг, например, от около 0,1 мг/кг до около 1 мг/кг, в таком количестве как около 0,1 мг/кг или около 0,5 мг/кг, или около 1 мг/кг. Поддерживающие дозы могут вводиться каждые 7-30 дней, как, например, каждые 10-15 дней, например, каждые 10 или 11, или 12, или 13, или 14, или 15 дней.
В некоторых примерах, белок вводят в дозе от около 0,01 мг/кг до около 50 мг/кг, в таком количестве как, например, от около 0,05 мг/кг до около 30 мг/кг, например, от около 0,1 мг/кг до около 20 мг/кг, например, от около 0,1 мг/кг до около 10 мг/кг, в таком количестве как, например, от около 0,1 мг/кг до около 2 мг/кг. Например, белок вводят в дозе от около 0,01 мг/кг до около 5 мг/кг, в таком количестве как от около 0,1 мг/кг до около 2 мг/кг, в таком количестве как около 0,2 мг/кг или 0,3 мг/кг, или 0,5 мг/кг, или 1 мг/кг, или 1,5 мг/кг (например, без более высокой нагрузочной дозы или более низкой поддерживающей дозы. В некоторых примерах вводят многократные дозы, например, каждый 7-30 дней, как, например, каждые 10-22 дня, например, каждые 10-15 дней, например, каждые 10 или 11, или 12, или 13, или 14, или 15, или 16, или 17, или 18, или 19, или 20, или 21, или 22 дня. Например, белок вводят каждые 7 дней или каждые 14 дней, или каждый 21 день.
В некоторых примерах, во время начала терапии, млекопитающему вводят белок в течение не более 7 последовательных дней или 6 последовательных дней, или 5 последовательных дней или 4 последовательных дней.
В случае если млекопитающее не реагирует на лечение надлежащим образом, то могут быть введены многократные дозы в течение недели. Альтернативно или дополнительно, могут быть введены увеличивающиеся дозы.
В другом примере, млекопитающим с неблагоприятной реакцией первоначальная (или нагрузочная) доза может быть разделена на несколько дней в течение одной недели или в течение нескольких последовательных дней.
Введение белка по способам настоящего описания может быть непрерывным или периодическим, в зависимости, например, от физиологического состояния реципиента, терапевтической или профилактической цели введения и других факторов, известных опытным практикующим врачом. Введение белка может быть практически непрерывным в течение заранее выбранного периода времени или может быть в форме серий отдельных доз, например, во время или после развития состояния.
Не ограничивающие примеры
Способы
Домены Ig и CRH G-CSFR участвуют в связывании с лигандом и рецепторной димеризации (Layton et al., J. Biol Chem, 272: 29735-29741, 1997 и Fukunaga et al, EMBO J. 10: 2855-2865 1991). Растворимые формы G-CSFR (с С-концевой полигистидиновой меткой или последовательностью Fc), содержащие эти части рецептора, были использованы в различных исследованиях указанного рецептора и мутации свободных цистеинов в положениях 78, 163 и 228 указанного рецептора, способствующей экспрессии и выделению растворимого рецепторного полипептида (Mine et al., Biochem., 43: 2458-2464 2004) без ухудшения связывания с лигандом. В текущих исследованиях были использованы, в основном, растворимые формы рецептора, содержащего аминокислоты 25-335 hG-CSFR с мутациями С78А, C163S и C228S (например, SEQ ID NO:1), и был использован соответствующий сегмент cynoG-CSFR с цистеиновыми мутациями для исследования на рецепторе яванского макака. Были также использованы различные точечные мутации растворимого рецептора SEQ ID NO:1. Упоминание hG-CSFR-Fc обозначает полипептид SEQ ID NO:1, в котором С-концевая полигистидиновая метка замещена последовательностью Fc. cynoG-CSFR-Fc обозначает соответствующий сегмент cynoG-CSFR с последовательностью Fc, присоединенной к его С-окончанию. В некоторых случаях могут быть использованы соответствующие внеклеточные домены рецептора дикого типа, и эти случаи упомянуты специально. Авторы настоящего изобретения показали, что антитела и белки, содержащие их антиген-связывающие сайты (например, Fab), связываются с полипептидами hG-CSF дикого типа и с этими мутантными белками с очень похожей аффинностью. Соответственно, исследования с использованием мутантных белков представляют собой модель исследований с использованием hG-CSFR дикого типа.
Идентификация Fab из фаговой библиотеки дисплея
Фаговую библиотеку дисплея скринировали на клоны, связывающиеся с hG-CSFR, которые элюируются при добавлении лиганда G-CSF. Fab оценили на их способность связывать hG-CSFR, конкурировать за связывание G-CSF, и на их перекрестную активность с G-CSFR яванского макака, а некоторые клоны переформатировали в антитела IgG4. Затем испытали эффективность вследствие нейтрализации G-CSF-опосредованной пролиферации в клеточной линии BaF3, устойчиво трансфицированной hG-CSFR (описано ниже), и ингибирования образования CFU-G в присутствии G-CSF.
Экспрессирующая векторная конструкция млекопитающих для экспрессии IgG
Экспрессирующие векторы млекопитающих создали при помощи стандартных приемов молекулярной биологии клонированном полной легкой цепи (вариабельной и константной областей) и вариабельной области тяжелой цепи из выбранных фаг-производных конструкций Fab.
Клеточная культура и транзиентная трансфекция
293-Т клетки, адаптированные к бессывороточной суспензии, приобрели у компании Genechoice Inc. Клетки выращивали в среде для экспрессии FreeStyle™ (Invitrogen) с добавлением пенициллина/стрептомицина/реагента фунгизона (Invitrogen). Перед трансфекцией клетки выдерживали при 37°С в увлажненных инкубаторах с атмосферой, содержащей 8% CO2.
Транзиентную трансфекцию экспрессирующих векторов млекопитающих с использованием 293-Т клеток выполнили, используя реагент для трансфекции 293Fectin (Invitrogen) по инструкциям производителя. Надосадочные жидкости клеточных культур собрали через 5 дней инкубации путем центрифугирования при 2500 об./мин., а затем пропустили через 0,45 мкМ фильтр (Nalgene) перед очисткой стандартными способами для очистки IgG.
Контрольные антитела
Мышиные моноклональные антитела 711, 744 и 774 (Layton et al., Growth Factors, 14: 117-130, 1997) использовали в качестве контрольных мышиных антител.
Измерения аффинности Fab
Для измерения аффинности Fab к G-CSFR или G-CSFR-Fc, Fab экспрессировали в Е. coli, а аффинность измерили при помощи Biacore 2000.
Измерение кинетики связывания для mAb
Античеловеческое (адсорбировали козье античеловеческое IgG (гамма) мышей, Invitrogen, №по каталогу HI 05 00) или мышиное специфическое Fc антитело (Jackson Immuno Research Labs inc. номер по каталогу 515-005-071) химически фиксировали на сенсорной поверхности СМ-5, используя химизм связывания аминов.
Затем фиксированные антитела использовали для захвата анти-hG-CSFR mAb из раствора. Затем растворимые белки hG-CSFR (описанные в разделе способов) впрыскивали поверх захваченных mAb в различных концентрациях. mAb улавливали в течение 180 секунд при 0,3 мкг/мл. Растворимый hG-CSFR в концентрации 0, 1,25, 2,5, 5, 10, 20 и 40 нМ (в двух экземплярах) впрыскивали в течение 10 минут и контролировали диссоциацию в течение 30 минут. Вычли ответы от эталонной проточной кюветы (в которой mAb не был захвачен, но в остальном он был обработан таким же образом). Затем из полученных сенсограмм вычли ответы от контрольного впрыскивания.
Окончательные скорректированные ответы нанесли на график, используя нелинейную регрессию для модели, описывающей кинетику 1:1, включая время для ограничения массопередачи. В определенном месте нанесли значение Rmax для подсчета небольших отклонений уровня захваченного mAb. Определили равновесную константу диссоциации (KD).
Кинетический анализ Fab С1.2, 5D11, 711 и 744
Фрагменты Fab получили поглощением папаина, причем 3 мг антитела было поглощено (1:500) предварительно активированным папаином за 40 минут, как указано в иснтрукциях, с использованием набора поглощения папаина (Sigma, США). Полученный Fab очистили адсорбцией от остаточного Fc и непоглощенного антитела с использованием очистки белка A (mAbSelect, GE, Швеция).
Выполнили двойной биосенсорный анализ Fab с использованием Biacore 2000 (GE, Швеция) с двойным разбавлением антител Fab (от 100 нМ до 0,39 нМ в 0,1 мг/мл BSA) при скорости потока 30 мкл/мл. Связывание (100 мкл) контролировали для соответствующих проточных ячеек, содержащих контрольный фиксированный образец, фиксированный cynoG-CSFR-Fc, фиксированный человеческий G-CSFR-Fc и фиксированный человеческий G-CSFR. Рецепторные белки (20 мкг на мл в 20 мМ ацетате натрия, рН 4,5) предварительно фиксировали на чипе СМ5, используя набор для связывания NHS/EDC, следуя инструкциям производителя (Biacore GE, Швеция). Заданные значения фиксации были установлены на 700, 700 и 500 резонансных единиц для cynoG-CSFR-Fc, hG-CSFR-Fc и hG-CSFR, соответственно. Фиксацию чипа остановили при помощи 50 мМ этаноламина, рН 8,0. Диссоциацию поверхностного связывания контролировали в течение 1000 секунд до десорбции оставшегося комплекса с использованием 50 мМ фосфорной кислоты. Затем контрольное связывание вычли из контрольного канала и построили кинетику, используя программное обеспечение для биологической оценки на Biacore 2000.
Выполнили двойной биосенсорный анализ антител с1.2 и 5D11 в формате IgG4 с использованием Biacore 2000, с двойным разбавлением антител (от 312 нМ до 2,4 нМ в 0,1 мг/мл BSA) при скорости потока 30 мкл/мл. Связывание (100 мкл) контролировали для соответствующих проточных ячеек, содержащих контрольный фиксированный образец, фиксированный cynoG-CSFR-Fc, фиксированный hG-CSFR-Fc и фиксированный hG-CSFR. Рецепторные белки (20 мкг на мл в 20 мМ ацетате натрия, рН 4,5) предварительно фиксировали на чипе СМ5, используя набор для связывания NHS/EDC, следуя инструкциям производителя (Biacore GE, Швеция). Заданные значения фиксации были установлены на 700, 700 и 500 резонансных единиц для cynoG-CSFR-Fc, hG-CSFR-Fc и hG-CSFR, соответственно. Фиксацию чипа остановили при помощи 50 мМ этаноламина, рН 8,0. Диссоциацию поверхностного связывания контролировали в течение 1000 секунд до десорбции оставшегося комплекса с использованием 50 мМ фосфорной кислоты. Затем контрольное связывание вычли из контрольного канала и построили кинетику, используя программное обеспечение для биологической оценки на Biacore 2000.
BIAcore Кинетика mAb антител C1.2G со «зрелой аффинностью»
Античеловеческое (адсорбировали козье античеловеческое IgG (гамма) мышей, Invitrogen, № по каталогу H10500) химически фиксировали на сенсорной поверхности СМ-5, используя химизм связывания аминов, а затем использовали для улавливания анти-hG-CSFR mAb C1.2G со «зрелой аффинностью» при 1 мг/мл в течение 3 минут. Затем растворимые белки hG-CSFR впрыскивали поверх захваченных mAb при 0, 10 и 40 нМ. Растворимый hG-CSFR впрыскивали в течение 5 минут, а диссоциацию контролировали в течение 30 минут. Вычли ответы от эталонной проточной кюветы (в которой mAb не был захвачен, но в остальном он был обработан таким же образом). Затем из полученных сенсограмм вычли ответы от контрольного впрыскивания.
Окончательные скорректированные ответы нанесли на график, используя нелинейную регрессию для модели, описывающей кинетику 1:1, включая время для ограничения массопередачи. В определенном месте нанесли значение Rmax для подсчета небольших отклонений уровня захваченного mAb. Определили скорость ассоциации (ka), скорость диссоциации (kd) и равновесную константу диссоциации (KD).
Биоанализ пролиферации hG-CSFR/BaF3 - восстановление МТТ
Клетки BaF3, экспрессирующие hG-CSFR, приобрели в институте имени Людвига в Мельбурне. Для оценки ингибирования G-CSF-опосредованной пролиферации анти-hG-CSFR антителами, серийные разбавления антитела добавили к 2×104 клеток/лунку в среде DME с 5% FCS и 0,5 нг/мл hGCSF в 96-луночных планшетах, и инкубировали в течение 48 часов при 37°С, 10% CO2. Клеточную пролиферацию определили по восстановлению МТТ и измерили поглощением при 490 нМ.
Биоанализ пролиферации hG-CSFR/BaF3 - внедрение ЗН-тимидина
Клетки BAF/3, созданные для экспрессии человеческого G-CSFR, которые разрастаются в ответ на человеческий G-CSF, использовали для измерения способности различных моноклональных антител нейтрализовать активность G-CSF. 1×104 клеток поместили в 96-луночные планшеты в RPMI/105FCS в присутствии 10 нг/мл человеческого G-CSF и повышающихся концентраций различных анти-G-CSFR моноклональных антител на 48 часов при 37°С. Клетки активировали Н-тимидином в течение, по меньшей мере, 6 часов выращивания, затем их собрали на фильтры из стекловолокна и определили уровень радиоактивного тимидина, встроенного в ДНК, при помощи жидкостного сцинтилляционного счетчика.
Биоанализ предшественника человеческого CFU-G
Клетки костного мозга CD34+ инкубировали в полутвердой среде в присутствии 10 нг/мл фактора стволовых клеток, 10 нг/мл hG-CSF и титровальных концентраций исследуемого антитела. CFU-G подсчитали через 14 дней выращивания.
Сравнение эпитопов - конкурентное связывание
Разработка этого эксперимента построена на предположении, что для 2 антител, способных одновременно связываться с одной молекулой, эпитопы этих 2 антител должны быть различными.
Растворимый G-CSFR SEQ ID NO:1 захватили из раствора при помощи поверхностно фиксированного антитела. Затем поверх этого комплекса впрыскивали второе антитело. Вычли ответы от эталонной проточной кюветы (в которой растворимый hG-CSFR не был захвачен, но в остальном он был обработан таким же образом). Связывание второго антитела указывает, что эти эпитопы указанных 2 антител отличаются.
Ответы, измеренные в конце фазы связывания антитела, разделили на ответ в конце фазы захвата hG-CSFR, для поправки степени связывания антитела, на количество захваченного hG-CSFR. Эти ответы с поправкой на захват затем использовали для сравнения связывания каждого антитела с hG-CSFR в присутствии других антител.
Антитела С1.2, 5D11, 711 и 744 химически фиксировали на сенсорной поверхности СМ, используя химизм связывания аминов. Растворимый hG-CSFR улавливали при 100 нМ в течение 180 секунд. Затем поверх захваченного hG-CSFR впрыскивали каждое из антител при концентрации 100 нМ в течение 180 секунд, в двух экземплярах. Выполнили также контрольное впрыскивание только буфера.
Картирование эпитопов C1.2G, 711, 744 и 774
Создали серии аланиновых точечных мутантов SEQ ID NO:1, экспрессированных в клетках HEK293, затем их очистили. Измерили связывающую аффинность этих мутантов к антителам С1.2, 744 и 774 и сравнили с этой характеристикой для SEQ ID NO:1. Если мутация привела к изменению аффинности более чем в 2 раза, чем для SEQ ID NO:1, то остаток считали способствующим связывающему взаимодействию и, следовательно, вероятно находящимся в эпитопе или вблизи него. Третье mAb (711) с эпитопом, отдельным и отличным от С 1.2, 744 и 774, включили в качестве контроля для учета любых основных структурных изменений, вносимых мутациями.
Античеловеческое (адсорбировали козье античеловеческое IgG (гамма) мышей Invitrogen, № по каталогу HI 0500) или мышиное специфическое Fc антитело (Jackson Immune Research Labs Inc., номер по каталогу 515-005-071) химически фиксировали на сенсорной поверхности СМ-5, используя химизм связывания аминов. Затем фиксированные антитела использовали для захвата анти-hG-CSFR mAb из раствора. Затем поверх захваченных mAb в различных концентрациях впрыскивали лиганд-связывающий домен (SEQ ID NO:1) hG-CSFR дикого типа и каждый аланиновый точечный мутант. Вычли ответы от эталонной проточной кюветы (в которой mAb не был захвачен, но в остальном он был обработан таким же образом). Затем из полученых сенсограмм вычли ответы от контрольного впрыскивания.
Окончательные скорректированные ответы нанесли на график, используя нелинейную регрессию для модели, описывающей кинетику 1:1, включая время для ограничения массопередачи. В определенном месте нанесли значение Rmax для подсчета небольших отклонений уровня захваченного mAb. Определили скорость ассоциации (ka), скорость диссоциации (kd) и равновесную константу диссоциации (KD).
mAb зародышевой линии С1.2 улавливали при 0,3 мкг/мл в течение 180 секунд, 711 при 1 мкг/мл в течение 180 секунд, а 744 и 774 при 5 мкг/мл в течение 180 секунд.
Для кинетики С1.2 и 744, hG-CSFR дикого типа и каждый ala-мутант впрыскивали при 0, 2, 10, 50 и 250 нМ в течение 300 секунд и контролировали диссоциацию в течение следующих 1800 секунд.
Для кинетики антитела 774, WT hG-CSFR и каждый ala-мутант впрыскивали при 0, 2, 10, 50 и 250 нМ в течение 300 секунд и контролировали диссоциацию в течение следующих 600 секунд.
Для кинетики антитела 711, WT hG-CSFR и каждый ala-мутант впрыскивали при 0 и 1000 нМ в течение 180 секунд и контролировали диссоциацию в течение следующих 180 секунд.
Пример 1: Полностью человеческие анти-hG-CSFR антитела представляют собой потенциальные ингибиторы передачи сигналов G-CSF
Используя измерения аффинности и анализ пролиферации BaF3, описанные выше, антитела 711 и 744 оценили в анализах на аффинность к hG-CSFR и нейтрализацию G-CSF. Было обнаружено, что антитело 711 связывается со слиянием hG-CSFR-Fc (на основании SEQ ID NO:1, как описано в способах) с аффинностью больше, чем антитело 744 (KD 0,86 нМ и 8,7 нМ, соответственно). Используя биоанализ, основанный на МТТ, описанный выше, было также обнаружено, что антитело 711 более эффективно ингибирует G-CSF-опосредованную клеточную пролиферацию, чем антитело 744 (IC50 (нм G-CSF) 8,8 нМ и 2,4 нМ, соответственно).
Используя анализ внедрения 3H-тимидина, было обнаружено, что антитело 711 ингибирует G-CSF-опосредованную клеточную пролиферацию с IC50 10,1 мкг/мл; было обнаружено, что антитело 774 ингибирует G-CSF-опосредованную клеточную пролиферацию с IC50 37,4 мкг/мл, a IC50 для антитела 744 было не обнаруживаемым (смотри Фигуру 1).
Человеческие антитела, выделенные из фаговой библиотеки дисплея (антитела С1.2 и 5D11) и мышиное моноклональное антитело 711 оценили на их способность ингибировать G-CSF-опосредованную пролиферацию клеток BaF3 с использованием биоанализа, описанного выше. Результаты показали, что антитело С1.2 ингибирует пролиферацию BaF3 с IC50 0,5 нМ; антитело 5D11 ингибирует пролиферацию с IC50 5,9 нМ; и 711 ингибирует пролиферацию с IC50 3,4 нМ.
Эти антитела оценили такхе на их способность снижать или ингибировать образование CFU-G клетками костного мозга CD34+ в присутствии G-CSF, как описано выше. Результаты показали, что антитело С1.2 ингибирует образование CFU-G с IC50 0,016 нМ; антитело 5D11 ингибирует образование CFU-G с IC50 0,039 нМ; и 711 ингибирует образование CFU-G с IC50 0,411 нМ.
На основании этих анализов, человеческие антитела С1.2 и 5D11 являются более эффективными, чем 711, при ингибировании образования CFU-G, а С1.2 является самым сильнодействующим антителом в обоих биоанализах.
Пример 2: Аффинность антител к человеческому G-CSFR и G-CSFR яванского макака
Оценили также аффинности Fab и IgG4 форм 5D11 и С 1.2, и Fab 711 и 744 для определения их аффинности к лиганд-связывающему домену hG-CSFR (SEQ ID NO:1), hG-CSFR-Fc и G-CSFR-Fc яванского макака (на основе SEQ ID NO:1, как рассмотрено в способах). В этих анализах области G-CSFR фиксировали, и определяли связывание указанного антитела или фрагмента с фиксированным полипептидом, как более подробно описано в общих способах (раздел, озаглавленный «Кинетические анализы Fab C1.2, 5D11, 711 и 744»). Результаты представлены в таблице 1.
Эти данные показывают, что 5D11 и C1.2 обладают высокой аффинностью к hG-CSFR, и что эти аффинности улучшаются при экспрессии Fab как полных IgG4 антител. Более того, аффинности к hG-CSFR и cynoG-CSFR для 5D11 или C1.2 являются одинаковыми. C1.2 обладает большей аффинностью к hG-CSFR, чем 5D11.
Было показано, что Fab антитела 711 обладает аффинностью к hG-CSFR-Fc 0,86 нМ, и к cynoG-CSFR 1,8 мкМ. Было показано, что Fab антитела 744 обладает аффинностью к hG-CSFR-Fc 8,7 нМ, и к cynoG-CSFR >10 мкМ. Следовательно, эти Fab обладают гораздо более слабой аффинностью к cynoG-CSFR, чем к hG-CSFR.
Были также выполнены реципрокные анализы (то есть, в которых антитела иммобилизуют и определяют связывание h-GCSFR дикого типа или cynoG-CSFR дикого типа с фиксированным антителом, в соответствии с общими способами (раздел, озаглавленный «Измерение кинетики связывания mAb»). Иллюстративные результаты представлены в Таблице 2.
Эти данные показывают, что C1.2G и 5D11 связываются с cynoG-CSFR дикого типа с более высокими аффинностями, чем 711, 744 и 774. Более того, аффинности C1.2G к hG-CSFR дикого типа и cynoG-CSFR дикого типа находится в пределах 3 раз относительно друг друга, а аффинности 5D11 к hG-CSFR дикого типа и cynoG-CSFR дикого типа находятся в пределах 13 раз относительно друг друга.
Пример 3: Превращение С1.2 в ближайшие последовательности зародышевого типа
Для минимизации потенциальной иммуногенности, каркас вариабельной области С1.2 изменили для соответствия ближайшему каркасу зародышевой линии человека. Для этого потребовалось одно изменение в каркасе тяжелой цепи и пять изменений в легкой цепи, что привело к VH с последовательностью, представленной SEQ ID NO:4, и VL с последовательностью, представленной в SEQ ID NO:5. Аффинность гуманизированного антитела (C1.2G) к G-CSFR была такой же, как для С1.2 (ka 9,54×104±5,5×103; kd 1,31×10-4±2,6×10-6; kd 1,37±0,07 (N=8)). Показано, что аффинность C1.2G к hG-CSFR, экспрессируемому на клеточной поверхности клеток BaF3, составляет 257 пМ.
Используя анализ внедрения 3H-тимидина, описанный выше, было обнаружено, что антитело C1.2G ингибирует G-CSF-опосредованную клеточную пролиферацию с IC50 0,8 мкг/мл (Фигура 1).
Переформатирование этого антитело в стабилизированный IgG4 привело к образованию антитела, содержащего тяжелую цепь с последовательностью, представленной в SEQ ID NO:64, и легкую цепь с последовательностью, представленной в SEQ ID NO:65.
При экспрессии в клетках СНО, наблюдали лизиновый вариант антитела, то есть в котором одна или обе тяжелые цепи не имеют С-концевого лизинового остатка (то есть содержащий последовательность, представленную в SEQ ID NO:64).
Пример 4: Картирование эпитопов
Конкурентное связывание
В опубликованных данных показано, что mAb711 и mAb744 связываются с разными доменами hG-CSFR. Эксперименты конкурентного связывания показали, что mAb711, но не mAb744, способно связываться с hG-CSFR после связывания С1.2Ab, что позволяет предположить, что С1.2 связывается с той же областью рецептора, что и mAb744, но с другой областью, чем mAb711.
Эпитопная эксцизия для определения пептидов, участвующих в связывании С1.2
Эпитопную эксцизию с последующим анализом масс-спектрометрии использовали для определения четырех пептидов hG-CSFR, которые участвуют в связывании С1.2. В этом способе белок hG-CSFR сначала связывают с фиксированным антителом С 1.2, а затем поглощают протеолитическими ферментами. Связанные пептиды затем идентифицируют при помощи MALDI и электрораспылительной масс-спектрометрии. Четыре пептида, идентифицированные по этому подходу, картированы к положениям 111-115, 170-176, 218-234 и/или 286-300 hG-CSFR (SEQ ID NO:1).
Связывание С1.2 и mAb744 с мутантами областей hG-CSFR
В опубликованных данных (Tamada et al Proc Natl AcadSci USA. 103:3135-3140, 2006; Aritomi et al Acta Crystallogr D Biol Crystallogr; 56:751-753 1999) идентифицированы поверхностные остатки hG-CSFR. Несколько этих остатков, расположенных в четырех пептидах, идентифицированных в экспериментах эпитопной эксцизии, были замещены аланином, а полученные мутантные формы области hG-CSFR экспрессировали и очистили. Оценили связывание С1.2 и mAb744 с каждым из этих мутантов и определили основные остатки, участвующие в связывании. Результаты показаны на Фигуре 2А. Аланиновое замещение остатков K167 и H168 привело к полной потере связывания mAb744, тогда как связывание С1.2 было не затронуто. Напротив, аланиновое замещение остатка R287 привело к полной потере связывания С1.2, без ухудшения связывания mAb744. Другими остатками, которые существенно снижают связывание С1.2, были L111, L171, Y172, M198 и Н237. MAb744 связывает эти мутанты с такой же аффинностью, как для рецептора дикого типа.
Представленный выше анализ повторили с теми же антителами вместе с mAb774. Как показано на Фигуре 2 В, аланиновое замещение остатков K167, H168 и L169 привело к полной потере связывания mAb774, тогда как связывание С1.2 было не затронуто. Как и с mAb 744, аланиновое замещение остатка L111, Y172, Н237 и R287 имело незначительный эффект или не влияло на связывание mAb774.
Пример 5: Созревание аффинности C1.2G
Созревание аффинности выполнили мутированием остатков в HCDR3 и/или LCDR3 C1.2G и скринированием на Fab, которые связываются с hG-CSFR. Библиотеки мутантных антител разделили методом пэннинга, используя биотилинированный рекомбинантный белок hG-CSFR-Fc как при постоянной концентрации в ходе нескольких циклов пэннинга, так и при понижающихся концентрациях.
После завершения пэннинга, из каждой обогащенной библиотеки выбрали ряд фаговых клонов и секвенировали их. Затем выбрали уникальные клоны на основании последовательности, и переформатировали в полностью человеческие IgG4/Kanna антитела для анализа связывания с hG-CSFR с использованием Biacore (по общим способам в разделе, озаглавленном «Измерение кинетики связывания для mAb») и, в некоторых случаях, способности ингибировать G-CSF-опосредованную пролиферацию клеток BaF3. Переформатированные антитела с улучшенными аффинностями по сравнению с исходными C1.2G mAb перечислены в Таблице 3.
Пример 6: C1.2G понижает уровни нейтрофилов, не вызывая нейтропению
Яванским макакам ввели пэгилированный G-CSF, а через 12 часов ввели C1.2G (10 мг/кг). Как показано на Фигуре 3, С1.2 существенно снижает уровень нейтрофилов по сравнению с контрольными животными, однако не вызывает нейтропению.
В таких же экспериментах, при введении яванским макакам от 0,1 до 10 мг/кг C1.2G через 2 часа до введения G-CSF, уровень нейтрофилов также был понижен по сравнению с контрольными животными, однако он не вызывает нейтропению.
| название | год | авторы | номер документа |
|---|---|---|---|
| CD131-СВЯЗЫВАЮЩИЕ БЕЛКИ И ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2773927C2 |
| СПОСОБ ИНГИБИРОВАНИЯ GMCSFRa У ПАЦИЕНТА | 2012 |
|
RU2639546C2 |
| ТЕРАПЕВТИЧЕСКИЕ DLL4-СВЯЗЫВАЮЩИЕ БЕЛКИ | 2010 |
|
RU2570639C2 |
| ТЕРАПЕВТИЧЕСКИЕ DLL4-СВЯЗЫВАЮЩИЕ БЕЛКИ | 2011 |
|
RU2605928C2 |
| АНТИТЕЛА К CD38 И КОМБИНАЦИИ С АНТИТЕЛАМИ К CD3 И CD28 | 2018 |
|
RU2812910C2 |
| АНТИТЕЛА ПРОТИВ БЕЛКА РЕЦЕПТОРА С-МЕТ | 2011 |
|
RU2608644C2 |
| СВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ, ВЫЗЫВАЮЩИЕ КЛЕТОЧНУЮ АКТИВАЦИЮ | 2019 |
|
RU2770620C1 |
| СПОСОБЫ РАЗРУШЕНИЯ КЛЕТОК С ИСПОЛЬЗОВАНИЕМ ЭФФЕКТОРНЫХ ФУНКЦИЙ АНТИ-EphA4 АНТИТЕЛ | 2007 |
|
RU2429246C2 |
| ПОЛИПЕПТИДЫ ДЛЯ СВЯЗЫВАНИЯ С "РЕЦЕПТОРОМ КОНЕЧНЫХ ПРОДУКТОВ ГЛИКИРОВАНИЯ", А ТАКЖЕ ИХ КОМПОЗИЦИИ И СПОСОБЫ, В КОТОРЫХ ОНИ ПРИНИМАЮТ УЧАСТИЕ | 2010 |
|
RU2558301C2 |
| БЕЛКИ, СВЯЗЫВАЮЩИЕ РЕЦЕПТОР ПРОЛАКТИНА, И ИХ ПРИМЕНЕНИЕ | 2013 |
|
RU2664463C2 |






















































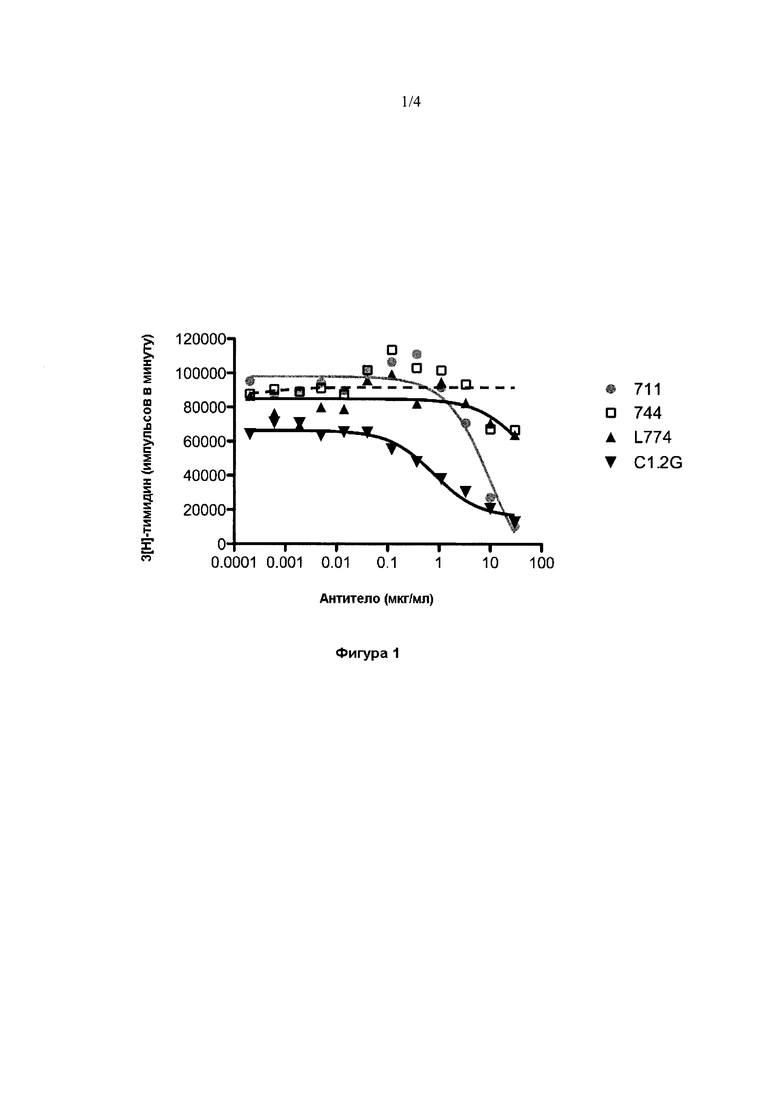
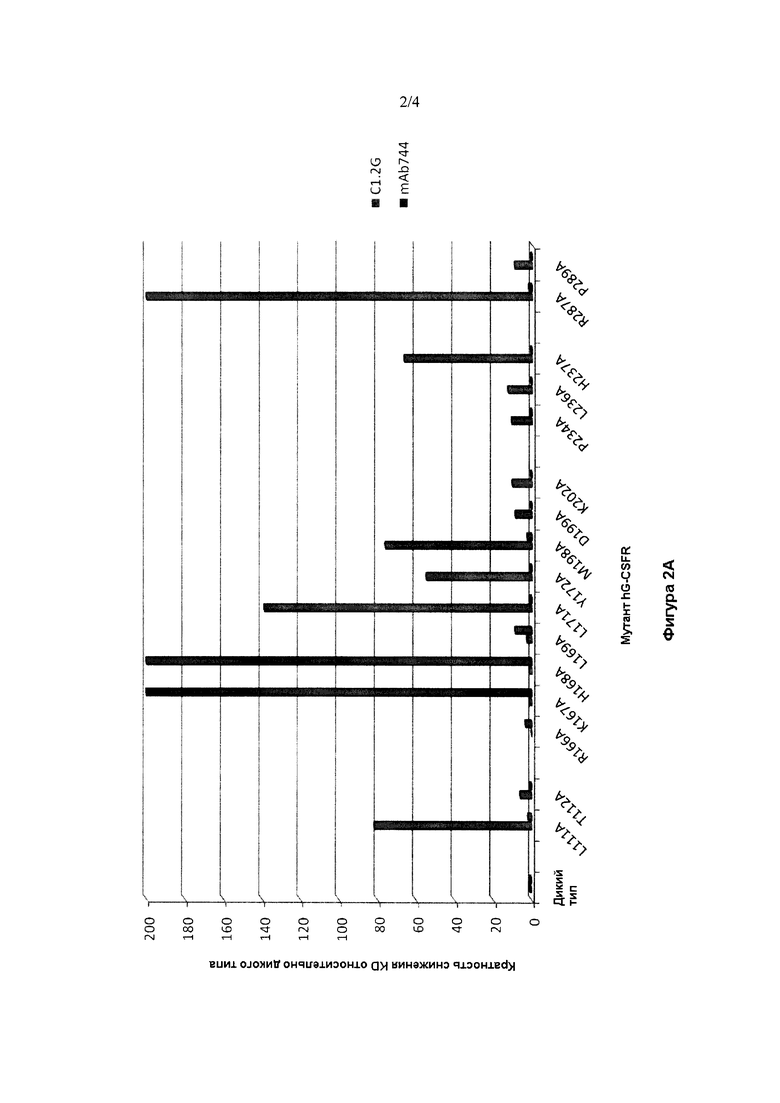
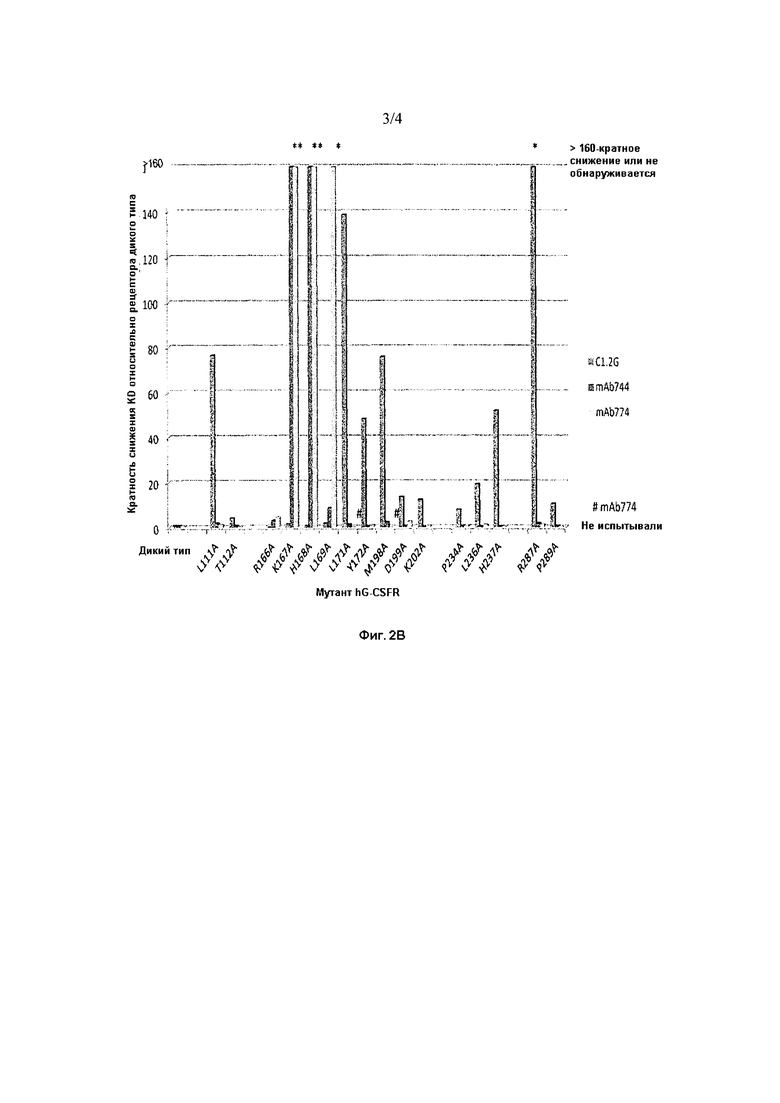
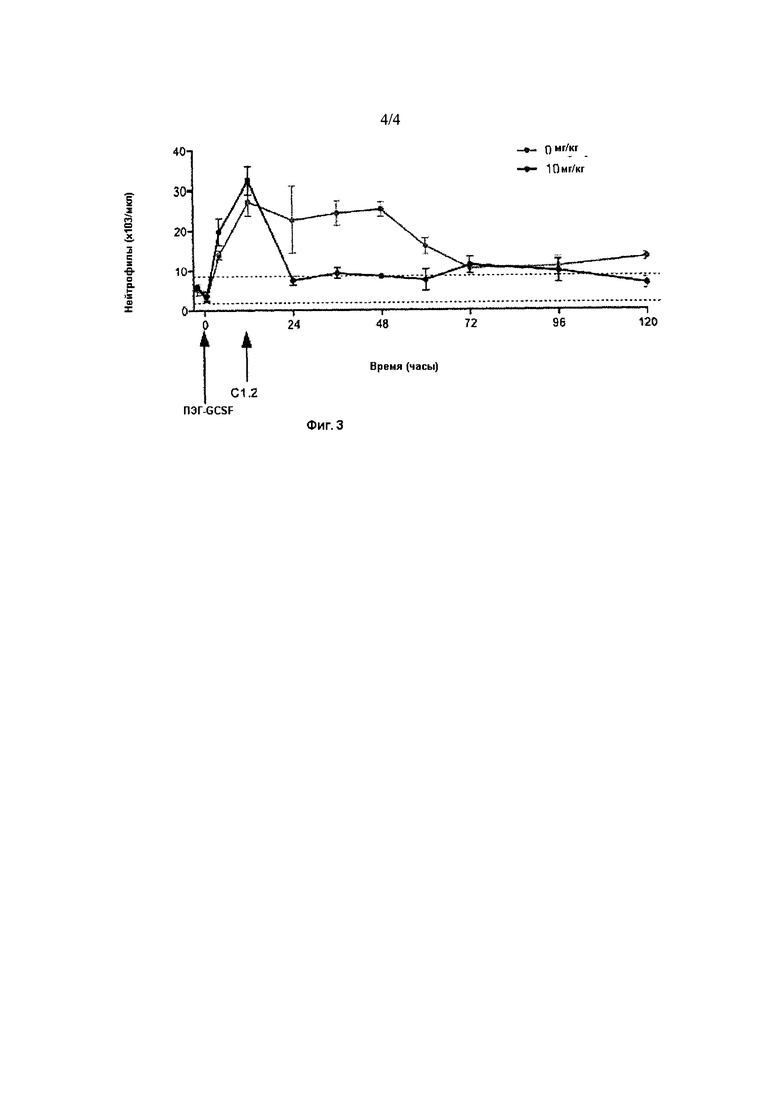
Изобретение относится к области биохимии. Предложены варианты антитела, связывающегося с человеческим рецептором гранулоцитарного колониестимулирующего фактора (hG-CSFR). Также предложены композиция и способ лечения опосредованного G-CSF состояния у субъекта. Изобретение позволяет связываться с hG-CSFR с высокой аффинностью и нейтрализовать передачу сигналов G-CSF. 9 н. и 4 з. п. ф-лы, 4 ил., 3 табл., 6 пр.
1. Антитело, которое связывается с человеческим рецептором гранулоцитарного колониестимулирующего фактора (hG-CSFR), и при этом антитело нейтрализует передачу сигналов гранулоцитарного колониестимулирующего фактора (G-CSF), указанное антитело содержит:
(i) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность, представленную в SEQ ID NO: 4, и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность, представленную в SEQ ID NO: 5;
(ii) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 2, и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 3;
(iii) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 15, и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 14;
(iv) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 4, и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 16;
(v) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 4, и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 17;
(vi) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 4, и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 18;
(vii) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 20, и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 19;
(viii) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 4, и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 21;
(ix) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 4, и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 22;
(x) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 24, и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 23;
(xi) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 4, и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 25;
(xii) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 4, и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 26;
(xiii) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 28, и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 27;
(xiv) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 4, и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 29;
(xv) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 31, и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 30;
(xvi) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 33, и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 32;
(xvii) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 4, и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 34;
(xviii) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 36, и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 35;
(xix) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 38, и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 37;
(xx) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 40, и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 39;
(xxi) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 42, и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 41;
(xxii) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 4, и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 43;
(xxiii) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 45, и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 44;
(xxiv) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 4, и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 46;
(xxv) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 4, и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 47;
(xxvi) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 49, и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 48;
(xxvii) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 51, и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 50;
(xxviii) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 53, и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 52;
(xxix) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 4, и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 54;
(xxx) VH, содержащей аминокислотную последовательность, представленную в SEQ ID NO: 55, и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 5;
(xxxi) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 57, и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 56;
(xxxii) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 59, и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 58;
(xxxiii) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 61, и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 60;
(xxxiv) VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 4, и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 62; или
(xxxv) VH, содержащей аминокислотную последовательность, представленную в SEQ ID NO: 4, и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 63.
2. Антитело, которое связывается с человеческим рецептором гранулоцитарного колониестимулирующего фактора (hG-CSFR), и при этом антитело нейтрализует передачу сигналов гранулоцитарного колониестимулирующего фактора (G-CSF), указанное антитело содержит:
(i) вариабельную область тяжелой цепи (VH), содержащую три CDR вариабельной области тяжелой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 4, и вариабельную область легкой цепи (VL), содержащую три CDR вариабельной области легкой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 5;
(ii) VH, содержащую три CDR вариабельной области тяжелой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 2, и VL, содержащую три CDR вариабельной области легкой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 3;
(iii) VH, содержащую три CDR вариабельной области тяжелой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 15, и VL, содержащую три CDR вариабельной области легкой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 14;
(iv) VH, содержащую три CDR вариабельной области тяжелой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 4, и VL, содержащую три CDR вариабельной области легкой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 16;
(v) VH, содержащую три CDR вариабельной области тяжелой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 4, и VL, содержащую три CDR вариабельной области легкой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 17;
(vi) VH, содержащую три CDR вариабельной области тяжелой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 4, и VL, содержащую три CDR вариабельной области легкой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 18;
(vii) VH, содержащую три CDR вариабельной области тяжелой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 20, и VL, содержащую три CDR вариабельной области легкой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 19;
(viii) VH, содержащую три CDR вариабельной области тяжелой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 4, и VL, содержащую три CDR вариабельной области легкой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 21;
(ix) VH, содержащую три CDR вариабельной области тяжелой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 4, и VL, содержащую три CDR вариабельной области легкой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 22;
(x) VH, содержащую три CDR вариабельной области тяжелой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 24, и VL, содержащую три CDR вариабельной области легкой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 23;
(xi) VH, содержащую три CDR вариабельной области тяжелой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 4, и VL, содержащую три CDR вариабельной области легкой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 25;
(xii) VH, содержащую три CDR вариабельной области тяжелой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 4, и VL, содержащую три CDR вариабельной области легкой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 26;
(xiii) VH, содержащую три CDR вариабельной области тяжелой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 28, и VL, содержащую три CDR вариабельной области легкой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 27;
(xiv) VH, содержащую три CDR вариабельной области тяжелой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 4, и VL, содержащую три CDR вариабельной области легкой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 29;
(xv) VH, содержащую три CDR вариабельной области тяжелой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 31, и VL, содержащую три CDR вариабельной области легкой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 30;
(xvi) VH, содержащую три CDR вариабельной области тяжелой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 33, и VL, содержащую три CDR вариабельной области легкой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 32;
(xvii) VH, содержащую три CDR вариабельной области тяжелой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 4, и VL, содержащую три CDR вариабельной области легкой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 34;
(xviii) VH, содержащую три CDR вариабельной области тяжелой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 36, и VL, содержащую три CDR вариабельной области легкой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 35;
(xix) VH, содержащую три CDR вариабельной области тяжелой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 38, и VL, содержащую три CDR вариабельной области легкой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 37;
(xx) VH, содержащую три CDR вариабельной области тяжелой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 40, и VL, содержащую три CDR вариабельной области легкой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 39;
(xxi) VH, содержащую три CDR вариабельной области тяжелой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 42, и VL, содержащую три CDR вариабельной области легкой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 41;
(xxii) VH, содержащую три CDR вариабельной области тяжелой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 4, и VL, содержащую три CDR вариабельной области легкой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 43;
(xxiii) VH, содержащую три CDR вариабельной области тяжелой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 45, и VL, содержащую три CDR вариабельной области легкой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 44;
(xxiv) VH, содержащую три CDR вариабельной области тяжелой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 4, и VL, содержащую три CDR вариабельной области легкой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 46;
(xxv) VH, содержащую три CDR вариабельной области тяжелой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 4, и VL, содержащую три CDR вариабельной области легкой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 47;
(xxvi) VH, содержащую три CDR вариабельной области тяжелой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 49, и VL, содержащую три CDR вариабельной области легкой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 48;
(xxvii) VH, содержащую три CDR вариабельной области тяжелой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 51, и VL, содержащую три CDR вариабельной области легкой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 50;
(xxviii) VH, содержащую три CDR вариабельной области тяжелой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 53, и VL, содержащую три CDR вариабельной области легкой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 52;
(xxix) VH, содержащую три CDR вариабельной области тяжелой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 4, и VL, содержащую три CDR вариабельной области легкой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 54;
(xxx) VH, содержащую три CDR вариабельной области тяжелой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 55, и VL, содержащую три CDR вариабельной области легкой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 5;
(xxxi) VH, содержащую три CDR вариабельной области тяжелой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 57, и VL, содержащую три CDR вариабельной области легкой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 56;
(xxxii) VH, содержащую три CDR вариабельной области тяжелой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 59, и VL, содержащую три CDR вариабельной области легкой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 58;
(xxxiii) VH, содержащую три CDR вариабельной области тяжелой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 61, и VL, содержащую три CDR вариабельной области легкой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 60;
(xxxiv) VH, содержащую три CDR вариабельной области тяжелой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 4, и VL, содержащую три CDR вариабельной области легкой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 62; или
(xxxv) VH, содержащей три CDR вариабельной области тяжелой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 4, и VL, содержащую три CDR вариабельной области легкой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 63.
3. Антитело, которое связывается с человеческим рецептором гранулоцитарного колониестимулирующего фактора (hG-CSFR), и при этом антитело нейтрализует передачу сигналов гранулоцитарного колониестимулирующего фактора (G-CSF), указанное антитело содержит вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность, представленную в SEQ ID NO: 4, и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность, представленную в SEQ ID NO: 5.
4. Антитело, которое связывается с человеческим рецептором гранулоцитарного колониестимулирующего фактора (hG-CSFR), и при этом антитело нейтрализует передачу сигналов гранулоцитарного колониестимулирующего фактора (G-CSF), указанное антитело содержит VH, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 2, и VL, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 3.
5. Антитело, которое связывается с человеческим рецептором гранулоцитарного колониестимулирующего фактора (hG-CSFR), и при этом антитело нейтрализует передачу сигналов гранулоцитарного колониестимулирующего фактора (G-CSF), указанное антитело содержит вариабельную область тяжелой цепи (VH), содержащую три CDR вариабельной области тяжелой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 4, и вариабельную область легкой цепи (VL), содержащую три CDR вариабельной области легкой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 5.
6. Антитело, которое связывается с человеческим рецептором гранулоцитарного колониестимулирующего фактора (hG-CSFR), и при этом антитело нейтрализует передачу сигналов гранулоцитарного колониестимулирующего фактора (G-CSF), указанное антитело содержит вариабельную область тяжелой цепи (VH), содержащую три CDR вариабельной области тяжелой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 2, и вариабельную область легкой цепи (VL), содержащую три CDR вариабельной области легкой цепи, состоящей из аминокислотной последовательности, представленной в SEQ ID NO: 3.
7. Антитело, которое связывается с человеческим рецептором гранулоцитарного колониестимулирующего фактора (hG-CSFR), и при этом антитело нейтрализует передачу сигналов гранулоцитарного колониестимулирующего фактора (G-CSF), указанное антитело содержит:
(i) тяжелую цепь, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 64 или 68, и легкую цепь, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 65; или
(ii) одну тяжелую цепь, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 64, и одну тяжелую цепь, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 68, и две легкие цепи, содержащие аминокислотную последовательность, представленную в SEQ ID NO: 65.
8. Композиция для лечения состояния у субъекта, опосредованного гранулоцитарным колониестимулирующим фактором (G-CSF), содержащая антитело по любому из пп. 1-7 и фармацевтически приемлемый носитель или содержащая:
(i) антитело, содержащее тяжелую цепь, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 64, и легкую цепь, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 65; или
(ii) (a) антитело, содержащее тяжелую цепь, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 64, и легкую цепь, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 65; и
(b) антитело, содержащее одну тяжелую цепь, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 64, и одну тяжелую цепь, содержащую аминокислотную последовательность, представленную в SEQ ID NO: 68, и две легкие цепи, содержащие аминокислотную последовательность, представленную в SEQ ID NO: 65,
и, необязательно, фармацевтически приемлемый носитель.
9. Способ лечения или предупреждения у субъекта состояния, опосредованного гранулоцитарным колониестимулирующим фактором (G-CSF), включающий введение субъекту антитела по любому из пп. 1-7 или композиции по п. 8.
10. Способ по п. 9, отличающийся тем, что G-CSF-опосредованное состояние представляет собой аутоиммунное заболевание, воспалительное заболевание или рак.
11. Способ по п. 10, отличающийся тем, что аутоиммунное заболевание или воспалительное заболевание представляет собой артрит, рассеянный склероз, воспаление легких или хроническую обструктивную болезнь легких.
12. Способ по п. 9, включающий введение количества антитела, достаточного для уменьшения количества нейтрофилов у субъекта без инициации нейтропении.
13. Способ по п. 12, отличающийся тем, что указанное количество антитела находится в диапазоне от 0,05 мг/кг до 30 мг/кг.
| WO 199521867 A1, 17.08.1995 | |||
| US 20090324591 A1, 31.12.2009 | |||
| LAYTON J.E | |||
| et al., Neutralising Antibodies to the Granulocyte Colony-stimulating Factor Receptor Recognise both the Immunoglobulin-like Domain and the Cytokine Receptor Homologous Domain, Growth Factors, 1997, Vol.14, Issue 2-3, pp.117-130 | |||
| NAGATA S., FUKUNAGA R., GRANULOCYTE |
Авторы
Даты
2016-12-20—Публикация
2012-06-13—Подача