Изобретение в области биотехнологии относится к микробиологической промышленности и представляет собой способ получения и культивирования рекомбинантного штамма мицелиального гриба Penicillium canescens CS15 ВКМ F-4679D, секретирующего термостабильную целлюлазу Cel48S из Clostridium thermocellum.
Промышленное применение ферментов для гидролиза целлюлозосодержащего сырья является актуальной задачей современной биотехнологии. Разработка новых рекомбинантных штаммов на основе мицелиального гриба Penicillium canescens, ферментный комплекс которых содержит такие термостабильные ферменты, как целлюлаза Cel48S, принадлежащая к 48-ому семейству гликозил-гидролаз, из Clostridium thermocellum, позволит получить продуценты, сочетающие высокую продуктивность мицелиального гриба Penicillium canescens и биохимические свойства высокотермостабильных бактериальных ферментов Clostridium thermocellum.
Cel48S является одной из основных структурных единиц целлюлосомы Clostridium thermocellum, мультиферментного комплекса, состоящего из ряда целлюлаз с различной субстратной специфичностью. Ранее было показано, что Cel48S обладает свойствами экзоглюканазы, включая высокую активность по отношению к аморфной или кристаллической целлюлозе по сравнению с карбоксиметилцеллюлозой (КМЦ) и отсутствие способности понижать вязкость раствора КМЦ [B.G. Guimaraes, Н. Souchon, В.L. Lytle, J.H.D. Wu, P.M. Alzari The Crystal Structure and Catalytic Mechanism of Cellobiohydrolase CelS, the Major Enzymatic Component of the Clostridium thermocellum Cellulosome, J. Mol. Biol. – 2002. - V. 320, - P. 587-596].
К числу наиболее перспективных микроорганизмов для получения ферментных препаратов карбогидраз, на сегодняшний день, относятся микроскопические грибы рода Trichoderma, Penicillium, а также Aspergillus, что обусловлено в основном их высоким уровнем секреции внеклеточных ферментов [Gusakov A.V. Alternatives to Trichoderma reseei in biofuel production / Trends in Biotechnology. - 2011. - T. 29. - №9. - C. 419-425, Чекушина A.B., Доценко Г.С., Синицын А.П. / Сравнение эффектиности процессов биоконверсии растительного сырья с использованием биокатализаторов на основе Penicillium и Trichoderma. II Катализ в промышленности. - 2012. - №6. - С. 68-76].
Одним из таких востребованных с точки зрения биотехнологии микроорганизмов является штамм P. canescens RN3-11-7 niaD(-), неоднократно успешно используемый как реципиент для получения продуцентов гомологичных и гетерологичных белков с использованием сильных промоторов гена ксиланазы и β-галактозидазы, например гетерологичной эндо-1,4-β-глюканазы III P. verruculosum с использованием сильных промоторов гена ксиланазы и β-галактозидазы [Рожкова A.M. Волков П.В., Кондратьева Е.А., Сатрутдинов А.Д. и др. Создание продуцентов биотехнологически важных ферментов на основе рекомбинантного штамма гриба Penicillium canescens. Хранение и переработка сельхозсырья. - 2010. - №7. - С. 37-39, Патент РФ 2238974 (С2) Дата Публ. 27.10.2004, "ДНК-фрагмент мицелиального гриба Penicillium verruculosum, кодирующего синтез секретируемой эндоглюканазы и группа штаммов Penicillium canescens, продуцирующих эндоглюканазу III Penicillium verruculosum, сконструированных методами трансформации и генетической инженерии, основываясь на этих фрагментах], α-галактозидазы и пектинлиазы А из P. canescens, целлобиогидролазы I, целлобиогидролазы II и ЭГ II из P. verruculosum [Бушина Е.В., Рожкова A.M., Зоров И.Н., Сатрутдинов А.Д., Беккаревич А.О., Кошелев А.В., Окунев О.Н., Синицын А.П. Создание комплексных ферментных препаратов пектиназ и целлюлаз для переработки свекловичного жома. // Прикладная биохимия и микробиология. - 2012. - Т. 48. - №5. - С. 543-549], β-глюкозидазы и инулиназ из A. niger [Волков П.В., Синицына О.А., Федорова Е.А., Рожкова A.M., Сатрутдинов А.Д., Зоров И.Н., Окунев О.Н., Гусаков А.В., Синицын А.П. Выделение и свойства рекомбинантных инулиназ Aspergillus sp. // Биохимия. - 2012. - Т. 77, - №5. - С. 611-621].
Прототипом разработанного технического решения может служить патент РФ №2378372 «Генетическая конструкция для обеспечения экспрессии целевых гомологичных и гетерологичных генов в клетках мицелиального гриба Penicillium verruculosum, используемого в качестве хозяина, способ получения штамма гриба Penicillium verruculosum и способ получения ферментного препарата».
Техническая задача, решаемая в результате применения группы разработанных технических решений, состоит в создании штамма-продуцента путем трансформации исходного штамма P. canescens RN3-11-7 niaD(-) плазмидой, несущей ген celS, кодирующей термостабильную целлюлазу Cel48S из Clostridium thermocellum, и подбор среды для культивирования полученного штамма-продуцента с целью получения полноразмерного белка Cel48S.
Техническим результатом, получаемым при реализации разработанных технических решений, является возможность эффективной продукции целлюлазы из Clostridium thermocellum в гетерологичном хозяине Penicillium canescens.
Для получения указанного технического результата используют полинуклеотидную последовательность гена целевого белка. Целевая плазмида содержит кодирующую последовательность гена celS и функционально связанные с ним регуляторные элементы, промотор и терминатор гена ксиланазы A (xylA) из P. canescens. При реализации указанного способа получают штамм гриба Penicillium canescens CS15 ВКМ F-4679D, мультикопийный по гену celS из С. thermocellum.
Кроме того, для получения указанного технического результата предложен способ культивирования полученного штамма-продуцента P. canescens, секретирующего целевой белок Cel48S, на среде, состав которой существенно отличается от стандартной среды для культивирования гриба P. canescens. Одним из ключевых изменений в составе среды является добавление дополнительного количества хлорида кальция, обеспечивающего стабильность секретируемого целевого белка Cel48S.
Указанные варианты не исчерпывают возможности разработанного способа получения рекомбинанатных штаммов P. canescens, экспрессирующих гетерологичные гены из С. thermocellum.
Схема разработки способа получения каждого из рекомбинантных штаммов, секретирующих целлюлосомальные ферменты из С. thermocellum, состоит из трех типовых этапов.
Этап 1. Амплифицируют целевой ген целлюлосомального фермента из С. thermocellum - celS, а также промоторную и терминаторную область гена xylA из P. canescens. Конструируют плазмиду pCelS, представляющую собой полинуклеотидную последовательность, состоящую из промоторной области гена xylA, сигнального пептида, целевого гена celS и терминаторной области гена xylA.
Этап 2. Проводят трансформацию реципиентного высокопродуктивного штамма P. canescens RN3-11-7 niaD(-) целевой плазмидой pCelS, полученной на Этапе 1, в условиях котрансформации вместе с плазмидой, несущей последовательность niaD гена, как маркера селекции, и осуществляют отбор трансформантов, секретирующих в культуральную жидкость целевой фермент. Проводят ферментацию отобранных трансформантов в качалочных колбах и среди них выбирают наиболее продуктивные варианты штаммов-продуцентов.
Этап 3 - Подбирают оптимальные условия культивирования наиболее продуктивного варианта штаммов-продуцентов, обеспечивающих стабильность целевого белка во время культивирования и его максимальную продуктивность.
Изобретение иллюстрируется следующими примерами.
Пример 1.
Получение целевой плазмиды pCelS заключалось в клонировании гена celS [http://www.ncbi.nlm.nih.gov/nucleotide/125712750?report=gbwithparts&from=2482535&to=2484760&RID=630WK5VY01R] в универсальный вектор, обеспечивающий экспрессию целевого гена под контролем промотора и терминатора гена xylA из P. canescens.
Амплификацию гена celS из С. thermocellum проводили с использованием праймеров соответствующего состава:
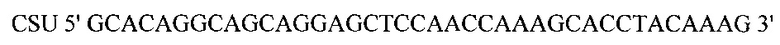
Методом секвенирования по Сэнгеру были определены нуклеотидные последовательности полученных фрагментов. Схематическое изображение структуры экспрессионных кассет показано на Рис. 1. Косым штрихом на Рис. 1 обозначена промоторная область гена ксиланазы A (xylA) из P. canescens, черным цветом - сигнальный пептид (bgaS SS), прямым штрихом - целевой ген из С.thermocellum (celS), квадратным штрихом - терминаторная область гена ксиланазы A (xylA) из P. canescens.
Аминокислотная последовательность целевого фермента CEL48S представлена на Рис. 2, где подчеркнут сигнальный пептид β-галактозидазы.
Пример 2. Трансформация высокопродуктивного штамма-реципиента P. canescens RN3-11-7 niaD(-) плазмидами, указанными в Примере 1 для получения набора рекомбинантных штаммов, секретирующих целлюлосомальный фермент Cel48S из С. thermocellum.
К смеси двух плазмид (1 мкг котрансформационной плазмиды PSTA10, несущей ген niaD из A. niger и 10 мкг плазмиды pCelS, несущей ген celS из С. thermocellum) объемом 20 мкл добавляют 200 мкл раствора протопластов штамма P. canescens RN3-11-7 niaD(-), полученных по методике, описанной в статье [A.Y. Aleksenko, N.A. Makarova, I.V. Nikolaev, A.J. Clutterbuck Integrative and replicative transformation of Penicillium canescens with a heterologous nitrate-reductase gene, Curr. Genet. - 1995. - V. 28. - P. 474-477] и 50 мкл буфера PCT1, содержащего: 50%-ный ПЭГ 4000 (по объему) +0.01 М трис-НС1 pH 7.5 + 0.02 М CaCl2. Смесь аккуратно перемешивают и оставляют на 20 мин во льду. Затем добавляют 500 мкл буфера РСТ1 и оставляют на 5 мин при комнатной температуре. Параллельно проводят эксперимент с контрольными протопластами без добавления ДНК. Далее пробирки со смесью протопластов и ДНК центрифугируют при 5000 об/мин в течение 20 мин. Супернатант сливают, а осадок ресуспендируют в 200 мкл стерильного раствора сорбитола (182,2 г/л). Трансформационную смесь стерильно переносят над пламенем горелки в 5 мл верхнего агара (для приготовления 100 мл верхнего агара берут 21,86 г 1,2 М сорбитола, 0,7 г агара, 0,8 г глюкозы, 1 мл 1М источника азота) перемешивают и распределяют агар по поверхности предварительно подготовленных чашек с нижним агаром (для приготовления 100 мл нижнего агара берут 21,86 г 1,2 М сорбитола, 2 г агара, 0,8 г глюкозы, 1 мл 1 М источника азота). Так же переносят и контрольные смеси.
Готовят три чашки Петри с нижним агаром, две с селективной средой (источник азота: NaNO3 10 mM) и одна - с неселективной (источник азота: NH4C1 10 mM). Чашки Петри помещают в инкубатор на 30°C и оставляют там на 6 дней. На шестой день роста трансформанты переносят на селективную минимальную среду (источник азота: NaNO3 10 mM). В результате трансформации реципиентного штамма P. canescens RN3-11-7 смесью плазмид получают около от 90 до 170 трансформантов на 10 мкг введенной целевой ДНК, что соответствует стандартной частоте трансформации грибных штаммов.
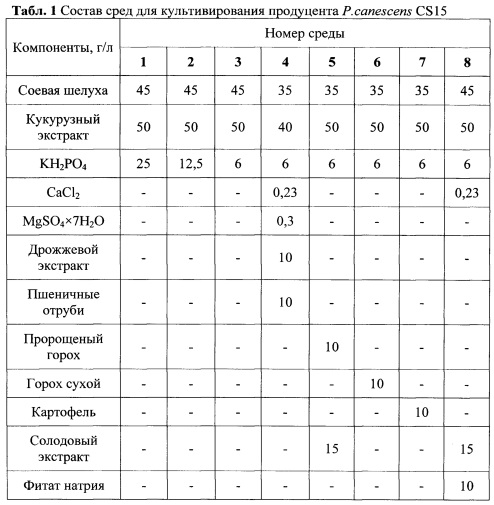
Чтобы среди полученных трансформантов отобрать штаммы, в хромосоме которых содержится встроенный ген целевого белка, проводят первичный скрининг трансформантов методом ПЦР-реакции. Скрининг трансформантов pCELS осуществляли с использованием пары праймеров CSU и CSL. Размер полученного ПЦР-продукта ~1500 п.н. соответствует размеру полинуклеотидной последовательности гена celS из С. thermocellum (Рис. 3, PC - штамм-реципиент, 1-46 - трансформанты, PR - плазмида pCELS, отобранные для культивирования клоны - подчеркнуты).
Пример 3. Получение рекомбинантных штаммов P. canescens CS15, мультикопийного по гену celS из С. thermocellum (48-е семейство гликозид-гидролаз, молекулярная масса 83 кДа).
Полученные в Примере 2 позитивные по целевому гену celS трансформанты пересевают на чашки с минимальной средой и источником азота NaNO3 и инкубируют при 28°C в течение 140 часов до образования конидий. Затем трансформанты ферментируют в качалочных колбах, используя ферментационную среду следующего состава, в г/л: соевая шелуха - 45, кукурузный экстракт - 50, KH2PO4 - 25. Колбы инкубируют на качалке при 30°C и 220 об/мин в течение 144 ч. Далее отбирают рекомбинантные штаммы, ферментный комплекс которых содержит целевой белок.
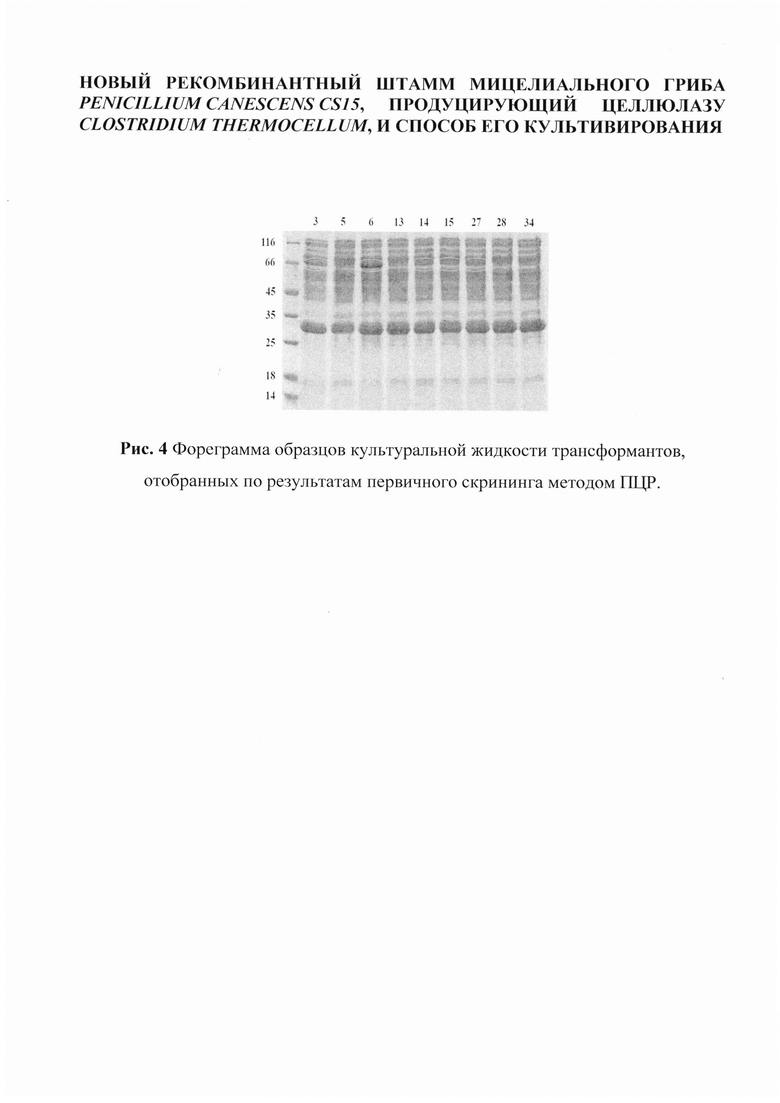
Для культуральной жидкости отобранных штаммов проводят ДДС-электрофорез в денатурирующих условиях, чтобы идентифицировать полосу, соответствующую целевому белку Cel48S (см. Рис. 4). Для доказательства принадлежности экспрессированного белка к целлюлазе CEL48S был проведен масс-спектрометрический анализ образцов гелей, молекуляпная масса которых соответствовала искомой - 70 кДа. Результаты MALDI-TOF спектрометрии подтвердили наличие ожидаемого CEL48S белка (см. Рис. 5, совпадающие пептиды обозначены подчеркиванием).
Таким образом, среди полученных трансформантов был выбран штамм Penicillium canescens CS15, который был депонирован в Всероссийскую коллекцию микроорганизмов под номером ВКМ F-4679D.
Пример 4. Оптимизация условий культивирования рекомбинантого штамма P. canescens CS15, мультикопийного по гену celS из С. thermocellum.
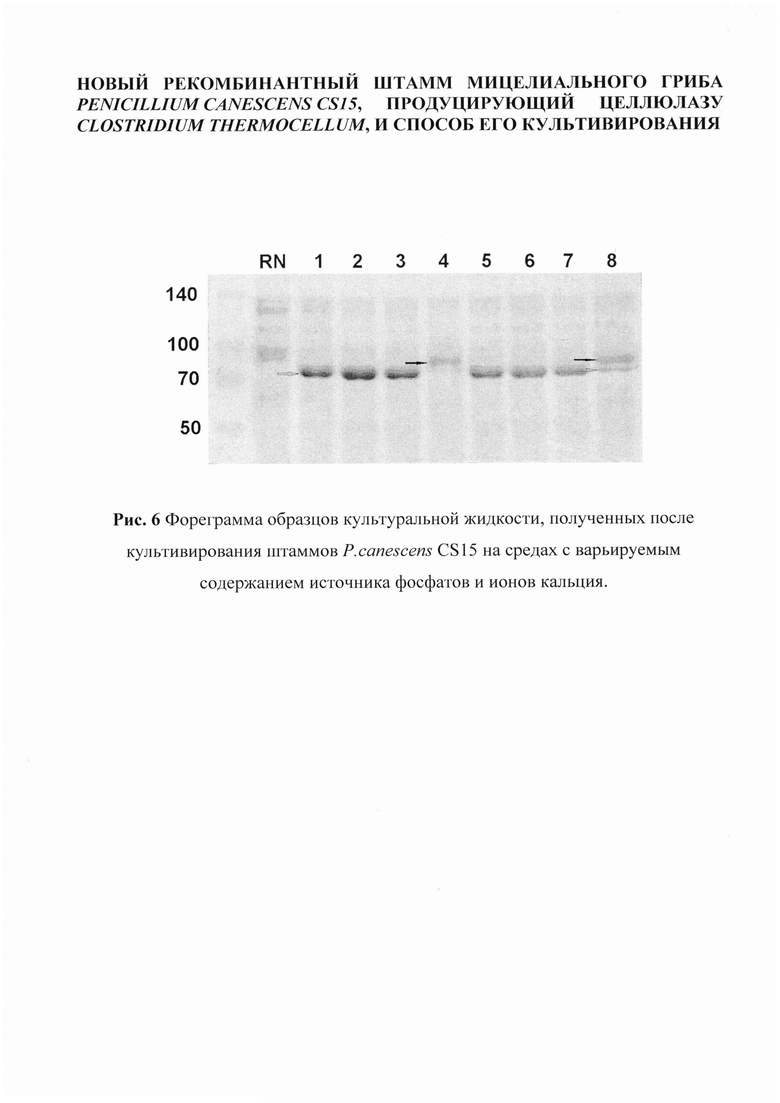
Поскольку стандартная среда для культивирования гриба P. canescens содержит 25 г/л дигидрофосфата калия, то в процессе культивирования в среде должен наблюдаться дефицит ионов кальция, выпадающего в осадок в виде фосфата. В отсутствие ионов кальция в среде для культивирования целлюлосомальный белок Cel48S из С. thermocellum неустойчив. На Рис. 6 видно, что молекулярная масса целевого белка составляет приблизительно 70 кДа, в то время как молекулярная масса нативного белка Cel48S составляет 83 кДа, в частности, RN - образец культуральной жидкости штамма-реципиента на среде 1, 1-8 - среды различного состава в соответствии с Табл. 1, а верхняя стрелка указывает на деградированный белок (~70 кДа), нижняя стрелка показывает полноразмерный белок (83 кДа).
Однако дигидрофосфат калия является одним из ключевых компонентов среды для культивирования гриба P. canescens, поскольку выступает в качестве источника фосфора. Также в качестве источника фосфора может выступать фитин, который содержится в семенах зерновых, бобовых и картофеле. Таким образом, проводят частичное замещение дигидрофосфата калия на растительные субстраты, содержащие фосфор, также в среду вносят дополнительно хлорид кальция. Состав сред указан в Табл. 1, отметим, что среда №1 - классическая среда для культивирования P. canescens, где в г/л: соевая шелуха - 45, кукурузный экстракт - 50, KH2PO4 - 25. Соевая шелуха используется качестве индуктора ксиланазного промотора;
среда №2 содержит в два раза меньше дигидрофосфата калия по сравнению со средой №1;
среда №3 содержит в четыре раза меньше дигидрофосфата калия по сравнению со средой №1;
среды №4-8 также содержат в четыре раза меньше KH2PO4 по сравнению со средой №1;
среда №4 содержит дополнительно 0,23 г/л хлорида кальция;
среда №5 в качестве дополнительного источника фосфатов содержит пророщеный горох, среда №6 - горох сухой, среда №7 - картофель;
среда №8 содержит фитат натрия и солодовый экстракт в качестве дополнительного источника фосфатов, а также 0,23 г/л хлорида кальция.
На фореграммах образцов культуральной жидкости рекомбинантных штаммов P. canescens CS15 в 7%-ном ПААГ на 6-е сутки культивирования (Рис. 6) видно, что снижение концентрации дигидрофосфата калия не привело к существенному снижению секретируемого белка P. canescens. В образцах 4 и 8 не наблюдали деградацию целевого белка, поскольку среды 4 и 8 содержали дополнительно 0,23 г/л хлорида кальция, концентрация ионов кальция в среде, по-видимому, была достаточной для стабилизации целевого белка. Молекулярная масса тяжелой полосы Cel48S соответствует 83 кДа, легкой полосы - около 70 кДа. Таким образом, целевые белки стабилизированы в результате снижения концентрации дигидрофосфата калия до 6 г/л и добавления 0,23 г/л хлорида кальция.
Анализируя полученные данные, можно заключить, что состав среды №4 является оптимальным для культивирования рекомбинантного штамма P. canescens CS15 ВКМ F-4679D.
| название | год | авторы | номер документа |
|---|---|---|---|
| РЕКОМБИНАНТНЫЙ ШТАММ МИЦЕЛИАЛЬНОГО ГРИБА PENICILLIUM CANESCENS CL14, ПРОДУЦИРУЮЩИЙ КОМПОНЕНТ ЦЕЛЛЛЮЛОСОМЫ CLOSTRIDIUM THERMOCELLUM, И СПОСОБ ЕГО КУЛЬТИВИРОВАНИЯ | 2016 |
|
RU2646132C1 |
| РЕКОМБИНАНТНЫЙ ШТАММ МИЦЕЛИАЛЬНОГО ГРИБА PENICILLIUM VERRUCULOSUM ( ВАРИАНТЫ) И СПОСОБ ПОЛУЧЕНИЯ ФЕРМЕНТНОГО ПРЕПАРАТА С ЕГО ИСПОЛЬЗОВАНИЕМ (ВАРИАНТЫ) | 2015 |
|
RU2646136C2 |
| НОВЫЙ РЕКОМБИНАНТНЫЙ ШТАММ (ВАРИАНТЫ) МИЦЕЛИАЛЬНОГО ГРИБА PENICILLIUM VERRUCULOSUM И ФЕРМЕНТНЫЙ ПРЕПАРАТ (ВАРИАНТЫ), ПРЕДНАЗНАЧЕННЫЙ ДЛЯ ГИДРОЛИЗА ПЛОДОВО-ЯГОДНОГО СЫРЬЯ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2014 |
|
RU2574206C1 |
| ШТАММ ГРИБА Penicillium verruculosum B10 EGII ПРОДУЦЕНТ ЭНДО-1.3/1.4-β-ГЛЮКАНАЗЫ, ЦЕЛЛЮЛАЗЫ, β-ГЛЮКОЗИДАЗЫ И КСИЛАНАЗЫ И СПОСОБ ПОЛУЧЕНИЯ КОРМОВОГО КОМПЛЕКСНОГО ФЕРМЕНТНОГО ПРЕПАРАТА | 2012 |
|
RU2532840C2 |
| ФРАГМЕНТ ДНК МИЦЕЛИАЛЬНОГО ГРИБА PENICILLIUM VERRUCULOSUM, КОДИРУЮЩИЙ СИНТЕЗ СЕКРЕТИРУЕМОЙ ЭНДОГЛЮКАНАЗЫ III И ГРУППА ШТАММОВ PENICILLIUM CANESCENS, СИНТЕЗИРУЮЩИХ ЭНДОГЛЮКАНАЗУ III PENICILLIUM VERRUCULOSUM, СКОНСТРУИРОВАННЫХ МЕТОДАМИ ТРАНСФОРМАЦИИ И ГЕНЕТИЧЕСКОЙ ИНЖЕНЕРИИ НА ОСНОВЕ ЭТОГО ФРАГМЕНТА ДНК | 2001 |
|
RU2238974C2 |
| ГЕНЕТИЧЕСКАЯ КОНСТРУКЦИЯ ДЛЯ ОБЕСПЕЧЕНИЯ ЭКСПРЕССИИ КОМПЛЕКСА ФЕРМЕНТОВ ЭНДОГЛЮКАНАЗ И КСИЛАНАЗ В КЛЕТКАХ ГРИБА PENICILLIUM VERRUCULOSUM И СПОСОБ ПОЛУЧЕНИЯ КОМПЛЕКСНЫХ ФЕРМЕНТНЫХ ПРЕПАРАТОВ НА ЕГО ОСНОВЕ, ПРЕДНАЗНАЧЕННЫХ ДЛЯ КОРМОПРОИЗВОДСТВА | 2017 |
|
RU2653429C1 |
| КЛЕТКА МИЦЕЛИАЛЬНОГО ГРИБА Penicillium canescens - ПРОДУЦЕНТ КСИЛАНАЗЫ И ЛАККАЗЫ, СПОСОБ ПОЛУЧЕНИЯ КОМБИНИРОВАННОГО ФЕРМЕНТНОГО ПРЕПАРАТА КСИЛАНАЗЫ И ЛАККАЗЫ | 2012 |
|
RU2538149C2 |
| ШТАММ ГРИБА PENICILLIUM CANESCENS mtCBHI ПРОДУЦЕНТ ТЕРМОСТАБИЛЬНОЙ ЦЕЛЛОБИОГИДРОЛАЗЫ I И ФЕРМЕНТНЫЙ ПРЕПАРАТ НА ЕГО ОСНОВЕ ДЛЯ БИОКОНВЕРСИИ ВОЗОБНОВЛЯЕМОГО РАСТИТЕЛЬНОГО СЫРЬЯ В САХАРА | 2019 |
|
RU2741078C1 |
| ГЕНЕТИЧЕСКАЯ КОНСТРУКЦИЯ ДЛЯ ОБЕСПЕЧЕНИЯ ЭКСПРЕССИИ ЦЕЛЕВЫХ ГОМОЛОГИЧНЫХ И ГЕТЕРОЛОГИЧНЫХ ГЕНОВ В КЛЕТКАХ МИЦЕЛИАЛЬНОГО ГРИБА PENICILLIUM VERRUCULOSUM, ИСПОЛЬЗУЕМОГО В КАЧЕСТВЕ ХОЗЯИНА, СПОСОБ ПОЛУЧЕНИЯ ШТАММА ГРИБА PENICILLIUM VERRUCULOSUM И СПОСОБ ПОЛУЧЕНИЯ ФЕРМЕНТНОГО ПРЕПАРАТА | 2008 |
|
RU2378372C2 |
| СПОСОБ ПОЛУЧЕНИЯ ФЕРМЕНТНОГО ПРЕПАРАТА ДЛЯ РАСЩЕПЛЕНИЯ ГЕМИЦЕЛЛЮЛОЗНЫХ ГЕТЕРОПОЛИСАХАРИДОВ КЛЕТОЧНОЙ СТЕНКИ РАСТЕНИЙ И ФЕРМЕНТНЫЙ ПРЕПАРАТ (ВАРИАНТЫ) | 2007 |
|
RU2358756C1 |



Настоящее изобретение относится к области биохимии, биотехнологии и микробиологической промышленности, в частности к рекомбинантному штамму мицелиального гриба Penicillium canescens CS15 ВКМ F-4679D, секретирующего термостабильную целлюлазу Cel48S из Clostridium thermocellum. Изобретение также раскрывает способ культивирования указанного штамма в особой питательной среде. Указанная питательная среда состоит из 35 г/л соевой шелухи, 40 г/л кукурузного экстракта, 6 г/л KH2PO4, 0,23 г/л CaCl2, 0,3 г/л MgSO4*7H2O, 10 г/л дрожжевого экстракта и 10 г/л пшеничных отрубей. Настоящее изобретение позволяет осуществлять эффективную продукцию целлюлазы из Clostridium thermocellum в гетерологичном хозяине Penicillium canescens. 2 н.п. ф-лы, 6 ил., 1 табл., 4 пр.
1. Рекомбинантный штамм гриба Penicillium canescens CS15 ВКМ F-4679D, продуцирующий бактериальную термофильную целлюлазу Clostridium thermocellum с молекулярной массой 83 кДа.
2. Способ культивирования, заключающийся в выращивании штамма по п. 1, на питательной среде следующего состава (г/л): соевая шелуха - 35, кукурузный экстракт - 40, KH2PO4 - 6, CaCl2 - 0,23, MgSO4×7H2O - 0,3, дрожжевой экстракт - 10, пшеничные отруби - 10.
| ШТАММ МИЦЕЛИАЛЬНОГО ГРИБА PENICILLIUM VERRUCULOSUM - ПРОДУЦЕНТ КОМПЛЕКСА ЦЕЛЛЮЛАЗ, КСИЛАНАЗЫ И КСИЛОГЛЮКАНАЗЫ И СПОСОБ ПОЛУЧЕНИЯ ФЕРМЕНТНОГО ПРЕПАРАТА КОМПЛЕКСА ЦЕЛЛЮЛАЗ, КСИЛАНАЗЫ И КСИЛОГЛЮКАНАЗЫ ДЛЯ ГИДРОЛИЗА ЦЕЛЛЮЛОЗЫ И ГЕМИЦЕЛЛЮЛОЗЫ | 2008 |
|
RU2361918C1 |
| СИНИЦЫНА О.А.и др., Рекомбинантная эндо-1,4-β-ксиланаза Penicillium canescens, Биохимия, 2003, том 68, номер 12, с.1631-1638 | |||
| ФРАГМЕНТ ДНК PCG 2,6, КОДИРУЮЩИЙ СИНТЕЗ СЕКРЕТИРУЕМОЙ БЕТА-ГАЛАКТОЗИДАЗЫ PENICILLIUM CANESCENS, И ШТАММ ГРИБА PENICILLIUM CANESCENS - ПРОДУЦЕНТ СЕКРЕТИРУЕМОЙ БЕТА-ГАЛАКТОЗИДАЗЫ | 1997 |
|
RU2126049C1 |
| US 20120030839 A1, 02.02.2012. | |||
Авторы
Даты
2017-03-02—Публикация
2015-12-18—Подача