Перекрестная ссылка на родственные заявки
По настоящей заявке испрашивается приоритет предварительной заявки Соединенных Штатов 61/322578, поданной 9 апреля 2010 г., и предварительной заявки Соединенных Штатов 61/345837, поданной 18 мая 2010 г., содержание которых приведено в настоящем описании в качестве ссылки в полном объеме.
Область техники, к которой относится изобретение
В настоящем документе описываются антитела и антигенсвязывающие фрагменты антител, которые связываются с растворимым белком человека, продуктом гена 2, экспрессируемым при стимуляции роста (ST2), наборы, содержащие эти антитела и фрагменты антител, и способы анализа с использованием этих антител и фрагментов антител.
Известный уровень техники
ST2 представляет собой член семейства рецепторов интерлейкина-1, имеющий трансмембранную и растворимую (sST2 или растворимый ST2) изоформы (Iwahana et al., Eur. J. Biochem. 264:397-406, 1999). В опубликованных в последнее время статьях описаны текущие представления об отношении ST2 к воспалительным заболеваниям (Arend et al., Immunol. Rev. 223:20-38, 2008; Kakkar et al., Nat. Rev. Drug Discov, 7:827-840, 2008; Hayakawa et al., J. Biol. Chem. 282:26369-26380, 2007; Trajkovic et al., Cytokine Growth Factor Rev. 15:87-95, 2004). Концентрации растворимого ST2 человека в циркуляторном русле повышены у больных, страдающих различными нарушениями, связанными с аномальным ответом Т-хелперных клеток типа 2 (Th2), включая системную красную волчанку и астму, а также воспалительные процессы, которые в основном не зависят от ответа Th2, такие как септический шок и травма (Trajkovic et al., Cytokine Growth Factor Rev. 15:87-95, 2004; Brunner et al., Intensive Care Med. 30:1468-1473, 2004). Более того, сигнализация системы интерлейкин-33/ST2L представляет собой ключевой механизм защиты сердца в случае механической перегрузки (Seki et al., Circulation Heart Fail. 2:684-691, 2009; Kakkar et al., Nat. Rev. Drug Discov. 7:827-40, 2008; Sanada et al., J. Clin. Invest. 117:1538-1549, 2007). Повышение растворимого ST2 человека служит также предсказанием плохого прогноза у больных с сердечной недостаточностью (HF) и больных инфарктом миокарда (Kakkar et al., Nat. Rev. Drug Discov. 7:827-40, 2008; Weinberg et al., Circulation 107:721-726, 2003; Shimpo et al., Circulation 109:2186-2190, 2004; Januzzi et al., J. Am. Coll. Cardiol. 50:607-613, 2007; Mueller et al., Clin. Chem. 54:752-756, 2008; Rehman et al., J. Am. Coll. Cardiol. 52:1458-65, 2008; Sabatine et al., Circulation 117:1936-1944, 2008). Повышенные уровни растворимого ST2 человека являются также прогностическими факторами смерти индивидуума в течение одного года (см., например, WO 07/127749). Суммируя изложенное выше, растворимый ST2 человека вовлечен в определенные воспалительные заболевания и в паракринную систему защиты сердца, а также является маркером, предсказывающим прогноз у больных сердечной недостаточностью и предсказывающим смерть индивидуума в течение года.
Сущность изобретения
Настоящее изобретение основывается, по меньшей мере частично, на разработке новых антител, специфичных в отношении растворимого белка ST2 человека. Эти антитела и их антигенсвязывающие фрагменты пригодны, например, для количественной оценки уровня растворимых белков ST2 человека в биологических образцах (например, в клинических образцах), для прогнозирования риска смерти в течение одного года у индивидуума, для определения того, надо ли выписывать индивидуума или следует начинать или продолжать терапию индивидуума (например, стационарного больного), и для отбора индивидуума для участия в клиническом исследовании. В настоящем описании предлагаются эти антитела и их антигенсвязывающие фрагменты, наборы, содержащие эти антитела и фрагменты антител, и различные способы использования этих антител и фрагментов антител.
В настоящем описании предлагаются выделенные антитела и их антигенсвязывающие фрагменты, которые являются конкурентами или связываются, конкурируя с антителом, продуцируемым гибридомами, депонированными в Американской коллекции типовых культур (ATCC) и обозначенными патентными депозитными номерами PTA-10431 и PTA-10432. В некоторых вариантах осуществления антитело или его фрагмент связывается, не конкурируя с любым или обоими антителами D066-3 или D067-3 (MBL International) (описанными в патенте США № 7087396), или обладает KD связывания с растворимым ST2 человека, равной или меньшей 1,51×10-9 M. В некоторых вариантах осуществления антитело или его фрагмент обладают KD связывания с растворимым ST2 человека, равной или меньшей 8,59×10-10 M. В некоторых вариантах осуществления антитело или его фрагмент являются гибридными или гуманизированными. В некоторых вариантах осуществления фрагмент выбран из группы: Fab фрагмента, F(ab’)2 фрагмента и scFv фрагмента. В некоторых вариантах осуществления антитело или его фрагмент гликозилированы. В некоторых вариантах осуществления антитело или его фрагмент содержат одну или более областей, определяющих комплементарность, легкой или тяжелой цепи антитела, продуцируемого гибридомой, депонированной в ATCC и обозначенной патентными депозитными номерами PTA-10431 и PTA-10432. В некоторых вариантах осуществления антитело представляет собой антитело, продуцируемое гибридомой, депонированной в ATCC и обозначенной патентным депозитным номером PTA-10431, или его антигенсвязывающий фрагмент, или антитело, продуцируемое гибридомой, депонированной в ATCC и обозначенной патентным депозитным номером PTA-10432, или его антигенсвязывающий фрагмент.
Изобретение также относится к выделенным антителам и их антигенсвязывающим фрагментам, которые специфически связываются с растворимым ST2 человека, где антитела и их антигенсвязывающие фрагменты получают с помощью способа, который предусматривает иммунизацию млекопитающего, не являющегося человеком (например, мыши, крысы, кролика, козы, коровы, свиньи, обезьяны или лошади), рекомбинантным растворимым ST2 человека, выделенным из клетки человека (например, фибробласта человека, нейрональной, эпителиальной или эндотелиальной клетки человека, клетки эмбриона или взрослого человека, особенно из эмбриональной клетки почки человека). В некоторых вариантах осуществления выделенный рекомбинантный растворимый ST2 человека является полностью гликозилированным, т.е. имеет по существу тот же самый профиль гликозилирования, что и природный эндогенный растворимый ST2 человека, присутствующий в сыворотке человека. В некоторых вариантах осуществления всех антител и фрагментов, описанных в настоящем документе, антитело или его фрагмент является меченым.
Настоящее изобретение также относится к клеткам гибридомы, депонированной в ATCC и обозначенной патентным депозитным номером PTA-10431, и клетки гибридомы, депонированной в ATCC и обозначенной патентным депозитным номером PTA-10432.
Настоящее изобретение также относится к способам количественной оценки уровня растворимого ST2 человека в образце, взятом у индивидуума. Способы включают приведение образца в контакт с по меньшей мере одним антителом или его фрагментом, описанными в настоящем документе, и определение связывания антитела или его фрагмента с растворимым ST2 человека. В некоторых вариантах осуществления способ включает использование по меньшей мере двух различных антител или их фрагментов, описанных в настоящем документе.
Настоящее изобретение также относится к способам прогнозирования риска смерти в течение одного года у индивидуума. Способы включают получение образца у индивидуума и определение уровня растворимого ST2 человека с использованием по меньшей мере одного антитела или его фрагмента, описанных в настоящем документе, где повышенный уровень растворимого ST2 человека в образце по сравнению с реперным уровнем растворимого ST2 человека указывает на то, что у индивидуума существует повышенный риск смерти в течение одного года (например, повышенный риск смерти в течение одного года по сравнению с индивидуумом (например, индивидуумом с тем же заболеванием), который имеет пониженный уровень или по существу тот же уровень растворимого ST2 человека по сравнению с тем же контролем), и где пониженный уровень или по существу тот же уровень растворимого ST2 человека указывает на то, что у индивидуума существует низкий риск смерти в течение одного года (например, низкий риск смерти в течение одного года по сравнению с индивидуумом (например, индивидуумом с тем же заболеванием), который имеет повышенный уровень или по существу тот же уровень растворимого ST2 человека по сравнению с тем же контролем).
Настоящее изобретение также относится к способам определения того, надо ли выписывать стационарного больного или следует начинать или продолжать лечение индивидуума на базе стационара, где способ включает получение образца у индивидуума и определение уровня растворимого ST2 человека в образце с использованием по меньшей мере одного антитела или его фрагмента, описанных в настоящем документе, где повышенный уровень растворимого ST2 человека в образце по сравнению с реперным уровнем растворимого ST2 человека указывает на то, что следует начинать или продолжать лечение стационарного больного, а пониженный уровень или одинаковый уровень растворимого ST2 человека указывает на то, что индивидуума можно выписывать из стационара. В некоторых вариантах осуществления индивидуум имеет по меньшей мере один или более из следующих симптомов: боль или дискомфорт в груди, одышка, тошнота, рвота, отрыжка, испарина, учащенное сердцебиение, головокружение, утомление и слабость.
Настоящее изобретение также относится к способам отбора индивидуума для участия в клиническом исследовании, где способы включают взятие образца у индивидуума, определение уровня растворимого ST2 человека в образце с использованием по меньшей мере одного антитела или его фрагмента, описанных в настоящем документе, и отбора индивидуума для участия в клиническом исследовании, если уровень растворимого ST2 человека у индивидуума относительно реперного уровня растворимого ST2 человека указывает на то, что индивидуум должен быть выбран для участия в клиническом исследовании. В некоторых вариантах осуществления наличие повышенного уровня растворимого ST2 человека указывает на то, что индивидуум должен быть выбран для участия в клиническом исследовании.
Настоящее изобретение также относится к способам выбора терапии индивидуума, включающим определение уровня растворимого ST2 человека в биологическом образце, взятом у индивидуума, с использованием по меньшей мере одного антитела или его фрагмента, описанных в настоящем документе, где уровень растворимого ST2 человека у индивидуума относительно реперного уровня растворимого ST2 человека используется для выбора терапии индивидуума. В некоторых вариантах осуществления наличие повышенного уровня растворимого ST2 человека используется для выбора терапии индивидуума.
В некоторых вариантах осуществления любого из описанных в настоящем документе способов у индивидуума отсутствует диагноз или отсутствуют два или более (например, по меньшей мере три, четыре или пять) симптома заболевания; индивидууму поставлен диагноз (например, диагноз сердечная недостаточность, заболевание коронарных артерий, сердечно-сосудистое заболевание, острый коронарный синдром, почечная недостаточность, инсульт или любое заболевание, описанное в настоящем документе); или у индивидуума наблюдается одно или более из: гипертриглицеридемии, гиперхолестеринемии, гипертензии и индекса массы тела ≥30. В некоторых вариантах осуществления любого из описанных в настоящем документе способов определение осуществляется с использованием по меньшей мере двух антител или их фрагментов, описанных в настоящем документе.
В некоторых вариантах осуществления любого из описанных в настоящем документе способов реперный уровень растворимого ST2 человека представляет собой пороговый уровень растворимого ST2 человека. В некоторых вариантах осуществления пороговый уровень представляет собой средний уровень растворимого ST2 человека в популяции здоровых людей (например, в популяции здоровых мужчин или в популяции здоровых женщин). В некоторых вариантах осуществления любого из описанных в настоящем документе способов реперный уровень представляет собой уровень растворимого ST2 человека, присутствующий в образце индивидуума, у которого отсутствуют два или более симптомов заболевания, индивидуума, у которого диагностировано отсутствие болезни, или индивидуума, у которого не идентифицирован риск развития заболевания.
В любом из описанных в настоящем документе способов у индивидуума диагностировано отсутствие болезни (например, сердечной недостаточности, заболевания коронарных артерий, сердечно-сосудистого заболевания, острого заболевания коронарных артерий, острого коронарного синдрома, почечной недостаточности или инсульта, или любого из заболеваний, описанных в настоящем документе). В любом из описанных в настоящем документе способов образец содержит кровь, сыворотку или плазму. Любое из антител и их фрагментов, описанных в настоящем документе, может быть использовано в любом из описанных в настоящем документе способов.
Настоящее изобретение также относится к способам диагностики заболевания у индивидуума, включающим взятие образца у индивидуума, определение уровня растворимого ST2 человека в образце с использованием по меньшей мере одного антитела или его фрагмента, описанных в настоящем документе, и уровня по меньшей мере одного дополнительного маркера, где повышенный уровень растворимого ST2 человека в образце по сравнению с реперным уровнем растворимого ST2 человека и измененный уровень по меньшей мере одного дополнительного маркера относительно реперного уровня по меньшей мере одного дополнительного маркера указывает на то, что у индивидуума есть заболевание (например, сердечно-сосудистое заболевание, легочное заболевание, сепсис, болезнь Кавасаки или заболевание, связанное с Th2, или любое из других заболеваний, описанных в настоящем документе).
Настоящее изобретение также относится к способам определения того, имеет ли индивидуум нормальный уровень растворимого ST2 человека (и, следовательно, очевидно не страдает тяжелым заболеванием, например, сердечно-сосудистым заболеванием, и имеет обычный риск смерти или госпитализации, например, в течение одного года), включающие взятие образца у индивидуума и определение уровня растворимого ST2 человека в образце, где индивидуум характеризуется как имеющий нормальный уровень растворимого ST2 человека, если уровень растворимого ST2 человека попадает в особый диапазон (например, от приблизительно 14,5 до приблизительно 25,3 нг/мл или от приблизительно 18,1 до приблизительно 19,9 нг/мл). В некоторых вариантах осуществления индивидуум мужского пола характеризуется как имеющий нормальный уровень растворимого ST2 человека, если уровень растворимого ST2 человека находится в пределах любого диапазона, представленного в таблице 9. В некоторых вариантах осуществления индивидуум женского пола характеризуется как имеющий нормальный уровень растворимого ST2 человека, если уровень растворимого ST2 человека находится в пределах любого диапазона, представленного в таблице 9.
Настоящее изобретение также относится к наборам, содержащим по меньшей мере одно (например, два, три, четыре или пять) антитело или его антигенсвязывающий фрагмент, описанное в настоящем документе. Некоторые варианты осуществления этих наборов содержат два антитела или их антигенсвязывающих фрагмента, описанных в настоящем документе. В некоторых вариантах осуществления этих наборов по меньшей мере одно из антител или их фрагментов характеризуется KD связывания с растворимым ST2 человека (например, с рекомбинантным растворимым ST2 человека), равной или меньшей 8,59×10-10 М. В некоторых вариантах осуществления набор предлагается в виде набора на основе твердофазного иммуноферментного анализа (ELISA). В некоторых вариантах осуществления набор дополнительно содержит рекомбинантный растворимый ST2 человека, выделенный из клетки человека (например, клетки эмбриональной почки человека). В некоторых вариантах осуществления рекомбинантный растворимый ST2 человека полностью гликозилирован.
Под термином «растворимый ST2» подразумевается растворимый белок, содержащий последовательность, которая по меньшей мере на 90% (например, по меньшей мере на 95%, 96%, 97%, 98%, 99% или 100%) идентична последовательности NCBI с № поступления NP 003847.2 (SEQ ID NO: 1), или нуклеиновая кислота, содержащая последовательность, которая по меньшей мере на 90% (например, по меньшей мере на 95%, 96%, 97%, 98%, 99% или 100%) идентична последовательности NCBI с № поступления NM_003856.2 (SEQ ID NO: 2).
Под термином «повышенный» или «повышение» подразумевается различие, например, статистически значимое различие (например, повышение), в определенном или измеренном уровне (например, в уровне растворимого белка ST2 человека) по сравнению с реперным уровнем (например, с уровнем растворимого ST2 человека у индивидуума, не страдающего заболеванием, у индивидуума, не проявляющего двух или более симптомов заболевания, или у индивидуума, у которого не идентифицировано наличие риска развития заболевания или порогового уровня растворимого ST2 человека). В некоторых вариантах осуществления реперным является пороговый уровень, и любой уровень выше этого рассматривается как «повышенный». Дополнительные реперные уровни растворимого ST2 человека описываются в настоящем документе.
Под термином «учреждение здравоохранения» подразумевается помещение, в котором индивидуум может получать медицинскую помощь от работника здравоохранения (например, медицинской сестры, врача или фельдшера). Неограничивающие примеры учреждений здравоохранения включают госпитали, клиники и учреждения лечебного попечения (например, дом престарелых).
Под термином «стационарный больной» подразумевается индивидуум, который госпитализирован в учреждение здравоохранения (например, в госпиталь или учреждение лечебного попечения).
Под термином «лечение стационарного больного» подразумевается мониторинг и/или медицинское лечение индивидуума, который госпитализирован в учреждение здравоохранения (например, в госпиталь или учреждение лечебного попечения). Например, индивидууму, получающему лечение в качестве стационарного больного, могут быть введены профессиональным работником здравоохранения одно или более терапевтических средств или ему может быть назначена лечебная процедура (например, хирургическое вмешательство (например, трансплантация органа, хирургическое шунтирование сердца), ангиопластика, визуализация (например, магниторезонансная визуализация, ультразвуковая визуализация и сканирование с помощью компьютерной томографии)). В других примерах один или более маркеров заболевания или тяжести состояния могут периодически измеряться профессиональным работником здравоохранения для оценки тяжести или прогрессирования заболевания или состояния индивидуума.
Под термином «реперный уровень» подразумевается пороговый уровень, или уровень у контрольного индивидуума, или в контрольной популяции больных. Реперный уровень может зависеть от осуществляемого метода тестирования и может быть определен специалистом в данной области техники. Реперный уровень может представлять собой исходный уровень или уровень у того же самого индивидуума, измеренный в более раннюю или более позднюю точку времени. Некоторые неограничивающие примеры реперных уровней растворимого ST2 человека включают уровень растворимого ST2 человека у индивидуума, у которого: отсутствует диагноз болезни; отсутствуют по меньшей мере два или более симптомов заболевания; нет высокого риска CVD; нет почечной недостаточности; нет гипертриглицеридемии, гиперхолестеринемии, гипертензии и/или индекс массы тела <30 (например, BMI ниже 25); нет риска развития заболевания; и/или он не страдает заболеванием, связанным с повышенными уровнями ST2 (например, сердечно-сосудистым заболеванием, легочным заболеванием, сепсисом, болезнью Кавасаки или заболеванием, связанным с Th2, или любым из других заболеваний, описанных в настоящем документе). Дополнительные контрольные популяции больных описаны в настоящем документе. Дополнительные примеры реперных уровней растворимого ST2 человека представляют собой пороговые уровни растворимого ST2 человека. Реперные уровни растворимого ST2 человекам могут быть определены с использованием методов, известных в данной области техники; некоторые иллюстративные уровни описаны в настоящем документе.
В некоторых вариантах осуществления рассчитывают отношение двух уровней растворимого ST2 человека у индивидуума. Реперное отношение можно сравнивать с реперным отношением уровней растворимого ST2 человека, измеренным у индивидуума (например, у любого из контрольных индивидуумов, описанных в настоящем документе, или у того же самого индивидуума), например, реперное отношение может представлять собой отношение уровней растворимого ST2 человека перед и после возникновения симптомов заболевания (например, заболевания сердца (например, сердечной недостаточности, заболевания коронарных артерий, сердечно-сосудистого заболевания, острого коронарного синдрома и стенокардии), почечной недостаточности или инсульта, или любого другого заболевания, связанного с повышенными уровнями растворимого ST2 человека, как описано в настоящем документе); отношение уровней растворимого ST2 человека перед диагностикой заболевания и после диагностики (например, заболевания сердца (например, сердечной недостаточности, заболевания коронарных артерий, сердечно-сосудистого заболевания, острого коронарного синдрома и стенокардии), почечной недостаточности или инсульта, или любого из других заболеваний, описанных в настоящем документе); отношение уровней ST2 перед терапией заболевания и после лечения (например, заболевания сердца (например, сердечной недостаточности, заболевания коронарных артерий, сердечно-сосудистого заболевания, острого коронарного синдрома и стенокардии), почечной недостаточности или инсульта, или любого из других заболеваний, описанных в настоящем документе); отношение уровней растворимого ST2 человека в двух различных точках времени в течение терапии (например, лечения стационарного или амбулаторного больного) заболевания (например, заболевания сердца (например, сердечной недостаточности, заболевания коронарных артерий, сердечно-сосудистого заболевания, острого коронарного синдрома и стенокардии), почечной недостаточности или инсульта, или любого из других заболеваний, описанных в настоящем документе); или отношение уровней растворимого ST2 человека перед эпизодом заболевания сердца (например, инфаркта миокарда) и после него.
В некоторых вариантах осуществления отношение уровней растворимого ST2 человека, измеренное у индивидуума, можно сравнивать с пороговым реперным отношением. Реперные отношения растворимого ST2 человека могут быть определены методами, известными в данной области; реперные отношения растворимого ST2 человека могут быть рассчитаны с использованием данных, представленных в настоящем описании. Например, реперное отношение растворимого ST2 человека может составлять от приблизительно 0,7 до приблизительно 1,1 или приблизительно 1.
Под термином «терапия» или «лечение» подразумевается введение одного или более терапевтических средств индивидууму или выполнение медицинской процедуры на организме индивидуума (например, хирургического вмешательства, такого как трансплантация органа или хирургия сердца). Неограничивающие примеры фармацевтических средств, которые можно вводить индивидууму, включают нитраты, блокаторы кальциевых каналов, диуретики, тромболитические средства, дигиталис, средства, модулирующие работу ренин-ангиотензин-альдостероновой системы (RAAS) (например, бета-адреноблокаторы, ингибиторы ангиотензинпревращающего фермента, антагонисты альдостерона, ингибиторы ренина и блокаторы рецептора ангиотензина II), и средства, понижающие холестерин (например, статин). Термин "терапия" также включает доведение дозы (например, повышение или снижение) или частоты введения одного или более фармацевтических средств, которые может принимать индивидуум, введение одного или более новых фармацевтических средств индивидууму или удаление одного или более фармацевтических средств из плана лечения индивидуума.
Как используется в настоящем описании, под «индивидуумом» понимают млекопитающее, например, человека.
Как используется в настоящем описании, под «биологическим образцом» понимают одно или более из крови, сыворотки, плазмы, мочи и ткани организма. Обычно биологический образец представляет собой образец, содержащий сыворотку, кровь или плазму.
Как используется в настоящем описании, термин «антитело» относится к белку, который обычно содержит полипептиды тяжелой цепи и полипептиды легкой цепи. Распознавание и связывание антигена осуществляется вариабельными областями тяжелых и легких цепей. Известны также антитела с одним доменом, имеющие одну тяжелую цепь и одну легкую цепь, и антитела из тяжелых цепей, лишенные легких цепей. Такое антитело включает один из пяти различных типов тяжелых цепей, называемых альфа, дельта, ипсилон, гамма и мю, классификация которых основывается на аминокислотной последовательности константной области тяжелой цепи. Эти различные типы тяжелых цепей дают начало пяти классам антител, IgA (включая IgA1 и IgA2), IgD, IgE, IgG (IgG1, IgG2, IgG3 и IgG4) и IgM, соответственно. Такое антитело включает также один из двух типов легких цепей, называемых каппа или лямбда, классификация которых основана на аминокислотной последовательности константных доменов легких цепей. Антитела IgG, IgD и IgE обычно содержат две идентичные тяжелые цепи и две идентичные легкие цепи, и два антигенсвязывающих домена, причем каждый включает вариабельную область тяжелой цепи (VH) и вариабельную область легкой цепи (VL). Обычно антитела IgA состоят из двух мономеров, где каждый мономер состоит из двух тяжелых цепей и двух легких цепей (как в случае антител IgG, IgD и IgE). В этом случае молекула IgA имеет четыре антигенсвязывающих домена, причем каждый снова состоит из VH и VL. Определенные антитела IgA являются мономерными в том смысле, что они состоят из двух тяжелых цепей и двух легких цепей. Секретируемые антитела IgM обычно состоят из пяти мономеров, причем каждый мономер состоит из двух тяжелых цепей и двух легких цепей (как в случае антител IgG и IgE). В этом случае секретируемая молекула IgM имеет десять антигенсвязывающих доменов, причем каждый снова состоит из VH и VL. Существует также форма IgM, связанная с клеточной поверхностью, и она имеет структуру две тяжелые цепи/две легкие цепи, сходно с антителами IgG, IgD и IgE.
Как используется в настоящем описании, термин «гибридное антитело» относится к антителу, которое сконструировано как содержащее по меньшей мере одну константную область человека. Например, одна или все (например, одна, две или три) вариабельные области легкой(ких) цепи(ей) и/или одна или все (например, одна, две или три) вариабельные области тяжелой(лых) цепи(ей) антитела мыши (например, мышиного моноклонального антитела) могут, каждая, присоединяться к константной области человека, такой как, без ограничения, константная область IgG1 человека. Гибридные антитела обычно менее иммуногенны для человека по сравнению с негибридными антителами и, следовательно, предоставляют терапевтические преимущества в определенных ситуациях. Специалисты в данной области техники должны быть знакомы с гибридными антителами и также должны быть знакомы с подходящими методами их создания. См., например, патенты США №№ 4816567; 4978775; 4975369; и патент США No. 4816397.
Как используется в настоящем описании, термин «полностью человеческие антитела» относится к антителам или антигенсвязывающим фрагментам антител, которые содержат аминокислотные последовательности, происходящие только от человека. Например, полностью человеческое антитело может быть получено из В-клетки человека или клетки гибридомы. В дополнительных вариантах осуществления антитело может быть получено от трансгенного животного, которое содержит локус тяжелой цепи иммуноглобулина человека и легкой цепи иммуноглобулина человека или содержит нуклеиновую кислоту, которая кодирует тяжелую и легкую цепи конкретного антитела человека.
«Область, определяющая комплементарность», или «CDR» в качестве термина используется в настоящем описании для обозначения коротких полипептидных последовательностей в пределах вариабельной области полипептидов как тяжелой, так и легкой цепи, которые, в первую очередь, опосредуют распознавание конкретного антигена. CDR описаны Kabat, et al., J. Biol. Chem. 252, 6609-6616, 1977; Chothia et al., J. Mol. Biol. 196:901-917, 1987; и MacCallum et al., J. Mol. Biol. 262:732-745, 1996. Существует три CDR (называемые CDR1, CDR2 и CDR3) в каждой VL и в каждой VH.
«Фрагмент» или «фрагмент антитела» в качестве термина используется в настоящем описании для обозначения полипептида, происходящего от полипептидной молекулы антитела (например, полипептида тяжелой и/или легкой цепи антитела), который не включает полноразмерный полипептид антитела, но который все еще включает по меньшей мере часть полипептида полноразмерного антитела, которая способна связывать антиген. Фрагменты антитела могут включать часть полипептида полноразмерного антитела после расщепления, хотя термин не ограничивается такими фрагментами расщепления. Фрагменты антитела могут включать, например, Fab фрагменты, F(ab’)2 фрагменты, scFv (одноцепочечные Fv) фрагменты, линейные антитела, моноспецифичные или мультиспецифичные фрагменты антител, таких как биспецифичные, триспецифичные и мультиспецифичные антитела (например, диатела, триатела, тетратела), минитела, хелатные рекомбинантные антитела, тритела или битела, нанотела, малые модуляторные иммунофармацевтические частицы (SMIP), слитые белки связывающих доменов иммуноглобулинов, антитела верблюдовых, и антитела, содержащие VHH. Дополнительные примеры антигенсвязывающих фрагментов антител известны в данной области техники.
«Каркасная область» в качестве термина используется в настоящем описании для обозначения аминокислотных последовательностей в пределах вариабельной области полипептидов как тяжелой, так и легкой цепей, которые не являются последовательностями CDR и, в первую очередь, отвечают за поддержание корректного положения последовательностей CDR для возможности связывания антигена. Хотя каркасные области сами по себе обычно прямо не участвуют в связывании антигена, как известно в данной области техники, определенные остатки в пределах каркасных областей определенных антител могут прямо участвовать в связывании антигена или могут влиять на способность одной или более аминокислот в CDR взаимодействовать с антигеном.
«Гуманизированное антитело» в качестве термина используется в настоящем описании для обозначения антитела, которое сконструировано как включающее в вариабельной области одну или более каркасных областей человека совместно с областями, определяющими комплементарность (CDR), не от человека (например, от мыши, крысы или хомячка) тяжелой и/или легкой цепи. В некоторых вариантах осуществления гуманизированное антитело включает последовательности, которые полностью происходят от человека за исключением областей CDR. Гуманизированные антитела обычно менее иммуногенны для человека по сравнению с негуманизированными антителами и таким образом предоставляют терапевтические преимущества в определенных ситуациях. Гуманизированные антитела известны в данной области техники и также известны подходящие способы создания гуманизированных антител. См., например, Hwang et al., Methods 36:35, 2005; Queen et al., Proc. Natl. Acad. Sci. U.S.A. 86:10029-10033, 1989; Jones et al., Nature 321:522-25, 1986; Riechmann et al., Nature 332:323-27, 1988; Verhoeyen et al., Science 239:1534-36, 1988; Orlandi et al., Proc. Natl. Acad. Sci. U.S.A. 86:3833-3837, 1989; патенты США №№ 5225539; 5530101; 5585089; 5693761; 5693762 и 6180370; и патент WO 90/07861.
Как используется в настоящем описании, термин «заболевание, связанное с Th2», относится к заболеванию, связанному с аномальным ответом клеток Т-хелперов типа 2 (Th2).
Как используется в настоящем описании, термин «сердечно-сосудистое заболевание» относится к нарушению работы кровеносных сосудов и сосудов сердца и включает нарушения работы артерий, вен, артериол, венул и капилляров.
Как используется в настоящем описании, термин «легочное заболевание» относится к нарушению работы легких.
Под термином «дополнительный маркер» подразумевается белок, нуклеиновая кислота, липид или углевод или их сочетание (например, двух или более), который является диагностическим критерием наличия конкретного заболевания. Описанные в настоящем документе способы диагностики наличия заболевания у индивидуума могут включать определение уровня растворимого ST2 человека и по меньшей мере одного дополнительного маркера в образце, взятом у индивидуума. Несколько дополнительных маркеров, пригодных для диагностирования заболевания, известны в данной области техники (например, proANP, NT-proANP, ANP, proBNP, NT-proBNP, BNP, тропонин, CRP, креатинин, азот мочевины крови (BUN), ферменты, характеризующие функцию печени, альбумин и бактериальный эндотоксин; и маркеры, которые описаны в патентных заявках США №№ 2007/0248981; 2011/0053170; 2010/0009356; 2010/0055683; 2009/0264779; каждая из которых таким образом включена в качестве ссылки).
Под термином «гипертриглицеридемия» понимают уровень триглицеридов, который выше или равен 180 нг/мл (например, выше или равен 200 нг/мл).
Под термином «гиперхолестеринемия» понимают повышенный уровень по меньшей мере одной формы холестерина или суммарного холестерина у индивидуума. Например, индивидуум с гиперхолестеринемией может иметь уровень липопротеинов высокой плотности (ЛПВП) ≥40 мг/дл (например, ≥50 мг/дл или ≥60 мг/дл), уровень липопротеинов низкой плотности (ЛПНП) ≥130 мг/дл (например, ≥160 мг/дл или ≥200 мг/дл) и/или уровень суммарного холестерина ≥200 мг/дл (например, 240 мг/дл).
Под термином «гипертензия» подразумевается повышенный уровень систолического и/или диастолического давления крови. Например, индивидуум, страдающий гипертензией, может иметь систолическое давление крови ≥120 мм Hg (например, ≥140 мм Hg или ≥160 мм Hg) и/или диастолическое давление крови ≥80 мм Hg (например, ≥90 мм Hg или ≥100 мм Hg).
Под термином «здоровый индивидуум» подразумевается индивидуум, который не имеет заболевания (например, сердечно-сосудистого заболевания или легочного заболевания). Например, у здорового индивидуума отсутствует диагноз болезни и не присутствуют один или более (например, два, три, четыре или пять) симптомов заболевания.
Под «риском смерти» подразумевается риск смерти индивидуума от заболевания или осложнений, связанных с заболеванием, относительно реперной популяции (например, контрольной популяции здоровых индивидуумов). Термин "риск смерти" при использовании в настоящем описании исключает предумышленную или случайную смерть, например, смерть от тупой травмы или травмы с размозжением, такой как при автомобильной аварии.
Если не указано иначе, все технические и научные термины, используемые в настоящем описании, имеют то же самое значение, что и обычно понимаемое специалистом в области техники, к которой принадлежит это изобретение. В настоящем документе описываются методы и вещества для использования в настоящем изобретении. Могут быть использованы также другие подходящие методы и вещества, известные в данной области техники. Вещества, методы и примеры являются только иллюстративными и не предназначены для ограничения. Все публикации, патентные заявки, патенты, последовательности, входы в базы данных и другие ссылки, упомянутые в настоящем описании, включены в качестве ссылок в полном объеме. В случае конфликта настоящее описание, включая определения, будет служить для контроля.
Другие признаки и преимущества изобретения должны быть понятны из приведенного ниже подробного описания и фигур, а также из формулы изобретения.
Описание фигур
Фиг.1 представляет собой изображение, демонстрирующее результаты анализа фракций в геле SDS-PAGE при очистке рекомбинантного растворимого белка ST2 человека. Дорожки (10 мкл пробы на дорожку) представляют собой следующее: 1 - MWM (5 мкл); 2 - His лестница (3 мкл); 3 - нетрансфицированный негативный контроль; 4 - супернатант перед очисткой; 5 - прохождение через колонку; 6 - отмывка 1 связывающим буфером; 7 - 5 мМ отмывка 2; 8 - 5 мМ отмывка 3; 9 - 200 мМ фракция 2 элюата; 10 - 200 мМ фракция 3 элюата; 11 - 200 мМ фракция 4 элюата; 12 - 200 мМ фракция 5 элюата; 13 - 200 мМ фракция 6 элюата; 14 - 200 мМ фракция 7 элюата; и 15 - 0,3 мкг растворимого ST2.
Фиг.2 представляет собой иммуноблотинг фракций очистки, определяющих гистидиновую метку в рекомбинантном растворимом белке ST2 человека. Дорожки (10 мкл пробы на дорожку) представляют собой следующее: 1 - MWM (5 мкл); 2 - His лестница (3 мкл); 3 - супернатант перед очисткой; 4 - прохождение через колонку; 5 - отмывка 1 связывающим буфером; 6 - отмывка 2 связывающим буфером; 7 - 5 мМ отмывка 2; 8 - 5 мМ отмывка 3; 9 - 200 мМ фракция 2 элюата; 10 - 200 мМ фракция 3 элюата; 11 - 200 мМ фракция 4 элюата; 12 - 200 мМ фракция 5 элюата; 13 - 200 мМ фракция 6 элюата; 14 - 200 мМ фракция 7 элюата; и 15 - 0,3 мкг растворимого ST2.
На фиг.3A-3C демонстрируется гель с Кумасси (фиг.3A) и два иммуноблота очищенного, рекомбинантного растворимого ST2, сравнивающих коммерческое антитело против ST2 D066 (MBL International) (фиг.3B) с гексагистидиновым антителом (фиг.3C). Дорожки (10 мкл образца/дорожка) представляют собой следующее: 1 - MWM; 2 - His лестница; 3 - 1000 нг ST2-His сыворотки; 4 - 500 нг ST2-His сыворотки; 5 - 200 нг ST2-His сыворотки; 6 - 100 нг ST2-His сыворотки; 7 - 50 нг ST2-His сыворотки; 8 - 1000 нг бессывороточного ST2-His; 9 - 500 нг бессывороточного ST2-His; 10 - 200 нг бессывороточного ST2-His; 11 - 100 нг бессывороточного ST2-His; и 12 - 50 нг бессывороточного ST2-His.
Фиг.4 представляет собой линейный график, демонстрирующий результаты оценки чувствительности к антигену антител 7E4 и 9F8.
Фиг.5 представляет собой линейный график, демонстрирующий результаты оценки чувствительности к антигену антител 7E4 и 9F8. Антителами 7E4 и 9F8 в концентрациях в диапазоне от 5 мкг/мл до 0 покрывали индивидуальные лунки в 96-луночном планшете и тестировали против единственной концентрации рекомбинантного растворимого ST2, конъюгированного с биотином.
Фиг.6 представляет собой линейный график, демонстрирующий результаты тестирования их способности использоваться вместе в конфигурации сендвич-метода иммуноферментного анализа (EIA) с моноклональными антителами, где либо антитело 7E4, либо антитело 9F8 биотинилировано.
Фиг.7A-7F представляют собой шесть графиков, демонстрирующих результаты анализа с помощью поверхностного плазмонного резонанса (SPR) образования комплексов антитело-антиген. На фиг.7A представлен анализ SPR антитела 9F8 (L1). На фиг.7B представлен анализ SPR антитела 7E4 (L2). На фиг.7C представлен анализ SPR антитела 11A7 (L3). На фиг.7D представлен анализ SPR антитела D066 (L4). На фиг.7E представлен анализ SPR антитела D067 (L5). На фиг.7F представлен анализ SPR неродственного антитела (L6).
Фиг.8A-8F представляют собой шесть графиков, демонстрирующих результаты анализа SPR образования комплексов антитело-антиген. На фиг.8A представлен анализ SPR антитела 9F8 (L1). На фиг.8B представлен анализ SPR антитела 7E4 (L2). На фиг.8C представлен анализ SPR антитела 11A7 (L3). На фиг.8D представлен анализ SPR антитела 15D6 (L4). На фиг.8E представлен анализ SPR антитела D066 (L5). На фиг.8F представлен анализ SPR антитела D067 (L6).
На фиг.9 представлена диаграмма медиан «боксы-усы», демонстрирующая концентрации растворимого ST2 человека в разных типах антикоагуляторных пробирок.
Фиг.10 представляет собой гистограмму, демонстрирующую распределение концентраций растворимого ST2 человека у нормальных здоровых доноров.
На фиг.11 представлена диаграмма медиан «боксы-усы», демонстрирующая концентрации растворимого ST2 человека как функцию пола и возраста у нормальных здоровых доноров.
Подробное описание
В настоящем документе описываются антитела и их антигенсвязывающие фрагменты, которые специфически связываются с растворимым ST2 человека, наборы, содержащие эти антитела и фрагменты, и способы использования этих антител и фрагментов.
ST2
Ген ST2 является членом семейства рецепторов интерлейкина-1, чей белковый продукт существует как в трансмембранной форме, так и в виде растворимого рецептора, который определяется в сыворотке (Kieser et al., FEBS Lett. 372(2-3): 189-193, 1995; Kumar et al., J. Biol. Chem. 270(46):27905-27913, 1995; Yanagisawa et al., FEBS Lett. 302(l):51-53, 1992; Kuroiwa et al., Hybridoma 19(2): 151-159, 2000). Растворимый ST2, как описано, существенно позитивно регулируется в экспериментальной модели сердечной недостаточности (Weinberg et al., Circulation 106(23):2961-2966, 2002), и данные предполагают, что концентрации растворимого ST2 человека также растут у больных с хронической тяжелой сердечной недостаточностью (Weinberg et al., Circulation 107(5) 721-726, 2003), а также у больных с острым инфарктом миокарда (Shimpo et al., Circulation 109(18):2186-2190, 2004).
Не желая привязываться к теории, трансмембранная форма ST2, как считается, играет роль в модулировании ответов Т-хелперных клеток типа 2 (Lohning et al., Proc. Natl. Acad. Sci. U.S.A. 95(12):6930-6935, 1998; Schmitz et al., Immunity 23(5):479-490, 2005) и может играть роль в развитии толерантности при состояниях тяжелого или хронического воспаления (Brint et al., Nat. Immunol. 5(4):373-379, 2004), тогда как растворимая форма ST2 позитивно регулируется в фибробластах при стимуляции роста (Yanagisawa et al., 1992, выше). Экспериментальные данные предполагают, что ген ST2 существенно позитивно регулируется при состояниях растяжения кардиомиоцитов (Weinberg et al., 2002, выше) способом, аналогичным индукции гена BNP (Bruneau et al., Cardiovasc. Res. 28(10): 1519-1525, 1994).
Tominaga et al. (FEBS Lett. 258:301-304, 1989) выделили гены мыши, которые экспрессируются в особенности при стимуляции роста в клетках BALB/c-3T3. Haga et al. (Eur. J. Biochem. 270: 163-170, 2003) пишут, что ген ST2 был назван на основании его индукции при стимуляции роста. Ген ST2 кодирует два белковых продукта: ST2 или sST2, который представляет собой растворимую секретируемую форму, и ST2L, трансмембранную рецепторную форму, которая очень сходна с рецепторами интерлейкина-1. Терминологический комитет HUGO назвал гомолог ST2 человека, клонирование которого описано в Tominaga et al., Biochim. Biophys. Acta. 1171:215-218, 1992, как белок, подобный рецептору 1 интерлейкина 1 (IL1RL1). Два эти термина используются в настоящем описании взаимозаменяемо.
Последовательность мРНК более короткой растворимой изоформы ST2 человека может быть найдена в GenBank Acc. No. NM_003856.2 (SEQ ID NO: 2), и полипептидная последовательность находится в GenBank Acc. No. NP_003847.2 (SEQ ID NO: 1). Последовательность мРНК более длинной формы ST2 человека находится в GenBank Acc. No. NM_016232.4 (SEQ ID NO: 4), и полипептидная последовательность находится в GenBank Acc. No. NP_057316.3 (SEQ ID NO: 3). Дополнительная информация имеется в распоряжении в общедоступных базах данных в GeneID: 9173, MIM ID # 601203 и UniGene No. Hs.66. В целом в описанных в настоящем документе способах измеряется растворимая полипептидная форма ST2 человека.
Антитела и антигенсвязывающие фрагменты антител
В настоящем описании предлагаются выделенные антитела и их антигенсвязывающие фрагменты, которые связываются с растворимым ST2 человека. Предлагаемые антитела и их фрагменты могут связываться, конкурируя с антителом, продуцируемым гибридомой, депонированной в ATCC и обозначенной патентным депозитным номером PTA-10431 или PTA-10432 (что соответствует продуцируемым антителам 7E4 и 9F8, соответственно). В некоторых вариантах осуществления антитело или фрагмент связывается, не конкурируя с антителами D066-3 и D067-3 (MBL International) (описанными в патенте США № 7087396), и обладают KD связывания с растворимым ST2 человека, равной или меньшей 1,51×10-9 M. В некоторых вариантах осуществления антитело или фрагмент обладают KD связывания с растворимым ST2 человека, равной или меньшей 8,59×10-10 M. Методы определения сродства (KD) связывания антитела или фрагмента с растворимым ST2 человека описаны в настоящем документе (например, поверхностный плазмонный резонанс) и дополнительные методы известны в данной области техники. Предлагаются также моноклональные антитела 7E4 и 9F8, продуцируемые с помощью способов, описанных в настоящем документе, и их антигенсвязывающие фрагменты.
Как используется в настоящем описании, выражение «связываться, конкурируя» относится к положению, в результате которого связывание одного антитела или фрагмента антитела с данным антигеном снижает связывание второго антитела или фрагмента антитела с тем же самым антигеном. В некоторых вариантах осуществления антитело или фрагмент связывается, конкурируя с другим антителом или фрагментом, когда два антитела или фрагмента связываются по существу с одним и тем же эпитопом, присутствующим на данном антигене (например, на растворимом ST2 человека). Как более подробно представлено в примерах ниже, каждое из антител, продуцируемых гибридомами, обозначенными патентными депозитными номерами PTA-10431 и PTA-10432, распознает эпитоп, который отличен от эпитопов, распознаваемых различными другими антителами, подвергаемыми тестированию (например, антителами D066-3 и D067-3 от MBL International) и таким образом связывается, не конкурируя с этими тестируемыми антителами. В некоторых вариантах осуществления антитело или фрагмент, описанные в настоящем документе, связываются с эпитопом на растворимом ST2 человека, который распознается антителом, продуцируемым гибридомой, обозначенной патентным депозитным номером PTA-10431 или PTA-10432. Методы определения того, будут ли два различных антитела или фрагмента связываться конкурентно, описаны в настоящем документе и известны в данной области техники (например, конкурентный твердофазный иммуноферментный анализ).
В некоторых вариантах осуществления антитела или фрагменты связываются или проявляют улучшенное связывание с эпитопом, присутствующим в рекомбинантном растворимом белке ST2 человека, продуцируемом клеткой человека (например, фибробластом человека, эпителиальной, эндотелиальной или нервной клеткой, эмбриональной клеткой или клеткой взрослого человека, или клеткой эмбриональной почки человека, например, HEK293), который не присутствует в рекомбинантном растворимом ST2 человека, продуцируемом в типе клеток, происходящих не от человека. В некоторых вариантах осуществления антитела или фрагменты связываются или проявляют улучшенное связывание с эпитопом, присутствующим в полностью гликозилированном растворимом белке ST2 человека (например, в растворимом белке ST2 человека, выделенном из клеток человека), который не присутствует в рекомбинантном растворимом белке ST2 человека, который не гликозилирован или недостаточно или не совсем гликозилирован (например, не полностью гликозилирован или который имеет характер гликозилирования (например, количество, положение и/или тип сахара(ров), не представленные в природном растворимом ST2 человека, имеющемся у человека, например, в сыворотке человека). В некоторых вариантах осуществления антитела и фрагменты антител связываются с природным растворимым ST2 человека лучше (например, с повышенным сродством) других имеющихся в продаже антител.
В некоторых вариантах осуществления антитело представляет собой моноклональное антитело, продуцируемое гибридомой, депонированной в ATCC и обозначенной патентным депозитным номером PTA-10431 (антитело 7E4), или представляет собой антигенсвязывающий фрагмент антитела, продуцируемого гибридомой, депонированной в ATCC и обозначенной патентным депозитным номером PTA-10431 (фрагменты антитела 7E4). В некоторых вариантах осуществления антитело представляет собой моноклональное антитело, продуцируемое гибридомой, депонированной в ATCC и обозначенной патентным депозитным номером PTA-10432 (антитело 9F8), или представляет собой антигенсвязывающий фрагмент антитела, продуцируемого гибридомой, депонированной в ATCC и обозначенной патентным депозитным номером PTA-10432 (фрагменты антитела 9F8). Сочетания двух или более антител или фрагментов, описанных в настоящем документе (например, двух или более из антитела 7E4, фрагментов антитела 7E4, антитела 9F8 и фрагментов антитела 9F8), пригодны в любом из способов, описанных в настоящем документе.
Моноклональные антитела, связывающие растворимый ST2 человека, продуцируются гибридомами, обозначенными патентными депозитными номерами PTA-10431 и PTA-10432, каждое создается в результате иммунизации млекопитающего, не являющегося человеком, рекомбинантным растворимым ST2 человека, выделенным из клеток эмбриональной почки человека (HEK)-293. Растворимый ST2 имеет существенное количество/число посттрансляционных модификаций. Растворимый ST2 человека имеет предсказываемую на основе своей аминокислотной последовательности молекулярную массу приблизительно 36 кДа. Однако природный белок имеет молекулярную массу приблизительно 58 кДа из-за присутствия посттрансляционных модификаций. Как известно в данной области техники, такие посттрансляционные модификации могут оказывать влияние на способность антитела или фрагмента антитела связываться с данным белком. Таким образом, как более подробно описано в разделе примеров ниже, моноклональные антитела, связывающие растворимый ST2 человека, продуцируемые гибридомой, обозначенной патентным депозитным номером PTA-10431, имеют более высокое сродство к природному растворимому ST2 человека, чем другие антитела и, следовательно, пригодны как диагностические и другие реагенты.
В некоторых вариантах осуществления антитело или фрагмент, описанные в настоящем документе, включает тяжелую и/или легкую цепь (или их фрагмент) антитела, продуцируемого гибридомой, обозначенной патентным депозитным номером PTA-10431 и/или PTA-10432. В некоторых вариантах осуществления антитело или фрагмент, описанные в настоящем документе, включает вариабельную область тяжелой и/или легкой цепи (или ее фрагмент) антитела, продуцируемого гибридомой, обозначенной патентным депозитным номером PTA-10431 и/или PTA-10432.
Как известно в данной области техники, специфичность антитела в отношении данного антигена определяется вариабельными областями тяжелой и легкой цепей. В частности, специфичность антитела в отношении данного антигена, в первую очередь, определяется короткими последовательностями в пределах вариабельных областей тяжелой и легкой цепей, называемыми областями, определяющими комплементарность, или CDR. В некоторых вариантах осуществления антитело или фрагмент, описанное в настоящем документе, содержит одну или более (например, одну, две, три, четыре, пять или шесть) CDR легкой и/или тяжелой цепи антитела, продуцируемого гибридомой, обозначенной патентным депозитным номером PTA-10431 и/или PTA-10432. В некоторых вариантах осуществления антитело или фрагмент, описанное в настоящем документе, включает каждую из CDR тяжелой цепи антитела, продуцируемого гибридомой, обозначенной патентным депозитным номером PTA-10431 или PTA-10432. В некоторых вариантах осуществления антитело или фрагмент, описанное в настоящем документе, включает каждую из CDR легкой цепи антитела, продуцируемого гибридомой, обозначенной патентным депозитным номером PTA-10431 или PTA-10432. В некоторых вариантах осуществления антитело или фрагмент, описанное в настоящем документе, включает каждую из CDR (все CDR тяжелой и легкой цепей) антитела, продуцируемого гибридомой, обозначенной патентным депозитным номером PTA-10431 или PTA-10432.
Предлагаются также выделенные антитела и антигенсвязывающие фрагменты антител, которые специфически связываются с растворимым ST2 человека, продуцируемые с помощью метода, который включает иммунизацию млекопитающего, не являющегося человеком, рекомбинантным растворимым ST2 человека, выделенным из клетки почки (например, клетки почки человека, клетки эмбриональной почки и клетки эмбриональной почки человека). В некоторых вариантах осуществления рекомбинантный растворимый ST2 человека полностью гликозилирован или содержит все посттрансляционные модификации, присутствующие в природном растворимом белке ST2.
В некоторых вариантах осуществления антитело или фрагмент, описанные в настоящем документе, являются гибридными в том смысле, что они включают по меньшей мере одну константную область человека. Например, константные области антител, продуцируемых гибридомой, обозначенной патентным депозитным номером PTA-10431 или PTA-10432, могут быть заменены константной областью человека. Гибридные антитела обычно менее иммуногены для людей по сравнению с негибридными антителами и, следовательно, предоставляют терапевтические преимущества в определенных ситуациях. В некоторых вариантах осуществления гибридное антитело, описанное в настоящем документе, включает константную область IgG1. Специалисты в данной области техники должны быть осведомлены о разнообразии константных областей человека. Методы создания гибридных антител известны в данной области техники.
В некоторых вариантах осуществления антитело или фрагмент, описанные в настоящем документе, являются гуманизированными в том смысле, что они включают по меньшей мере одну каркасную область, происходящую от человека. Например, одна или более (например, одна, две, три, четыре, пять или шесть) каркасных областей антител, продуцируемых гибридомой, обозначенной патентным депозитным номером PTA-10431 или PTA-10432, могут быть заменены одной или более (например, одной, двумя, тремя, четырьмя, пятью или шестью) каркасными областями, происходящими от человека. Гуманизированные антитела обычно менее иммуногены для людей по сравнению с негуманизированными антителами и, следовательно, предоставляют терапевтические преимущества в определенных ситуациях. Специалисты в данной области техники должны быть осведомлены о разнообразии каркасных областей, происходящих от человека. Методы создания гуманизированных антител известны в данной области техники.
Например, для гуманизации могут быть использованы методы, основанные на гомологии CDR (см., например, Hwang et al., Methods 36:35, 2005). Эти методы обычно включают подстановку CDR, происходящих не от человека, в вариабельный домен каркаса, происходящего от человека, основываясь на структурном сходстве CDR, происходящих не от человека и от человека, а не на структурном сходстве каркасов, происходящих не от человека и от человека. Сходство CDR, происходящих не от человека и от человека, обычно определяют путем идентификации генов того же самого типа цепи (тяжелой или легкой), происходящей от человека, которые имеют то же самое сочетание канонических структур CDR, что и связывающие молекулы, происходящие не от человека (например, от мыши), и таким образом сохраняют трехмерную конформацию каркасов пептидов CDR. Во-вторых, для каждого из кандидатных вариабельных генов с подогнанными каноническими структурами оценивают гомологию остатков между CDR, происходящей не от человека, и кандидатными CDR, происходящими от человека. Наконец, для создания гуманизированной связывающей молекулы остатки CDR выбранной кандидатной CDR, происходящей от человека, уже не идентичные CDR, происходящей не от человека, преобразуют в последовательность, происходящую не от человека (например, от мыши). В некоторых вариантах осуществления в гуманизированную связывающую молекулу не вводят мутаций в каркас, происходящий от человека.
В некоторых вариантах осуществления подстановка CDR, происходящих не от человека, в вариабельный домен каркаса, происходящего от человека, основывается на сохранении корректной пространственной ориентации вариабельного домена каркаса, происходящего не от человека, путем идентификации вариабельных доменов каркасов, происходящих от человека, которые должны сохранять ту же самую конфигурацию, что и вариабельные домены каркасов, происходящих не от человека, из которых произошли CDR. В некоторых вариантах осуществления это достигается путем получения вариабельных доменов, происходящих от человека, из связывающих молекул, происходящих от человека, чьи последовательности каркасов проявляют высокую степень идентичности последовательности с вариабельными доменами каркасов, происходящих не от человека, из которых произошли CDR. См., например, Kettleborough et al., Protein Engineering 4:773, 1991; Kolbinger et al., Protein Engineering 6:971 , 1993; и патент WO 92/22653.
В некоторых вариантах осуществления антитело или фрагмент, описанные в настоящем документе, являются моноспецифичными в том смысле, что они распознают только один эпитоп. Моноспецифичные антитела известны в данной области техники (см., например, патент WO/9639858). В некоторых вариантах осуществления антитело или фрагмент, описанные в настоящем документе, являются биспецифичными в том смысле, что они распознают более одного эпитопа (например, два эпитопа). Биспецифичные антитела известны в данной области техники (см., например, публикацию патентной заявки США № 2009/0162360). В некоторых вариантах осуществления моноспецифичные или биспецифичные антитела или фрагменты, описанные в настоящем документе, связывают эпитоп, распознаваемый антителом или фрагментом антитела, обладающим CDR моноклонального антитела, продуцируемого гибридомой, обозначенной патентным депозитным номером PTA-10431 или PTA-10432. В некоторых вариантах осуществления биспецифичное антитело или фрагмент связывают растворимый ST2 человека, а также отличный полипептид, не являющийся ST2. В некоторых вариантах осуществления биспецифичное антитело или фрагмент связывают два различных эпитопа растворимого ST2 человека. В некоторых вариантах осуществления антитело или фрагмент, описанные в настоящем документе, являются двухвалентными (см., например, патент WO/1999/064460). Для дополнительного описания других типов антител и фрагментов, которые могут включать одну или более CDR моноклональных антител, продуцируемых гибридомами, обозначенными патентным депозитным номером PTA-10431 или PTA-10432, см. публикацию патентной заявки США № 20070105199 и патент WO/2007/059782.
В некоторых вариантах осуществления фрагмент (например, антигенсвязывающий фрагмент) происходит от полной молекулы антитела, например, моноклонального антитела. Антитело может быть, например, расщеплено на карбоксиконцевом участке его шарнирной области (например, пепсином) с созданием F(ab’)2 фрагмента или на аминоконцевом участке его шарнирной области (например, папаином) с созданием Fab фрагментов. В некоторых вариантах осуществления антигенсвязывающий фрагмент, описанный в настоящем документе, представляет собой Fab фрагмент, F(ab’)2 фрагмент, scFv фрагмент, линейное антитело, фрагмент мультиспецифичного антитела, такого как биспецифичное, триспецифичное или мультиспецифичное антитело (например, диатело, триатело или тетратело), минитело, хелатное рекомбинантное антитело, интратело, нанотело, малую модуляторную иммунофармацевтическую частицу (SMIP), слитый белок связывающих доменов иммуноглобулинов, антитело верблюдовых или антитело, содержащее VHH. Методы получения этих фрагментов известны в данной области техники.
В некоторых вариантах осуществления антитело, связывающее растворимый ST2 человека, или антигенсвязывающий фрагмент антитела, описанные в настоящем документе, содержат полипептид, имеющий одну или более аминокислотных замен, делеций или вставок по сравнению с тяжелой и/или легкой цепью антитела, продуцируемого гибридомой, обозначенной патентным депозитным номером PTA-10431 или PTA-10432. Замены, делеции или вставки могут быть введены стандартными способами, такими как сайт-направленный мутагенез или ПЦР-опосредованный мутагенез молекулы нуклеиновой кислоты, кодирующей полипептид, включающий тяжелую и/или легкую цепь антитела, продуцируемого гибридомой, обозначенной патентным депозитным номером PTA-10431 или PTA-10432 (например, нуклеиновой кислоты, кодирующей одну или более (например, одну, две или три) области CDR тяжелой или легкой цепи). В некоторых вариантах осуществления делают консервативные аминокислотные замены в одном или более положений. «Консервативная аминокислотная замена» представляет собой замену, при которой аминокислотный остаток заменяют аминокислотным остатком, имеющим сходную боковую цепь. Семейства аминокислотных остатков, имеющих сходные боковые цепи, описаны в данной области техники, включая основные боковые цепи (например, лизин, аргинин, гистидин), кислые боковые цепи (например, аспарагиновая кислота, глутаминовая кислота), незаряженные полярные боковые цепи (например, глицин, аспарагин, глутамин, серин, треонин, тирозин, цистеин), неполярные боковые цепи (например, аланин, валин, лейцин, изолейцин, пролин, фенилаланин, метионин, триптофан), бета-разветвленные боковые цепи (например, треонин, валин, изолейцин) и ароматические боковые цепи (например, тирозин, фенилаланин, триптофан; гистидин). Таким образом, аминокислотный остаток в полипептидном антителе против растворимого ST2 человека или во фрагменте антитела, связывающем растворимый ST2 человека, может быть заменен другим аминокислотным остатком, включающим боковые цепи из того же самого семейства.
В некоторых вариантах осуществления антитело, связывающее растворимый ST2 человека, или фрагмент антитела, связывающий растворимый ST2 человека, описанные в настоящем документе, включают аминокислотную последовательность, которая по меньшей мере на 90% идентична, по меньшей мере на 95%, 96%, 97%, 98%, 99% или 100% идентична тяжелой и/или легкой цепи антитела, продуцируемого гибридомой, обозначенной патентным депозитным номером PTA-10431 или PTA-10432 (например или по меньшей мере, на 90%, 95%, 96%, 97%, 98%, 99% или 100% идентична по меньшей мере одной (например, одной, двум или трем) CDR тяжелой или легкой цепи антитела, продуцируемого гибридомой, обозначенной патентным депозитным номером PTA-10431 или PTA-10432). Например, антитело, связывающее растворимый ST2 человека, или фрагмент антитела, связывающий растворимый ST2 человека, описанные в настоящем документе, могут содержать одну или более CDR, которые содержат одну или более аминокислотных замен, делеций или вставок в соответствующей последовательности CDR, найденной в тяжелой или легкой цепи антитела, продуцируемого гибридомой, обозначенной патентным депозитным номером PTA-10431 или PTA-10432.
В некоторых вариантах осуществления композиции, описанные в настоящем документе, содержат два или более различных антител, связывающих растворимый ST2 человека, или фрагментов антитела, связывающих растворимый ST2 человека, описанных в настоящем документе. Например, композиция, описанная в настоящем документе, может содержать антитела, продуцируемые гибридомами, обозначенными патентными депозитными номерами PTA-10431 и PTA-10432. Как описано более подробно в разделе примеров ниже, такое сочетание антител проявляет повышенное сродство к антигену ST2 по сравнению с любым антителом поодиночке и по сравнению с другими имеющимися в продаже антителами. Такие композиции, содержащие антитела или антигенсвязывающие фрагменты, описанные в настоящем документе, должны быть пригодны для разнообразных методов, например, диагностических методов. В некоторых вариантах осуществления композиции, описанные в настоящем документе, содержат два или более различных фрагментов, связывающих ST2 (например, Fab фрагментов, F(ab)2 фрагментов или scFv фрагментов), таких как фрагменты, происходящие от антител, продуцируемых гибридомами, обозначенными патентными депозитными номерами PTA-10431 или PTA-10432.
В любом из указанных выше методов антитело или фрагмент антитела может быть гликозилирован или помечен. Например, антитела и фрагменты антител могут быть помечены определяемым веществом, включая, но, не ограничиваясь этим, различные ферменты, простетические группы, флуоресцентные вещества, люминесцентные вещества, биолюминесцентные вещества и радиоактивные вещества. Примеры подходящих ферментов включают пероксидазу хрена, щелочную фосфатазу, β-галактозидазу или ацетилхолинэстеразу; примеры подходящих простетических групп включают стрептавидин/биотин и авидин/биотин; примеры подходящих флуоресцентных веществ включают умбеллиферон, флуоресцеин, флуоресцеина изотиоционат, родамин, дихлортриазиниламинфлуоресцеин, данзилхлорид, квантовые точки или фикоэритрин; пример люминесцентного вещества включает люминол; примеры биолюминесцентных веществ включают люциферазу, люциферин и экворин, и примеры подходящего радиоактивного вещества включают 125I, 131I, 35S или 3H.
Гибридомы
В настоящем описании предлагаются также новые гибридомы, которые продуцируют антитела, связывающие растворимый ST2 человека. Как известно в данной области техники, термин «гибридома» относится к клетке, которая создана путем слияния продуцирующего антитело лимфоцита и не продуцирующей антитело раковой клетки, обычно клетки миеломы или лимфомы. После слияния гибридомы пролиферируют и продуцируют специфичное моноклональное антитело, которое исходно продуцировалось лимфоцитом, используемым для слияния. В некоторых вариантах осуществления предлагаемая гибридома представляет собой гибридому, депонированную в ATCC и обозначенную патентным депозитным номером PTA-10431 или PTA-10432. В некоторых вариантах осуществления предлагаются также индивидуальные клетки, собранные клетки и культуры, содержащие клетки, которые происходят из гибридомы, депонированной в ATCC и обозначенной патентным депозитным номером PTA-10431 или PTA-10432.
Способы применения предлагаемых антител и фрагментов
Одно или более из любых антител или фрагментов антител, описанных в настоящем документе, может быть использовано в способах количественного определения уровня растворимого ST2 человека в образце, например, в образце, взятом у индивидуума, особенно для прогнозирования риска смерти в течение года, для определения того, надо ли выписывать или следует начинать или продолжать лечение индивидуума на базе стационара, для отбора индивидуума для участия в клиническом исследовании, для диагностики заболевания у индивидуума или для идентификации индивидуума с риском развития заболевания.
Способы количественного определения уровня растворимого ST2 человека
В настоящем описании предлагаются способы определения уровня растворимого ST2 человека в образце, взятом у индивидуума, включающие приведение образца в контакт по меньшей мере с одним антителом или фрагментом антитела, описанными в настоящем документе; и определение связывания антитела или фрагмента антитела с растворимым ST2 человека. В некоторых вариантах осуществления по меньшей мере два (например, два, три или четыре) антитела или фрагмента антитела, описанные в настоящем документе, используются для определения уровня растворимого ST2 человека в образце, взятом у индивидуума. В некоторых вариантах осуществления индивидуум не имеет диагноза болезни или у него отсутствует один или более (например, два, три или четыре) симптомов заболевания. В некоторых вариантах осуществления у индивидуума диагностировано заболевание, связанное с повышенными уровнями ST2 (например, сердечная недостаточность, заболевание коронарных артерий, сердечно-сосудистое заболевание, острый коронарный синдром, почечная недостаточность, инсульт или любое другое из описанных в настоящем документе заболеваний). В некоторых вариантах осуществления у индивидуума выявлено одно или более (например, два, три или четыре) из: гипертриглицеридемии, гиперхолестеринемии, гипертензии, почечной недостаточности и индекса массы тела ≥30. В некоторых вариантах осуществления образец содержит кровь, сыворотку или плазму.
В некоторых вариантах осуществления образец может быть взят у индивидуума профессиональным работником здравоохранения (например, специалистом по взятию крови, врачом, сестрой, фельдшером или специалистом лаборатории). Образец можно хранить (например, при ≤4°С, ≤0°С или -80°С) в течение периода времени до приведения образца в контакт по меньшей мере с одним антителом или фрагментом, описанными в настоящем документе, и определения связывания антитела или фрагмента. Методы приведения в контакт биологического образца с антителом или фрагментом антитела и определения связывания антитела или фрагмента описаны в настоящем документе, и дополнительные методы известны в данной области техники. Количественное определение также может включать контрольные эксперименты для определения связывания по меньшей мере одного антитела или фрагмента антитела, описанных в настоящем документе, с рекомбинантным очищенным растворимым ST2 человека (например, с рекомбинантным очищенным растворимым ST2 человека, выделенным из клеток эмбриональной почки человека).
В некоторых вариантах осуществления количественно определяется уровень растворимого ST2 человека у нормального или здорового индивидуума. Нормальный или здоровый индивидуум представляет собой индивидуума, который не страдает заболеванием, связанным с ST2 (например, заболеванием, связанным с ST2, описанным в настоящем документе), у него не диагностировано заболевание (например, любое из заболеваний, описанных в настоящем документе) и у него не представлено два или более (например, два, три или четыре) симптома заболевания. Состояние нормального или здорового индивидуума может быть подтверждено любым из разнообразных методов, известных в данной области техники, включая без ограничения скрининг биомаркеров или физикальное обследование (например, внешней манифестации отсутствия двух или более симптомов, связанных с состоянием, ассоциированном с ST2, или с любым другим заболеванием, описанным в настоящем документе). Например, может быть проведен скрининг нормальных или здоровых индивидуумов на отсутствие скрытого CVD или воспалительного заболевания с помощью скрининга на низкие уровни одного или более маркеров, включая, но, не ограничиваясь этим, мозговой натрийуретический пептид (BNP), прокальцитонин (PCT), С-реактивный белок (CRP) и интерлейкин-6 (IL-6). Специалисты в данной области техники должны быть осведомлены о других подходящих маркерах для определения того, что у нормального или здорового индивидуума не выявлено скрытое CVD или воспалительное заболевание или любое из других заболеваний, описанных в настоящем документе.
Количественная оценка уровней растворимого ST2 человека в образце, взятом у индивидуума (например, нормального или здорового индивидуума), полезна в различных случаях. В некоторых вариантах осуществления уровни растворимого ST2 человека у индивидуумов (например, у нормальных или здоровых индивидуумов, индивидуумов, имеющих повышенный риск развития заболевания, индивидуумов, у которых диагностировано заболевание, или индивидуумов с проявлением двух или более симптомов заболевания) могут быть количественно определены в периодические интервалы, например, ежедневно, еженедельно, раз в две недели, ежемесячно, раз в два месяца, ежегодно и т.д. или при периодическом физикальном обследовании. Любой из различных методов, известных специалистам в данной области техники, включая описанные в настоящем документе, может быть использован для количественного определения уровней растворимого ST2 человека у индивидуума с использованием антител и антигенсвязывающих фрагментов антител, описанных в настоящем документе.
В некоторых вариантах осуществления уровень растворимого ST2 человека у контрольного индивидуума (например, у нормального или здорового индивидуума) количественно определяется как достигший реперного уровня для использования при определении того, что у индивидуума нет заболевания, связанного с ST2, того что он находится в состоянии риска развития заболевания или риска смерти в течение одного года. Например, уровни растворимого ST2 человека у индивидуума, который не страдает заболеванием, таким как, без ограничения, сердечно-сосудистое заболевание, сердечная недостаточность, заболевание коронарных артерий, острый коронарный синдром, почечная недостаточность, инсульт, легочное заболевание, сепсис, болезнь Кавасаки или заболевание, связанное с Th2, или любое другое заболевание, описанное в настоящем документе, могут быть количественно определены как достигшие реперного уровня растворимого ST2 человека.
В некоторых вариантах осуществления по меньшей мере одно из любых антител или антигенсвязывающих фрагментов, раскрытых в настоящем описании, может быть использовано для количественной оценки уровней растворимого ST2 человека у индивидуума (например, нормального или здорового индивидуума). Например, уровни растворимого ST2 человека у индивидуума (например, нормального или здорового индивидуума) могут быть количественно определены с помощью иммуноанализов с использованием по меньшей мере одного из любых антител или антигенсвязывающих фрагментов, раскрытых в настоящем описании (например, антитела или фрагмента, которые связываются, конкурируя с антителом, продуцируемым гибридомой, депонированной в ATCC и обозначенной патентным депозитным номером PTA-10431 или PTA-10432, или обеими).
В некоторых вариантах осуществления уровень растворимого ST2 человека в образце количественно определяется для гарантии воспроизводимости стандартного выполнения, определения диапазонов реперных интервалов, клинических ограничений и тому подобного. Например, могут быть количественно определены уровни растворимого ST2 человека в двух или более образцах, например, реперных образцах, и может быть оценен коэффициент вариации («CV») между уровнями растворимого ST2 человека в двух или более образцах. Дополнительно или альтернативно, уровень растворимого ST2 человека в образце (или у индивидуума) может быть количественно определен два или более раз отдельно (например, с использованием различных партий реперного образца или различных образцов, полученных от одного и того же индивидуума), и может быть определен CV между уровнями растворимого ST2 человека. В некоторых вариантах осуществления CV между уровнями растворимого ST2 человека составляет менее 20%, например, менее 19%, 18%, 17%, 16%, 15%, 14%, 13%, 12%, 11%, 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2%, 1% или менее.
В некоторых вариантах осуществления предлагаются способы определения того, имеет ли индивидуум нормальный уровень растворимого ST2 человека. Определение того, имеет ли индивидуум нормальный уровень растворимого ST2 человека, пригодно в различных случаях. В некоторых вариантах осуществления способы определения того, имеет ли индивидуум нормальный уровень растворимого ST2 человека, включают оценку уровня растворимого ST2 человека в образце, взятом у индивидуума (например, в любом из образцов, описанных выше, таких как, без ограничения, образцы, содержащие кровь, сыворотку или плазму), где индивидуум характеризуется как имеющий нормальный уровень растворимого ST2 человека, если уровень растворимого ST2 человека в образце, как обнаруживается, является по существу сходным с известным нормальным уровнем или медианой уровня растворимого ST2 человека, или если уровень растворимого ST2 человека в образце попадает в определенный диапазон, например, вокруг известного нормального уровня или медианы уровня растворимого ST2 человека (например, в 95% доверительный интервал или межквартильный диапазон или в любой из диапазонов, перечисленных в таблице 9). Например, индивидуум может характеризоваться как имеющий нормальный уровень растворимого ST2 человека, если исследуется образец, взятый у индивидуума, и уровень растворимого ST2 человека в образце, как обнаруживается, находится в пределах 95% доверительного интервала вокруг известного нормального уровня или медианы уровня растворимого ST2 человека, например, медианы уровня у нормального или здорового индивидуума. Дополнительно или альтернативно индивидуум может быть охарактеризован как имеющий нормальный уровень растворимого ST2 человека, если оценивается образец, взятый у индивидуума, и уровень растворимого ST2 человека в образце, как обнаруживается, находится в пределах межквартильного размаха вокруг известного нормального уровня или медианы уровня растворимого ST2 человека.
В некоторых вариантах осуществления индивидуум характеризуется как имеющий нормальный уровень растворимого ST2 человека, если уровень растворимого ST2 человека в образце, взятом у индивидуума составляет приблизительно 18,8 нг/мл. В некоторых вариантах осуществления индивидуум характеризуется как имеющий нормальный уровень растворимого ST2 человека, если уровень растворимого ST2 человека в образце находится в пределах диапазона от приблизительно 14,5 до приблизительно 25,3 нг/мл. В некоторых вариантах осуществления индивидуум характеризуется как имеющий нормальный уровень растворимого ST2 человека, если уровень растворимого ST2 человека в образце находится в пределах диапазона от приблизительно 18,1 до приблизительно 19,9 нг/мл.
В некоторых вариантах осуществления индивидуум женского пола характеризуется как имеющий нормальный уровень растворимого ST2 человека, если уровень растворимого ST2 человека в образце, взятом у индивидуума, составляет приблизительно 16,2 нг/мл. В некоторых вариантах осуществления женщина характеризуется как имеющая нормальный уровень растворимого ST2 человека, если уровень растворимого ST2 человека в образце находится в пределах любого из диапазонов, представленных в таблице 9.
В некоторых вариантах осуществления индивидуум мужского пола характеризуется как имеющий нормальный уровень растворимого ST2 человека, если уровень растворимого ST2 человека в образце, взятом у индивидуума, составляет приблизительно 23,6 нг/мл. В некоторых вариантах осуществления мужчина характеризуется как имеющий нормальный уровень растворимого ST2 человека, если уровень растворимого ST2 человека в образце находится в пределах любого из диапазонов, представленных в таблице 9.
В некоторых вариантах осуществления индивидуум (например, индивидуум мужского или женского пола) характеризуется как имеющий нормальный уровень растворимого ST2 человека, если уровень растворимого ST2 человека в образце, взятом у индивидуума, находится ниже порогового (например, 25,3 нг/мл, или 19,9 нг/мл (для женщин), 30,6 нг/мл для мужчин)).
Термин «приблизительно» или «по существу такие же» при применении в отношении величины или диапазона уровней растворимого ST2 человека (например, диапазона нормальных уровней растворимого ST2 человека) у индивидуума относится к интервалу вокруг реперной величины или диапазона, например, величины или диапазона, который специалист в данной области техники должен рассматривать как эквивалентный реперной величине или диапазону (например, любому из диапазонов, представленных в таблице 9), с целью оценки уровней растворимого ST2 человека (например, нормальных уровней растворимого ST2 человека или уровней растворимого ST2 человека в группе больных, имеющих заболевание или имеющих два или более симптомов заболевания). Как используется в настоящем описании, уровни величины или диапазона растворимого ST2 человека (например, нормальные уровни растворимого ST2 человека) составляют «приблизительно» реперную величину или диапазон, когда они находятся в пределах ±25% от реперной величины или диапазона, например, ±20%, ±15%, ±10%, ±9%, ±8%, ±7%, ±6%, ±5%, ±4%, ±3%, ±2% или ±1% от реперной величины или диапазона.
В некоторых вариантах осуществления по меньшей мере одно или два из любых антител или антигенсвязывающих фрагментов, описанных в настоящем документе, могут быть использованы для определения того, имеет ли индивидуум нормальный уровень растворимого ST2 человека, уровень растворимого ST2 человека, который коррелирует с заболеванием, или уровень растворимого ST2 человека, который коррелирует с повышенным риском развития заболевания или повышенным риском смерти в течение года.
Методы прогнозирования риска смерти в течение одного года
Предлагаются также методы прогнозирования риска смерти индивидуума в течение одного года, которые включают взятие образца у индивидуума и определение уровня растворимого ST2 человека с использованием по меньшей мере одного антитела или фрагмента антитела, описанного в настоящем описании. Повышенный уровень или по существу такой же уровень растворимого ST2 человека в образце относительно реперного уровня растворимого ST2 человека указывает на то, что индивидуум имеет повышенный риск смерти в течение одного года (например, повышенный риск смерти в течение одного года по сравнению с индивидуумами (например, индивидуумами, у которых имеется или диагностировано такое же заболевание), имеющими пониженный уровень растворимого ST2 человека в образце относительно того же реперного уровня ST2). Пониженный уровень растворимого ST2 человека в образце относительно реперного уровня растворимого ST2 человека указывает на то, что индивидуум имеет меньший риск смерти в течение одного года (например, меньший риск смерти по сравнению с индивидуумами (например, индивидуумами, у которых имеется или диагностировано такое же заболевание), имеющими повышенный или по существу такой же уровень растворимого ST2 человека в образце относительно реперного уровня растворимого ST2 человека). Степень риска смерти в течение одного года определяется описанными в настоящем описании методами и обычно зависит от стадии заболевания.
В некоторых вариантах осуществления диагностирование индивидуума не производилось, или у индивидуума отсутствует один или более (например, два, три, четыре или пять) симптомов заболевания. В некоторых вариантах осуществления у индивидуума было диагностировано заболевание (например, сердечная недостаточность, заболевание коронарной артерии, сердечно-сосудистое заболевание, синдром острой коронарной недостаточности, почечная недостаточность или инсульт или любое из заболеваний, описанных в настоящем описании). В некоторых вариантах осуществления у индивидуума имеется одно или более (например, одно, два, три или четыре) из: гипертриглицеридемии, гиперхолестеринемии, гипертонии и индекс массы тела ≥30. В некоторых вариантах осуществления определение производят с использованием по меньшей мере одного (например, двух, трех, четырех или пяти) антитела или фрагмента, описанного в настоящем описании.
В некоторых вариантах осуществления реперный уровень растворимого ST2 человека представляет собой пороговый уровень растворимого ST2 человека (например, медианный уровень растворимого ST2 человека или процентиль (например, 75-й, 80-й, 85-й, 90-й или 95-й процентиль или любое количество из диапазонов или концентраций, перечисленных в таблице 9) от медианного уровня растворимого ST2 человека в популяции здоровых людей, например, в популяции здоровых мужчин или в популяции здоровых женщин). В некоторых вариантах осуществления реперный уровень может представлять собой уровень растворимого ST2 человека в образце, взятом у индивидуума, не проявляющего один или более симптомов заболевания, связанного с повышенным уровнем ST2. В некоторых вариантах осуществления реперный уровень может представлять собой уровень растворимого ST2 человека в образце, взятом у индивидуума, у которого не было диагностировано наличие заболевания (например, сердечной недостаточности, заболевания коронарной артерии, сердечно-сосудистого заболевания, синдрома острой коронарной недостаточности, почечной недостаточности, инсульта или любого из заболеваний, описанных в настоящем описании), или у индивидуума, у которого не было выявлено риска развития заболевания (например, любого из заболеваний, описанных в настоящем описании). Специалистами в данной области техники могут быть определены дополнительные реперные уровни.
В некоторых вариантах осуществления реперный уровень растворимого ST2 человека находится в диапазоне от приблизительно 30 нг/мл до приблизительно 35 нг/мл. В некоторых вариантах осуществления, когда у индивидуума имеется сердечная недостаточность, реперный уровень растворимого ST2 человека находится в диапазоне от приблизительно 30 нг/мл до приблизительно 35 нг/мл. В некоторых вариантах осуществления реперный уровень растворимого ST2 человека находится в диапазоне от приблизительно 35 нг/мл до приблизительно 60 нг/мл.
В некоторых вариантах осуществления образец содержит кровь, сыворотку или плазму. Может быть получен образец и может быть произведено определение уровня растворимого ST2 человека с использованием по меньшей мере одного описанного в настоящем описании антитела или фрагмента, как описано в настоящем описании.
Методы определения того, следует ли выписывать индивидуума из стационара или начинать или продолжать его лечение в стационаре
Предлагаются также методы определения того, следует ли выписывать индивидуума из стационара или начинать или продолжать его лечение в стационаре, включающие взятие образца у индивидуума и определение уровня растворимого ST2 человека в образце с использованием по меньшей мере одного (например, двух) описанного в настоящем описании антитела или фрагмента, когда повышенный уровень растворимого ST2 человека в образце по сравнению с реперным уровнем растворимого ST2 человека указывает на то, что следует начать или продолжить лечение индивидуума в стационаре (например, госпитализацию или разрешение на субсидируемую медицинскую помощь), а сниженный или равный уровень растворимого ST2 человека в образце по сравнению с реперным уровнем растворимого ST2 человека в образце указывает на то, что индивидуума следует выписать из стационара. Метод может быть применен к одному и тому же индивидууму несколько раз для определения того, следует ли продолжать лечение в стационаре (например, метод применяют раз в неделю, дважды в неделю, трижды в неделю, раз в месяц, дважды в месяц, трижды в месяц и четырежды в месяц).
В некоторых вариантах осуществления индивидуума не подвергали диагностированию, у него не проявляются два или более симптомов болезненного состояния, или для него не обнаружен риск развития заболевания (например, любого из заболеваний, описанных в настоящем описании). В некоторых вариантах осуществления у индивидуума было диагностировано наличие заболевания (например, сердечной недостаточности, заболевания коронарной артерии, сердечно-сосудистого заболевания, синдрома острой коронарной недостаточности, почечной недостаточности или инсульта или любого из заболеваний, описанных в настоящем описании), у него проявляются один или более симптомов заболевания (например, любого из заболеваний, описанных в настоящем описании), или было обнаружено, что у него имеется риск развития заболевания (например, любого из заболеваний, описанных в настоящем описании). В некоторых вариантах осуществления у индивидуума имеется одно или более (например, одно, два, три или четыре) из: гипертриглицеридемии, гиперхолестеринемии, гипертонии и индекса массы тела ≥30. В некоторых вариантах осуществления у индивидуума не было диагностировано наличие сердечной недостаточности, заболевания коронарной артерии, сердечно-сосудистого заболевания, синдрома острой коронарной недостаточности, почечной недостаточности или инсульта или любого из заболеваний, описанных в настоящем описании. В некоторых вариантах осуществления определение уровня растворимого ST2 человека производят с использованием по меньшей мере двух антител или фрагментов антител, описанных в настоящем описании.
В некоторых вариантах осуществления реперные уровни растворимого ST2 человека могут быть любыми из реперных уровней, описанных в настоящем описании. Специалистами в данной области техники могут быть определены дополнительные реперные уровни. В некоторых вариантах осуществления образец содержит кровь, сыворотку или плазму. Может быть получен образец и может быть произведено определение уровня растворимого ST2 человека с использованием по меньшей мере одного описанного в настоящем описании антитела или фрагмента, как описано в настоящем описании.
Методы отбора индивидуума для участия в клиническом исследовании
Предлагаются также методы отбора индивидуума для участия в клиническом исследовании. Эти методы включают взятие образца у индивидуума, определение уровня растворимого ST2 человека с использованием по меньшей мере одного описанного в настоящем описании антитела или фрагмента и отбор индивидуума для участия в клиническом исследовании в случае, если уровень растворимого ST2 человека у индивидуума относительно реперного уровня растворимого ST2 человека указывает на то, что индивидуума следует отобрать для участия в клиническом исследовании. В некоторых вариантах осуществления наличие повышенного уровня растворимого ST2 человека указывает на то, что индивидуума следует отобрать для участия в клиническом исследовании. В некоторых вариантах осуществления наличие повышенного уровня растворимого ST2 человека указывает на то, что индивидуума следует исключить из клинического исследования.
В некоторых вариантах осуществления индивидуума не подвергали диагностированию, у него не проявляются один или более симптомов заболевания (например, любого из заболеваний, описанных в настоящем описании), или для него не был обнаружен риск развития заболевания (например, любого из заболеваний, описанных в настоящем описании). В некоторых вариантах осуществления у индивидуума было диагностировано наличие заболевания (например, сердечной недостаточности, заболевания коронарной артерии, сердечно-сосудистого заболевания, синдрома острой коронарной недостаточности, почечной недостаточности или инсульта или любого из заболеваний, описанных в настоящем описании), у него проявляются один или более симптомов заболевания (например, любого из заболеваний, описанных в настоящем описании), или было обнаружено, что у него имеется малый риск развития заболевания (например, любого из заболеваний, описанных в настоящем описании). В некоторых вариантах осуществления у индивидуума имеется одно или более (например, одно, два, три или четыре) из: гипертриглицеридемии, гиперхолестеринемии, гипертонии и индекса массы тела ≥30. В некоторых вариантах осуществления определение производят с использованием по меньшей мере двух антител или фрагментов, описанных в настоящем описании.
В некоторых вариантах осуществления реперные уровни растворимого ST2 человека могут быть любыми из реперных уровней, описанных в настоящем описании. Специалистами в данной области техники могут быть определены дополнительные реперные уровни. В некоторых вариантах осуществления образец содержит кровь, сыворотку или плазму. Может быть получен образец и может быть произведено определение уровня растворимого ST2 человека с использованием по меньшей мере одного описанного в настоящем описании антитела или фрагмента, как описано в настоящем описании.
Методы выбора лечения
Предлагаются также методы выбора терапии индивидуума, включающие взятие образца у индивидуума и определение в образце уровня растворимого ST2 человека с использованием по меньшей мере одного из описанных в настоящем описании антител и фрагментов, когда повышенный уровень растворимого ST2 человека в образце относительно реперного уровня растворимого ST2 человека указывает на то, что индивидууму следует предоставить специфическую терапия. Например, специфическое лечение может быть выбрано из группы: нитратов, блокаторов кальциевых каналов, диуретиков, тромболитических средств, дигиталиса, средств, модулирующих систему ренин-ангиотензин-альдостерон (RAAS) (например, бета-адренергических блокаторов (например, альпренолола, буциндолола, картеолола, карведилола, лабеталола, надолола, пенбутолола, пиндолола, пропранолола, соталола, тимолола, цебутолола, атенолола, бетаксолола, бисопролола, целипролола, эсмолола, метопролола и небиволола), ингибиторов ангиотензин-превращающего фермента (например, беназеприла, каптоприла, эналаприла, фозиноприла, лизиноприла, моэксиприла, периндоприла, квинаприла, рамиприла и трандолаприла), антагонистов альдостерона (например, спиронолактона, эплеренона, канренона (канреноата калия), проренона (прореноата калия) и мексренона (мексреноата калия)), ингибиторов ренина (например, алискирена, ремикирена и эналкирена) и блокаторов рецептора ангиотензина II (например, валсартана, телмисартана, лосартана, ирбесартана и олмесартана)) и средств, снижающих холестерин (например, статина). В данной области техники известны также дополнительные способы лечения, например, Braunwald’s Heart Disease: A Textbook of Cardiovascular Medicine, Single Volume, 9th Edition. Специфическое лечение может также заключаться во введении индивидууму по меньшей мере одного или более новых терапевтических средств, в изменении (повышении или снижении) частоты, дозы или продолжительности введения одного или более терапевтических средств индивидууму или в исключении из схемы лечения больного по меньшей мере одного или более терапевтических средств. Лечение также может заключаться в стационарном лечении (например, путем направления или повторного направления больного на госпитализацию (например, в отделение интенсивной терапии или интенсивной терапии и реанимации) или в учреждение, оказывающее субсидируемую медицинскую помощь). В некоторых вариантах осуществления лечение является хирургическим (например, трансплантацией органа или ткани или пластической операцией на сосудах).
В некоторых вариантах осуществления реперные уровни растворимого ST2 человека могут быть любыми из реперных уровней, описанных в настоящем описании. Специалистами в данной области техники могут быть определены дополнительные реперные уровни. В некоторых вариантах осуществления образец содержит кровь, сыворотку или плазму. Может быть получен образец и может быть произведено определение уровня растворимого ST2 человека с использованием по меньшей мере одного описанного в настоящем описании антитела или фрагмента, как описано в настоящем описании.
Методы диагностирования индивидуума
Описанные в настоящем описании методы пригодны в широком диапазоне клинических обстоятельств. Например, такие методы могут быть использованы для скрининга всей популяции, включая скрининг, производимый врачами, например, в больницах и амбулаторных клиниках, а также в службе экстренной медицинской помощи.
В некоторых вариантах осуществления описанные в настоящем описании методы пригодны для определения вероятности наличия заболевания у индивидуума. Повышенные уровни растворимого ST2 человека часто связаны с наличием определенных заболеваний, таких как, без ограничения, сердечно-сосудистые заболевания, легочные заболевания, сепсис, болезнь Кавасаки и связанные с Th2 заболевания и любые из других заболеваний, описанных в настоящем описании.
Связанное с Th2 заболевание представляет собой заболевание, связанное с аномальным ответом хелперных T-клеток типа 2 (Th2). Связанное с Th2 заболевание отличается несколькими факторами, включая, без ограничения, наличие TNF-альфа, IL-4, -5, -6, 10 и -13, но не IFN-гамма (Robinson, J. Allergy Clin. Immunol. 92:313, 1993). CD4+ T-клетки классифицируют в соответствии с цитокинами, которые они секретируют. Th2 клетки секретируют в большом количестве интерлейкин-4 (IL-4), IL-5 и IL-13, которые способствуют продукции антител B-клетками и синтезу коллагена фибробластами, тогда как Th1 клетки секретируют в большом количестве интерферон-γ и связанные с ним провоспалительные цитокины. Цитокины Th1-типа и Th2-типа могут перекрестно регулировать ответы друг друга. Полагают, что нарушение баланса между ответами Th1/Th2 вносит вклад в патогенез различных инфекционных, аллергических и аутоиммунных заболеваний. Определенные иллюстративные связанные с Th2 заболевания включают, без ограничения, системную красную волчанку и астму, а также состояния воспаления, которые преимущественно не зависят от Th2 ответа, такие как септический шок или травма (Trajkovic et al., Cytokine Growth Factor Rev. 15:87-95, 2004; Brunner et al., Intensive Care Med. 30:1468-1473, 2004). Другие иллюстративные связанные с Th2 заболевания включают преэклампсию и рассеянный склероз. В некоторых вариантах осуществления связанное с Th2 заболевание представляет собой аутоиммунное заболевание. Аутоиммунное заболевание обычно возникает тогда, когда иммунная система индивидуума активируется против одного или более компонентов (клеток, тканей или внеклеточных/внетканевых молекул) индивидуума и атакует собственные нормальные органы, ткани или клетки индивидуума. Иллюстративные аутоиммунные заболевания включают, но не ограничиваются этим, устойчивость к адренергическим лекарствам, очаговую алопецию, анкилозирующий спондилоартрит, антифосфолипидный синдром, аутоиммунную болезнь Аддисона, аутоиммунные заболевания надпочечника, аллергический энцефаломиелит, аутоиммунную гемолитическую анемию, аутоиммунный гепатит, аутоиммунное воспалительное заболевание глаза, аутоиммунную неонатальную тромбоцитопению, аутоиммунную нейтропению, аутоиммунный оофорит и орхит, аутоиммунную тромбоцитопению, аутоиммунный тиреоидит, болезнь Бехчета, буллезный пемфигоид, кардиомиопатию, посткардиотомный синдром, брюшные спру-дерматит, хронический активный гепатит, синдром хронической усталости и иммунной дисфункции (CFIDS), хроническую воспалительную демиелинизирующую полиневропатию, синдром Черга-Страуса, рубцовый пемфингоид, синдром CREST, болезнь холодового агглютинина, болезнь Крона, болезнь плотных отложений, заболевания, связанные с эффектами трансплантации органов, дискоидную волчанку, идиопатическую смешанную криоглобулинемию, фибромиалгию-фибромиозит, гломерулонефрит (например, IgA нефропатию), глютензависимую энтеропатию, синдром Гудпасчера, болезнь трансплантат против хозяина (GVHD), болезнь Грейвса (включая тиреоидит Грейвса и офтальмопатию Грейвса), болезнь Гийена-Барре, гипертиреоз (т.е. тиреоидит Хашимото), идиопатический фиброз легкого, идиопатическую болезнь Аддисона, идиопатическую тромбоцитопеническую пурпуру (ITP), IgA нефропатию, синдром резистентности к инсулину, юношеский артрит, красный плоский лишай, красную волчанку, болезнь Меньера, метаболический синдром, смешанное заболевание соединительной ткани, рассеянный склероз, миастению gravis, миокардит, диабет (например, диабет типа I или диабет типа II), неврит, недостаточность других эндокринных желез, обыкновенную пузырчатку, злокачественную анемию, нодозный полиартериит, множественное воспаление хрящей, множественные эндокринопатии, полигландулярные синдромы, ревматическую полимиалгию, полимиозит и дерматомиозит, постинфарктный синдром, первичную агаммаглобулинемию, первичный билиарный цирроз печени, псориаз, псориатичесий артрит, феномен Рейно, рецидивирующее множественное воспаление хрящей, синдром Рейтера, ревматическое заболевание сердца, ревматоидный артрит, саркоидоз, склеродермию, синдром Шегрена, синдром окостенелости, системную красную волчанку, артериит Такаясу, преходящий артериит/гигантоклеточный артериит, язвенный колит, крапивницу, увеит, увеитную офтальмию, васкулиты, такие как дерматитный герпетиформный васкулит, витилиго и грануломатоз Вегенера.
Сердечно-сосудистое заболевание представляет собой повреждение сердца и кровеносных сосудов и включает повреждения артерий, вен, артериол, венул и капилляров. Сердечно-сосудистые заболевания, диагностируемые с помощью метода, описанного в настоящем описании, могут включать, без ограничения, застойную сердечную недостаточность (HF), заболевание коронарной артерии (CAD), аритмию, асимметричную гипертрофию перегородки (например, гипертрофию левого желудочка с возникновением диастолической дисфункции), кардиомиопатию, дисфункцию клапана, перикардит, атеросклероз и острый инфаркт миокарда (MI).
Заболевание легких представляет собой повреждение легких. Заболевания легких, диагностируемые с помощью метода, описанного в настоящем описании, могут включать, без ограничения, хроническую обструктивную болезнь легких (ХОБЛ), астму, пневмонию, пневмоторакс, эмболию сосудов легких, синдром тяжелого респираторного дистресса (ARDS), плевральный выпот, метастазирующую опухоль, отек легкого, гастроэзофагеальную рефлюксную болезнь с эвакуацией, интерстициальный фиброз, пневмокониоз, гранулематозное заболевание, коллагеноз сосудов и рестриктивный легочный процесс.
Если у индивидуума имеется повышенный уровень растворимого ST2 человека, например, по сравнению с реперным контролем, может быть принято решение об интенсивном лечении индивидуума, и индивидуум может быть направлен в больницу для лечения в качестве стационарного больного, например, в больницу (например, в отделение интенсивной терапии и реанимации) или в учреждение, оказывающее субсидируемую медицинскую помощь. Во многих ситуациях желательно определение того, имеется ли у индивидуума заболевание, такое как сердечно-сосудистое заболевание или легочное заболевание, сепсис, болезнь Кавасаки или связанное с Th2 заболевание или любые из заболеваний, описанных в настоящем описании. Например, портативные наборы для тестирования могли бы позволить персоналу скорой помощи произвести оценку индивидуума на месте для определения того, следует ли его доставить в отделение неотложной помощи. Более того, на основании информации, полученной с помощью методов, описанных в настоящем описании, могут быть также приняты решения о сортировке больных, например, направлении в отделение неотложной помощи или другое подразделение клиники. Больным с повышенным уровнем растворимого ST2 человека, может быть уделено большее внимание по сравнению с больными, имеющими более низкий уровень.
В некоторых вариантах осуществления уровень растворимого ST2 человека определяют один раз, например, в момент, когда у индивидуума подозревают наличие заболевания (например, при явке к специалисту-медику или в учреждение здравоохранения). В некоторых вариантах осуществления уровень растворимого ST2 человека определяют один или более раз через 2, 4, 6, 8, 12, 18 и/или 24 часа и/или 1-7 дней или более после момента возникновения подозрения о наличии у индивидуума заболевания (например, при явке к специалисту-медику или в учреждение здравоохранения).
В некоторых вариантах осуществления уровень растворимого ST2 человека определяют более одного раза. В некоторых вариантах осуществления, когда уровень растворимого ST2 человека определяют более одного раза, может быть использован наиболее высокий уровень или может быть определено и использовано изменение уровня. Уровень растворимого ST2 человека может быть также определен многократно для оценки ответа индивидуума на лечение. Например, уровень растворимого ST2 человека, полученный после проведения курса лечения, например, введения одной или более доз или циклов терапии, может быть сопоставлен с уровнем растворимого ST2 человека до начала терапии, например, с базальным уровнем. Изменение уровня растворимого ST2 человека будет указывать на то, было ли лечение эффективным; например, снижение уровня растворимого ST2 человека будет указывать на то, что лечение было эффективным.
В некоторых вариантах осуществления определяют уровень растворимого ST2 человека у индивидуума и сравнивают с реперным уровнем растворимого ST2 человека. Для оценки уровня растворимого ST2 человека у индивидуума может быть использован любой из множества методов, известных специалистам в данной области техники. Иллюстративные методы анализа включают, без ограничения, такие известные в данной области техники методы, как количественная ПЦР или анализ нозерн-блот. В некоторых вариантах осуществления уровень растворимого ST2 человека у индивидуума определяют с помощью иммунологических методов, таких как твердофазный иммуноферментный анализ (ELISA). Например, в некоторых вариантах осуществления описанное в настоящем описании антитело или его антигенсвязывающий фрагмент вводят в контакт с образцом, взятом у индивидуума. Образец может включать или быть полученным из любой из множества клеток или тканей индивидуума. Например, образец может включать одно или более из крови, сыворотки или плазмы. После этого выявляют и необязательно количественно измеряют связывание антитела или фрагмента антитела и определяют уровень белка на основании уровня связывания антитела или фрагмента антитела. В некоторых вариантах осуществления образец практически не содержит форму ST2L белка ST2, так что весь или основная часть ST2 в образце, выявленного методами, раскрытыми в настоящем описании, представляет собой растворимый ST2 человека. В некоторых вариантах осуществления образец не содержит выявляемый ST2L, так что лишь выявляемый ST2 в образце представляет собой растворимый ST2 человека. В некоторых вариантах осуществления образец, по существу не содержащий ST2L или выявляемый ST2L, представляет собой образец сыворотки или крови. В некоторых вариантах осуществления уровень растворимого ST2 человека у индивидуума оценивают иммунологическими методами с использованием по меньшей мере одного антитела или антигенсвязывающего фрагмента, описанного в настоящем описании.
Как более подробно описано в разделе "Примеры" ниже, композиции, включающие антитела, продуцированные гибридомой, депонированной в ATCC и обозначенной патентным депозитным номером PTA-10431, проявляют повышенное сродство к антигену растворимого ST2 человека по сравнению с другими имеющимися в продаже антителами. Такие антитела могут быть использованы в соответствии с методами, описанными в настоящем описании.
Методы, описанные в настоящем описании, пригодны для определения того, что у индивидуума отсутствует состояние, связанное с ST2. Связанное с ST2 состояние представляет собой состояние, которое связано с повышенным уровнем ST2. Определенные иллюстративные связанные с ST2 состояния включают, без ограничения, сердечно-сосудистое заболевание, легочное заболевание, сепсис, болезнь Кавасаки и связанные с Th2 заболевания. Связанные с ST2 состояния обычно являются тяжелыми, и для них часто показана интенсивная терапия. У индивидуумов, проявляющих определенные неспецифические симптомы, может иметься или может отсутствовать связанное с ST2 состояние (например, сердечно-сосудистое заболевание, легочное заболевание, сепсис, болезнь Кавасаки или связанное с Th2 заболевание). Неспецифические симптомы включают, но не ограничиваются этим, боль или дискомфорт в грудной клетке, учащенное дыхание, тошноту, рвоту, отрыжку, потоотделение, учащенное сердцебиение, головокружение, утомляемость и слабость. Каждый из симптомов может иметь различную этиологию.
В некоторых вариантах осуществления описанные в настоящем описании методы пригодны для расслоения риска, например, определения того, что у индивидуума имеется форма связанного с ST2 состояния малой тяжести или с малым риском. Например, у определенных индивидуумов с сердечно-сосудистым заболеванием (например, инфарктом миокарда или сердечной недостаточностью) имеется малый риск неблагоприятного исхода, такого как смерть или повторение сердечного приступа, и также обнаруживается меньшая концентрация растворимого ST2 человека по сравнению с другими индивидуумами, имеющими сердечно-сосудистое заболевание с большим риском неблагоприятного исхода. Такие индивидуумы могут рассматриваться как имеющие форму связанного с ST2 состояния «малой тяжести» или «с малым риском». Однако в обеих популяциях, с высоким и низким риском, наблюдаются более высокие концентрации растворимого ST2 человека, чем у индивидуумов, не имеющих связанного с ST2 состояния. У индивидуумов с формой связанного с ST2 состояния малой тяжести обычно имеются концентрации растворимого ST2 человека, превышающие реперный уровень растворимого ST2 человека (например, медианную концентрацию растворимого ST2 человека у здоровых или нормальных индивидуумов), а у индивидуумов с тяжелой формой связанного с ST2 состояния обычно имеются концентрации растворимого ST2 человека, превышающие 80-й процентиль реперного уровня растворимого ST2 человека (например, концентраций растворимого ST2 человека, наблюдаемых у здоровых или нормальных индивидуумов). Определение того, что у индивидуума, проявляющего определенные неспецифические симптомы, отсутствует связанное с ST2 состояние или имеется форма связанного с ST2 состояния малой тяжести, может обеспечить получение улучшенного диагноза и/или принятие решения о более эффективном лечении, например, о том, что такому индивидууму может не потребоваться интенсивная терапия. Например, у больных с повышенными концентрациями растворимого ST2 человека после острого инфаркта миокарда ремоделирование сердца (усиленный фиброз) было более интенсивным, чем у больных с низкими концентрациями растворимого ST2 человека, и эплеренон дифференцированно подавлял ремоделирование сердца у индивидуумов с высокими концентрациями растворимого ST2 человека (Weir et al., J. Am. Coll. Cardiol. 55:243-250, 2010). Таким образом, концентрации растворимого ST2 человека могут быть использованы для выявления больных, которые должны получать иную, возможно нестандартную, терапию в стационаре или более интенсивную терапию.
Боль в грудной клетке
Боль в грудной клетке является главной жалобой в от 1 до 2 процентах амбулаторных визитов, и, хотя причина боли часто не связана с сердцем, сердечное заболевание остается ведущей причиной смертности в Соединенных Штатах. Поэтому разграничение тяжелых и легких случаев боли в грудной клетке является решающим. Методы, описанные в настоящем описании, пригодны для осуществления такого определения.
У индивидуума, поступившего в отделение неотложной помощи с болью в грудной клетке, может быть боль пищевода, язва, острые проблемы с легкими, такие как легочная эмболия (PE) (потенциально фатальная), разрывная или расслаивающая аневризма аорты (высоколетальная), приступ желчного пузыря, перикардит (воспаление мешка, окружающего сердце), стенокардия (сердечная боль без повреждения) или инфаркт миокарда (потенциально фатальный). Немедленное установление точного диагноза может быть затруднительным, но решение о госпитализации или об интенсивной терапии индивидуума обычно должно приниматься немедленно. Если описанные в настоящем описании методы указывают на то, что у индивидуума имеется повышенный уровень растворимого ST2, например, на наличие связанного с ST2 состояния, может быть принято решение об интенсивной терапии индивидуума, например, для профилактики потенциально неблагоприятного исхода, который мог бы возникнуть в отсутствие лечения. Дополнительную информацию о лечении и диагностике боли в грудной клетке можно найти, например, в Cayley (Am. Fam. Phys. 72(10):2012-2028, 2005).
Одышка
Одышка, или учащенное дыхание (определяемая также как аномальное или стесненное дыхание) является обычным симптомом у индивидуумов, поступающих в отделение неотложной помощи. Дифференциальный диагноз одышки включает четыре общие категории: (1) сердечную, (2) легочную, (3) смешанную сердечную или легочную и (4) несердечную или нелегочную.
Сердечные причины одышки включают правую, левую или двухжелудочковую застойную сердечную недостаточность с возникающими в результате систолической дисфункцией, заболеванием коронарной артерии, недавним или отдаленным инфарктом миокарда, кардиомиопатией, дисфункцией клапана, гипертрофией левого желудочка с возникающей в результате диастолической дисфункцией, асимметричной гипертрофией перегородки, перикардитом и аритмией.
Легочные причины включают обструктивные (например, хроническая обструктивная болезнь легких (ХОБЛ) и астма) и рестриктивные процессы (например, внелегочные причины, такие как ожирение, деформации позвоночника или грудной клетки, и внутрилегочная патология, такая как интерстициальный фиброз, пневмокониоз, грануломатозное заболевание или коллагеновое заболевание сосудов). Смешанные сердечные и легочные нарушения включают ХОБЛ с легочной гипертонией и легочным сердцем, детренированность, легочную эмболию, ARDS и травму. Несердечные или нелегочные нарушения включают такие метаболические состояния, как анемия, диабетический кетоацидоз и другие, менее распространенные причины метаболического ацидоза, боль в стенке груди или в другом месте организма и нервно-мышечные нарушения, такие как рассеянный склероз и мышечная дистрофия. Обструктивные риноларингеальные проблемы включают назальную обструкцию из-за полипов или смещения перегородки, увеличенные миндалевидные железы и надгортанное или подгортанное сужение воздушных путей.
Одышка может также присутствовать в качестве соматического проявления психических нарушений, например, состояния тревоги, с гипервентиляцией в итоге. Дополнительную информацию относительно оценки и лечения одышки можно найти, например, в Morgan and Hodge, Am. Fam. Phys. 57(4):711-718, 1998.
Любое из антител или антигенсвязывающих фрагментов, раскрытых в настоящем описании, может быть использовано в определении того, что у индивидуума отсутствует связанное с ST2 состояние. В некоторых вариантах осуществления уровень растворимого ST2 человека у индивидуума оценивают (например, с помощью любого из методов, описанных в настоящем описании) и сравнивают с реперным уровнем растворимого ST2 человека. Если уровень растворимого ST2 человека у индивидуума сходен с реперным уровнем растворимого ST2 человека, можно определить, что вероятность наличия у индивидуума связанного с ST2 состояния очень мала. Уровень растворимого ST2 человека у индивидуума «сходен» с реперным уровнем растворимого ST2 человека тогда, когда два уровня в значительной мере близки друг другу в диапазоне, в котором имеется малая вероятность наличия у индивидуума связанного с ST2 состояния. Обычно уровень растворимого ST2 человека у индивидуума «сходен» с реперным уровнем растворимого ST2 человека тогда, кода эти два уровня отличаются друг от друга в пределах приблизительно 25%, например, в пределах приблизительно 25%, 20%, 15%, 10%, 5% или менее. Специалисты в данной области техники должны быть способны определить подходящие реперные уровни растворимого ST2 человека для рассматриваемого связанного с ST2 состояния. Специалисты в данной области техники должны быть также осведомлены о нормальных колебаниях таких уровней растворимого ST2 человека и после прочтения настоящего раскрытия должны быть способны определить, сходен ли измеренный уровень растворимого ST2 человека с реперным уровнем растворимого ST2 человека.
В некоторых вариантах осуществления уровень растворимого ST2 человека определяют один раз, например, в момент, когда имеется подозрение о наличии у индивидуума связанного с ST2 состояния. В некоторых вариантах осуществления уровень растворимого ST2 человека определяют в один или более моментов через 2, 4, 6, 8, 12, 18 и/или 24 часа и/или 1-7 дней после момента возникновения подозрения о наличии у индивидуума связанного с ST2 состояния. В некоторых вариантах осуществления уровень растворимого ST2 человека определяют более одного раза, например, для подтверждения или проверки уровня растворимого ST2 человека, измеренного при первом анализе.
В некоторых вариантах осуществления связывающие растворимый ST2 человека антитела и их антигенсвязывающие фрагменты, описанные в настоящем описании, могут быть использованы в одном или более методах, описанных в публикациях патентных заявок США №№ US 2007/0248981, US 2009/0264779, US 2009/0305265 и US 2010/0009356, публикации заявки PCT WO2007/131031.
В некоторых вариантах осуществления методы диагностирования заболевания у индивидуума включают взятие образца у индивидуума, определение уровня растворимого ST2 человека в образце с использованием по меньшей мере одного антитела или фрагмента, описанного в настоящем описании, и уровня по меньшей мере одного (например, двух, трех, четырех или пяти) дополнительных маркеров, когда повышенный уровень растворимого ST2 человека в образце по сравнению с реперным уровнем растворимого ST2 человека и измененный (например, повышенный или пониженный) уровень по меньшей мере одного дополнительного маркера относительно реперного уровня по меньшей мере одного (например, двух, трех, четырех или пяти) дополнительных маркеров указывают на наличие у индивидуума заболевания (например, сердечно-сосудистого заболевания, легочного заболевания, сепсиса, болезни Кавасаки или связанного с Th2 заболевания или любого другого из заболеваний, описанных в настоящем описании). Реперный уровень по меньшей мере одного дополнительного маркера может представлять собой уровень маркера у индивидуума, у которого не диагностировано наличие заболевания, уровень маркера у индивидуума, у которого не проявляются два или более симптомов заболевания, у индивидуума, не имеющего риска развития заболевания, или уровня у того же самого индивидуума в предшествующий период. Дополнительные маркеры известны в данной области техники, и специалистами в данной области техники могут быть определены методы измерения реперных уровней дополнительных маркеров.
В некоторых вариантах осуществления реперные уровни растворимого ST2 человека могут быть любыми из реперных уровней, описанных в настоящем описании. Специалистами в данной области техники могут быть определены дополнительные реперные уровни растворимого ST2 человека. В некоторых вариантах осуществления образец содержит кровь, сыворотку или плазму. Может быть получен образец и может быть произведено определение уровня растворимого ST2 человека с использованием по меньшей мере одного описанного в настоящем описании антитела или фрагмента как описано выше.
Терапевтические методы
В некоторых вариантах осуществления связывающее ST2 антитело или его антигенсвязывающий фрагмент вводят индивидууму для лечения любого из множества заболеваний или состояний (например, любого из заболеваний, описанных в настоящем описании). Например, уровни растворимого ST2 человека повышены у индивидуумов с заболеваниями, такими как, без ограничения, сердечно-сосудистое заболевание, легочное заболевание, сепсис, болезнь Кавасаки и/или связанные с Th2 заболевания. Для лечения таких заболеваний или состояний может быть использовано любое из антител, связывающих растворимый ST2 человека, или их антигенсвязывающих фрагментов, а также модифицированных антител или антигенсвязывающих фрагментов, полученных на основе таких антител или фрагментов (например, человеческих, гибридных или гуманизированных антител или фрагментов).
В некоторых вариантах осуществления индивидууму вводят антитело или его антигенсвязывающий фрагмент, которое конкурирует за связывание с антителом, продуцируемым гибридомой, депонированной в ATCC и обозначенной патентным депозитным номером PTA-10431 или PTA-104312, или обеими. В некоторых вариантах осуществления индивидууму вводят антитело или антигенсвязывающий фрагмент, описанное в настоящем описании, которое является человеческим, гибридным или гуманизированным. Как известно в данной области техники, такие человеческие, гибридные или гуманизированные антитела и фрагменты обычно менее иммуногены, чем родственные антитела, отличные от человеческих, гибридных или негуманизированных антител. Таким образом, такие человеческие, гибридные или гуманизированные антитела и фрагменты обеспечивают такие терапевтические преимущества, как, без ограничения, сниженный уровень побочных эффектов, переносимость повышенных доз и улучшенные фармакокинетические и/или фармакодинамические свойства. В некоторых вариантах осуществления человеческое, гибридное или гуманизированное антитело или фрагмент, предназначенное для введения индивидууму, получено из антитела, продуцируемого гибридомой, депонированной в ATCC и обозначенной патентным депозитным номером PTA-10431 или PTA-104312, или обеими. Например, для создания гибридного антитела или фрагмента вариабельные области тяжелой и/или легкой цепи таких антител могут быть соединены с константной областью человека или ее фрагментом. Альтернативно, для создания гуманизированного антитела или фрагмента одна или более CDR (например, каждая из CDR) таких антител может быть вставлена в одну или более каркасных областей человека.
В некоторых вариантах осуществления антитело против растворимого ST2 человека или связывающий растворимый ST2 человека фрагмент антитела вводят индивидууму непосредственно. Антитело против растворимого ST2 человека или фрагмент может быть введено в количестве, эффективном при используемых дозах и временных интервалах, необходимом для достижения желаемого результата. Например, терапевтически эффективное количество антитела или фрагмента может меняться в зависимости от таких факторов, как стадия заболевания, возраст, пол и масса тела индивидуума, и способности антитела или фрагмента вызывать желаемый ответ у индивидуума. Режимы доз могут быть адаптированы для обеспечения оптимального ответа на терапию. Например, ежедневно можно вводить несколько разделенных доз или доза может быть пропорционально снижена в соответствии с требованиями терапевтической ситуации. Специалисты в данной области техники должны быть осведомлены о дозах и режимах доз, пригодных для введения индивидууму антитела против растворимого ST2 человека или фрагмента. См., например, Physicians’ Desk Reference, 63rd edition, Thomson Reuters, November 30, 2008.
Антитела против растворимого ST2 человека или связывающие растворимый ST2 человека фрагменты антитела могут быть составлены для доставки любым доступным путем, включая, но не ограничиваясь этим, парентеральный (например, внутривенный), внутрикожный, подкожный, пероральный, назальный, бронхиальный, глазной, чрескожный (местный), через слизистую оболочку, ректальный и вагинальный пути. Антитела или фрагменты могут включать средство для доставки (например, катионный полимер, транспортер для пептидных молекул, поверхностно-активное вещество и т.д.) в сочетании с фармацевтически активным носителем. Применяемый в настоящем описании термин «фармацевтически активный носитель» включает растворители, диспергирующие среды, покрытия, антибактериальные и противогрибковые средства, изотоничные и задерживающие всасывание средства и тому подобное, совместимые с фармацевтическим введением. В фармацевтические составы, которые содержат антитело или его антигенсвязывающий фрагмент, описанные в настоящем описании, могут быть включены дополнительные активные соединения.
Наборы
В настоящем описании также предлагаются наборы, которые включают реагент, содержащий по меньшей мере одно (например по меньшей мере два, три, четыре или пять) антитело против растворимого ST2 человека или антигенсвязывающий фрагмент, описанное в настоящем описании. Наборы обычно состоят из следующих основных элементов: упаковка, реагенты, включающие описанные выше связывающие композиции, необязательно контроль и инструкции. Упаковка может представлять собой коробку для хранения сосуда (или нескольких сосудов), содержащих указанные связывающие композиции, сосуда (или нескольких сосудов), содержащих контроль, и инструкции по применению описанного в настоящем описании метода. Специалисты в данной области техники могут легко модифицировать упаковку для удовлетворения индивидуальных потребностей.
В некоторых вариантах осуществления предлагаемый в настоящем описании набор может содержать по меньшей мере одно (например, по меньшей мере два, три, четыре или пять) из любых антител или антигенсвязывающих фрагментов, описанных в настоящем описании. Например, набор может содержать по меньшей мере одно (например, по меньшей мере два, три, четыре или пять) антитело или его антигенсвязывающий фрагмент, которое конкурирует за связывание с антителом, продуцируемым гибридомой, депонированной в ATCC и обозначенной патентным депозитным номером PTA-10431 или PTA-104312, или обеими.
В некоторых вариантах осуществления предлагаемый в настоящем описании набор содержит по меньшей мере одно (например, по меньшей мере два, три, четыре или пять) антитело против растворимого ST2 человека или антигенсвязывающий фрагмент, описанное в настоящем описании, и один или более реагент для выявления связывания антитела или антигенсвязывающего фрагмента с растворимым ST2 человека. Например, набор может быть разработан для использования в хемилюминесцентном иммунологическом анализе с микрочастицами (CMIA), таком как анализы ARCHITECT от Abbot Diagnostics (Abbott Park, IL), и таким образом могут содержать парамагнитные микрочастицы, покрытые антителами против BNP, и парамагнитные микрочастицы, покрытые антителами против растворимого ST2 человека. Эти микрочастицы вводят в контакт с образцом, и находящийся в образце растворимый ST2 человека может связаться с покрытыми микрочастицами. Необязательно образец может быть разделен по меньшей мере на две аликвоты, и микрочастицы каждого типа могут быть введены в контакт с отдельной аликвотой. После промывки может быть добавлен меченный акридином конъюгат антитела против растворимого ST2 человека для образования реакционной смеси на второй стадии. После дополнительного цикла промывки к реакционной смеси добавляют предтриггерный и триггерный растворы. Возникшую хемилюминесцентную реакцию измеряют, например, с помощью ARCHITECT i System optics (Abbot Diagnostics, Abbott Park, Illinois). Между количеством растворимого ST2 человека в образце и определяемой хемилюминесценцией имеется прямая зависимость.
В некоторых вариантах осуществления предлагаемый в настоящем описании набор содержит по меньшей мере одно (например, по меньшей мере два, три, четыре или пять) антитело против растворимого ST2 человека или антигенсвязывающий фрагмент, описанное в настоящем описании, и один или более компонентов твердофазного иммунологического анализа для определения растворимого ST2 человека посредством твердофазного анализа. В твердофазных иммунологических анализах используется твердая подложка, с которой связан один из членов пары лиганд-рецептор, например, антитело или его антигенсвязывающий фрагмент. Неограничивающие примеры твердых подложек включают чашки, пробирки, шарики из полистирола и различные пористые материалы, например, такие как нейлон, нитроцеллюлоза, ацетат целлюлозы и стеклянные волокна. См., например, патенты США №№ 4703017; 4743560; и 5073484. В некоторых вариантах осуществления набор включает компоненты для твердофазного иммунологического анализа, в котором связанное с твердой фазой антитело или его антигенсвязывающий фрагмент (например, антитело против растворимого ST2 человека или его антигенсвязывающий фрагмент) вводят в контакт с образцом, содержащим интересующее анализируемое вещество (например, растворимый ST2 человека), после чего твердую фазу промывают для удаления несвязавшегося вещества.
В некоторых вариантах осуществления набор содержит компоненты для проточного твердофазного иммунологического анализа. В проточных твердофазных иммунологических анализах нет необходимости в стадиях инкубации и промывки, связанных с другими типами твердофазного иммунологического анализа. В данной области техники известно множество проточных твердофазных иммунологических анализов. Например, в патенте США № 4632901 раскрыто устройство для проточного иммунологического анализа, где антитело (специфичное в отношении целевого анализируемого антигена) связано с пористой мембраной или фильтром, к которой добавляют жидкий образец. При прохождении жидкости через мембрану целевое анализируемое вещество связывается с антителом. После добавления образца добавляют меченое антитело. Визуальное выявление меченого антитела указывает на наличие в образце целевого анализируемого антигена. Более того, в патенте США № 5229073 описан полуколичественный метод конкурентного иммунологического анализа с латеральным потоком, в котором используется множество зон или линий захвата, содержащих иммобилизованные антитела, для измерения уровней липопротеида в плазме. Дополнительные примеры тестов с латеральным потоком для определения анализируемых веществ раскрыты в патентах США №№ 4168,146; 4366241; 4703017; 4855240; 4861711; и 5120643; Европейском патенте № 0296724; WO 97/06439; и WO 98/36278. Специалисты в данной области техники должны быть осведомлены о других подходящих методах и устройствах твердофазного иммунологического анализа и должны быть способны использовать в таких методах и устройствах одно или более антител против растворимого ST2 человека или антигенсвязывающие фрагменты, описанные в настоящем описании.
В некоторых вариантах осуществления могут быть использованы другие методы детектирования, например, колориметрический анализ, радиоиммунологический анализ или хемилюминесцентный анализ. Могут быть также использованы сэндвичные тесты, например, с использованием двух моноклональных антител, одно из которых метят йодом 125, а другое адсорбируют на шариках, например, как это используется в наборе IRMA-BNP2 от CISBIO International (Франция) и наборах ShionoRIA BNP или ANP (SHIONOGI USA Inc.).
Предлагаемые в настоящем описании наборы можно использовать в любых методах (например, методах диагностики), описанных выше. Например, наборы, содержащие по меньшей мере одно (например, по меньшей мере два, три, четыре или пять) антитело против растворимого ST2 человека или его антигенсвязывающий фрагмент, описанное в настоящем описании, могут быть использованы для определения уровня растворимого ST2 человека в образце. Более того, наборы, содержащие по меньшей мере одно (например, по меньшей мере два, три, четыре или пять) антитело против растворимого ST2 человека или его антигенсвязывающий фрагмент, могут быть использованы для определения реперного уровня растворимого ST2 человека. Специалисты в данной области техники должны быть осведомлены о других подходящих применениях предлагаемых в настоящем описании наборов, а также должны быть способны использовать наборы для таких применений.
В некоторых вариантах осуществления наборов по меньшей мере одно (например, одно, два, три или четыре) из антител или фрагментов имеет KD для связывания растворимого ST2 человека, равную 8,59×10-10 М или ниже. В некоторых вариантах осуществления наборов предлагается набор для твердофазного иммуноферментного анализа. В некоторых вариантах осуществления наборы дополнительно включают рекомбинантный растворимый ST2 человека, выделенный из клеток человека (например, клеток почки эмбриона человека). В некоторых вариантах осуществления наборы дополнительно включают полностью гликозилированный растворимый ST2 человека (например, находящийся в клеточном экстракте или поставляемый в виде выделенного белка).
Примеры
Изобретение дополнительно описывается в следующих примерах, которые не ограничивают объем изобретения, описанного в формуле изобретения.
Пример 1: Получение и характеристика моноклональных антител против ST2
Моноклональные антитела против белка растворимого ST2 человека (sST2) получали иммунизацией мышей рекомбинантным белком, полученным на основе последовательности кДНК человека для sST2.
Получение антигена и подтверждение: клон кДНК sST2 человека с номером регистрации в GeneBank NM_003856.2 был приобретен у Origene Technologies, Inc. of Rockville, MD. С помощью стандартных методов ПЦР этот клон был использован в качестве источника последовательности для создания экспрессионного вектора, включающего полную последовательность растворимого ST2 человека с гексагистидиновой меткой для очистки, включенной в область N-конца белка. Целостность экспрессионного клона была подтверждена секвенированием ДНК. Рекомбинантный белок получали путем преходящей трансфекции и экспрессии в клетках почки эмбриона человека (HEK293). Рекомбинантный белок растворимого ST2 человека очищали пропусканием клеточного лизата через хелатирующую металл колонку, специфически связывающую гистидиновую метку для очистки, включенную в экспрессируемый белок. Очистка рекомбинантного растворимого ST2 человека была подтверждена с помощью окрашивания кумасси полиакриламидного геля и вестерн-блот анализа с использованием имеющихся в продаже антител против ST2 (моноклональное антитело D067, полученное от MBL International), а также антител против метки His. См. фиг.1, 2 и 3A-3C. На основании аминокислотной последовательности сам белок имеет молекулярную массу 36 кДа, а Kuroiwa et al. (Biochem. Biophys. Res. Comm. 284: 1104-1108, 2001) было показано, что нативный белок в сыворотке человека имеет молекулярную массу ~58 кДа. Очищенный рекомбинантный белок, полученный с помощью данной экспрессионной системы, имел кажущуюся молекулярную массу ~58 кДа полностью гликозилированного белка и соответствующим образом распознавался имеющимися в продаже антителами против ST2. Количественную оценку осуществляли с помощью анализа Bradford для суммарного белка.
Гибридома и получение моноклонального антитела: Моноклональные антитела получали иммунизацией мышей рекомбинантным белком, полученным, как описано выше.
Три мыши Balb/c иммунизировали следующим образом:
После последней иммунизации титр антитела определяли в крови из хвоста каждого животного. Животное с наибольшим титром антитела использовали для слияния с селезенкой и получения гибридомы. После получения гибридом в виде стабильных клеточных культур в 96-луночных планшетах их подвергали скринингу на связывание с рекомбинантным белком растворимого ST2 человека и с типичным белком, содержащим используемую для очистки метку гекса-his для отбраковки гибридом, специфичных в отношении этой метки. Для дополнительной характеристики и получения продукта были отобраны две гибридомы: 7E4 и 9F8. Оба моноклональных антитела тестировали на чувствительность к рекомбинантному растворимому ST2 человека как антигену путем покрытия отдельных лунок 96-луночных планшетов для микротитрования одинаковыми количествами каждого антитела, 7E4 и 9F8, и затем тестировали против 3-кратных последовательных разведений конъюгированного с биотином рекомбинантного растворимого ST2 человека в диапазоне концентраций от 300 до 0,41 нг/мл (см. фиг.4).
Два антитела демонстрируют сопоставимую чувствительность к анализируемому веществу с очень высокой величиной абсорбции ~1,0, наблюдаемой при наименьшей тестированной концентрации анализируемого вещества, 0,41 нг/мл. Кроме того, двумя антителами покрывали отдельные лунки 96-луночного планшета при концентрациях, варьирующих от 5 мкг/мл до 0, и тестировали против одной концентрации конъюгированного с биотином рекомбинантного растворимого ST2 человека (см. фиг.5). Оба антитела проявляли значительную чувствительность при концентрации ≥1,25 мкг/мл, притом что антитело 9F8 демонстрировало чуть большую чувствительность.
Антитела 7E4 и 9F8 тестировали также на их способность к совместному использованию в конфигурации сэндвичного иммуноферментного анализа (EIA) с моноклональными антителами. Каждым моноклональным антителом покрывали отдельные лунки 96-луночного планшета для микротитрования при постоянной концентрации и анализировали против 3-кратных последовательных разведений растворимого ST2 человека в диапазоне концентраций от 10 нг/мл до 0,01 нг/мл с использованием для выявления комплекса другого моноклонального антитела, конъюгированного с биотином. Как показано на фиг.6, обе комбинации антител обеспечивают сопоставимую чувствительность и легко выявляют даже 0,01 нг/мл растворимого ST2 человека.
Дополнительный анализ с использованием поверхностного плазмонного резонанса (SPR) подтвердил, что каждое из антител 7E4 и 9F8 распознает индивидуальный эпитоп и что эти эпитопы отличны от эпитопов, распознаваемых имеющимися в продаже антителами D066 и D067, моноклональными антителами, используемыми MBL International Corporation (MBL) в их ELISA. Фиг.7 иллюстрирует результаты SPR анализа антител 7E4, 9F8 и третьего нового антитела против растворимого ST2 человека, включенного в качестве репера (11A7), обоих имеющихся в продаже моноклональных антител от MBL (D066 and D067) плюс постороннего антитела для определения базальной линии. Были получены индивидуальные чипы путем покрытия каждым моноклональным антителом. Рекомбинантный растворимый ST2 человека пропускали через чип и давали ему связаться. Затем через комплекс первое антитело-растворимый ST2 человека пропускали тестируемые моноклональные антитела для оценки того, может ли и второе антитело связаться с комплексом через растворимый ST2 человека. С комплексом должны связываться лишь те вторые антитела, которые распознают эпитоп, отличный от эпитопа, распознаваемого первым антителом.
Результаты анализа SPR представлены на фиг.7A-F.
График A1 (фиг.7A): Когда в качестве первого захватывающего антитела использовали антитело 9F8 (A1), каждое тестируемое антитело давало по меньшей мере минимальный выявляемый сигнал. Тестируемое антитело 7E4 (L2) давало наибольший сигнал, а постороннее антитело (L6) давало наименьший сигнал. Вывод из этого графика заключается в том, что антитело 9F8 распознает эпитоп, отличный от эпитопов, распознаваемых любым из тестированных антител, и что пара 9F8-7E4 обеспечивает наибольшее суммарное связывание.
График A2 (фиг.7B): Когда в качестве первого захватывающего антитела использовали антитело 7E4 (A2), тестируемое антитело 9F8 (L1) проявляло очень хорошее связывание, постороннее антитело не давало измеряемого сигнала, а остальные тестируемые антитела давали слабый, но измеримый сигнал. Вывод из этого графика заключается в том, что антитело 7E4 распознает эпитоп, отличный от эпитопов, распознаваемых любым из тестированных антител, и что пара 9F8-7E4 обеспечивает наибольшее суммарное связывание.
График A3 (фиг.7C): Когда в качестве первого захватывающего антитела использовали новое антитело 11A7 (A3), тестируемое антитело 9F8 (L1) проявляло очень хорошее связывание, постороннее антитело не давало измеряемого сигнала, а остальные тестируемые антитела давали слабый, но измеримый сигнал. Результаты были практически идентичными результатам, полученным при использовании в качестве захватывающего антитела 7E4.
График A4 (фиг.7D): Когда в качестве первого захватывающего антитела использовали антитело D066 MBL (A4), тестируемое антитело 9F8 (L1) проявляло очень хорошее связывание, за которым по силе связывания следовало антитело 7E4 (L2). Постороннее антитело не давало измеряемого сигнала, а остальные тестируемые антитела давали слабый, но измеримый сигнал. Вывод из этого графика заключается в том, что антитело D066 распознает эпитоп, отличный от эпитопов, распознаваемых любым из тестированных антител, и что оно образует связывающую пару со вторым антителом MBL, D067, но с гораздо меньшим сродством связывания по сравнению с парой 9F8-7E4.
График A5 (фиг.7E): Когда в качестве первого захватывающего антитела использовали антитело D067 MBL (A5), тестируемое антитело 9F8 (L1) проявляло очень хорошее связывание, за которым по силе связывания следовали антитела 7E4 (L2) и D066 (L4). Постороннее антитело не давало измеряемого сигнала, а антитело 11A7 давало очень слабый сигнал. Вывод из этого графика заключается в том, что антитело D067 распознает эпитоп, отличный от эпитопов, распознаваемых любым из тестированных антител, и что оно образует связывающую пару со вторым антителом MBL, D066, но с гораздо меньшим сродством связывания по сравнению с парой 9F8-7E4.
График A6 (фиг.7F): Когда в качестве первого антитела использовали постороннее антитело, любое из тестируемых антител не давало измеримого сигнала, что подтверждает специфичность тестируемых антител в отношении сродства к растворимому ST2 человека.
Этот анализ подтвердил, что новые моноклональные антитела 9F8 и 7E4 против растворимого ST2 человека распознают эпитопы, отличные от эпитопов, распознаваемых моноклональными антителами MBL D066 и D067. Более того, анализ также подтвердил, что пара 9F8-7E4 обладает более высоким сродством связывания по сравнению с парой D066-D067.
Это повышенное сродство связывания, наблюдаемое для пары 9F8-7E4, было подтверждено путем прямого сравнения двух пар моноклональных антител при тестировании образцов человеческой плазмы. В эксперименте, результаты которого резюмированы в таблице 1, MBL ELISA, включающий пару антител D066-D067, сравнивали с новой парой антител 9F8-7E4. Четыре (4) образца плазмы тестировали при 2-кратных последовательных разведениях, причем использовали соответствующую пару плазмы с ЭДТА и гепарином от донора с низкой концентрацией растворимого ST2 человека и оба образца плазмы с ЭДТА и гепарином от донора с повышенной концентрацией растворимого ST2 человека.
Чувствительность D066-D067 и 9F8-7E4 при использовании образцов человеческой плазмы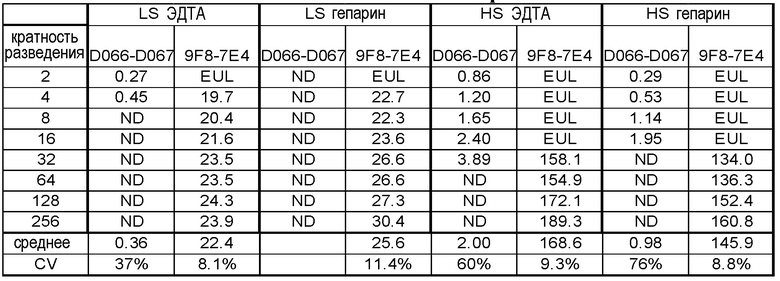
Результаты, представленные в таблице 1, были получены при использовании анализа, оптимизированного для каждого отдельного случая, и выражены в нг/мл на основе калибратора, оптимизированного для каждой пары антител. Сообщаемые в настоящем описании величины не приведены в соответствие друг другу, поскольку использованные для калибровки белки не нормировали относительно друг друга, а определяли независимо друг от друга. Как показано в таблице 1, пределом измерения для пары D066-D067 было разведение 1:4 образца LS ЭДТА при низкой точности, в то время как пара 9F8-7E4 обеспечивала точное измерение вплоть до разведения 1:256 при хорошей сходимости, CV<10%. Эта разница в чувствительности сохранялась при тестировании образца плазмы HS ЭДТА. Примечательно также, что пара D066-D067 не обеспечивала выявление даже при наименьшем разведении образца плазмы LS с гепарином, а в образцах плазмы HS с гепарином давала значительно меньший сигнал по сравнению с сигналом пары D066-D067 от образца плазмы с ЭДТА, что указывает на чувствительность к гепарину или ингибирование гепарином этой пары антител. Пара 9F8-7E4 не проявляла этой чувствительности к гепарину и сохраняла хорошую сходимость, низкую CV, в обоих тестируемых образцах плазмы с низкой и высокой концентрацией растворимого ST2 человека.
Пример 2: Характеристика методом EIA пары моноклональных антител 9F8-7E4
Характеристики пары моноклональных антител 9F8-7E4 анализировали с помощью иммуноферментного анализа (EIA).
Функциональная чувствительность (предел количественного определения): предел функциональной чувствительности определяли путем оценки различных концентраций разводимого калибратора в 20 повторах. В дополнение к пустой пробе в виде буфера тестируемые концентрации калибратора включали 0,0625, 0,125 и 0,25 нг/мл. Функциональная чувствительность определяется как самая низкая концентрация с CV≤20%. Как показано в последующей таблице 2, все тестируемые концентрации удовлетворяют этому критерию, включая самую низкую концентрацию, составляющую 0,0625 нг/мл.
Сводка анализа функциональной чувствительности
Для определения аффинности четырех антител, полученных описанными в настоящем документе способами (9F8, 7E4, 11A7 и 15D06), и двух антител, полученных MBL International (D066-3 и D067-3), использовали также SPR. Каждый эксперимент осуществляли путем определения связывания следующих концентраций рекомбинантного растворимого белка ST2 человека, используемого для получения описанных в настоящем документе антител 9F8 и 7E4: 50 нМ, 25 нМ, 12,5 нМ, 6,25 нМ, 3,25 нМ, и 0 нМ. Данные этих экспериментов представлены на фиг.8A-8F. Рассчитанные KD связывания каждого антитела с рекомбинантным растворимым ST2 человека, выделенным из клеток эмбриональной почки человека, представлены в таблице 3.
KD связывания каждого антитела с растворимым ST2 человека
Точность: Оценку точности метода осуществляли в соответствии с руководством по оценке точности выполнения количественных методов измерения института клинической и лабораторной стандартизации (CLSI): Approved Guideline-Second Edition. (InVitro Diagnostics) EP5-A2. Три образца пулированной плазмы больных аликвотировали в двадцать 1,5-мл пластиковых пробирок для каждого концентрационного уровня и замораживали при -80°С. Эти образцы анализировали в двух параллельных пробах с одним прогоном в день в течение 20 дней в пределах 2 месяцев после взятия крови. Рассчитывали аналитическую неточность (CVA) в пределах одного прогона и суммарную с использованием теста оценки точности для одного прогона CLSI. Тест характеризовался CVA в пределах одного прогона 2,4% и суммарным CVA 4,0% при средней концентрации 11 нг/мл (пул 1, низкая), CVA в пределах одного прогона 2,0% и суммарным CVA 3,9% при средней концентрации 87 нг/мл (пул 2, средняя), и CVA в пределах одного прогона 2,2% и суммарным CVA 3,9% при средней концентрации 140 нг/мл (пул 3, высокая). См. таблицу 4.
Сводка анализа точности
В тесте не выявляется какой-либо систематической ошибки точности в пределах диапазона тестируемых концентраций.
Оценка мешающих веществ (чувствительности к антикоагулянту): У тридцати несомненно здоровых добровольцев отбирали образцы плазмы в наиболее обычные типы пробирок: для сыворотки, ЭДТА-плазмы, цитратной плазмы и гепаринизированной плазмы. Анализ осуществляли немедленно после обычного центрифугирования и обработки образцов с помощью набора для отдельного анализа растворимого ST2 человека. Добровольцы включали 9 мужчин и 21 женщину возрастом 22-66 лет. Результаты анализа суммированы в таблице 5. Как указано в таблице 5, величина медианы для пробирки с цитратом была слегка ниже, чем для других типов пробирок, что не является неожиданным, так как пробирки с цитратом содержат небольшой объем жидкого антикоагулянта в пробирке, что дает умеренное разведение собранного образца относительно других типов пробирок, в которых не существует влияния на объем образца. Для тестирования согласованности измерений каждый тип пробирки с плазмой сравнивали с пробиркой с сывороткой. Каждое сравнение приводило к очень высокой величине R2, находящейся в диапазоне от 0,849 до 0,964. Таким образом, с учетом предположения об умеренном разведении в пробирках с цитратом, которое может влиять на измерения нормальных концентраций, не наблюдалось измеряемой систематической ошибки в зависимости от типа пробирки.
Сводка результатов тестирования антикоагулянтов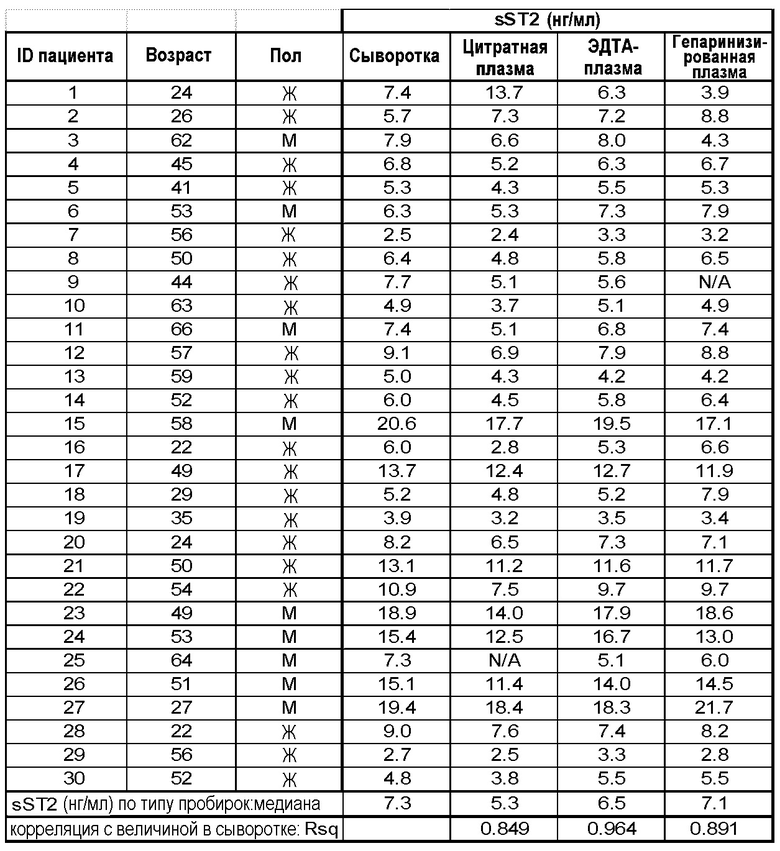
Определение реперного интервала нормальных концентраций: для этого анализа была набрана когорта из 490 доноров с самооценкой как здоровые, не имеющие ни серьезного заболевания, ни текущего лечения по поводу любого серьезного заболевания, равномерно распределенных по полу и в возрасте от 18 до 84 лет.
В таблице 6 представлена сводка количества индивидуумов в каждой возрастной группе с разделением по полу для реперного диапазона этой когорты здоровых индивидуумов, и фиг.10 представляет собой гистограмму распределения концентраций растворимого ST2 человека. Столбики представляют собой реальные данные, а вертикальные линии внутри столбиков представляют собой теоретическое нормальное распределение. Распределение концентраций у этих здоровых индивидуумов не было нормальным. В таблице 7 проведено сравнение концентраций растворимого ST2 человека в зависимости от пола. В этой нормальной популяции здоровых индивидуумов медиана концентраций у мужчин была значимо выше, чем у женщин (тест Крускала-Уоллиса: p<0,0001).
Реперный диапазон когорты здоровых индивидуумов
Сравнение реперных групп по величинам медиан в зависимости от пола
При стратификации концентраций растворимого ST2 человека в зависимости от возраста выявлено, что между этими группами нет значимых различий, фиг.11 (тест Крускала-Уоллиса; мужчины=0,501, женщины=0,056). Таким образом, зависимые от пола реперные величины, а также величины всей группы рассчитывали с использованием непараметрического метода процентилей (90%, односторонний). Эти результаты суммированы в таблице 8.
Сводка CDD здоровой реперной группы
В таблице 9 перечислена концентрация растворимого ST2 человека при некоторых характерных пороговых величинах.
Концентрации sST2 при характерных пороговых величинах у когорты людей США с самооценкой как здоровые
Концентрации растворимого ST2 натощак по сравнению со статусом после еды: образцы плазмы брали у двадцати пяти больных (19 мужчин и 6 женщин) с различными заболеваниями (8 из них с сахарным диабетом типа 2) в 7.00 утра после периода голодания в течение ночи. После этого больным давали стандартизированный завтрак (730 ккал для больных, не страдающих диабетом, и 522 ккал для больных диабетом). Второе взятие крови для определения концентрации растворимого ST2 человека осуществляли в 11.00 утра. Затем все больные получали стандартизированный ленч (800 ккал для больных, не страдающих диабетом, и 716 ккал для больных диабетом). Третий и последний забор крови проводили в 2.00 дня. Средние концентрации растворимого ST2 человека 25 индивидуумов рассчитывали во всех трех временных точках. Парные t-критерии использовали для определения того, есть ли различие между концентрациями растворимого ST2 человека в плазме в отсутствие голодания (т.е. при взятии крови в 11.00 утра и 2.00 дня) по сравнению с соответствующими величинами на фоне голодания (т.е. при взятии крови в 7.00 утра). Относительное изменение концентраций растворимого ST2 человека с течением времени сравнивали с RCV для определения влияния приема пищи на концентрацию анализируемого соединения.
Средняя концентрация растворимого ST2 человека при голодании составляла 18 Е/мл (медиана 17 Е/мл; диапазон 9-26 Е/мл) в 7.00 утра, средняя концентрация растворимого ST2 человека после завтрака составляла 19 Е/мл (медиана 18 Е/мл; диапазон 11-28 Е/мл; p=0,025 по сравнению с ST2 при голодании) в 11.00 утра, и средняя концентрация растворимого ST2 человека после ленча составляла 18 Е/мл (медиана 18 Е/мл; диапазон 10-28 Е/мл; p=0,014 по сравнению с растворимым ST2 человека при голодании) в 2.00 часа дня. Средние концентрации растворимого ST2 человека в 11.00 утра и 2.00 дня, таким образом, были <5% выше, чем величина среднего, полученная в 7.00 утра.
Сравнение нормальных концентраций растворимого ST2 человека и концентраций при заболеваниях: концентрации растворимого ST2 человека были заметно выше у больных сердечной недостаточностью по сравнению с нормальными, здоровыми индивидуумами. При последующем анализе нормальную концентрацию, определенную у 490 здоровых доноров, сравнивали с отдельными различающимися популяциями; с 528 здоровыми добровольцами с подтвержденным с помощью скрининга биомаркеров отсутствием скрытого сердечно-сосудистого заболевания (CVD) или воспалительного заболевания (скрининг по BNP, PCT, CRP, и IL-6), с 709 больными с диагнозом острой сердечной недостаточности, с 1159 больными с диагнозом хронической стабильной сердечной недостаточности, с 190 больными с диагнозом легочной артериальной гипертензии (PAH), с 48 больными с диагнозом астмы, с 223 больными с диагнозом астмы или ХОБЛ, с 58 больными с диагнозом легочной эмболии (PE), с 119 больными с диагнозом пневмонии (PNA), с 109 больными с диагностированным синдромом прогрессирующего респираторного заболевания, с 50 подростками с диагнозом болезни Кавасаки (KD) и с 15 больными с диагнозом сепсиса. В таблице 10 представлены величины медиан, 95% доверительный интервал и межквартильный размах (IQR) концентраций растворимого ST2 человека в каждой группе.
Концентрации sST2 в зависимости от типа заболевания
Сравнение концентраций растворимого ST2 человека и риска смерти в течение 1 года: концентрации растворимого ST2 человека измеряли также в образцах крови от когорты PRIDE (Junuzzi et al., J. Am. Coll. Cardiol. 50:607-613, 2007). Из 599 индивидуумов в исходной когорте PRIDE у 586 были образцы крови, доступные для измерения растворимого ST2 человека с использованием описанных выше методов. Используемые образцы представляли собой аликвоты ЭДТА-плазмы, замороженные при -80°С. Анализировали графики характеристических кривых обнаружения (ROC), построенные против смерти в течение одного года в качестве реперного стандарта, и области под кривой (AUC) сравнивали в соответствии с методом Hanley et al. (Radiology 148:839-843, 1983) для определения способности теста предсказывать смертность в течение 1 года по всем причинам в когорте PRIDE.
В этих экспериментах медианные концентрации для полной когорты составляли 27 нг/мл (диапазон <2-393 нг/мл) для этого теста. В данной когорте с помощью непараметрического корреляционного анализа обнаружен коэффициент корреляции (rs) 0,955 (95%CI, 0,947-0,962; p<0,001) для обоих методов. Из 586 больных 92 (16%) индивидуума умерли в течение одного года и 494 (84%) выжили. При анализе кривых продемонстрирована AUC, составляющая 0,803 (95% CI, 0,768-0,834), с помощью теста для прогноза смерти в течение 1 года.
Другие варианты осуществления
Должно быть понятно, что, в то время как изобретение описано в связи с его подробным описанием, предшествующее описание предназначено для иллюстрации и не ограничивает объем изобретения, который определяется объемом прилагаемой формулой изобретения. Другие аспекты, преимущества и модификации входят в объем последующей формулы изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИТЕЛА ПРОТИВ РАСТВОРИМОГО ST-2 ЧЕЛОВЕКА И СПОСОБЫ АНАЛИЗА | 2011 |
|
RU2684724C2 |
| СПОСОБЫ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ГИПЕРТЕНЗИИ | 2013 |
|
RU2683026C2 |
| ТЕСТОВЫЙ АППАРАТ И СПОСОБЫ ДЛЯ СЕРДЕЧНОГО БИОЛОГИЧЕСКОГО МАРКЕРА ST2 | 2015 |
|
RU2702645C2 |
| АНТИТЕЛА К СЕАСАМ1 И СПОСОБЫ ИХ ИСПОЛЬЗОВАНИЯ | 2010 |
|
RU2598710C2 |
| АНТИТЕЛА ПРОТИВ IL-33, КОМПОЗИЦИИ, СПОСОБЫ И ИХ ПРИМЕНЕНИЕ | 2017 |
|
RU2740309C2 |
| СПОСОБЫ ЛЕЧЕНИЯ БОЛИ И ВОСПАЛЕНИЯ В НЕЙРОННОЙ ТКАНИ С ПРИМЕНЕНИЕМ АНТАГОНИСТОВ IL-31 | 2007 |
|
RU2440130C2 |
| МОНОКЛОНАЛЬНЫЕ АНТИТЕЛА ПРОТИВ IL-31 И СПОСОБЫ ПРИМЕНЕНИЯ | 2006 |
|
RU2444528C2 |
| НОВЫЕ АНТИТЕЛА ПРОТИВ PD-L1 | 2016 |
|
RU2736151C2 |
| ТВЕРДОФАЗНЫЙ ИММУНОФЕРМЕНТНЫЙ АНАЛИЗ (ELISA) ДЛЯ ФАКТОРА РОСТА ЭНДОТЕЛИЯ СОСУДОВ (VEGF) | 2007 |
|
RU2517301C2 |
| МОНОКЛОНАЛЬНЫЕ АНТЕТЕЛА К CD44, ПРЕДНАЗНАЧЕННЫЕ ДЛЯ ПРИМЕНЕНИЯ ПРИ ЛЕЧЕНИИ ПЛОСКОКЛЕТОЧНОЙ КАРЦИНОМЫ ГОЛОВЫ И ШЕИ | 2011 |
|
RU2599447C2 |




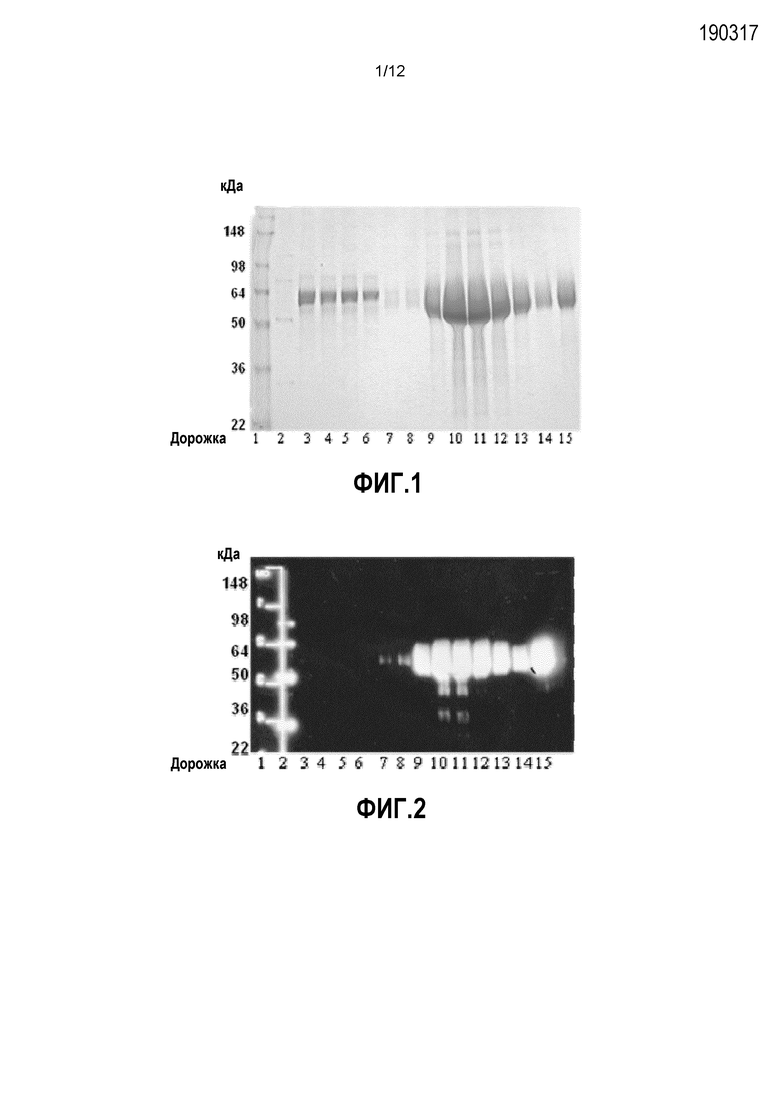
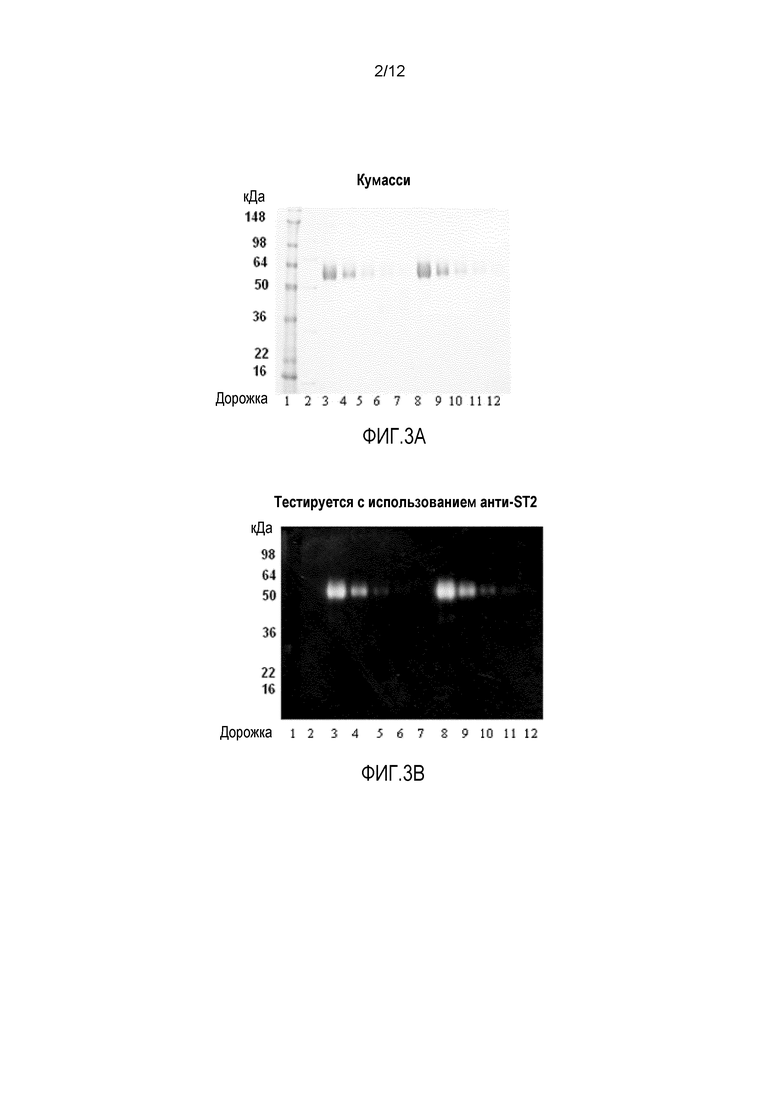
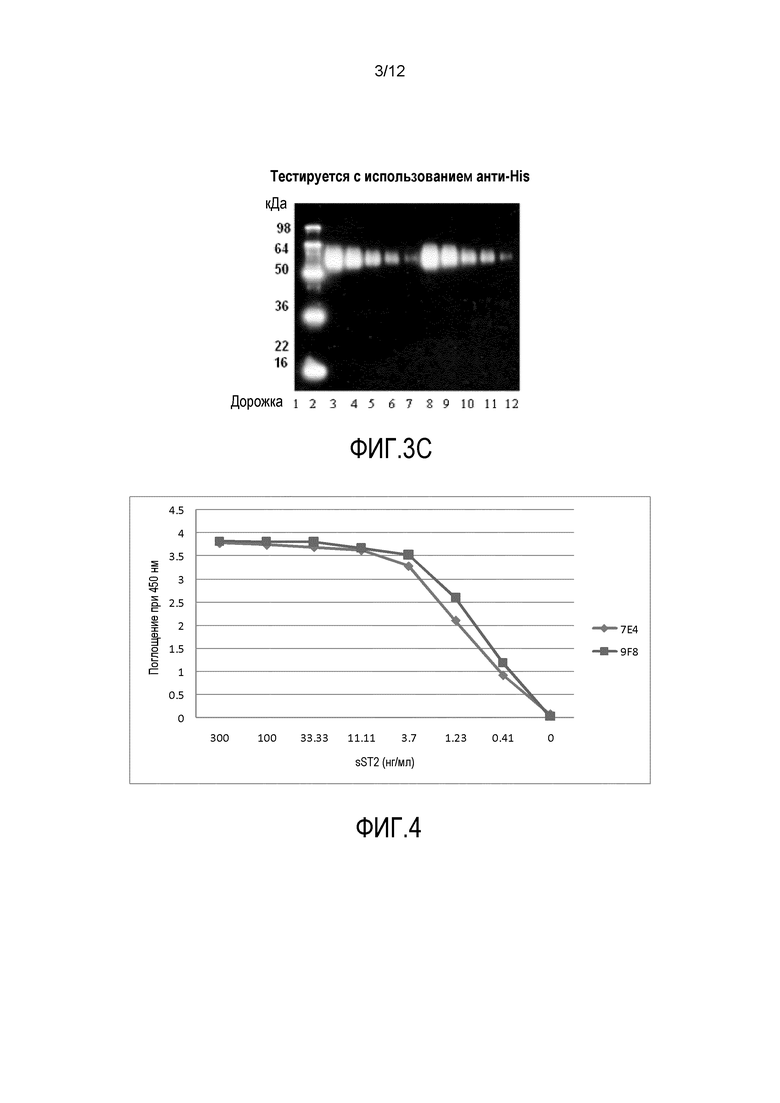
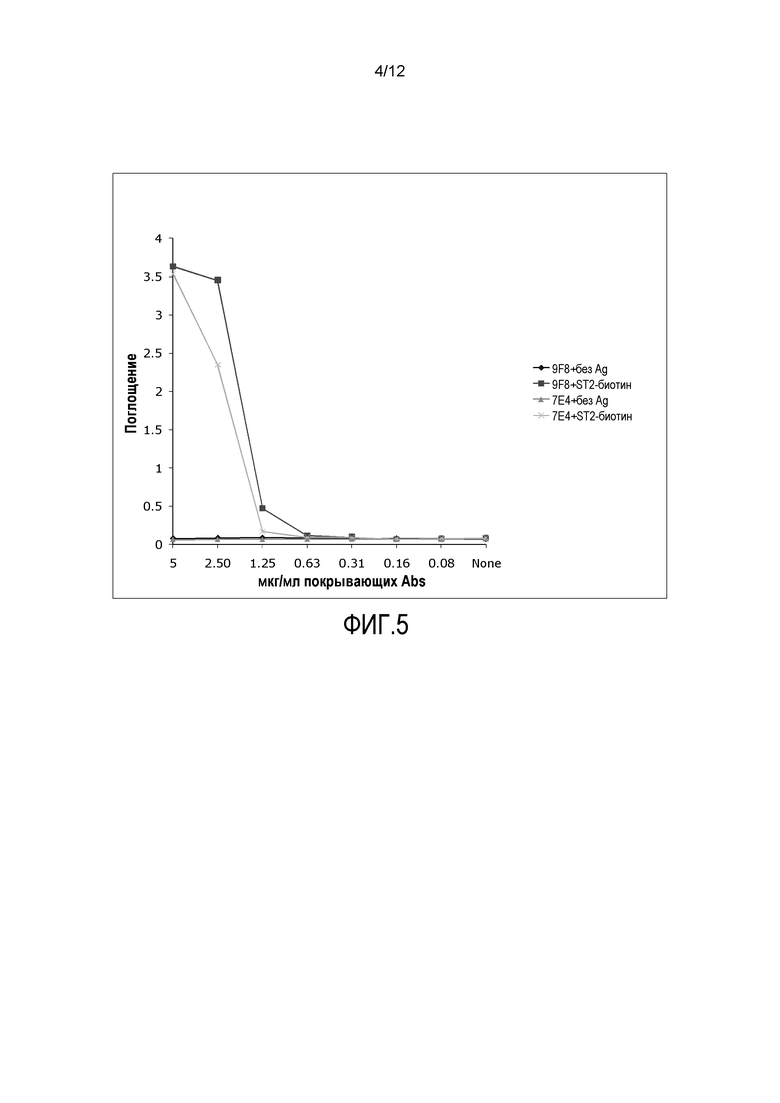
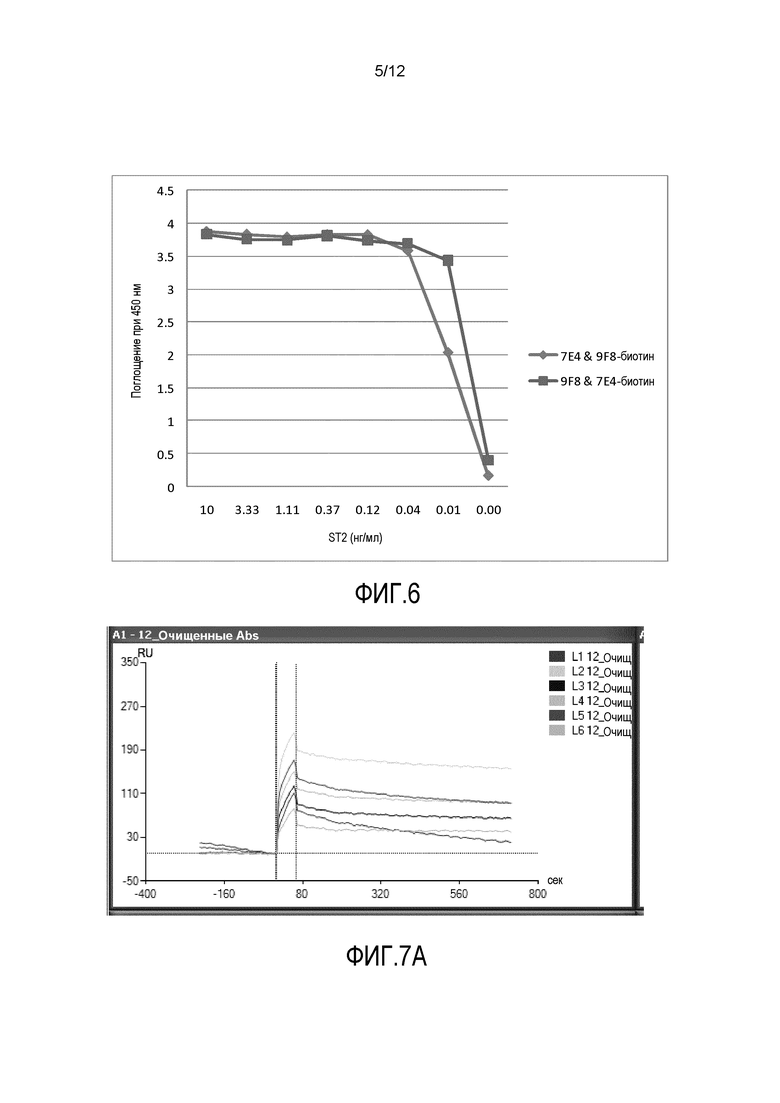
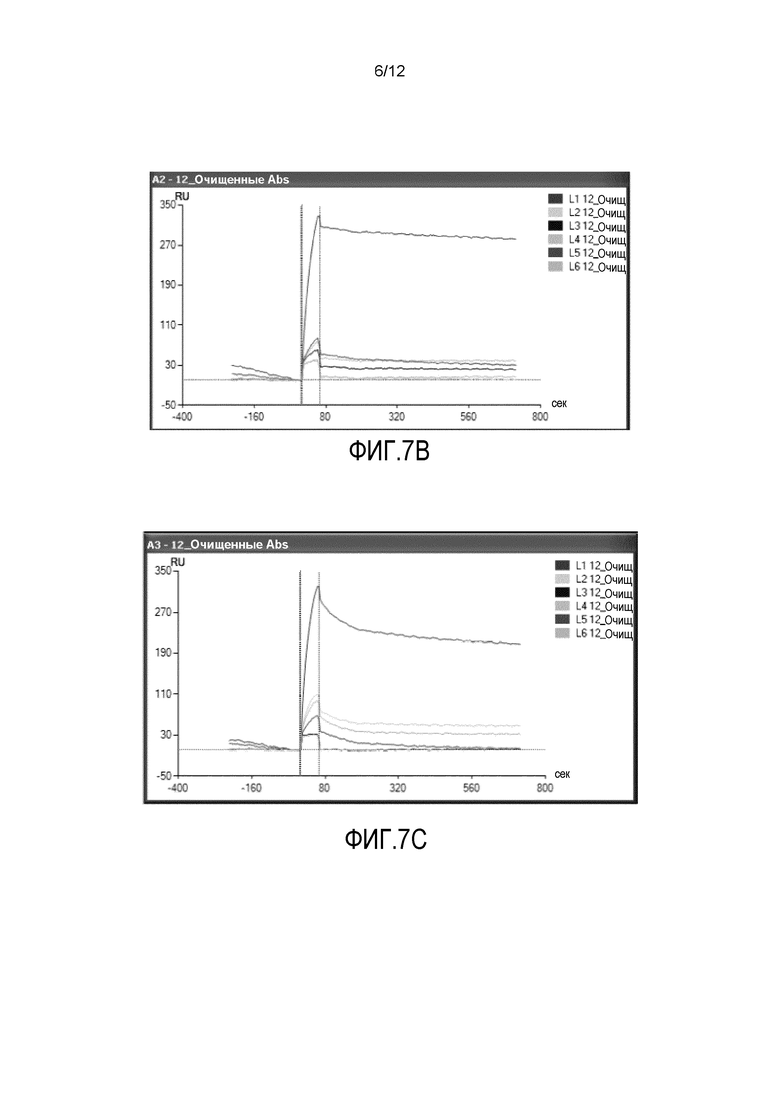
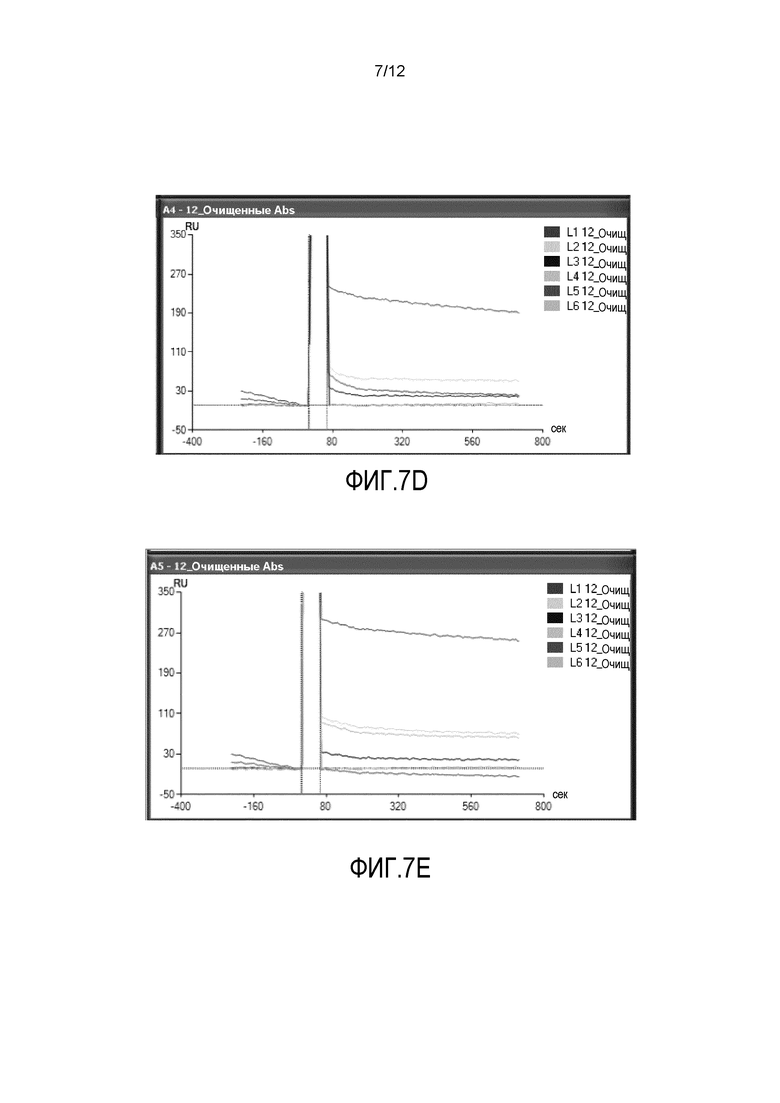
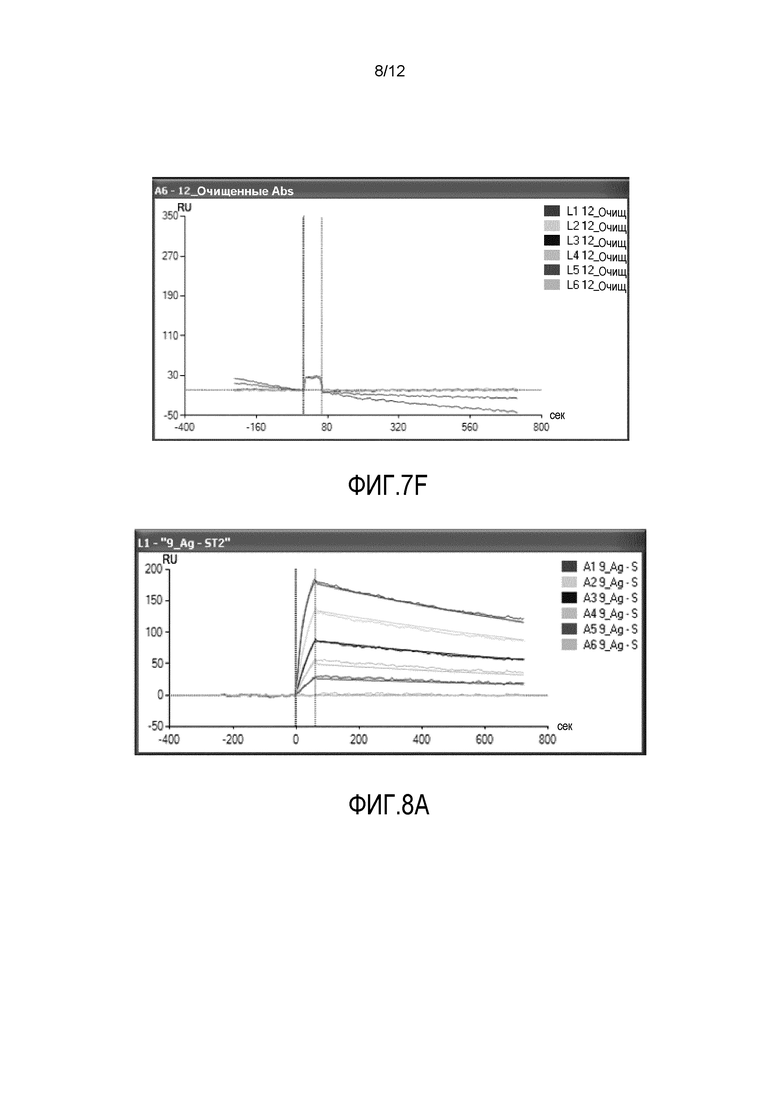
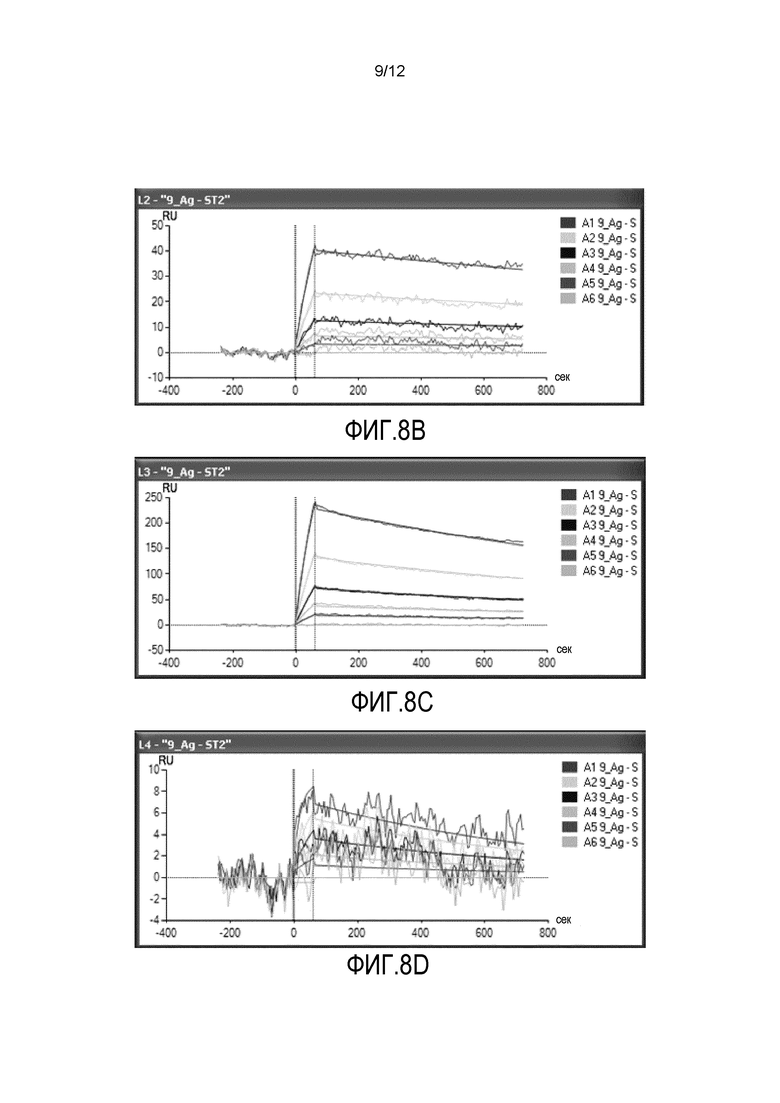
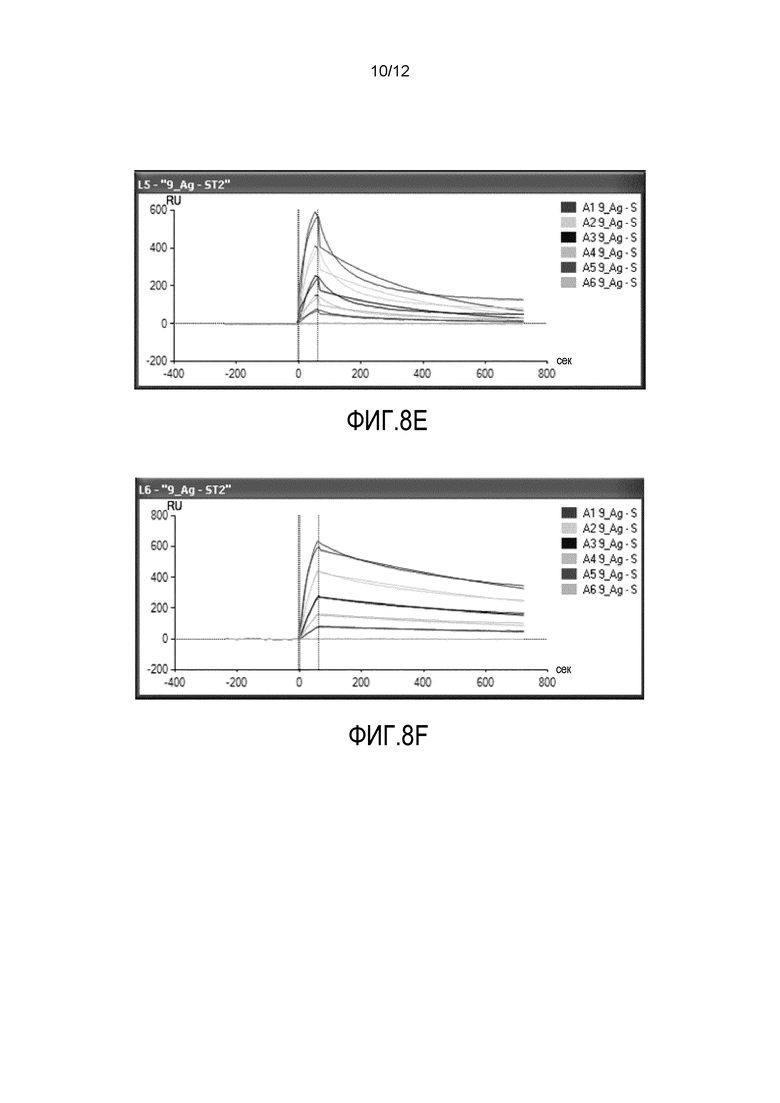
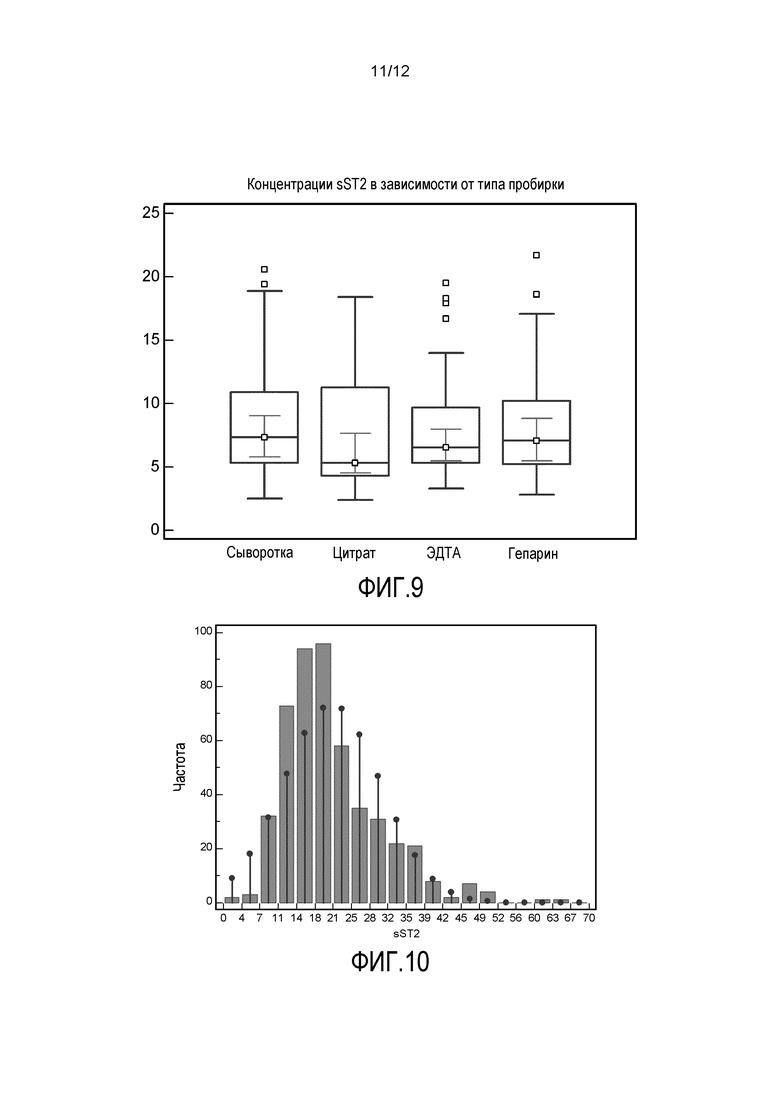
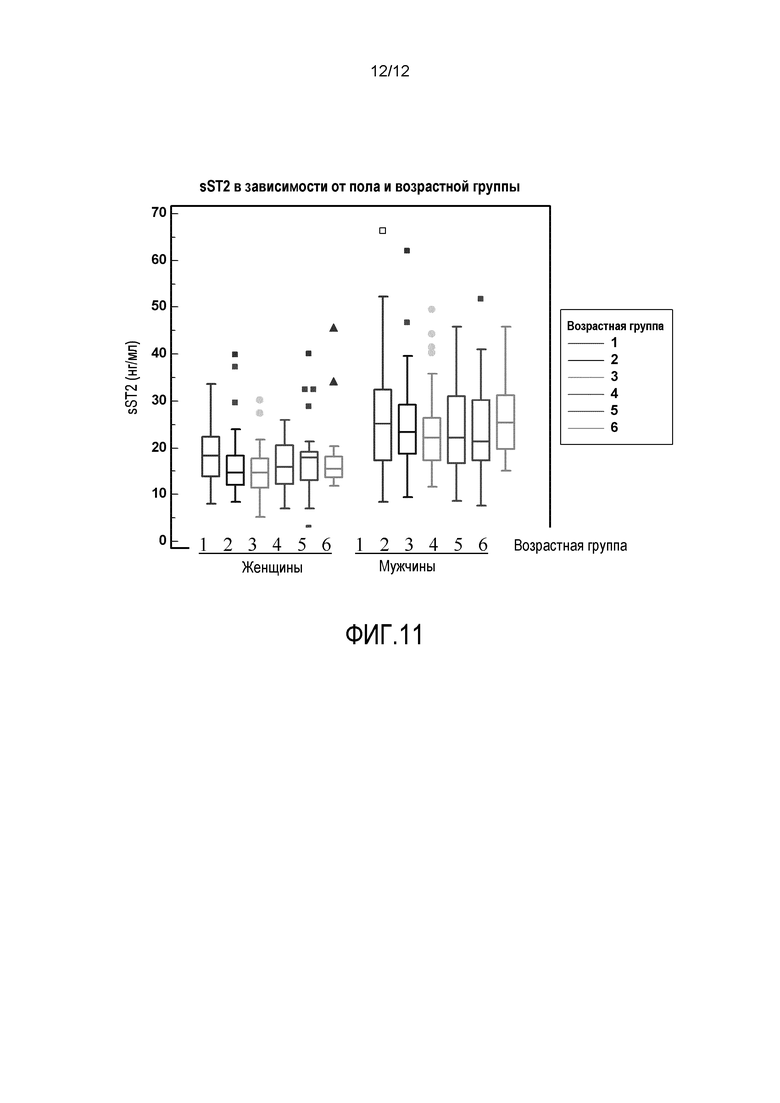
Изобретение относится к области биотехнологии и иммунологии. Описаны антитела и их антигенсвязывающие фрагменты, которые связываются с растворимым белком человека, продуктом гена 2, экспрессируемым при стимуляции роста (ST2). Также описаны наборы, содержащие эти антитела и фрагменты антител, и способы использования этих антител и фрагментов антител. Предложенная группа изобретений может быть использована в медицине. 8 н. и 15 з.п. ф-лы, 23 ил., 10 табл., 2 пр.
1. Выделенное антитело или его антигенсвязывающий фрагмент, которые специфически связываются с растворимым белком человека, продуктом гена 2, экспрессируемым при стимуляции роста (ST2), где антитело или его фрагмент продуцируются гибридомой, депонированной в Американской коллекции типовых культур (АТСС) и обозначенной патентным депозитным номером РТА-10431, где антитело или его фрагмент имеют KD связывания с растворимым продуктом гена 2 человека, экспрессируемым при стимуляции роста (ST2), равную или меньше 1,51×10-9 М.
2. Антитело или фрагмент по п. 1, где фрагмент представляет собой Fab фрагмент или F(ab')2 фрагмент.
3. Антитело или фрагмент по п. 1, где антитело или его фрагмент гликозилированы.
4. Антитело или фрагмент по п. 1, где антитело или его фрагмент включают одну или более областей, определяющих комплементарность, легкой или тяжелой цепи антитела, продуцируемого гибридомой, депонированной в АТСС и обозначенной патентным депозитным номером РТА-10431.
5. Гибридома для продуцирования антитела, которое специфически связывается с растворимым ST2 человека, где гибридома представляет собой гибридому, депонированную в Американской коллекции типовых культур (АТСС) и обозначенную патентным депозитным номером РТА-10431.
6. Способ определения растворимого ST2 человека в образце, взятом у индивидуума, где способ предусматривает:
приведение образца в контакт по меньшей мере с одним антителом или его фрагментом по любому из пп. 1-4; и
определение связывания по меньшей мере одного антитела или его фрагмента с растворимым ST2 человека.
7. Способ по п. 6, где способ предусматривает использование по меньшей мере двух различных антител или их фрагментов.
8. Набор для определения растворимого ST2 человека в образце, взятом у индивидуума, где набор содержит по меньшей мере одно антитело или его антигенсвязывающий фрагмент по любому из пп. 1-4; и
инструкции по применению по меньшей мере одного антитела или его антигенсвязывающего фрагмента в способе определения растворимого ST2 человека в образце, взятом у индивидуума.
9. Набор по п. 8, где набор содержит два антитела или их антигенсвязывающих фрагментов.
10. Набор по п. 8, где набор предлагается как набор для твердофазного иммуноферментного анализа.
11. Набор по п. 8, дополнительно содержащий рекомбинантный растворимый ST2 человека, выделенный из клетки человека.
12. Выделенное антитело или его антигенсвязывающий фрагмент, которые специфически связываются с растворимым белком человека, продуктом гена 2, экспрессируемым при стимуляции роста (ST2), где антитело или его фрагмент продуцируются гибридомой, депонированной в Американской коллекции типовых культур (АТСС) и обозначенной патентным депозитным номером РТА-10432, где антитело или его фрагмент имеют KD связывания с растворимым продуктом гена 2 человека, экспрессируемым при стимуляции роста (ST2), равную или меньше 1,51×10-9 М.
13. Антитело или его фрагмент по п. 12, где антитело или его фрагмент имеют KD связывания с растворимым продуктом гена 2 человека, экспрессируемым при стимуляции роста (ST2), равную или меньше чем 8,59×10-10 М.
14. Антитело или его фрагмент по п. 12, где фрагмент представляет собой фрагмент Fab или фрагмент F(ab')2.
15. Антитело или его фрагмент по п. 12, где антитело или его фрагмент гликозилированы.
16. Антитело или его фрагмент по п. 12, где антитело или его фрагмент содержат один или несколько из гипервариабельных областей легкой или тяжелой цепи антитела, продуцируемого гибридомой, депонированной в АТСС и обозначенной патентным депозитным номером РТА-10432.
17. Гибридома для продуцирования антитела, которое специфически связывается с растворимым ST2 человека, где гибридома представляет собой гибридому, депонированную в Американской коллекции типовых культур (АТСС) и обозначенную патентным депозитным номером РТА-10432.
18. Способ определения растворимого ST2 человека в образце, взятом у индивидуума, где способ предусматривает:
приведение образца в контакт по меньшей мере с одним антителом или его фрагментом по любому из пп. 12-16; и
определение связывания по меньшей мере одного антитела или его фрагмента с растворимым ST2 человека.
19. Способ по п. 18, где способ предусматривает использование по меньшей мере двух различных антител или их фрагментов.
20. Набор для определения растворимого ST2 человека в образце, взятом у индивидуума, где набор содержит по меньшей мере одно антитело или его антигенсвязывающий фрагмент по любому из пп. 12-16; и
инструкции по применению по меньшей мере одного антитела или его антигенсвязывающего фрагмента в способе определения растворимого ST2 человека в образце, взятом у индивидуума.
21. Набор по п. 20, где набор содержит два антитела или их антигенсвязывающих фрагментов.
22. Набор по п. 20, где набор предлагается как набор для твердофазного иммуноферментного анализа.
23. Набор по п. 20, дополнительно содержащий рекомбинантный растворимый ST2 человека, выделенный из клетки человека.
| WO 1999034217 A1, 08.07.1999 | |||
| US 0007087396 B2, 08.08.2006 | |||
| US 20030124624 A1, 03.07.2003 | |||
| US 20100009356 A1, 14.01.2010 | |||
| US 20090304699 A1, 10.12.2009 | |||
| OSHIDA K | |||
| ET AL., Studies on natural ST2 gene products in the human leukemic cell line UT-7 using monoclonal antihuman ST2 antibodies, HYBRIDOMA, LIEBERT, 1995, v | |||
| Паровоз для отопления неспекающейся каменноугольной мелочью | 1916 |
|
SU14A1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Устройство для биологического очищения сточных вод | 1924 |
|
SU419A1 |
| SHIMPO MASAHISA ET AL., Serum levels of the interleukin-1 receptor family member ST2 predict mortality and clinical outcome in acute myocardial infarction, CIRCULATION, 2004, v | |||
| Шкив для канатной передачи | 1920 |
|
SU109A1 |
| Способ использования делительного аппарата ровничных (чесальных) машин, предназначенных для мериносовой шерсти, с целью переработки на них грубых шерстей | 1921 |
|
SU18A1 |
| Способ получения фотографических увеличений | 1924 |
|
SU2186A1 |
| МОНОКЛОНАЛЬНОЕ АНТИТЕЛО И ПРОДУЦИРУЮЩАЯ ЕГО ГИБРИДОМА | 2004 |
|
RU2312109C2 |
| . | |||
Авторы
Даты
2017-07-11—Публикация
2011-04-08—Подача